Согласно определению специального заседания Европейского общества репарации тканей, «хронической следует считать рану, не заживающую в течение периода, который является нормальным для ран подобного типа или локализации» [7]. По нашим данным, хроническим считается раневой процесс, существующий более 45 дней без признаков активного заживления.
В последнее время число больных, инфицированных микроорганизмами, передающихся половым путем, продолжает неуклонно расти. Заболевания, передающиеся половым путем (ЗППП), нередко протекают бессимптомно или малосимптомно, поэтому многие пациенты не обращаются к врачу, в этой связи половые инфекции имеют выраженную тенденцию перехода в хроническую форму [2].
В ранах промежности после оперативных вмешательств встречаются полимикробные ассоциации, представленные условно-патогенными бактериями [3], в т. ч. и клинически значимыми, в сочетании с хламидиями, трихомонадами, гарднереллами, микоплазмами, уреаплазмами, цитомегаловирусом (ЦМВ), генитальным герпесом (вирусом простого герпеса 2-го типа (ВПГ-2)), а также кандидой, т. е. возбудителями, передающимися половым путем [1, 4, 8, 11, 12].
Однако работ, посвященных данной проблеме, имеется очень немного, преимущественно они касаются гинекологической и урологической практики. В этой связи для изучения влияния инфекций, передающихся половым путем, на течение раневого процесса мы решили изучить микробиоценоз послеоперационных ран у пациентов после операций на дистальном отделе прямой кишки, анальном канале и промежности.
Было проведено исследование, целью которого являлись изучение раневого микробиоценоза и разработка комплекса специфической корригирующей терапии в послеоперационном периоде, направленной на улучшение результатов лечения больных с длительно незаживающими ранами анального канала и промежности.
Материалы и методы
Исследование проводится с сентября 2010 г. по настоящее время. В исследование было включено 96 человек, оперированных в ФБГУ «Государственный научный центр колопроктологии» по поводу свищей прямой кишки, хронических анальных трещин и геморроя.
Основную группу составили 49 пациентов с вялотекущим раневым процессом, подтвержденным при клинико-цитологическом исследовании, результатом которого явились длительно незаживающие раны (со дня операции прошло от 46 до 118 дней, в среднем – 81,3±49,3). Контрольная группа – 47 больных, у которых по данным клинико-цитологических исследований отклонений в течении раневого процесса отмечено не было, раны зажили в нормальные сроки – в среднем на 37±10,5 дня (р<0,05).
Сравнительный анализ 2-х групп пациентов не выявил существенных различий по половому и возрастному составу. Так, в основной и контрольной группах было больше мужчин – 28 (57,1%) и 29 (61,7%) соответственно. В основной группе была 21 (42,9%) женщина, в контрольной – 18 (38,3%).
Возраст пациентов основной группы колебался от 19 до 74 лет, но в большинстве своем это были люди работоспособного возраста, их средний возраст составил 41,0±13,2 года. У больных контрольной группы (лица от 18 до 72 лет) средний возраст был 42,8±12,2 года.
Также больные были сравнимы и по нозологическим формам. Среди 49 пациентов основной группы было 13 (26,5%) больных с хроническими анальными трещинами, 28 (57,1%) – со свищами прямой кишки и 8 (16,3%) – с геморроем. У большинства пациентов контрольной группы – 24 (51,1%) также диагностированы свищи, у 13 (27,7%) наблюдались трещины и у 10 (21,3%) – геморрой.
Достоверно значимых различий по характеру оперативных вмешательств также выявлено не было. В большинстве случаев у пациентов как основной, так и контрольной групп проводились оперативные вмешательства в объеме иссечения свищей в просвет прямой кишки: у 21 (42,9%) и 17 (36,2%) соответственно. Иссечение свищей с ушиванием сфинктера выполнялось у 3 (6,1%) больных основной группы и у 5 (10,6%) – контрольной. Иссечение свища с низведением лоскута проводилось у 4 (8,2%) пациентов основной группы и 2 (4,3%) – контрольной.
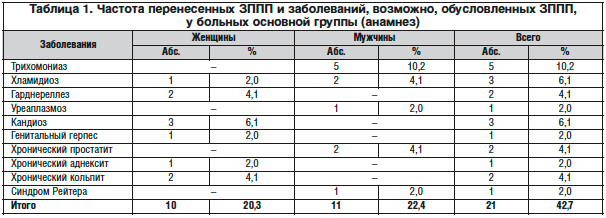
У 21 (42,8%) (11 мужчин и 10 женщин) больного основной группы были указания на наличие в анамнезе ЗППП и заболеваний, которые могли быть обусловлены инфекциями, передающимися половым путем, а у пациентов контрольной группы указаний на такие заболевания не было ни в одном наблюдении (р<0,001). У больных основной группы были выявлены следующие заболевания: 2 (4,1%) наблюдались у уролога по поводу хронического простатита; у 2 (4,1%) пациенток в прошлом диагностирован кольпит, при этом возбудители данного заболевания установлены не были; указание на перенесенный аднексит имело место у 1 (2,0%) больной; 1 пациенту (2,0%) проводилось лечение по поводу синдрома Рейтера; 5 мужчин (10,2%) перенесли трихомониаз; 3 пациента (6,1%) (женщина и двое мужчин) – хламидиоз; 2 пациентки (4,1%) – гарднереллез и 3 (6,1%) – кандидоз, а также 1 (2,0%) – генитальный герпес; 1 больной (2,0%) перенес в прошлом уреаплазмоз (табл. 1).
У всех больных в послеоперационном периоде проводились бактериологические и бактериоскопические исследования отделяемого ран анального канала, уретры, у женщин дополнительно – из цервикального канала: у пациентов контрольной группы – на 25–й день после операции и у пациентов основной группы – на момент обращения, а затем спустя 14 дней от начала проведенного лечения.
При помощи светового микроскопа определяли возбудителей таких инфекций, как трихомониаз, кандидоз, гарднереллез, наличие грамположительных и грамотрицательных кокков и палочек. Кроме того, для диагностики инфекций, передающихся половым путем, использовался метод полимеразной цепной реакции (ПЦР). У всех пациентов, у которых были обнаружены хламидии, микоплазмы, уреаплазмы, гарднереллы, диагноз подтверждался методом прямой иммунофлюоресценции. При выявлении ВПГ-2 и ЦМВ диагноз подтверждался с помощью культурального метода. Микробиологические исследования проводились в бактериологической лаборатории с использованием методики, позволяющей определить количественное содержание и видовой спектр аэробных и факультативно-анаэробных микроорганизмов.
У больных основной группы сразу после обращения по поводу длительно незаживающей раны (на 46–118-й день), а затем через 14 дней от начала лечения проводились цитологические и патоморфологические исследования отделяемого из послеоперационных ран. У пациентов контрольной группы эти исследования проводили на 25-й день после операции.
Результаты
При цитологическом исследовании во время обращения по поводу длительно незаживающей раны у 45 (91,8%) больных основной группы наблюдалась картина «извращенной» репарации – наличие многоядерных клеток типа инородных тел в мазках-отпечатках из ран, а также у всех 49 пациентов – хронический воспалительный процесс с большим количеством неизмененных лейкоцитов. Количество лейкоцитов в ранах от 30 до 40 в поле зрения наблюдалось у 8 (16,3%) больных, 40–60 – у 7 (14,3%), 60–80 – у 9 (18,4%), все поле зрения –у 25 (51%) пациентов. К 25-му дню у всех больных контрольной группы лейкоциты с явлениями дистрофии были в небольшом количестве и не превышали 5 в поле зрения (р<0,001).
Данные цитологического исследования коррелировали с данными, полученными при патоморфологическом исследовании. У пациентов основной группы в биоптате обнаружено большое количество неизмененных нейтрофилов, микрофлора локализуется как вне-, так и внутриклеточно; явления фагоцитоза слабо выражены. У больных контрольной группы в биоптате выявлялись единичные, дистрофически измененные лейкоциты, а также макрофаги и фибробласты.
При микробиологическом исследовании в момент обращения (на 46–118-й день после операции) у всех 49 (100%) больных основной группы в отделяемом послеоперационных ран определялись различные микроорганизмы; у пациентов контрольной группы на 25-й день после операции в 44 (93,6%) из 47 наблюдений были выявлены какие-либо микроорганизмы, а у 3 (6,4%) из них отсутствовал рост в бактериальных посевах.
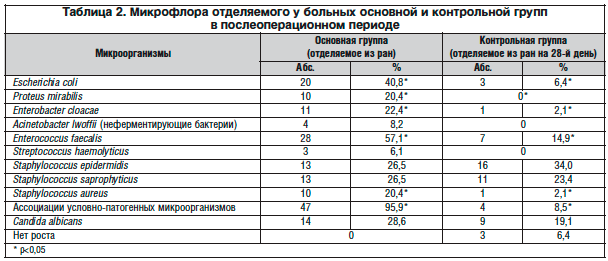
У пациентов основной группы среди микроорганизмов преобладали Enterococcus faecalis (фекальные стрептококки) – у 28 (57,1%), а также Escherichia coli (кишечная палочка) – у 20 (40,8%); первые встречались более чем в 4 раза чаще, вторые – в 6 раз чаще, чем у больных контрольной группы. Enterobacter cloacae (энтеробактер) в 11 раз чаще обнаруживался у пациентов основной группы по сравнению с больными контрольной (этот микроорганизм обнаружен лишь у 1 больного контрольной группы). Candida albicans (дрожжевой грибок) высевался у 14 (28,6%) пациентов основной группы и у 9 (19,1%) – контрольной.
У пациентов основной группы в бактериальных посевах из послеоперационных ран такие клинически значимые микроорганизмы, как Proteus mirabilis (протей), были обнаружены в 10 (20,4%), Acinetobacter lwoffii (ацинетобактер) – в 4 (8,2%), Staphylococcus aureus (золотистый стафилококк) – в 10 (20,4%), Streptococcus haemolyticus (гемолитический стрептококк) – в 3 (6,1%) наблюдениях. Суммарно частота выявления этих клинически значимых условно-патогенных микроорганизмов у больных основной группы составила 27 (55,1%) случаев, количество микроорганизмов превышало 105 КОЕ. У пациентов контрольной группы клинически значимые микроорганизмы обнаруживались только у 1 (2,1%) пациента (высевался Staphylococcus aureus), микробное число в данном случае составило 105 КОЕ (р<0,001).
Ассоциации микроорганизмов в бактериальных посевах встречались у 47 (95,9%) пациентов основной группы: 5 различных возбудителей обнаружено у 5 (10,2%), 4 – у 5 (10,2%), 3 – у 5 (10,2%), 2 – у 32 (65,3%) больных; тогда как в контрольной группе – лишь у 4 (8,5%) пациентов была выявлена ассоциация 2-х микроорганизмов (р<0,001) (табл. 2).
У всех пациентов основной группы с длительно незаживающими ранами были выявлены различные микроорганизмы, передающиеся половым путем, из них у 98% пациентов обнаружены патогенные возбудители ЗППП, тогда как в контрольной группе этот показатель составил лишь 23,4% (у 11 из 47 больных), при этом все обнаруженные микроорганизмы – возбудители ЗППП у последних были условно-патогенными (р<0,01) (рис. 1).
У 26 (53,1%), т. е. более половины пациентов основной группы, в раневом отделяемом обнаруживались хламидии. При этом Chlamydia trachomatis только у 3 (6,1%) больных была обнаружена также и в уретре, и в цервикальном канале у женщин. В контрольной группе хламидиоз не диагностирован (р<0,001).
Трихомонада была выявлена более чем у трети пациентов основной группы – в 19 (38,8%) случаях: у 2 (4,1%) пациенток в отделяемом из ран, а также уретры, анального и цервикального каналов и у 2 (4,1%) мужчин – в уретре и отделяемом из ран, а у 15 (30,6%) больных – только в отделяемом из послеоперационных ран. В контрольной группе трихомониаз не был обнаружен (р<0,001).
Гарднерелла определялась у 17 (34,7%) пациентов основной группы: у 8 (16,3%) из них этот микроорганизм обнаруживался во всем исследуемом материале, у 9 (18,4%) – только в раневом отделяемом. У 7 (14,9%) пациентов контрольной группы данный микроорганизм выявлялся в 5 (10,6%) наблюдениях во всем исследуемом материале, в 2 (4,3%) – только в отделяемом из уретры и цервикального канала.
Кандида выявлялась в 29 (59,2%) случаях у пациентов основной группы в отделяемом из анального канала, уретры, цервикального канала и послеоперационных ран. В контрольной группе кандидоз был обнаружен у 5 (10,6%) человек также во всем исследуемом материале (р<0,001).

Несколько реже встречались такие внутриклеточные микроорганизмы, как уреаплазма и микоплазма. У 6 (12,2%) пациентов основной группы уреаплазма обнаруживалась во всем исследуемом материале, тогда как в контрольной группе этот микроорганизм определялся у 1 (2,1%) больного только в отделяемом из уретры (р<0,05). В 1 (2,0%) случае у больной основной группы была диагностирована Мycoplasma hominis, которая определялась в отделяемом послеоперационных ран и анального канала. У 1 (2,1%) больного контрольной группы Мycoplasma hominis была обнаружена в отделяемом послеоперационной раны и уретры.
У 6 (12,2%) пациентов основной группы выявлен ВПГ-2: у 3 (6,1%) в материале из уретры, цервикального канала и послеоперационных ран и у 3 (6,1%) только в отделяемом из ран. В контрольной группе ВПГ-2 не встречался (р<0,05).
ЦМВ обнаружен у 10 (20,4%) больных основной группы: у 9 (18,4%) в анальном канале и раневом отделяемом и у 1 (2,0%) пациента в уретре, цервикальном канале и раневом отделяемом; тогда как в контрольной группе – не выявлен ни в одном наблюдении (р<0,001).
Частота выявления трихомонады у больных основной группы только из отделяемого из послеоперационных ран при отсутствии их в отделяемом из гениталий составила 30,6% (в 15 наблюдениях), хламидии – 46,9% (в 23 наблюдениях), ЦМВ – 18,4% (в 9 наблюдениях) и ВПГ-2 – 6,1%. Этот факт свидетельствует о длительно существующем хроническом процессе, при котором бывает трудно обнаружить возбудителей ЗППП, если нет какого-либо провоцирующего фактора. Поскольку возбудители хронической инфекции, передающейся половым путем, находятся в эпителиальной клетке в неактивном, «дремлющем» состоянии, появление раны в области промежности либо анального канала является тем самым провоцирующим фактором, который позволяет хронической латентной инфекции активизироваться.
Возбудители ЗППП у всех 49 пациентов основной группы, у которых они были диагностированы, ни в одном наблюдении не встречались как моноинфекция, а обнаруживались только в ассоциациях с другими возбудителями ЗППП. Наличие сразу 2-х микроорганизмов, вызывающих ЗППП, обнаружены у 33 (67,3%) больных, а у 16 (32,7%) пациентов основной группы встречалось сочетание 3-х возбудителей.
У 11 больных контрольной группы, у которых были выявлены микроорганизмы, передающиеся половым путем, напротив, наиболее часто встречался 1 возбудитель – у 8 (17,0%), сочетание 2-х микроорганизмов выявлено у 3 (6,4%) пациентов, а наличие сразу 3-х и более микроорганизмов ни в одном наблюдении обнаружено не было (р<0,001).

У пациентов основной группы частота обнаружения ассоциаций микроорганизмов составила: трихомонада, ЦМВ и кандида – 10,2% (5 больных); хламидия, трихомонада и кандида – 8,2% (4 пациента); трихомонада, гарднерелла и кандида – 10,2% (5 больных); хламидия и гарднерелла – 20,4% (10 наблюдений); хламидия и кандида – 14,3% (7 больных); трихомонада и кандида – 8,2% (4 случая). У 3 (6,4%) больных контрольной группы кандида встречалась в сочетании с гарднереллой.
Среди ассоциаций условно-патогенных микроорганизмов с возбудителями ЗППП у пациентов основной группы встречались сочетания: золотистого стафилококка с трихомонадой, хламидией и кандидой – у 4 (8,2%) больных; протея с трихомонадой и кандидой – у 3 (6,1%); протея с хламидией и кандидой – у 6 (12,2%). Как уже указывалось, золотистый стафилококк обнаруживался в посеве только у 1 (2,1%) пациента контрольной группы и ассоциировался с кандидой.
Гемолитические стрептококки ассоциировались с энтерококками, хламидией, кандидой и ВПГ-2 у 2 (4,1%) больных, в ассоциации с хламидией и кандидой – у 1 (2,0%) пациента основной группы.
Таким образом, условно-патогенные, клинически значимые микроорганизмы часто ассоциируются с патогенными микроорганизмами, к которым относятся трихомонада, хламидия, ЦМВ и ВПГ-2. Можно сказать, что патогенные микроорганизмы, передаваемые половым путем, создают благоприятные условия для размножения условно-патогенных микроорганизмов, таких как золотистый стафилококк, протей, гемолитический стрептококк и др., что в свою очередь приводит к длительному поддержанию воспалительной раневой реакции и замедлению процессов репарации в ранах.
Всем больным с длительно незаживающими ранами, у которых обнаружены ЗППП, была назначена соответствующая терапия в зависимости от выделенного возбудителя.
При хламидиозе назначались антибиотики с учетом того, что антихламидийный агент должен активно воздействовать на делящиеся ретикулярные тельца. К таким антибиотикам относятся: макролиды (рокситромицин, кларитромицин, джозамицин), тетрациклины (тетрациклин, доксициклин), эритромицин, фторхинолоны (ципрофлоксацин, офлоксацин).
При микоплазмозе и уреаплазмозе пациенты получали антибиотики из следующих групп: макролиды (рокситромицин, клатритромицин, джозамицин), тетрациклины (тетрациклин, доксициклин), фторхинолоны (ципрофлоксацин, офлоксацин), линкозамины (линкомицин, клиндамицин), аминогликозиды (гентамицин, стрептомицин).
При трихомониазе и гарднереллезе использовались препараты, обладающие противопротозойным и противомикробным действием: метронидазол, тинидазол, орнидазол.
Лечение кандидоза проводилось антимикотическими препаратами из групп триазола (флуконазол, итраконазол), имидазола, полиена (нистатин, леворин, амфотерицин В), аллиламина, эхинокандина (каспофунгин).
При генитальном герпесе назначались интерферон и соединения, обладающие интерферониндуцирующей активностью; ингибиторы репликации вирусной нуклеиновой кислоты (аналоги нуклеозидов (ацикловир), аналоги пирофосфата (фоскарнет натрий)).
При ЦМВ-инфекции назначались ингибиторы репликации вирусной нуклеиновой кислоты: ганцикловир, аналоги пирофосфата (фоскарнет натрий), экстракт побегов картофеля.
Всем больным в комплексе с этиотропными препаратами назначались пробиотики для восстановления нормальной флоры ЖКТ.
В результате проведенного лечения отмечено выздоровление всех пациентов с длительно незаживающими ранами, вошедших в основную группу, которое подтверждалось при клиническом, цитологическом и патоморфологическом исследованиях.
Клинический пример: пациентка В., оперированная по поводу чрессфинктерного свища прямой кишки. По поводу длительно незаживающей раны обратилась на 56-й день после операции. В области раны определялись гипергрануляции, которые при контакте легко кровоточили, на отдельных участках рана была покрыта фибрином (рис. 2).
При ПЦР и бактериоскопическом исследовании отделяемого из раны обнаружены трихомонада, хламидия и кандида. Через 3 нед. после проведенной специфической терапии, направленной на элиминацию выявленных инфекционных агентов, рана зажила полностью.
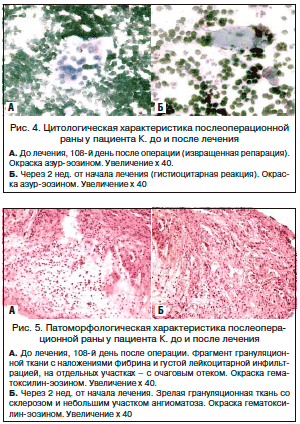
Клинический пример: пациент К., оперирован по поводу экстрасфинктерного свища прямой кишки. На 108-й день после операции при клиническом осмотре – обильное отделяемое из раны слизисто-гнойного и слизисто-сукровичного характера (рис. 3).
Данные клинического обследования коррелировали с цитологическими (рис. 4) и патоморфологическими (рис. 5) исследованиями. При ПЦР и бактериоскопическом исследовании отделяемого из раны обнаружены ЦМВ, ВПГ-2 и кандида. После проведенного этиотропного лечения (противовирусная терапия, антимикотические препараты) рана зажила полностью.
Заключение
1. У больных с длительно незаживающими послеоперационными ранами в анамнезе частота выявленных мочеполовых инфекций и заболеваний, возможно, обусловленных ЗППП, была 42,8%, тогда как у больных контрольной группы анамнестических указаний на перенесенные ЗППП не было (р<0,001).
2. При цитологическом исследовании в мазках-отпечатках из ран у 91,8% больных основной группы наблюдалась картина извращенной репарации. У всех больных контрольной группы к 25-му дню лейкоциты обнаружены лишь в небольшом количестве (до 5 в поле зрения), с явлениями дистрофии (р<0,001).
3. Частота обнаружения таких клинически значимых микроорганизмов, как протеи, гемолитические стрептококки, золотистые стафилококки, ацинетобактер у больных основной группы составила 55,1%. И лишь у 1 (2,1%) больного контрольной группы высеялся золотистый стафилококк (р<0,001). Ассоциации микроорганизмов в бактериальных посевах были обнаружены у 95,9% пациентов основной группы, тогда как в контрольной группе – лишь у 8,5% больных (р<0,001).
4. У всех пациентов основной группы с длительно незаживающими ранами были выявлены различные ЗППП, в т. ч. у 98% – облигатные патогенные микроорганизмы. У 23,4% больных контрольной группы обнаруженные микроорганизмы, передающиеся половым путем, являлись лишь условно-патогенными (р<0,01).
5. У большинства больных с длительно незаживающими ранами трихомонады (30,6%), хламидии (46,9%) и ЦМВ (18,4%), герпесвирусы (6,1%) выявлялись только в отделяемом из ран и не были обнаружены в соскобах из гениталий. Наличие в области промежности либо анального канала раневого дефекта является провоцирующим фактором, который позволяет хронической, латентной инфекции активизироваться.
6. Клинически значимые условно-патогенные микроорганизмы (протей, ацинетобактер, гемолитический стрептококк и золотистый стафилококк) наиболее часто ассоциируются с патогенными микроорганизмами, передающимися половым путем, к которым относятся трихомонады, хламидии, ЦМВ и ВПГ-2.











