Л.В. Коркоташвили
НИИ детской гастроэнтерологии, МоскваО.И. Гусева
Нижегородская медицинская академияА.Л. Верткин, О.Н. Ткачева
МГМСУ им. Н.А. СемашкоДисплазия соединительной ткани – группа генетически гетерогенных и клинически полиморфных патологических состояний, характеризующихся нарушением формирования соединительной ткани в эмбриональном и постнатальном периодах и объединяющая ряд генных синдромов (Марфана, Элерса–Данлоса) и недифференцированные (несиндромные) формы с мультифакториальными механизмами развития. На практике особенно часто приходится сталкиваться с недифференцированной дисплазией соединительной ткани (НДСТ). В отличие от синдромных форм проявления НДСТ не столь манифестны и нередко остаются без должного внимания. Вместе с тем универсальность соединительнотканого дефекта при НДСТ предполагает разнообразие висцеральных изменений, часть из которых может иметь серьезные клинические последствия. В частности, генерализованный характер поражения соединительной ткани с вовлечением в патологический процесс репродуктивной системы не может не отразиться на течении беременности и родов. Однако данный аспект проблемы НДСТ изучен недостаточно.
Целью настоящей работы являлось изучение особенностей течения и исходов беременности у женщин с НДСТ и возможностей профилактики осложнений пре– и перинатального периода.
Материал и методы
В основную группу вошло 56 первородящих женщин в возрасте от 18 до 32 лет (средний возраст 23,6±0,49 года) с внешними и висцеральными фенотипическими маркерами дисплазии соединительной ткани.
К внешним проявлениям «слабости» соединительной ткани относились астеническое телосложение, некоторые особенности строения скелета и связочного аппарата (аномалии прикуса, искривленные мизинцы, сколиоз, плоскостопие, миопия). За висцеральные фенотипические маркеры дисплазии соединительной ткани принимались аномалии развития сердечно–сосудистой и мочевыделительной систем, диагностированные в ходе ультразвукового обследования, и варикозное расширение вен нижних конечностей, устанавливаемое при общем осмотре (табл. 1). В среднем у женщин основной группы выявлялось по 1,4 висцеральных маркера дисплазии соединительной ткани, поэтому общая сумма превышала 100%. Наиболее распространенными изменениями оказались микроаномалии сердца – первичный пролапс митрального клапана и дефект межпредсердной перегородки.

Достоверность различий в частоте анализируемых осложнений в указанных группах пациенток оценивалась по критерию c2, при анализе количественных признаков использовался критерий Стьюдента, порядковых – критерий Манна–Уитни.
Результаты и обсуждение
Сведения об особенностях течения беременности и родов у женщин с НДСТ противоречивы. Изучая пре– и перинатальные исходы у женщин с одним из наиболее известных висцеральных проявлений дисплазии соединительной ткани – первичным пролапсом митрального клапана, ряд авторов отмечали значительное увеличение частоты осложнений родов и послеродового периода по сравнению с соматически здоровыми [1–4], другие не наблюдали подобной закономерности [5–7].
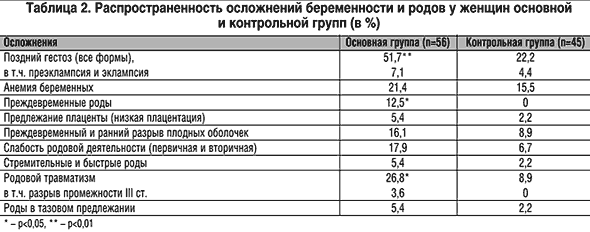
По нашим данным, у женщин с НДСТ значительно чаще отмечалось осложненное течение беременности и родов (87,5% против 53,3%, р<0,001). Распространенность отдельных патологических состояний пре– и перинатального периода у пациенток обследуемых групп отражена в таблице 2. В основной группе достоверно чаще встречались случаи поздних гестозов (включая отеки, нефропатию, преэклампсию и эклампсию), преждевременных родов, родового травматизма (разрывы промежности и влагалища), а также иные осложнения. Кроме того, у женщин с НДСТ отмечен больший объем кровопотери в родах: 348,2±53,4 мл против 310,7±45,1 мл.
Отдельному анализу были подвергнуты случаи патологии плода и новорожденного у женщин обследуемых групп (табл. 3). У женщин с НДСТ более часто регистрировались задержка внутриутробного развития и хроническая гипоксия плода. В основной группе втрое чаще рождались недоношенные дети, выше был процент больных новорожденных – соответственно 42,9% и 37,8%. В структуре заболеваемости младенцев, рожденных от матерей с НДСТ, преобладало ишемически–гипоксическое повреждение центральной нервной системы, несколько чаще встречались врожденные пороки развития (крипторхизм, дисплазия тазобедренного сустава). Кроме того, в основной группе отмечены более низкая масса тела детей при рождении (3633,3±54,0 г против 3990,8±69,8 г, р<0,001) и более низкий балл по шкале Апгар (7,5±0,2 против 8,0±0,1, р<0,05).

Одним из возможных объяснений акушерских осложнений у женщин с НДСТ может служить эндокринный дисбаланс, установленный у подобной категории пациентов. В ряде работ показана распространенность нейроэндокринных расстройств в виде нарушений менструального цикла и предместруального синдрома, высокая частота гипоэстрогенного гормонального фенотипа и овариальных дисфункций у девушек и женщин с фенотипическими проявлениями дисплазии соединительной ткани [8,9].
Однако наше внимание было привлечено к иной потенциальной причине анте–, пери– и неонатальных осложнений у женщин с НДСТ – дефициту магния. Последнее время нарушению магниевого обмена уделяется большое внимание как существенному фактору многих патологических состояний, включая дисплазию соединительной ткани и ряд акушерских осложнений.
Ионы магния входят в состав основного вещества соединительной ткани и участвуют в регуляции ее метаболизма, в условиях магниевой недостаточности нарушается способность фибробластов продуцировать коллаген [10,11]. Подтвержден дефицит магния при первичном пролапсе митрального клапана [11–13], на практике показана эффективность препаратов магния при данной патологии [14].
С другой стороны, недостаток магния сопряжен с широким спектром осложнений беременности и родов. В частности, снижение содержания магния приводит к повышению тонуса миометрия и лежит в основе преждевременных родов [15,16]. Нарушению гомеостаза магния придается особое место в патогенезе преэклампсии и эклампсии, очевидное снижение его уровня при этом показано во многих работах [17–19]. Низкий уровень внутриклеточного магния может способствовать развитию артериальной гипертонии беременных [19], выявлена связь между уровнем магния в эритроцитах и величиной АД в III триместре беременности [18]. В экспериментальных и клинических исследованиях доказана способность препаратов магния защищать мозг у новорожденных [20–22], установлено, что дефицит магния при беременности может выступать причиной задержки внутриутробного развития плода [23] и ухудшения выживаемости потомства [24]. Участие магния в процессе родоразрешения и значение его дефицита в возникновении неблагоприятных исходов у матери, плода и новорожденного обусловливают широкое применение его препаратов в акушерской практике.
Установленная в настоящем исследовании распространенность позднего гестоза, преждевременных, стремительных и быстрых родов, задержки развития плода и повреждения центральной нервной системы у новорожденного заставила обратиться к изучению особенностей магниевого гомеостаза у обследованных пациенток. Было предпринято исследование концентрации магния в сыворотке крови и слюне беременных основной и контрольной групп. Выбор в качестве объекта исследования двух биологических сред организма обусловлен отсутствием четкой корреляции между сывороточным и внутритканевым содержанием магния и низкой чувствительностью гипомагниемии в отражении истинного дефицита магния [25,26].
Как следует из таблицы 4, уровни магниемии у женщин основной и контрольной групп достоверно не отличались, тогда как исследование концентрации магния в слюне документировало дефицит данного макроэлемента у пациенток с НДСТ.

Даже под влиянием столь непродолжительного лечения Магнеротом была достигнута нормализация магниевого гомеостаза: концентрация магния в слюне достигла 0,34±0,02 при исходной 0,14±0,02 ммоль/л (р<0,001). Наряду с этим отмечались снижение уровня систолического и диастолического АД в среднем соответственно на 7,3±1,4 и 2,4±0,7 мм рт.ст., а также улучшение самочувствия в виде уменьшения слабости, исчезновения головных болей.
Таким образом, результаты проведенного исследования позволяют отнести женщин с генетически предопределенной «слабостью» соединительной ткани, обозначаемой как НДСТ, к группе риска по акушерской и перинатальной патологии. Одним из реальных факторов развития осложнений беременности и родов у данной категории лиц может выступать дефицит магния, а заместительная терапия препаратом Магнерот может оказать отчетливое положительное действие.
1. Jana N., Vasishta K., Khunnu B. Pregnancy in association with mitral valve prolapse. Asia Oceania J Obstet Gynaecol 1993; 19 (1): 61–65
2. Chia Y.T., Yeoh S.C., Viegas O.A. et al. Maternal congenital heart disease and pregnancy outcome. J Obstet Gynaecol Res 1996; 22 (2): 185–191
3. Chia Y.T., Yeoh S.C., Lim M.C. Pregnancy outcome and mitral valve prolapse. Asia Oceania J Obstet Gynaecol 1994; 20 (4): 383–388
4. Елисеева И.В. Клинико–функциональные особенности соматического состояния и течения родов у женщин с пролапсом митрального клапана. Клин мед 2003; 81 (3): 22–24
5. Rayburn W.F., Fontana M.E. Mitral valve prolapse and pregnancy. Am J Obstet Gynecol 1981; 141 (1): 9–11
6. Tang L.C., Chan S.Y., Wong V.C., Ma H.K. Pregnancy in patients with mitral valve prolapse. Int J Gynaecol Obstet 1985; 23 (3): 217–221
7. Plotti G., Tropeano G., Colucci P. et al. Mitral valve prolapse and pregnancy. Minerva Med 1985; 76 (42): 2007–2010
8. Перекальская М.А., Макарова Л.И., Верещагина Г.Н. Нейроэндокринная дисфункция у женщин с системной дисплазией соединительной ткани //Клиническая медицина.– 2002.– Т.80, № 4.– С.48–51
9. Куликов А.М., Медведев В.П. Роль семейного врача в охране здоровья подростка: YI. Дисплазии соединительной ткани у подростков и их распознавание. Росс семейный врач 2000; 4: 37–51
10. Levi–Schaffer F., Shani J., Politi Y. et al. Inhibition of proliferation of psoriatic and healthy fibroblasts in cell culture by selected Dead–sea salts. Pharmacology 1996; 52 (5): 321–329
11. Zeana C.D. Recent data of mitral valve prolapse and magnesium deficit. Magnes Res 1988 l1 (3–4): 203–211
12. Coghlan H.C., Natello G. Erythrocyte magnesium in synptomatic patients with primary mitral valve prolapse: relationship to symptoms, mitral leaflet thickness, joint hypermobility and autonomic regulation. Magnes Trace Flem 1991; 10 (2–4): 205–214
13. Lichodziejewska B., Klos J., Rezler J. et al. Clinical symptoms of mitral valve prolapse are related to hypomagnesemia and attenuated by magnesium supplementation. Amer J Cardiol 1997; 79 (6): 768–772
14. Степура О.Б., Мельник О.О., Шехтер А.Б. и др. Результаты применения магниевой соли оротовой кислоты (Магнерот( при лечении больных с идиопатическим пролапсом митрального клапана. Росс мед вести 1999; 4 (2): 64–69
15. Lemancewicz A., Laudanska H., Laudanski T. et al. Permeability of fetal membranes to calcium and magnesium: possible role in preterm labour. Hum Reprod 2000; 15 (9): 2018–2222
16. Wojcicka–Jagodzinska J., Romejko E., Piekarski P. et al. Second trimester calcium–phosphorus–magnesium homeostasis in women with threatened preterm delivery. Int J Gynaecol Obstet 1998; 61 (2): 121–125
17. Manyemba J. Magnesium sulphate for eclampsia: putting the evidence into clinical practice. Cent Afr J Med 2000; 46 (6): 166–169
18. Dawson E.B., Evans D.R., Kelly R. et al. Blood cell lead, calcium, and magnesium levels associated with pregnancy–induced hypertension and preeclampsia. Biol Trace Elem Res 2000; 74 (2): 107–116
19. Kisters K., Barenbrock M., Louwen F. et al. Membrane, intracellular, and plasma magnesium and calcium concentrations in preeclampsia Am J Hypertens 2000; 13 (7): 765–769
20. Sameshima H., Ikenoue T. Long–term magnesium sulfate treatment as protection against hypoxic–ischemic brain injury in seven–day–old rats. Am J Obstet Gynecol 2001; 184 (2): 185–190
21. Berger R., Garnier Y. Perinatal brain injury. J Perinat Med 2000; 28 (4): 261–285
22. Matsuda Y., Kouno S., Hiroyama Y. et al. Intrauterine infection, magnesium sulfate exposure and cerebral palsy in infants born between 26 and 30 weeks of gestation. Eur J Obstet Gynecol Reprod Biol 2000; 91 (2): 159–164
23. Tan Y., Zhang W., Lu B. Treatment of intrauterine growth retardation with magnesium sulfate. Zhonghua Fu Chan Ke Za Zhi 2000; 35 (11): 664–666
24. Caddell J.L. The apparent impact of gestational magnesium (Mg) deficiency on the sudden infant death syndrome (SIDS). Magnes Res 2001; 14 (4): 291–303
25. Taber E.B., Tan L., Chao C.R. et al. Pharmacokinetics of ionized versus total magnesium in subjects with preterm labor and preeclampsia. Am J Obstet Gynecol 2002; 186 (5): 1017–1021
26. Школьникова М.А., Чупрова С.Н., Калинин Л.А. и др. Метаболизм магния и терапевтическое значение его препаратов: Пособие для врачей. М: Медпрактика–М; 2002








.gif)



