профессор А.С. Лопатин
Центральная клиническая больница МЦ УД Президента РФАллергический ринит (АР) – одно из самых распространенных заболеваний человека, от которого сейчас страдает более 20% взрослого населения (Н.И. Ильина, 1997). АР является классическим примером IgE–опосредованного процесса. Главными участниками аллергического воспаления в слизистой оболочке носа являются тучные клетки, выделяющие основной медиатор аллергического воспаления – гистамин. Деятельность этих клеток определяет особенности ранней и в какой–то степени поздней фаз аллергического воспаления (И.С. Гущин, 1998). Действие гистамина на Н1–рецепторы после контакта с аллергеном в случае АР проявляется заложенностью носа, ринореей, чиханием и зудом.
Антигистаминные препараты давно используются в лечении АР. В связи с этим заметным событием в терапии аллергических заболеваний явилось создание в начале 1980–х годов нового антигистаминного препарата, не обладающего седативным действием, – терфенадина. Однако существенным недостатком терфенадина, как и некоторых других неседативных антигистаминных препаратов, было наличие кардиотоксического эффекта, который иногда приводил к развитию тяжелых аритмий.
Клинические испытания установили, что в отличие от других Н1–блокаторов, новый препарат – фексофенадин не оказывает негативного действия на сердечно–сосудистую систему (M.H. Terrien et al., 1999). В исследованиях in vitro было доказано, что фексофенадин обладает в два раза более высоким сродством к Н1–рецепторам, чем терфенадин и при этом лишен антихолинергического и блокирующего кальциевые каналы действия, что и обусловливает полное отсутствие кардиотоксического эффекта. Фексофенадин был тщательно исследован в отношении возможной кардиотоксичности. Проводились мониторинг сердечного ритма, контроль артериального давления и давления в левом желудочке. Ни по одному из этих показателей не было зарегистрировано никаких отклонений (C. Pratt et al., 1997). Фексофенадин не проникает через гематоэнцефалический барьер, не подвергается биотрансформации и быстро выводится из организма преимущественно путем билиарной экскреции.
Для изучения фармакологического действия и безопасности фексофенадина проводились клинические исследования у более чем 4000 пациентов с проявлениями аллергии, 500 здоровых добровольцев, а также у больных с печеночной и почечной недостаточностью. Более 470 человек приняли участие в длительном исследовании по изучению безопасности препарата. Эти исследования показали, что фексофенадин в дозе 60 и 120 мг купирует симптомы сезонного АР в течение 60 минут. В плацебо-контролируемых исследованиях было установлено, что однократное введение фексофенадина в дозе до 800 мг или повторные введения дозы до 690 мг не вызывают таких побочных реакций, как сонливость, сухость слизистых оболочек, изменения сердечного ритма и артериального давления. Прием фексофенадина в дозе до 1380 мг в сутки не оказывал влияния на показатели ЭКГ.
Сейчас доказано, что фексофенадин угнетает экспрессию молекул адгезии ICAM–1, а также индуцированное эозинофилами выделение ICAM–1 и других медиаторов воспаления в культуре клеток эпителия носа, то есть обладает не только антиаллергическим, но и противовоспалительным действием (M. Muntasir et al., 1998). В исследованиях in vivo фексофенадин в дозе 1,6 мг/кг угнетал образование кожного волдыря у морских свинок при провокационной гистаминовой пробе, что свидетельствует о чисто конкурентном антагонизме.
Влияние фексофенадина на способность управлять транспортными средствами и воздействие на психомоторные реакции оценивались в двойном слепом перекрестном исследовании в сравнении с плацебо и клемастином (препаратом, обладающим седативным эффектом). Независимо от этого влияние препарата на психомоторное состояние и дневную активность изучалось Британским агентством по оборонным разработкам в двойном слепом плацебо-контролируемом исследовании на 6 группах пациентов. В качестве активного контроля использовался прометазин, обладающим выраженным седативным действием. Результаты этих независимых исследований были идентичными. Они показали, что фексофенадин не действует на психомоторные реакции и не вызывает сонливости, поэтому он был признан пригодным для лечения аллергии у лиц, занятых в автоматизированном производстве и у водителей транспортных средств (A.N. Nicholson, C. Turner, 1998), причем доза фексофенадина не требует коррекции у пациентов с почечной и печеночной недостаточностью (A.Markham, A.J.Wagstaff, 1998). Проведенное в 1997 г. в США мультицентровое плацебо-контролируемое исследование доказало, что прием фексофенадина один раз в сутки в дозе 120 мг является столь же эффективным и более удобным для пациентов (T.B. Casale et al., 1999).
Материал и методы исследования
Нами было проведено изучение эффективности фексофенадина (Телфаста) у больных, страдающих сезонным аллергическим ринитом (САР). В исследовании участвовало 20 человек в возрасте от 22 до 63 лет (средний возраст – 33,5 года), среди которых было 14 женщин и 6 мужчин. Длительность заболевания – от 2 до 40 лет (в среднем – 10,5 лет). Среди сопутствующих заболеваний аллергический конъюнктивит был отмечен у 9, мигрень – у 4, бронхиальная астма – у 6, крапивница – у 7, аллергический дерматит – у 2 пациентов.
При кожном тестировании с небактериальными аллергенами у 15 пациентов была выявлена аллергия к пыльце деревьев, у 11 – к пыльце злаковых, у 14 – к пыльце сорных трав. У 13 обследованных отмечена положительная реакция на эпидермальные аллергены.
Фексофенадин назначали в дозе 120 мг 1 раз в день на фоне максимальных клинических проявлений САР во время сезона цветения деревьев и злаковых трав. Продолжительность курса лечения составила 28 дней. Выраженность стандартных симптомов заболевания (выделения из носа, чихание, заложенность носа, зуд в глазах, слезотечение, покраснение глаз и першение в горле) оценивалась по 4–балльной шкале: 0 – отсутствие симптомов, 1 – слабо выраженные, 2 – умеренно выраженные, 3 – интенсивные.
Для объективной оценки эффективности и безопасности препарата использовались следующие методы исследования:
- передняя активная риноманометрия (ПАР);
- эндоскопия и фотографирование полости носа;
- общий анализ крови;
- подсчет количества эозинофилов в мазках–отпечатках со слизистой оболочки носа;
- ЭКГ;
- измерение артериального давления и частоты сердечных сокращений (ЧСС).
4 – отличный результат – все симптомы САР исчезли;
3 – хороший – почти все симптомы исчезли, но 1–2 из них сохраняются, хотя стали значительно менее выраженными;
2 – удовлетворительный – исчезновение или регресс большей части симптомов САР;
1 – отсутствие эффекта;
0 – ухудшение.
Оценка клинических и лабораторных показателей проводилась врачом при первом визите пациента, на 14 и 28 день приема препарата.
Результаты исследования
Как видно из таблицы 1, на фоне лечения фексофенадином наблюдалась четкая положительная динамика выраженности всех симптомов САР.
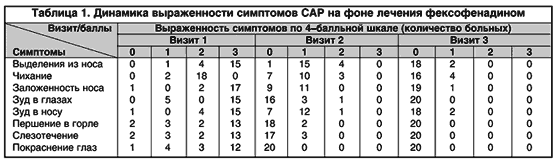
Через две недели после начала приема препарата было зарегистрировано резкое снижение интенсивности клинических проявлений САР. Во время последнего визита небольшие выделения из носа беспокоили лишь 2, а чихание– 4 пациентов, легкая заложенность носа и щекотание в носу были отмечены у 1 и 2 пациентов соответственно. Остальные симптомы САР полностью купировались на фоне приема фексофенадина (рис.1, 2).

Рис.1. Динамика выраженности симптомов ринита на фоне лечения фексофенадином

Рис.2. Динамика выраженности сопутствующих симптомов на фоне лечения фексофенадином
Методом передней активной риноманометрии были изучены показатели суммарного объемного потока (СОП)и суммарного сопротивления воздушному потоку (СС). Нормальные показатели СОП (682,6±35,8 см3/с) и СС (0,22±0,01 Па/см3/с) для сравнения были выведены на основании обследования контрольной группы из 14 здоровых лиц без каких–либо заболеваний носа.При первом визите среднее значение СОП у больных САР было равно 260,8±46,2 см3/с, при втором – 425,7±58,2 см3/с, а при третьем – 643,6±47,7 см3/с, то есть приблизилось к норме. Среднее значение СС изменилось от 1,2±0,27 Па/см3/с (первый визит), до 0,54±0,12 Па/см3/с (второй визит) и 0,26±0,05 Па/см3/с в конце лечения препаратом. По данным парного t–теста среднее значение СОП достоверно возросло от первого к третьему визиту (р<0,0001), соответственно среднее значение СС достоверно уменьшилось (р<0,0001).
Таким образом, несмотря на широко распространенное мнение о том, что затруднение носового дыхания не является основным симптомом САР, данные передней активной риноманометрии свидетельствуют о статистически достоверном существенном улучшении носового дыхания у пациентов на фоне приема фексофенадина.
Динамика размеров носовых раковин, ширины носовых ходов при эндоскопии полости носа также свидетельствовала о восстановлении носового дыхания у больных САР на фоне лечения.
При исследовании мазков–отпечатков со слизистой оболочки носа до лечения эозинофилы были обнаружены у 19 (95%) пациентов, а по окончании курса лечения – лишь у 2 (10%). До начала приема препарата у 12 (60%) больных была отмечена эозинофилия крови, к концу исследования она сохранялась лишь у 1 пациента, однако и в этом случае количество эозинофилов снизилось с 14% до 8%.
ЭКГ у всех пациентов регистрировалась до, после и во время лечения. Отрицательной динамики не было отмечено ни у одного из обследованных. В пределах нормы оставались артериальное давление и ЧСС. Следует отметить, что на фоне приема фексофенадина в указанной дозировке у одного пациента исчезли проявления аллергического дерматита, еще один больной во время лечения фексофенадином смог отказаться от инсуффляций кортикостероидного препарата фликсоназе.
Таким образом, фексофенадин оказался эффективным у всех 20 больных. Общая оценка результатов лечения, сделанная врачом и больными, совпали. Отличный результат отмечен у 15 (75%), а хороший – у 5 пациентов (25%). Отсутствия эффекта и увеличения выраженности симптомов заболевания в данной группе больных не наблюдалось. Полученные результаты позволяют сделать вывод о том, что фексофенадин является высокоэффективным и безопасным препаратом для лечения САР.
1. Гущин И.С. Аллергическое воспаление и его фармакологический контроль. – М.: Фармус принт, 1998.
2. Ильина Н.И. Аллергический ринит // Информационный сборник. Новости науки и техники. Серия: Медицина. Выпуск: Аллергия, астма и клиническая иммунология.– 1997. – №4 – C.20–24.
3. Abdelaziz M.M., Devalia J.L., Khair O.A., et al. Effect of fexofenadine on eosinofil–induced changes in epithelial permeability and cytokine release from nasal epithelial cells of patients with seasonal allergic rhinitis // J. Allergy Clin. Immunol. – 1998. – Vol.101, N.3. – P.410–420.
4. Casale T.B., Andrade C., Qu R. Safety and efficacy of once–daily fexofenadine HCI in the treatment of autumn seasonal allergic rhinitis // Allergy and Asthma Proc. – 1999. – Vol.20, N.3. – P.194–198.
5. Markham A.,Wagstaff A.J. Fexofenadine. Adis new drug profile // Drug. – 1998. – Vol.55. – P.269–274.
6. Nicholson A.N., Turner C. Central effects of the H1–antihistamin, cetirizin // Aviation Space Environ. Med. – 1998. – Vol.69. – P.166–171.
7. Pratt C., Mason J., Russell T., Ahlbrandt R. Effect of fexofenadine HCI on corrected QT interval (QTc) // Paper presented at the Congress of European Academy Of Allergology and Clinical Immunology. –, Rhodos, Greece, June 1997.
8. Terrien M.H., Rahm F., Fellrath J.M., Spertini F. Comparison of the effects of terfenadine on nasal provocation tests with allergen // J. Allergy Clin. Immunol. – 1999.– Vol.103, N.6. – P.1025–1030.












