–Ъ –љ–µ–Њ—Б–ї–Њ–ґ–љ–µ–љ–љ—Л–Љ –Є–љ—Д–µ–Ї—Ж–Є—П–Љ –Њ—В–љ–Њ—Б—П—В —Б–ї—Г—З–∞–Є –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П, –≤ –Њ—Б–љ–Њ–≤–µ –Ї–Њ—В–Њ—А—Л—Е –љ–µ—В –∞–љ–∞—В–Њ–Љ–Є—З–µ—Б–Ї–Є—Е –Є–ї–Є —Д—Г–љ–Ї—Ж–Є–Њ–љ–∞–ї—М–љ—Л—Е –љ–∞—А—Г—И–µ–љ–Є–є –Ь–Т–Я –Є –Њ—В—Б—Г—В—Б—В–≤—Г—О—В –і—А—Г–≥–Є–µ —Д–∞–Ї—В–Њ—А—Л, —Б–њ–Њ—Б–Њ–±—Б—В–≤—Г—О—Й–Є–µ –≤–Њ–Ј–љ–Є–Ї–љ–Њ–≤–µ–љ–Є—О –Є–љ—Д–µ–Ї—Ж–Є–Є –Є –µ–µ –њ–µ—А—Б–Є—Б—В–Є—А–Њ–≤–∞–љ–Є—О. –Ъ –љ–µ–Њ—Б–ї–Њ–ґ–љ–µ–љ–љ—Л–Љ –Є–љ—Д–µ–Ї—Ж–Є—П–Љ –Ь–Т–Я –Њ—В–љ–Њ—Б—П—В –Њ—Б—В—А—Л–є –Є —А–µ—Ж–Є–і–Є–≤–Є—А—Г—О—Й–Є–є —Ж–Є—Б—В–Є—В —Г –ґ–µ–љ—Й–Є–љ –Є –Њ—Б—В—А—Л–є –њ–Є–µ–ї–Њ–љ–µ—Д—А–Є—В. –£ –Љ—Г–ґ—З–Є–љ –Є–љ—Д–µ–Ї—Ж–Є–Є –≤ –±–Њ–ї—М—И–Є–љ—Б—В–≤–µ —Б–ї—Г—З–∞–µ–≤ –≤—В–Њ—А–Є—З–љ—Л, —В–Њ –µ—Б—В—М –≤–Њ–Ј–љ–Є–Ї–∞—О—В –љ–∞ —Д–Њ–љ–µ –Ї–∞–Ї–Є—Е––ї–Є–±–Њ —Б—В—А—Г–Ї—В—Г—А–љ—Л—Е –Є–Ј–Љ–µ–љ–µ–љ–Є–є –Љ–Њ—З–µ–њ–Њ–ї–Њ–≤—Л—Е –Њ—А–≥–∞–љ–Њ–≤, —З–∞—Й–µ –≤—Б–µ–≥–Њ –њ—А–µ–і—Б—В–∞—В–µ–ї—М–љ–Њ–є –ґ–µ–ї–µ–Ј—Л.
–Т—Б–µ –љ–µ–Њ—Б–ї–Њ–ґ–љ–µ–љ–љ—Л–µ –≤–љ–µ–±–Њ–ї—М–љ–Є—З–љ—Л–µ –Є–љ—Д–µ–Ї—Ж–Є–Є –Ь–Т–Я —Е–∞—А–∞–Ї—В–µ—А–Є–Ј—Г—О—В—Б—П –Њ–і–Є–љ–∞–Ї–Њ–≤–Њ–є —Н—В–Є–Њ–ї–Њ–≥–Є–µ–є —Б –њ—А–µ–Њ–±–ї–∞–і–∞–љ–Є–µ–Љ Escherichia coli, —Б—Е–Њ–і–љ—Л–Љ —Г—А–Њ–≤–љ–µ–Љ –∞–љ—В–Є–±–Є–Њ—В–Є–Ї–Њ—А–µ–Ј–Є—Б—В–µ–љ—В–љ–Њ—Б—В–Є —Г—А–Њ–њ–∞—В–Њ–≥–µ–љ–Њ–≤ –≤ –Ї–Њ–љ–Ї—А–µ—В–љ–Њ–Љ —А–µ–≥–Є–Њ–љ–µ, –љ–Є–Ј–Ї–Є–Љ —А–Є—Б–Ї–Њ–Љ —А–∞–Ј–≤–Є—В–Є—П –Њ—Б–ї–Њ–ґ–љ–µ–љ–Є–є. –≠—Д—Д–µ–Ї—В –∞–љ—В–Є–±–∞–Ї—В–µ—А–Є–∞–ї—М–љ–Њ–є —В–µ—А–∞–њ–Є–Є –љ–µ–Њ—Б–ї–Њ–ґ–љ–µ–љ–љ—Л—Е –Є–љ—Д–µ–Ї—Ж–Є–є –Ь–Т–Я, –Ї–∞–Ї –њ—А–∞–≤–Є–ї–Њ, –і–Њ—Б—В–Є–≥–∞–µ—В—Б—П –њ—А–Є —Н–Љ–њ–Є—А–Є—З–µ—Б–Ї–Њ–Љ –љ–∞–Ј–љ–∞—З–µ–љ–Є–Є –∞–љ—В–Є–±–Є–Њ—В–Є–Ї–Њ–≤ –Ї–Њ—А–Њ—В–Ї–Є–Љ–Є –Ї—Г—А—Б–∞–Љ–Є.
–Т –љ–∞—Б—В–Њ—П—Й–µ–є —А–∞–±–Њ—В–µ –±—Г–і—Г—В –Њ–±—Б—Г–ґ–і–µ–љ—Л –њ—А–Њ–±–ї–µ–Љ—Л –і–Є–∞–≥–љ–Њ—Б—В–Є–Ї–Є, –∞–љ—В–Є–±–∞–Ї—В–µ—А–Є–∞–ї—М–љ–Њ–є —В–µ—А–∞–њ–Є–Є –Є –њ—А–Њ—Д–Є–ї–∞–Ї—В–Є–Ї–Є –Њ—Б—В—А—Л—Е –Є —А–µ—Ж–Є–і–Є–≤–Є—А—Г—О—Й–Є—Е –љ–µ–Њ—Б–ї–Њ–ґ–љ–µ–љ–љ—Л—Е –Є–љ—Д–µ–Ї—Ж–Є–є –Ь–Т–Я —Г –ґ–µ–љ—Й–Є–љ, —Г—З–Є—В—Л–≤–∞—П —А–Њ—Б—Б–Є–є—Б–Ї–Є–µ –Њ—Б–Њ–±–µ–љ–љ–Њ—Б—В–Є —Н—В–Є–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Њ–є —Б—В—А—Г–Ї—В—Г—А—Л –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є–є –Є —Г—А–Њ–≤–љ—П –∞–љ—В–Є–±–Є–Њ—В–Є–Ї–Њ—А–µ–Ј–Є—Б—В–µ–љ—В–љ–Њ—Б—В–Є –≤–Њ–Ј–±—Г–і–Є—В–µ–ї–µ–є. –Ґ–∞–Ї–ґ–µ –±—Г–і—Г—В –њ—А–Є–≤–µ–і–µ–љ—Л —А–µ–Ї–Њ–Љ–µ–љ–і–∞—Ж–Є–Є –њ–Њ –ї–µ—З–µ–љ–Є—О –Є–љ—Д–µ–Ї—Ж–Є–є –Ь–Т–Я —Г –±–µ—А–µ–Љ–µ–љ–љ—Л—Е –ґ–µ–љ—Й–Є–љ (–Ї–Њ—В–Њ—А—Л–µ, –Њ–і–љ–∞–Ї–Њ, –≤ –±–Њ–ї—М—И–µ–є —Б—В–µ–њ–µ–љ–Є –Љ–Њ–ґ–љ–Њ –Њ—В–љ–µ—Б—В–Є –Ї –Њ—Б–ї–Њ–ґ–љ–µ–љ–љ—Л–Љ –Є–љ—Д–µ–Ї—Ж–Є—П–Љ) –Є —В–∞–Ї—В–Є–Ї–µ –≤–µ–і–µ–љ–Є—П –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –±–µ—Б—Б–Є–Љ–њ—В–Њ–Љ–љ–Њ–є –±–∞–Ї—В–µ—А–Є—Г—А–Є–µ–є.
–†–µ–Ї–Њ–Љ–µ–љ–і–∞—Ж–Є–Є –њ–Њ –і–Є–∞–≥–љ–Њ—Б—В–Є–Ї–µ –Є —В–µ—А–∞–њ–Є–Є –љ–µ–Њ—Б–ї–Њ–ґ–љ–µ–љ–љ—Л—Е –Є–љ—Д–µ–Ї—Ж–Є–є –Ь–Т–Я –њ—А–Є–≤–µ–і–µ–љ—Л —Б —Г—З–µ—В–Њ–Љ —А–µ–Ї–Њ–Љ–µ–љ–і–∞—Ж–Є–є –Х–≤—А–Њ–њ–µ–є—Б–Ї–Њ–є –∞—Б—Б–Њ—Ж–Є–∞—Ж–Є–Є —Г—А–Њ–ї–Њ–≥–Њ–≤ 2001 –Є 2006 –≥–≥. [2–3] –Є —А–µ–Ї–Њ–Љ–µ–љ–і–∞—Ж–Є–є –Р–Љ–µ—А–Є–Ї–∞–љ—Б–Ї–Њ–≥–Њ –Њ–±—Й–µ—Б—В–≤–∞ –Є–љ—Д–µ–Ї—Ж–Є–Њ–љ–љ—Л—Е –±–Њ–ї–µ–Ј–љ–µ–є (IDSA) 1999 –≥. [4].
–Ф–Є–∞–≥–љ–Њ—Б—В–Є–Ї–∞
–° –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є—Е –њ–Њ–Ј–Є—Ж–Є–є –≤–∞–ґ–љ–Њ –і–Є—Д—Д–µ—А–µ–љ—Ж–Є—А–Њ–≤–∞—В—М –љ–µ–Њ—Б–ї–Њ–ґ–љ–µ–љ–љ—Л–µ –Є –Њ—Б–ї–Њ–ґ–љ–µ–љ–љ—Л–µ –Є–љ—Д–µ–Ї—Ж–Є–Є –Ь–Т–Я, —В–∞–Ї –Ї–∞–Ї –Њ–љ–Є —А–∞–Ј–ї–Є—З–∞—О—В—Б—П –њ–Њ –њ—А–Њ–≥–љ–Њ–Ј—Г –Є —В–∞–Ї—В–Є–Ї–µ –∞–љ—В–Є–±–∞–Ї—В–µ—А–Є–∞–ї—М–љ–Њ–є —В–µ—А–∞–њ–Є–Є. –Я—А–Є –љ–µ–Њ—Б–ї–Њ–ґ–љ–µ–љ–љ—Л—Е –Є–љ—Д–µ–Ї—Ж–Є—П—Е –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є–є —Н—Д—Д–µ–Ї—В –Є —Н—А–∞–і–Є–Ї–∞—Ж–Є—П –≤–Њ–Ј–±—Г–і–Є—В–µ–ї—П –і–Њ—Б—В–Є–≥–∞—О—В—Б—П –Ї–∞–Ї –њ—А–∞–≤–Є–ї–Њ, –њ—А–Є –Ї–Њ—А–Њ—В–Ї–Є—Е –Ї—Г—А—Б–∞—Е –∞–љ—В–Є–±–∞–Ї—В–µ—А–Є–∞–ї—М–љ–Њ–є —В–µ—А–∞–њ–Є–Є. –Ъ—А–Њ–Љ–µ —В–Њ–≥–Њ, –њ—А–Є –љ–µ–Њ—Б–ї–Њ–ґ–љ–µ–љ–љ—Л—Е –Є–љ—Д–µ–Ї—Ж–Є—П—Е –љ–µ —В—А–µ–±—Г–µ—В—Б—П —А—Г—В–Є–љ–љ–Њ –њ—А–Њ–≤–Њ–і–Є—В—М –Љ–Є–Ї—А–Њ–±–Є–Њ–ї–Њ–≥–Є—З–µ—Б–Ї—Г—О –і–Є–∞–≥–љ–Њ—Б—В–Є–Ї—Г –Є –ї–∞–±–Њ—А–∞—В–Њ—А–љ—Л–є –Ї–Њ–љ—В—А–Њ–ї—М –Є–Ј–ї–µ—З–µ–љ–Є—П. –Ю—Б–ї–Њ–ґ–љ–µ–љ–љ—Л–µ –Є–љ—Д–µ–Ї—Ж–Є–Є –Ь–Т–Я –∞—Б—Б–Њ—Ж–Є–Є—А—Г—О—В—Б—П —Б –љ–∞–ї–Є—З–Є–µ–Љ —Д–∞–Ї—В–Њ—А–Њ–≤, –њ—А–µ–і—А–∞—Б–њ–Њ–ї–∞–≥–∞—О—Й–Є—Е –Ї –Є—Е —А–∞–Ј–≤–Є—В–Є—О, –і–ї–Є—В–µ–ї—М–љ–Њ–Љ—Г —Б–Њ—Е—А–∞–љ–µ–љ–Є—О —Б–Є–Љ–њ—В–Њ–Љ–Њ–≤, –≤–Њ–Ј–љ–Є–Ї–љ–Њ–≤–µ–љ–Є—О –Њ—Б–ї–Њ–ґ–љ–µ–љ–Є–є –Є –љ–µ—Г—Б–њ–µ—Е—Г –∞–љ—В–Є–±–∞–Ї—В–µ—А–Є–∞–ї—М–љ–Њ–є —В–µ—А–∞–њ–Є–Є. –Ъ —Д–∞–Ї—В–Њ—А–∞–Љ, –∞—Б—Б–Њ—Ж–Є–Є—А–Њ–≤–∞–љ–љ—Л–Љ —Б –Њ—Б–ї–Њ–ґ–љ–µ–љ–љ—Л–Љ–Є –Є–љ—Д–µ–Ї—Ж–Є—П–Љ–Є –Љ–Њ—З–µ–≤—Л–≤–Њ–і—П—Й–Є—Е –њ—Г—В–µ–є, –Њ—В–љ–Њ—Б—П—В—Б—П:
• –Ь—Г–ґ—З–Є–љ—Л
• –Я–Њ–ґ–Є–ї—Л–µ
• –Ш–љ—Д–µ–Ї—Ж–Є—П, —А–∞–Ј–≤–Є–≤—И–∞—П—Б—П –≤ —Б—В–∞—Ж–Є–Њ–љ–∞—А–µ
• –С–µ—А–µ–Љ–µ–љ–љ–Њ—Б—В—М
• –Э–∞–ї–Є—З–Є–µ –Љ–Њ—З–µ–≤–Њ–≥–Њ –Ї–∞—В–µ—В–µ—А–∞
• –Э–µ–і–∞–≤–љ–Њ –њ–µ—А–µ–љ–µ—Б–µ–љ–љ–∞—П –Њ–њ–µ—А–∞—Ж–Є—П –љ–∞ –Њ—А–≥–∞–љ–∞—Е –Љ–Њ—З–µ–њ–Њ–ї–Њ–≤–Њ–є —Б–Є—Б—В–µ–Љ—Л
• –§—Г–љ–Ї—Ж–Є–Њ–љ–∞–ї—М–љ—Л–µ –Є–ї–Є –∞–љ–∞—В–Њ–Љ–Є—З–µ—Б–Ї–Є–µ –љ–∞—А—Г—И–µ–љ–Є—П –Љ–Њ—З–µ–≤—Л—Е –њ—Г—В–µ–є
• –Э–µ–і–∞–≤–љ–µ–µ –њ—А–Є–Љ–µ–љ–µ–љ–Є–µ –∞–љ—В–Є–±–Є–Њ—В–Є–Ї–Њ–≤
• –°–Њ—Е—А–∞–љ–µ–љ–Є–µ —Б–Є–Љ–њ—В–Њ–Љ–Њ–≤ –±–Њ–ї–µ–µ 7 –і–љ–µ–є
• –°–∞—Е–∞—А–љ—Л–є –і–Є–∞–±–µ—В
• –Ш–Љ–Љ—Г–љ–Њ—Б—Г–њ—А–µ—Б—Б–Є—П.
–Ґ–∞–Ї–ґ–µ —Ж–µ–ї–µ—Б–Њ–Њ–±—А–∞–Ј–љ–Њ –≤—Л–і–µ–ї—П—В—М –±–µ—Б—Б–Є–Љ–њ—В–Њ–Љ–љ—Г—О –±–∞–Ї—В–µ—А–Є—Г—А–Є—О, –Ї–Њ—В–Њ—А–∞—П —З–∞—Б—В–Њ –≤—Л—П–≤–ї—П–µ—В—Б—П —Г –Њ–њ—А–µ–і–µ–ї–µ–љ–љ—Л—Е –Ї–∞—В–µ–≥–Њ—А–Є–є –њ–∞—Ж–Є–µ–љ—В–Њ–≤ (–њ–Њ–ґ–Є–ї—Л–µ, –±–µ—А–µ–Љ–µ–љ–љ—Л–µ –ґ–µ–љ—Й–Є–љ—Л, –љ–∞–ї–Є—З–Є–µ –њ–Њ—Б—В–Њ—П–љ–љ–Њ–≥–Њ –Љ–Њ—З–µ–≤–Њ–≥–Њ –Ї–∞—В–µ—В–µ—А–∞, –±–Њ–ї—М–љ—Л–µ —Б–∞—Е–∞—А–љ—Л–Љ –і–Є–∞–±–µ—В–Њ–Љ), –Є —В—А–µ–±—Г–µ—В —А–µ—И–µ–љ–Є—П –≤–Њ–њ—А–Њ—Б–∞ –Њ —Ж–µ–ї–µ—Б–Њ–Њ–±—А–∞–Ј–љ–Њ—Б—В–Є –њ—А–Њ–≤–µ–і–µ–љ–Є—П –∞–љ—В–Є–±–∞–Ї—В–µ—А–Є–∞–ї—М–љ–Њ–є —В–µ—А–∞–њ–Є–Є. –С–µ—Б—Б–Є–Љ–њ—В–Њ–Љ–љ–∞—П –±–∞–Ї—В–µ—А–Є—Г—А–Є—П —А–µ–і–Ї–Њ –∞—Б—Б–Њ—Ж–Є–Є—А—Г–µ—В—Б—П —Б –љ–µ–±–ї–∞–≥–Њ–њ—А–Є—П—В–љ—Л–Љ–Є –њ–Њ—Б–ї–µ–і—Б—В–≤–Є—П–Љ–Є –Є –љ–µ–љ–∞–Ј–љ–∞—З–µ–љ–Є–µ –∞–љ—В–Є–±–Є–Њ—В–Є–Ї–Њ–≤ –љ–µ —Б–Њ–њ—А–Њ–≤–Њ–ґ–і–∞–µ—В—Б—П –њ–Њ–≤—Л—И–µ–љ–љ—Л–Љ —А–Є—Б–Ї–Њ–Љ —А–∞–Ј–≤–Є—В–Є—П –Є–љ—Д–µ–Ї—Ж–Є–є —Г –±–Њ–ї—М—И–Є–љ—Б—В–≤–∞ –њ–∞—Ж–Є–µ–љ—В–Њ–≤.
–Ф–Є–∞–≥–љ–Њ—Б—В–Є–Ї–∞ –љ–µ–Њ—Б–ї–Њ–ґ–љ–µ–љ–љ—Л—Е –Є–љ—Д–µ–Ї—Ж–Є–є –Ь–Т–Я –Њ—Б–љ–Њ–≤–∞–љ–∞ –љ–∞ –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Њ–є –Ї–∞—А—В–Є–љ–µ –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П. –Ю—Б—В—А—Л–є —Ж–Є—Б—В–Є—В –Њ–±—Л—З–љ–Њ —Б–Њ–њ—А–Њ–≤–Њ–ґ–і–∞–µ—В—Б—П —В–∞–Ї–Є–Љ–Є —Б–Є–Љ–њ—В–Њ–Љ–∞–Љ–Є, –Ї–∞–Ї –і–Є–Ј—Г—А–Є—П, —А–µ–Ј–Є –Є –±–Њ–ї–Є –њ—А–Є –Љ–Њ—З–µ–Є—Б–њ—Г—Б–Ї–∞–љ–Є–Є, —Г—З–∞—Й–µ–љ–љ–Њ–µ –Љ–Њ—З–µ–Є—Б–њ—Г—Б–Ї–∞–љ–Є–µ, –њ–Њ–Ј—Л–≤—Л –љ–∞ –Љ–Њ—З–µ–Є—Б–њ—Г—Б–Ї–∞–љ–Є–µ, –±–Њ–ї–Є –≤ –љ–∞–і–ї–Њ–±–Ї–Њ–≤–Њ–є –Њ–±–ї–∞—Б—В–Є. –Я—А–Є–Љ–µ—А–љ–Њ —Г 40% –ґ–µ–љ—Й–Є–љ —Б –Њ—Б—В—А—Л–Љ —Ж–Є—Б—В–Є—В–Њ–Љ –љ–∞–±–ї—О–і–∞–µ—В—Б—П –≥–µ–Љ–∞—В—Г—А–Є—П, –Ї–Њ—В–Њ—А–∞—П –љ–µ —П–≤–ї—П–µ—В—Б—П –њ—А–Є–Ј–љ–∞–Ї–Њ–Љ –Њ—Б–ї–Њ–ґ–љ–µ–љ–љ–Њ–є –Є–љ—Д–µ–Ї—Ж–Є–Є. –Ю—Б—В—А–Њ –≤–Њ–Ј–љ–Є–Ї—И–∞—П –і–Є–Ј—Г—А–Є—П —Г –ґ–µ–љ—Й–Є–љ —В—А–µ–±—Г–µ—В –Є—Б–Ї–ї—О—З–µ–љ–Є—П –і—А—Г–≥–Є—Е —Б–Є–Љ–њ—В–Њ–Љ–Њ–—Б—Е–Њ–і–љ—Л—Е –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є–є – –Њ—Б—В—А—Л–є —Г—А–µ—В—А–Є—В, –≤—Л–Ј–≤–∞–љ–љ—Л–є Chlamydia trachomatis, Neisseria gonorrhoeae –Є–ї–Є –≤–Є—А—Г—Б–Њ–Љ –њ—А–Њ—Б—В–Њ–≥–Њ –≥–µ—А–њ–µ—Б–∞, –Є–ї–Є –≤–∞–≥–Є–љ–Є—В, –≤—Л–Ј–≤–∞–љ–љ—Л–є Candida spp. –Є–ї–Є Trichomonas vaginalis. –Я—А–Є –Њ—Б—В—А–Њ–Љ —Ж–Є—Б—В–Є—В–µ –Є –њ–Є–µ–ї–Њ–љ–µ—Д—А–Є—В–µ –≤ –Њ–±—Й–µ–Љ –∞–љ–∞–ї–Є–Ј–µ –Љ–Њ—З–Є –≤—Б–µ–≥–і–∞ –≤—Л—П–≤–ї—П–µ—В—Б—П –њ–Є—Г—А–Є—П –Є –±–∞–Ї—В–µ—А–Є—Г—А–Є—П (—В–∞–±–ї. 1). –Ю—В—Б—Г—В—Б—В–≤–Є–µ –њ–Є—Г—А–Є–Є —Б–≤–Є–і–µ—В–µ–ї—М—Б—В–≤—Г–µ—В –≤ –њ–Њ–ї—М–Ј—Г –і—А—Г–≥–Њ–≥–Њ –і–Є–∞–≥–љ–Њ–Ј–∞. –Т —В–Њ –ґ–µ –≤—А–µ–Љ—П —Б–ї–µ–і—Г–µ—В –≤—Л–і–µ–ї—П—В—М –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є–µ —Б–Є—В—Г–∞—Ж–Є–Є, –≤ –Ї–Њ—В–Њ—А—Л—Е –њ—А–Є –љ–∞–ї–Є—З–Є–Є –њ–Є—Г—А–Є–Є –≤ –∞–љ–∞–ї–Є–Ј–µ –Љ–Њ—З–Є –љ–µ –Њ–њ—А–µ–і–µ–ї—П—О—В—Б—П –±–∞–Ї—В–µ—А–Є–Є –Љ–Є–Ї—А–Њ—Б–Ї–Њ–њ–Є—З–µ—Б–Ї–Є –Є–ї–Є –њ—А–Є –±–∞–Ї—В–µ—А–Є–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Њ–Љ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є (—В–∞–±–ї. 2). –≠—В–Є —Б–Є—В—Г–∞—Ж–Є–Є —В—А–µ–±—Г—О—В –њ—А–Њ–≤–µ–і–µ–љ–Є—П –і–Њ–њ–Њ–ї–љ–Є—В–µ–ї—М–љ–Њ–≥–Њ –Њ–±—Б–ї–µ–і–Њ–≤–∞–љ–Є—П –њ–∞—Ж–Є–µ–љ—В–Њ–≤.
–Ґ—А–∞–і–Є—Ж–Є–Њ–љ–љ—Л–є –Ї–Њ–ї–Є—З–µ—Б—В–≤–µ–љ–љ—Л–є –Ї—А–Є—В–µ—А–Є–є –і–Є–∞–≥–љ–Њ–Ј–∞ –Њ—Б—В—А–Њ–є –Є–љ—Д–µ–Ї—Ж–Є–Є –Љ–Њ—З–µ–≤—Л–≤–Њ–і—П—Й–Є—Е –њ—Г—В–µ–є >105 –Ї–Њ–ї–Њ–љ–Є–µ–Њ–±—А–∞–Ј—Г—О—Й–Є—Е –µ–і–Є–љ–Є—Ж (–Ъ–Ю–Х) –Љ–Є–Ї—А–Њ–Њ—А–≥–∞–љ–Є–Ј–Љ–Њ–≤ –≤ —Б—А–µ–і–љ–µ–є –њ–Њ—А—Ж–Є–Є –Љ–Њ—З–Є –≤ –њ–Њ—Б–ї–µ–і–љ–Є–µ –≥–Њ–і—Л –њ–µ—А–µ—Б–Љ–Њ—В—А–µ–љ. –С—Л–ї–Њ –њ–Њ–Ї–∞–Ј–∞–љ–Њ, —З—В–Њ –њ—А–Є–Љ–µ—А–љ–Њ —Г 1/3 –ґ–µ–љ—Й–Є–љ —Б –і–Њ–Ї—Г–Љ–µ–љ—В–Є—А–Њ–≤–∞–љ–љ—Л–Љ –і–Є–∞–≥–љ–Њ–Ј–Њ–Љ –Њ—Б—В—А–Њ–≥–Њ —Ж–Є—Б—В–Є—В–∞ –љ–∞–±–ї—О–і–∞–µ—В—Б—П –±–∞–Ї—В–µ—А–Є—Г—А–Є—П <105 –Ъ–Ю–Х/–Љ–ї [5]. –Ф–ї—П –і–Є–∞–≥–љ–Њ—Б—В–Є–Ї–Є –Њ—Б—В—А–Њ–≥–Њ —Ж–Є—Б—В–Є—В–∞ —А–µ–Ї–Њ–Љ–µ–љ–і—Г–µ—В—Б—П —Г—З–Є—В—Л–≤–∞—В—М –±–∞–Ї—В–µ—А–Є—Г—А–Є—О >102 –Ъ–Ю–Х/–Љ–ї. –Я—А–Њ–≤–µ–і–µ–љ–Є–µ –±–∞–Ї—В–µ—А–Є–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Њ–≥–Њ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П –Љ–Њ—З–Є (–≤—Л–і–µ–ї–µ–љ–Є–µ —З–Є—Б—В–Њ–є –Ї—Г–ї—М—В—Г—А—Л –≤–Њ–Ј–±—Г–і–Є—В–µ–ї—П –Є –Њ–њ—А–µ–і–µ–ї–µ–љ–Є–µ —З—Г–≤—Б—В–≤–Є—В–µ–ї—М–љ–Њ—Б—В–Є –Ї –∞–љ—В–Є–±–Є–Њ—В–Є–Ї–∞–Љ) —Г –љ–µ–±–µ—А–µ–Љ–µ–љ–љ—Л—Е –ґ–µ–љ—Й–Є–љ —Б –Њ—Б—В—А—Л–Љ —Ж–Є—Б—В–Є—В–Њ–Љ –љ–µ —А–µ–Ї–Њ–Љ–µ–љ–і—Г–µ—В—Б—П, —В–∞–Ї –Ї–∞–Ї —Н—В–Є–Њ–ї–Њ–≥–Є—П –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П –Є –∞–љ—В–Є–±–Є–Њ—В–Є–Ї–Њ—З—Г–≤—Б—В–≤–Є—В–µ–ї—М–љ–Њ—Б—В—М –≤–Њ–Ј–±—Г–і–Є—В–µ–ї–µ–є —Е–Њ—А–Њ—И–Њ –њ—А–Њ–≥–љ–Њ–Ј–Є—А—Г—О—В—Б—П.
–†–µ—Ж–Є–і–Є–≤–Є—А—Г—О—Й–∞—П –љ–µ–Њ—Б–ї–Њ–ґ–љ–µ–љ–љ–∞—П –Є–љ—Д–µ–Ї—Ж–Є—П –Ь–Т–Я –Њ–њ—А–µ–і–µ–ї—П–µ—В—Б—П –Ї–∞–Ї —В—А–Є –Є –±–Њ–ї–µ–µ —Н–њ–Є–Ј–Њ–і–Њ–≤ –Њ—Б—В—А–Њ–є –Є–љ—Д–µ–Ї—Ж–Є–Є –≤ –њ–Њ—Б–ї–µ–і–љ–Є–µ 12 –Љ–µ—Б—П—Ж–µ–≤ –Є–ї–Є –і–≤–∞ –Є –±–Њ–ї–µ–µ —Н–њ–Є–Ј–Њ–і–∞ –≤ –њ–Њ—Б–ї–µ–і–љ–Є–µ 6 –Љ–µ—Б—П—Ж–µ–≤.
–Т –Њ—В–ї–Є—З–Є–µ –Њ—В –Њ—Б—В—А–Њ–≥–Њ —Ж–Є—Б—В–Є—В–∞, –Њ—Б—В—А—Л–є –њ–Є–µ–ї–Њ–љ–µ—Д—А–Є—В —Е–∞—А–∞–Ї—В–µ—А–Є–Ј—Г–µ—В—Б—П —Б–Є–Љ–њ—В–Њ–Љ–∞–Љ–Є –≥–µ–љ–µ—А–∞–ї–Є–Ј–Њ–≤–∞–љ–љ–Њ–є –Є–љ—Д–µ–Ї—Ж–Є–Є (–≥–µ–Ї—В–Є—З–µ—Б–Ї–∞—П –ї–Є—Е–Њ—А–∞–і–Ї–∞, –Њ–Ј–љ–Њ–±—Л) –Є –Є–љ—В–Њ–Ї—Б–Є–Ї–∞—Ж–Є–Є (–≥–Њ–ї–Њ–≤–љ–∞—П –±–Њ–ї—М, —В–Њ—И–љ–Њ—В–∞, —А–≤–Њ—В–∞); —В–∞–Ї–ґ–µ –Њ–±—Л—З–љ–Њ –љ–∞–±–ї—О–і–∞—О—В—Б—П –±–Њ–ї–Є –≤ –њ–Њ—П—Б–љ–Є—З–љ–Њ–є –Њ–±–ї–∞—Б—В–Є. –Я—А–Є —Н—В–Њ–Љ —Б–Є–Љ–њ—В–Њ–Љ—Л —Ж–Є—Б—В–Є—В–∞ –Љ–Њ–≥—Г—В –њ—А–Є—Б—Г—В—Б—В–≤–Њ–≤–∞—В—М –Є–ї–Є –Њ—В—Б—Г—В—Б—В–≤–Њ–≤–∞—В—М. –Т –∞–љ–∞–ї–Є–Ј–µ –Љ–Њ—З–Є –≤—Б–µ–≥–і–∞ –љ–∞–±–ї—О–і–∞–µ—В—Б—П –њ–Є—Г—А–Є—П. –Ъ–ї–Є–љ–Є—З–µ—Б–Ї–Є –Ј–љ–∞—З–Є–Љ–Њ–є –±–∞–Ї—В–µ—А–Є—Г—А–Є–µ–є —Б—З–Є—В–∞–µ—В—Б—П >103 –Ъ–Ю–Х/–Љ–ї. –Ф–Њ–њ–Њ–ї–љ–Є—В–µ–ї—М–љ–Њ–µ –Њ–±—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ –њ—А–Є –њ–Є–µ–ї–Њ–љ–µ—Д—А–Є—В–µ —Ж–µ–ї–µ—Б–Њ–Њ–±—А–∞–Ј–љ–Њ –і–ї—П –≤—Л—П–≤–ї–µ–љ–Є—П –Њ–±—Б—В—А—Г–Ї—Ж–Є–Є –Ь–Т–Я, —Г—А–Њ–ї–Є—В–Є–∞–Ј–∞ (–£–Ч–Ш, –Ъ–Ґ). –Я—А–Є –Њ—В—Б—Г—В—Б—В–≤–Є–Є —Н—Д—Д–µ–Ї—В–∞ –Њ—В –∞–і–µ–Ї–≤–∞—В–љ–Њ–є –∞–љ—В–Є–±–∞–Ї—В–µ—А–Є–∞–ї—М–љ–Њ–є —В–µ—А–∞–њ–Є–Є –≤ —В–µ—З–µ–љ–Є–µ 72 —З–∞—Б–Њ–≤ –љ–µ–Њ–±—Е–Њ–і–Є–Љ–Њ –і–∞–ї—М–љ–µ–є—И–µ–µ –Њ–±—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ –і–ї—П –Є—Б–Ї–ї—О—З–µ–љ–Є—П –≤–Њ–Ј–Љ–Њ–ґ–љ—Л—Е –Њ—Б–ї–Њ–ґ–љ—П—О—Й–Є—Е —Д–∞–Ї—В–Њ—А–Њ–≤ (—Г—А–Њ–ї–Є—В–Є–∞–Ј, –∞–±—Б—Ж–µ—Б—Б).
–Ф–Є–∞–≥–љ–Њ—Б—В–Є—З–µ—Б–Ї–Є –Ј–љ–∞—З–Є–Љ—Л–Љ —Г—А–Њ–≤–љ–µ–Љ –±–∞–Ї—В–µ—А–Є—Г—А–Є–Є –і–ї—П –њ–Њ—Б—В–∞–љ–Њ–≤–Ї–Є –і–Є–∞–≥–љ–Њ–Ј–∞ «–±–µ—Б—Б–Є–Љ–њ—В–Њ–Љ–љ–∞—П –±–∞–Ї—В–µ—А–Є—Г—А–Є—П» —Б–ї–µ–і—Г–µ—В —Б—З–Є—В–∞—В—М >104 –Ъ–Ю–Х/–Љ–ї –Љ–Є–Ї—А–Њ–Њ—А–≥–∞–љ–Є–Ј–Љ–Њ–≤ –≤ –і–≤—Г—Е –њ–Њ—А—Ж–Є—П—Е –Љ–Њ—З–Є, —Б–Њ–±—А–∞–љ–љ—Л—Е —Б –Є–љ—В–µ—А–≤–∞–ї–Њ–Љ >24 —З–∞—Б–∞.
–≠—В–Є–Њ–ї–Њ–≥–Є—П
–≠—В–Є–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є–є —Б–њ–µ–Ї—В—А –≤–Њ–Ј–±—Г–і–Є—В–µ–ї–µ–є –Њ—Б—В—А—Л—Е –љ–µ–Њ—Б–ї–Њ–ґ–љ–µ–љ–љ—Л—Е –Є–љ—Д–µ–Ї—Ж–Є–є –≤–µ—А—Е–љ–Є—Е (—Ж–Є—Б—В–Є—В) –Є –љ–Є–ґ–љ–Є—Е –Њ—В–і–µ–ї–Њ–≤ (–њ–Є–µ–ї–Њ–љ–µ—Д—А–Є—В) –Љ–Њ—З–µ–≤—Л–≤–Њ–і—П—Й–Є—Е –њ—Г—В–µ–є —Б—Е–Њ–і–µ–љ. –Ф–Њ–Љ–Є–љ–Є—А—Г—О—Й–Є–Љ –≤–Њ–Ј–±—Г–і–Є—В–µ–ї–µ–Љ —П–≤–ї—П–µ—В—Б—П Escherichia coli, –љ–∞ –і–Њ–ї—О –Ї–Њ—В–Њ—А–Њ–≥–Њ –њ—А–Є—Е–Њ–і–Є—В—Б—П 70–95% —Б–ї—Г—З–∞–µ–≤ –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є–є. –Т 5–19% –≤—Л–і–µ–ї—П—О—В—Б—П –Ї–Њ–∞–≥—Г–ї–∞–Ј–Њ–љ–µ–≥–∞—В–Є–≤–љ—Л–µ —Б—В–∞—Д–Є–ї–Њ–Ї–Њ–Ї–Ї–Є (–≥–ї–∞–≤–љ—Л–Љ –Њ–±—А–∞–Ј–Њ–Љ Staphylococcus saprophyticus). –Т –Њ—Б—В–∞–ї—М–љ—Л—Е —Б–ї—Г—З–∞—П—Е –≤–Њ–Ј–±—Г–і–Є—В–µ–ї—П–Љ–Є –Љ–Њ–≥—Г—В –±—Л—В—М –і—А—Г–≥–Є–µ —Н–љ—В–µ—А–Њ–±–∞–Ї—В–µ—А–Є–Є (Proteus mirabilis, Klebsiella spp.) –Є —Н–љ—В–µ—А–Њ–Ї–Њ–Ї–Ї–Є (Enterococcus faecalis) [2].
–°–ї–µ–і—Г–µ—В –≤—Л–і–µ–ї–Є—В—М –љ–µ–Ї–Њ—В–Њ—А—Л–µ –љ–∞—Ж–Є–Њ–љ–∞–ї—М–љ—Л–µ –Њ—Б–Њ–±–µ–љ–љ–Њ—Б—В–Є –≤ —Б–њ–µ–Ї—В—А–µ –≤–Њ–Ј–±—Г–і–Є—В–µ–ї–µ–є –Њ—Б—В—А—Л—Е –Є–љ—Д–µ–Ї—Ж–Є–є –Ь–Т–Я. –Я—А–Є –∞–љ–∞–ї–Є–Ј–µ –±–Њ–ї–µ–µ 1000 —И—В–∞–Љ–Љ–Њ–≤ –Љ–Є–Ї—А–Њ–Њ—А–≥–∞–љ–Є–Ј–Љ–Њ–≤, –њ–Њ–ї—Г—З–µ–љ–љ—Л—Е –Њ—В –∞–Љ–±—Г–ї–∞—В–Њ—А–љ—Л—Е –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –Њ—Б—В—А—Л–Љ–Є –Љ–Њ—З–µ–≤—Л–Љ–Є –Є–љ—Д–µ–Ї—Ж–Є—П–Љ–Є –≤ –≥. –Ь–Њ—Б–Ї–≤–µ –≤ 2004–2005 –≥–≥., –±—Л–ї–Њ —Г—Б—В–∞–љ–Њ–≤–ї–µ–љ–Њ, —З—В–Њ –љ–∞–Є–±–Њ–ї–µ–µ —З–∞—Б—В—Л–Љ–Є –≤–Њ–Ј–±—Г–і–Є—В–µ–ї—П–Љ–Є –±—Л–ї–Є –Љ–Є–Ї—А–Њ–Њ—А–≥–∞–љ–Є–Ј–Љ—Л —Б–µ–Љ–µ–є—Б—В–≤–∞ Enterobacteriaceae (68%), —Б—А–µ–і–Є –Ї–Њ—В–Њ—А—Л—Е –њ—А–µ–Њ–±–ї–∞–і–∞–ї–∞ E. coli – 53% [6]. –Т —В–Њ –ґ–µ –≤—А–µ–Љ—П –≤—Л—П–≤–ї–µ–љ –≤—Л—Б–Њ–Ї–Є–є —Г–і–µ–ї—М–љ—Л–є –≤–µ—Б —Н–љ—В–µ—А–Њ–Ї–Њ–Ї–Ї–Њ–≤ (18,7%), —Б—А–µ–і–Є –Ї–Њ—В–Њ—А—Л—Е –њ—А–µ–Њ–±–ї–∞–і–∞–ї Enterococcus faecalis (15%); –љ–∞ –і–Њ–ї—О –Ї–Њ–∞–≥—Г–ї–∞–Ј–Њ–љ–µ–≥–∞—В–Є–≤–љ—Л—Е —Б—В–∞—Д–Є–ї–Њ–Ї–Њ–Ї–Ї–Њ–≤ –њ—А–Є—Е–Њ–і–Є–ї–Њ—Б—М 7,5%. –Т –і—А—Г–≥–Њ–Љ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є, –њ—А–Њ–≤–µ–і–µ–љ–љ–Њ–Љ –≤ 3 –≥–Њ—А–Њ–і–∞—Е –†–§, –≤ —Н—В–Є–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Њ–є —Б—В—А—Г–Ї—В—Г—А–µ –Њ—Б—В—А–Њ–≥–Њ –љ–µ–Њ—Б–ї–Њ–ґ–љ–µ–љ–љ–Њ–≥–Њ —Ж–Є—Б—В–Є—В–∞ —Г –ґ–µ–љ—Й–Є–љ —В–∞–Ї–ґ–µ –Њ—В–Љ–µ—З–µ–љ –≤—Л—Б–Њ–Ї–Є–є —Г–і–µ–ї—М–љ—Л–є –≤–µ—Б –≥—А–∞–Љ–њ–Њ–ї–Њ–ґ–Є—В–µ–ї—М–љ–Њ–є –Љ–Є–Ї—А–Њ—Д–ї–Њ—А—Л: E. coli – 67%, –і—А—Г–≥–Є–µ –≥—А–∞–Љ–Њ—В—А–Є—Ж–∞—В–µ–ї—М–љ—Л–µ – 11%, S. saprophyticus – 13%, E. faecalis – 9% [7]. –Ґ–∞–Ї–Є–Љ –Њ–±—А–∞–Ј–Њ–Љ, –Њ—В–µ—З–µ—Б—В–≤–µ–љ–љ—Л–µ –і–∞–љ–љ—Л–µ —Б–≤–Є–і–µ—В–µ–ї—М—Б—В–≤—Г—О—В –Њ –љ–µ—Б–Ї–Њ–ї—М–Ї–Њ –Љ–µ–љ—М—И–µ–Љ —Г–і–µ–ї—М–љ–Њ–Љ –≤–µ—Б–µ E. coli –≤ —Н—В–Є–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Њ–є —Б—В—А—Г–Ї—В—Г—А–µ –Њ—Б—В—А—Л—Е –Є–љ—Д–µ–Ї—Ж–Є–є –Ь–Т–Я –Ј–∞ —Б—З–µ—В –≤–Њ–Ј—А–∞—Б—В–∞–љ–Є—П —А–Њ–ї–Є –≥—А–∞–Љ–њ–Њ–ї–Њ–ґ–Є—В–µ–ї—М–љ—Л—Е –Љ–Є–Ї—А–Њ–Њ—А–≥–∞–љ–Є–Ј–Љ–Њ–≤, –њ—А–µ–ґ–і–µ –≤—Б–µ–≥–Њ E. faecalis –Є S. saprophyticus.
–Р–љ—В–Є–±–Є–Њ—В–Є–Ї–Њ—А–µ–Ј–Є—Б—В–µ–љ—В–љ–Њ—Б—В—М
—Г—А–Њ–њ–∞—В–Њ–≥–µ–љ–Њ–≤
–Т –њ–Њ—Б–ї–µ–і–љ–Є–µ –≥–Њ–і—Л, –њ–Њ –і–∞–љ–љ—Л–Љ –Ј–∞—А—Г–±–µ–ґ–љ—Л—Е –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–є, –љ–∞–±–ї—О–і–∞—О—В—Б—П –Њ—В—З–µ—В–ї–Є–≤—Л–µ —В–µ–љ–і–µ–љ—Ж–Є–Є –Ї —А–Њ—Б—В—Г —Г—Б—В–Њ–є—З–Є–≤–Њ—Б—В–Є —Г—А–Њ–њ–∞—В–Њ–≥–µ–љ–љ—Л—Е —И—В–∞–Љ–Љ–Њ–≤ E. coli –Ї –∞–љ—В–Є–±–∞–Ї—В–µ—А–Є–∞–ї—М–љ—Л–Љ –њ—А–µ–њ–∞—А–∞—В–∞–Љ, –Ї–Њ—В–Њ—А—Л–µ —В—А–∞–і–Є—Ж–Є–Њ–љ–љ–Њ —И–Є—А–Њ–Ї–Њ –љ–∞–Ј–љ–∞—З–∞—О—В—Б—П –њ—А–Є –≤–љ–µ–±–Њ–ї—М–љ–Є—З–љ—Л—Е –Є–љ—Д–µ–Ї—Ж–Є—П—Е –Љ–Њ—З–µ–≤—Л–≤–Њ–і—П—Й–Є—Е –њ—Г—В–µ–є, –њ—А–µ–ґ–і–µ –≤—Б–µ–≥–Њ –Ї –∞–Љ–њ–Є—Ж–Є–ї–ї–Є–љ—Г (—Г—Б—В–Њ–є—З–Є–≤–Њ—Б—В—М >30%) –Є –Ї–Њ–—В—А–Є–Љ–Њ–Ї—Б–∞–Ј–Њ–ї—Г (20–30%), –љ–µ—Д—В–Њ—А–Є—А–Њ–≤–∞–љ–љ—Л–Љ —Е–Є–љ–Њ–ї–Њ–љ–∞–Љ (5–27%) [8–11]. –Э–µ–±–ї–∞–≥–Њ–њ—А–Є—П—В–љ–Њ–є —В–µ–љ–і–µ–љ—Ж–Є–µ–є —П–≤–ї—П–µ—В—Б—П –њ–Њ–≤—Л—И–µ–љ–Є–µ —Г—Б—В–Њ–є—З–Є–≤–Њ—Б—В–Є –Ї–Є—И–µ—З–љ–Њ–є –њ–∞–ї–Њ—З–Ї–Є —В–∞–Ї–ґ–µ –Ї –∞–Љ–Њ–Ї—Б–Є—Ж–Є–ї–ї–Є–љ/–Ї–ї–∞–≤—Г–ї–∞–љ–∞—В—Г –Є —Д—В–Њ—А–Є—А–Њ–≤–∞–љ–љ—Л–Љ —Е–Є–љ–Њ–ї–Њ–љ–∞–Љ (—Ж–Є–њ—А–Њ—Д–ї–Њ–Ї—Б–∞—Ж–Є–љ—Г, –љ–Њ—А—Д–ї–Њ–Ї—Б–∞—Ж–Є–љ—Г –Є –і—А.), –≤ –љ–µ–Ї–Њ—В–Њ—А—Л—Е —Б—В—А–∞–љ–∞—Е –Х–≤—А–Њ–њ—Л –і–Њ 9 –Є 15% —Б–Њ–Њ—В–≤–µ—В—Б—В–≤–µ–љ–љ–Њ [12]. –Э–∞–Є–Љ–µ–љ—М—И–Є–є —Г—А–Њ–≤–µ–љ—М —Г—Б—В–Њ–є—З–Є–≤–Њ—Б—В–Є E. coli –≤ –Х–≤—А–Њ–њ–µ –љ–∞–±–ї—О–і–∞–ї—Б—П –Ї —Ж–µ—Д–∞–ї–Њ—Б–њ–Њ—А–Є–љ–∞–Љ III –њ–Њ–Ї–Њ–ї–µ–љ–Є—П (—Ж–µ—Д–∞–і—А–Њ–Ї—Б–Є–ї—Г, –Љ–µ—Ж–Є–ї–ї–Є–љ–∞–Љ—Г), –≥–µ–љ—В–∞–Љ–Є—Ж–Є–љ—Г, —Д–Њ—Б—Д–Њ–Љ–Є—Ж–Є–љ—Г –Є –љ–Є—В—А–Њ—Д—Г—А–∞–љ—В–Њ–Є–љ—Г. –°—В–∞–±–Є–ї—М–љ–Њ –≤—Л—Б–Њ–Ї–∞—П —З—Г–≤—Б—В–≤–Є—В–µ–ї—М–љ–Њ—Б—В—М —Г—А–Њ–њ–∞—В–Њ–≥–µ–љ–Њ–≤ –Ї —Д–Њ—Б—Д–Њ–Љ–Є—Ж–Є–љ—Г –Є –љ–Є—В—А–Њ—Д—Г—А–∞–љ—В–Њ–Є–љ—Г –љ–∞ –њ—А–Њ—В—П–ґ–µ–љ–Є–Є –Љ–љ–Њ–≥–Є—Е –ї–µ—В –Њ—В–Љ–µ—З–µ–љ–∞ —В–∞–Ї–ґ–µ –≤ –і—А—Г–≥–Њ–Љ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є [13].
–Ш—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ –∞–љ—В–Є–±–Є–Њ—В–Є–Ї–Њ—З—Г–≤—Б—В–≤–Є—В–µ–ї—М–љ–Њ—Б—В–Є –≤–Њ–Ј–±—Г–і–Є—В–µ–ї–µ–є –Њ—Б—В—А—Л—Е –≤–љ–µ–±–Њ–ї—М–љ–Є—З–љ—Л—Е –Љ–Њ—З–µ–≤—Л—Е –Є–љ—Д–µ–Ї—Ж–Є–є –≤ –≥. –Ь–Њ—Б–Ї–≤–µ —В–∞–Ї–ґ–µ –њ–Њ–Ї–∞–Ј–∞–ї–Њ –≤—Л—Б–Њ–Ї–Є–є —Г—А–Њ–≤–µ–љ—М —Г—Б—В–Њ–є—З–Є–≤–Њ—Б—В–Є E. coli –Ї –∞–Љ–њ–Є—Ж–Є–ї–ї–Є–љ—Г (43,5%), –∞–Љ–њ–Є—Ж–Є–ї–ї–Є–љ/—Б—Г–ї—М–±–∞–Ї—В–∞–Љ—Г (28,5%), –Ї–Њ–—В—А–Є–Љ–Њ–Ї—Б–∞–Ј–Њ–ї—Г (31%), –љ–∞–ї–Є–і–Є–Ї—Б–Њ–≤–Њ–є –Ї–Є—Б–ї–Њ—В–µ (21%) –Є —Д—В–Њ—А—Е–Є–љ–Њ–ї–Њ–љ–∞–Љ – —Ж–Є–њ—А–Њ—Д–ї–Њ–Ї—Б–∞—Ж–Є–љ—Г (15,5%) –Є –ї–µ–≤–Њ—Д–ї–Њ–Ї—Б–∞—Ж–Є–љ—Г (15%) [6]. –Э–∞ —Н—В–Њ–Љ —Д–Њ–љ–µ —Б–Њ—Е—А–∞–љ—П–µ—В—Б—П –љ–Є–Ј–Ї–Є–є —Г—А–Њ–≤–µ–љ—М —Г—Б—В–Њ–є—З–Є–≤–Њ—Б—В–Є E. coli –Ї —Ж–µ—Д–∞–ї–Њ—Б–њ–Њ—А–Є–љ–∞–Љ III –њ–Њ–Ї–Њ–ї–µ–љ–Є—П –Є –љ–Є—В—А–Њ—Д—Г—А–∞–љ–∞–Љ (–≤ –њ—А–µ–і–µ–ї–∞—Е 5%). –°—А–µ–і–Є –љ–Є—В—А–Њ—Д—Г—А–∞–љ–Њ–≤ —Б–∞–Љ—Л–Љ –∞–Ї—В–Є–≤–љ—Л–Љ –њ—А–µ–њ–∞—А–∞—В–Њ–Љ –≤ –Њ—В–љ–Њ—И–µ–љ–Є–Є E. coli –Є –і—А—Г–≥–Є—Е Enterobacteriaceae –±—Л–ї —Д—Г—А–∞–Ј–Є–і–Є–љ –Ъ (–Ї–∞–ї–Є–µ–≤–∞—П —Б–Њ–ї—М —Д—Г—А–∞–Ј–Є–і–Є–љ–∞), –њ—А–Њ—Ж–µ–љ—В —З—Г–≤—Б—В–≤–Є—В–µ–ї—М–љ—Л—Е —И—В–∞–Љ–Љ–Њ–≤ –Ї –љ–µ–Љ—Г –±—Л–ї –≤—Л—И–µ, —З–µ–Љ –Ї —Д—Г—А–∞–Ј–Є–і–Є–љ—Г –Є –љ–Є—В—А–Њ—Д—Г—А–∞–љ—В–Њ–Є–љ—Г. –Я—А–µ–і—Б—В–∞–≤–Є—В–µ–ї–Є Enterobacteriaceae —Е–∞—А–∞–Ї—В–µ—А–Є–Ј–Њ–≤–∞–ї–Є—Б—М –Љ–µ–љ—М—И–µ–є —З—Г–≤—Б—В–≤–Є—В–µ–ї—М–љ–Њ—Б—В—М—О –Ї –∞–љ—В–Є–±–Є–Њ—В–Є–Ї–∞–Љ: —З–∞—Б—В–Њ—В–∞ —Г—Б—В–Њ–є—З–Є–≤—Л—Е —И—В–∞–Љ–Љ–Њ–≤ Klebsiella spp. –Ї –≥–µ–љ—В–∞–Љ–Є—Ж–Є–љ—Г, —Ж–µ—Д–Њ—В–∞–Ї—Б–Є–Љ—Г, —Ж–Є–њ—А–Њ—Д–ї–Њ–Ї—Б–∞—Ж–Є–љ—Г, –ї–µ–≤–Њ—Д–ї–Њ–Ї—Б–∞—Ж–Є–љ—Г –Є –љ–Є—В—А–Њ—Д—Г—А–∞–љ—В–Њ–Є–љ—Г —Б–Њ—Б—В–∞–≤–Є–ї–∞ —Б–Њ–Њ—В–≤–µ—В—Б—В–≤–µ–љ–љ–Њ 17, 17, 17, 21 –Є 67%, Proteus spp. – 18, 18, 18, 18 –Є 88%. –°—А–µ–і–Є —Б—В–∞—Д–Є–ї–Њ–Ї–Њ–Ї–Ї–Њ–≤ –≤—Б–µ —И—В–∞–Љ–Љ—Л —Б–Њ—Е—А–∞–љ—П–ї–Є —З—Г–≤—Б—В–≤–Є—В–µ–ї—М–љ–Њ—Б—В—М –Ї –љ–Є—В—А–Њ—Д—Г—А–∞–љ–∞–Љ, –љ–µ–≤—Л—Б–Њ–Ї–∞—П —Г—Б—В–Њ–є—З–Є–≤–Њ—Б—В—М –Њ—В–Љ–µ—З–µ–љ–∞ –Ї –Ї–Њ–—В—А–Є–Љ–Њ–Ї—Б–∞–Ј–Њ–ї—Г –Є –≥–µ–љ—В–∞–Љ–Є—Ж–Є–љ—Г (7%), –±–Њ–ї–µ–µ –≤—Л—Б–Њ–Ї–∞—П – –Ї –ї–µ–≤–Њ—Д–ї–Њ–Ї—Б–∞—Ж–Є–љ—Г (11%) –Є —Ж–Є–њ—А–Њ—Д–ї–Њ–Ї—Б–∞—Ж–Є–љ—Г (14%). –≠–љ—В–µ—А–Њ–Ї–Њ–Ї–Ї–Є —Е–∞—А–∞–Ї—В–µ—А–Є–Ј–Њ–≤–∞–ї–Є—Б—М —Е–Њ—А–Њ—И–µ–є —З—Г–≤—Б—В–≤–Є—В–µ–ї—М–љ–Њ—Б—В—М—О –Ї –∞–Љ–њ–Є—Ж–Є–ї–ї–Є–љ—Г –Є –љ–Є—В—А–Њ—Д—Г—А–∞–љ–∞–Љ (–љ–µ—В —Г—Б—В–Њ–є—З–Є–≤—Л—Е —И—В–∞–Љ–Љ–Њ–≤), –ї–µ–≤–Њ—Д–ї–Њ–Ї—Б–∞—Ж–Є–љ—Г (6%); —Г—Б—В–Њ–є—З–Є–≤–Њ—Б—В—М –Ї —Ж–Є–њ—А–Њ—Д–ї–Њ–Ї—Б–∞—Ж–Є–љ—Г –Є –≥–µ–љ—В–∞–Љ–Є—Ж–Є–љ—Г –±—Л–ї–∞ –≤—Л—И–µ (11 –Є 30%).
–Т –і—А—Г–≥–Њ–Љ –Љ–љ–Њ–≥–Њ—Ж–µ–љ—В—А–Њ–≤–Њ–Љ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є, –њ—А–Њ–≤–µ–і–µ–љ–љ–Њ–Љ –≤ —А–∞–Ј–ї–Є—З–љ—Л—Е —А–µ–≥–Є–Њ–љ–∞—Е –†–§, –≤—Л—Б–Њ–Ї–Є–є —Г—А–Њ–≤–µ–љ—М —Г—Б—В–Њ–є—З–Є–≤–Њ—Б—В–Є E. coli —В–∞–Ї–ґ–µ –Њ—В–Љ–µ—З–µ–љ –Ї –∞–Љ–њ–Є—Ж–Є–ї–ї–Є–љ—Г (37%), –Ї–Њ–—В—А–Є–Љ–Њ–Ї—Б–∞–Ј–Њ–ї—Г (21%); –Ї –і—А—Г–≥–Є–Љ –∞–љ—В–Є–±–∞–Ї—В–µ—А–Є–∞–ї—М–љ—Л–Љ –њ—А–µ–њ–∞—А–∞—В–∞–Љ —Г—Б—В–Њ–є—З–Є–≤–Њ—Б—В—М –±—Л–ї–∞ –љ–µ–≤—Л—Б–Њ–Ї–Њ–є: –љ–Њ—А—Д–ї–Њ–Ї—Б–∞—Ж–Є–љ, —Ж–Є–њ—А–Њ—Д–ї–Њ–Ї—Б–∞—Ж–Є–љ – 4%, –∞–Љ–Њ–Ї—Б–Є—Ж–Є–ї–ї–Є–љ/–Ї–ї–∞–≤—Г–ї–∞–љ–∞—В – 3%, —Ж–µ—Д—Г—А–Њ–Ї—Б–Є–Љ – 2%, –љ–Є—В—А–Њ—Д—Г—А–∞–љ—В–Њ–Є–љ – 1% [14].
–Т –љ–∞—И–µ–Љ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є [7] –љ–Є–Ј–Ї–Є–є —Г—А–Њ–≤–µ–љ—М —Г—Б—В–Њ–є—З–Є–≤–Њ—Б—В–Є –≤–љ–µ–±–Њ–ї—М–љ–Є—З–љ—Л—Е —И—В–∞–Љ–Љ–Њ–≤ E. coli –Њ—В–Љ–µ—З–µ–љ –Ї –≥–µ–љ—В–∞–Љ–Є—Ж–Є–љ—Г, —Ж–µ—Д–Њ—В–∞–Ї—Б–Є–Љ—Г, —Д—Г—А–∞–Ј–Є–і–Є–љ—Г –Ъ, —Ж–Є–њ—А–Њ—Д–ї–Њ–Ї—Б–∞—Ж–Є–љ—Г (—Б–Њ–Њ—В–≤–µ—В—Б—В–≤–µ–љ–љ–Њ 7,7%, 8,5%, 13% –Є 14,9%), –±–Њ–ї–µ–µ –≤—Л—Б–Њ–Ї–Є–є —Г—А–Њ–≤–µ–љ—М – –Ї –∞–Љ–Њ–Ї—Б–Є—Ж–Є–ї–ї–Є–љ/–Ї–ї–∞–≤—Г–ї–∞–љ–∞—В—Г (19,1%), –Ї–Њ–—В—А–Є–Љ–Њ–Ї—Б–∞–Ј–Њ–ї—Г (23,4%), –љ–∞–ї–Є–і–Є–Ї—Б–Њ–≤–Њ–є –Ї–Є—Б–ї–Њ—В–µ (33,3%), —Ж–µ—Д–∞–Ј–Њ–ї–Є–љ—Г (34,6%), –∞–Љ–њ–Є—Ж–Є–ї–ї–Є–љ—Г (46,7%). –І—Г–≤—Б—В–≤–Є—В–µ–ї—М–љ–Њ—Б—В—М –і—А—Г–≥–Є—Е —Н–љ—В–µ—А–Њ–±–∞–Ї—В–µ—А–Є–є (Klebsiella spp., Proteus mirabilis) –Ї –∞–љ—В–Є–±–Є–Њ—В–Є–Ї–∞–Љ –±—Л–ї–∞ –Ј–∞–Ї–Њ–љ–Њ–Љ–µ—А–љ–Њ —Е—Г–ґ–µ, –≤ –Њ—В–љ–Њ—И–µ–љ–Є–Є —Н—В–Є—Е –±–∞–Ї—В–µ—А–Є–є –љ–∞–Є–Љ–µ–љ—М—И–µ–µ –Ї–Њ–ї–Є—З–µ—Б—В–≤–Њ —Г—Б—В–Њ–є—З–Є–≤—Л—Е —И—В–∞–Љ–Љ–Њ–≤ –љ–∞–±–ї—О–і–∞–ї–Њ—Б—М –Ї —Ж–µ—Д–Њ—В–∞–Ї—Б–Є–Љ—Г. S. saprophyticus –њ—А–Њ—П–≤–ї—П–ї —Е–Њ—А–Њ—И—Г—О —З—Г–≤—Б—В–≤–Є—В–µ–ї—М–љ–Њ—Б—В—М –Ї –љ–Є—В—А–Њ—Д—Г—А–∞–љ—В–Њ–Є–љ—Г, —Д—Г—А–∞–Ј–Є–і–Є–љ—Г –Ъ, –∞–Љ–Њ–Ї—Б–Є—Ж–Є–ї–ї–Є–љ/–Ї–ї–∞–≤—Г–ї–∞–љ–∞—В—Г, —Ж–Є–њ—А–Њ—Д–ї–Њ–Ї—Б–∞—Ж–Є–љ—Г; —Г—Б—В–Њ–є—З–Є–≤–Њ—Б—В—М –±—Л–ї–∞ –≤—Л—Б–Њ–Ї–Њ–є –Ї —Ж–µ—Д–Њ—В–∞–Ї—Б–Є–Љ—Г. –І—Г–≤—Б—В–≤–Є—В–µ–ї—М–љ–Њ—Б—В—М E. faecalis –±—Л–ї–∞ –≤—Л—Б–Њ–Ї–Њ–є –Ї –∞–Љ–њ–Є—Ж–Є–ї–ї–Є–љ—Г, –∞–Љ–Њ–Ї—Б–Є—Ж–Є–ї–ї–Є–љ/–Ї–ї–∞–≤—Г–ї–∞–љ–∞—В—Г, –љ–Є—В—А–Њ—Д—Г—А–∞–љ—В–Њ–Є–љ—Г, —Д—Г—А–∞–Ј–Є–і–Є–љ—Г –Ъ –Є –љ–Є–Ј–Ї–Њ–є –Ї —Ж–Є–њ—А–Њ—Д–ї–Њ–Ї—Б–∞—Ж–Є–љ—Г –Є –Ї–Њ–—В—А–Є–Љ–Њ–Ї—Б–∞–Ј–Њ–ї—Г.
–Ґ–∞–Ї–Є–Љ –Њ–±—А–∞–Ј–Њ–Љ, –љ–∞ –Њ—Б–љ–Њ–≤–∞–љ–Є–Є –Њ—В–µ—З–µ—Б—В–≤–µ–љ–љ—Л—Е –і–∞–љ–љ—Л—Е –њ–Њ –∞–љ—В–Є–±–Є–Њ—В–Є–Ї–Њ—А–µ–Ј–Є—Б—В–µ–љ—В–љ–Њ—Б—В–Є –≤–љ–µ–±–Њ–ї—М–љ–Є—З–љ—Л—Е —И—В–∞–Љ–Љ–Њ–≤ —Г—А–Њ–њ–∞—В–Њ–≥–µ–љ–Њ–≤ –і–ї—П –ї–µ—З–µ–љ–Є—П –Њ—Б—В—А—Л—Е –љ–µ–Њ—Б–ї–Њ–ґ–љ–µ–љ–љ—Л—Е –Є–љ—Д–µ–Ї—Ж–Є–є –Ь–Т–Я –Љ–Њ–≥—Г—В –±—Л—В—М —А–µ–Ї–Њ–Љ–µ–љ–і–Њ–≤–∞–љ—Л –љ–Є—В—А–Њ—Д—Г—А–∞–љ—Л, —Ж–µ—Д–∞–ї–Њ—Б–њ–Њ—А–Є–љ—Л III –њ–Њ–Ї–Њ–ї–µ–љ–Є—П, –≥–µ–љ—В–∞–Љ–Є—Ж–Є–љ, —Д—В–Њ—А—Е–Є–љ–Њ–ї–Њ–љ—Л, –њ–Њ—Б–ї–µ–і–љ–Є–µ – —Б –Њ–≥–Њ–≤–Њ—А–Ї–Њ–є –Њ –љ–µ–±–ї–∞–≥–Њ–њ—А–Є—П—В–љ—Л—Е —В–µ–љ–і–µ–љ—Ж–Є—П—Е –Ї —А–Њ—Б—В—Г —Г—Б—В–Њ–є—З–Є–≤–Њ—Б—В–Є. –°—А–µ–і–Є —Г–Ї–∞–Ј–∞–љ–љ—Л—Е –њ—А–µ–њ–∞—А–∞—В–Њ–≤ —Б–ї–µ–і—Г–µ—В –Њ—В–Љ–µ—В–Є—В—М, —З—В–Њ —Ж–µ—Д–∞–ї–Њ—Б–њ–Њ—А–Є–љ—Л –ї–Є—И–µ–љ—Л –∞–Ї—В–Є–≤–љ–Њ—Б—В–Є –њ—А–Њ—В–Є–≤ —Н–љ—В–µ—А–Њ–Ї–Њ–Ї–Ї–Њ–≤, –љ–∞ –і–Њ–ї—О –Ї–Њ—В–Њ—А—Л—Е –≤ –†–§ –њ—А–Є—Е–Њ–і–Є—В—Б—П –Њ–Ї–Њ–ї–Њ 15% –Њ—Б—В—А—Л—Е –Љ–Њ—З–µ–≤—Л—Е –Є–љ—Д–µ–Ї—Ж–Є–є, –∞ —А–∞–љ–љ–Є–µ —Д—В–Њ—А—Е–Є–љ–Њ–ї–Њ–љ—Л (–ї–Њ–Љ–µ—Д–ї–Њ–Ї—Б–∞—Ж–Є–љ, –љ–Њ—А—Д–ї–Њ–Ї—Б–∞—Ж–Є–љ, –Њ—Д–ї–Њ–Ї—Б–∞—Ж–Є–љ, –њ–µ—Д–ї–Њ–Ї—Б–∞—Ж–Є–љ, —Ж–Є–њ—А–Њ—Д–ї–Њ–Ї—Б–∞—Ж–Є–љ) –Њ–±–ї–∞–і–∞—О—В —Б–ї–∞–±–Њ–є –∞–Ї—В–Є–≤–љ–Њ—Б—В—М—О –њ—А–Њ—В–Є–≤ —Н—В–Њ–≥–Њ –≤–Њ–Ј–±—Г–і–Є—В–µ–ї—П. –Ф–ї—П –ї–µ—З–µ–љ–Є—П –Њ—Б—В—А—Л—Е –љ–µ–Њ—Б–ї–Њ–ґ–љ–µ–љ–љ—Л—Е –Љ–Њ—З–µ–≤—Л—Е –Є–љ—Д–µ–Ї—Ж–Є–є –≤ –†–§ –љ–µ —Б–ї–µ–і—Г–µ—В –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞—В—М –Ї–Њ–—В—А–Є–Љ–Њ–Ї—Б–∞–Ј–Њ–ї, –Є–љ–≥–Є–±–Є—В–Њ—А–Њ–Ј–∞—Й–Є—Й–µ–љ–љ—Л–µ –∞–Љ–Є–љ–Њ–њ–µ–љ–Є—Ж–Є–ї–ї–Є–љ—Л, –∞–Љ–њ–Є—Ж–Є–ї–ї–Є–љ –Є –∞–Љ–Њ–Ї—Б–Є—Ж–Є–ї–ї–Є–љ, –љ–µ—Д—В–Њ—А–Є—А–Њ–≤–∞–љ–љ—Л–µ —Е–Є–љ–Њ–ї–Њ–љ—Л (–љ–∞–ї–Є–і–Є–Ї—Б–Њ–≤–∞—П –Ї–Є—Б–ї–Њ—В–∞, –њ–Є–њ–µ–Љ–Є–і–Є–µ–≤–∞—П –Ї–Є—Б–ї–Њ—В–∞), –Ї –Ї–Њ—В–Њ—А—Л–Љ –Њ—В–Љ–µ—З–∞–µ—В—Б—П –≤—Л—Б–Њ–Ї–Є–є —Г—А–Њ–≤–µ–љ—М —А–µ–Ј–Є—Б—В–µ–љ—В–љ–Њ—Б—В–Є E. coli.
–†–µ–Ї–Њ–Љ–µ–љ–і–∞—Ж–Є–Є –њ–Њ –∞–љ—В–Є–±–∞–Ї—В–µ—А–Є–∞–ї—М–љ–Њ–є —В–µ—А–∞–њ–Є–Є –≤–љ–µ–±–Њ–ї—М–љ–Є—З–љ—Л—Е –Є–љ—Д–µ–Ї—Ж–Є–є –Љ–Њ—З–µ–≤—Л–≤–Њ–і—П—Й–Є—Е –њ—Г—В–µ–є
–Ю—Б—В—А—Л–є –љ–µ–Њ—Б–ї–Њ–ґ–љ–µ–љ–љ—Л–є —Ж–Є—Б—В–Є—В
—Г –љ–µ–±–µ—А–µ–Љ–µ–љ–љ—Л—Е –ґ–µ–љ—Й–Є–љ
–•–Њ—В—П –Њ—Б—В—А—Л–є —Ж–Є—Б—В–Є—В —Е–∞—А–∞–Ї—В–µ—А–Є–Ј—Г–µ—В—Б—П –±–ї–∞–≥–Њ–њ—А–Є—П—В–љ—Л–Љ –њ—А–Њ–≥–љ–Њ–Ј–Њ–Љ –Є –≤—Л—Б–Њ–Ї–Є–Љ —Г—А–Њ–≤–љ–µ–Љ —Б–њ–Њ–љ—В–∞–љ–љ–Њ–≥–Њ –≤—Л–Ј–і–Њ—А–Њ–≤–ї–µ–љ–Є—П, –≤ –Ї–Њ–љ—В—А–Њ–ї–Є—А—Г–µ–Љ—Л—Е –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П—Е –њ–Њ–Ї–∞–Ј–∞–љ–Њ –њ—А–µ–Є–Љ—Г—Й–µ—Б—В–≤–Њ –∞–љ—В–Є–±–Є–Њ—В–Є–Ї–Њ–≤ –њ–Њ —Б—А–∞–≤–љ–µ–љ–Є—О —Б –њ–ї–∞—Ж–µ–±–Њ, –Ї–∞–Ї –њ–Њ –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Њ–є, —В–∞–Ї –Є –±–∞–Ї—В–µ—А–Є–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Њ–є —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В–Є –Є –±—Л—Б—В—А–Њ—В–µ –њ—А–µ–Ї—А–∞—Й–µ–љ–Є—П —Б–Є–Љ–њ—В–Њ–Љ–Њ–≤ –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П [4].
–≠—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В—М –ї–µ—З–µ–љ–Є—П –Њ—Б—В—А–Њ–≥–Њ —Ж–Є—Б—В–Є—В–∞ –њ–Њ–Ї–∞–Ј–∞–љ–∞ –і–ї—П –Љ–љ–Њ–≥–Є—Е –∞–љ—В–Є–±–∞–Ї—В–µ—А–Є–∞–ї—М–љ—Л—Е —Б—А–µ–і—Б—В–≤ –≤ –Ї–Њ–љ—В—А–Њ–ї–Є—А—Г–µ–Љ—Л—Е –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є—Е –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П—Е: —В—А–Є–Љ–µ—В–Њ–њ—А–Є–Љ, –Ї–Њ–—В—А–Є–Љ–Њ–Ї—Б–∞–Ј–Њ–ї, —Д—В–Њ—А—Е–Є–љ–Њ–ї–Њ–љ—Л (–≥–∞—В–Є—Д–ї–Њ–Ї—Б–∞—Ж–Є–љ, –ї–µ–≤–Њ—Д–ї–Њ–Ї—Б–∞—Ж–Є–љ, –ї–Њ–Љ–µ—Д–ї–Њ–Ї—Б–∞—Ж–Є–љ, –Љ–Њ–Ї—Б–Є—Д–ї–Њ–Ї—Б–∞—Ж–Є–љ, –љ–Њ—А—Д–ї–Њ–Ї—Б–∞—Ж–Є–љ, –Њ—Д–ї–Њ–Ї—Б–∞—Ж–Є–љ, –њ–µ—Д–ї–Њ–Ї—Б–∞—Ж–Є–љ, —А—Г—Д–ї–Њ–Ї—Б–∞—Ж–Є–љ, —Д–ї–µ—А–Њ–Ї—Б–∞—Ж–Є–љ, —Ж–Є–њ—А–Њ—Д–ї–Њ–Ї—Б–∞—Ж–Є–љ, —Н–љ–Њ–Ї—Б–∞—Ж–Є–љ), b––ї–∞–Ї—В–∞–Љ—Л (–∞–Љ–Њ–Ї—Б–Є—Ж–Є–ї–ї–Є–љ, –∞–Љ–њ–Є—Ж–Є–ї–ї–Є–љ, –∞–Љ–Њ–Ї—Б–Є—Ж–Є–ї–ї–Є–љ/–Ї–ї–∞–≤—Г–ї–∞–љ–∞—В, —Ж–µ—Д–∞–і—А–Њ–Ї—Б–Є–ї, —Ж–µ—Д—Г—А–Њ–Ї—Б–Є–Љ –∞–Ї—Б–µ—В–Є–ї, —Ж–µ—Д–њ–Њ–і–Њ–Ї—Б–Є–Љ –њ—А–Њ–Ї—Б–µ—В–Є–ї, —Ж–µ—Д—В–Є–±—Г—В–µ–љ, –њ–Є–≤–Љ–µ—Ж–Є–ї–ї–Є–љ–∞–Љ, —А–Є—В–Є–њ–µ–љ–µ–Љ –∞–Ї—Б–µ—В–Є–ї, —Ж–µ—Д–Є–Ї—Б–Є–Љ), —Д–Њ—Б—Д–Њ–Љ–Є—Ж–Є–љ —В—А–Њ–Љ–µ—В–∞–Љ–Њ–ї, –љ–Є—В—А–Њ—Д—Г—А–∞–љ—Л (–љ–Є—В—А–Њ—Д—Г—А–∞–љ—В–Њ–Є–љ, —Д—Г—А–∞–Ј–Є–і–Є–љ). –Т –Ј–∞—А—Г–±–µ–ґ–љ—Л—Е –Я—А–∞–Ї—В–Є—З–µ—Б–Ї–Є—Е —А–µ–Ї–Њ–Љ–µ–љ–і–∞—Ж–Є—П—Е [2,4] –њ–Њ–і—З–µ—А–Ї–Є–≤–∞–µ—В—Б—П, —З—В–Њ —Б–ї–Њ–ґ–љ–Њ –њ—А–µ–і–Њ—Б—В–∞–≤–Є—В—М –µ–і–Є–љ—Л–µ —А–µ–Ї–Њ–Љ–µ–љ–і–∞—Ж–Є–Є –њ–Њ –≤—Л–±–Њ—А—Г —А–µ–ґ–Є–Љ–Њ–≤ –∞–љ—В–Є–±–∞–Ї—В–µ—А–Є–∞–ї—М–љ–Њ–є —В–µ—А–∞–њ–Є–Є –Њ—Б—В—А–Њ–≥–Њ —Ж–Є—Б—В–Є—В–∞ –і–ї—П –≤—Б–µ—Е —Б—В—А–∞–љ –Є–Ј––Ј–∞ —А–µ–≥–Є–Њ–љ–∞–ї—М–љ—Л—Е –Њ—Б–Њ–±–µ–љ–љ–Њ—Б—В–µ–є —А–∞—Б–њ—А–Њ—Б—В—А–∞–љ–µ–љ–Є—П –∞–љ—В–Є–±–Є–Њ—В–Є–Ї–Њ—А–µ–Ј–Є—Б—В–µ–љ—В–љ–Њ—Б—В–Є.
–Т –љ–∞—И–µ–є —Б—В—А–∞–љ–µ –љ–µ–≤—Л—Б–Њ–Ї–Є–є —Г—А–Њ–≤–µ–љ—М —Г—Б—В–Њ–є—З–Є–≤–Њ—Б—В–Є —Г—А–Њ–≥–µ–љ–Є—В–∞–ї—М–љ—Л—Е –≤–љ–µ–±–Њ–ї—М–љ–Є—З–љ—Л—Е —И—В–∞–Љ–Љ–Њ–≤ –Ї–Є—И–µ—З–љ–Њ–є –њ–∞–ї–Њ—З–Ї–Є –Њ—В–Љ–µ—З–µ–љ –Ї —Ж–µ—Д–∞–ї–Њ—Б–њ–Њ—А–Є–љ–∞–Љ III –њ–Њ–Ї–Њ–ї–µ–љ–Є—П, —Д–Њ—Б—Д–Њ–Љ–Є—Ж–Є–љ—Г –Є –љ–Є—В—А–Њ—Д—Г—А–∞–љ–∞–Љ. –£—Б—В–Њ–є—З–Є–≤–Њ—Б—В—М –Ї–Є—И–µ—З–љ–Њ–є –њ–∞–ї–Њ—З–Ї–Є –Ї —Д—В–Њ—А—Е–Є–љ–Њ–ї–Њ–љ–∞–Љ –≤ –љ–∞—Б—В–Њ—П—Й–µ–µ –≤—А–µ–Љ—П –њ—А–µ–≤—Л—И–∞–µ—В 10%, —З—В–Њ –Љ–Њ–ґ–µ—В –Њ–≥—А–∞–љ–Є—З–Є–≤–∞—В—М –Є—Е —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В—М –њ—А–Є —Б–Њ—Е—А–∞–љ–µ–љ–Є–Є —В–∞–Ї–Є—Е —В–µ–љ–і–µ–љ—Ж–Є–є. –Т—Л—Б–Њ–Ї–Є–є —Г—А–Њ–≤–µ–љ—М —Г—Б—В–Њ–є—З–Є–≤–Њ—Б—В–Є –љ–∞–±–ї—О–і–∞–µ—В—Б—П –Ї –љ–µ—Д—В–Њ—А–Є—А–Њ–≤–∞–љ–љ—Л–Љ —Е–Є–љ–Њ–ї–Њ–љ–∞–Љ, –∞–Љ–Є–љ–Њ–њ–µ–љ–Є—Ж–Є–ї–ї–Є–љ–∞–Љ –Є –Ј–∞—Й–Є—Й–µ–љ–љ—Л–Љ –њ–µ–љ–Є—Ж–Є–ї–ї–Є–љ–∞–Љ, –Ї–Њ–—В—А–Є–Љ–Њ–Ї—Б–∞–Ј–Њ–ї—Г.
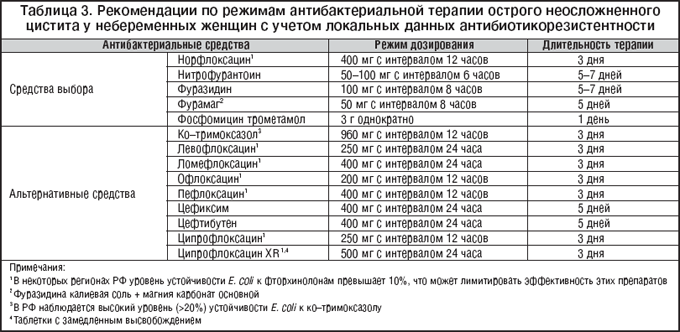
–†–µ–Ї–Њ–Љ–µ–љ–і–∞—Ж–Є–Є –њ–Њ —А–µ–ґ–Є–Љ–∞–Љ –∞–љ—В–Є–±–∞–Ї—В–µ—А–Є–∞–ї—М–љ–Њ–є —В–µ—А–∞–њ–Є–Є –Њ—Б—В—А–Њ–≥–Њ –љ–µ–Њ—Б–ї–Њ–ґ–љ–µ–љ–љ–Њ–≥–Њ —Ж–Є—Б—В–Є—В–∞ —Б —Г—З–µ—В–Њ–Љ –ї–Њ–Ї–∞–ї—М–љ—Л—Е –і–∞–љ–љ—Л—Е –њ–Њ –∞–љ—В–Є–±–Є–Њ—В–Є–Ї–Њ—А–µ–Ј–Є—Б—В–µ–љ—В–љ–Њ—Б—В–Є —Г—А–Њ–њ–∞—В–Њ–≥–µ–љ–Њ–≤ –њ—А–µ–і—Б—В–∞–≤–ї–µ–љ—Л –≤ —В–∞–±–ї–Є—Ж–µ 3. –Т –љ–∞—Б—В–Њ—П—Й–µ–µ –≤—А–µ–Љ—П –≤ –Ї–∞—З–µ—Б—В–≤–µ —Б—А–µ–і—Б—В–≤ –≤—Л–±–Њ—А–∞ –і–ї—П –ї–µ—З–µ–љ–Є—П –Њ—Б—В—А–Њ–≥–Њ –љ–µ–Њ—Б–ї–Њ–ґ–љ–µ–љ–љ–Њ–≥–Њ —Ж–Є—Б—В–Є—В–∞ —Г –љ–µ–±–µ—А–µ–Љ–µ–љ–љ—Л—Е –ґ–µ–љ—Й–Є–љ –Љ–Њ–≥—Г—В –±—Л—В—М —А–µ–Ї–Њ–Љ–µ–љ–і–Њ–≤–∞–љ—Л –љ–Є—В—А–Њ—Д—Г—А–∞–љ—Л, —Д–Њ—Б—Д–Њ–Љ–Є—Ж–Є–љ —В—А–Њ–Љ–µ—В–∞–Љ–Њ–ї –Є —Д—В–Њ—А—Е–Є–љ–Њ–ї–Њ–љ—Л. –°—А–µ–і–Є –љ–Є—В—А–Њ—Д—Г—А–∞–љ–Њ–≤ –Њ–њ—В–Є–Љ–∞–ї—М–љ–Њ –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞—В—М –њ—А–µ–њ–∞—А–∞—В—Л –Ї–∞–ї–Є–µ–≤–Њ–є —Б–Њ–ї–Є —Д—Г—А–∞–Ј–Є–і–Є–љ–∞ (—Д—Г—А–∞–Ј–Є–і–Є–љ –Ъ), –Њ–±–ї–∞–і–∞—О—Й–Є–µ –±–Њ–ї–µ–µ –≤—Л—Б–Њ–Ї–Њ–є –±–Є–Њ–і–Њ—Б—В—Г–њ–љ–Њ—Б—В—М—О –њ–Њ —Б—А–∞–≤–љ–µ–љ–Є—О —Б –Њ–±—Л—З–љ—Л–Љ —Д—Г—А–∞–Ј–Є–і–Є–љ–Њ–Љ (—Д—Г—А–∞–≥–Є–љ–Њ–Љ) –Є –ї—Г—З—И–µ–є –њ–µ—А–µ–љ–Њ—Б–Є–Љ–Њ—Б—В—М—О, –∞ –њ–Њ —Б—А–∞–≤–љ–µ–љ–Є—О —Б –љ–Є—В—А–Њ—Д—Г—А–∞–љ—В–Њ–Є–љ–Њ–Љ –Њ–љ–Є —Е–∞—А–∞–Ї—В–µ—А–Є–Ј—Г—О—В—Б—П –±–Њ–ї–µ–µ —Г–і–Њ–±–љ—Л–Љ –њ—А–Є–µ–Љ–Њ–Љ (3 —А–∞–Ј–∞ –≤ —Б—Г—В–Ї–Є) –Є –Љ–µ–љ—М—И–Є–Љ —Г—А–Њ–≤–љ–µ–Љ —Г—Б—В–Њ–є—З–Є–≤–Њ—Б—В–Є Enterobacteriaceae. –°—А–µ–і–Є —Д—В–Њ—А—Е–Є–љ–Њ–ї–Њ–љ–Њ–≤ –і–ї—П –ї–µ—З–µ–љ–Є—П –Њ—Б—В—А–Њ–≥–Њ —Ж–Є—Б—В–Є—В–∞ —Ж–µ–ї–µ—Б–Њ–Њ–±—А–∞–Ј–љ–µ–µ –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞—В—М –љ–Њ—А—Д–ї–Њ–Ї—Б–∞—Ж–Є–љ, —В–∞–Ї –Ї–∞–Ї –њ–Њ –∞–љ—В–Є–Љ–Є–Ї—А–Њ–±–љ–Њ–є –∞–Ї—В–Є–≤–љ–Њ—Б—В–Є –њ—А–Њ—В–Є–≤ –љ–∞–Є–±–Њ–ї–µ–µ –Ј–љ–∞—З–Є–Љ—Л—Е —Г—А–Њ–њ–∞—В–Њ–≥–µ–љ–Њ–≤ –Њ–љ –љ–µ —Г—Б—В—Г–њ–∞–µ—В —Ж–Є–њ—А–Њ—Д–ї–Њ–Ї—Б–∞—Ж–Є–љ—Г, –љ–Њ, –≤ –Њ—В–ї–Є—З–Є–µ –Њ—В –і—А—Г–≥–Є—Е —Д—В–Њ—А—Е–Є–љ–Њ–ї–Њ–љ–Њ–≤, –Є–Ј––Ј–∞ –Њ—Б–Њ–±–µ–љ–љ–Њ—Б—В–µ–є —Д–∞—А–Љ–∞–Ї–Њ–Ї–Є–љ–µ—В–Є–Ї–Є –Њ–±–ї–∞–і–∞–µ—В –Љ–µ–љ—М—И–Є–Љ —Б–Є—Б—В–µ–Љ–љ—Л–Љ –і–µ–є—Б—В–≤–Є–µ–Љ –Є —Б–Њ–Њ—В–≤–µ—В—Б—В–≤–µ–љ–љ–Њ –≤ –Љ–µ–љ—М—И–µ–є —Б—В–µ–њ–µ–љ–Є –±—Г–і–µ—В —Б–њ–Њ—Б–Њ–±—Б—В–≤–Њ–≤–∞—В—М —Б–µ–ї–µ–Ї—Ж–Є–Є —Г—Б—В–Њ–є—З–Є–≤—Л—Е —И—В–∞–Љ–Љ–Њ–≤ –Љ–Є–Ї—А–Њ–Њ—А–≥–∞–љ–Є–Ј–Љ–Њ–≤. –Я—А–Є–Љ–µ–љ–µ–љ–Є–µ –і—А—Г–≥–Є—Е —Д—В–Њ—А—Е–Є–љ–Њ–ї–Њ–љ–Њ–≤ –і–ї—П –ї–µ—З–µ–љ–Є—П –Њ—Б—В—А–Њ–≥–Њ –љ–µ–Њ—Б–ї–Њ–ґ–љ–µ–љ–љ–Њ–≥–Њ —Ж–Є—Б—В–Є—В–∞ –≤—А—П–і –ї–Є –Љ–Њ–ґ–µ—В –±—Л—В—М –њ—А–Є–Ј–љ–∞–љ–Њ —Ж–µ–ї–µ—Б–Њ–Њ–±—А–∞–Ј–љ—Л–Љ.
–Ъ–Њ—А–Њ—В–Ї–Є–µ –Ї—Г—А—Б—Л —В–µ—А–∞–њ–Є–Є –Є–Љ–µ—О—В –њ—А–µ–Є–Љ—Г—Й–µ—Б—В–≤–∞ –≤ –њ–ї–∞–љ–µ –ї—Г—З—И–µ–є –њ–µ—А–µ–љ–Њ—Б–Є–Љ–Њ—Б—В–Є –Є —Б–љ–Є–ґ–µ–љ–Є—П —Б—В–Њ–Є–Љ–Њ—Б—В–Є –ї–µ—З–µ–љ–Є—П –Є –Љ–Њ–≥—Г—В –±—Л—В—М –њ—А–Є–Љ–µ–љ–µ–љ—Л —Г –љ–µ–±–µ—А–µ–Љ–µ–љ–љ—Л—Е –ґ–µ–љ—Й–Є–љ –і–Њ –Љ–µ–љ–Њ–њ–∞—Г–Ј—Л –њ—А–Є –љ–∞–Ј–љ–∞—З–µ–љ–Є–Є –љ–Њ—А—Д–ї–Њ–Ї—Б–∞—Ж–Є–љ–∞ –Є –Ї–Њ–—В—А–Є–Љ–Њ–Ї—Б–∞–Ј–Њ–ї–∞ (3 –і–љ—П), —Д–Њ—Б—Д–Њ–Љ–Є—Ж–Є–љ–∞ (1 –і–µ–љ—М). b––ї–∞–Ї—В–∞–Љ—Л –Є –љ–Є—В—А–Њ—Д—Г—А–∞–љ—Л —Ж–µ–ї–µ—Б–Њ–Њ–±—А–∞–Ј–љ–Њ –њ—А–Є–Љ–µ–љ—П—В—М –≤ —В–µ—З–µ–љ–Є–µ 5–7 –і–љ–µ–є.
–Я—А–Є –љ–∞–Ј–љ–∞—З–µ–љ–Є–Є –∞–љ—В–Є–±–Є–Њ—В–Є–Ї–Њ–≤ –њ–∞—Ж–Є–µ–љ—В–∞–Љ —Б–ї–µ–і—Г–µ—В –Њ–±—К—П—Б–љ–Є—В—М, —З—В–Њ –і–∞–ґ–µ –њ—А–Є —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ–Љ –ї–µ—З–µ–љ–Є–Є —Б–Є–Љ–њ—В–Њ–Љ—Л –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П –Љ–Њ–≥—Г—В —Б–Њ—Е—А–∞–љ—П—В—М—Б—П –≤ —В–µ—З–µ–љ–Є–µ 2–3 –і–љ–µ–є. –Я—А–Є –≤—Л—А–∞–ґ–µ–љ–љ—Л—Е —Б–Є–Љ–њ—В–Њ–Љ–∞—Е –≤–Њ–Ј–Љ–Њ–ґ–љ–Њ –љ–∞–Ј–љ–∞—З–µ–љ–Є–µ –∞–љ–∞–ї—М–≥–µ—В–Є–Ї–Њ–≤, —В–∞–Ї–Є—Е –Ї–∞–Ї —Д–µ–љ–∞–Ј–Њ–њ–Є—А–Є–і–Є–љ –≤ –і–Њ–Ј–µ 200 –Љ–≥ —Б –Є–љ—В–µ—А–≤–∞–ї–Њ–Љ 8 —З–∞—Б–Њ–≤. –¶–µ–ї–µ—Б–Њ–Њ–±—А–∞–Ј–љ—Л —В–∞–Ї–ґ–µ —А–µ–Ї–Њ–Љ–µ–љ–і–∞—Ж–Є–Є –њ–Њ —Г–≤–µ–ї–Є—З–µ–љ–Є—О –Ї–Њ–ї–Є—З–µ—Б—В–≤–∞ –њ—А–Є–љ–Є–Љ–∞–µ–Љ–Њ–є –ґ–Є–і–Ї–Њ—Б—В–Є, –Њ–і–љ–∞–Ї–Њ —Г–±–µ–і–Є—В–µ–ї—М–љ—Л—Е –і–Њ–Ї–∞–Ј–∞—В–µ–ї—М—Б—В–≤ –≤ –њ–Њ–ї—М–Ј—Г —Н—В–Њ–≥–Њ —Г—В–≤–µ—А–ґ–і–µ–љ–Є—П –љ–µ—В.
–Ю—Б—В—А—Л–є –љ–µ–Њ—Б–ї–Њ–ґ–љ–µ–љ–љ—Л–є –њ–Є–µ–ї–Њ–љ–µ—Д—А–Є—В
—Г –љ–µ–±–µ—А–µ–Љ–µ–љ–љ—Л—Е –ґ–µ–љ—Й–Є–љ
–Э–µ—Б–Љ–Њ—В—А—П –љ–∞ –љ–µ—Б–Ї–Њ–ї—М–Ї–Њ —Б–Њ—В–µ–љ –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є—Е –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–є –∞–љ—В–Є–±–Є–Њ—В–Є–Ї–Њ–≤ –њ—А–Є –њ–Є–µ–ї–Њ–љ–µ—Д—А–Є—В–µ, —В–Њ–ї—М–Ї–Њ 5 –Є–Ј –љ–Є—Е –Љ–Њ–≥—Г—В –±—Л—В—М –Њ—В–љ–µ—Б–µ–љ—Л –Ї –њ—А–Њ—Б–њ–µ–Ї—В–Є–≤–љ—Л–Љ, —А–∞–љ–і–Њ–Љ–Є–Ј–Є—А–Њ–≤–∞–љ–љ—Л–Љ, –Ї–Њ–љ—В—А–Њ–ї–Є—А—Г–µ–Љ—Л–Љ. –†–µ–Ј—О–Љ–µ –њ–Њ —Н—В–Є–Љ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П–Љ –Є –µ—Й–µ 4 —Е–Њ—А–Њ—И–Њ —Б–њ–ї–∞–љ–Є—А–Њ–≤–∞–љ–љ—Л–Љ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П–Љ –њ—А–µ–і—Б—В–∞–≤–ї–µ–љ–Њ –љ–Є–ґ–µ [2].
1. –Ъ–Њ–—В—А–Є–Љ–Њ–Ї—Б–∞–Ј–Њ–ї –њ—А–µ–≤–Њ—Б—Е–Њ–і–Є—В –∞–Љ–њ–Є—Ж–Є–ї–ї–Є–љ –њ—А–Є –Њ—Б—В—А–Њ–Љ –њ–Є–µ–ї–Њ–љ–µ—Д—А–Є—В–µ.
2. 2––љ–µ–і–µ–ї—М–љ—Л–є –Ї—Г—А—Б –ї–µ—З–µ–љ–Є—П –Ї–Њ–—В—А–Є–Љ–Њ–Ї—Б–∞–Ј–Њ–ї–Њ–Љ –Њ—Б—В—А–Њ–≥–Њ –љ–µ–Њ—Б–ї–Њ–ґ–љ–µ–љ–љ–Њ–≥–Њ –њ–Є–µ–ї–Њ–љ–µ—Д—А–Є—В–∞ —П–≤–ї—П–µ—В—Б—П –∞–і–µ–Ї–≤–∞—В–љ—Л–Љ –Є –і–Њ—Б—В–∞—В–Њ—З–љ—Л–Љ —Г –±–Њ–ї—М—И–Є–љ—Б—В–≤–∞ –ґ–µ–љ—Й–Є–љ. –Т –љ–µ–Ї–Њ—В–Њ—А—Л—Е –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П—Е –њ–Њ–Ї–∞–Ј–∞–љ–∞ —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В—М –і—А—Г–≥–Є—Е –∞–љ—В–Є–±–Є–Њ—В–Є–Ї–Њ–≤ –≤ –±–Њ–ї–µ–µ –Ї–Њ—А–Њ—В–Ї–Є—Е –Ї—Г—А—Б–∞—Е (7–10 –і–љ–µ–є), –∞ –∞–Љ–Є–љ–Њ–≥–ї–Є–Ї–Њ–Ј–Є–і–Њ–≤ – –і–∞–ґ–µ –њ—А–Є 5–7––і–љ–µ–≤–љ–Њ–є —В–µ—А–∞–њ–Є–Є, –Њ–і–љ–∞–Ї–Њ –і–Њ–Ї–∞–Ј–∞—В–µ–ї—М–љ–∞—П —Б–Є–ї–∞ —Н—В–Є—Е –і–∞–љ–љ—Л—Е –љ–µ –Њ—З–µ–љ—М –≤—Л—Б–Њ–Ї–∞—П.
3. –Т —А–µ–≥–Є–Њ–љ–∞—Е, –≥–і–µ —Г—А–Њ–≤–µ–љ—М —Г—Б—В–Њ–є—З–Є–≤–Њ—Б—В–Є E. coli –Ї –Ї–Њ–—В—А–Є–Љ–Њ–Ї—Б–∞–Ј–Њ–ї—Г –њ—А–µ–≤—Л—И–∞–µ—В 10% (–≤ –†–Њ—Б—Б–Є–Є >20%, –њ—А–Є–Љ. –∞–≤—В.), —Д—В–Њ—А—Е–Є–љ–Њ–ї–Њ–љ—Л –і–Њ–ї–ґ–љ—Л —А–∞—Б—Ж–µ–љ–Є–≤–∞—В—М—Б—П –Ї–∞–Ї —Б—А–µ–і—Б—В–≤–∞ –≤—Л–±–Њ—А–∞. –Я–Њ–Ї–∞–Ј–∞–љ–Њ –њ—А–µ–Є–Љ—Г—Й–µ—Б—В–≤–Њ 7––і–љ–µ–≤–љ–Њ–≥–Њ –Ї—Г—А—Б–∞ —Ж–Є–њ—А–Њ—Д–ї–Њ–Ї—Б–∞—Ж–Є–љ–Њ–Љ –њ–Њ —Б—А–∞–≤–љ–µ–љ–Є—О —Б 14––і–љ–µ–≤–љ—Л–Љ –Ї—Г—А—Б–Њ–Љ –Ї–Њ–—В—А–Є–Љ–Њ–Ї—Б–∞–Ј–Њ–ї–Њ–Љ –њ–Њ —Г—А–Њ–≤–љ—О —Н—А–∞–і–Є–Ї–∞—Ж–Є–Є –≤–Њ–Ј–±—Г–і–Є—В–µ–ї–µ–є. –Ю–і–Є–љ–∞–Ї–Њ–≤–∞—П —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В—М —Б —Ж–Є–њ—А–Њ—Д–ї–Њ–Ї—Б–∞—Ж–Є–љ–Њ–Љ –≤ –і–Њ–Ј–µ 500 –Љ–≥ —Б –Є–љ—В–µ—А–≤–∞–ї–Њ–Љ 12 —З–∞—Б–Њ–≤ –њ–Њ–Ї–∞–Ј–∞–љ–∞ –і–ї—П –і—А—Г–≥–Є—Е —Д—В–Њ—А—Е–Є–љ–Њ–ї–Њ–љ–Њ–≤: —Ж–Є–њ—А–Њ—Д–ї–Њ–Ї—Б–∞—Ж–Є–љ —Б –Ј–∞–Љ–µ–і–ї–µ–љ–љ—Л–Љ –≤—Л—Б–≤–Њ–±–Њ–ґ–і–µ–љ–Є–µ–Љ (1 –≥ —Б –Є–љ—В–µ—А–≤–∞–ї–Њ–Љ 24 —З–∞—Б–∞), –≥–∞—В–Є—Д–ї–Њ–Ї—Б–∞—Ж–Є–љ (400 –Љ–≥ —Б –Є–љ—В–µ—А–≤–∞–ї–Њ–Љ 24 —З–∞—Б–∞), –ї–µ–≤–Њ—Д–ї–Њ–Ї—Б–∞—Ж–Є–љ (250 –Љ–≥ —Б –Є–љ—В–µ—А–≤–∞–ї–Њ–Љ 12 —З–∞—Б–Њ–≤), –ї–Њ–Љ–µ—Д–ї–Њ–Ї—Б–∞—Ж–Є–љ (400 –Љ–≥ —Б –Є–љ—В–µ—А–≤–∞–ї–Њ–Љ 24 —З–∞—Б–∞).
4. –Т–Њ–Ј–Љ–Њ–ґ–љ–Њ—Б—В—М –њ—А–Є–Љ–µ–љ–µ–љ–Є—П –Є–љ–≥–Є–±–Є—В–Њ—А–Њ–Ј–∞—Й–Є—Й–µ–љ–љ—Л—Е –њ–µ–љ–Є—Ж–Є–ї–ї–Є–љ–Њ–≤ (–∞–Љ–Њ–Ї—Б–Є—Ж–Є–ї–ї–Є–љ/–Ї–ї–∞–≤—Г–ї–∞–љ–∞—В) –Є –њ–µ—А–Њ—А–∞–ї—М–љ—Л—Е —Ж–µ—Д–∞–ї–Њ—Б–њ–Њ—А–Є–љ–Њ–≤ II–III –њ–Њ–Ї–Њ–ї–µ–љ–Є—П –њ—А–Є –Њ—Б—В—А–Њ–Љ –њ–Є–µ–ї–Њ–љ–µ—Д—А–Є—В–µ –љ–µ –њ–Њ–і—В–≤–µ—А–ґ–і–µ–љ–∞ –≤ —А–∞–љ–і–Њ–Љ–Є–Ј–Є—А–Њ–≤–∞–љ–љ—Л—Е —Б—А–∞–≤–љ–Є—В–µ–ї—М–љ—Л—Е –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П—Е —Б —Д—В–Њ—А—Е–Є–љ–Њ–ї–Њ–љ–∞–Љ–Є –Є–ї–Є –Ї–Њ–—В—А–Є–Љ–Њ–Ї—Б–∞–Ј–Њ–ї–Њ–Љ. –Т –µ–і–Є–љ—Б—В–≤–µ–љ–љ–Њ–Љ –Ї–Њ–љ—В—А–Њ–ї–Є—А—Г–µ–Љ–Њ–Љ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є b––ї–∞–Ї—В–∞–Љ–Њ–≤ –њ–Њ–Ї–∞–Ј–∞–љ–∞ –Њ–і–Є–љ–∞–Ї–Њ–≤–∞—П —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В—М 10––і–љ–µ–≤–љ–Њ–є —В–µ—А–∞–њ–Є–Є —Ж–µ—Д–њ–Њ–і–Њ–Ї—Б–Є–Љ –њ—А–Њ–Ї—Б–µ—В–Є–ї–Њ–Љ (200 –Љ–≥ —Б –Є–љ—В–µ—А–≤–∞–ї–Њ–Љ 12 —З–∞—Б–Њ–≤) –Є —Ж–Є–њ—А–Њ—Д–ї–Њ–Ї—Б–∞—Ж–Є–љ–∞ –≤ –і–Њ–Ј–µ 500 –Љ–≥ —Б –Є–љ—В–µ—А–≤–∞–ї–Њ–Љ 12 —З–∞—Б–Њ–≤.
5. –Т —А–µ–≥–Є–Њ–љ–∞—Е —Б —Г—А–Њ–≤–љ–µ–Љ —Г—Б—В–Њ–є—З–Є–≤–Њ—Б—В–Є E. coli –Ї —Д—В–Њ—А—Е–Є–љ–Њ–ї–Њ–љ–∞–Љ >10% (–≤ –†–Њ—Б—Б–Є–Є, –њ–Њ –і–∞–љ–љ—Л–Љ —В—А–µ—Е –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–є, —Г—Б—В–Њ–є—З–Є–≤–Њ—Б—В—М —Б–Њ—Б—В–∞–≤–ї—П–ї–∞ 15,4 –Є 15% – –њ—А–Є–Љ. –∞–≤—В.) –Є–ї–Є –≤ —В–µ—Е —Б–Є—В—Г–∞—Ж–Є—П—Е, –Ї–Њ–≥–і–∞ —Д—В–Њ—А—Е–Є–љ–Њ–ї–Њ–љ—Л –њ—А–Њ—В–Є–≤–Њ–њ–Њ–Ї–∞–Ј–∞–љ—Л (–±–µ—А–µ–Љ–µ–љ–љ—Л–µ, –њ–µ—А–Є–Њ–і –ї–∞–Ї—В–∞—Ж–Є–Є, –і–µ—В–Є –Є –њ–Њ–і—А–Њ—Б—В–Ї–Є), –њ—А–µ–њ–∞—А–∞—В–∞–Љ–Є –≤—Л–±–Њ—А–∞ –Љ–Њ–≥—Г—В —Б—З–Є—В–∞—В—М—Б—П –Є–љ–≥–Є–±–Є—В–Њ—А–Њ–Ј–∞—Й–Є—Й–µ–љ–љ—Л–µ –∞–Љ–Є–љ–Њ–њ–µ–љ–Є—Ж–Є–ї–ї–Є–љ—Л –Є–ї–Є —Ж–µ—Д–∞–ї–Њ—Б–њ–Њ—А–Є–љ—Л III –њ–Њ–Ї–Њ–ї–µ–љ–Є—П. –Т –љ–∞—И–µ–є —Б—В—А–∞–љ–µ –њ—А–µ–і–њ–Њ—З—В–Є—В–µ–ї—М–љ–µ–µ –њ–µ—А–Њ—А–∞–ї—М–љ—Л–µ (—Ж–µ—Д–Є–Ї—Б–Є–Љ, —Ж–µ—Д—В–Є–±—Г—В–µ–љ) –Є–ї–Є –њ–∞—А–µ–љ—В–µ—А–∞–ї—М–љ—Л–µ (—Ж–µ—Д—В—А–Є–∞–Ї—Б–Њ–љ, —Ж–µ—Д–Њ—В–∞–Ї—Б–Є–Љ) —Ж–µ—Д–∞–ї–Њ—Б–њ–Њ—А–Є–љ—Л III –њ–Њ–Ї–Њ–ї–µ–љ–Є—П, —Г—З–Є—В—Л–≤–∞—П –±–Њ–ї–µ–µ –≤—Л—Б–Њ–Ї–Є–є —Г—А–Њ–≤–µ–љ—М —Г—Б—В–Њ–є—З–Є–≤–Њ—Б—В–Є —Г—А–Њ–њ–∞—В–Њ–≥–µ–љ–љ—Л—Е —И—В–∞–Љ–Љ–Њ–≤ E. coli –Ї –∞–Љ–Њ–Ї—Б–Є—Ж–Є–ї–ї–Є–љ/–Ї–ї–∞–≤—Г–ї–∞–љ–∞—В—Г –Є –∞–Љ–њ–Є—Ж–Є–ї–ї–Є–љ/—Б—Г–ї—М–±–∞–Ї—В–∞–Љ—Г (–њ—А–Є–Љ. –∞–≤—В.).
–Ґ–∞–Ї–Є–Љ –Њ–±—А–∞–Ј–Њ–Љ, –≤ —Б–ї—Г—З–∞—П—Е –љ–µ—В—П–ґ–µ–ї–Њ–≥–Њ —В–µ—З–µ–љ–Є—П –њ–Є–µ–ї–Њ–љ–µ—Д—А–Є—В–∞ —Ж–µ–ї–µ—Б–Њ–Њ–±—А–∞–Ј–µ–љ 7––і–љ–µ–≤–љ—Л–є –Ї—Г—А—Б –ї–µ—З–µ–љ–Є—П –ї—О–±—Л–Љ –њ–µ—А–Њ—А–∞–ї—М–љ—Л–Љ —Д—В–Њ—А—Е–Є–љ–Њ–ї–Њ–љ–Њ–Љ, –Ї—А–Њ–Љ–µ –љ–Њ—А—Д–ї–Њ–Ї—Б–∞—Ж–Є–љ–∞, –Ї–Њ–љ—Ж–µ–љ—В—А–∞—Ж–Є–Є –Ї–Њ—В–Њ—А–Њ–≥–Њ –≤ –њ–Њ—З–µ—З–љ–Њ–є —В–Ї–∞–љ–Є –љ–µ –і–Њ—Б—В–Є–≥–∞—О—В —В–µ—А–∞–њ–µ–≤—В–Є—З–µ—Б–Ї–Њ–≥–Њ —Г—А–Њ–≤–љ—П. –Т —Б–ї—Г—З–∞—П—Е –љ–µ–≤–Њ–Ј–Љ–Њ–ґ–љ–Њ—Б—В–Є –њ—А–Є–Љ–µ–љ–µ–љ–Є—П —Д—В–Њ—А—Е–Є–љ–Њ–ї–Њ–љ–Њ–≤ –Њ–њ—А–∞–≤–і–∞–љ–Њ –љ–∞–Ј–љ–∞—З–µ–љ–Є–µ –њ–µ—А–Њ—А–∞–ї—М–љ–Њ–≥–Њ —Ж–µ—Д–∞–ї–Њ—Б–њ–Њ—А–Є–љ–∞ III –њ–Њ–Ї–Њ–ї–µ–љ–Є—П – —Ж–µ—Д–Є–Ї—Б–Є–Љ–∞ –Є–ї–Є —Ж–µ—Д—В–Є–±—Г—В–µ–љ–∞. –Э–∞–Ј–љ–∞—З–µ–љ–Є–µ –∞–Љ–Њ–Ї—Б–Є—Ж–Є–ї–ї–Є–љ/–Ї–ї–∞–≤—Г–ї–∞–љ–∞—В–∞ —Ж–µ–ї–µ—Б–Њ–Њ–±—А–∞–Ј–љ–Њ –њ—А–Є –≤—Л—П–≤–ї–µ–љ–Є–Є –њ—А–Є –Њ–Ї—А–∞—Б–Ї–Є –њ–Њ –У—А–∞–Љ—Г –≥—А–∞–Љ–њ–Њ–ї–Њ–ґ–Є—В–µ–ї—М–љ—Л—Е –±–∞–Ї—В–µ—А–Є–є [2]. –Я–Њ —Г—Б–Љ–Њ—В—А–µ–љ–Є—О –≤—А–∞—З–∞ –њ–∞—Ж–Є–µ–љ—В—Л –Љ–Њ–≥—Г—В –њ–Њ–ї—Г—З–∞—В—М —В–∞–Ї–ґ–µ –њ–∞—А–µ–љ—В–µ—А–∞–ї—М–љ—Г—О –∞–љ—В–Є–±–Є–Њ—В–Є–Ї–Њ—В–µ—А–∞–њ–Є—О –љ–∞ –і–Њ–Љ—Г, –≤ —Н—В–Њ–Љ —Б–ї—Г—З–∞–µ –њ—А–µ–і–њ–Њ—З—В–Є—В–µ–ї—М–љ–µ–µ –љ–∞–Ј–љ–∞—З–µ–љ–Є–µ —Ж–µ—Д—В—А–Є–∞–Ї—Б–Њ–љ–∞ (1–2 –≥ —Б –Є–љ—В–µ—А–≤–∞–ї–Њ–Љ 24 —З–∞—Б–∞).
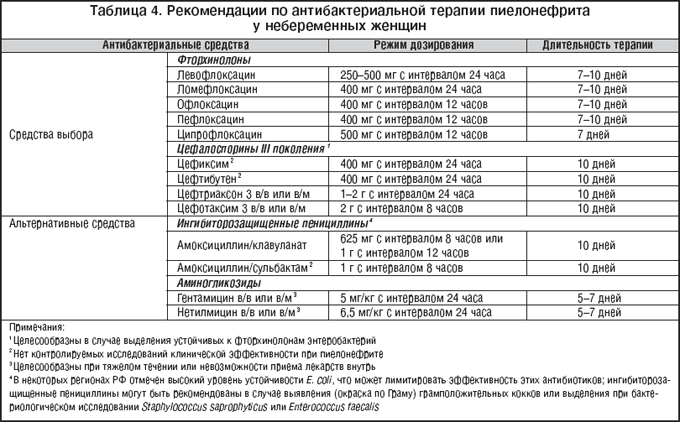
–†–µ–Ї–Њ–Љ–µ–љ–і–Њ–≤–∞–љ–љ—Л–µ —А–µ–ґ–Є–Љ—Л –∞–љ—В–Є–±–∞–Ї—В–µ—А–Є–∞–ї—М–љ–Њ–є —В–µ—А–∞–њ–Є–Є –Њ—Б—В—А–Њ–≥–Њ –љ–µ–Њ—Б–ї–Њ–ґ–љ–µ–љ–љ–Њ–≥–Њ –њ–Є–µ–ї–Њ–љ–µ—Д—А–Є—В–∞ —Б —Г—З–µ—В–Њ–Љ –ї–Њ–Ї–∞–ї—М–љ—Л—Е –і–∞–љ–љ—Л—Е –њ–Њ –∞–љ—В–Є–±–Є–Њ—В–Є–Ї–Њ—А–µ–Ј–Є—Б—В–µ–љ—В–љ–Њ—Б—В–Є –њ—А–µ–і—Б—В–∞–≤–ї–µ–љ—Л –≤ —В–∞–±–ї–Є—Ж–µ 4.
–Я—А–Є —В—П–ґ–µ–ї–Њ–Љ —В–µ—З–µ–љ–Є–Є –њ–Є–µ–ї–Њ–љ–µ—Д—А–Є—В–∞ –њ–∞—Ж–Є–µ–љ—В–∞ —Б–ї–µ–і—Г–µ—В –≥–Њ—Б–њ–Є—В–∞–ї–Є–Ј–Є—А–Њ–≤–∞—В—М –Є –ї–µ—З–µ–љ–Є–µ –њ—А–Њ–≤–Њ–і–Є—В—М –њ–∞—А–µ–љ—В–µ—А–∞–ї—М–љ—Л–Љ –∞–љ—В–Є–±–Є–Њ—В–Є–Ї–Њ–Љ – —Д—В–Њ—А—Е–Є–љ–Њ–ї–Њ–љ–Њ–Љ –Є–ї–Є —Ж–µ—Д–∞–ї–Њ—Б–њ–Њ—А–Є–љ–Њ–Љ III –њ–Њ–Ї–Њ–ї–µ–љ–Є—П –Є–ї–Є –∞–Љ–Є–љ–Њ–≥–ї–Є–Ї–Њ–Ј–Є–і–Њ–Љ. –Я—А–Є —Г–ї—Г—З—И–µ–љ–Є–Є —Б–Њ—Б—В–Њ—П–љ–Є—П –і–Њ–ї–µ—З–Є–≤–∞–љ–Є–µ –њ–∞—Ж–Є–µ–љ—В–∞ (–і–Њ –њ–Њ–ї–љ–Њ–≥–Њ –Ї—Г—А—Б–∞ 1–2 –љ–µ–і–µ–ї–Є) –Љ–Њ–ґ–µ—В –Њ—Б—Г—Й–µ—Б—В–≤–ї—П—В—М—Б—П –њ–µ—А–Њ—А–∞–ї—М–љ—Л–Љ –∞–љ—В–Є–±–Є–Њ—В–Є–Ї–Њ–Љ (—Б—В—Г–њ–µ–љ—З–∞—В–∞—П —В–µ—А–∞–њ–Є—П).
–Ю–Ї–Њ–ї–Њ 12% –≥–Њ—Б–њ–Є—В–∞–ї–Є–Ј–Є—А–Њ–≤–∞–љ–љ—Л—Е –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –њ–Є–µ–ї–Њ–љ–µ—Д—А–Є—В–Њ–Љ –Є–Љ–µ—О—В –±–∞–Ї—В–µ—А–Є–µ–Љ–Є—О, –Њ–і–љ–∞–Ї–Њ –љ–µ—В –і–∞–љ–љ—Л—Е –њ–Њ –њ—А–Њ–≥–љ–Њ—Б—В–Є—З–µ—Б–Ї–Њ–Љ—Г –Ј–љ–∞—З–µ–љ–Є—О —Н—В–Њ–≥–Њ —Д–µ–љ–Њ–Љ–µ–љ–∞. –£ –≤—Б–µ—Е –≥–Њ—Б–њ–Є—В–∞–ї–Є–Ј–Є—А–Њ–≤–∞–љ–љ—Л—Е –њ–∞—Ж–Є–µ–љ—В–Њ–≤, –љ–∞—А—П–і—Г —Б –±–∞–Ї—В–µ—А–Є–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є–Љ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ–Љ –Љ–Њ—З–Є, –≤–Ј—П—В–Њ–є –і–Њ –љ–∞—З–∞–ї–∞ –∞–љ—В–Є–±–Є–Њ—В–Є–Ї–Њ—В–µ—А–∞–њ–Є–Є, —Ж–µ–ї–µ—Б–Њ–Њ–±—А–∞–Ј–љ–Њ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ –≥–µ–Љ–Њ–Ї—Г–ї—М—В—Г—А—Л.
–Я–Њ—Б–ї–µ –Њ–Ї–Њ–љ—З–∞–љ–Є—П —В–µ—А–∞–њ–Є–Є –Є –Њ—В—Б—Г—В—Б—В–≤–Є—П —Б–Є–Љ–њ—В–Њ–Љ–Њ–≤ –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П –љ–µ—В –љ–µ–Њ–±—Е–Њ–і–Є–Љ–Њ—Б—В–Є –њ—А–Њ–≤–Њ–і–Є—В—М –њ–Њ–≤—В–Њ—А–љ–Њ–µ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ –Љ–Њ—З–Є. –Т —Б–ї—Г—З–∞–µ, –µ—Б–ї–Є —Б–Є–Љ–њ—В–Њ–Љ—Л –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П —Б–Њ—Е—А–∞–љ—П—О—В—Б—П —Б–≤—Л—И–µ 3 –і–љ–µ–є –љ–∞ —Д–Њ–љ–µ –∞–і–µ–Ї–≤–∞—В–љ–Њ–є –∞–љ—В–Є–±–Є–Њ—В–Є–Ї–Њ—В–µ—А–∞–њ–Є–Є –Є–ї–Є –µ—Б–ї–Є –љ–∞–±–ї—О–і–∞–µ—В—Б—П —А–µ—Ж–Є–і–Є–≤ –Є–љ—Д–µ–Ї—Ж–Є–Є –≤ —В–µ—З–µ–љ–Є–µ 2 –љ–µ–і–µ–ї—М –њ–Њ—Б–ї–µ –Њ–Ї–Њ–љ—З–∞–љ–Є—П —В–µ—А–∞–њ–Є–Є, –љ–µ–Њ–±—Е–Њ–і–Є–Љ–Њ –њ—А–Њ–≤–µ–і–µ–љ–Є–µ –±–∞–Ї—В–µ—А–Є–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Њ–≥–Њ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П –Љ–Њ—З–Є –Є –Њ–њ—А–µ–і–µ–ї–µ–љ–Є–µ —З—Г–≤—Б—В–≤–Є—В–µ–ї—М–љ–Њ—Б—В–Є –≤–Њ–Ј–±—Г–і–Є—В–µ–ї—П –Ї –∞–љ—В–Є–±–Є–Њ—В–Є–Ї–∞–Љ, –∞ —В–∞–Ї–ґ–µ –љ–∞–і–ї–µ–ґ–∞—Й–µ–µ –Є–љ—Б—В—А—Г–Љ–µ–љ—В–∞–ї—М–љ–Њ–µ –Њ–±—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ (–£–Ч–Ш, –Ъ–Ґ). –Я—А–Є –Њ—В—Б—Г—В—Б—В–≤–Є–Є —Г—А–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Њ–є –њ–∞—В–Њ–ї–Њ–≥–Є–Є –≤ —Н—В–Є—Е —Б–Є—В—Г–∞—Ж–Є—П—Е –љ–µ–Њ–±—Е–Њ–і–Є–Љ –њ–Њ–≤—В–Њ—А–љ—Л–є 2––љ–µ–і–µ–ї—М–љ—Л–є –Ї—Г—А—Б —В–µ—А–∞–њ–Є–Є –і—А—Г–≥–Є–Љ –∞–љ—В–Є–±–Є–Њ—В–Є–Ї–Њ–Љ —Б —Г—З–µ—В–Њ–Љ –і–∞–љ–љ—Л—Е —З—Г–≤—Б—В–≤–Є—В–µ–ї—М–љ–Њ—Б—В–Є. –Т —Б–ї—Г—З–∞–µ, –µ—Б–ї–Є —А–µ—Ж–Є–і–Є–≤ –±—Л–ї –≤—Л–Ј–≤–∞–љ —В–µ–Љ –ґ–µ —И—В–∞–Љ–Љ–Њ–Љ –≤–Њ–Ј–±—Г–і–Є—В–µ–ї—П, —З—В–Њ –Є –њ–µ—А–≤–Є—З–љ–∞—П –Є–љ—Д–µ–Ї—Ж–Є—П, —В–Њ –љ–µ–Њ–±—Е–Њ–і–Є–Љ –±–Њ–ї–µ–µ –і–ї–Є—В–µ–ї—М–љ—Л–є, 6––љ–µ–і–µ–ї—М–љ—Л–є –Ї—Г—А—Б –∞–љ—В–Є–±–Є–Њ—В–Є–Ї–Њ—В–µ—А–∞–њ–Є–Є [2].
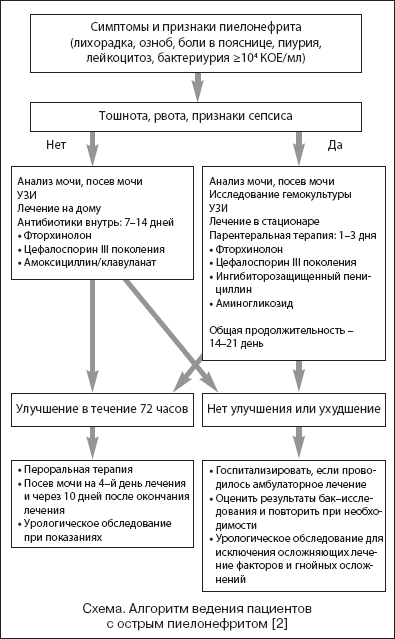
–Р–ї–≥–Њ—А–Є—В–Љ –≤–µ–і–µ–љ–Є—П –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –Њ—Б—В—А—Л–Љ –њ–Є–µ–ї–Њ–љ–µ—Д—А–Є—В–Њ–Љ –њ—А–µ–і—Б—В–∞–≤–ї–µ–љ –љ–∞ —Б—Е–µ–Љ–µ.
–†–µ—Ж–Є–і–Є–≤–Є—А—Г—О—Й–∞—П (–љ–µ–Њ—Б–ї–Њ–ґ–љ–µ–љ–љ–∞—П)
–Є–љ—Д–µ–Ї—Ж–Є—П –Љ–Њ—З–µ–≤—Л–≤–Њ–і—П—Й–Є—Е –њ—Г—В–µ–є —Г –ґ–µ–љ—Й–Є–љ
–†–µ—Ж–Є–і–Є–≤–Є—А—Г—О—Й–∞—П –љ–µ–Њ—Б–ї–Њ–ґ–љ–µ–љ–љ–∞—П –Є–љ—Д–µ–Ї—Ж–Є—П –Ь–Т–Я –Њ–њ—А–µ–і–µ–ї—П–µ—В—Б—П –Ї–∞–Ї —В—А–Є –Є –±–Њ–ї–µ–µ —Н–њ–Є–Ј–Њ–і–Њ–≤ –Њ—Б—В—А–Њ–є –Є–љ—Д–µ–Ї—Ж–Є–Є –≤ –њ–Њ—Б–ї–µ–і–љ–Є–µ 12 –Љ–µ—Б—П—Ж–µ–≤ –Є–ї–Є –і–≤–∞ –Є –±–Њ–ї–µ–µ —Н–њ–Є–Ј–Њ–і–∞ –≤ –њ–Њ—Б–ї–µ–і–љ–Є–µ 6 –Љ–µ—Б—П—Ж–µ–≤.
–Я—А–Є —А–µ—Ж–Є–і–Є–≤–Є—А—Г—О—Й–Є—Е –љ–µ–Њ—Б–ї–Њ–ґ–љ–µ–љ–љ—Л—Е –Є–љ—Д–µ–Ї—Ж–Є—П—Е –Ь–Т–Я –њ—А–µ–і–ї–Њ–ґ–µ–љ—Л —А–∞–Ј–ї–Є—З–љ—Л–µ –Љ–µ—В–Њ–і—Л –њ—А–Њ—Д–Є–ї–∞–Ї—В–Є–Ї–Є, –≤–Ї–ї—О—З–∞—О—Й–Є–µ –∞–љ—В–Є–±–Є–Њ—В–Є–Ї–Њ–њ—А–Њ—Д–Є–ї–∞–Ї—В–Є–Ї—Г, –Њ–њ–Њ—А–Њ–ґ–љ–µ–љ–Є–µ –Љ–Њ—З–µ–≤–Њ–≥–Њ –њ—Г–Ј—Л—А—П –њ–Њ—Б–ї–µ –њ–Њ–ї–Њ–≤–Њ–≥–Њ –∞–Ї—В–∞, –њ—А–Є–µ–Љ –Ї–ї—О–Ї–≤–µ–љ–љ–Њ–≥–Њ —Б–Њ–Ї–∞.
–Я—А–Њ—Д–Є–ї–∞–Ї—В–Є—З–µ—Б–Ї–Є–µ —А–µ–ґ–Є–Љ—Л –∞–љ—В–Є–±–Є–Њ—В–Є–Ї–Њ–≤. –Т –Њ—В–љ–Њ—И–µ–љ–Є–Є –∞–љ—В–Є–±–Є–Њ—В–Є–Ї–Њ–њ—А–Њ—Д–Є–ї–∞–Ї—В–Є–Ї–Є –љ–µ —Г—Б—В–∞–љ–Њ–≤–ї–µ–љ—Л –Њ–њ—В–Є–Љ–∞–ї—М–љ–∞—П –њ—А–Њ–і–Њ–ї–ґ–Є—В–µ–ї—М–љ–Њ—Б—В—М –њ—А–Є–Љ–µ–љ–µ–љ–Є—П –∞–љ—В–Є–±–Є–Њ—В–Є–Ї–Њ–≤ –Є –љ–∞–Є–±–Њ–ї–µ–µ —Н—Д—Д–µ–Ї—В–Є–≤–љ—Л–µ —Б—Е–µ–Љ—Л –њ—А–Њ—Д–Є–ї–∞–Ї—В–Є–Ї–Є. –Т –љ–∞—Б—В–Њ—П—Й–µ–µ –≤—А–µ–Љ—П –±–Њ–ї—М—И–Є–љ—Б—В–≤–Њ —Б–њ–µ—Ж–Є–∞–ї–Є—Б—В–Њ–≤ —Б—З–Є—В–∞–µ—В –љ–∞–Є–±–Њ–ї–µ–µ –∞–і–µ–Ї–≤–∞—В–љ—Л–Љ —Б–њ–Њ—Б–Њ–±–Њ–Љ –њ—А–Њ—Д–Є–ї–∞–Ї—В–Є–Ї–Є —А–µ–≥—Г–ї—П—А–љ—Л–є –њ—А–Є–µ–Љ –∞–љ—В–Є–±–Є–Њ—В–Є–Ї–∞ –њ–µ—А–µ–і —Б–љ–Њ–Љ –Є–ї–Є –њ–Њ—Б–ї–µ –њ–Њ–ї–Њ–≤–Њ–≥–Њ –∞–Ї—В–∞. –Т –Ъ–Њ–Ї—А—Н–љ–Њ–≤—Б–Ї–Њ–Љ –Њ–±–Ј–Њ—А–µ [15] –њ—А–Њ–∞–љ–∞–ї–Є–Ј–Є—А–Њ–≤–∞–љ—Л 108 –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–є –∞–љ—В–Є–±–Є–Њ—В–Є–Ї–Њ–њ—А–Њ—Д–Є–ї–∞–Ї—В–Є–Ї–Є. –Т –њ–ї–∞—Ж–µ–±–Њ––Ї–Њ–љ—В—А–Њ–ї–Є—А—Г–µ–Љ—Л—Е –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П—Е –±—Л–ї–Њ –њ–Њ–Ї–∞–Ј–∞–љ–Њ, —З—В–Њ —З–∞—Б—В–Њ—В–∞ —А–µ—Ж–Є–і–Є–≤–Њ–≤ –љ–∞ —Д–Њ–љ–µ –∞–љ—В–Є–±–Є–Њ—В–Є–Ї–Њ–≤ —Б–Њ—Б—В–∞–≤–Є–ї–∞ –Њ—В 0 –і–Њ 0,9 –љ–∞ –њ–∞—Ж–Є–µ–љ—В–∞/–≥–Њ–і –Є –±—Л–ї–∞ –і–Њ—Б—В–Њ–≤–µ—А–љ–Њ –љ–Є–ґ–µ, —З–µ–Љ –љ–∞ —Д–Њ–љ–µ –њ–ї–∞—Ж–µ–±–Њ (–Њ—В 0,8 –і–Њ 3,6). –Ю—В–љ–Њ—Б–Є—В–µ–ї—М–љ—Л–є —А–Є—Б–Ї —А–µ—Ж–Є–і–Є–≤–∞ –Є–љ—Д–µ–Ї—Ж–Є–Є —Б–Њ—Б—В–∞–≤–Є–ї 0,21 (95% –і–Њ–≤–µ—А–Є—В–µ–ї—М–љ—Л–є –Є–љ—В–µ—А–≤–∞–ї 0,13–0,34) –≤ –њ–Њ–ї—М–Ј—Г –∞–љ—В–Є–±–Є–Њ—В–Є–Ї–Њ–≤, –љ–Њ —А–Є—Б–Ї –љ–µ–ґ–µ–ї–∞—В–µ–ї—М–љ—Л—Е —П–≤–ї–µ–љ–Є–є –њ—А–Є –њ—А–Є–Љ–µ–љ–µ–љ–Є–Є –∞–љ—В–Є–±–Є–Њ—В–Є–Ї–Њ–≤ –±—Л–ї –і–Њ—Б—В–Њ–≤–µ—А–љ–Њ –≤—Л—И–µ – 1,78 (95% –Ф–Ш 1,06–3,00), –љ–∞–Є–±–Њ–ї–µ–µ —З–∞—Б—В—Л–Љ–Є –±—Л–ї–Є –Ї–∞–љ–і–Є–і–Њ–Ј –њ–Њ–ї–Њ—Б—В–Є —А—В–∞ –Є–ї–Є –≤–ї–∞–≥–∞–ї–Є—Й–∞, –ґ–µ–ї—Г–і–Њ—З–љ–Њ––Ї–Є—И–µ—З–љ—Л–µ —Б–Є–Љ–њ—В–Њ–Љ—Л. –Ґ–∞–Ї–Є–Љ –Њ–±—А–∞–Ј–Њ–Љ, —З–∞—Б—В–Њ—В–∞ —А–µ—Ж–Є–і–Є–≤–Њ–≤ –љ–∞ —Д–Њ–љ–µ –∞–љ—В–Є–±–Є–Њ—В–Є–Ї–Њ–њ—А–Њ—Д–Є–ї–∞–Ї—В–Є–Ї–Є —Б–љ–Є–ґ–∞–µ—В—Б—П –≤ 8 —А–∞–Ј –њ–Њ —Б—А–∞–≤–љ–µ–љ–Є—О —Б –њ–µ—А–Є–Њ–і–Њ–Љ –і–Њ –њ—А–Њ—Д–Є–ї–∞–Ї—В–Є–Ї–Є –Є –≤ 5 —А–∞–Ј –њ–Њ —Б—А–∞–≤–љ–µ–љ–Є—О —Б –њ–ї–∞—Ж–µ–±–Њ. –Я–µ—А–Є–Њ–і –њ—А–Њ—Д–Є–ї–∞–Ї—В–Є—З–µ—Б–Ї–Њ–≥–Њ –њ—А–Є–Љ–µ–љ–µ–љ–Є—П –∞–љ—В–Є–±–Є–Њ—В–Є–Ї–Њ–≤ —Б–Њ—Б—В–∞–≤–ї—П–ї –Њ—В 6 –і–Њ 12 –Љ–µ—Б—П—Ж–µ–≤. –Ю–і–љ–∞–Ї–Њ –њ–Њ—Б–ї–µ –Њ–Ї–Њ–љ—З–∞–љ–Є—П –њ—А–Њ—Д–Є–ї–∞–Ї—В–Є—З–µ—Б–Ї–Њ–≥–Њ –њ—А–Є–µ–Љ–∞ –∞–љ—В–Є–±–Є–Њ—В–Є–Ї–Њ–≤ –њ—А–Є–Љ–µ—А–љ–Њ —Г 60% –ґ–µ–љ—Й–Є–љ –≤ —В–µ—З–µ–љ–Є–µ 3–4 –Љ–µ—Б—П—Ж–µ–≤ –љ–∞–±–ї—О–і–∞–ї—Б—П —А–µ—Ж–Є–і–Є–≤ –Є–љ—Д–µ–Ї—Ж–Є–Є.
–Ъ–ї–Є–љ–Є—З–µ—Б–Ї–∞—П —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В—М –њ—А–Њ—Д–Є–ї–∞–Ї—В–Є—З–µ—Б–Ї–Њ–≥–Њ –њ—А–Є–Љ–µ–љ–µ–љ–Є—П –∞–љ—В–Є–±–Є–Њ—В–Є–Ї–Њ–≤ –њ–Њ–Ї–∞–Ј–∞–љ–∞ –≤ –Ї–Њ–љ—В—А–Њ–ї–Є—А—Г–µ–Љ—Л—Е –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П—Е –і–ї—П —Д—В–Њ—А—Е–Є–љ–Њ–ї–Њ–љ–Њ–≤ (–љ–Њ—А—Д–ї–Њ–Ї—Б–∞—Ж–Є–љ, —Ж–Є–њ—А–Њ—Д–ї–Њ–Ї—Б–∞—Ж–Є–љ, –њ–µ—Д–ї–Њ–Ї—Б–∞—Ж–Є–љ, —Ж–Є–љ–Њ–Ї—Б–∞—Ж–Є–љ), –љ–Є—В—А–Њ—Д—Г—А–∞–љ—В–Њ–Є–љ–∞, –Ї–Њ–—В—А–Є–Љ–Њ–Ї—Б–∞–Ј–Њ–ї–∞, —Ж–µ—Д–∞–ї–µ–Ї—Б–Є–љ–∞, —Ж–µ—Д–∞–Ї–ї–Њ—А–∞, —В—А–Є–Љ–µ—В–Њ–њ—А–Є–Љ–∞.
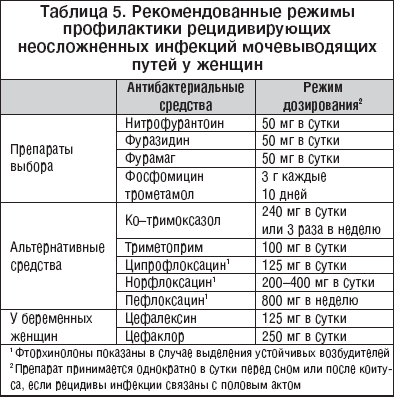
–†–µ–Ї–Њ–Љ–µ–љ–і–Њ–≤–∞–љ–љ—Л–µ —А–µ–ґ–Є–Љ—Л –њ—А–Њ—Д–Є–ї–∞–Ї—В–Є–Ї–Є —А–µ—Ж–Є–і–Є–≤–Є—А—Г—О—Й–µ–≥–Њ —Ж–Є—Б—В–Є—В–∞ —Б —Г—З–µ—В–Њ–Љ –љ–∞—Ж–Є–Њ–љ–∞–ї—М–љ—Л—Е –Њ—Б–Њ–±–µ–љ–љ–Њ—Б—В–µ–є –∞–љ—В–Є–±–Є–Њ—В–Є–Ї–Њ—А–µ–Ј–Є—Б—В–µ–љ—В–љ–Њ—Б—В–Є –Є –∞–љ—В–Є–±–Є–Њ—В–Є–Ї–Њ—В–µ—А–∞–њ–Є–Є –њ—А–µ–і—Б—В–∞–≤–ї–µ–љ—Л –≤ —В–∞–±–ї–Є—Ж–µ 5.
–Ю–њ—В–Є–Љ–∞–ї—М–љ–∞—П –њ—А–Њ–і–Њ–ї–ґ–Є—В–µ–ї—М–љ–Њ—Б—В—М –њ—А–Њ—Д–Є–ї–∞–Ї—В–Є–Ї–Є –љ–µ —Г—Б—В–∞–љ–Њ–≤–ї–µ–љ–∞, –љ–Њ –Њ–±—Л—З–љ–Њ —Б–Њ—Б—В–∞–≤–ї—П–µ—В –љ–µ –Љ–µ–љ–µ–µ 6–12 –Љ–µ—Б—П—Ж–µ–≤.
–Ф—А—Г–≥–Є–µ –Љ–µ—А—Л –њ—А–Њ—Д–Є–ї–∞–Ї—В–Є–Ї–Є –≤–Ї–ї—О—З–∞—О—В –њ—А–Є–Љ–µ–љ–µ–љ–Є–µ –Є–Љ–Љ—Г–љ–Њ–∞–Ї—В–Є–≤–љ—Л—Е —Д—А–∞–Ї—Ж–Є–є –Ї–Є—И–µ—З–љ–Њ–є –њ–∞–ї–Њ—З–Ї–Є –Ю–Ь–89, –Ї–ї—О–Ї–≤–µ–љ–љ—Л–є —Б–Њ–Ї, –≤–∞–≥–Є–љ–∞–ї—М–љ—Г—О –∞–њ–њ–ї–Є–Ї–∞—Ж–Є—О –ї–∞–Ї—В–Њ–±–∞—Ж–Є–ї–ї, –Њ–і–љ–∞–Ї–Њ –µ–і–Є–љ–Њ–≥–Њ –Љ–љ–µ–љ–Є—П –њ–Њ –Є—Е —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В–Є –≤ –љ–∞—Б—В–Њ—П—Й–µ–µ –≤—А–µ–Љ—П –љ–µ—В.
–£ –Љ–Њ–ї–Њ–і—Л—Е –Њ–±—А–∞–Ј–Њ–≤–∞–љ–љ—Л—Е –ґ–µ–љ—Й–Є–љ —Б –љ–µ—З–∞—Б—В—Л–Љ–Є —А–µ—Ж–Є–і–Є–≤–∞–Љ–Є –Є–љ—Д–µ–Ї—Ж–Є–є –≤–Њ–Ј–Љ–Њ–ґ–љ—Л —А–µ–Ї–Њ–Љ–µ–љ–і–∞—Ж–Є–Є –њ–Њ —В–∞–Ї –љ–∞–Ј—Л–≤–∞–µ–Љ–Њ–Љ—Г —Б–∞–Љ–Њ–љ–∞–Ј–љ–∞—З–µ–љ–Є—О –∞–љ—В–Є–±–Є–Њ—В–Є–Ї–∞ (—В–Њ –µ—Б—В—М —Б–∞–Љ–Њ—Б—В–Њ—П—В–µ–ї—М–љ—Л–є –њ—А–Є–µ–Љ –њ—А–µ–њ–∞—А–∞—В–∞ –≤ —А–∞–љ–љ–Є–µ —Б—А–Њ–Ї–Є –њ–Њ—Б–ї–µ –љ–∞—З–∞–ї–∞ –Є–љ—Д–µ–Ї—Ж–Є–Є –±–µ–Ј –Њ–±—А–∞—Й–µ–љ–Є—П –Ї –≤—А–∞—З—Г).
–Т –љ–∞—Б—В–Њ—П—Й–µ–µ –≤—А–µ–Љ—П –љ–µ –њ–Њ–ї—Г—З–µ–љ–Њ –і–∞–љ–љ—Л—Е –Њ —В–Њ–Љ, —З—В–Њ –і–ї–Є—В–µ–ї—М–љ—Л–є –њ—А–Є–µ–Љ –∞–љ—В–Є–±–∞–Ї—В–µ—А–Є–∞–ї—М–љ—Л—Е –њ—А–µ–њ–∞—А–∞—В–Њ–≤ –і–ї—П –њ—А–Њ—Д–Є–ї–∞–Ї—В–Є–Ї–Є —А–µ—Ж–Є–і–Є–≤–Њ–≤ –Є–љ—Д–µ–Ї—Ж–Є–Є –Ь–Т–Я —Б–Њ–њ—А–Њ–≤–Њ–ґ–і–∞–µ—В—Б—П –≤–Њ–Ј–љ–Є–Ї–љ–Њ–≤–µ–љ–Є–µ–Љ —Г—Б—В–Њ–є—З–Є–≤—Л—Е —И—В–∞–Љ–Љ–Њ–≤ —Г—А–Њ–њ–∞—В–Њ–≥–µ–љ–Њ–≤ [16–18].
–Ш–љ—Д–µ–Ї—Ж–Є–Є –Љ–Њ—З–µ–≤—Л–≤–Њ–і—П—Й–Є—Е –њ—Г—В–µ–є
—Г –±–µ—А–µ–Љ–µ–љ–љ—Л—Е
–Ш–љ—Д–µ–Ї—Ж–Є–Є –Ь–Т–Я —П–≤–ї—П—О—В—Б—П –љ–∞–Є–±–Њ–ї–µ–µ —З–∞—Б—В—Л–Љ–Є –Є–љ—Д–µ–Ї—Ж–Є–Њ–љ–љ—Л–Љ–Є –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П–Љ–Є —Г –±–µ—А–µ–Љ–µ–љ–љ—Л—Е –ґ–µ–љ—Й–Є–љ. –С–µ—Б—Б–Є–Љ–њ—В–Њ–Љ–љ–∞—П –±–∞–Ї—В–µ—А–Є—Г—А–Є—П –≤—Л—П–≤–ї—П–µ—В—Б—П —Г 4–7% –±–µ—А–µ–Љ–µ–љ–љ—Л—Е –ґ–µ–љ—Й–Є–љ, –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є –Љ–∞–љ–Є—Д–µ—Б—В–Є—А–Њ–≤–∞–љ–љ–∞—П –Є–љ—Д–µ–Ї—Ж–Є—П —А–∞–Ј–≤–Є–≤–∞–µ—В—Б—П —Г 1–2% –ґ–µ–љ—Й–Є–љ [19]. –Э–∞–Є–±–Њ–ї—М—И–∞—П —З–∞—Б—В–Њ—В–∞ –Є–љ—Д–µ–Ї—Ж–Є–є –Ь–Т–Я –Њ—В–Љ–µ—З–∞–µ—В—Б—П –Љ–µ–ґ–і—Г 9 –Є 17 –љ–µ–і–µ–ї—П–Љ–Є –±–µ—А–µ–Љ–µ–љ–љ–Њ—Б—В–Є [20]. –С–∞–Ї—В–µ—А–Є—Г—А–Є—П –≤–Њ –≤—А–µ–Љ—П –±–µ—А–µ–Љ–µ–љ–љ–Њ—Б—В–Є —Б–Њ–њ—А–Њ–≤–Њ–ґ–і–∞–µ—В—Б—П 50% —Г–≤–µ–ї–Є—З–µ–љ–Є–µ–Љ —А–Є—Б–Ї–∞ —А–Њ–ґ–і–µ–љ–Є—П —А–µ–±–µ–љ–Ї–∞ —Б –љ–Є–Ј–Ї–Њ–є –Љ–∞—Б—Б–Њ–є —В–µ–ї–∞ (<2500 –≥), –њ—А–µ–ґ–і–µ–≤—А–µ–Љ–µ–љ–љ—Л—Е —А–Њ–і–Њ–≤ –Є –љ–µ–Њ–љ–∞—В–∞–ї—М–љ–Њ–є –ї–µ—В–∞–ї—М–љ–Њ—Б—В–Є [20–21].
–£ –±–µ—А–µ–Љ–µ–љ–љ—Л—Е –ґ–µ–љ—Й–Є–љ –љ–µ –њ—А–Њ–≤–Њ–і—П—В—Б—П –Ї–Њ—А–Њ—В–Ї–Є–µ 3––і–љ–µ–≤–љ—Л–µ –Ї—Г—А—Б—Л –∞–љ—В–Є–±–Є–Њ—В–Є–Ї–Њ—В–µ—А–∞–њ–Є–Є –Њ—Б—В—А–Њ–≥–Њ —Ж–Є—Б—В–Є—В–∞ –Є–Ј––Ј–∞ –≤—Л—Б–Њ–Ї–Њ–≥–Њ —А–Є—Б–Ї–∞ —А–µ—Ж–Є–і–Є–≤–Њ–≤ –Є–љ—Д–µ–Ї—Ж–Є–Є. –Ю–±—Л—З–љ–Њ —А–µ–Ї–Њ–Љ–µ–љ–і—Г—О—В—Б—П 7––і–љ–µ–≤–љ—Л–µ –Ї—Г—А—Б—Л —В–µ—А–∞–њ–Є–Є –њ–µ—А–Њ—А–∞–ї—М–љ—Л–Љ —Ж–µ—Д–∞–ї–Њ—Б–њ–Њ—А–Є–љ–Њ–Љ III –њ–Њ–Ї–Њ–ї–µ–љ–Є—П (—Ж–µ—Д–Є–Ї—Б–Є–Љ, —Ж–µ—Д—В–Є–±—Г—В–µ–љ) –Є–ї–Є –љ–Є—В—А–Њ—Д—Г—А–∞–љ–Њ–Љ; —Д–Њ—Б—Д–Њ–Љ–Є—Ж–Є–љ —В—А–Њ–Љ–µ—В–∞–Љ–Њ–ї –Љ–Њ–ґ–µ—В –љ–∞–Ј–љ–∞—З–∞—В—М—Б—П –≤ –Њ–і–љ–Њ–Ї—А–∞—В–љ–Њ–є –і–Њ–Ј–µ 3 –≥. –Ф–Њ –љ–∞—З–∞–ї–∞ —В–µ—А–∞–њ–Є–Є –Є –њ–Њ—Б–ї–µ –Њ–Ї–Њ–љ—З–∞–љ–Є—П —Ж–µ–ї–µ—Б–Њ–Њ–±—А–∞–Ј–љ–Њ –њ—А–Њ–≤–Њ–і–Є—В—М –±–∞–Ї—В–µ—А–Є–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Њ–µ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ –Љ–Њ—З–Є.
–Ю—В—Б—Г—В—Б—В–≤–Є–µ —В–µ—А–∞—В–Њ–≥–µ–љ–љ—Л—Е —Б–≤–Њ–є—Б—В–≤ –Є –±–µ–Ј–Њ–њ–∞—Б–љ–Њ—Б—В—М –і–ї—П –њ–ї–Њ–і–∞ –њ–Њ–Ї–∞–Ј–∞–љ—Л –і–ї—П b––ї–∞–Ї—В–∞–Љ–Њ–≤ [22], –љ–Є—В—А–Њ—Д—Г—А–∞–љ—В–Њ–Є–љ–∞ [23], —Д—Г—А–∞–Ј–Є–і–Є–љ–∞ [24] –≤ –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є—Е –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П—Е; –і–ї—П —Д–Њ—Б—Д–Њ–Љ–Є—Ж–Є–љ–∞ –µ—Б—В—М —В–Њ–ї—М–Ї–Њ —Н–Ї—Б–њ–µ—А–Є–Љ–µ–љ—В–∞–ї—М–љ—Л–µ –і–∞–љ–љ—Л–µ [25].
–Ф–ї—П –ї–µ—З–µ–љ–Є—П –Њ—Б—В—А–Њ–≥–Њ –њ–Є–µ–ї–Њ–љ–µ—Д—А–Є—В–∞ —Б–ї–µ–і—Г–µ—В –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞—В—М —Ж–µ—Д–∞–ї–Њ—Б–њ–Њ—А–Є–љ—Л III –њ–Њ–Ї–Њ–ї–µ–љ–Є—П –Є–ї–Є –Є–љ–≥–Є–±–Є—В–Њ—А–Њ–Ј–∞—Й–Є—Й–µ–љ–љ—Л–µ –њ–µ–љ–Є—Ж–Є–ї–ї–Є–љ—Л –Є–ї–Є –∞–Љ–Є–љ–Њ–≥–ї–Є–Ї–Њ–Ј–Є–і—Л. –Ю–њ—В–Є–Љ–∞–ї—М–љ–∞—П –њ—А–Њ–і–Њ–ї–ґ–Є—В–µ–ї—М–љ–Њ—Б—В—М —В–µ—А–∞–њ–Є–Є –љ–µ —Г—Б—В–∞–љ–Њ–≤–ї–µ–љ–∞. –Т –Ъ–Њ–Ї—А—Н–љ–Њ–≤—Б–Ї–Њ–Љ –∞–љ–∞–ї–Є–Ј–µ –љ–µ —Г—Б—В–∞–љ–Њ–≤–ї–µ–љ–Њ —А–∞–Ј–ї–Є—З–Є–є –≤ –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Њ–є –Є–ї–Є –±–∞–Ї—В–µ—А–Є–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Њ–є —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В–Є, —З–∞—Б—В–Њ—В–µ —А–µ—Ж–Є–і–Є–≤–Њ–≤, –∞ —В–∞–Ї–ґ–µ –Њ—В–і–∞–ї–µ–љ–љ—Л—Е —А–µ–Ј—Г–ї—М—В–∞—В–∞—Е (–њ—А–µ–ґ–і–µ–≤—А–µ–Љ–µ–љ–љ—Л–µ —А–Њ–і—Л, –Њ—Б–ї–Њ–ґ–љ–µ–љ–Є—П –≤ —А–Њ–і–∞—Е, –љ–µ–Њ–љ–∞—В–∞–ї—М–љ–∞—П —Б–Љ–µ—А—В–љ–Њ—Б—В—М) –Љ–µ–ґ–і—Г –љ–∞–Ј–≤–∞–љ–љ—Л–Љ–Є —А–µ–ґ–Є–Љ–∞–Љ–Є –∞–љ—В–Є–±–∞–Ї—В–µ—А–Є–∞–ї—М–љ–Њ–є —В–µ—А–∞–њ–Є–Є –њ–Є–µ–ї–Њ–љ–µ—Д—А–Є—В–∞ —Г –±–µ—А–µ–Љ–µ–љ–љ—Л—Е –ґ–µ–љ—Й–Є–љ [26].
–£ –±–µ—А–µ–Љ–µ–љ–љ—Л—Е –ґ–µ–љ—Й–Є–љ –њ—А–Њ—В–Є–≤–Њ–њ–Њ–Ї–∞–Ј–∞–љ—Л —Д—В–Њ—А—Е–Є–љ–Њ–ї–Њ–љ—Л, —В–µ—В—А–∞—Ж–Є–Ї–ї–Є–љ—Л –Є –Ї–Њ–—В—А–Є–Љ–Њ–Ї—Б–∞–Ј–Њ–ї.
–Ш–љ—Д–µ–Ї—Ж–Є–Є –Љ–Њ—З–µ–≤—Л–≤–Њ–і—П—Й–Є—Е –њ—Г—В–µ–є
—Г –ґ–µ–љ—Й–Є–љ –≤ –њ–Њ—Б—В–Љ–µ–љ–Њ–њ–∞—Г–Ј–µ
–Я–Њ–і—Е–Њ–і—Л –Ї –∞–љ—В–Є–±–∞–Ї—В–µ—А–Є–∞–ї—М–љ–Њ–є —В–µ—А–∞–њ–Є–Є —Б—Е–Њ–і–љ—Л–µ, –Ї–∞–Ї —Г –ґ–µ–љ—Й–Є–љ –і–Њ –Љ–µ–љ–Њ–њ–∞—Г–Ј—Л. –Я—А–Є –Њ—Б—В—А–Њ–Љ —Ж–Є—Б—В–Є—В–µ –Ї–Њ—А–Њ—В–Ї–Є–µ –Ї—Г—А—Б—Л –∞–љ—В–Є–±–Є–Њ—В–Є–Ї–Њ—В–µ—А–∞–њ–Є–Є –њ–Њ–і–і–µ—А–ґ–Є–≤–∞—О—В—Б—П –љ–µ –≤—Б–µ–Љ–Є —Б–њ–µ—Ж–Є–∞–ї–Є—Б—В–∞–Љ–Є. –Т —В–Њ –ґ–µ –≤—А–µ–Љ—П –µ—Б—В—М –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П, –њ–Њ–і—В–≤–µ—А–ґ–і–∞—О—Й–Є–µ –≤–Њ–Ј–Љ–Њ–ґ–љ–Њ—Б—В—М –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є—П —Д—В–Њ—А—Е–Є–љ–Њ–ї–Њ–љ–Њ–≤ (–љ–Њ—А—Д–ї–Њ–Ї—Б–∞—Ж–Є–љ, —Ж–Є–њ—А–Њ—Д–ї–Њ–Ї—Б–∞—Ж–Є–љ, –Њ—Д–ї–Њ–Ї—Б–∞—Ж–Є–љ) –≤ 3––і–љ–µ–≤–љ–Њ–Љ —А–µ–ґ–Є–Љ–µ. –Я—А–Є –≤–Њ–Ј–љ–Є–Ї–љ–Њ–≤–µ–љ–Є–Є –Њ—Б—В—А–Њ–≥–Њ —Ж–Є—Б—В–Є—В–∞ —Г –ґ–µ–љ—Й–Є–љ—Л –≤ –њ–Њ—Б—В–Љ–µ–љ–Њ–њ–∞—Г–Ј–µ —А–µ–Ї–Њ–Љ–µ–љ–і—Г–µ—В—Б—П –њ—А–Њ–≤–µ–і–µ–љ–Є–µ –≥–Є–љ–µ–Ї–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Њ–≥–Њ –Њ–±—Б–ї–µ–і–Њ–≤–∞–љ–Є—П. –Я—А–Є —З–∞—Б—В—Л—Е —А–µ—Ж–Є–і–Є–≤–∞—Е –Є–љ—Д–µ–Ї—Ж–Є–є –Ь–Т–Я —Г –ґ–µ–љ—Й–Є–љ –≤ –њ–Њ—Б—В–Љ–µ–љ–Њ–њ–∞—Г–Ј–µ —А–µ–Ї–Њ–Љ–µ–љ–і–Њ–≤–∞–љ–Њ –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є–µ –Љ–µ—Б—В–љ—Л—Е —Н—Б—В—А–Њ–≥–µ–љ–Њ–≤, –Ї–Њ—В–Њ—А—Л–µ –і–Њ—Б—В–Њ–≤–µ—А–љ–Њ —Б–љ–Є–ґ–∞—О—В —З–∞—Б—В–Њ—В—Г —А–µ—Ж–Є–і–Є–≤–Њ–≤ [27].
–С–µ—Б—Б–Є–Љ–њ—В–Њ–Љ–љ–∞—П –±–∞–Ї—В–µ—А–Є—Г—А–Є—П
–С–µ—Б—Б–Є–Љ–њ—В–Њ–Љ–љ–∞—П –±–∞–Ї—В–µ—А–Є—Г—А–Є—П –і–Є–∞–≥–љ–Њ—Б—В–Є—А—Г–µ—В—Б—П –њ—А–Є –≤—Л–і–µ–ї–µ–љ–Є–Є –≤ –і–≤—Г—Е –њ–Њ—Б–ї–µ–і–Њ–≤–∞—В–µ–ї—М–љ—Л—Е –∞–љ–∞–ї–Є–Ј–∞—Е –Љ–Њ—З–Є –±–∞–Ї—В–µ—А–Є–є –≤ –Ї–Њ–ї–Є—З–µ—Б—В–≤–µ >105 –Ъ–Ю–Х/–Љ–ї. –С–µ—Б—Б–Є–Љ–њ—В–Њ–Љ–љ–∞—П –±–∞–Ї—В–µ—А–Є—Г—А–Є—П —З–∞—Б—В–Њ –≤—Л—П–≤–ї—П–µ—В—Б—П —Г –Њ–њ—А–µ–і–µ–ї–µ–љ–љ—Л—Е –Ї–∞—В–µ–≥–Њ—А–Є–є –њ–∞—Ж–Є–µ–љ—В–Њ–≤ (–њ–Њ–ґ–Є–ї—Л–µ, –±–µ—А–µ–Љ–µ–љ–љ—Л–µ –ґ–µ–љ—Й–Є–љ—Л, –љ–∞–ї–Є—З–Є–µ –њ–Њ—Б—В–Њ—П–љ–љ–Њ–≥–Њ –Љ–Њ—З–µ–≤–Њ–≥–Њ –Ї–∞—В–µ—В–µ—А–∞, –±–Њ–ї—М–љ—Л–µ —Б–∞—Е–∞—А–љ—Л–Љ –і–Є–∞–±–µ—В–Њ–Љ) –Є —В—А–µ–±—Г–µ—В —А–µ—И–µ–љ–Є—П –≤–Њ–њ—А–Њ—Б–∞ –Њ —Ж–µ–ї–µ—Б–Њ–Њ–±—А–∞–Ј–љ–Њ—Б—В–Є –њ—А–Њ–≤–µ–і–µ–љ–Є—П –∞–љ—В–Є–±–∞–Ї—В–µ—А–Є–∞–ї—М–љ–Њ–є —В–µ—А–∞–њ–Є–Є.
–С–µ—Б—Б–Є–Љ–њ—В–Њ–Љ–љ–∞—П –±–∞–Ї—В–µ—А–Є—Г—А–Є—П —А–µ–і–Ї–Њ –∞—Б—Б–Њ—Ж–Є–Є—А—Г–µ—В—Б—П —Б –љ–µ–±–ї–∞–≥–Њ–њ—А–Є—П—В–љ—Л–Љ–Є –њ–Њ—Б–ї–µ–і—Б—В–≤–Є—П–Љ–Є –Є –љ–µ–љ–∞–Ј–љ–∞—З–µ–љ–Є–µ –∞–љ—В–Є–±–Є–Њ—В–Є–Ї–Њ–≤ –љ–µ —Б–Њ–њ—А–Њ–≤–Њ–ґ–і–∞–µ—В—Б—П –њ–Њ–≤—Л—И–µ–љ–љ—Л–Љ —А–Є—Б–Ї–Њ–Љ —А–∞–Ј–≤–Є—В–Є—П –Є–љ—Д–µ–Ї—Ж–Є–є —Г –±–Њ–ї—М—И–Є–љ—Б—В–≤–∞ –њ–∞—Ж–Є–µ–љ—В–Њ–≤. –Э–µ —А–µ–Ї–Њ–Љ–µ–љ–і—Г–µ—В—Б—П –і–∞–ї—М–љ–µ–є—И–µ–µ –Њ–±—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ –Є –∞–љ—В–Є–±–Є–Њ—В–Є–Ї–Њ—В–µ—А–∞–њ–Є—П –њ—А–Є –±–µ—Б—Б–Є–Љ–њ—В–Њ–Љ–љ–Њ–є –±–∞–Ї—В–µ—А–Є—Г—А–Є–Є —Г —Б–ї–µ–і—Г—О—Й–Є—Е –Ї–∞—В–µ–≥–Њ—А–Є–є –њ–∞—Ж–Є–µ–љ—В–Њ–≤ [28]:
• –Э–µ–±–µ—А–µ–Љ–µ–љ–љ—Л–µ –ґ–µ–љ—Й–Є–љ—Л –і–Њ –Љ–µ–љ–Њ–њ–∞—Г–Ј—Л;
• –Ц–µ–љ—Й–Є–љ—Л —Б —Б–∞—Е–∞—А–љ—Л–Љ –і–Є–∞–±–µ—В–Њ–Љ;
• –Ы–Є—Ж–∞ –њ–Њ–ґ–Є–ї–Њ–≥–Њ –≤–Њ–Ј—А–∞—Б—В–∞, –ґ–Є–≤—Г—Й–Є–µ –і–Њ–Љ–∞;
• –Ы–Є—Ж–∞ –њ–Њ–ґ–Є–ї–Њ–≥–Њ –≤–Њ–Ј—А–∞—Б—В–∞ –≤ –і–Њ–Љ–∞—Е –њ—А–µ—Б—В–∞—А–µ–ї—Л—Е;
• –Я–∞—Ж–Є–µ–љ—В—Л —Б –њ–Њ–≤—А–µ–ґ–і–µ–љ–Є—П–Љ–Є —Б–њ–Є–љ–љ–Њ–≥–Њ –Љ–Њ–Ј–≥–∞;
• –Я–∞—Ж–Є–µ–љ—В—Л —Б –њ–Њ—Б—В–Њ—П–љ–љ—Л–Љ –Љ–Њ—З–µ–≤—Л–Љ –Ї–∞—В–µ—В–µ—А–Њ–Љ.
–°–Ї—А–Є–љ–Є–љ–≥ –љ–∞ –љ–∞–ї–Є—З–Є–µ –±–∞–Ї—В–µ—А–Є—Г—А–Є–Є –Є –∞–љ—В–Є–±–∞–Ї—В–µ—А–Є–∞–ї—М–љ–∞—П —В–µ—А–∞–њ–Є—П —А–µ–Ї–Њ–Љ–µ–љ–і—Г—О—В—Б—П —В–Њ–ї—М–Ї–Њ –≤ —В—А–µ—Е —Б–Є—В—Г–∞—Ж–Є—П—Е:
• –С–µ—А–µ–Љ–µ–љ–љ—Л–µ –ґ–µ–љ—Й–Є–љ—Л;
• –Я–µ—А–µ–і —В—А–∞–љ—Б—Г—А–µ—В—А–∞–ї—М–љ–Њ–є —А–µ–Ј–µ–Ї—Ж–Є–µ–є –њ—А–µ–і—Б—В–∞—В–µ–ї—М–љ–Њ–є –ґ–µ–ї–µ–Ј—Л;
• –Я–µ—А–µ–і –і—А—Г–≥–Є–Љ–Є —В—А–∞–≤–Љ–∞—В–Є—З–µ—Б–Ї–Є–Љ–Є —Г—А–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є–Љ–Є –≤–Љ–µ—И–∞—В–µ–ї—М—Б—В–≤–∞–Љ–Є.
–Т –і–≤—Г—Е –њ–Њ—Б–ї–µ–і–љ–Є—Е —Б–ї—Г—З–∞—П—Е –∞–љ—В–Є–±–Є–Њ—В–Є–Ї–Є —Б–ї–µ–і—Г–µ—В –љ–∞–Ј–љ–∞—З–Є—В—М –љ–µ–Ј–∞–і–Њ–ї–≥–Њ –і–Њ –Њ–њ–µ—А–∞—Ж–Є–Є – –Њ–±—Л—З–љ–Њ –Ј–∞ 1–3 –і–љ—П. –Т–Њ–Ј–Љ–Њ–ґ–љ–Њ –њ—А–Є–Љ–µ–љ–µ–љ–Є–µ —Д—В–Њ—А—Е–Є–љ–Њ–ї–Њ–љ–Њ–≤ –Є–ї–Є –љ–Є—В—А–Њ—Д—Г—А–∞–љ–Њ–≤.
–£ –±–µ—А–µ–Љ–µ–љ–љ—Л—Е –ґ–µ–љ—Й–Є–љ –≤ —Б–ї—Г—З–∞–µ –≤—Л—П–≤–ї–µ–љ–Є—П –±–µ—Б—Б–Є–Љ–њ—В–Њ–Љ–љ–Њ–є –±–∞–Ї—В–µ—А–Є—Г—А–Є–Є –њ—А–Є–Љ–µ–љ—П–µ—В—Б—П 5–7–і–љ–µ–≤–љ—Л–є –Ї—Г—А—Б —В–µ—А–∞–њ–Є–Є –Њ–і–љ–Є–Љ –Є–Ј —Б–ї–µ–і—Г—О—Й–Є—Е –∞–љ—В–Є–±–∞–Ї—В–µ—А–Є–∞–ї—М–љ—Л—Е –њ—А–µ–њ–∞—А–∞—В–Њ–≤: —Ж–µ—Д–Є–Ї—Б–Є–Љ (400 –Љ–≥ –≤ —Б—Г—В–Ї–Є), —Ж–µ—Д—В–Є–±—Г—В–µ–љ (400 –Љ–≥ –≤ —Б—Г—В–Ї–Є), –љ–Є—В—А–Њ—Д—Г—А–∞–љ—В–Њ–Є–љ (400 –Љ–≥ –≤ —Б—Г—В–Ї–Є), —Д—Г—А–∞–Ј–Є–і–Є–љ (300 –Љ–≥ –≤ —Б—Г—В–Ї–Є), —Д—Г—А–∞–Љ–∞–≥ (150 –Љ–≥ –≤ —Б—Г—В–Ї–Є). –Ъ–Њ–љ—В—А–Њ–ї—М–љ–Њ–µ –±–∞–Ї—В–µ—А–Є–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Њ–µ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ –Љ–Њ—З–Є —Б–ї–µ–і—Г–µ—В –њ—А–Њ–≤–Њ–і–Є—В—М —З–µ—А–µ–Ј 1–4 –љ–µ–і–µ–ї–Є –њ–Њ—Б–ї–µ –ї–µ—З–µ–љ–Є—П –Є –µ—Й–µ —А–∞–Ј –њ–µ—А–µ–і —А–Њ–і–∞–Љ–Є.


–Ы–Є—В–µ—А–∞—В—Г—А–∞
1. Foxman B. Epidemiology of urinary tract infections: incidence, morbidity, and economic costs. Am J Med 2002;113(Suppl 1A):5S–13S.
2. Naber KG, Bishop MC, Bjerklund–Johansen TE, et al. Guidelines on the management of urinary and male genital tract infections. European Association of Urology (update 2006), 2006. ISBN 90–70244–37–3.
3. Naber KG, Bergman B, Bishop MC, et al. Urinary tract infection (UTI) Working Group of the Health Care Office (HCO) of the European Association of Urology (EAU). EAU guidelines for the management of urinary and male genital tract infections. Eur Urol 2001;40:576–88.
4. Warren JW, Abrutyn E, Hebel JR, et al. Guidelines for antimicrobial treatment of uncomplicated acute bacterial cystitis and acute pyelonephritis in women. Clin Infect Dis 1999;29:745–58.
5. Stamm WE, Counts GW, Running KR, et al. Diagnosis of coliform infection in acutely dysuric women. N Engl J Med 1982;307:463–468.
6. –°–Є–і–Њ—А–µ–љ–Ї–Њ –°.–Т., –Ш–≤–∞–љ–Њ–≤ –Ф.–Т. –†–µ–Ј—Г–ї—М—В–∞—В—Л –Є–Ј—Г—З–µ–љ–Є—П —А–∞—Б–њ—А–Њ—Б—В—А–∞–љ–µ–љ–Є—П –∞–љ—В–Є–±–Є–Њ—В–Є–Ї–Њ—А–µ–Ј–Є—Б—В–µ–љ—В–љ–Њ—Б—В–Є —Б—А–µ–і–Є –≤–Њ–Ј–±—Г–і–Є—В–µ–ї–µ–є –≤–љ–µ–±–Њ–ї—М–љ–Є—З–љ—Л—Е –Є–љ—Д–µ–Ї—Ж–Є–є –Љ–Њ—З–µ–≤—Л–≤–Њ–і—П—Й–Є—Е –њ—Г—В–µ–є. –Р–љ—В–Є–±–Є–Њ—В–Є–Ї–Є –Є —Е–Є–Љ–Є–Њ—В–µ—А–∞–њ–Є—П 2005; 50(1): 3–10.
7. –ѓ–Ї–Њ–≤–ї–µ–≤ –°.–Т., –Ы–Њ–≥–≤–Є–љ–Њ–≤ –Ы.–Р., –Ъ–ї–Њ—З–Ї–Њ–≤ –Ш.–Р. –Є –і—А. –Ъ–ї–Є–љ–Є—З–µ—Б–Ї–∞—П –Є –±–∞–Ї—В–µ—А–Є–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–∞—П —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В—М –њ—А–µ–њ–∞—А–∞—В–∞ «–§—Г—А–∞–Љ–∞–≥» —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –Њ—Б—В—А—Л–Љ —Ж–Є—Б—В–Є—В–Њ–Љ. –Ш–љ—Д–µ–Ї—Ж–Є–Є –Є –∞–љ—В–Є–Љ–Є–Ї—А–Њ–±–љ–∞—П —В–µ—А–∞–њ–Є—П 2005; 7 (4): 120–6.
8. Hooton TM, Besser R, Foxman B, et al. Acute uncomplicated cystitis in an era of increasing antibiotic resistance: a proposed approach to empirical therapy. Clin Infect Dis 2004;39:75–80.
9. Gupta K, Hooton TM, Stamm WE. Increasing antimicrobial resistance and the management of uncomplicated community–acquired urinary tract infections. Ann Intern Med 2001;135:41–50.
10. Gupta K, Scholes D, Stamm WE. Increasing prevalence of antimicrobial resistance among uropathogens causing acute uncomplicated cystitis in women. JAMA 1999;281:736–8.
11. Wiedermann B. Changing resistance patterns in urinary tract infections: global perspectives ant treatment consequences. Clin Drug Invest 2001;21 (Suppl 1):1–24.
12. Kahlmeter G. An international survey of the antimicrobial susceptibility of pathogens fron uncomplicated urinary tract infections: the ECO–SENS Project. J Antimicrob Chemother 2003;51:69–76.
13. Honderlick P, Cahen P, Gravisse J, Vignon D. Uncomplicated urinary tract infections, what about fosfomycin and nitrofurantoin in 2006. Pathol Biol (Paris) 2006; Oct 4 [Epub ahead of print].
14. –†–∞—Д–∞–ї—М—Б–Ї–Є–є –Т–Т, –°—В—А–∞—З—Г–љ—Б–Ї–Є–є –Ы.–°., –Ъ—А–µ—З–Є–Ї–Њ–≤–∞ –Ю.–Ш. –†–µ–Ј–Є—Б—В–µ–љ—В–љ–Њ—Б—В—М –≤–љ–µ–±–Њ–ї—М–љ–Є—З–љ—Л—Е –≤–Њ–Ј–±—Г–і–Є—В–µ–ї–µ–є –Є–љ—Д–µ–Ї—Ж–Є–є –Љ–Њ—З–µ–≤—Л–≤–Њ–і—П—Й–Є—Е –њ—Г—В–µ–є –љ–∞ –Њ—Б–љ–Њ–≤–∞–љ–Є–Є –Љ–љ–Њ–≥–Њ—Ж–µ–љ—В—А–Њ–≤—Л—Е –Љ–Є–Ї—А–Њ–±–Є–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є—Е –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–є UTIAP–1 –Є UTIAP–II. –£—А–Њ–ї–Њ–≥–Є—П 2004; вДЦ2: 13–7.
15. Albert X, Huertas I, Pereiro II, et al. Antibiotics for preventing recurrent urinary tract infection in non–pregnant women. Cochrane Database Syst Rev 2004:CD001209.
16. Brumfitt W, Hamilton–Miller JM. Efficacy and safety profile of long–term nitrofurantoin in urinary tract infections: 18 years’ experience. J Antimicrob Chemother 1998;42:363–371.
17. Nunez U, Solis Z. Macrocrystalline nitrofurantoin versus norfloxacin as treatment and prophylaxis in uncomplicated recurrent urinary tract infection. Curr Therap Res Clin Exp 1990;48:234–245.
18. Melekos MD, Asbach HW, Gerharz E, et al. Post–intercourse versus daily ciprofloxacin prophylaxis for recurrent urinary tract infections in premenopausal women. J Urol 1997;157:935–939.
19. MacLean AB. Urinary tract infection in pregnancy. Br J Urol 1997;80(Suppl 1):10–13.
20. Stenqvist K, Dahlen–Nilsson I, Lidin–Janson G, et al. Bacteriuria in pregnancy. Frequency and risk of acquisition. Am J Epidemiol 1989;129:372–379.
21. Christensen B. Which antibiotics are appropriate for the treating bacteriuria in pregnancy? J Antimicrob Chemother 2000;46(Suppl S1):29–34.
22. Reeves DS. A perspective on the safety of antibacterials used to treat urinary tract infections. J Antimicrob Chemother 1994;33(Suppl A):111–20.
23. Ben David S, Einarson T, Ben David Y, et al. The safety of nitrofurantoin during the first trimester of pregnancy: meta–analysis. Fundament Clin Pharmacology 1995;9:503–7.
24. Czeizel AE, Rockenbauer M, Sorensen HT, Olsen J. A population–based case–control teratologic study of furazidine, a nitrofuran–derivative treatment during pregnancy. Clin Nephrol 2000;53(4):257–63.
25. Stein GE. Single–dose treatment of acute cystitis with fosfomycin tromethamine. Ann Pharmacother 1998;32:215–9.
26. Vazquez JC, Villar J. Treatments for symptomatic urinary tract infections during pregnancy. Cochrane Database Syst Rev 2003:CD002256.
27. Raz R, Stamm WE. A controlled trial of intravaginal estriol in postmenopausal women with recurrent urinary tract infections. N Engl J Med 1993;329:753–756.
28. Nicolle LE, Bradley S, Colgan R, Rice JC, Schaeffer A, Hooton TM; Infectious Diseases Society of America; American Society of Nephrology; American Geriatric Society. Infectious Diseases Society of America guidelines for the diagnosis and treatment of asymptomatic bacteriuria in adults. Clin Infect Dis 2005;40:643–654.












