–Ю–Ї–Њ–ї–Њ 75% –∞–љ—В–Є–±–Є–Њ—В–Є–Ї–Њ–≤, –Ї–Њ—В–Њ—А—Л–µ –њ—А–Є–Љ–µ–љ—П—О—В—Б—П –≤ —Б—В–∞—Ж–Є–Њ–љ–∞—А–µ –і–ї—П –ї–µ—З–µ–љ–Є—П —В—П–ґ–µ–ї—Л—Е –Є–љ—Д–µ–Ї—Ж–Є–є – b––ї–∞–Ї—В–∞–Љ–љ—Л–µ –∞–љ—В–Є–±–Є–Њ—В–Є–Ї–Є. –Т –Є—Е —З–Є—Б–ї–µ –Ї–∞—А–±–∞–њ–µ–љ–µ–Љ—Л, –Њ–±–ї–∞–і–∞—О—Й–Є–µ –љ–∞–Є–±–Њ–ї–µ–µ —И–Є—А–Њ–Ї–Є–Љ —Б–њ–µ–Ї—В—А–Њ–Љ –∞–Ї—В–Є–≤–љ–Њ—Б—В–Є –Є —Б–њ–Њ—Б–Њ–±–љ–Њ—Б—В—М—О –њ—А–µ–Њ–і–Њ–ї–µ–≤–∞—В—М –∞–Ї—В—Г–∞–ї—М–љ—Л–µ –Љ–µ—Е–∞–љ–Є–Ј–Љ—Л —А–µ–Ј–Є—Б—В–µ–љ—В–љ–Њ—Б—В–Є –≤–∞–ґ–љ–µ–є—И–Є—Е –≤–Њ–Ј–±—Г–і–Є—В–µ–ї–µ–є –љ–Њ–Ј–Њ–Ї–Њ–Љ–Є–∞–ї—М–љ—Л—Е –Є–љ—Д–µ–Ї—Ж–Є–є. –Т –≥—А—Г–њ–њ—Г –Ї–∞—А–±–∞–њ–µ–љ–µ–Љ–Њ–≤ –≤ –љ–∞—Б—В–Њ—П—Й–µ–µ –≤—А–µ–Љ—П –≤—Е–Њ–і—П—В –Љ–µ—А–Њ–њ–µ–љ–µ–Љ, –Є–Љ–Є–њ–µ–љ–µ–Љ, –і–Њ—А–Є–њ–µ–љ–µ–Љ, —Н—А—В–∞–њ–µ–љ–µ–Љ, –±–Є–∞–њ–µ–љ–µ–Љ –Є –њ–∞–љ–Є–њ–µ–љ–µ–Љ (–і–≤–∞ –њ–Њ—Б–ї–µ–і–љ–Є—Е –љ–µ –њ—А–Є–Љ–µ–љ—П—О—В—Б—П –≤ –†–§). –Я—А–Є —Н—В–Њ–Љ —В–Њ–ї—М–Ї–Њ –Љ–µ—А–Њ–њ–µ–љ–µ–Љ, –Є–Љ–Є–њ–µ–љ–µ–Љ –Є –≤ –њ–µ—А—Б–њ–µ–Ї—В–Є–≤–µ –і–Њ—А–Є–њ–µ–љ–µ–Љ – —А–∞—Б—Б–Љ–∞—В—А–Є–≤–∞—О—В—Б—П –Ї–∞–Ї –њ—А–µ–њ–∞—А–∞—В—Л –і–ї—П —Н–Љ–њ–Є—А–Є—З–µ—Б–Ї–Њ–є —В–µ—А–∞–њ–Є–Є –њ–∞—Ж–Є–µ–љ—В–Њ–≤ –≤ –Ї—А–Є—В–Є—З–µ—Б–Ї–Њ–Љ —Б–Њ—Б—В–Њ—П–љ–Є–Є –Є–ї–Є –і–ї—П –ї–µ—З–µ–љ–Є—П –Є–љ—Д–µ–Ї—Ж–Є–є, –≤—Л–Ј–≤–∞–љ–љ—Л—Е –њ–Њ–ї–Є—А–µ–Ј–Є—Б—В–µ–љ—В–љ–Њ–є —Д–ї–Њ—А–Њ–є. –Э–µ—Б–Љ–Њ—В—А—П –љ–∞ –≤—Л—Б–Њ–Ї—Г—О –∞–Ї—В–Є–≤–љ–Њ—Б—В—М –≤ –Њ—В–љ–Њ—И–µ–љ–Є–Є —И–Є—А–Њ–Ї–Њ–≥–Њ —Б–њ–µ–Ї—В—А–∞ –≥—А–∞–Љ–Њ—В—А–Є—Ж–∞—В–µ–ї—М–љ–Њ–є, –≥—А–∞–Љ–њ–Њ–ї–Њ–ґ–Є—В–µ–ї—М–љ–Њ–є –Є –∞–љ–∞—Н—А–Њ–±–љ–Њ–є —Д–ї–Њ—А—Л, –Љ–µ–ґ–і—Г –љ–Є–Љ–Є –Є–Љ–µ—О—В—Б—П –Њ–њ–µ—А–µ–і–µ–ї–µ–љ–љ—Л–µ —А–∞–Ј–ї–Є—З–Є—П. –Ь–µ—А–Њ–њ–µ–љ–µ–Љ –Є –і–Њ—А–Є–њ–µ–љ–µ–Љ –±–Њ–ї–µ–µ –∞–Ї—В–Є–≤–љ—Л –≤ –Њ—В–љ–Њ—И–µ–љ–Є–Є –≥—А–∞–Љ–Њ—В—А–Є—Ж–∞—В–µ–ї—М–љ—Л—Е, –Є–Љ–Є–њ–µ–љ–µ–Љ – –≤ –Њ—В–љ–Њ—И–µ–љ–Є–Є –≥—А–∞–Љ–њ–Њ–ї–Њ–ґ–Є—В–µ–ї—М–љ—Л—Е –±–∞–Ї—В–µ—А–Є–є. –Т –Њ—В–ї–Є—З–Є–µ –Њ—В –љ–Є—Е —Н—А—В–∞–њ–µ–љ–µ–Љ –љ–µ –∞–Ї—В–Є–≤–µ–љ –≤ –Њ—В–љ–Њ—И–µ–љ–Є–Є –љ–µ—Д–µ—А–Љ–µ–љ—В–Є—А—Г—О—Й–Є—Е –±–∞–Ї—В–µ—А–Є–є (P. aerugnosa –Є –Рcinetobacter species) [4].
–Ъ–∞—А–±–∞–њ–µ–љ–µ–Љ—Л –Њ–±–ї–∞–і–∞—О—В –±–ї–Є–Ј–Ї–Є–Љ–Є —Д–∞—А–Љ–∞–Ї–Њ–Ї–Є–љ–µ—В–Є—З–µ—Б–Ї–Є–Љ–Є —Е–∞—А–∞–Ї—В–µ—А–Є—Б—В–Є–Ї–∞–Љ–Є, –Њ—Б–Њ–±–µ–љ–љ–Њ –Љ–µ—А–Њ–њ–µ–љ–µ–Љ, –Є–Љ–Є–њ–µ–љ–µ–Љ –Є –і–Њ—А–Є–њ–µ–љ–µ–Љ. –≠—А—В–∞–њ–µ–љ–µ–Љ –Њ—В–ї–Є—З–∞–µ—В—Б—П –Њ—З–µ–љ—М –≤—Л—Б–Њ–Ї–Є–Љ —Б–≤—П–Ј—Л–≤–∞–љ–Є–µ–Љ —Б –±–µ–ї–Ї–∞–Љ–Є, —З—В–Њ —Б–њ–Њ—Б–Њ–±—Б—В–≤—Г–µ—В —Г–≤–µ–ї–Є—З–µ–љ–Є—О –њ—А–Њ–і–Њ–ї–ґ–Є—В–µ–ї—М–љ–Њ—Б—В–Є –µ–≥–Њ –њ–Њ–ї—Г–≤—Л–≤–µ–і–µ–љ–Є—П –і–Њ 4 —З–∞—Б–Њ–≤ –њ–Њ —Б—А–∞–≤–љ–µ–љ–Є—О —Б 1 —З–∞—Б–Њ–Љ —Г –і—А—Г–≥–Є—Е –Ї–∞—А–±–∞–њ–µ–љ–µ–Љ–Њ–≤ [5].
–Т –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є—Е –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П—Е –њ–Њ–Ї–∞–Ј–∞–љ–Њ, —З—В–Њ –Ї–∞—А–±–∞–њ–µ–љ–µ–Љ—Л —З–∞—Б—В–Њ –њ—А–Є–Љ–µ–љ—П—О—В –≤ –Ї–∞—З–µ—Б—В–≤–µ —А–µ–Ј–µ—А–≤–∞ –≤ –Њ—В—Б—Г—В—Б—В–≤–Є–µ —Н—Д—Д–µ–Ї—В–∞ –Њ—В –і—А—Г–≥–Є—Е –њ—А–µ–њ–∞—А–∞—В–Њ–≤. –Ф–Њ–Ї–∞–Ј–∞–љ–∞ –≤–∞–ґ–љ–Њ—Б—В—М –∞–і–µ–Ї–≤–∞—В–љ–Њ–є —Б—В–∞—А—В–Њ–≤–Њ–є —В–µ—А–∞–њ–Є–Є, –Ї–Њ—В–Њ—А–∞—П —Б—Г—Й–µ—Б—В–≤–µ–љ–љ–Њ —Б–љ–Є–ґ–∞–ї–∞ –ї–µ—В–∞–ї—М–љ–Њ—Б—В—М —А–µ–∞–љ–Є–Љ–∞—Ж–Є–Њ–љ–љ—Л—Е –±–Њ–ї—М–љ—Л—Е [6]. –†–µ–Ї–Њ–Љ–µ–љ–і–∞—Ж–Є–Є –њ–Њ –±–Њ–ї–µ–µ —И–Є—А–Њ–Ї–Њ–Љ—Г –њ—А–Є–Љ–µ–љ–µ–љ–Є—О –Ї–∞—А–±–∞–њ–µ–љ–µ–Љ–Њ–≤ –Њ–±–Њ—Б–љ–Њ–≤–∞–љ—Л –љ–Є–Ј–Ї–Њ–є —А–µ–Ј–Є—Б—В–µ–љ—В–љ–Њ—Б—В—М—О –љ–Њ–Ј–Њ–Ї–Њ–Љ–Є–∞–ї—М–љ–Њ–є —Д–ї–Њ—А—Л –Є –≤—Л—Б–Њ–Ї–Њ–є –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Њ–є —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В—М—О —Н—В–Њ–є –≥—А—Г–њ–њ—Л –њ—А–µ–њ–∞—А–∞—В–Њ–≤.
–Ю–і–љ–Є–Љ –Є–Ј –≤–∞–ґ–љ–µ–є—И–Є—Е —Д–∞–Ї—В–Њ—А–Њ–≤, —Б–њ–Њ—Б–Њ–±–љ—Л—Е –њ–Њ–≤—Л—Б–Є—В—М –Є—Е —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В—М, —П–≤–ї—П–µ—В—Б—П –Њ–њ—В–Є–Љ–Є–Ј–∞—Ж–Є—П —Д–∞—А–Љ–∞–Ї–Њ–і–Є–љ–∞–Љ–Є—З–µ—Б–Ї–Є—Е –њ–∞—А–∞–Љ–µ—В—А–Њ–≤, –Ї—А–Њ–Љ–µ —В–Њ–≥–Њ, —Н—В–Є–Љ –ґ–µ —Б–њ–Њ—Б–Њ–±–Њ–Љ –Љ–Њ–ґ–µ—В –±—Л—В—М —Б–љ–Є–ґ–µ–љ–∞ –≤–µ—А–Њ—П—В–љ–Њ—Б—В—М —А–∞–Ј–≤–Є—В–Є—П —А–µ–Ј–Є—Б—В–µ–љ—В–љ–Њ—Б—В–Є –Є –Ј–∞—В—А–∞—В, —Б–≤—П–Ј–∞–љ–љ—Л—Е —Б –ї–µ—З–µ–љ–Є–µ–Љ —В—П–ґ–µ–ї—Л—Е –±–Њ–ї—М–љ—Л—Е [7]. –°–Њ—З–µ—В–∞–љ–Є–µ –Њ–њ—В–Є–Љ–∞–ї—М–љ—Л—Е —А–µ–ґ–Є–Љ–Њ–≤ –і–Њ–Ј–Є—А–Њ–≤–∞–љ–Є—П –Є –≤—Л—Б–Њ–Ї–Њ–є –∞–љ—В–Є–±–∞–Ї—В–µ—А–Є–∞–ї—М–љ–Њ–є –∞–Ї—В–Є–≤–љ–Њ—Б—В–Є –Њ–±—Г—Б–ї–Њ–≤–ї–Є–≤–∞–µ—В –њ–Њ–ї—Г—З–µ–љ–Є–µ –Љ–∞–Ї—Б–Є–Љ–∞–ї—М–љ–Њ–є —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В–Є –њ—А–Є —Б–љ–Є–ґ–µ–љ–Є–Є –Ї–Њ–ї–Є—З–µ—Б—В–≤–∞ —И—В–∞–Љ–Љ–Њ–≤ –±–∞–Ї—В–µ—А–Є–є, —Б–њ–Њ—Б–Њ–±–љ—Л—Е –≤—Л–ґ–Є–≤–∞—В—М, –њ–Њ–і–≤–µ—А–≥–∞—В—М—Б—П –Љ—Г—В–∞—Ж–Є—П–Љ –Є–ї–Є –≤—Л–Ј—Л–≤–∞—В—М —А–µ—Ж–Є–і–Є–≤—Л –Є–љ—Д–µ–Ї—Ж–Є–Є [8].
–§–∞—А–Љ–∞–Ї–Њ–і–Є–љ–∞–Љ–Є—З–µ—Б–Ї–Є–µ –њ–Њ–Ї–∞–Ј–∞—В–µ–ї–Є
–Ш–і–µ–∞–ї—М–љ–Њ–є –і–Њ–Ј–Є—А–Њ–≤–Ї–Њ–є –∞–љ—В–Є–±–Є–Њ—В–Є–Ї–∞ —П–≤–ї—П–µ—В—Б—П —В–∞, –Ї–Њ—В–Њ—А–∞—П —Б–Њ–Ј–і–∞–µ—В —Г—Б–ї–Њ–≤–Є—П –і–ї—П –≥–Є–±–µ–ї–Є –Љ–∞–Ї—Б–Є–Љ–∞–ї—М–љ–Њ–≥–Њ –Ї–Њ–ї–Є—З–µ—Б—В–≤–∞ –≤–Њ–Ј–±—Г–і–Є—В–µ–ї–µ–є –Є–љ—Д–µ–Ї—Ж–Є–Є. –Ф–Њ—Б—В–Є–ґ–µ–љ–Є–µ –Љ–∞–Ї—Б–Є–Љ–∞–ї—М–љ–Њ–є –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Њ–є –Є –Љ–Є–Ї—А–Њ–±–Є–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Њ–є —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В–Є –љ–µ –і–Њ–ї–ґ–љ–Њ —Б–Њ–њ—А–Њ–≤–Њ–ґ–і–∞—В—М—Б—П –њ–Њ—П–≤–ї–µ–љ–Є–µ–Љ –њ–Њ–±–Њ—З–љ—Л—Е —Н—Д—Д–µ–Ї—В–Њ–≤. –Ь–∞–Ї—Б–Є–Љ–∞–ї—М–љ–∞—П —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В—М –њ—А–µ–њ–∞—А–∞—В–∞ –Љ–Њ–ґ–µ—В –±—Л—В—М –і–Њ—Б—В–Є–≥–љ—Г—В–∞ —Б –њ–Њ–Љ–Њ—Й—М—О —А–∞–Ј–ї–Є—З–љ—Л—Е –і–Њ–Ј–Є—А–Њ–≤–Њ–Ї –њ—А–µ–њ–∞—А–∞—В–∞. –Ю—Б–љ–Њ–≤–љ—Л–Љ —Д–∞—А–Љ–∞–Ї–Њ–і–Є–љ–∞–Љ–Є—З–µ—Б–Ї–Є–Љ –њ–Њ–Ї–∞–Ј–∞—В–µ–ї–µ–Љ –і–ї—П b––ї–∞–Ї—В–∞–Љ–љ—Л—Е –∞–љ—В–Є–±–Є–Њ—В–Є–Ї–Њ–≤ —П–≤–ї—П–µ—В—Б—П –Њ—В–љ–Њ—И–µ–љ–Є–µ (–≤ %) –њ–µ—А–Є–Њ–і–∞ –њ—А–µ–≤—Л—И–µ–љ–Є—П —Д–∞—А–Љ–∞–Ї–Њ–Ї–Є–љ–µ—В–Є—З–µ—Б–Ї–Є–є –Ї—А–Є–≤–Њ–є –Ј–љ–∞—З–µ–љ–Є—П –Ь–Я–Ъ –і–ї—П –Ї–Њ–љ–Ї—А–µ—В–љ–Њ–≥–Њ –Љ–Є–Ї—А–Њ–Њ—А–≥–∞–љ–Є–Ј–Љ–∞ –Є –њ–µ—А–Є–Њ–і–∞ –Љ–µ–ґ–і—Г –≤–≤–µ–і–µ–љ–Є—П–Љ–Є –њ—А–µ–њ–∞—А–∞—В–∞ (%T>–Ь–Я–Ъ) [8]. –£ –њ–µ–љ–Є—Ж–Є–ї–ї–Є–љ–Њ–≤, —Ж–µ—Д–∞–ї–Њ—Б–њ–Њ—А–Є–љ–Њ–≤ –Є –Ї–∞—А–±–∞–њ–µ–љ–µ–Љ–Њ–≤ –љ–∞–±–ї—О–і–∞–µ—В—Б—П –Ї–Є–ї–ї–Є–љ–≥ –Љ–Є–Ї—А–Њ–±–Њ–≤, –Ї–Њ—В–Њ—А—Л–є –љ–∞–Ј—Л–≤–∞—О—В –Ј–∞–≤–Є—Б–Є–Љ—Л–Љ –Њ—В –≤—А–µ–Љ–µ–љ–Є [9]. –Х—Б–ї–Є —Б—Л–≤–Њ—А–Њ—В–Њ—З–љ–∞—П –Ї–Њ–љ—Ж–µ–љ—В—А–∞—Ж–Є—П –њ—А–µ–њ–∞—А–∞—В–∞ –≤ 2–4 —А–∞–Ј–∞ –њ—А–µ–≤—Л—И–∞–µ—В –Ь–Я–Ъ –і–ї—П –і–∞–љ–Њ–≥–Њ –Љ–Є–Ї—А–Њ–Њ—А–≥–∞–љ–Є–Ј–Љ–∞, –≤–∞–ґ–љ–µ–є—И–Є–Љ –њ–∞—А–∞–Љ–µ—В—А–Њ–Љ –±–∞–Ї—В–µ—А–Є–∞–ї—М–љ–Њ–≥–Њ –Ї–Є–ї–ї–Є–љ–≥–∞ —П–≤–ї—П–µ—В—Б—П –≤–µ–ї–Є—З–Є–љ–∞ %T>–Ь–Я–Ъ. –Я—А–Є –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є in vitro –Є in vivo —Г –ґ–Є–≤–Њ—В–љ—Л—Е –±—Л–ї–Њ –њ–Њ–Ї–∞–Ј–∞–љ–Њ, —З—В–Њ –і–ї—П –њ–µ–љ–Є—Ж–Є–ї–ї–Є–љ–Њ–≤ –Њ–њ—В–Є–Љ–∞–ї—М–Љ—Л–Љ —П–≤–ї—П–µ—В—Б—П —Б–Њ–Њ—В–љ–Њ—И–µ–љ–Є–µ –Њ–Ї–Њ–ї–Њ 50% T>–Ь–Я–Ъ –і–ї—П –і–Њ—Б—В–Є–ґ–µ–љ–Є—П –±–∞–Ї—В–µ—А–Є—Ж–Є–і–љ–Њ–є –Ї–Њ–љ—Ж–µ–љ—В—А–∞—Ж–Є–Є, –∞ –і–ї—П —Ж–µ—Д–∞–ї–Њ—Б–њ–Њ—А–Є–љ–Њ–≤ – 65–75% [9]. –Я—А–Є —Н–Ї—Б–њ–µ—А–Є–Љ–µ–љ—В–∞–ї—М–љ–Њ–Љ –ї–µ—З–µ–љ–Є–Є –Љ—Л—И–µ–є —Б –Є–љ—Д–µ–Ї—Ж–Є—П–Љ–Є –Љ—П–≥–Ї–Є—Е —В–Ї–∞–љ–µ–є, –≤—Л–Ј–≤–∞–љ–љ—Л–Љ–Є E. coli –Є P. aeruginosa, –і–ї—П –Ї–∞—А–±–∞–њ–µ–љ–µ–Љ–Њ–≤ —В—А–µ–±–Њ–≤–∞–ї–Њ—Б—М –і–Њ—Б—В–Є–ґ–µ–љ–Є–µ –њ–Њ–Ї–∞–Ј–∞—В–µ–ї—П 20% T>–Ь–Я–Ъ –і–ї—П –і–Њ—Б—В–Є–ґ–µ–љ–Є—П –±–∞–Ї—В–µ—А–Є–Њ—Б—В–∞—В–Є—З–µ—Б–Ї–Њ–≥–Њ –Є 40% – –і–ї—П –і–Њ—Б—В–Є–ґ–µ–љ–Є—П –±–∞–Ї—В–µ—А–Є—Ж–Є–і–љ–Њ–≥–Њ —Н—Д—Д–µ–Ї—В–∞. –Э–Є–Ј–Ї–Є–µ –Ј–љ–∞—З–µ–љ–Є—П –≤–µ–ї–Є—З–Є–љ—Л T>–Ь–Я–Ъ –і–ї—П –Ї–∞—А–±–∞–њ–µ–љ–µ–Љ–Њ–≤ –±—Л–ї–Є —Б–≤—П–Ј–∞–љ—Л —Б –љ–∞–ї–Є—З–Є–µ–Љ –њ–Њ—Б—В–∞–љ—В–Є–±–Є–Њ—В–Є—З–µ—Б–Ї–Њ–≥–Њ —Н—Д—Д–µ–Ї—В–∞ –≤ –Њ—В–љ–Њ—И–µ–љ–Є–Є –≥—А–∞–Љ–Њ—В—А–Є—Ж–∞—В–µ–ї—М–љ—Л—Е –±–∞–Ї—В–µ—А–Є–є [10]. –Я–Њ–≤—Л—И–µ–љ–Є—П —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В–Є –Љ–Њ–ґ–љ–Њ –і–Њ—Б—В–Є–≥–∞—В—М: 1) –њ—Г—В–µ–Љ —Г–≤–µ–ї–Є—З–µ–љ–Є—П –і–Њ–Ј—Л –њ—А–µ–њ–∞—А–∞—В–∞ –њ—А–Є —В–Њ–є –ґ–µ –Ї—А–∞—В–љ–Њ—Б—В–Є –≤–≤–µ–і–µ–љ–Є—П, —В.–µ. —Г–≤–µ–ї–Є—З–µ–љ–Є–µ–Љ —Б—Г—В–Њ—З–љ–Њ–є –і–Њ–Ј—Л; 2) –њ—Г—В–µ–Љ —Г–Ї–Њ—А–Њ—З–µ–љ–Є—П –Є–љ—В–µ—А–≤–∞–ї–∞ –Љ–µ–ґ–і—Г –≤–≤–µ–і–µ–љ–Є—П–Љ–Є –њ—А–µ–њ–∞—А–∞—В–∞ (–±–Њ–ї–µ–µ —З–∞—Б—В–Њ–µ –≤–≤–µ–і–µ–љ–Є–µ) –њ—А–Є –њ–Њ—Б—В–Њ—П–љ–љ–Њ–є —Б—Г—В–Њ—З–љ–Њ–є –і–Њ–Ј–µ; 3) –њ—Г—В–µ–Љ —Г–≤–µ–ї–Є—З–µ–љ–Є—П –њ—А–Њ–і–Њ–ї–ґ–Є—В–µ–ї—М–љ–Њ—Б—В–Є –≤–љ—Г—В—А–Є–≤–µ–љ–љ–Њ–є –Є–љ—Д—Г–Ј–Є–Є –њ—А–µ–њ–∞—А–∞—В–Њ–≤.
–¶–µ—Д–∞–ї–Њ—Б–њ–Њ—А–Є–љ—Л –і–ї—П –і–Њ—Б—В–Є–ґ–µ–љ–Є—П –Љ–∞–Ї—Б–Є–Љ–∞–ї—М–љ–Њ–≥–Њ –±–∞–Ї—В–µ—А–Є–∞–ї—М–љ–Њ–≥–Њ –Ї–Є–ї–ї–Є–љ–≥–∞ —В—А–µ–±—Г—О—В 65–75%T>–Ь–Я–Ъ –Є –Љ–Њ–≥—Г—В –≤–≤–Њ–і–Є—В—М—Б—П –≤ –≤–Є–і–µ –њ–Њ—Б—В–Њ—П–љ–љ–Њ–є –Є–љ—Д—Г–Ј–Є–Є. –Ф–ї—П –Ї–∞—А–±–∞–њ–µ–љ–µ–Љ–Њ–≤ –љ–µ–Њ–±—Е–Њ–і–Є–Љ–∞ –Љ–µ–љ—М—И–∞—П –≤–µ–ї–Є—З–Є–љ–∞ T>–Ь–Я–Ъ –Є –њ–Њ–≤—Л—И–µ–љ–Є–µ —Д–∞—А–Љ–∞–Ї–Њ–і–Є–љ–∞–Љ–Є—З–µ—Б–Ї–Є—Е –њ–Њ–Ї–∞–Ј–∞—В–µ–ї–µ–є –Љ–Њ–ґ–µ—В –±—Л—В—М –і–Њ—Б—В–Є–≥–љ—Г—В–Њ –њ—А–Є–Љ–µ–љ–µ–љ–Є–µ–Љ –њ—А–Њ–і–ї–µ–љ–љ–Њ–є –Є–љ—Д—Г–Ј–Є–Є (–≤ —В–µ—З–µ–љ–Є–µ 3 —З–∞—Б–Њ–≤) [7,11].
–Э–µ–Њ–±—Е–Њ–і–Є–Љ–Њ –Њ—В–Љ–µ—В–Є—В—М –њ—А–Є–љ—Ж–Є–њ–Є–∞–ї—М–љ—Г—О —Б–≤—П–Ј—М –Љ–µ–ґ–і—Г –≤—Л–±–Њ—А–Њ–Љ –і–Њ–Ј—Л –њ—А–µ–њ–∞—А–∞—В–∞ –Є –≤–µ–ї–Є—З–Є–љ–Њ–є –Ь–Я–Ъ –≤–Њ–Ј–±—Г–і–Є—В–µ–ї—П: –њ—А–Є –≤—Л—Б–Њ–Ї–Є—Е –Ь–Я–Ъ (—А–µ–Ј–Є—Б—В–µ–љ—В–љ–∞—П —Д–ї–Њ—А–∞) —В—А–µ–±—Г–µ—В—Б—П —Б–Њ—З–µ—В–∞–љ–Є–µ –Љ–∞–Ї—Б–Є–Љ–∞–ї—М–љ–Њ–є —Б—Г—В–Њ—З–љ–Њ–є –і–Њ–Ј–Є—А–Њ–≤–Ї–Є –Є –њ—А–Њ–і–Њ–ї–ґ–Є—В–µ–ї—М–љ–Њ–≥–Њ –Є–ї–Є –њ–Њ—Б—В–Њ—П–љ–љ–Њ–≥–Њ –≤–≤–µ–і–µ–љ–Є—П. –Ю–і–љ–∞–Ї–Њ –і–ї—П –ї–µ—З–µ–љ–Є—П –Є–љ—Д–µ–Ї—Ж–Є–є, –≤ —В–Њ–Љ —З–Є—Б–ї–µ –љ–Њ–Ј–Њ–Ї–Њ–Љ–Є–∞–ї—М–љ—Л—Е, –љ–Њ –≤—Л–Ј–≤–∞–љ–љ—Л—Е —Д–ї–Њ—А–Њ–є, –љ–µ –Њ–±–ї–∞–і–∞—О—Й–µ–є –≤—Л—Б–Њ–Ї–Є–Љ–Є –Ь–Я–Ъ, –Љ–Њ–≥—Г—В –њ—А–Є–Љ–µ–љ—П—В—М—Б—П –Њ–±—Л—З–љ—Л–µ –Є–ї–Є –і–∞–ґ–µ —Б–љ–Є–ґ–µ–љ–љ—Л–µ –і–Њ–Ј–Є—А–Њ–≤–Ї–Є –њ—А–µ–њ–∞—А–∞—В–Њ–≤, —Б–њ–Њ—Б–Њ–±–љ—Л–µ –Њ–±–µ—Б–њ–µ—З–Є—В—М –Є—Е –Њ–њ—В–Є–Љ–∞–ї—М–љ—Л–µ —Д–∞—А–Љ–∞–Ї–Њ–і–Є–љ–∞–Љ–Є—З–µ—Б–Ї–Є–µ –њ–∞—А–∞–Љ–µ—В—А—Л.
–Ь–µ—В–Њ–і –Љ–Њ–і–µ–ї–Є—А–Њ–≤–∞–љ–Є—П
—Д–∞—А–Љ–∞–Ї–Њ–і–Є–љ–∞–Љ–Є—З–µ—Б–Ї–Є—Е –њ–Њ–Ї–∞–Ј–∞—В–µ–ї–µ–є
–Ю–њ—А–µ–і–µ–ї–µ–љ–Є–µ —Д–∞—А–Љ–∞–Ї–Њ–і–Є–љ–∞–Љ–Є—З–µ—Б–Ї–Є—Е –њ–Њ–Ї–∞–Ј–∞—В–µ–ї–µ–є —Г –Ї–∞–ґ–і–Њ–≥–Њ –Ї–Њ–љ–Ї—А–µ—В–љ–Њ–≥–Њ –њ–∞—Ж–Є–µ–љ—В–∞ –≤–µ—Б—М–Љ–∞ –Ј–∞—В—А—Г–і–љ–Є—В–µ–ї—М–љ–Њ –Є –Њ–±—Л—З–љ–Њ –≤ —А—Г—В–Є–љ–љ–Њ–є –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Њ–є –њ—А–∞–Ї—В–Є–Ї–µ –љ–µ –њ—А–Є–Љ–µ–љ—П–µ—В—Б—П. –Ю–і–љ–Є–Љ –Є–Ј –љ–∞–Є–±–Њ–ї–µ–µ –і–Њ—Б—В–Њ–≤–µ—А–љ—Л—Е —Б–Њ–≤—А–µ–Љ–µ–љ–љ—Л—Е –Љ–µ—В–Њ–і–Њ–≤ —П–≤–ї—П–µ—В—Б—П –Љ–Њ–і–µ–ї–Є—А–Њ–≤–∞–љ–Є–µ –њ–Њ Monte Carlo, –Ї–Њ—В–Њ—А–Њ–µ –њ–Њ–Ј–≤–Њ–ї—П–µ—В —Г–љ–Є–Ї–∞–ї—М–љ—Л–Љ –Њ–±—А–∞–Ј–Њ–Љ –∞–љ–∞–ї–Є–Ј–Є—А–Њ–≤–∞—В—М –≤–µ—А–Њ—П—В–љ–Њ—Б—В—М –і–Њ—Б—В–Є–ґ–µ–љ–Є—П —Ж–µ–ї–µ–≤—Л—Е —Д–∞—А–Љ–∞–Ї–Њ–і–Є–љ–∞–Љ–Є—З–µ—Б–Ї–Є—Е –њ–Њ–Ї–∞–Ј–∞—В–µ–ї–µ–є [13–17]. –Т –Њ—В–ї–Є—З–Є–µ –Њ—В –Њ—Ж–µ–љ–Ї–Є —Б—А–µ–і–љ–Є—Е –≤–µ–ї–Є—З–Є–љ –і–Њ–Ј, –њ—А–Є –Ї–Њ—В–Њ—А—Л—Е –і–Њ—Б—В–Є–≥–∞–µ—В—Б—П –Є–ї–Є –љ–µ –і–Њ—Б—В–Є–≥–∞–µ—В—Б—П –Ј–∞–і–∞–љ–љ—Л–є –њ–Њ–Ї–∞–Ј–∞—В–µ–ї—М T>–Ь–Я–Ъ, —Н—В–Њ—В –Љ–µ—В–Њ–і —Г—З–Є—В—Л–≤–∞–µ—В —Д–∞–Ї—В–Њ—А—Л –≤–∞—А–Є–∞–±–µ–ї—М–љ–Њ—Б—В–Є –Њ—Ж–µ–љ–Ї–Є —Д–∞—А–Љ–∞–Ї–Њ–Ї–Є–љ–µ—В–Є—З–µ—Б–Ї–Є—Е –њ–∞—А–∞–Љ–µ—В—А–Њ–≤, —А–µ–ґ–Є–Љ–Њ–≤ –і–Њ–Ј–Є—А–Њ–≤–∞–љ–Є—П –Є —А–∞—Б–њ—А–µ–і–µ–ї–µ–љ–Є—П –Ь–Я–Ъ –њ—А–Є —А–∞—Б—З–µ—В–µ –≤–µ—А–Њ—П—В–љ–Њ—Б—В–Є –і–Њ—Б—В–Є–ґ–µ–љ–Є—П —Б–Њ—В–≤–µ—В—Б—В–≤—Г—О—Й–µ–є —Д–∞—А–Љ–∞–Ї–Њ–і–Є–љ–∞–Љ–Є—З–µ—Б–Ї–Њ–є –Ј–∞–і–∞—З–Є. –Э–∞–њ—А–Є–Љ–µ—А, –і–Њ—Б—В–Є–ґ–µ–љ–Є–µ –њ–Њ–Ї–∞–Ј–∞—В–µ–ї—П –Ї–∞—А–±–∞–њ–µ–љ–µ–Љ–Њ–≤ –≤—Л—И–µ 40%T>–Ь–Я–Ъ –Ї–Њ—А—А–µ–ї–Є—А—Г–µ—В —Б –Љ–∞–Ї—Б–Є–Љ–∞–ї—М–љ—Л–Љ –±–∞–Ї—В–µ—А–Є–∞–ї—М–љ—Л–Љ –Ї–Є–ї–ї–Є–љ–≥–Њ–Љ. –Ь–Њ–і–µ–ї–Є—А–Њ–≤–∞–љ–Є–µ –њ–Њ Monte Carlo –њ–Њ–Ј–≤–Њ–ї—П–µ—В –≤—Л–±—А–∞—В—М –љ–∞–Є–±–Њ–ї–µ–µ –≤–∞–ґ–љ—Л–є –≤–Є–і –њ–µ—А–µ–Љ–µ–љ–љ–Њ–є (–љ–∞–њ—А–Є–Љ–µ—А, —Д–∞—А–Љ–∞–Ї–Њ–Ї–Є–љ–µ—В–Є–Ї—Г –Є –Ь–Я–Ъ) –і–ї—П –Є–Ј—Г—З–µ–љ–Є—П –Ј–∞–≤–Є—Б–Є–Љ–Њ—Б—В–Є –і–Њ–Ј—Л –њ—А–µ–њ–∞—А–∞—В–∞ –Є –Љ–∞–Ї—Б–Є–Љ–∞–ї—М–љ–Њ–≥–Њ –Ї–Є–ї–ї–Є–љ–≥–∞ –±–∞–Ї—В–µ—А–Є–є –Є–ї–Є –і—А—Г–≥–Є—Е –Ї–Њ–љ–µ—З–љ—Л—Е —А–µ–Ј—Г–ї—М—В–∞—В–Њ–≤, –љ–∞–њ—А–Є–Љ–µ—А, –њ—А–Њ—Д–Є–ї–∞–Ї—В–Є–Ї–Є –≤–Њ–Ј–љ–Є–Ї–љ–Њ–≤–µ–љ–Є—П —А–µ–Ј–Є—Б—В–µ–љ—В–љ–Њ—Б—В–Є [9,13–17]. –§–∞—А–Љ–∞–Ї–Њ–Ї–Є–љ–µ—В–Є—З–µ—Б–Ї–Є–µ –і–∞–љ–љ—Л–µ, –љ–µ–Њ–±—Е–Њ–і–Є–Љ—Л–µ –і–ї—П –Љ–µ—В–Њ–і–∞ –Љ–Њ–і–µ–ї–Є—А–Њ–≤–∞–љ–Є—П Monte Carlo, –Љ–Њ–≥—Г—В –±—Л—В—М –њ–Њ–ї—Г—З–µ–љ—Л —Г –Ї–Њ–љ–Ї—А–µ—В–љ—Л—Е –њ–∞—Ж–Є–µ–љ—В–Њ–≤ –Є–ї–Є –Є–Ј —А–µ–Ј—Г–ї—М—В–∞—В–Њ–≤ –Њ–њ—Г–±–ї–Є–Ї–Њ–≤–∞–љ—Л—Е —Д–∞—А–Љ–∞–Ї–Њ–Ї–Є–љ–µ—В–Є—З–µ—Б–Ї–Є—Е –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–є —Г –±–Њ–ї—М–љ—Л—Е –Є–ї–Є –Ј–і–Њ—А–Њ–≤—Л—Е –ї–Є—Ж. –С–Њ–ї—М—И–Є–љ—Б—В–≤–Њ –і–∞–љ–љ—Л—Е –±—Л–ї–Є –њ–Њ–ї—Г—З–µ–љ—Л –≤ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П—Е –љ–∞ –і–Њ–±—А–Њ–≤–Њ–ї—М—Ж–∞—Е, –Ї–Њ—В–Њ—А—Л–µ, –њ–Њ––≤–Є–і–Є–Љ–Њ–Љ—Г, –Њ—В–ї–Є—З–∞—О—В—Б—П —Г–Ј–Ї–Є–Љ —Б–њ–µ–Ї—В—А–Њ–Љ –Ї–Њ–ї–µ–±–∞–љ–Є–є —Д–∞—А–Љ–∞–Ї–Њ–і–Є–љ–∞–Љ–Є—З–µ—Б–Ї–Є—Е –≤–µ–ї–Є—З–Є–љ –Є–Ј––Ј–∞ –љ–Њ—А–Љ–∞–ї—М–љ–Њ–є —Д—Г–љ–Ї—Ж–Є–Є –њ–Њ—З–µ–Ї –Є –±—Л—Б—В—А–Њ–≥–Њ –≤—Л–≤–µ–і–µ–љ–Є—П –Ї–∞—А–±–∞–њ–µ–љ–µ–Љ–Њ–≤. –§–∞—А–Љ–∞–Ї–Њ–і–Є–љ–∞–Љ–Є—З–µ—Б–Ї–Є–µ –њ–∞—А–∞–Љ–µ—В—А—Л –њ–∞—Ж–Є–µ–љ—В–Њ–≤ –Љ–Њ–≥—Г—В —Б—Г—Й–µ—Б—В–≤–µ–љ–љ–Њ –Њ—В–ї–Є—З–∞—В—М—Б—П –Њ—В –Ј–і–Њ—А–Њ–≤—Л—Е –ї–Є—Ж. –Ю—Б–љ–Њ–≤–љ—Л–Љ–Є –њ–∞—А–∞–Љ–µ—В—А–∞–Љ–Є, –≤–ї–Є—П—О—Й–Є–Љ–Є –љ–∞ —А–µ–Ј—Г–ї—М—В–∞—В—Л, —П–≤–ї—П—О—В—Б—П –Ї–ї–Є—А–µ–љ—Б –Є –Њ–±—К–µ–Љ —А–∞—Б–њ—А–µ–і–µ–ї–µ–љ–Є—П. –£ –њ–∞—Ж–Є–µ–љ—В–Њ–≤ –≤ –Ї—А–Є—В–Є—З–µ—Б–Ї–Њ–Љ —Б–Њ—Б—В–Њ—П–љ–Є—П–Є –Њ–±—К–µ–Љ —А–∞—Б–њ—А–µ–і–µ–ї–µ–љ–Є—П —З–∞—Б—В–Њ –Њ–Ї–∞–Ј—Л–≤–∞–µ—В—Б—П —Б—Г—Й–µ—Б—В–≤–µ–љ–љ–Њ –≤—Л—И–µ, —З–µ–Љ —Г –Ј–і–Њ—А–Њ–≤—Л—Е –ї–Є—Ж, –∞ –Ї–ї–Є—А–µ–љ—Б –Љ–Њ–ґ–µ—В –±—Л—В—М —Б–љ–Є–ґ–µ–љ. –Я–Њ—Н—В–Њ–Љ—Г –і–ї—П –њ—А–µ–њ–∞—А–∞—В–Њ–≤, –Ї–Њ—В–Њ—А—Л–µ –Є–Љ–µ—О—В –Ј–∞–≤–Є—Б–Є–Љ—Л–є –Њ—В –≤—А–µ–Љ–µ–љ–Є –Ї–Є–ї–ї–Є–љ–≥, —Н—В–Є –Є–Ј–Љ–µ–љ–µ–љ–Є—П –Љ–Њ–≥—Г—В –Ї–Њ–Љ–њ–µ–љ—Б–Є—А–Њ–≤–∞—В—М –і—А—Г–≥ –і—А—Г–≥–∞ –Є —А–µ–Ј—Г–ї—М—В–Є—А—Г—О—Й–Є–µ —Д–∞—А–Љ–∞–Ї–Њ–і–Є–љ–∞–Љ–Є—З–µ—Б–Ї–Є–µ –њ–Њ–Ї–∞–Ј–∞—В–µ–ї–Є —З–∞—Б—В–Њ –љ–µ–Ј–љ–∞—З–Є—В–µ–ї—М–љ–Њ –Њ—В–ї–Є—З–∞—О—В—Б—П –Њ—В –њ–Њ–Ї–∞–Ј–∞—В–µ–ї–µ–є –Ј–і–Њ—А–Њ–≤—Л—Е –ї–Є—Ж [18]. –Ф–∞–љ–љ—Л–µ –Ь–Я–Ъ –Љ–Њ–≥—Г—В –±—Л—В—М –њ–Њ–ї—Г—З–µ–љ—Л –≤ –ї—О–±–Њ–є –њ–Њ–њ—Г–ї—П—Ж–Є–Є –±–∞–Ї—В–µ—А–Є–є, –≤—Л–і–µ–ї–µ–љ–љ—Л—Е –Њ—В –њ–∞—Ж–Є–µ–љ—В–Њ–≤ –њ—А–Њ—Д–Є–ї—М–љ—Л—Е –Њ—В–і–µ–ї–µ–љ–Є–є –Є–ї–Є –њ–∞—Ж–Є–µ–љ—В–Њ–≤ –Ю–†–Ш–Ґ.
–Ф–Њ–Ј–Є—А–Њ–≤–Ї–∞ –њ—А–µ–њ–∞—А–∞—В–∞
–Т –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Њ–є –њ—А–∞–Ї—В–Є–Ї–µ –њ—А–Є–Љ–µ–љ—П—О—В —А–∞–Ј–ї–Є—З–љ—Л–µ –і–Њ–Ј—Л –њ—А–µ–њ–∞—А–∞—В–Њ–≤, –Ї–Њ—В–Њ—А—Л–µ –Љ–Њ–≥—Г—В –±—Л—В—М —Б—Г—Й–µ—Б—В–≤–µ–љ–љ–Њ –Њ–њ—В–Є–Љ–Є–Ј–Є—А–Њ–≤–∞–љ—Л [3,12]. –≠—В–Њ –і–Њ—Б—В–Є–≥–∞–µ—В—Б—П —Б–ї–µ–і—Г—О—Й–Є–Љ–Є –Љ–µ—В–Њ–і–∞–Љ–Є: —Г–≤–µ–ї–Є—З–µ–љ–Є–µ–Љ –і–Њ–Ј—Л, —Г–≤–µ–ї–Є—З–µ–љ–Є–µ–Љ —З–∞—Б—В–Њ—В—Л –≤–≤–µ–і–µ–љ–Є—П –њ—А–µ–њ–∞—А–∞—В–∞ (–њ–µ—А–µ—Е–Њ–і —Б 8 —З–∞—Б–Њ–≤–Њ–≥–Њ –љ–∞ 6 —З–∞—Б–Њ–≤–Њ–є –Є–љ—В–µ—А–≤–∞–ї –і–Њ–Ј–Є—А–Њ–≤–∞–љ–Є—П) –Є —Г–≤–µ–ї–Є—З–µ–љ–Є–µ–Љ –њ—А–Њ–і–Њ–ї–ґ–Є—В–µ–ї—М–љ–Њ—Б—В–Є –Є–љ—Д—Г–Ј–Є–Є –Є–ї–Є –Ї–Њ–Љ–±–Є–љ–∞—Ж–Є–Є —Н—В–Є—Е –Љ–µ—В–Њ–і–Њ–≤. –Э–µ–і–∞–≤–љ–Њ –±—Л–ї–Є –њ—А–Њ–≤–µ–і–µ–љ—Л —Д–∞—А–Љ–∞–Ї–Њ–Ї–Є–љ–µ—В–Є—З–µ—Б–Ї–Є–µ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П –љ–∞ –і–Њ–±—А–Њ–≤–Њ–ї—М—Ж–∞—Е, —А–µ–Ј—Г–ї—М—В–∞—В—Л –Ї–Њ—В–Њ—А—Л—Е –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ—Л –і–ї—П –Љ–Њ–і–µ–ї–Є—А–Њ–≤–∞–љ–Є—П Monte Carlo, –њ–Њ–і—В–≤–µ—А–і–Є–≤—И–µ–≥–Њ —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В—М —Н—В–Њ–≥–Њ –Љ–µ—В–Њ–і–∞ –і–ї—П –Њ–њ—В–Є–Љ–Є–Ј–∞—Ж–Є–Є —Д–∞—А–Љ–∞–Ї–Њ–і–Є–љ–∞–Љ–Є—З–µ—Б–Ї–Њ–≥–Њ –њ—А–Њ—Д–Є–ї—П –њ—А–µ–њ–∞—А–∞—В–∞. –Э–µ–Њ–±—Е–Њ–і–Є–Љ–Њ –Њ—В–Љ–µ—В–Є—В—М, —З—В–Њ –њ–Њ–і–∞–≤–ї—П—О—Й–µ–µ –Ї–Њ–ї–Є—З–µ—Б—В–≤–Њ —Д–∞—А–Љ–∞–Ї–Њ–і–Є–љ–∞–Љ–Є—З–µ—Б–Ї–Є—Е –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–є –∞–љ—В–Є–±–Є–Њ—В–Є–Ї–Њ–≤ –≤ –љ–∞—Б—В–Њ—П—Й–µ–µ –≤—А–µ–Љ—П –њ—А–Њ–≤–µ–і–µ–љ–Њ —Б —Ж–µ–ї—М—О –Њ–њ—В–Є–Љ–Є–Ј–∞—Ж–Є–Є –њ—А–Є–Љ–µ–љ–µ–љ–Є—П –Љ–µ—А–Њ–њ–µ–љ–µ–Љ–∞.
–Э–∞–Є–±–Њ–ї–µ–µ –њ—А–Њ—Б—В—Л–Љ –Љ–µ—В–Њ–і–Њ–Љ –Њ–њ—В–Є–Љ–Є–Ј–∞—Ж–Є–Є —Д–∞—А–Љ–∞–Ї–Њ–і–Є–љ–∞–Љ–Є–Ї–Є –Љ–µ—А–Њ–њ–µ–љ–µ–Љ–∞ —П–≤–ї—П–µ—В—Б—П —Г–≤–µ–ї–Є—З–µ–љ–Є–µ –і–Њ–Ј—Л –Є–ї–Є —З–∞—Б—В–Њ—В—Л –≤–≤–µ–і–µ–љ–Є—П. –Я—А–Є —Б—А–∞–≤–љ–µ–љ–Є–Є –і–Њ–Ј—Л –Љ–µ—А–Њ–њ–µ–љ–µ–Љ–∞ 0,5 –≥ —З–µ—А–µ–Ј 6 —З–∞—Б–Њ–≤ –Є 1 –≥ —З–µ—А–µ–Ј 8 —З–∞—Б–Њ–≤ –±—Л–ї–Њ –њ–Њ–Ї–∞–Ј–∞–љ–Њ, —З—В–Њ –±–Њ–ї–µ–µ –љ–Є–Ј–Ї–∞—П —А–∞–Ј–Њ–≤–∞—П –і–Њ–Ј–∞ –њ—А–µ–њ–∞—А–∞—В–∞, –Ї–Њ—В–Њ—А–∞—П –≤–≤–Њ–і–Є–ї–∞—Б—М –±–Њ–ї–µ–µ —З–∞—Б—В–Њ, –Є–Љ–µ–ї–∞ —В–∞–Ї—Г—О –ґ–µ —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В—М, –Ї–∞–Ї —Б—В–∞–љ–і–∞—А—В–љ–∞—П, –Є –њ—А–Є–≤–Њ–і–Є–ї–∞ –Ї —Б–љ–Є–ґ–µ–љ–Є—О –Ј–∞—В—А–∞—В [19]. –Я—А–Є –Ь–Я–Ъ 4 –Љ–≥/–ї (–Љ–∞–Ї—Б–Є–Љ–∞–ї—М–љ–∞—П –Ї–Њ–љ—Ж–µ–љ—В—А–∞—Ж–Є—П –Љ–µ—А–Њ–њ–µ–љ–µ–Љ–∞, –њ—А–Є –Ї–Њ—В–Њ—А–Њ–є –Љ–Є–Ї—А–Њ–Њ—А–≥–∞–љ–Є–Ј–Љ —А–∞—Б—Б–Љ–∞—В—А–Є–≤–∞–µ—В—Б—П –Ї–∞–Ї —З—Г–≤—Б—В–≤–Є—В–µ–ї—М–љ—Л–є) –±—Л–ї–Њ –Њ–±–љ–∞—А—Г–ґ–µ–љ–Њ, —З—В–Њ –≤–µ–ї–Є—З–Є–љ–∞ T>–Ь–Я–Ъ –і–ї—П –Њ–±–Њ–Є—Е —А–µ–ґ–Є–Љ–Њ–≤ –±—Л–ї–∞ —А–∞–≤–љ–Њ–є 42% (0,5 –≥ —З–µ—А–µ–Ј 6 —З–∞—Б–Њ–≤) –Є 46% (1 –≥ —З–µ—А–µ–Ј 8 —З–∞—Б–Њ–≤). –≠—В–Є –і–∞–љ—Л–µ —Г–Ї–∞–Ј–∞–ї–Є –љ–∞ —В–Њ, —З—В–Њ –±–ї–Є–Ј–Ї–Є–µ –≤–µ–ї–Є—З–Є–љ—Л T>–Ь–Я–Ъ –Љ–Њ–≥—Г—В –±—Л—В—М –і–Њ—Б—В–Є–≥–љ—Г—В—Л —Б –њ–Њ–Љ–Њ—Й—М—О —А–∞–Ј–љ—Л—Е —А–µ–ґ–Є–Љ–Њ–≤, –љ–Њ –њ—А–Є–Љ–µ–љ–µ–љ–Є–µ –љ–Є–Ј–Ї–Њ–є –і–Њ–Ј—Л —Б –±–Њ–ї–µ–µ —З–∞—Б—В—Л–Љ –≤–≤–µ–і–µ–љ–Є–µ–Љ –њ—А–Є–≤–Њ–і–Є–ї–Њ –Ї —Г–Љ–µ–љ—М—И–µ–љ–Є—О –њ–Њ—В—А–µ–±–ї–µ–љ–Є—П –∞–љ—В–Є–±–Є–Њ—В–Є–Ї–Њ–≤ –Є —Б–љ–Є–Ј–Є–ї–Њ –Ј–∞—В—А–∞—В—Л –љ–∞ $38 –≤ —Б—Г—В–Ї–Є –љ–∞ –≥–Њ—Б–њ–Є—В–∞–ї–Є–Ј–Є—А–Њ–≤–∞–љ–љ–Њ–≥–Њ –њ–∞—Ж–Є–µ–љ—В–∞ (—Ж–µ–љ—Л 2001 –≥–Њ–і–∞). –Ф–Њ–Ј—Л –≤ 1 –≥ —З–µ—А–µ–Ј 6 —З–∞—Б–Њ–≤ –Є 2 –≥ —З–µ—А–µ–Ј 8 —З–∞—Б–Њ–≤ —В–∞–Ї–ґ–µ –Њ–±–ї–∞–і–∞–ї–Є –±–ї–Є–Ј–Ї–Є–Љ–Є –њ–Њ–Ї–∞–Ј–∞—В–µ–ї—П–Љ–Є T> –Ь–Я–Ъ: 61 –Є 58%.
–Я—А–Њ–≤–µ–і–µ–љ —А–µ—В—А–Њ—Б–њ–µ–Ї—В–Є–≤–љ—Л–є –∞–љ–∞–ї–Є–Ј –њ—А–Є–Љ–µ–љ–µ–љ–Є—П –Љ–µ—А–Њ–њ–µ–љ–µ–Љ–∞ –≤ –і–Њ–Ј–µ 0,5 –≥ —З–µ—А–µ–Ј 6 —З–∞—Б–Њ–≤ –Є 1 –≥ —З–µ—А–µ–Ј 8 —З–∞—Б–Њ–≤ [20]. –Ю–±–µ –≥—А—Г–њ–њ—Л –љ–µ —А–∞–Ј–ї–Є—З–∞–ї–Є—Б—М –њ–Њ –і–µ–Љ–Њ–≥—А–∞—Д–Є—З–µ—Б–Ї–Є–Љ –њ–Њ–Ї–∞–Ј–∞—В–µ–ї—П–Љ, –Њ–±–ї–∞—Б—В–Є –Є–љ—Д–µ–Ї—Ж–Є–Є, –њ—А–Њ–і–Њ–ї–ґ–Є—В–µ–ї—М–љ–Њ—Б—В–Є –≥–Њ–њ–Є—В–∞–ї–Є–Ј–∞—Ж–Є–Є –Є —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В–Є –і–≤—Г—Е —А–µ–ґ–Є–Љ–Њ–≤ –і–Њ–Ј–Є—А–Њ–≤–∞–љ–Є—П. –Э–µ—Б–Љ–Њ—В—А—П –љ–∞ –Њ–≥—А–∞–љ–Є—З–µ–љ–љ–Њ–µ —З–Є—Б–ї–Њ –њ–∞—Ж–Є–µ–љ—В–Њ–≤, –Ї–ї–Є–љ–Є—З–µ—Б–Ї–∞—П —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В—М –љ–Є–Ј–Ї–Њ–є –і–Њ–Ј—Л —Б–Њ—Б—В–∞–≤–Є–ї–∞ 78%, –∞ –≤—Л—Б–Њ–Ї–Њ–є – 82% (—Б—В–∞—В–Є—Б—В–Є—З–µ—Б–Ї–Є–µ —А–∞–Ј–ї–Є—З–Є—П –љ–µ–і–Њ—Б—В–Њ–≤–µ—А–љ—Л). –Я—А–Є –њ—А–Є–Љ–µ–љ–µ–љ–Є–Є —А–∞–Ј–Њ–≤–Њ–є –і–Њ–Ј—Л 1 –≥ –Є 0,5 –≥ –Ї—Г—А—Б–Њ–≤–∞—П –і–Њ–Ј–∞ –Њ–Ї–∞–Ј–∞–ї–∞—Б—М 18 –Є 13 –≥ (—А=0,012). –≠—В–Њ –њ—А–Є–≤–µ–ї–Њ –Ї —Б–љ–Є–ґ–µ–љ–Є—О –Љ–µ–і–Є–∞–љ—Л –Ј–∞—В—А–∞—В, —Б–≤—П–Ј–∞–љ–љ—Л—Е —Б –њ–Њ—В—А–µ–±–ї–µ–љ–Є–µ–Љ –њ—А–µ–њ–∞—А–∞—В–∞ –љ–∞ –њ–∞—Ж–Є–µ–љ—В–∞ —Б $982 –і–Њ 576 (p=0,009) (–≤ —Ж–µ–љ–∞—Е 2002 –≥–Њ–і–∞). –†–µ–∞–ї—М–љ–Њ–µ —Б–љ–Є–ґ–µ–љ–Є–µ –Ј–∞—В—А–∞—В –љ–∞ –њ–∞—Ж–Є–µ–љ—В–∞ –≤ 2002 –≥–Њ–і—Г —Б–Њ—Б—В–∞–≤–Є–ї–Њ $49 –Є –±—Л–ї–Њ —Б–Њ–њ–Њ—Б—В–∞–≤–Є–Љ–Њ —Б —А–µ–Ј—Г–ї—М—В–∞—В–Њ–Љ, –њ–Њ–ї—Г—З–µ–љ–љ—Л–Љ –њ—А–Є –Љ–Њ–і–µ–ї–Є—А–Њ–≤–∞–љ–Є–Є. –°—А–µ–і–љ—П—П –њ—А–Њ–і–Њ–ї–ґ–Є—В–µ–ї—М–љ–Њ—Б—В—М —Б—В–∞—Ж–Є–Њ–љ–∞—А–љ–Њ–≥–Њ –ї–µ—З–µ–љ–Є—П (8 —Б—Г—В–Њ–Ї) –±—Л–ї–∞ –Њ–і–Є–љ–∞–Ї–Њ–≤–Њ–є –њ—А–Є –њ—А–Є–Љ–µ–љ–µ–љ–Є–Є –Њ–±–Њ–Є—Е —А–µ–ґ–Є–Љ–Њ–≤. –Э–µ—Б–Љ–Њ—В—А—П –љ–∞ –≤–Ї–ї—О—З–µ–љ–Є–µ –≤ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ –љ–µ–±–Њ–ї—М—И–Њ–≥–Њ —З–Є—Б–ї–∞ –њ–∞—Ж–Є–µ–љ—В–Њ–≤, –±—Л–ї–Є –њ–Њ–ї—Г—З–µ–љ—Л –і–Њ–Ї–∞–Ј–∞—В–µ–ї—М—Б—В–≤–∞ –њ—А–µ–Є–Љ—Г—Й–µ—Б—В–≤–∞ —А–µ–ґ–Є–Љ–∞ 0,5 –≥ —З–µ—А–µ–Ј 6 —З–∞—Б–Њ–≤ –њ–µ—А–µ–і 1 –≥ —З–µ—А–µ–Ј 8 —З–∞—Б–Њ–≤, –њ—А–Є—З–µ–Љ –≤–µ–ї–Є—З–Є–љ–∞ T>–Ь–Я–Ъ –њ—А–µ–і—Б–Ї–∞–Ј—Л–≤–∞–ї–∞ —Н–Ї–≤–Є–≤–∞–ї–µ–љ—В–љ–Њ—Б—В—М —Н—В–Є—Е —А–µ–ґ–Є–Љ–Њ–≤.
–Я–Њ–≤—Л—И–µ–љ–Є–µ —Д–∞—А–Љ–∞–Ї–Њ–і–Є–љ–∞–Љ–Є—З–µ—Б–Ї–Є—Е –њ–Њ–Ї–∞–Ј–∞—В–µ–ї–µ–є —Б –њ–Њ–Љ–Њ—Й—М—О
–њ—А–Њ–і–Њ–ї–ґ–Є—В–µ–ї—М–љ–Њ–є –Є–љ—Д—Г–Ј–Є–Є –њ—А–µ–њ–∞—А–∞—В–∞
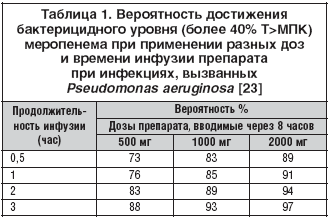
–Ф—А—Г–≥–Є–Љ –Љ–µ—В–Њ–і–Њ–Љ –Њ–њ—В–Є–Љ–Є–Ј–∞—Ж–Є–Є —Д–∞—А–Љ–∞–Ї–Њ–і–Є–љ–∞–Љ–Є–Ї–Є —П–≤–ї—П–µ—В—Б—П —Г–і–ї–Є–љ–µ–љ–Є–µ –≤—А–µ–Љ–µ–љ–Є –Є–љ—Д—Г–Ј–Є–Є –њ—А–µ–њ–∞—А–∞—В–∞. –Я—А–Є —Г–≤–µ–ї–Є—З–µ–љ–Є–Є –њ–µ—А–Є–Њ–і–∞ –Є–љ—Д—Г–Ј–Є–Є –Љ–µ—А–Њ–њ–µ–љ–µ–Љ–∞ —Б 30 –Љ–Є–љ. –і–Њ 3 —З –њ—А–Њ–Є—Б—Е–Њ–і–Є—В —Г–≤–µ–ї–Є—З–µ–љ–Є–µ –њ–Њ–Ї–∞–Ј–∞—В–µ–ї—П T>–Ь–Я–Ъ [21]. –Ф–Њ–Ј—Л 0,5 –≥ –Є 2 –≥ —З–µ—А–µ–Ј 8 —З–∞—Б–Њ–≤ –њ—А–Є–Љ–µ–љ—П–ї–Є—Б—М –≤ –≤–Є–і–µ 30––Љ–Є–љ—Г—В–љ–Њ–є –Є 3–—З–∞—Б–Њ–≤–Њ–є –Є–љ—Д—Г–Ј–Є–Є. –Я—А–Є –Ь–Я–Ъ –Љ–Є–Ї—А–Њ–±–∞ 4 –Љ–≥/–ї 30––Љ–Є–љ—Г—В–љ–∞—П –Є–љ—Д—Г–Ј–Є—П 0,5 –≥ –њ—А–µ–њ–∞—А–∞—В–∞ –і–Њ—Б—В–Є–≥–∞–ї—Б—П 30% T>–Ь–Я–Ъ, –∞ –њ—А–Є –≤–≤–µ–і–µ–љ–Є–Є 2 –≥ – 58% T>–Ь–Я–Ъ. –Я—А–Є —Г–≤–µ–ї–Є—З–µ–љ–Є–Є –≤—А–µ–Љ–µ–љ–Є –Є–љ—Д—Г–Ј–Є–Є –і–Њ 3 —З–∞—Б–Њ–≤ T>–Ь–Я–Ъ —Г–≤–µ–ї–Є—З–Є–ї—Б—П —Б–Њ–Њ—В–≤–µ—В—Б—В–≤–µ–љ–љ–Њ –і–Њ 43 –Є 73%. –Я—А–Є –Ь–Я–Ъ 16 –Љ–≥/–ї –њ–Њ–Ї–∞–Ј–∞—В–µ–ї—М T>–Ь–Я–Ъ –њ—А–Є 30––Љ–Є–љ—Г—В–љ–Њ–є –Є 3–—З–∞—Б–Њ–≤–Њ–є –Є–љ—Д–µ–Ї—Ж–Є–Є —Б–Њ—Б—В–∞–≤–Є–ї 32 –Є 48%. –Ґ–∞–Ї–Є–Љ –Њ–±—А–∞–Ј–Њ–Љ, –њ—А–Є 3–—З–∞—Б–Њ–≤–Њ–є –Є–љ—Д—Г–Ј–Є–Є –і–Њ—Б—В–Є–≥–∞–ї—Б—П –±–∞–Ї—В–µ—А–Є—Ж–Є–і–љ—Л–є —Н—Д—Д–µ–Ї—В –≤ –Њ—В–љ–Њ—И–µ–љ–Є–Є —А–µ–Ј–Є—Б—В–µ–љ—В–љ—Л—Е –Ї –Љ–µ—А–Њ–њ–µ–љ–µ–Љ—Г –≤–Њ–Ј–±—Г–і–Є—В–µ–ї–µ–є. –Т –і—А—Г–≥–Њ–Љ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є –Љ–µ—А–Њ–њ–µ–љ–µ–Љ–∞ (0,5 –Љ–≥ –≤ –≤–Є–і–µ 3–—З–∞—Б–Њ–≤–Њ–є –Є–љ—Д—Г–Ј–Є–Є) –±—Л–ї–Њ –њ–Њ–Ї–∞–Ј–∞–љ–Њ, —З—В–Њ –њ—А–Є –Ь–Я–Ъ 4 –Љ–≥/–ї –Є 1 –Љ–≥/–ї –њ–Њ–Ї–∞–Ј–∞—В–µ–ї—М T>–Ь–Я–Ъ —Б–Њ—Б—В–∞–≤–Є–ї 47 –Є 71 % —Б–Њ–Њ—В–≤–µ—В—Б—В–≤–µ–љ–љ–Њ (—А<0,05) [22]. –Я—А–Є –Љ–Њ–і–µ–ї–Є—А–Њ–≤–∞–љ–Є–Є –≤–≤–µ–і–µ–љ–Є—П –Љ–µ—А–Њ–њ–µ–љ–µ–Љ–∞ –≤ –і–Њ–Ј–µ 0,5, 1 –Є 2 –≥ —Б —А–∞–Ј–ї–Є—З–љ—Л–Љ –≤—А–µ–Љ–µ–љ–µ–Љ –Є–љ—Д—Г–Ј–Є–Є (0,5, 1, 2 –Є 3 —З–∞—Б–∞) –±—Л–ї–∞ –Є–Ј—Г—З–µ–љ–∞ –≤–µ—А–Њ—П—В–љ–Њ—Б—В—М –і–Њ—Б—В–Є–ґ–µ–љ–Є—П –њ–Њ–Ї–∞–Ј–∞—В–µ–ї—П 40% T>–Ь–Я–Ъ –≤ –Њ—В–љ–Њ—И–µ–љ–Є–Є P. aeruginosa (—В–∞–±–ї. 1). –†–µ–Ј—Г–ї—М—В–∞—В—Л –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П —Б–≤–Є–і–µ—В–µ–ї—М—Б—В–≤—Г—О—В, —З—В–Њ –≤–µ—А–Њ—П—В–љ–Њ—Б—В—М –і–Њ—Б—В–Є–ґ–µ–љ–Є—П –Ј–∞–і–∞–љ–љ–Њ–є –Ї–Њ–љ—Ж–µ–љ—В—А–∞—Ж–Є–Є –≤–Њ–Ј—А–∞—Б—В–∞–ї–∞ –њ—А–Њ–њ–Њ—А—Ж–Є–Њ–љ–∞–ї—М–љ–Њ —Г–≤–µ–ї–Є—З–µ–љ–Є—О –њ—А–Њ–і–Њ–ї–ґ–Є—В–µ–ї—М–љ–Њ—Б—В–Є –Є–љ—Д—Г–Ј–Є–Є. –Э–∞–±–Њ–ї–µ–µ –≤—Л—Б–Њ–Ї–Є–µ –њ–Њ–Ї–∞–Ј–∞—В–µ–ї–Є –±—Л–ї–Є –і–Њ—Б—В–Є–≥–љ—Г—В—Л –њ—А–Є –≤–≤–µ–і–µ–љ–Є–Є 2 –≥ –≤ —В–µ—З–µ–љ–Є–µ 3 —З–∞—Б–Њ–≤. –Т –Њ—В–љ–Њ—И–µ–љ–Є–Є P. aeruginosa —Б –Ь–Я–Ъ 0,25–64 –Љ–≥/–ї –≤–µ—А–Њ—П—В–љ–Њ—Б—В—М —Н–ї–Є–Љ–Є–љ–∞—Ж–Є–Є –≤–Њ–Ј–±—Г–і–Є—В–µ–ї—П –±—Л–ї–∞ –љ–∞–Є–≤—Л—Б—И–µ–є –њ—А–Є –њ—А–Є–Љ–µ–љ–µ–љ–Є–Є –Љ–∞–Ї—Б–Є–Љ–∞–ї—М–љ–Њ–є –і–Њ–Ј—Л –Є –Љ–∞–Ї—Б–Є–Љ–∞–ї—М–љ–Њ–≥–Њ –≤—А–µ–Љ–µ–љ–Є –Є–љ—Д—Г–Ј–Є–Є –∞–љ—В–Є–±–Є–Њ—В–Є–Ї–∞.
–Я–Њ–Ї–∞–Ј–∞—В–µ–ї—М T>–Ь–Я–Ъ –њ—А–Є –њ—А–Є–Љ–µ–љ–µ–љ–Є–Є 2 –≥ –Љ–µ—А–Њ–њ–µ–љ–µ–Љ–∞ —З–µ—А–µ–Ј 8 —З–∞—Б–Њ–≤ –≤ –≤–Є–і–µ 3–—З–∞—Б–Њ–≤–Њ–є –Є–љ—Д—Г–Ј–Є–Є –њ—А–Є –Љ–∞—В–µ–Љ–∞—В–Є—З–µ—Б–Ї–Њ–Љ –Љ–Њ–і–µ–ї–Є—А–Њ–≤–∞–љ–Є–Є –Љ–Њ–≥ –і–Њ—Б—В–Є–≥–∞—В—М 97% –≤ –Њ—В–љ–Њ—И–µ–љ–Є–Є P. aeruginosa. –Я—А–Є –њ—А–Є–Љ–µ–љ–µ–љ–Є–Є —Н—В–Є—Е —А–µ–ґ–Є–Љ–Њ–≤ —Г –±–Њ–ї–µ–µ —З–µ–Љ 80% –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–љ—Л—Е –њ–µ—А–Є–Њ–і –њ—А–µ–≤—Л—И–µ–љ–Є—П —Д–∞—А–Љ–∞–Ї–Њ–Ї–Є–љ–µ—В–Є—З–µ—Б–Ї–Њ–є –Ї—А–Є–≤–Њ–є –њ—А–Є –Ь–Я–Ъ 16 –Љ–≥/–ї —Б–Њ—Б—В–∞–≤–ї—П–ї –±–Њ–ї–µ–µ 40% –њ–µ—А–Є–Њ–і–∞ –і–Њ–Ј–Є—А–Њ–≤–∞–љ–Є—П, —З—В–Њ —Б–Њ–Њ—В–≤–µ—В—Б—В–≤—Г–µ—В –Љ–∞–Ї—Б–Є–Љ–∞–ї—М–љ–Њ–Љ—Г –Ї–Є–ї–ї–Є–љ–≥—Г, –Є –≤–µ—Б—М –њ–µ—А–Є–Њ–і –і–Њ–Ј–Є—А–Њ–≤–∞–љ–Є—П –њ—А–µ–≤—Л—И–∞–ї–∞ –±–∞–Ї—В–µ—А–Є–Њ—Б—В–∞—В–Є—З–µ—Б–Ї–Є–є —Г—А–Њ–≤–µ–љ—М. –≠—В–Њ—В —Г—А–Њ–≤–µ–љ—М –њ—А–µ–њ–∞—А–∞—В–∞ —Б–њ–Њ—Б–Њ–±–µ–љ –њ—А–µ–і—Г–њ—А–µ–ґ–і–∞—В—М –њ–Њ—П–≤–ї–µ–љ–Є–µ —А–µ–Ј–Є—Б—В–µ–љ—В–љ–Њ—Б—В–Є –Ї –Љ–µ—А–Њ–њ–µ–љ–µ–Љ—Г, —В–∞–Ї –Ї–∞–Ї –≤ 100% –Њ–љ –њ—А–µ–і–Њ—В–≤—А–∞—Й–∞–µ—В –Љ—Г—В–∞—Ж–Є–Є –Є –≤—Л–Ј–≤–∞–µ—В –≥–Є–±–µ–ї—М 80% –≤–Њ–Ј–±—Г–і–Є—В–µ–ї–µ–є [23].
–Я—А–Њ–≤–µ–і–µ–љ–Њ —Б—А–∞–≤–љ–Є—В–µ–ї—М–љ–Њ–µ –Љ–Њ–і–µ–ї–Є—А–Њ–≤–∞–љ–Є–µ –њ—А–Є–Љ–µ–љ–µ–љ–Є—П —А–∞–Ј–ї–Є—З–љ—Л—Е –і–Њ–Ј –Є –Є–љ—В–µ—А–≤–∞–ї–Њ–≤ –і–Њ–Ј–Є—А–Њ–≤–∞–љ–Є—П –≤ –Њ—В–љ–Њ—И–µ–љ–Є–Є Enterobacteriaceae, Acinetobacter sp –Є P. aeruruginosa. –Ф–Њ–Ј–∞ –њ—А–µ–њ–∞—А–∞—В–∞ —Б–Њ–Њ—В–≤–µ—В—Б—В–≤–Њ–≤–∞–ї–∞ 30––Љ–Є–љ—Г—В–љ–Њ–є –Є–љ—Д—Г–Ј–Є–Є 1 –Є–ї–Є 2 –≥ —З–µ—А–µ–Ј 8 —З–∞—Б–Њ–≤ –Є 3–—З–∞—Б–Њ–≤–Њ–є –Є–љ—Д—Г–Ј–Є–Є 0,5, 1 –Є 2 –≥ —З–µ—А–µ–Ј 8 —З–∞—Б–Њ–≤ –Є 1 –Є–ї–Є 2 –≥ —З–µ—А–µ–Ј 12 —З–∞—Б–Њ–≤. –†–µ–Ј—Г–ї—М—В–∞—В—Л –Љ–Њ–і–µ–ї–Є—А–Њ–≤–∞–љ–Є—П –њ–Њ–і—В–≤–µ—А–і–Є–ї–Є, —З—В–Њ –њ—А–Њ–і–Њ–ї–ґ–Є—В–µ–ї—М–љ–∞—П –Є–љ—Д—Г–Ј–Є—П –Њ–і–љ–Њ–є –Є —В–Њ–є –ґ–µ –і–Њ–Ј—Л (1 –≥ –≤ —В–µ—З–µ–љ–Є–µ 30 –Љ–Є–љ—Г—В –Є–ї–Є 3 —З–∞—Б–Њ–≤ —З–µ—А–µ–Ј 8 —З–∞—Б–Њ–≤) –љ–µ –±—Г–і–µ—В —Г–≤–µ–ї–Є—З–Є–≤–∞—В—М, –ї–Є–±–Њ –љ–µ–Ј–љ–∞—З–Є—В–µ–ї—М–љ–Њ —Г–≤–µ–ї–Є—З–Є—В –±–∞–Ї—В–µ—А–Є—Ж–Є–і–љ—Г—О –∞–Ї—В–Є–≤–љ–Њ—Б—В—М –≤ –Њ—В–љ–Њ—И–µ–љ–Є–Є —А–∞–Ј–ї–Є—З–љ—Л—Е Enterobacteriaceae (0% –і–ї—П E. coli, Enterobacter cloacae –Є Serratia sp, –љ–∞ 0,5% – –і–ї—П Klebsiella pneumoniae). –Ґ–∞–Ї–Є–Љ –Њ–±—А–∞–Ј–Њ–Љ, –њ—А–Њ–і–Њ–ї–ґ–Є—В–µ–ї—М–љ–Њ—Б—В—М –≤—А–µ–Љ–µ–љ–Є –Є–љ—Д—Г–Ј–Є–Є –љ–µ –≤–ї–Є—П–µ—В –љ–∞ –±–∞–Ї—В–µ—А–Є—Ж–Є–і–љ–Њ—Б—В—М –Є–Ј––Ј–∞ —В–Њ–≥–Њ, —З—В–Њ —Н—В–Є –±–∞–Ї—В–µ—А–Є–Є –Є–Љ–µ—О—В —З—А–µ–Ј–≤—Л—З–∞–є–љ–Њ –≤—Л—Б–Њ–Ї—Г—О –њ—А–Є—А–Њ–і–љ—Г—О —З—Г–≤—Б—В–≤–Є—В–µ–ї—М–љ–Њ—Б—В—М –Ї –Љ–µ—А–Њ–њ–µ–љ–µ–Љ—Г –Є 30––Љ–Є–љ—Г—В–љ–∞—П –Є–љ—Д—Г–Ј–Є—П –њ–Њ–Ј–≤–Њ–ї—П–µ—В –і–Њ—Б—В–Є–≥–∞—В—М –Њ–њ—В–Є–Љ–∞–ї—М–љ—Л—Е —Д–∞—А–Љ–∞–Ї–Њ–і–Є–љ–∞–Љ–Є—З–µ—Б–Ї–Є—Е –њ–Њ–Ї–∞–Ј–∞—В–µ–ї–µ–є. –Ю–і–љ–∞–Ї–Њ –≤—Л—Б–Њ–Ї–Є–є —Г—А–Њ–≤–µ–љ—М –њ—А–µ–њ–∞—А–∞—В–∞, —Б–Њ–Њ—В–≤–µ—В—Б—В–≤—Г—О—Й–Є–є –±–∞–Ї—В–µ—А–Є—Ж–Є–і–љ–Њ–Љ—Г, –њ–Њ–ї—Г—З–µ–љ–љ—Л–є –њ—А–Є –Љ–Њ–і–µ–ї–Є—А–Њ–≤–∞–љ–Є–Є –њ—А–Њ–і–Њ–ї–ґ–Є—В–µ–ї—М–љ–Њ–є –Є–љ—Д—Г–Ј–Є–Є –љ–Є–Ј–Ї–Є—Е (3–—З–∞—Б–Њ–≤–∞—П –Є–љ—Д—Г–Ј–Є—П 0,5 –≥ —З–µ—А–µ–Ј 8 —З) –Є–ї–Є —Б—В–∞–љ–і–∞—А—В–љ—Л—Е –і–Њ–Ј (3–—З–∞—Б–Њ–≤–∞—П –Є–љ—Д—Г–Ј–Є—П 1 –≥ —З–µ—А–µ–Ј 12 —З) —Г–Ї–∞–Ј—Л–≤–∞–ї –љ–∞ —Ж–µ–ї–µ—Б–Њ–Њ–±—А–∞–Ј–љ–Њ—Б—В—М –њ—А–Є–Љ–µ–љ–µ–љ–Є—П –љ–Є–Ј–Ї–Є—Е —Б—Г—В–Њ—З–љ—Л—Е –і–Њ–Ј. –Ю—Б–љ–Њ–≤–љ–Њ–µ –њ—А–µ–Є–Љ—Г—Й–µ—Б—В–≤–Њ –њ—А–Њ–і–ї–µ–љ–љ–Њ–є –Є–љ—Д—Г–Ј–Є–Є –і–Њ—Б—В–Є–≥–∞–µ—В—Б—П –Є–Љ–µ–љ–љ–Њ –≤ –Њ—В–љ–Њ—И–µ–љ–Є–Є –њ–Њ–њ—Г–ї—П—Ж–Є–Є –±–∞–Ї—В–µ—А–Є–є —Б –≤—Л—Б–Њ–Ї–Є–Љ —Г—А–Њ–≤–љ–µ–Љ –Ь–Я–Ъ. –Т –Њ—В–љ–Њ—И–µ–љ–Є–Є P. aerugonosa –Љ–Њ–і–µ–ї–Є—А–Њ–≤–∞–љ–Є–µ –і–Њ–Ј—Л 2 –≥ —З–µ—А–µ–Ј 8 —З–∞—Б–Њ–≤ –≤ –≤–Є–і–µ 3–—З–∞—Б–Њ–≤–Њ–є –Є–љ—Д—Г–Ј–Є–Є —Г–Ї–∞–Ј–∞–ї–Њ –љ–∞ –і–Њ—Б—В–Є–ґ–µ–љ–Є–µ –±–∞–Ї—В–µ—А–Є—Ж–Є–і–љ–Њ–є –Ї–Њ–љ—Ж–µ–љ—В—А–∞—Ж–Є–Є –≤ —В–µ—З–µ–љ–Є–µ 84% –њ–µ—А–Є–Њ–і–∞ –і–Њ–Ј–Є—А–Њ–≤–∞–љ–Є—П –њ–Њ —Б—А–∞–≤–љ–µ–љ–Є—О —Б 80% —В–Њ–є –ґ–µ —Б–∞–Љ–Њ–є –і–Њ–Ј—Л –њ—А–Є 30––Љ–Є–љ—Г—В–љ–Њ–є –Є–љ—Д—Г–Ј–Є–Є. –Я—А–µ–і–њ–Њ–ї–∞–≥–∞–µ—В—Б—П, —З—В–Њ –і–Њ–Ј–∞ 2 –≥ —З–µ—А–µ–Ј 8 —З–∞—Б–Њ–≤ –≤ –≤–Є–і–µ 3–—З–∞—Б–Њ–≤–Њ–є –Є–љ—Д—Г–Ј–Є–Є –±—Г–і–µ—В –њ—А–Є–Љ–µ–љ—П—В—М—Б—П –і–ї—П –ї–µ—З–µ–љ–Є—П –Є–љ—Д–µ–Ї—Ж–Є–є, –≤—Л–Ј–≤–∞–љ–љ—Л—Е Acinetobacter –Є P. aeruginosa. –≠—В–Њ –±—Л–ї–Њ –њ–Њ–і—В–≤–µ—А–ґ–і–µ–љ–Є–µ–Љ –њ–Њ–ї—Г—З–µ–љ–љ—Л—Е —А–∞–љ–µ–µ –і–∞–љ–љ—Л—Е, —З—В–Њ 2 –≥ –Љ–µ—А–Њ–њ–µ–љ–µ–Љ–∞ —З–µ—А–µ–Ј 8 —З–∞—Б–Њ–≤ –≤ –≤–Є–і–µ –њ—А–Њ–і–ї–µ–љ–љ–Њ–є –Є–љ—Д—Г–Ј–Є–Є –њ–Њ–Ј–≤–Њ–ї—П—О—В –і–Њ—Б—В–Є–≥–∞—В—М –±–∞–Ї—В–µ—А–Є—Ж–Є–і–љ–Њ–≥–Њ —Г—А–Њ–≤–љ—П –і–ї—П –±–∞–Ї—В–µ—А–Є–є, –Ї–Њ—В–Њ—А—Л–µ —А–∞—Б—Б–Љ–∞—В—А–Є–≤–∞—О—В—Б—П —А–µ–Ј–Є—Б—В–µ–љ—В–љ—Л–Љ–Є –Ї –Љ–µ—А–Њ–њ–µ–љ–µ–Љ—Г (–Ь–Я–Ъ=16 –Љ–≥/–ї).
–Ъ–ї–Є–љ–Є—З–µ—Б–Ї–Њ–µ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ —Н—В–Њ–≥–Њ —А–µ–ґ–Є–Љ–∞ –±—Л–ї–Њ –њ—А–Њ–≤–µ–і–µ–љ–Њ —Г 32––ї–µ—В–љ–µ–≥–Њ –њ–∞—Ж–Є–µ–љ—В–∞ —Б –Љ—Г–Ї–Њ–≤–Є—Б—Ж–µ–і–Њ–Ј–Њ–Љ –Є –њ–љ–µ–≤–Љ–Њ–љ–Є–µ–є, –≤—Л–Ј–≤–∞–љ–љ–Њ–є Burkholderia cepacia, —А–µ–Ј–Є—Б—В–µ–љ—В–љ–Њ–є –Ї–Њ –≤—Б–µ–Љ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–љ—Л–Љ –∞–љ—В–Є–±–Є–Њ—В–Є–Ї–∞–Љ. –Ь–Я–Ъ –Љ–µ—А–Њ–њ–µ–љ–µ–Љ–∞ —Б–Њ—Б—В–∞–≤–Є–ї–∞ 8 –Љ–≥/–ї –Є –њ–∞—Ж–Є–µ–љ—В –±—Л–ї —Г—Б–њ–µ—И–љ–Њ –Є–Ј–ї–µ—З–µ–љ –Љ–µ—А–Њ–њ–µ–љ–µ–Љ–Њ–Љ –≤ –і–Њ–Ј–µ 2 –≥ —З–µ—А–µ–Ј 8 —З–∞—Б–Њ–≤ –≤ –≤–Є–і–µ 3–—З–∞—Б–Њ–≤–Њ–є –Є–љ—Д—Г–Ј–Є–Є. –Я–Њ—Б–ї–µ –Ј–∞–±–Њ—А–∞ –Њ–±—А–∞–Ј—Ж–Њ–≤ –Ї—А–Њ–≤–Є –Є –Њ–њ—А–µ–і–µ–ї–µ–љ–Є—П –Ї–Њ–љ—Ж–µ–љ—В—А–∞—Ж–Є–Є –Љ–µ—А–Њ–њ–µ–љ–µ–Љ–∞ —Г –і–∞–љ–љ–Њ–≥–Њ –њ–∞—Ж–Є–µ–љ—В–∞ –±—Л–ї–Њ –њ–Њ–Ї–∞–Ј–∞–љ–Њ, —З—В–Њ –њ—А–Є —Н—В–Њ–Љ —А–µ–ґ–Є–Љ–µ –і–Њ–Ј–Є—А–Њ–≤–∞–љ–Є—П –њ—А–Є –Ь–Я–Ъ 8 –Љ–≥/–ї –і–Њ—Б—В–Є–≥–∞–ї–Є—Б—М 52% T>–Ь–Я–Ъ.
–°—А–∞–≤–љ–µ–љ–Є–µ —Д–∞—А–Љ–∞–Ї–Њ–і–Є–љ–∞–Љ–Є—З–µ—Б–Ї–Є—Е –њ–Њ–Ї–∞–Ј–∞—В–µ–ї–µ–є –Љ–µ—А–Њ–њ–µ–љ–µ–Љ–∞
–Є –Є–Љ–Є–њ–µ–љ–µ–Љ–∞
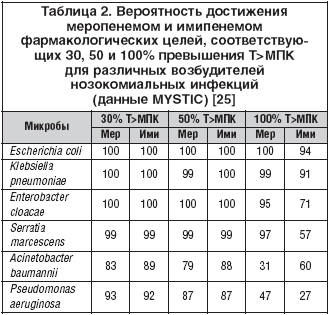
–Т —В–∞–±–ї–Є—Ж–µ 2 –њ—А–µ–і—Б—В–∞–≤–ї–µ–љ–∞ –≤–µ—А–Њ—П—В–љ–Њ—Б—В—М –і–Њ—Б—В–Є–ґ–µ–љ–Є—П —Д–∞—А–Љ–∞–Ї–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є—Е –њ–∞—А–∞–Љ–µ—В—А–Њ–≤ –≤ –Њ—В–љ–Њ—И–µ–љ–Є–Є –љ–∞–Є–±–Њ–ї–µ–µ –∞–Ї—В—Г–∞–ї—М–љ—Л—Е –≤–Њ–Ј–±—Г–і–Є—В–µ–ї–µ–є –љ–Њ–Ј–Њ–Ї–Њ–Љ–Є–∞–ї—М–љ—Л—Е –Є–љ—Д–µ–Ї—Ж–Є–є [24]. –Ю–±–∞ –Ї–∞—А–±–∞–њ–µ–љ–µ–Љ–∞ –Њ–±–ї–∞–і–∞–ї–Є –Њ—З–µ–љ—М –≤—Л—Б–Њ–Ї–Є–Љ –±–∞–Ї—В–µ—А–Є–Њ—Б—В–∞—В–Є—З–µ—Б–Ї–Є–Љ (30% T>–Ь–Я–Ъ) –Є –±–∞–Ї—В–µ—А–Є—Ж–Є–і–љ—Л–Љ (50% T>–Ь–Я–Ъ) –њ–Њ—В–µ–љ—Ж–Є–∞–ї–Њ–Љ. –Ю–і–љ–∞–Ї–Њ –і–ї—П –і–Њ—Б—В–Є–ґ–µ–љ–Є—П —Ж–µ–ї–Є –њ—А–Њ—Д–Є–ї–∞–Ї—В–Є–Ї–Є –њ–Њ—П–≤–ї–µ–љ–Є—П –Љ—Г—В–∞—Ж–Є–є (100% T>–Ь–Я–Ъ) —Д–∞—А–Љ–∞–Ї–Њ–і–Є–љ–∞–Љ–Є—З–µ—Б–Ї–Є–µ –њ–Њ–Ї–∞–Ј–∞—В–µ–ї–Є –Њ–Ї–∞–Ј–∞–ї–Є—Б—М –≤—Л—И–µ —Г –Љ–µ—А–Њ–њ–µ–љ–µ–Љ–∞ –і–ї—П S. marcescens (57%), E. cloacae (71%) –Є K. pneumoniae (91%). –Я—А–Њ—В–Є–≤ P. aeruginosa —Ж–µ–ї–µ–≤—Л–µ –њ–Њ–Ї–∞–Ј–∞—В–µ–ї–Є –Љ–µ—А–Њ–њ–µ–љ–µ–Љ–∞ –Є –Є–Љ–Є–њ–µ–љ–µ–Љ–∞ –≤ –Њ—В–љ–Њ—И–µ–љ–Є–Є –±–∞–Ї—В–µ—А–Є–Њ—Б—В–∞—В–Є—З–µ—Б–Ї–Њ–≥–Њ –Є –±–∞–Ї—В–µ—А–Є—Ж–Є–і–љ–Њ–≥–Њ —Н—Д—Д–µ–Ї—В–∞ –Њ–Ї–∞–Ј–∞–ї–Є—Б—М –Њ–і–Є–љ–∞–Ї–Њ–≤—Л–Љ–Є; –≤ –Њ—В–љ–Њ—И–µ–љ–Є–Є –њ—А–Њ—Д–Є–ї–∞–Ї—В–Є–Ї–Є –Љ—Г—В–∞—Ж–Є–є (100% T>–Ь–Я–Ъ) –њ–Њ–Ї–∞–Ј–∞—В–µ–ї–Є –Љ–µ—А–Њ–њ–µ–љ–µ–Љ–∞ –Њ–Ї–∞–Ј–∞–ї–Є—Б—М –њ—А–Є–Љ–µ—А–љ–Њ –≤ 2 —А–∞–Ј–∞ –≤—Л—И–µ, –Њ–і–љ–∞–Ї–Њ –і–∞–ґ–µ —Н—В–Њ—В —Г—А–Њ–≤–µ–љ—М –Њ–Ї–∞–Ј–∞–ї—Б—П –љ–µ —Б–ї–Є—И–Ї–Њ–Љ –≤—Л—Б–Њ–Ї–Є–Љ. –Т–µ—А–Њ—П—В–љ–Њ—Б—В—М –і–Њ—Б—В–Є–ґ–µ–љ–Є—П –±–∞–Ї—В–µ—А–Є–Њ—Б—В–∞—В–Є—З–µ—Б–Ї–Њ–≥–Њ, –±–∞–Ї—В–µ—А–Є—Ж–Є–і–љ–Њ–≥–Њ –Є 100% T>–Ь–Я–Ъ –≤ –Њ—В–љ–Њ—И–µ–љ–Є–Є A. baumannii, —Б–Њ–Њ—В–≤–µ—В—Б—В–≤–µ–љ–љ–Њ, –љ–∞ 5, 9 –Є 29% –≤—Л—И–µ —Г –Є–Љ–Є–њ–µ–љ–µ–Љ–∞, —З–µ–Љ —Г –Љ–µ—А–Њ–њ–µ–љ–µ–Љ–∞. –Ф–ї—П –Љ–µ—А–Њ–њ–µ–љ–µ–Љ–∞ –љ–∞–Є–±–Њ–ї–µ–µ —Б–ї–Њ–ґ–љ—Л–Љ –±—Л–ї–Њ –і–Њ—Б—В–Є–ґ–µ–љ–Є–µ –њ–Њ–Ї–∞–Ј–∞—В–µ–ї–µ–є 50% –Є 100% T>–Ь–Я–Ъ, –њ–Њ–Ї–∞–Ј–∞—В–µ–ї–Є –Є–Љ–Є–њ–µ–љ–µ–Љ–∞ —В–∞–Ї–ґ–µ –љ–µ –±—Л–ї–Є —Г–і–Њ–≤–ї–µ—В–≤–Њ—А–Є—В–µ–ї—М–љ—Л–Љ–Є –њ—А–Є 100% T>–Ь–Я–Ъ.
–°–љ–Є–ґ–µ–љ–Є–µ –і–Њ–Ј–Є—А–Њ–≤–Ї–Є –Љ–µ—А–Њ–њ–µ–љ–µ–Љ–∞
–≤ –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є—Е —Г—Б–ї–Њ–≤–Є—П—Е
–Ю–і–љ–Њ–є –Є–Ј –њ—А–Њ–±–ї–µ–Љ –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Њ–≥–Њ –њ—А–Є–Љ–µ–љ–µ–љ–Є—П –Ї–∞—А–±–∞–њ–µ–љ–µ–Љ–Њ–≤ —П–≤–ї—П–µ—В—Б—П –Є—Е —Б—В–Њ–Є–Љ–Њ—Б—В—М –њ–Њ —Б—А–∞–≤–љ–µ–љ–Є—О —Б –і—А—Г–≥–Є–Љ–Є b––ї–∞–Ї—В–∞–Љ–љ—Л–Љ–Є –∞–љ—В–Є–±–Є–Њ—В–Є–Ї–∞–Љ–Є. –° —Г—З–µ—В–Њ–Љ –≤—Л—Б–Њ–Ї–Њ–є –∞–Ї—В–Є–≤–љ–Њ—Б—В–Є –њ—А–µ–њ–∞—А–∞—В–Њ–≤ in vitro, –Є—Е –≤—Л—Б–Њ–Ї–Њ–є –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Њ–є —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В–Є –њ—А–µ–і–њ—А–Є–љ–Є–Љ–∞—О—В—Б—П –њ–Њ–њ—Л—В–Ї–Є —Б–љ–Є–ґ–µ–љ–Є—П –Ј–∞—В—А–∞—В —Б –њ–Њ–Љ–Њ—Й—М—О –Њ–±–Њ—Б–љ–Њ–≤–∞–љ–љ–Њ–≥–Њ –≤–∞—А—М–Є—А–Њ–≤–∞–љ–Є—П –і–Њ–Ј–Є—А–Њ–≤–Ї–Є –њ—А–µ–њ–∞—А–∞—В–∞.
–Т —А–µ—В—А–Њ—Б–њ–µ–Ї—В–Є–≤–љ–Њ–Љ –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Њ–Љ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є –Љ–µ—А–Њ–њ–µ–љ–µ–Љ–∞ 100 –њ–∞—Ж–Є–µ–љ—В–Њ–≤ –њ–Њ–ї—Г—З–Є–ї–Є –Њ–±—Л—З–љ—Г—О –і–Њ–Ј—Г –Љ–µ—А–Њ–њ–µ–љ–µ–Љ–∞ –Є 192 – –∞–ї—М—В–µ—А–љ–∞—В–Є–≤–љ—Г—О [26]. –Ш–Ј–Љ–µ–љ–µ–љ–Є–µ –і–Њ–Ј–Є—А–Њ–≤–Ї–Є –Њ–Ї–∞–Ј–∞–ї–Њ—Б—М —Г—Б–њ–µ—И–љ—Л–Љ —Г 99% –њ–∞—Ж–Є–µ–љ—В–Њ–≤. –Т –њ–µ—А–≤–Њ–є –≥—А—Г–њ–њ–µ –њ–∞—Ж–Є–µ–љ—В—Л –њ–Њ–ї—Г—З–∞–ї–Є –њ—А–µ–њ–∞—А–∞—В –њ–Њ 1 –≥ —З–µ—А–µ–Ј 8 —З–∞—Б–Њ–≤ (77%) –Є–ї–Є 1 –≥ —З–µ—А–µ–Ј 12 —З–∞—Б–Њ–≤ (23%) –њ—А–Є –њ–Њ—З–µ—З–љ–Њ–є –љ–µ–і–Њ—Б—В–∞—В–Њ—З–љ–Њ—Б—В–Є. –Т–Њ 2 –≥—А—Г–њ–њ–µ (–∞–ї—М—В–µ—А–љ–∞—В–Є–≤–љ—Л–є —А–µ–ґ–Є–Љ) –њ–∞—Ж–Є–µ–љ—В—Л –њ–Њ–ї—Г—З–∞–ї–Є –Љ–µ—А–Њ–њ–µ–љ–µ–Љ –≤ –і–Њ–Ј–µ 500 –Љ–≥ —З–µ—А–µ–Ј 6 —З–∞—Б–Њ–≤ (68%) –Є–ї–Є –њ–Њ 500 –Љ–≥ —З–µ—А–µ–Ј 8 —З–∞—Б–Њ–≤ (32%) –Є–Ј––Ј–∞ –њ–Њ—З–µ—З–љ–Њ–є –љ–µ–і–Њ—Б—В–∞—В–Њ—З–љ–Њ—Б—В–Є. –Э–µ –≤—Л—П–≤–ї–µ–љ–Њ —А–∞–Ј–ї–Є—З–Є–є –Љ–µ–ґ–і—Г –≥—А—Г–њ–њ–∞–Љ–Є –њ–Њ –і–µ–Љ–Њ–≥—А–∞—Д–Є—З–µ—Б–Ї–Є–Љ –њ–Њ–Ї–∞–Ј–∞—В–µ–ї—П–Љ, —Б–Њ–њ—Г—В—Б—В–≤—Г—О—Й–µ–є –њ–∞—В–Њ–ї–Њ–≥–Є–Є (Charlson Comorbidity Index), –ї–Њ–Ї–∞–ї–Є–Ј–∞—Ж–Є–Є –Њ—З–∞–≥–∞ –Є–љ—Д–µ–Ї—Ж–Є–Є, –њ—А–Њ–і–Њ–ї–ґ–Є—В–µ–ї—М–љ–Њ—Б—В–Є –≥–Њ—Б–њ–Є—В–∞–ї–Є–Ј–∞—Ж–Є–Є –і–Њ –љ–∞–Ј–љ–∞—З–µ–љ–Є—П –Љ–µ—А–Њ–њ–µ–љ–µ–Љ–∞ –Є–ї–Є –њ–Њ —Н—В–Є–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Њ–є —Б—В—А—Г–Ї—В—Г—А–µ. –Э–µ –±—Л–ї–Њ –Њ–±–љ–∞—А—Г–ґ–µ–љ–Њ —А–∞–Ј–ї–Є—З–Є–є –≤ –љ–∞–Ј–љ–∞—З–µ–љ–Є–Є —Б–Њ–њ—Г—В—Б—В–≤—Г—О—Й–µ–є —В–µ—А–∞–њ–Є–Є –Љ–µ–ґ–і—Г –Ї–Њ–≥–Њ—А—В–∞–Љ–Є –њ–∞—Ж–Є–µ–љ—В–Њ–≤. –≠—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В—М –ї–µ—З–µ–љ–Є—П –і–Њ—Б—В–Њ–≤–µ—А–љ–Њ –љ–µ —А–∞–Ј–ї–Є—З–∞–ї–∞—Б—М –Љ–µ–ґ–і—Г –Љ–Њ–љ–Њ– –Є –Ї–Њ–Љ–±–Є–љ–Є—А–Њ–≤–∞–љ–љ–Њ–є —В–µ—А–∞–њ–Є–µ–є (95,4 –Є 89%, p=0,286). –Я—А–Њ–і–Њ–ї–ґ–Є—В–µ–ї—М–љ–Њ—Б—В—М –ї–µ—З–µ–љ–Є—П, –±–Њ–ї—М–љ–Є—З–љ–∞—П –ї–µ—В–∞–ї—М–љ–Њ—Б—В—М –Є –њ—А–Њ–і–Њ–ї–ґ–Є—В–µ–ї—М–љ–Њ—Б—В—М –ї–µ—З–µ–љ–Є—П –±—Л–ї–Є —А–∞–≤–љ—Л–Љ–Є.
–Я—А–Є —В—А–∞–і–Є—Ж–Є–Њ–љ–љ–Њ–Љ –і–Њ–Ј–Є—А–Њ–≤–∞–љ–Є–Є —Г 87 –њ–∞—Ж–Є–µ–љ—В–Њ–≤ –њ–µ—А–Є–Њ–і —А–∞–Ј—А–µ—И–µ–љ–Є—П –Є–љ—Д–µ–Ї—Ж–Є–Є –≤ —Б—А–µ–і–љ–µ–Љ —Б–Њ—Б—В–∞–≤–Є–ї 3 –і–љ—П (1–22 –і–љ—П) –њ–Њ —Б—А–∞–≤–љ–µ–љ–Є—О —Б 1,5 –і–љ—П–Љ–Є (1–10 –і–љ–µ–є) —Г 156 –њ–∞—Ж–Є–µ–љ—В–Њ–≤, –њ–Њ–ї—Г—З–Є–≤—И–Є—Е –∞–ї—М—В–µ—А–љ–∞—В–Є–≤–љ—Л–є —А–µ–ґ–Є–Љ (p<0,0001). –≠—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В—М –Њ–±—Л—З–љ–Њ–є –Є –∞–ї—М—В–µ—А–љ–∞—В–Є–≤–љ–Њ–є –і–Њ–Ј–Є—А–Њ–≤–Ї–Є –і–Њ—Б—В–Њ–≤–µ—А–љ–Њ –љ–µ —А–∞–Ј–ї–Є—З–∞–ї–∞—Б—М (90,9 –Є 92,1%, p=0,72). –Я–Њ–ї–Є–Љ–Є–Ї—А–Њ–±–љ—Л–µ –Є–љ—Д–µ–Ї—Ж–Є–Є, –і–Є–∞–±–µ—В –Є —Б–µ–њ—Б–Є—Б —Б–љ–Є–ґ–∞–ї–Є —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В—М –ї–µ—З–µ–љ–Є—П. –Я–Њ—Б–ї–µ –Є—Б–Ї–ї—О—З–µ–љ–Є—П —Н—В–Є—Е —Д–∞–Ї—В–Њ—А–Њ–≤ –њ—А–Њ–≤–µ–і–µ–љ–∞ –Њ—Ж–µ–љ–Ї–∞ –Њ–±–Њ–Є—Е —А–µ–ґ–Є–Љ–Њ–≤ –і–Њ–Ј–Є—А–Њ–≤–∞–љ–Є—П —Б –њ–Њ–Љ–Њ—Й—М—О –Љ–љ–Њ–≥–Њ–≤–∞—А–Є–∞–љ—В–љ–Њ–≥–Њ —А–µ–≥—А–µ—Б—Б–Є–Њ–љ–љ–Њ–≥–Њ –∞–љ–∞–ї–Є–Ј–∞: –љ–∞–ї–Є—З–Є–µ —Б–µ–њ—Б–Є—Б–∞ –Є –њ–Њ–ї–Є–Љ–Є–Ї—А–Њ–±–љ–Њ–є –Є–љ—Д–µ–Ї—Ж–Є–Є –њ—А–Є–≤–Њ–і–Є–ї–Њ –Ї —Б–љ–Є–ґ–µ–љ–Є—О –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Њ–≥–Њ —Н—Д—Д–µ–Ї—В–∞ –∞–љ—В–Є–±–∞–Ї—В–µ—А–Є–∞–ї—М–љ–Њ–є —В–µ—А–∞–њ–Є–Є.
–Р–љ–∞–ї–Є–Ј –Љ–Є–љ–Є–Љ–∞–ї–Є–Ј–∞—Ж–Є–Є –Ј–∞—В—А–∞—В —Г–Ї–∞–Ј–∞–ї –љ–∞ –і–Њ—Б—В–Њ–≤–µ—А–љ–Њ–µ —Б–љ–Є–ґ–µ–љ–Є–µ –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є—П –њ—А–µ–њ–∞—А–∞—В–∞ –≤ –∞–ї—М—В–µ—А–љ–∞—В–Є–≤–љ–Њ–Љ —А–µ–ґ–Є–Љ–µ. –°—А–µ–і–љ–Є–µ –Ј–∞—В—А–∞—В—Л –љ–∞ –њ–∞—Ж–Є–µ–љ—В–∞ –њ—А–Є —В—А–∞–і–Є—Ж–Є–Њ–љ–љ–Њ–Љ –і–Њ–Ј–Є—А–Њ–≤–∞–љ–Є–Є —Б–Њ—Б—В–∞–≤–Є–ї–Є $439,05, –њ—А–Є –∞–ї—М—В–µ—А–љ–∞—В–Є–≤–љ–Њ–Љ – $234,08 (p<0,0001). –Ґ–∞–Ї–Є–Љ –Њ–±—А–∞–Ј–Њ–Љ, –њ–Њ–Ї–∞–Ј–∞–љ–∞ –≤–Њ–Ј–Љ–Њ–ґ–љ–Њ—Б—В—М —Б–љ–Є–ґ–µ–љ–Є—П –Ј–∞—В—А–∞—В –љ–∞ $204,97 (–Њ–Ї–Њ–ї–Њ 50%) –љ–∞ 1 –њ–∞—Ж–Є–µ–љ—В–∞. –Т —В–µ—З–µ–љ–Є–µ –≥–Њ–і–∞ 192 –њ–∞—Ж–Є–µ–љ—В–∞ –њ–Њ–ї—Г—З–Є–ї–Є –∞–ї—М—В–µ—А–љ–∞—В–Є–≤–љ—Л–є —А–µ–ґ–Є–Љ –і–Њ–Ј–Є—А–Њ–≤–∞–љ–Є—П, —З—В–Њ –њ–Њ–Ј–≤–Њ–ї–Є–ї–Њ —Б—Н–Ї–Њ–љ–Њ–Љ–Є—В—М –њ–Њ—З—В–Є $40000.
–Ч–∞–Ї–ї—О—З–µ–љ–Є–µ
–Ъ–∞—А–±–∞–њ–µ–љ–µ–Љ—Л —П–≤–ї—П—О—В—Б—П –∞–Ї—В–Є–≤–љ—Л–Љ–Є –Є –±–µ–Ј–Њ–њ–∞—Б–љ—Л–Љ–Є –њ—А–µ–њ–∞—А–∞—В–∞–Љ–Є. –Ф–ї—П –і–Њ—Б—В–Є–ґ–µ–љ–Є—П –Њ–њ—В–Є–Љ–∞–ї—М–љ—Л—Е —А–µ–Ј—Г–ї—М—В–∞—В–Њ–≤ –ї–µ—З–µ–љ–Є—П –Љ–Њ–≥—Г—В –њ—А–Є–Љ–µ–љ—П—В—М—Б—П —А–∞–Ј–ї–Є—З–љ—Л–µ –і–Њ–Ј—Л –њ—А–µ–њ–∞—А–∞—В–Њ–≤ –≤ –Ј–∞–≤–Є—Б–Є–Љ–Њ—Б—В–Є –Њ—В –Њ—Б–Њ–±–µ–љ–љ–Њ—Б—В–µ–є –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Њ–є —Б–Є—В—Г–∞—Ж–Є–Є. –Я—А–Є —В—П–ґ–µ–ї—Л—Е –Є —Б—А–µ–і–љ–µ—В—П–ґ–µ–ї—Л—Е –Є–љ—Д–µ–Ї—Ж–Є—П—Е, –≤—Л–Ј–≤–∞–љ–љ—Л—Е —Д–ї–Њ—А–Њ–є —Б –≤—Л—Б–Њ–Ї–Њ–є –њ—А–Є—А–Њ–і–љ–Њ–є —З—Г–≤—Б—В–≤–Є—В–µ–ї—М–љ–Њ—Б—В—М—О –Є –љ–Є–Ј–Ї–Њ–є –Ь–Я–Ъ (E. coli –Є K. pneumoniae), –Љ–µ—А–Њ–њ–µ–љ–µ–Љ –Љ–Њ–ґ–µ—В –њ—А–Є–Љ–µ–љ—П—В—М—Б—П –≤ –і–Њ–Ј–µ 0,5 –≥ —З–µ—А–µ–Ј 6–8 —З–∞—Б–Њ–≤ –≤ –≤–Є–і–µ 30––Љ–Є–љ—Г—В–љ–Њ–є –Є–љ—Д—Г–Ј–Є–Є —Б —В–∞–Ї–Њ–є –ґ–µ —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В—М—О, –Ї–∞–Ї –Є 1 –≥ —З–µ—А–µ–Ј 8 —З–∞—Б–Њ–≤. –°–љ–Є–ґ–µ–љ–Є–µ —Б—Г—В–Њ—З–љ–Њ–є –і–Њ–Ј—Л –њ–Њ–Ј–≤–Њ–ї—П–µ—В –њ–Њ–ї—Г—З–∞—В—М –±–Њ–ї–µ–µ –≤—Л—Б–Њ–Ї–Є–µ —Н–Ї–Њ–љ–Њ–Љ–Є—З–µ—Б–Ї–Є–µ –њ–Њ–Ї–∞–Ј–∞—В–µ–ї–Є –њ—А–Є–Љ–µ–љ–µ–љ–Є—П –њ—А–µ–њ–∞—А–∞—В–∞. –Я—А–Є –ї–µ—З–µ–љ–Є–Є —В—П–ґ–µ–ї—Л—Е –Є–љ—Д–µ–Ї—Ж–Є–є –њ—А–Є–Љ–µ–љ–µ–љ–Є–µ 0,5 –≥ —З–µ—А–µ–Ј 8 —З–∞—Б–Њ–≤ –≤ –≤–Є–і–µ 3–—З–∞—Б–Њ–≤–Њ–є –Є–љ—Д—Г–Ј–Є–Є, 1 –≥ —З–µ—А–µ–Ј 8 —З–∞—Б–Њ–≤ –≤ –≤–Є–і–µ 30––Љ–Є–љ—Г—В–љ–Њ–є –Є–љ—Д—Г–Ј–Є–Є –Є–ї–Є 0,5 –Љ–≥ —З–µ—А–µ–Ј 6 —З–∞—Б–Њ–≤ –≤ –≤–Є–і–µ 30––Љ–Є–љ—Г—В–љ–Њ–є –Є–љ—Д—Г–Ј–Є–Є –њ–Њ–Ј–≤–Њ–ї—П–µ—В –і–Њ—Б—В–Є–≥–∞—В—М –Њ–і–Є–љ–∞–Ї–Њ–≤–Њ–є –±–∞–Ї—В–µ—А–Є—Ж–Є–і–љ–Њ–є –∞–Ї—В–Є–≤–љ–Њ—Б—В–Є –≤ –Њ—В–љ–Њ—И–µ–љ–Є–Є —З—Г–≤—Б—В–≤–Є—В–µ–ї—М–љ–Њ–є –Ї –Љ–µ—А–Њ–њ–µ–љ–µ–Љ—Г —Д–ї–Њ—А—Л.
–Я—А–Є –Є–љ—Д–µ–Ї—Ж–Є—П—Е —Б –≤—Л—Б–Њ–Ї–Є–Љ —А–Є—Б–Ї–Њ–Љ –љ–µ—Д–µ—А–Љ–µ–љ—В–Є—А—Г—О—Й–µ–є —Д–ї–Њ—А—Л (P. aeruginosa, Acinetobacter sp.) –Є–ї–Є –і—А—Г–≥–Є—Е —А–µ–Ј–Є—Б—В–µ–љ—В–љ—Л—Е –≥—А–∞–Љ–Њ—В—А–Є—Ж–∞—В–µ–ї—М–љ—Л—Е –≤–Њ–Ј–±—Г–і–Є—В–µ–ї–µ–є –њ—А–Є–Љ–µ–љ–µ–љ–Є–µ –Љ–µ—А–Њ–њ–µ–љ–µ–Љ–∞ –њ–Њ 1 –≥ —З–µ—А–µ–Ј 8 —З–∞—Б–Њ–≤ –≤ –≤–Є–і–µ 3–—З–∞—Б–Њ–≤–Њ–є –Є–љ—Д—Г–Ј–Є–Є –Є–ї–Є 2 –≥ —З–µ—А–µ–Ј 8 —З–∞—Б–Њ–≤ –≤ –≤–Є–і–µ 30––Љ–Є–љ—Г—В–љ–Њ–є –Є–ї–Є 3–—З–∞—Б–Њ–≤–Њ–є –Є–љ—Д—Г–Ј–Є–Є —Б–њ–Њ—Б–Њ–±—Б—В–≤—Г–µ—В –Њ–њ—В–Є–Љ–Є–Ј–∞—Ж–Є–Є —Д–∞—А–Љ–∞–Ї–Њ–і–Є–љ–∞–Љ–Є—З–µ—Б–Ї–Є—Е –њ–∞—А–∞–Љ–µ—В—А–Њ–≤ –Є –њ–Њ–Ј–≤–Њ–ї—П–µ—В —Г–≤–µ–ї–Є—З–Є—В—М –њ–Њ–Ї–∞–Ј–∞—В–µ–ї—М T>–Ь–Я–Ъ.
–Т –Њ—В–љ–Њ—И–µ–љ–Є–Є –±–Њ–ї–µ–µ —А–µ–Ј–Є—Б—В–µ–љ—В–љ–Њ–є —Д–ї–Њ—А—Л –Љ–Њ–ґ–µ—В –±—Л—В—М —Ж–µ–ї–µ—Б–Њ–Њ–±—А–∞–љ–∞ –Ї–Њ–Љ–±–Є–љ–∞—Ж–Є—П —Б –∞–Љ–Є–љ–Њ–≥–ї–Є–Ї–Њ–Ј–Є–і–∞–Љ–Є, –њ–Њ –Ї—А–∞–є–љ–µ–є –Љ–µ—А–µ, –љ–∞ –Ї–Њ—А–Њ—В–Ї–Є–є –њ–µ—А–Є–Њ–і –≤—А–µ–Љ–µ–љ–Є – —Б —Ж–µ–ї—М—О –њ—А–Њ—Д–Є–ї–∞–Ї—В–Є–Ї–Є —А–∞–Ј–≤–Є—В–Є—П —А–µ–Ј–Є—Б—В–µ–љ—В–љ–Њ—Б—В–Є. –Ъ–Њ–Љ–±–Є–љ–∞—Ж–Є—П —Б –љ–Є–Ј–Ї–Є–Љ–Є –і–Њ–Ј–∞–Љ–Є —В–Њ–±—А–∞–Љ–Є—Ж–Є–љ–∞ —Б–њ–Њ—Б–Њ–±–љ–∞ —Б–љ–Є–ґ–∞—В—М –њ–Њ—П–≤–ї–µ–љ–Є–µ —А–µ–Ј–Є—Б—В–µ–љ—В–љ–Њ—Б—В–Є –њ—А–Є —Н–Ї—Б–њ–µ—А–Є–Љ–µ–љ—В–∞–ї—М–љ—Л—Е –Є–љ—Д–µ–Ї—Ж–Є—П—Е, –≤—Л–Ј–≤–∞–љ–љ—Л—Е P. aeruginosa.
–Т–µ—А–Њ—П—В–љ–Њ, –і—А—Г–≥–Є–µ –Ї–∞—А–±–∞–њ–µ–љ–µ–Љ—Л –Љ–Њ–≥—Г—В –њ—А–Њ—П–≤–ї—П—В—М —Б—Е–Њ–і–љ—Л–µ —Д–∞—А–Љ–∞–Ї–Њ–і–Є–љ–∞–Љ–Є—З–µ—Б–Ї–Є–µ —Б–≤–Њ–є—Б—В–≤–∞, –Њ–і–љ–∞–Ї–Њ —Н—В–Њ –љ—Г–ґ–і–∞–µ—В—Б—П –≤ –і–Њ–Ї–∞–Ј–∞—В–µ–ї—М—Б—В–≤–∞—Е, —В–∞–Ї –Ї–∞–Ї –Љ–µ–ґ–і—Г –њ—А–µ–њ–∞—А–∞—В–∞–Љ–Є –Є–Љ–µ—О—В—Б—П —А–∞–Ј–ї–Є—З–Є—П –≤ —В–Њ–Ї—Б–Є—З–љ–Њ—Б—В–Є, —Д–∞—А–Љ–∞–Ї–Њ–Ї–Є–љ–µ—В–Є–Ї–µ –Є –њ–Њ –і—А—Г–≥–Є–Љ –њ–∞—А–∞–Љ–µ—В—А–∞–Љ.
–£–Ї–∞–Ј–∞–љ–љ—Л–µ —А–µ–ґ–Є–Љ—Л –Њ–њ—В–Є–Љ–Є–Ј–∞—Ж–Є–Є –њ—А–Є–Љ–µ–љ–µ–љ–Є—П –Ї–∞—А–±–∞–њ–µ–љ–µ–Љ–Њ–≤, –њ–Њ––≤–Є–і–Є–Љ–Њ–Љ—Г, –љ–µ –Љ–Њ–≥—Г—В –±—Л—В—М –њ—А–Є–Љ–µ–љ–Є–Љ—Л –Ї —Н—А—В–∞–њ–µ–љ–µ–Љ—Г, –њ–Њ—Б–Ї–Њ–ї—М–Ї—Г –Њ–љ —Б—Г—Й–µ—Б—В–≤–µ–љ–љ–Њ –Њ—В–ї–Є—З–∞–µ—В—Б—П –њ–Њ –Њ—Б–љ–Њ–≤–љ—Л–Љ —Д–∞—А–Љ–∞–Ї–Њ–Ї–Є–љ–µ—В–Є—З–µ—Б–Ї–Є–Љ –њ–∞—А–∞–Љ–µ—В—А–∞–Љ (–≤ —З–∞—Б—В–љ–Њ—Б—В–Є, –±–Њ–ї–µ–µ –њ—А–Њ–і–Њ–ї–ґ–Є—В–µ–ї—М–љ—Л–є –њ–µ—А–Є–Њ–і –њ–Њ–ї—Г–≤—Л–≤–µ–і–µ–љ–Є—П).
–Ы–Є—В–µ—А–∞—В—Г—А–∞
1. –°–Є–і–Њ—А–µ–љ–Ї–Њ –°.–Т., –†–µ–Ј–≤–∞–љ –°.–Я., –Х—А–µ–Љ–Є–љ–∞ –Ы.–Т., –Я–Њ–ї–Є–Ї–∞—А–њ–Њ–≤–∞ –°.–Т., –Ъ–∞—А–∞–±–∞–Ї –Т.–Ш., –Ь–µ–љ—М—И–Є–Ї–Њ–≤–∞ –Х.–Ф., –Ґ–Є—И–Ї–Њ–≤ –Т.–Ш., –І–µ—А–Ї–∞—И–Є–љ –Х.–Р., –С–µ–ї–Њ–±–Њ—А–Њ–і–Њ–≤ –Т.–С. –≠—В–Є–Њ–ї–Њ–≥–Є—П —В—П–ґ–µ–ї—Л—Е –≥–Њ—Б–њ–Є—В–∞–ї—М–љ—Л—Е –Є–љ—Д–µ–Ї—Ж–Є–є –≤ –Њ—В–і–µ–ї–µ–љ–Є—П—Е —А–µ–∞–љ–Є–Љ–∞—Ж–Є–Є –Є –∞–љ—В–Є–±–Є–Њ—В–Є–Ї–Њ—А–µ–Ј–Є—Б—В–µ–љ—В–љ–Њ—Б—В—М —Б—А–µ–і–Є –Є—Е –≤–Њ–Ј–±—Г–і–Є—В–µ–ї–µ–є. –Р–љ—В–Є–±–Є–Њ—В–Є–Ї–Є –Є —Е–Є–Љ–Є–Њ—В–µ—А–∞–њ–Є—П, 2005, 50; 2–3: 33–41.
2. Giamarellou H. Prescribing guidelines for severe Pseudomonas infections. J Antimicrob Chemother. 2002; 49:229–233.
3. Jones R.N. Detection of emerging resistance patterns within longitudinal surveillance systems: Data sensitivity and microbial susceptibility. J Antimicrob Chemother. 2000; 46(Suppl B): 1–8.
4. Jones R.N. In vitro evaluation of ertapenem (MK–0826), a long–acting carbapenem, tested against selected resistant strains. J Chemother. 2001; 13:363–376.
5. Mouton J.W., Touzw D.J., Horrevorts A.M., Vinks A.A. Comparative pharmacokinetics of the carbapenems: Clinical implications. Clin Pharmacokinet. 2000;39:185–201.
6. Kollef M.H., Sherman G., Ward S., Fraser V.J. Inadequate antimicrobial treatment of infections: A risk factor for hospital mortality among critically ill patients. Chest. 1999;115:462–474.
7. Kuti J.L., Capitano B., Nicolau D.P. Cost–effective approaches to the treatment of community–acquired pneumonia m the era of resistance. PharmacoEconomics. 2002;20:513–528.
8. Craig W.A. Pharmacokinetic/pharmacodynamic parameters: Rationale for antimicrobial dosing of mice and men. Clin Infect Dis. 1998;26:1–12.
9. Turnidge J.D. The pharmacodynamics of beta–lactams. Clin Infect Dis. 1998;27:10–22.
10. Bustamente C.I., Drusano G.L., Tatem B.A., Standiford H.C. Postantibiotic effect of imipenem on Pseudomonas aeruginosa. Antimicrob Agents Chemother. 1984;26:678–682.
11. Craig W.A., Ebert S.C. Continuous infusion of beta–lactam antibiotics. Antimicrob Agents Chemother. 1992;36: 2577–2583.
12. Mouton J.W., van den Anker J.N. Meropenem clinical pharmacokinetics. Clin Pharmacokinet. 1995;28:275–286.
13. Lomaestro B.M., Rodvold K.A., Danziger L.H. et al. Pharmacodynamic evaluation of extending the infusion time of piperacillin/tazobactam doses using Monte Carlo analysis. In: Program and Abstracts of the 41 ICAAC (Chicago). Washington, DC: American Society for Microbiology; 2001:36. Abstract. 1196.
14. Drusano G.L., Preston S.L., Hardalo C. et al. Use of preclinical data for selection of a phase II/III dose for evernimicin and identification of a preclinical MIC breakpoint. Antimicrob Agents Chemother. 2001;45:13–22.
15. Ambrose P.G., Grasela D.M. The use of Monte Carlo simulation to examine pharmacodynamic variances of drugs: Fluoroquinolone pharmacodynamics against Streptococcus pneumoniae. Diagn Microbiol Infect Dis. 2000;38:151–157.
16. Drusano G.L., Preston S.L., Fowler C. et al. Relationship between fluoroquinolone area under the curve: Minimum inhibitory concentration ratio and the probability of eradication of the infecting pathogen, in patients with nosocomial pneumonia. J Infect Dis. 2004; 189: 1590–1597.
17. Paterson D.L., Clark L., Ndirangu M.W. et al. Use of pharmacodynamic principles and stochastic modeling to choose an optimal empiric cefepime dose for suspected Pseudomonas aeruginosa infections within a single institution. In: Program and Abstracts of the 42nd ICAAC (San Diego). Washington, DC: American Society for Microbiology; 2002:9. Abstract.
18. Kuti J.L., Kotapati S., Nightingale C.H. et al. Evaluation of pharmacodynamic target attainment between healthy subject and patient data using Monte Carlo simulation. In: Program and Abstracts of the 43nd ICAAC (Chicago). Washington, DC: American Society for Microbiology; 2003:2. Abstract.
19. Kuti J.L., Maglio D., Nightingale C.H., Nicolau D.P. Economic benefit of a meropenem dosage strategy based on pharmacodynamic concepts. Am J Health Pharm. 2003;60:565–568.
20. Kotapati S., Nicolau D.P., Nightingale C.H. et al. Clinical and economic benefits of a meropenem dosage strategy based on pharmacodynamic concepts in a large teaching hospital. Am J Health Pharm. 2004;61: 1264–1270.
21. Dandekar P.K., Maglio D., Sutherland C.A. et al. Pharmacokinetics of meropenem 0.5 and 2 g every 8 hours as a 3–hour infusion. Pharmacotherapy. 2003;23:988–991.
22. Jaruratanasirikul S., Sriwiriyajan S. Comparison of the pharmacodynamics of meropenem in healthy volunteers following administration by intermittent infusion or bolus injection. J Antimicrob Chemother. 2003; 52: 518–521.
23. Drusano G.L., Louie A., Miller M.H. et al. Prevention of emergence of resistance in Pseudomonas aerugnosa infections through pharmacodynamic dosing and combination chemotherapy In: Program and Abstracts of the International Conference of the American Thoracic Society (Atlanta). New York: American Thoracic Society; 2002. Abstract.
24. Kuti J.L., Florea N.R., Nightingale C.H., Nicolau D.P. Pharmacodynamics of Meropenem and Imipenem Against Enterobacteriaceae, Acinetobacter baumannii, and Pseudomonas aeruginosa.Pharmacotherapy, 2004; 24(1):8–15.
25. Rhomberg P.R., Jones R.N., for the MYSTIC Program (USA) Study Group. Antimicrobial spectrum of activity for meropenem and nine broad–spectrum antimicrobials: report from the MYSTICProgram (2002) in North America. Diagn Microbiol Infect Dis 2003;47:365–72.
26. Patel G.W., Duquaine S.M., McKinnon P.S. –Ъ–ї–Є–љ–Є—З–µ—Б–Ї–Є–µ —А–µ–Ј—Г–ї—М—В–∞—В—Л –ї–µ—З–µ–љ–Є—П –Є —Б–љ–Є–ґ–µ–љ–Є–µ —Б—В–Њ–Є–Љ–Њ—Б—В–Є —Б –њ–Њ–Љ–Њ—Й—М—О –∞–ї—М—В–µ—А–љ–∞—В–Є–≤–љ—Л—Е —А–µ–ґ–Є–Љ–Њ–≤ –і–Њ–Ј–Є—А–Њ–≤–∞–љ–Є—П –Љ–µ—А–Њ–њ–µ–љ–µ–Љ–∞ –≤ –±–Њ–ї—М–љ–Є—Ж–µ. Pharmacotherapy. 2007;27(12):1637–1643.












