–Ы–µ—З–µ–љ–Є–µ
–Т —Б–Њ–≤—А–µ–Љ–µ–љ–љ—Л—Е —Г—Б–ї–Њ–≤–Є—П—Е –ї–µ—З–µ–љ–Є–µ –Є–љ—Д–µ–Ї—Ж–Є–Њ–љ–љ–Њ–≥–Њ —Н–љ–і–Њ–Ї–∞—А–і–Є—В–∞ (–Ш–≠) –Њ—Б—В–∞–µ—В—Б—П –∞–Ї—В—Г–∞–ї—М–љ–Њ–є –њ—А–Њ–±–ї–µ–Љ–Њ–є, —В—А–µ–±—Г—О—Й–µ–є —Б–∞–Љ–Њ–≥–Њ –њ—А–Є—Б—В–∞–ї—М–љ–Њ–≥–Њ –≤–љ–Є–Љ–∞–љ–Є—П, –Ї–∞–Ї –≤ –љ–∞—Г—З–љ–Њ–Љ, —В–∞–Ї –Є –≤ –њ—А–∞–Ї—В–Є—З–µ—Б–Ї–Њ–Љ –њ–ї–∞–љ–µ. –Э–µ—Б–Љ–Њ—В—А—П –љ–∞ –Њ–±—И–Є—А–љ—Л–є –∞—А—Б–µ–љ–∞–ї –∞–љ—В–Є–Љ–Є–Ї—А–Њ–±–љ—Л—Е —Б—А–µ–і—Б—В–≤, —А–∞–Ј—А–∞–±–Њ—В–∞–љ–љ—Л—Е –Є –≤–љ–µ–і—А–µ–љ–љ—Л—Е –≤ –Ї–ї–Є–љ–Є—З–µ—Б–Ї—Г—О –њ—А–∞–Ї—В–Є–Ї—Г –≤ —В–µ—З–µ–љ–Є–µ –њ–Њ—Б–ї–µ–і–љ–Є—Е 50 –ї–µ—В, –Є –Є–љ—В–µ–љ—Б–Є–≤–љ–Њ–µ —А–∞–Ј–≤–Є—В–Є–µ –Ї–∞—А–і–Є–Њ—Е–Є—А—Г—А–≥–Є–Є, –Ї—Г—А–∞—Ж–Є—П –±–Њ–ї—М–љ–Њ–≥–Њ —Б –Ш–≠ –њ–Њ-–њ—А–µ–ґ–љ–µ–Љ—Г –њ—А–µ–і—Б—В–∞–≤–ї—П–µ—В —Б–Њ–±–Њ–є –і–Њ—Б—В–∞—В–Њ—З–љ–Њ —Б–ї–Њ–ґ–љ—Г—О –Ј–∞–і–∞—З—Г.
–Т —Б–Њ–≤—А–µ–Љ–µ–љ–љ—Л—Е —Г—Б–ї–Њ–≤–Є—П—Е –ї–µ—З–µ–љ–Є–µ –Є–љ—Д–µ–Ї—Ж–Є–Њ–љ–љ–Њ–≥–Њ —Н–љ–і–Њ–Ї–∞—А–і–Є—В–∞ (–Ш–≠) –Њ—Б—В–∞–µ—В—Б—П –∞–Ї—В—Г–∞–ї—М–љ–Њ–є –њ—А–Њ–±–ї–µ–Љ–Њ–є, —В—А–µ–±—Г—О—Й–µ–є —Б–∞–Љ–Њ–≥–Њ –њ—А–Є—Б—В–∞–ї—М–љ–Њ–≥–Њ –≤–љ–Є–Љ–∞–љ–Є—П, –Ї–∞–Ї –≤ –љ–∞—Г—З–љ–Њ–Љ, —В–∞–Ї –Є –≤ –њ—А–∞–Ї—В–Є—З–µ—Б–Ї–Њ–Љ –њ–ї–∞–љ–µ. –Э–µ—Б–Љ–Њ—В—А—П –љ–∞ –Њ–±—И–Є—А–љ—Л–є –∞—А—Б–µ–љ–∞–ї –∞–љ—В–Є–Љ–Є–Ї—А–Њ–±–љ—Л—Е —Б—А–µ–і—Б—В–≤, —А–∞–Ј—А–∞–±–Њ—В–∞–љ–љ—Л—Е –Є –≤–љ–µ–і—А–µ–љ–љ—Л—Е –≤ –Ї–ї–Є–љ–Є—З–µ—Б–Ї—Г—О –њ—А–∞–Ї—В–Є–Ї—Г –≤ —В–µ—З–µ–љ–Є–µ –њ–Њ—Б–ї–µ–і–љ–Є—Е 50 –ї–µ—В, –Є –Є–љ—В–µ–љ—Б–Є–≤–љ–Њ–µ —А–∞–Ј–≤–Є—В–Є–µ –Ї–∞—А–і–Є–Њ—Е–Є—А—Г—А–≥–Є–Є, –Ї—Г—А–∞—Ж–Є—П –±–Њ–ї—М–љ–Њ–≥–Њ —Б –Ш–≠ –њ–Њ-–њ—А–µ–ґ–љ–µ–Љ—Г –њ—А–µ–і—Б—В–∞–≤–ї—П–µ—В —Б–Њ–±–Њ–є –і–Њ—Б—В–∞—В–Њ—З–љ–Њ —Б–ї–Њ–ґ–љ—Г—О –Ј–∞–і–∞—З—Г.–Т–µ–і—Г—Й–Є–є –њ—А–Є–љ—Ж–Є–њ –ї–µ—З–µ–љ–Є—П –Є–љ—Д–µ–Ї—Ж–Є–Њ–љ–љ–Њ–≥–Њ —Н–љ–і–Њ–Ї–∞—А–і–Є—В–∞ - —А–∞–љ–љ—П—П, –Љ–∞—Б—Б–Є–≤–љ–∞—П –Є –і–ї–Є—В–µ–ї—М–љ–∞—П (–љ–µ –Љ–µ–љ–µ–µ 4-6 –љ–µ–і.) –∞–љ—В–Є–±–∞–Ї—В–µ—А–Є–∞–ї—М–љ–∞—П —В–µ—А–∞–њ–Є—П —Б —Г—З–µ—В–Њ–Љ —З—Г–≤—Б—В–≤–Є—В–µ–ї—М–љ–Њ—Б—В–Є –≤—Л–і–µ–ї–µ–љ–љ–Њ–≥–Њ –≤–Њ–Ј–±—Г–і–Є—В–µ–ї—П –Ї –∞–љ—В–Є–±–Є–Њ—В–Є–Ї–∞–Љ. –°–ї–µ–і—Г–µ—В –њ—А–Є–Љ–µ–љ—П—В—М –∞–љ—В–Є–±–Є–Њ—В–Є–Ї–Є, –Њ–Ї–∞–Ј—Л–≤–∞—О—Й–Є–µ –±–∞–Ї—В–µ—А–Є—Ж–Є–і–љ–Њ–µ –і–µ–є—Б—В–≤–Є–µ.
–Т —В–∞–±–ї–Є—Ж–µ 1 –њ—А–µ–і—Б—В–∞–≤–ї–µ–љ—Л –Њ—Б–љ–Њ–≤–љ—Л–µ —Б—Е–µ–Љ—Л –∞–љ—В–Є–±–∞–Ї—В–µ—А–Є–∞–ї—М–љ–Њ–є —В–µ—А–∞–њ–Є–Є –Ш–≠ –≤ –Ј–∞–≤–Є—Б–Є–Љ–Њ—Б—В–Є –Њ—В –љ–∞–Є–±–Њ–ї–µ–µ —З–∞—Б—В–Њ –≤—Л—П–≤–ї—П–µ–Љ—Л—Е –њ–∞—В–Њ–≥–µ–љ–Њ–≤.
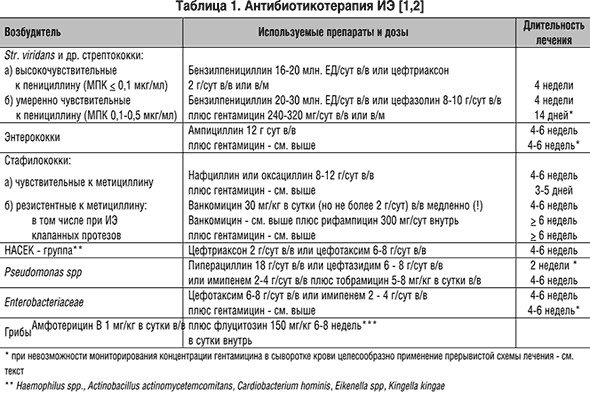
–Ш–Ј–≤–µ—Б—В–љ–Њ, —З—В–Њ –њ–µ–љ–Є—Ж–Є–ї–ї–Є–љ –Є –≥–µ–љ—В–∞–Љ–Є—Ж–Є–љ –Њ–±–ї–∞–і–∞—О—В —Б–Є–љ–µ—А–≥–Є–Ј–Љ–Њ–Љ –±–∞–Ї—В–µ—А–Є—Ж–Є–і–љ–Њ–≥–Њ –і–µ–є—Б—В–≤–Є—П –љ–∞ –Ј–µ–ї–µ–љ—П—Й–Є–µ —Б—В—А–µ–њ—В–Њ–Ї–Њ–Ї–Ї–Є in vitro. –Ю–і–љ–∞–Ї–Њ –њ–Њ –і–∞–љ–љ—Л–Љ –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є—Е –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–є, –њ—А–Є Str. viridans - –Ш–≠ —З–∞—Б—В–Њ—В–∞ –Є–Ј–ї–µ—З–µ–љ–Є—П, –і–Њ—Б—В–Є–≥–љ—Г—В–Њ–≥–Њ –њ—А–Є –Ї–Њ–Љ–±–Є–љ–Є—А–Њ–≤–∞–љ–љ–Њ–Љ –њ—А–Є–Љ–µ–љ–µ–љ–Є–Є –њ–µ–љ–Є—Ж–Є–ї–ї–Є–љ–∞ –Є –≥–µ–љ—В–∞–Љ–Є—Ж–Є–љ–∞, –љ–µ –њ—А–µ–≤–Њ—Б—Е–Њ–і–Є–ї–∞ —В–∞–Ї–Њ–≤—Г—О –њ—А–Є 4-–љ–µ–і–µ–ї—М–љ–Њ–є —В–µ—А–∞–њ–Є–Є –њ–µ–љ–Є—Ж–Є–ї–ї–Є–љ–Њ–Љ –Є–ї–Є —Ж–µ—Д—В—А–Є–∞–Ї—Б–Њ–љ–Њ–Љ [1].
–Т –Ї–∞—З–µ—Б—В–≤–µ –∞–ї—М—В–µ—А–љ–∞—В–Є–≤—Л 4-–љ–µ–і–µ–ї—М–љ–Њ–Љ—Г –Ї—Г—А—Б—Г –Љ–Њ–ґ–µ—В —А–∞—Б—Б–Љ–∞—В—А–Є–≤–∞—В—М—Б—П 2-–љ–µ–і–µ–ї—М–љ–Њ–µ –Ї–Њ–Љ–±–Є–љ–Є—А–Њ–≤–∞–љ–љ–Њ–µ –ї–µ—З–µ–љ–Є–µ –њ–µ–љ–Є—Ж–Є–ї–ї–Є–љ–Њ–Љ –Є –≥–µ–љ—В–∞–Љ–Є—Ж–Є–љ–Њ–Љ –ї–Є–±–Њ —Ж–µ—Д—В—А–Є–∞–Ї—Б–Њ–љ–Њ–Љ –Є –љ–µ—В–Є–ї–Љ–Є—Ж–Є–љ–Њ–Љ [4]. –Т —В–Њ –ґ–µ –≤—А–µ–Љ—П –њ—А–Є–Љ–µ–љ–µ–љ–Є–µ —Г–Ї–∞–Ј–∞–љ–љ—Л—Е –Ї—Г—А—Б–Њ–≤ –ї–µ—З–µ–љ–Є—П –Њ–њ—А–∞–≤–і–∞–љ–Њ —В–Њ–ї—М–Ї–Њ —Г –±–Њ–ї—М–љ—Л—Е –Љ–Њ–ї–Њ–ґ–µ 65 –ї–µ—В —Б –Њ–њ—А–µ–і–µ–ї–µ–љ–љ—Л–Љ –і–Є–∞–≥–љ–Њ–Ј–Њ–Љ –Ш–≠, –≤—Л–Ј–≤–∞–љ–љ–Њ–≥–Њ –≤—Л—Б–Њ–Ї–Њ—З—Г–≤—Б—В–≤–Є—В–µ–ї—М–љ—Л–Љ–Є –Ї –њ–µ–љ–Є—Ж–Є–ї–ї–Є–љ—Г —Б—В—А–µ–њ—В–Њ–Ї–Њ–Ї–Ї–Њ–≤—Л–Љ–Є —И—В–∞–Љ–Љ–∞–Љ–Є (–Ь–Я–Ъ < 0,1 –Љ–Ї–≥/–Љ–ї), –њ—А–Њ—В–µ–Ї–∞—О—Й–µ–≥–Њ —Б –њ–Њ—А–∞–ґ–µ–љ–Є–µ–Љ –љ–∞—В–Є–≤–љ–Њ–≥–Њ (–µ—Б—В–µ—Б—В–≤–µ–љ–љ–Њ–≥–Њ) –Ї–ї–∞–њ–∞–љ–∞ —Б–µ—А–і—Ж–∞ –Є –±–µ–Ј –Њ—Б–ї–Њ–ґ–љ–µ–љ–Є–є (–≤–љ—Г—В—А–Є—Б–µ—А–і–µ—З–љ—Л–є –∞–±—Б—Ж–µ—Б—Б, —Н–Ї—Б—В—А–∞–Ї–∞—А–і–Є–∞–ї—М–љ—Л–µ –Њ—З–∞–≥–Є –Є–љ—Д–µ–Ї—Ж–Є–Є, —Б–µ—А–і–µ—З–љ–∞—П –љ–µ–і–Њ—Б—В–∞—В–Њ—З–љ–Њ—Б—В—М, —В—А–Њ–Љ–±–Њ—Н–Љ–±–Њ–ї–Є—З–µ—Б–Ї–Є–µ —Д–µ–љ–Њ–Љ–µ–љ—Л), –њ—А–Є —Б–Њ—Е—А–∞–љ–љ–Њ–є —Д—Г–љ–Ї—Ж–Є–Є –њ–Њ—З–µ–Ї –Є VIII –њ–∞—А—Л —З–µ—А–µ–њ–љ–Њ-–Љ–Њ–Ј–≥–Њ–≤—Л—Е –љ–µ—А–≤–Њ–≤, –∞ —В–∞–Ї–ґ–µ –≤—Л—А–∞–ґ–µ–љ–љ–Њ–є –њ–Њ–ї–Њ–ґ–Є—В–µ–ї—М–љ–Њ–є –і–Є–љ–∞–Љ–Є–Ї–µ –њ–Њ—Б–ї–µ 7 –і–љ–µ–є –ї–µ—З–µ–љ–Є—П.
–Ъ–Њ–Љ–±–Є–љ–Є—А–Њ–≤–∞–љ–љ–∞—П —В–µ—А–∞–њ–Є—П —В–∞–Ї–ґ–µ –њ—А–Њ–≤–Њ–і–Є—В—Б—П –≤ —Б–ї—Г—З–∞—П—Е –Ш–≠, –≤—Л–Ј–≤–∞–љ–љ–Њ–≥–Њ —Б—В—А–µ–њ—В–Њ–Ї–Њ–Ї–Ї–∞–Љ–Є, —Г–Љ–µ—А–µ–љ–љ–Њ —З—Г–≤—Б—В–≤–Є—В–µ–ї—М–љ—Л–Љ–Є –Ї –њ–µ–љ–Є—Ж–Є–ї–ї–Є–љ—Г. –Я—А–Є —Н—В–Њ–Љ —Ж–µ–ї–µ—Б–Њ–Њ–±—А–∞–Ј–љ–Њ –њ–Њ–≤—Л—Б–Є—В—М —Б—Г—В–Њ—З–љ—Г—О –і–Њ–Ј—Г –њ–µ–љ–Є—Ж–Є–ї–ї–Є–љ–∞ –і–Њ 30 –Љ–ї–љ. –Х–Ф. –Я—А–Є –љ–µ–њ–µ—А–µ–љ–Њ—Б–Є–Љ–Њ—Б—В–Є –њ–µ–љ–Є—Ж–Є–ї–ї–Є–љ–∞ –њ—А–Є–Љ–µ–љ—П—О—В —Ж–µ—Д–∞–ї–Њ—Б–њ–Њ—А–Є–љ—Л I (—Ж–µ—Д–∞–Ј–Њ–ї–Є–љ) –Є–ї–Є III (—Ж–µ—Д—В—А–Є–∞–Ї—Б–Њ–љ) –њ–Њ–Ї–Њ–ї–µ–љ–Є—П. –°–ї–µ–і—Г–µ—В –њ–Њ–Љ–љ–Є—В—М –Њ –≤–Њ–Ј–Љ–Њ–ґ–љ–Њ—Б—В–Є –њ–µ—А–µ–Ї—А–µ—Б—В–љ—Л—Е –∞–ї–ї–µ—А–≥–Є—З–µ—Б–Ї–Є—Е —А–µ–∞–Ї—Ж–Є–є –љ–∞ –њ–µ–љ–Є—Ж–Є–ї–ї–Є–љ—Л –Є —Ж–µ—Д–∞–ї–Њ—Б–њ–Њ—А–Є–љ—Л, –Ї–Њ—В–Њ—А—Л–µ, –њ–Њ –і–∞–љ–љ—Л–Љ —А–∞–Ј–љ—Л—Е –∞–≤—В–Њ—А–Њ–≤, –≤—Б—В—А–µ—З–∞—О—В—Б—П –≤ 10-15% —Б–ї—Г—З–∞–µ–≤. –Я–Њ—Н—В–Њ–Љ—Г —Г –±–Њ–ї—М–љ—Л—Е —Б –∞–љ–∞–Љ–љ–µ—Б—В–Є—З–µ—Б–Ї–Є–Љ–Є —Г–Ї–∞–Ј–∞–љ–Є—П–Љ–Є –љ–∞ –љ–µ–њ–µ—А–µ–љ–Њ—Б–Є–Љ–Њ—Б—В—М –њ–µ–љ–Є—Ж–Є–ї–ї–Є–љ–∞ —А–µ–Ї–Њ–Љ–µ–љ–і—Г–µ—В—Б—П –љ–∞–Ј–љ–∞—З–∞—В—М —Ж–µ—Д–∞–ї–Њ—Б–њ–Њ—А–Є–љ—Л —В–Њ–ї—М–Ї–Њ –њ–Њ—Б–ї–µ –њ—А–Њ–≤–µ–і–µ–љ–Є—П —Б–Њ–Њ—В–≤–µ—В—Б—В–≤—Г—О—Й–Є—Е –Ї–Њ–ґ–љ—Л—Е —В–µ—Б—В–Њ–≤. –Ъ–Њ–Љ–±–Є–љ–Є—А–Њ–≤–∞–љ–љ–∞—П —В–µ—А–∞–њ–Є—П –і–≤—Г–Љ—П –њ—А–µ–њ–∞—А–∞—В–∞–Љ–Є —В–∞–Ї–ґ–µ –њ—А–Њ–≤–Њ–і–Є—В—Б—П —Г –±–Њ–ї—М–љ—Л—Е Str. viridans-–Ш–≠ –Ї–ї–∞–њ–∞–љ–љ—Л—Е –њ—А–Њ—В–µ–Ј–Њ–≤, –њ—А–Є —Н—В–Њ–Љ –ї–µ—З–µ–љ–Є–µ –њ–µ–љ–Є—Ж–Є–ї–ї–Є–љ–Њ–Љ –Є–ї–Є —Ж–µ—Д–∞–ї–Њ—Б–њ–Њ—А–Є–љ–∞–Љ–Є —Б–Њ—З–µ—В–∞—О—В —Б –≥–µ–љ—В–∞–Љ–Є—Ж–Є–љ–Њ–Љ, –Ї–Њ—В–Њ—А—Л–є —Б–ї–µ–і—Г–µ—В –њ—А–Є–Љ–µ–љ—П—В—М –≤ —В–µ—З–µ–љ–Є–µ, –Ї–∞–Ї –Љ–Є–љ–Є–Љ—Г–Љ, 2 –љ–µ–і–µ–ї—М. –Э–µ–Њ–±—Е–Њ–і–Є–Љ–Њ –Њ—В–Љ–µ—В–Є—В—М, —З—В–Њ –і–ї–Є—В–µ–ї—М–љ–Њ–µ –њ—А–Є–Љ–µ–љ–µ–љ–Є–µ –∞–Љ–Є–љ–Њ–≥–ї–Є–Ї–Њ–Ј–Є–і–Њ–≤, –≤ —З–∞—Б—В–љ–Њ—Б—В–Є, –≥–µ–љ—В–∞–Љ–Є—Ж–Є–љ–∞ –≤ –≤—Л—Б–Њ–Ї–Є—Е –і–Њ–Ј–∞—Е –љ–µ—А–µ–і–Ї–Њ —Б–Њ–њ—А–Њ–≤–Њ–ґ–і–∞–µ—В—Б—П –Њ—В–Њ- –Є –љ–µ—Д—А–Њ—В–Њ–Ї—Б–Є—З–µ—Б–Ї–Є–Љ —Н—Д—Д–µ–Ї—В–Њ–Љ, –Њ—Б–Њ–±–µ–љ–љ–Њ —Г –њ–Њ–ґ–Є–ї—Л—Е –±–Њ–ї—М–љ—Л—Е. –° —Ж–µ–ї—М—О –њ—А–µ–і—Г–њ—А–µ–ґ–і–µ–љ–Є—П —В–Њ–Ї—Б–Є—З–µ—Б–Ї–Њ–≥–Њ –і–µ–є—Б—В–≤–Є—П –љ–µ–Њ–±—Е–Њ–і–Є–Љ–Њ –Љ–Њ–љ–Є—В–Њ—А–Є—А–Њ–≤–∞–љ–Є–µ –Ї–Њ–љ—Ж–µ–љ—В—А–∞—Ж–Є–Є —Н—В–Є—Е –њ—А–µ–њ–∞—А–∞—В–Њ–≤ –≤ —Б—Л–≤–Њ—А–Њ—В–Ї–µ –Ї—А–Њ–≤–Є. –Ю–і–љ–∞–Ї–Њ —Б–Њ–±–ї—О–і–µ–љ–Є–µ —Н—В–Њ–≥–Њ —В—А–µ–±–Њ–≤–∞–љ–Є—П –љ–µ –≤—Б–µ–≥–і–∞ –≤–Њ–Ј–Љ–Њ–ґ–љ–Њ –≤ —Г—Б–ї–Њ–≤–Є—П—Е —А–Њ—Б—Б–Є–є—Б–Ї–Є—Е —Б—В–∞—Ж–Є–Њ–љ–∞—А–Њ–≤ –Њ–±—Й–µ–≥–Њ –њ—А–Њ—Д–Є–ї—П, —Г—З–Є—В—Л–≤–∞—П –Є—Е –љ–µ–і–Њ—Б—В–∞—В–Њ—З–љ—Г—О —В–µ—Е–љ–Є—З–µ—Б–Ї—Г—О –Њ—Б–љ–∞—Й–µ–љ–љ–Њ—Б—В—М. –Я–Њ—Н—В–Њ–Љ—Г —Б –њ—А–∞–Ї—В–Є—З–µ—Б–Ї–Њ–є —В–Њ—З–Ї–Є –Ј—А–µ–љ–Є—П –Љ–Њ–ґ–µ—В –±—Л—В—М –Њ–њ—А–∞–≤–і–∞–љ–∞ –њ—А–µ—А—Л–≤–Є—Б—В–∞—П —Б—Е–µ–Љ–∞ –њ—А–Є–Љ–µ–љ–µ–љ–Є—П –≥–µ–љ—В–∞–Љ–Є—Ж–Є–љ–∞ –њ—А–Є –Ш–≠. –Я—А–µ–њ–∞—А–∞—В –љ–∞–Ј–љ–∞—З–∞—О—В –≤ —В–µ—З–µ–љ–Є–µ 7-10 –і–љ–µ–є —Б –њ–Њ—Б–ї–µ–і—Г—О—Й–Є–Љ 5-7-–і–љ–µ–≤–љ—Л–Љ –њ–µ—А–µ—А—Л–≤–Њ–Љ —Б —Ж–µ–ї—М—О –њ—А–Њ—Д–Є–ї–∞–Ї—В–Є–Ї–Є —В–Њ–Ї—Б–Є—З–µ—Б–Ї–Є—Е —Н—Д—Д–µ–Ї—В–Њ–≤, –Ј–∞—В–µ–Љ –њ—А–Њ–≤–Њ–і—П—В –њ–Њ–≤—В–Њ—А–љ—Л–µ –Ї—Г—А—Б—Л –≤ —В–µ—Е –ґ–µ –і–Њ–Ј–∞—Е. –Я—А–µ–Є–Љ—Г—Й–µ—Б—В–≤–∞ –Њ–і–љ–Њ–Ї—А–∞—В–љ–Њ–≥–Њ –≤–≤–µ–і–µ–љ–Є—П —Б—Г—В–Њ—З–љ–Њ–є –і–Њ–Ј—Л –∞–Љ–Є–љ–Њ–≥–ї–Є–Ї–Њ–Ј–Є–і–Њ–≤ –њ—А–Є –Ш–≠ —В—А–µ–±—Г—О—В –њ–Њ–і—В–≤–µ—А–ґ–і–µ–љ–Є—П –≤ –і–∞–ї—М–љ–µ–є—И–Є—Е —Н–Ї—Б–њ–µ—А–Є–Љ–µ–љ—В–∞–ї—М–љ—Л—Е –Є –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є—Е –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П—Е.
–Я—А–Є –Ш–≠, –≤—Л–Ј–≤–∞–љ–љ–Њ–Љ —Б—В—А–µ–њ—В–Њ–Ї–Њ–Ї–Ї–Њ–≤—Л–Љ–Є —И—В–∞–Љ–Љ–∞–Љ–Є, —А–µ–Ј–Є—Б—В–µ–љ—В–љ—Л–Љ–Є –Ї –њ–µ–љ–Є—Ж–Є–ї–ї–Є–љ—Г (–Ь–Я–Ъ 0,5 –Љ–Ї–≥/–Љ–ї), –Є–ї–Є –њ—А–Є –љ–µ–њ–µ—А–µ–љ–Њ—Б–Є–Љ–Њ—Б—В–Є b-–ї–∞–Ї—В–∞–Љ–љ—Л—Е –∞–љ—В–Є–±–Є–Њ—В–Є–Ї–Њ–≤ —А–µ–Ї–Њ–Љ–µ–љ–і—Г–µ—В—Б—П –љ–∞–Ј–љ–∞—З–µ–љ–Є–µ –∞–љ—В–Є–Љ–Є–Ї—А–Њ–±–љ–Њ–≥–Њ –њ—А–µ–њ–∞—А–∞—В–∞ –Є–Ј –≥—А—Г–њ–њ—Л –≥–ї–Є–Ї–Њ–њ–µ–њ—В–Є–і–Њ–≤-–≤–∞–љ–Ї–Њ–Љ–Є—Ж–Є–љ–∞. –Э–µ–Њ–±—Е–Њ–і–Є–Љ—Л–Љ —Г—Б–ї–Њ–≤–Є–µ–Љ –µ–≥–Њ –њ—А–Є–Љ–µ–љ–µ–љ–Є—П —П–≤–ї—П–µ—В—Б—П –Љ–µ–і–ї–µ–љ–љ–Њ–µ (–Ї–∞–Ї –Љ–Є–љ–Є–Љ—Г–Љ, –≤ —В–µ—З–µ–љ–Є–µ 1 —З–∞—Б–∞) –≤–љ—Г—В—А–Є–≤–µ–љ–љ–Њ–µ –≤–≤–µ–і–µ–љ–Є–µ —А–∞–Ј–Њ–≤–Њ–є –і–Њ–Ј—Л –≤–Њ –Є–Ј–±–µ–ґ–∞–љ–Є–µ —А–∞–Ј–≤–Є—В–Є—П —Б–≤—П–Ј–∞–љ–љ–Њ–є —Б –≤—Л—Б–≤–Њ–±–Њ–ґ–і–µ–љ–Є–µ–Љ –≥–Є—Б—В–∞–Љ–Є–љ–∞ —Б–њ–µ—Ж–Є—Д–Є—З–µ—Б–Ї–Њ–є —А–µ–∞–Ї—Ж–Є–Є, –Ј–∞–Ї–ї—О—З–∞—О—Й–µ–є—Б—П –≤ –≤—Л—А–∞–ґ–µ–љ–љ–Њ–є –≥–Є–њ–µ—А–µ–Љ–Є–Є –ї–Є—Ж–∞ —И–µ–Є –Є –≤–µ—А—Е–љ–µ–є —З–∞—Б—В–Є —В—Г–ї–Њ–≤–Є—Й–∞ (—Б–Є–љ–і—А–Њ–Љ «–Ї—А–∞—Б–љ–Њ–Ї–Њ–ґ–µ–≥–Њ»). –Ъ —Б–Њ–ґ–∞–ї–µ–љ–Є—О, –њ—А–µ–њ–∞—А–∞—В –і–Њ—Б—В–∞—В–Њ—З–љ–Њ —В–Њ–Ї—Б–Є—З–µ–љ –њ—А–Є –µ–≥–Њ –і–ї–Є—В–µ–ї—М–љ–Њ–Љ –≤–љ—Г—В—А–Є–≤–µ–љ–љ–Њ–Љ –≤–≤–µ–і–µ–љ–Є–Є; –≤–Њ–Ј–Љ–Њ–ґ–љ–Њ —А–∞–Ј–≤–Є—В–Є–µ —В—А–Њ–Љ–±–Њ—Д–ї–µ–±–Є—В–∞, —Б—Л–њ–Є, –ї–Є—Е–Њ—А–∞–і–Ї–Є, –Њ—В–Њ- –Є –љ–µ—Д—А–Њ—В–Њ–Ї—Б–Є—З–µ—Б–Ї–Є—Е —А–µ–∞–Ї—Ж–Є–є.
–Я—А–Њ–±–ї–µ–Љ—Л –ї–µ—З–µ–љ–Є—П —Н–љ—В–µ—А–Њ–Ї–Њ–Ї–Ї–Њ–≤–Њ–≥–Њ –Ш–≠ –Њ–±—Г—Б–ї–Њ–≤–ї–µ–љ—Л —В–µ–Љ, —З—В–Њ –Њ–±–∞ –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є –Ј–љ–∞—З–Є–Љ—Л—Е –њ—А–µ–і—Б—В–∞–≤–Є—В–µ–ї—П –і–∞–љ–љ–Њ–є –≥—А—Г–њ–њ—Л - Enterococcus faecalis –Є Enterococcus faecium, –Ї–∞–Ї –њ—А–∞–≤–Є–ї–Њ, —А–µ–Ј–Є—Б—В–µ–љ—В–љ—Л –Ї —Ж–µ—Д–∞–ї–Њ—Б–њ–Њ—А–Є–љ–∞–Љ, –Њ—В–љ–Њ—Б–Є—В–µ–ї—М–љ–Њ —Г—Б—В–Њ–є—З–Є–≤—Л –Ї –њ–µ–љ–Є—Ж–Є–ї–ї–Є–љ—Г (–Љ–µ–і–Є–∞–љ–∞ –Ь–Я–Ъ = 2 –Љ–Ї–≥/–Љ–ї) –Є –≥–µ–љ—В–∞–Љ–Є—Ж–Є–љ—Г –≤ —Б—В–∞–љ–і–∞—А—В–љ—Л—Е —В–µ—А–∞–њ–µ–≤—В–Є—З–µ—Б–Ї–Є—Е –Ї–Њ–љ—Ж–µ–љ—В—А–∞—Ж–Є—П—Е. –Т –њ–Њ—Б–ї–µ–і–љ–µ–µ –≤—А–µ–Љ—П –Њ—В–Љ–µ—З–∞—О—В —В—А–µ–≤–Њ–ґ–љ—Г—О —В–µ–љ–і–µ–љ—Ж–Є—О –Ї –љ–∞—А–∞—Б—В–∞–љ–Є—О —З–∞—Б—В–Њ—В—Л –≤–∞–љ–Ї–Њ–Љ–Є—Ж–Є–љ-—А–µ–Ј–Є—Б—В–µ–љ—В–љ—Л—Е —Н–љ—В–µ—А–Њ–Ї–Њ–Ї–Ї–Њ–≤—Л—Е —И—В–∞–Љ–Љ–Њ–≤, –≤ —В.—З. —Б—А–µ–і–Є –±–Њ–ї—М–љ—Л—Е –Ш–≠ [6, 7]. –Т —Б–≤—П–Ј–Є —Б —Н—В–Є–Љ –ї–µ—З–µ–љ–Є–µ —Н–љ—В–µ—А–Њ–Ї–Њ–Ї–Ї–Њ–≤–Њ–≥–Њ –Ш–≠ —А–µ–Ї–Њ–Љ–µ–љ–і—Г–µ—В—Б—П –љ–∞—З–Є–љ–∞—В—М —В–Њ–ї—М–Ї–Њ –њ–Њ—Б–ї–µ –Њ–њ—А–µ–і–µ–ї–µ–љ–Є—П —З—Г–≤—Б—В–≤–Є—В–µ–ї—М–љ–Њ—Б—В–Є –≤—Л–і–µ–ї–µ–љ–љ–Њ–≥–Њ –≤–Њ–Ј–±—Г–і–Є—В–µ–ї—П –Ї –∞–љ—В–Є–±–Є–Њ—В–Є–Ї–∞–Љ. –°—В–∞–љ–і–∞—А—В–љ—Л–µ —Б—Е–µ–Љ—Л —В–µ—А–∞–њ–Є–Є –≤–Ї–ї—О—З–∞—О—В –њ—А–Є–Љ–µ–љ–µ–љ–Є–µ –њ–µ–љ–Є—Ж–Є–ї–ї–Є–љ–∞ –≤ –≤—Л—Б–Њ–Ї–Є—Е –і–Њ–Ј–∞—Е (30 –Љ–ї–љ. –Х–Ф –≤ —Б—Г—В–Ї–Є –≤ 6 –≤–≤–µ–і–µ–љ–Є—П—Е) –Є–ї–Є –∞–Љ–њ–Є—Ж–Є–ї–ї–Є–љ–∞ –Є–ї–Є –≤–∞–љ–Ї–Њ–Љ–Є—Ж–Є–љ–∞ –≤ —Б–Њ—З–µ—В–∞–љ–Є–Є —Б –≥–µ–љ—В–∞–Љ–Є—Ж–Є–љ–Њ–Љ –Є–ї–Є –і—А—Г–≥–Є–Љ–Є –∞–Љ–Є–љ–Њ–≥–ї–Є–Ї–Њ–Ј–Є–і–∞–Љ–Є. –Ы–µ—З–µ–љ–Є–µ –њ—А–Њ–≤–Њ–і—П—В, –њ–Њ –Љ–µ–љ—М—И–µ–є –Љ–µ—А–µ, 4 –љ–µ–і–µ–ї–Є. –Т —В–µ—Е —Б–ї—Г—З–∞—П—Е, –Ї–Њ–≥–і–∞ —Б–Є–Љ–њ—В–Њ–Љ–∞—В–Є–Ї–∞ –Ш–≠ –і–ї–Є—В—Б—П –±–Њ–ї–µ–µ 3 –Љ–µ—Б., –∞ —В–∞–Ї–ґ–µ –њ—А–Є –Ш–≠ –Ї–ї–∞–њ–∞–љ–љ—Л—Е –њ—А–Њ—В–µ–Ј–Њ–≤ –і–ї–Є—В–µ–ї—М–љ–Њ—Б—В—М –Ї–Њ–Љ–±–Є–љ–Є—А–Њ–≤–∞–љ–љ–Њ–є —В–µ—А–∞–њ–Є–Є –і–Њ–ї–ґ–љ–∞ —Б–Њ—Б—В–∞–≤–ї—П—В—М –љ–µ –Љ–µ–љ–µ–µ 6 –љ–µ–і–µ–ї—М.
–С–Њ–ї—М—И–Є–љ—Б—В–≤–Њ —Б—В–∞—Д–Є–ї–Њ–Ї–Њ–Ї–Ї–Њ–≤ (–Ї–∞–Ї –≤–љ–µ–±–Њ–ї—М–љ–Є—З–љ—Л—Е, —В–∞–Ї –Є –≥–Њ—Б–њ–Є—В–∞–ї—М–љ—Л—Е) –њ—А–Њ–і—Г—Ж–Є—А—Г—О—В b-–ї–∞–Ї—В–∞–Љ–∞–Ј—Л –Є —П–≤–ї—П—О—В—Б—П —А–µ–Ј–Є—Б—В–µ–љ—В–љ—Л–Љ–Є –Ї –њ–µ–љ–Є—Ж–Є–ї–ї–Є–љ—Г. –Я–Њ—Н—В–Њ–Љ—Г –њ—А–µ–њ–∞—А–∞—В–∞–Љ–Є –≤—Л–±–Њ—А–∞ –і–ї—П –ї–µ—З–µ–љ–Є—П –Ш–≠, –≤—Л–Ј–≤–∞–љ–љ–Њ–≥–Њ –Љ–µ—В–Є—Ж–Є–ї–ї–Є–љ—З—Г–≤—Б—В–≤–Є—В–µ–ї—М–љ—Л–Љ–Є —И—В–∞–Љ–Љ–∞–Љ–Є —Б—В–∞—Д–Є–ї–Њ–Ї–Њ–Ї–Ї–Њ–≤, —П–≤–ї—П—О—В—Б—П —Г—Б—В–Њ–є—З–Є–≤—Л–µ –Ї —Д–µ—А–Љ–µ–љ—В–∞—В–Є–≤–љ–Њ–Љ—Г –≥–Є–і—А–Њ–ї–Є–Ј—Г –њ–Њ–ї—Г—Б–Є–љ—В–µ—В–Є—З–µ—Б–Ї–Є–µ –њ–µ–љ–Є—Ж–Є–ї–ї–Є–љ—Л (–Њ–Ї—Б–∞—Ж–Є–ї–ї–Є–љ), –љ–∞–Ј–љ–∞—З–∞–µ–Љ—Л–µ –≤ —В–µ—З–µ–љ–Є–µ 4-6 –љ–µ–і–µ–ї—М. –£—З–Є—В—Л–≤–∞—П –±–Њ–ї–µ–µ –±—Л—Б—В—А—Г—О –ї–Є–Ї–≤–Є–і–∞—Ж–Є—О –±–∞–Ї—В–µ—А–Є–µ–Љ–Є–Є –њ—А–Є –Ї–Њ–Љ–±–Є–љ–Є—А–Њ–≤–∞–љ–љ–Њ–є —В–µ—А–∞–њ–Є–Є, –њ—А–Є–Ј–љ–∞–љ–Њ —Ж–µ–ї–µ—Б–Њ–Њ–±—А–∞–Ј–љ—Л–Љ –њ—А–Є–Љ–µ–љ—П—В—М –≥–µ–љ—В–∞–Љ–Є—Ж–Є–љ —В–Њ–ї—М–Ї–Њ –≤ —В–µ—З–µ–љ–Є–µ –њ–µ—А–≤—Л—Е 3-5 –і–љ–µ–є —Б —Ж–µ–ї—М—О –Љ–Є–љ–Є–Љ–Є–Ј–∞—Ж–Є–Є –њ–Њ–≤—А–µ–ґ–і–µ–љ–Є—П –Ї–ї–∞–њ–∞–љ–Њ–≤ —Б–µ—А–і—Ж–∞ –Є –њ—А–µ–і—Г–њ—А–µ–ґ–і–µ–љ–Є—П —Д–Њ—А–Љ–Є—А–Њ–≤–∞–љ–Є—П —Н–Ї—Б—В—А–∞–Ї–∞—А–і–Є–∞–ї—М–љ—Л—Е –∞–±—Б—Ж–µ—Б—Б–Њ–≤. –Ф–∞–љ–љ–∞—П —Б—Е–µ–Љ–∞ —В–∞–Ї–ґ–µ –њ–Њ–Ј–≤–Њ–ї—П–µ—В —Г–Љ–µ–љ—М—И–Є—В—М —А–Є—Б–Ї —А–∞–Ј–≤–Є—В–Є—П –≥–µ–љ—В–∞–Љ–Є—Ж–Є–љ - –Њ–њ–Њ—Б—А–µ–і–Њ–≤–∞–љ–љ—Л—Е —В–Њ–Ї—Б–Є—З–µ—Б–Ї–Є—Е —А–µ–∞–Ї—Ж–Є–є. –Т –Ї–∞—З–µ—Б—В–≤–µ –∞–ї—М—В–µ—А–љ–∞—В–Є–≤—Л –њ–Њ–ї—Г—Б–Є–љ—В–µ—В–Є—З–µ—Б–Ї–Є–Љ –њ–µ–љ–Є—Ж–Є–ї–ї–Є–љ–∞–Љ —А–∞—Б—Б–Љ–∞—В—А–Є–≤–∞—О—В—Б—П —Ж–µ—Д–∞–ї–Њ—Б–њ–Њ—А–Є–љ—Л I –њ–Њ–Ї–Њ–ї–µ–љ–Є—П (—Ж–µ—Д–∞–Ј–Њ–ї–Є–љ). –Я–Њ—Б–Ї–Њ–ї—М–Ї—Г –≤–∞–љ–Ї–Њ–Љ–Є—Ж–Є–љ –Љ–Њ–ґ–µ—В —Г—Б—В—Г–њ–∞—В—М –Њ–Ї—Б–∞—Ж–Є–ї–ї–Є–љ—Г –≤ –∞–Ї—В–Є–≤–љ–Њ—Б—В–Є –њ–Њ –Њ—В–љ–Њ—И–µ–љ–Є—О –Ї –Љ–µ—В–Є—Ж–Є–ї–ї–Є–љ—З—Г–≤—Б—В–≤–Є—В–µ–ї—М–љ—Л–Љ —И—В–∞–Љ–Љ–∞–Љ –Ј–Њ–ї–Њ—В–Є—Б—В–Њ–≥–Њ —Б—В–∞—Д–Є–ї–Њ–Ї–Њ–Ї–Ї–∞, –Њ–љ —Б—З–Є—В–∞–µ—В—Б—П –њ—А–µ–њ–∞—А–∞—В–Њ–Љ —А–µ–Ј–µ—А–≤–∞ –Є –љ–∞–Ј–љ–∞—З–∞–µ—В—Б—П –њ—А–Є –∞–ї–ї–µ—А–≥–Є–Є –Ї b-–ї–∞–Ї—В–∞–Љ–љ—Л–Љ –∞–љ—В–Є–±–Є–Њ—В–Є–Ї–∞–Љ.
–Я—А–µ–і—Б—В–∞–≤–ї—П—О—В –Є–љ—В–µ—А–µ—Б –і–∞–љ–љ—Л–µ –Њ –≤–Њ–Ј–Љ–Њ–ґ–љ–Њ—Б—В–Є –Ї—А–∞—В–Ї–Њ—Б—А–Њ—З–љ–Њ–≥–Њ –Ї—Г—А—Б–∞ –ї–µ—З–µ–љ–Є—П –њ—А–∞–≤–Њ—Б–µ—А–і–µ—З–љ–Њ–≥–Њ –Ш–≠ –љ–∞—А–Ї–Њ–Љ–∞–љ–Њ–≤, –Њ–±—Г—Б–ї–Њ–≤–ї–µ–љ–љ–Њ–≥–Њ –Љ–µ—В–Є—Ж–Є–ї–ї–Є–љ—З—Г–≤—Б—В–≤–Є—В–µ–ї—М–љ—Л–Љ–Є —И—В–∞–Љ–Љ–∞–Љ–Є S. aureus. –Я—А–Є–Љ–µ–љ–µ–љ–Є–µ –Ї–Њ–Љ–±–Є–љ–Є—А–Њ–≤–∞–љ–љ–Њ–є —В–µ—А–∞–њ–Є–Є –Њ–Ї—Б–∞—Ж–Є–ї–ї–Є–љ–Њ–Љ (1,5 –≥ –≤/–≤ 6 —А–∞–Ј –≤ —Б—Г—В–Ї–Є) –Є —В–Њ–±—А–∞–Љ–Є—Ж–Є–љ–Њ–Љ (1 –Љ–≥/–Ї–≥ –≤/–≤ —В—А–Є–ґ–і—Л –≤ —Б—Г—В–Ї–Є) –≤ —В–µ—З–µ–љ–Є–µ 2 –љ–µ–і–µ–ї—М —Г —Г–њ–Њ–Љ—П–љ—Г—В–Њ–≥–Њ –Ї–Њ–љ—В–Є–љ–≥–µ–љ—В–∞ –±–Њ–ї—М–љ—Л—Е –њ–Њ–Ј–≤–Њ–ї–Є–ї–Њ –і–Њ–±–Є—В—М—Б—П –Є–Ј–ї–µ—З–µ–љ–Є—П –≤ 94% —Б–ї—Г—З–∞–µ–≤ [8]. –Я—А–µ–і–њ—А–Є–љ—П—В–∞—П –≤ —Е–Њ–і–µ —Н—В–Њ–≥–Њ –ґ–µ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П –њ–Њ–њ—Л—В–Ї–∞ –Ј–∞–Љ–µ–љ—Л –Њ–Ї—Б–∞—Ж–Є–ї–ї–Є–љ–∞ –љ–∞ –≤–∞–љ–Ї–Њ–Љ–Є—Ж–Є–љ —Г—Б–њ–µ—Е–∞ –љ–µ –Є–Љ–µ–ї–∞. –Э–µ–Њ–±—Е–Њ–і–Є–Љ—Л –і–∞–ї—М–љ–µ–є—И–Є–µ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П –њ–Њ –Є–Ј—Г—З–µ–љ–Є—О –≤–Њ–Ј–Љ–Њ–ґ–љ–Њ—Б—В–µ–є –њ—А–Є–Љ–µ–љ–µ–љ–Є—П –і–∞–љ–љ–Њ–є —Б—Е–µ–Љ—Л —Г –±–Њ–ї—М–љ—Л—Е –њ—А–∞–≤–Њ—Б–µ—А–і–µ—З–љ—Л–Љ St. aureus-–Ш–≠ —Б –љ–∞–ї–Є—З–Є–µ–Љ –≤–Є–Ј—Г–∞–ї–Є–Ј–Є—А—Г–µ–Љ—Л—Е —Б –њ–Њ–Љ–Њ—Й—М—О —Н—Е–Њ–Ї–∞—А–і–Є–Њ–≥—А–∞—Д–Є–Є –Ї—А—Г–њ–љ—Л—Е (–±–Њ–ї–µ–µ 1 —Б–Љ) –≤–µ–≥–µ—В–∞—Ж–Є–є –љ–∞ —В—А–Є–Ї—Г—Б–њ–Є–і–∞–ї—М–љ–Њ–Љ –Ї–ї–∞–њ–∞–љ–µ, –∞ —В–∞–Ї–ґ–µ –њ—А–Є —З–∞—Б—В–Њ –≤—Б—В—А–µ—З–∞—О—Й–Є—Е—Б—П —Б–µ–њ—В–Є—З–µ—Б–Ї–Є—Е –Є —Н–Љ–±–Њ–ї–Є—З–µ—Б–Ї–Є—Е –Њ—Б–ї–Њ–ґ–љ–µ–љ–Є—П—Е —Б–Њ —Б—В–Њ—А–Њ–љ—Л –ї–µ–≥–Ї–Є—Е (—Н–Љ–њ–Є–µ–Љ–∞, –∞–±—Б—Ж–µ—Б—Б, –Љ–љ–Њ–ґ–µ—Б—В–≤–µ–љ–љ—Л–µ –Є–љ—Д–∞—А–Ї—В—Л –Є —В.–і.).
–Т –њ–Њ—Б–ї–µ–і–љ–µ–µ –≤—А–µ–Љ—П –љ–∞–±–ї—О–і–∞–µ—В—Б—П —А–Њ—Б—В —З–Є—Б–ї–∞ –Љ–µ—В–Є—Ж–Є–ї–ї–Є–љ—А–µ–Ј–Є—Б—В–µ–љ—В–љ—Л—Е —И—В–∞–Љ–Љ–Њ–≤ —Б—В–∞—Д–Є–ї–Њ–Ї–Њ–Ї–Ї–Њ–≤ (–Њ—Б–Њ–±–µ–љ–љ–Њ –Ї–Њ–∞–≥—Г–ї–∞–Ј–Њ–љ–µ–≥–∞—В–Є–≤–љ—Л—Е), —Г—Б—В–Њ–є—З–Є–≤—Л—Е –Ї–Њ –≤—Б–µ–Љ –ї–∞–Ї—В–∞–Љ–љ—Л–Љ –∞–љ—В–Є–±–Є–Њ—В–Є–Ї–∞–Љ. –Э–∞–Є–±–Њ–ї–µ–µ —З–∞—Б—В–Њ –Њ–љ–Є –≤—Л—П–≤–ї—П—О—В—Б—П –њ—А–Є –Ш–≠ —Г –љ–∞—А–Ї–Њ–Љ–∞–љ–Њ–≤, –∞ —В–∞–Ї–ґ–µ –њ—А–Є –љ–Њ–Ј–Њ–Ї–Њ–Љ–Є–∞–ї—М–љ–Њ–Љ (–≥–Њ—Б–њ–Є—В–∞–ї—М–љ–Њ–Љ) —Н–љ–і–Њ–Ї–∞—А–і–Є—В–µ. –Т –њ–Њ–і–Њ–±–љ—Л—Е —Б–Є—В—Г–∞—Ж–Є—П—Е –њ–Њ–Ї–∞–Ј–∞–љ–Њ –љ–∞–Ј–љ–∞—З–µ–љ–Є–µ –≤–∞–љ–Ї–Њ–Љ–Є—Ж–Є–љ–∞. –Я—А–Є –Њ—В—Б—Г—В—Б—В–≤–Є–Є –Њ—В–≤–µ—В–∞ –љ–∞ –Љ–Њ–љ–Њ—В–µ—А–∞–њ–Є—О –≤–∞–љ–Ї–Њ–Љ–Є—Ж–Є–љ–Њ–Љ –Љ–Њ–ґ–µ—В –±—Л—В—М –њ–Њ–ї–µ–Ј–љ—Л–Љ –µ–≥–Њ —Б–Њ—З–µ—В–∞–љ–Є–µ —Б —А–Є—Д–∞–Љ–њ–Є—Ж–Є–љ–Њ–Љ –Є/–Є–ї–Є –∞–Љ–Є–љ–Њ–≥–ї–Є–Ї–Њ–Ј–Є–і–∞–Љ–Є. –°–Њ–Њ–±—Й–∞—О—В –Њ–± —Г—Б–њ–µ—И–љ–Њ–Љ –њ—А–Є–Љ–µ–љ–µ–љ–Є–Є –Ї–Њ–Љ–±–Є–љ–∞—Ж–Є–Є —Ж–Є–њ—А–Њ—Д–ї–Њ–Ї—Б–∞—Ж–Є–љ–∞ —Б —А–Є—Д–∞–Љ–њ–Є—Ж–Є–љ–Њ–Љ —Г –і–∞–љ–љ–Њ–є –Ї–∞—В–µ–≥–Њ—А–Є–Є –±–Њ–ї—М–љ—Л—Е [9], –Њ–і–љ–∞–Ї–Њ –Є–Ј-–Ј–∞ –Љ–∞–ї–Њ–≥–Њ —З–Є—Б–ї–∞ –љ–∞–±–ї—О–і–µ–љ–Є–є –і–∞—В—М –Ї–∞–Ї–Є–µ-–ї–Є–±–Њ –Ї–Њ–љ–Ї—А–µ—В–љ—Л–µ —В–µ—А–∞–њ–µ–≤—В–Є—З–µ—Б–Ї–Є–µ —А–µ–Ї–Њ–Љ–µ–љ–і–∞—Ж–Є–Є –љ–µ –њ—А–µ–і—Б—В–∞–≤–ї—П–µ—В—Б—П –≤–Њ–Ј–Љ–Њ–ґ–љ—Л–Љ.
–Э–µ—Б–Ї–Њ–ї—М–Ї–Њ –Њ—В–ї–Є—З–∞–µ—В—Б—П –Њ—В –≤—Л—И–µ–Є–Ј–ї–Њ–ґ–µ–љ–љ–Њ–є —В–µ—А–∞–њ–µ–≤—В–Є—З–µ—Б–Ї–∞—П —В–∞–Ї—В–Є–Ї–∞ –њ—А–Є —Б—В–∞—Д–Є–ї–Њ–Ї–Њ–Ї–Ї–Њ–≤–Њ–Љ –Ш–≠ –њ—А–Њ—В–µ–Ј–Є—А–Њ–≤–∞–љ–љ—Л—Е –Ї–ї–∞–њ–∞–љ–Њ–≤ —Б–µ—А–і—Ж–∞. –Я—А–Є —Н—В–Њ–Љ –≤–µ–і—Г—Й—Г—О —Н—В–Є–Њ–ї–Њ–≥–Є—З–µ—Б–Ї—Г—О —А–Њ–ї—М –Є–≥—А–∞—О—В –Ї–Њ–∞–≥—Г–ї–∞–Ј–Њ–љ–µ–≥–∞—В–Є–≤–љ—Л–µ –Љ–µ—В–Є—Ж–Є–ї–ї–Є–љ-—А–µ–Ј–Є—Б—В–µ–љ—В–љ—Л–µ —Б—В–∞—Д–Є–ї–Њ–Ї–Њ–Ї–Ї–Є. –†–µ–Ј—Г–ї—М—В–∞—В—Л —Н–Ї—Б–њ–µ—А–Є–Љ–µ–љ—В–∞–ї—М–љ—Л—Е –Є –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є—Е –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–є —Б–≤–Є–і–µ—В–µ–ї—М—Б—В–≤—Г—О—В –Њ —В–Њ–Љ, —З—В–Њ –њ—А–Є –і–∞–љ–љ–Њ–є —Д–Њ—А–Љ–µ –Ш–≠ –Њ–њ—В–Є–Љ–∞–ї—М–љ–Њ–є —Б—З–Є—В–∞–µ—В—Б—П –Ї–Њ–Љ–±–Є–љ–Є—А–Њ–≤–∞–љ–љ–∞—П —В–µ—А–∞–њ–Є—П –≤–∞–љ–Ї–Њ–Љ–Є—Ж–Є–љ–Њ–Љ, —А–Є—Д–∞–Љ–њ–Є—Ж–Є–љ–Њ–Љ –Є –≥–µ–љ—В–∞–Љ–Є—Ж–Є–љ–Њ–Љ, –њ–Њ–Ј–≤–Њ–ї—П—О—Й–∞—П –і–Њ–±–Є—В—М—Б—П –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Њ–≥–Њ –Є–Ј–ї–µ—З–µ–љ–Є—П –≤ 80-90% —Б–ї—Г—З–∞–µ–≤ [10,11]. –Ы–µ—З–µ–љ–Є–µ –≤–∞–љ–Ї–Њ–Љ–Є—Ж–Є–љ–Њ–Љ –Є —А–Є—Д–∞–Љ–њ–Є—Ж–Є–љ–Њ–Љ –њ—А–Њ–≤–Њ–і—П—В, –Ї–∞–Ї –Љ–Є–љ–Є–Љ—Г–Љ, –≤ —В–µ—З–µ–љ–Є–µ 6 –љ–µ–і–µ–ї—М, –њ—А–Є–Љ–µ–љ–µ–љ–Є–µ –≥–µ–љ—В–∞–Љ–Є—Ж–Є–љ–∞ –Є–ї–Є –і—А—Г–≥–Њ–≥–Њ –∞–Љ–Є–љ–Њ–≥–ї–Є–Ї–Њ–Ј–Є–і–∞ –Њ–≥—А–∞–љ–Є—З–Є–≤–∞—О—В –њ–µ—А–≤—Л–Љ–Є –і–≤—Г–Љ—П –љ–µ–і–µ–ї—П–Љ–Є. –Я—А–Є –љ–∞–ї–Є—З–Є–Є —А–µ–Ј–Є—Б—В–µ–љ—В–љ–Њ—Б—В–Є –≤—Л–і–µ–ї–µ–љ–љ—Л—Е –Љ–Є–Ї—А–Њ–Њ—А–≥–∞–љ–Є–Ј–Љ–Њ–≤ –Ї –∞–Љ–Є–љ–Њ–≥–ї–Є–Ї–Њ–Ј–Є–і–∞–Љ –њ–Њ—Б–ї–µ–і–љ–Є–µ –њ—А–Є–Љ–µ–љ—П—В—М –љ–µ —А–µ–Ї–Њ–Љ–µ–љ–і—Г–µ—В—Б—П. –†–Є—Д–∞–Љ–њ–Є—Ж–Є–љ —А–∞—Б—Б–Љ–∞—В—А–Є–≤–∞–µ—В—Б—П –Ї–∞–Ї –Њ—З–µ–љ—М —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ–µ —Б—А–µ–і—Б—В–≤–Њ –≤ –ї–µ—З–µ–љ–Є–Є —Б—В–∞—Д–Є–ї–Њ–Ї–Њ–Ї–Ї–Њ–≤–Њ–≥–Њ –Ш–≠ –Ї–ї–∞–њ–∞–љ–љ—Л—Е –њ—А–Њ—В–µ–Ј–Њ–≤. –Т —В–Њ –ґ–µ –≤—А–µ–Љ—П –њ—А–Є –Љ–Њ–љ–Њ—В–µ—А–∞–њ–Є–Є —Н—В–Є–Љ –њ—А–µ–њ–∞—А–∞—В–Њ–Љ –Ї –љ–µ–Љ—Г –±—Л—Б—В—А–Њ —А–∞–Ј–≤–Є–≤–∞–µ—В—Б—П —Г—Б—В–Њ–є—З–Є–≤–Њ—Б—В—М —Б—В–∞—Д–Є–ї–Њ–Ї–Њ–Ї–Ї–Њ–≤, –њ–Њ—Н—В–Њ–Љ—Г —А–Є—Д–∞–Љ–њ–Є—Ж–Є–љ –љ–∞–Ј–љ–∞—З–∞—О—В —В–Њ–ї—М–Ї–Њ –≤ –Ї–Њ–Љ–±–Є–љ–∞—Ж–Є–Є —Б –і—А—Г–≥–Є–Љ–Є —Б—А–µ–і—Б—В–≤–∞–Љ–Є. –Я–Њ—Б–Ї–Њ–ї—М–Ї—Г —Г—Б—В–Њ–є—З–Є–≤–Њ—Б—В—М –Љ–Є–Ї—А–Њ–Њ—А–≥–∞–љ–Є–Ј–Љ–Њ–≤ –Љ–Њ–ґ–µ—В —А–∞–Ј–≤–Є—В—М—Б—П –Є –≤–Њ –≤—А–µ–Љ—П –ї–µ—З–µ–љ–Є—П, —А–µ–Ї–Њ–Љ–µ–љ–і—Г–µ—В—Б—П –Љ–Њ–љ–Є—В–Њ—А–Є–љ–≥ —З—Г–≤—Б—В–≤–Є—В–µ–ї—М–љ–Њ—Б—В–Є –≤—Л–і–µ–ї–µ–љ–љ—Л—Е –≤–Њ–Ј–±—Г–і–Є—В–µ–ї–µ–є –Ї –∞–љ—В–Є–±–Є–Њ—В–Є–Ї–∞–Љ –Є –њ—А–Є –љ–µ–Њ–±—Е–Њ–і–Є–Љ–Њ—Б—В–Є - –Ї–Њ—А—А–µ–Ї—Ж–Є—П —В–µ—А–∞–њ–µ–≤—В–Є—З–µ—Б–Ї–Њ–є —Б—Е–µ–Љ—Л. –Х—Б–ї–Є —Б—В–∞—Д–Є–ї–Њ–Ї–Њ–Ї–Ї–Њ–≤—Л–µ —И—В–∞–Љ–Љ—Л-–Є–љ—Д–µ–Ї—В–Њ–≥–µ–љ—Л —З—Г–≤—Б—В–≤–Є—В–µ–ї—М–љ—Л –Ї –Љ–µ—В–Є—Ж–Є–ї–ї–Є–љ—Г, —В–Њ –≤–Љ–µ—Б—В–Њ –≤–∞–љ–Ї–Њ–Љ–Є—Ж–Є–љ–∞ –±–Њ–ї–µ–µ –њ—А–µ–і–њ–Њ—З—В–Є—В–µ–ї—М–љ–Њ –љ–∞–Ј–љ–∞—З–µ–љ–Є–µ –Њ–Ї—Б–∞—Ж–Є–ї–ї–Є–љ–∞, –Ї–Њ—В–Њ—А—Л–є —В–∞–Ї–ґ–µ –њ—А–Є–Љ–µ–љ—П—О—В –≤ –Ї–Њ–Љ–±–Є–љ–∞—Ж–Є–Є —Б —А–Є—Д–∞–Љ–њ–Є—Ж–Є–љ–Њ–Љ –Є –≥–µ–љ—В–∞–Љ–Є—Ж–Є–љ–Њ–Љ.
–Ф–ї—П –ї–µ—З–µ–љ–Є—П –Ш–≠, –≤—Л–Ј–≤–∞–љ–љ–Њ–≥–Њ –Љ–µ—В–Є—Ж–Є–ї–ї–Є–љ—А–µ–Ј–Є—Б—В–µ–љ—В–љ—Л–Љ–Є —Б—В–∞—Д–Є–ї–Њ–Ї–Њ–Ї–Ї–∞–Љ–Є –Є–ї–Є –≤–∞–љ–Ї–Њ–Љ–Є—Ж–Є–љ—А–µ–Ј–Є—Б—В–µ–љ—В–љ—Л–Љ–Є —Н–љ—В–µ—А–Њ–Ї–Њ–Ї–Ї–∞–Љ–Є, –љ–µ—Б–Њ–Љ–љ–µ–љ–љ–Њ –њ–µ—А—Б–њ–µ–Ї—В–Є–≤–љ—Л–Љ –њ—А–µ–і—Б—В–∞–≤–ї—П–µ—В—Б—П –њ—А–Є–Љ–µ–љ–µ–љ–Є–µ –ї–Є–љ–µ–Ј–Њ–ї–Є–і–∞ - –њ–µ—А–≤–Њ–≥–Њ –њ—А–µ–і—Б—В–∞–≤–Є—В–µ–ї—П –љ–Њ–≤–Њ–≥–Њ –Ї–ї–∞—Б—Б–∞ —Б–Є–љ—В–µ—В–Є—З–µ—Б–Ї–Є—Е –∞–љ—В–Є–Љ–Є–Ї—А–Њ–±–љ—Л—Е —Б—А–µ–і—Б—В–≤ - –Њ–Ї—Б–∞–Ј–Њ–ї–Є–і–Є–љ–Њ–љ–Њ–≤. –Ш–Љ–µ—О—Й–Є–µ—Б—П –і–∞–љ–љ—Л–µ —Н–Ї—Б–њ–µ—А–Є–Љ–µ–љ—В–∞–ї—М–љ—Л—Е –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–є –Є –Њ—В–і–µ–ї—М–љ—Л–µ –Њ–њ–Є—Б–∞–љ–Є—П –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є—Е —Б–ї—Г—З–∞–µ–≤ —Б–≤–Є–і–µ—В–µ–ї—М—Б—В–≤—Г—О—В –Њ –≤—Л—Б–Њ–Ї–Њ–є —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В–Є –ї–Є–љ–µ–Ј–Њ–ї–Є–і–∞ –њ—А–Є —Г–Ї–∞–Ј–∞–љ–љ—Л—Е —Д–Њ—А–Љ–∞—Е –Ш–≠ [12, 13, 14]
–Т –њ–Њ—Б–ї–µ–і–љ–Є–µ –≥–Њ–і—Л –Њ—В–Љ–µ—З–µ–љ–Њ –љ–∞—А–∞—Б—В–∞–љ–Є–µ —З–∞—Б—В–Њ—В—Л —И—В–∞–Љ–Љ–Њ–≤ –Љ–Є–Ї—А–Њ–Њ—А–≥–∞–љ–Є–Ј–Љ–Њ–≤ –≥—А—Г–њ–њ—Л HACEK, –њ—А–Њ–і—Г—Ж–Є—А—Г—О—Й–Є—Е b-–ї–∞–Ї—В–∞–Љ–∞–Ј—Л. –Я—А–Є–љ–Є–Љ–∞—П –≤–Њ –≤–љ–Є–Љ–∞–љ–Є–µ —А—П–і —В–µ—Е–љ–Є—З–µ—Б–Ї–Є—Е —В—А—Г–і–љ–Њ—Б—В–µ–є –≤ –Ї—Г–ї—М—В—Г—А–Є—А–Њ–≤–∞–љ–Є–Є –Є —В–µ—Б—В–Є—А–Њ–≤–∞–љ–Є–Є –∞–љ—В–Є–Љ–Є–Ї—А–Њ–±–љ–Њ–є —З—Г–≤—Б—В–≤–Є—В–µ–ї—М–љ–Њ—Б—В–Є, –≤ –љ–∞—Б—В–Њ—П—Й–µ–µ –≤—А–µ–Љ—П –≤–Њ–Ј–±—Г–і–Є—В–µ–ї–Є –і–∞–љ–љ–Њ–є –≥—А—Г–њ–њ—Л —Г—Б–ї–Њ–≤–љ–Њ —А–∞—Б—Б–Љ–∞—В—А–Є–≤–∞—О—В—Б—П –Ї–∞–Ї –∞–Љ–њ–Є—Ж–Є–ї–ї–Є–љ-—А–µ–Ј–Є—Б—В–µ–љ—В–љ—Л–µ. –Т —Б–≤—П–Ј–Є —Б —Н—В–Є–Љ –њ—А–µ–њ–∞—А–∞—В–∞–Љ–Є –≤—Л–±–Њ—А–∞ –њ—А–Є HACEK-–Ш–≠ —Б—З–Є—В–∞—О—В—Б—П —Ж–µ—Д–∞–ї–Њ—Б–њ–Њ—А–Є–љ—Л III –њ–Њ–Ї–Њ–ї–µ–љ–Є—П (—Ж–µ—Д—В—А–Є–∞–Ї—Б–Њ–љ, —Ж–µ—Д–Њ—В–∞–Ї—Б–Є–Љ), –Ї–Њ—В–Њ—А—Л–µ –љ–∞–Ј–љ–∞—З–∞—О—В—Б—П –≤ —В–µ—З–µ–љ–Є–µ 4 –љ–µ–і–µ–ї—М; —Г –±–Њ–ї—М–љ—Л—Е —Б –њ–Њ—А–∞–ґ–µ–љ–Є–µ–Љ –Ї–ї–∞–њ–∞–љ–љ—Л—Е –њ—А–Њ—В–µ–Ј–Њ–≤ —Н—В–Њ—В —Б—А–Њ–Ї —Г–і–ї–Є–љ—П–µ—В—Б—П –і–Њ 6 –љ–µ–і–µ–ї—М. –£—З–Є—В—Л–≤–∞—П —З—Г–≤—Б—В–≤–Є—В–µ–ї—М–љ–Њ—Б—В—М –і–∞–љ–љ—Л—Е –Љ–Є–Ї—А–Њ–Њ—А–≥–∞–љ–Є–Ј–Љ–Њ–≤ –Ї –Ї–Њ-—В—А–Є–Љ–Њ–Ї—Б–∞–Ј–Њ–ї—Г, —Д—В–Њ—А—Е–Є–љ–Њ–ї–Њ–љ–∞–Љ –Є –∞–Ј—В—А–µ–Њ–љ–∞–Љ—Г, —Н—В–Є –њ—А–µ–њ–∞—А–∞—В—Л –Љ–Њ–≥—Г—В —А–∞—Б—Б–Љ–∞—В—А–Є–≤–∞—В—М—Б—П –≤ –Ї–∞—З–µ—Б—В–≤–µ –∞–ї—М—В–µ—А–љ–∞—В–Є–≤—Л —Г –±–Њ–ї—М–љ—Л—Е HACEK-–Ш–≠ —Б –љ–µ–њ–µ—А–µ–љ–Њ—Б–Є–Љ–Њ—Б—В—М—О b-–ї–∞–Ї—В–∞–Љ–љ—Л—Е –∞–љ—В–Є–±–Є–Њ—В–Є–Ї–Њ–≤. –Ю–і–љ–∞–Ї–Њ –Є—Е –љ–∞–Ј–љ–∞—З–µ–љ–Є–µ —А–µ–Ї–Њ–Љ–µ–љ–і—Г–µ—В—Б—П —В–Њ–ї—М–Ї–Њ –њ–Њ—Б–ї–µ —В—Й–∞—В–µ–ї—М–љ–Њ –≤—Л–њ–Њ–ї–љ–µ–љ–љ–Њ–≥–Њ –Љ–Є–Ї—А–Њ–±–Є–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Њ–≥–Њ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П –Є –Ї–Њ–љ—Б—Г–ї—М—В–∞—Ж–Є–Є –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Њ–≥–Њ –Љ–Є–Ї—А–Њ–±–Є–Њ–ї–Њ–≥–∞.
–Ы–µ—З–µ–љ–Є–µ –Ш–≠, –≤—Л–Ј–≤–∞–љ–љ–Њ–≥–Њ –і—А—Г–≥–Є–Љ–Є —А–µ–і–Ї–Њ –≤—Б—В—А–µ—З–∞—О—Й–Є–Љ–Є—Б—П –≤–Њ–Ј–±—Г–і–Є—В–µ–ї—П–Љ–Є, –±–∞–Ј–Є—А—Г–µ—В—Б—П –љ–∞ –Є–і–µ–љ—В–Є—Д–Є–Ї–∞—Ж–Є–Є –Љ–Є–Ї—А–Њ–Њ—А–≥–∞–љ–Є–Ј–Љ–∞-–Є–љ—Д–µ–Ї—В–Њ–≥–µ–љ–∞ –Є –µ–≥–Њ —З—Г–≤—Б—В–≤–Є—В–µ–ї—М–љ–Њ—Б—В–Є –Ї –∞–љ—В–Є–±–∞–Ї—В–µ—А–Є–∞–ї—М–љ—Л–Љ –њ—А–µ–њ–∞—А–∞—В–∞–Љ. –Т —З–∞—Б—В–љ–Њ—Б—В–Є, –њ—А–Є –њ—Б–µ–≤–і–Њ–Љ–Њ–љ–∞–і–љ–Њ–Љ –Ш–≠, —З–∞—Й–µ –≤—Б—В—А–µ—З–∞—О—Й–µ–Љ—Б—П —Б—А–µ–і–Є –љ–∞—А–Ї–Њ–Љ–∞–љ–Њ–≤, –Њ–±—Л—З–љ–Њ –њ—А–Є–Љ–µ–љ—П—О—В –∞–љ—В–Є—Б–Є–љ–µ–≥–љ–Њ–є–љ—Л–µ –њ–µ–љ–Є—Ж–Є–ї–ї–Є–љ—Л (–њ–Є–њ–µ—А–∞—Ж–Є–ї–ї–Є–љ, —В–Є–Ї–∞—А—Ж–Є–ї–ї–Є–љ) –Є–ї–Є —Ж–µ—Д–∞–ї–Њ—Б–њ–Њ—А–Є–љ—Л III –њ–Њ–Ї–Њ–ї–µ–љ–Є—П (—Ж–µ—Д—В–∞–Ј–Є–і–Є–Љ) –≤ —Б–Њ—З–µ—В–∞–љ–Є–Є —Б —В–Њ–±—А–∞–Љ–Є—Ж–Є–љ–Њ–Љ; —В–∞–Ї–ґ–µ –Є–Љ–µ—О—В—Б—П –Њ—В–і–µ–ї—М–љ—Л–µ —Б–Њ–Њ–±—Й–µ–љ–Є—П –Њ–± —Г—Б–њ–µ—И–љ–Њ–Љ –њ—А–Є–Љ–µ–љ–µ–љ–Є–Є –Є–Љ–Є–њ–µ–љ–µ–Љ-—Ж–Є–ї–∞—Б—В–∞—В–Є–љ–∞ –Є –∞–Ј—В—А–µ–Њ–љ–∞–Љ–∞ –≤ –Ї–Њ–Љ–±–Є–љ–∞—Ж–Є–Є —Б —В–Њ–±—А–∞–Љ–Є—Ж–Є–љ–Њ–Љ [2,15]. –Х—Б–ї–Є –≤ –Ї–∞—З–µ—Б—В–≤–µ –≤–Њ–Ј–±—Г–і–Є—В–µ–ї–µ–є –Ш–≠ —Д–Є–≥—Г—А–Є—А—Г—О—В –њ—А–µ–і—Б—В–∞–≤–Є—В–µ–ї–Є —Б–µ–Љ–µ–є—Б—В–≤–∞ Enterobacteriaceae (E. coli, Klebsiella spp., Proteus spp –Є –і—А.), –Њ–њ—А–∞–≤–і–∞–љ–Њ –љ–∞–Ј–љ–∞—З–µ–љ–Є–µ —Ж–µ—Д–∞–ї–Њ—Б–њ–Њ—А–Є–љ–Њ–≤ III –њ–Њ–Ї–Њ–ї–µ–љ–Є—П (—Ж–µ—Д–Њ—В–∞–Ї—Б–Є–Љ), –Є–Љ–Є–њ–µ–љ–µ–Љ-—Ж–Є–ї–∞—Б—В–∞—В–Є–љ–∞ –Є–ї–Є —Д—В–Њ—А—Е–Є–љ–Њ–ї–Њ–љ–Њ–≤ –≤ —Б–Њ—З–µ—В–∞–љ–Є–Є —Б –∞–Љ–Є–љ–Њ–≥–ї–Є–Ї–Њ–Ј–Є–і–∞–Љ–Є (–Є–ї–Є –±–µ–Ј —В–∞–Ї–Њ–≤—Л—Е).
–Я—А–Є –≥—А–Є–±–Ї–Њ–≤–Њ–Љ –Ш–≠ –њ—А–Є–Љ–µ–љ—П—О—В –∞–Љ—Д–Њ—В–µ—А–Є—Ж–Є–љ –Т –≤ —Б–Њ—З–µ—В–∞–љ–Є–Є —Б —Д–ї—Г—Ж–Є—В–Њ–Ј–Є–љ–Њ–Љ, –Њ–і–љ–∞–Ї–Њ –њ–Њ–ї—М–Ј–∞ —В–µ—А–∞–њ–Є–Є –љ–µ–≤—Л—Б–Њ–Ї–∞ –Є –Њ–±—Л—З–љ–Њ —В—А–µ–±—Г–µ—В—Б—П –Њ–њ–µ—А–∞—В–Є–≤–љ–Њ–µ –ї–µ—З–µ–љ–Є–µ; –Њ–њ–Є—Б–∞–љ—Л –Њ—В–і–µ–ї—М–љ—Л–µ —Б–ї—Г—З–∞–Є —Г—Б–њ–µ—И–љ–Њ–≥–Њ –і–ї–Є—В–µ–ї—М–љ–Њ–≥–Њ –ї–µ—З–µ–љ–Є—П —Д–ї—Г–Ї–Њ–љ–∞–Ј–Њ–ї–Њ–Љ –Є–ї–Є –Є—В—А–∞–Ї–Њ–љ–∞–Ј–Њ–ї–Њ–Љ, –љ–Њ –і–Њ—Б—В–Њ–≤–µ—А–љ–∞—П –Є—Е —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В—М –њ—А–Є –і–∞–љ–љ–Њ–є —Д–Њ—А–Љ–µ –Ш–≠ –љ–µ –і–Њ–Ї–∞–Ј–∞–љ–∞ [16]. –С–Њ–ї—М—И–Њ–≥–Њ –≤–љ–Є–Љ–∞–љ–Є—П –Ј–∞—Б–ї—Г–ґ–Є–≤–∞–µ—В –њ—А–µ–і—Б—В–∞–≤–Є—В–µ–ї—М –≥—А—Г–њ–њ—Л –∞–Ј–Њ–ї–Њ–≤ –≤–Њ—А–Є–Ї–Њ–љ–∞–Ј–Њ–ї. –Э–∞–ї–Є—З–Є–µ –њ–µ—А–Њ—А–∞–ї—М–љ–Њ–є –Є –њ–∞—А–µ–љ—В–µ—А–∞–ї—М–љ–Њ–є –ї–µ–Ї–∞—А—Б—В–≤–µ–љ–љ—Л—Е —Д–Њ—А–Љ, –±–Њ–ї–µ–µ —И–Є—А–Њ–Ї–Є–є —Б–њ–µ–Ї—В—А –∞–Ї—В–Є–≤–љ–Њ—Б—В–Є, –≤–Ї–ї—О—З–∞—О—Й–Є–є Aspergillus spp, –љ–Є–Ј–Ї–∞—П —З–∞—Б—В–Њ—В–∞ –њ–Њ–±–Њ—З–љ—Л—Е —Н—Д—Д–µ–Ї—В–Њ–≤ –≤ —Е–Њ–і–µ III —Д–∞–Ј—Л –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є—Е –Є—Б–њ—Л—В–∞–љ–Є–є –њ–Њ–Ј–≤–Њ–ї—П—О—В —А–∞—Б—Б–Љ–∞—В—А–Є–≤–∞—В—М –і–∞–љ–љ—Л–є –њ—А–µ–њ–∞—А–∞—В, –Ї–∞–Ї –Њ–і–љ–Њ –Є–Ј –љ–∞–Є–±–Њ–ї–µ–µ –њ–µ—А—Б–њ–µ–Ї—В–Є–≤–љ—Л—Е —Б—А–µ–і—Б—В–≤ –і–ї—П –ї–µ—З–µ–љ–Є—П –≥—А–Є–±–Ї–Њ–≤–Њ–≥–Њ –Ш–≠ [17, 18].
–Т –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Њ–є –њ—А–∞–Ї—В–Є–Ї–µ –≤–µ—Б—М–Љ–∞ –љ–µ—А–µ–і–Ї–Њ –≤—Б—В—А–µ—З–∞—О—В—Б—П —Б–ї—Г—З–∞–Є, –Ї–Њ–≥–і–∞ —Г –±–Њ–ї—М–љ–Њ–≥–Њ —Б –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Њ–є —Б–Є–Љ–њ—В–Њ–Љ–∞—В–Є–Ї–Њ–є –Ш–≠ –њ–Њ—Б–µ–≤—Л –Ї—А–Њ–≤–Є –љ–µ –і–∞—О—В –њ–Њ–ї–Њ–ґ–Є—В–µ–ї—М–љ–Њ–≥–Њ —А–µ–Ј—Г–ї—М—В–∞—В–∞. –Т —Н—В–Є—Е —Б–Є—В—Г–∞—Ж–Є—П—Е –≤—А–∞—З—Г –њ—А–Є—Е–Њ–і–Є—В—Б—П –њ—А–Є–љ–Є–Љ–∞—В—М –і–Њ—Б—В–∞—В–Њ—З–љ–Њ –љ–µ–ї–µ–≥–Ї–Њ–µ —А–µ—И–µ–љ–Є–µ –Є –љ–∞–Ј–љ–∞—З–∞—В—М –∞–љ—В–Є–±–∞–Ї—В–µ—А–Є–∞–ї—М–љ—Г—О —В–µ—А–∞–њ–Є—О –љ–∞ –Њ—Б–љ–Њ–≤–∞–љ–Є–Є –њ—А–µ–і–њ–Њ–ї–∞–≥–∞–µ–Љ—Л—Е –≤–Њ–Ј–±—Г–і–Є—В–µ–ї–µ–є –Ш–≠ —Б —Г—З–µ—В–Њ–Љ –≤–Њ–Ј—А–∞—Б—В–∞ –±–Њ–ї—М–љ–Њ–≥–Њ, —Е–∞—А–∞–Ї—В–µ—А–∞ —В–µ—З–µ–љ–Є—П –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П, –љ–∞–ї–Є—З–Є—П –Ї–ї–∞–њ–∞–љ–љ—Л—Е –њ—А–Њ—В–µ–Ј–Њ–≤ –Є —В.–і. –Т —З–∞—Б—В–љ–Њ—Б—В–Є, —Г –±–Њ–ї—М–љ—Л—Е, –љ–µ —Г–њ–Њ—В—А–µ–±–ї—П—О—Й–Є—Е –љ–∞—А–Ї–Њ—В–Є–Ї–Є, —Б –њ–Њ–і–Њ—Б—В—А—Л–Љ –Ш–≠ –љ–∞ —Д–Њ–љ–µ –њ—А–Є–Њ–±—А–µ—В–µ–љ–љ—Л—Е –њ–Њ—А–Њ–Ї–Њ–≤ —Б–µ—А–і—Ж–∞ –љ–∞–Є–±–Њ–ї–µ–µ –≤–µ—А–Њ—П—В–љ—Л–Љ —Н—В–Є–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є–Љ —Д–∞–Ї—В–Њ—А–Њ–Љ —П–≤–ї—П—О—В—Б—П —Б—В—А–µ–њ—В–Њ–Ї–Њ–Ї–Ї–Є. –Т —Н—В–Њ–Љ —Б–ї—Г—З–∞–µ —Н–Љ–њ–Є—А–Є—З–µ—Б–Ї–∞—П –∞–љ—В–Є–±–Є–Њ—В–Є–Ї–Њ—В–µ—А–∞–њ–Є—П –і–Њ–ї–ґ–љ–∞ –Њ—Е–≤–∞—В—Л–≤–∞—В—М –Є –њ—А–µ–і—Б—В–∞–≤–Є—В–µ–ї–µ–є –і–∞–љ–љ–Њ–≥–Њ —Б–µ–Љ–µ–є—Б—В–≤–∞ —Б –Љ–∞–Ї—Б–Є–Љ–∞–ї—М–љ–Њ–є –≤–µ—А–Њ—П—В–љ–Њ—Б—В—М—О —А–µ–Ј–Є—Б—В–µ–љ—В–љ–Њ—Б—В–Є, —В.–µ. —Н–љ—В–µ—А–Њ–Ї–Њ–Ї–Ї–Њ–≤ (–∞–Љ–њ–Є—Ж–Є–ї–ї–Є–љ + –≥–µ–љ—В–∞–Љ–Є—Ж–Є–љ). –Я—А–Є –Њ—Б—В—А–Њ–Љ –њ—А–Њ—Ж–µ—Б—Б–µ, –њ—А–Њ—В–µ–Ї–∞—О—Й–µ–Љ —Б –±—Л—Б—В—А–Њ–є –і–µ—Б—В—А—Г–Ї—Ж–Є–µ–є –Ї–ї–∞–њ–∞–љ–Њ–≤, —Ж–µ–ї–µ—Б–Њ–Њ–±—А–∞–Ј–љ–Њ –љ–∞–Ј–љ–∞—З–µ–љ–Є–µ —Б—Е–µ–Љ—Л, –њ—А–Є–Љ–µ–љ—П–µ–Љ–Њ–є –і–ї—П –ї–µ—З–µ–љ–Є—П –Ш–≠, –≤—Л–Ј–≤–∞–љ–љ–Њ–≥–Њ –Љ–µ—В–Є—Ж–Є–ї–ї–Є–љ-—З—Г–≤—Б—В–≤–Є—В–µ–ї—М–љ—Л–Љ–Є St. aureus. –Я—А–Є –њ–Њ–і–Њ–Ј—А–µ–љ–Є–Є –љ–∞ –Є–љ—Д–Є—Ж–Є—А–Њ–≤–∞–љ–Є–µ –њ—А–Њ—В–µ–Ј–Є—А–Њ–≤–∞–љ–љ—Л—Е –Ї–ї–∞–њ–∞–љ–Њ–≤ –љ–∞–Ј–љ–∞—З–∞—О—В –Ї–Њ–Љ–±–Є–љ–Є—А–Њ–≤–∞–љ–љ—Г—О —В–µ—А–∞–њ–Є—О, –љ–∞–њ—А–∞–≤–ї–µ–љ–љ—Г—О –љ–∞ –Љ–µ—В–Є—Ж–Є–ї–ї–Є–љ-—А–µ–Ј–Є—Б—В–µ–љ—В–љ—Л–µ —И—В–∞–Љ–Љ—Л —Б—В–∞—Д–Є–ї–Њ–Ї–Њ–Ї–Ї–Њ–≤. –Х—Б–ї–Є —Г –±–Њ–ї—М–љ–Њ–≥–Њ –Њ—В–Љ–µ—З–∞–µ—В—Б—П –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є–є —Н—Д—Д–µ–Ї—В (—Б–љ–Є–ґ–µ–љ–Є–µ —В–µ–Љ–њ–µ—А–∞—В—Г—А—Л, –Є—Б—З–µ–Ј–љ–Њ–≤–µ–љ–Є–µ –Њ–Ј–љ–Њ–±–Њ–≤, —Г–Љ–µ–љ—М—И–µ–љ–Є–µ —Б–ї–∞–±–Њ—Б—В–Є, —Г–ї—Г—З—И–µ–љ–Є–µ –Њ–±—Й–µ–≥–Њ —Б–∞–Љ–Њ—З—Г–≤—Б—В–≤–Є—П), –њ—А–Њ–≤–Њ–і–Є–Љ—Г—О —В–µ—А–∞–њ–Є—О –њ—А–Њ–і–Њ–ї–ґ–∞—О—В –і–Њ –Ј–∞–≤–µ—А—И–µ–љ–Є—П –њ–Њ–ї–љ–Њ–≥–Њ –Ї—Г—А—Б–∞ (4-6 –љ–µ–і–µ–ї—М). –Я—А–Є –Њ—В—Б—Г—В—Б—В–≤–Є–Є –њ–Њ–ї–Њ–ґ–Є—В–µ–ї—М–љ–Њ–є –і–Є–љ–∞–Љ–Є–Ї–Є –≤ —В–µ—З–µ–љ–Є–µ 5-7 –і–љ–µ–є –Њ—В –љ–∞—З–∞–ї–∞ –ї–µ—З–µ–љ–Є—П —Ж–µ–ї–µ—Б–Њ–Њ–±—А–∞–Ј–љ–∞ –Ї–Њ—А—А–µ–Ї—Ж–Є—П —Б—Е–µ–Љ—Л –∞–љ—В–Є–Љ–Є–Ї—А–Њ–±–љ–Њ–є —В–µ—А–∞–њ–Є–Є.
–Я—А–Є –≤—Л—А–∞–ґ–µ–љ–љ—Л—Е –Є–Љ–Љ—Г–љ–Њ–њ–∞—В–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є—Е –њ—А–Њ—П–≤–ї–µ–љ–Є—П—Е –Ш–≠ –Њ–њ—А–∞–≤–і–∞–љ–Њ –љ–∞–Ј–љ–∞—З–µ–љ–Є–µ –њ—А–µ–і–љ–Є–Ј–Њ–ї–Њ–љ–∞ –≤ –і–Њ–Ј–µ 15-20 (—А–µ–ґ–µ - 30) –Љ–≥ –≤ —Б—Г—В–Ї–Є.
–Т –љ–∞—Б—В–Њ—П—Й–µ–µ –≤—А–µ–Љ—П –≤ –ї–Є—В–µ—А–∞—В—Г—А–µ —И–Є—А–Њ–Ї–Њ –Њ–±—Б—Г–ґ–і–∞—О—В—Б—П –≤–Њ–Ј–Љ–Њ–ґ–љ–Њ—Б—В–Є –њ—А–Є–Љ–µ–љ–µ–љ–Є—П –Љ–µ–і–Є–Ї–∞–Љ–µ–љ—В–Њ–Ј–љ–Њ–є –Є–Љ–Љ—Г–љ–Њ–Ї–Њ—А—А–µ–Ї—Ж–Є–Є (—В–Є–Љ–∞–ї–Є–љ, —В-–∞–Ї—В–Є–≤–Є–љ, –њ—А–µ–њ–∞—А–∞—В—Л –Є–љ—В–µ—А—Д–µ—А–Њ–љ–∞ –Є —В.–і.) –Є —Н–Ї—Б—В—А–∞–Ї–Њ—А–њ–Њ—А–∞–ї—М–љ—Л—Е –Љ–µ—В–Њ–і–Њ–≤ –ї–µ—З–µ–љ–Є—П (–≥–µ–Љ–Њ—Б–Њ—А–±—Ж–Є—П, –њ–ї–∞–Ј–Љ–∞—Д–µ—А–µ–Ј) —Г –±–Њ–ї—М–љ—Л—Е –Ш–≠. –Ю–і–љ–∞–Ї–Њ –і–Њ—Б—В–∞—В–Њ—З–љ–Њ –Љ–∞–ї—Л–є –Њ–њ—Л—В –њ—А–Є–Љ–µ–љ–µ–љ–Є—П —Н—В–Є—Е –њ—А–µ–њ–∞—А–∞—В–Њ–≤ –Є –њ—А–Њ—Ж–µ–і—Г—А –њ—А–Є –Ш–≠ –љ–µ –њ–Њ–Ј–≤–Њ–ї—П–µ—В –і–∞—В—М –Ї–∞–Ї–Є—Е-–ї–Є–±–Њ –Њ–і–љ–Њ–Ј–љ–∞—З–љ—Л—Е —А–µ–Ї–Њ–Љ–µ–љ–і–∞—Ж–Є–є. –°–ї–µ–і–Њ–≤–∞—В–µ–ї—М–љ–Њ, —В—А–µ–±—Г—О—В—Б—П –і–∞–ї—М–љ–µ–є—И–Є–µ –љ–∞—Г—З–љ—Л–µ —А–∞–Ј—А–∞–±–Њ—В–Ї–Є –≤ —Н—В–Њ–Љ –љ–∞–њ—А–∞–≤–ї–µ–љ–Є–Є.
–Т —Б–ї—Г—З–∞—П—Е –љ–µ—Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В–Є –ї–µ–Ї–∞—А—Б—В–≤–µ–љ–љ–Њ–є —В–µ—А–∞–њ–Є–Є –љ–µ–Њ–±—Е–Њ–і–Є–Љ–Њ —Е–Є—А—Г—А–≥–Є—З–µ—Б–Ї–Њ–µ –ї–µ—З–µ–љ–Є–µ, –Њ—Б–љ–Њ–≤–љ—Л–µ –њ–Њ–Ї–∞–Ј–∞–љ–Є—П –Ї –Ї–Њ—В–Њ—А–Њ–Љ—Г –Њ—В—А–∞–ґ–µ–љ—Л –≤ —В–∞–±–ї–Є—Ж–µ 2. –°–ї–µ–і—Г–µ—В –њ–Њ–і—З–µ—А–Ї–љ—Г—В—М, —З—В–Њ –∞–Ї—В–Є–≤–љ—Л–є –Ш–≠ –љ–µ —П–≤–ї—П–µ—В—Б—П –њ—А–Њ—В–Є–≤–Њ–њ–Њ–Ї–∞–Ј–∞–љ–Є–µ–Љ –Ї –Њ–њ–µ—А–∞—В–Є–≤–љ–Њ–Љ—Г –ї–µ—З–µ–љ–Є—О.

–Э–µ—Б–Љ–Њ—В—А—П –љ–∞ —Б–Њ–≤—А–µ–Љ–µ–љ–љ—Л–µ –і–Њ—Б—В–Є–ґ–µ–љ–Є—П –≤ –ї–µ—З–µ–љ–Є–Є –Ш–≠, –≤—Л—Б–Њ–Ї–∞—П –ї–µ—В–∞–ї—М–љ–Њ—Б—В—М –њ—А–Є —Н—В–Њ–Љ –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є–Є (20-45%) –Њ–њ—А–µ–і–µ–ї—П–µ—В –µ–≥–Њ –њ—А–Њ—Д–Є–ї–∞–Ї—В–Є–Ї—Г, –Ї–∞–Ї –Ј–∞–і–∞—З—Г –њ–µ—А–≤–Њ—Б—В–µ–њ–µ–љ–љ–Њ–є –≤–∞–ґ–љ–Њ—Б—В–Є.
–Э–µ—Б–Љ–Њ—В—А—П –љ–∞ —Б–Њ–≤—А–µ–Љ–µ–љ–љ—Л–µ –і–Њ—Б—В–Є–ґ–µ–љ–Є—П –≤ –ї–µ—З–µ–љ–Є–Є –Ш–≠, –≤—Л—Б–Њ–Ї–∞—П –ї–µ—В–∞–ї—М–љ–Њ—Б—В—М –њ—А–Є —Н—В–Њ–Љ –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є–Є (20-45%) –Њ–њ—А–µ–і–µ–ї—П–µ—В –µ–≥–Њ –њ—А–Њ—Д–Є–ї–∞–Ї—В–Є–Ї—Г, –Ї–∞–Ї –Ј–∞–і–∞—З—Г –њ–µ—А–≤–Њ—Б—В–µ–њ–µ–љ–љ–Њ–є –≤–∞–ґ–љ–Њ—Б—В–Є.–•–Њ—В—П –Ї–Њ–љ—В—А–Њ–ї–Є—А—Г–µ–Љ—Л–µ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П, –њ–Њ—Б–≤—П—Й–µ–љ–љ—Л–µ –Є–Ј—Г—З–µ–љ–Є—О —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В–Є –∞–љ—В–Є–±–Є–Њ—В–Є–Ї–Њ–њ—А–Њ—Д–Є–ї–∞–Ї—В–Є–Ї–Є –Ш–≠ —Г –ї–Є—Ж —Б–Њ —Б—В—А—Г–Ї—В—Г—А–љ—Л–Љ–Є –і–µ—Д–µ–Ї—В–∞–Љ–Є —Б–µ—А–і—Ж–∞, –љ–µ –њ—А–Њ–≤–Њ–і–Є–ї–Є—Б—М, –≤ –Љ–љ–Њ–≥–Њ—З–Є—Б–ї–µ–љ–љ—Л—Е —А–∞–±–Њ—В–∞—Е –њ–Њ–Ї–∞–Ј–∞–љ–∞ –≤–Њ–Ј–Љ–Њ–ґ–љ–Њ—Б—В—М —Г—Б–њ–µ—И–љ–Њ–≥–Њ –њ–Њ–і–∞–≤–ї–µ–љ–Є—П –±–∞–Ї—В–µ—А–Є–µ–Љ–Є–Є, –≤–Њ–Ј–љ–Є–Ї–∞—О—Й–µ–є –њ—А–Є —А–∞–Ј–ї–Є—З–љ—Л—Е –Љ–µ–і–Є—Ж–Є–љ—Б–Ї–Є—Е –Љ–∞–љ–Є–њ—Г–ї—П—Ж–Є—П—Е. –Т —В–Њ –ґ–µ –≤—А–µ–Љ—П –њ—А–Є –≤—Л–њ–Њ–ї–љ–µ–љ–Є–Є –Љ–љ–Њ–≥–Є—Е –њ—А–Њ—Ж–µ–і—Г—А —Г –ї–Є—Ж —Б–Њ —Б—В—А—Г–Ї—В—Г—А–љ–Њ –Є–Ј–Љ–µ–љ–µ–љ–љ—Л–Љ —Б–µ—А–і—Ж–µ–Љ —З–∞—Б—В–Њ—В–∞ —А–∞–Ј–≤–Є—В–Є—П –Ш–≠ –љ–µ –Њ—В–ї–Є—З–∞–µ—В—Б—П –Њ—В —В–∞–Ї–Њ–≤–Њ–є –≤ –Њ–±—Й–µ–є –њ–Њ–њ—Г–ї—П—Ж–Є–Є. –Я–Њ—Н—В–Њ–Љ—Г –њ—А–Є —А–∞—Ж–Є–Њ–љ–∞–ї—М–љ–Њ–Љ –њ–Њ–і—Е–Њ–і–µ –Ї –њ—А–Њ—Д–Є–ї–∞–Ї—В–Є–Ї–µ –Ш–≠ –њ–Њ–і—А–∞–Ј—Г–Љ–µ–≤–∞–µ—В—Б—П —Г—З–µ—В —Б–ї–µ–і—Г—О—Й–Є—Е —Д–∞–Ї—В–Њ—А–Њ–≤:
–∞) —Б—В–µ–њ–µ–љ—М —А–Є—Б–Ї–∞ —А–∞–Ј–≤–Є—В–Є—П –Ш–≠ –і–ї—П –±–Њ–ї—М–љ–Њ–≥–Њ —Б —В–Њ–є –Є–ї–Є –Є–љ–Њ–є —Д–Њ–љ–Њ–≤–Њ–є —Б–µ—А–і–µ—З–љ–Њ–є –њ–∞—В–Њ–ї–Њ–≥–Є–µ–є;
–±) —Б—В–µ–њ–µ–љ—М —А–Є—Б–Ї–∞ –±–∞–Ї—В–µ—А–Є–µ–Љ–Є–Є –њ—А–Є –Њ–њ—А–µ–і–µ–ї–µ–љ–љ—Л—Е –Љ–µ–і–Є—Ж–Є–љ—Б–Ї–Є—Е –≤–Љ–µ—И–∞—В–µ–ї—М—Б—В–≤–∞—Е;
–≤) –≤–Њ–Ј–Љ–Њ–ґ–љ—Л–µ –љ–µ–ґ–µ–ї–∞—В–µ–ї—М–љ—Л–µ —Н—Д—Д–µ–Ї—В—Л –∞–љ—В–Є–Љ–Є–Ї—А–Њ–±–љ–Њ–≥–Њ —Б—А–µ–і—Б—В–≤–∞;
–≥) —Б—В–Њ–Є–Љ–Њ—Б—В–љ—Л–µ –∞—Б–њ–µ–Ї—В—Л —А–µ–Ї–Њ–Љ–µ–љ–і—Г–µ–Љ–Њ–є –њ—А–Њ—Д–Є–ї–∞–Ї—В–Є—З–µ—Б–Ї–Њ–є —Б—Е–µ–Љ—Л.
–Т —Б–Њ–Њ—В–≤–µ—В—Б—В–≤–Є–Є —Б —А–µ–Ї–Њ–Љ–µ–љ–і–∞—Ж–Є—П–Љ–Є, —А–∞–Ј—А–∞–±–Њ—В–∞–љ–љ—Л–Љ–Є –Ї–Њ–Љ–Є—В–µ—В–Њ–Љ —Н–Ї—Б–њ–µ—А—В–Њ–≤ –Р–Љ–µ—А–Є–Ї–∞–љ—Б–Ї–Њ–є –Ї–∞—А–і–Є–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Њ–є –∞—Б—Б–Њ—Ж–Є–∞—Ж–Є–Є [19], –∞–љ—В–Є–±–Є–Њ—В–Є–Ї–Њ–њ—А–Њ—Д–Є–ї–∞–Ї—В–Є–Ї–∞ –њ–Њ–Ї–∞–Ј–∞–љ–∞ –≤ –љ–∞–Є–±–Њ–ї—М—И–µ–є —Б—В–µ–њ–µ–љ–Є —В–∞–Ї–Є–Љ –±–Њ–ї—М–љ—Л–Љ, —Г –Ї–Њ—В–Њ—А—Л—Е –Ш–≠ –љ–µ —В–Њ–ї—М–Ї–Њ —А–∞–Ј–≤–Є–≤–∞–µ—В—Б—П –Ј–љ–∞—З–Є—В–µ–ї—М–љ–Њ —З–∞—Й–µ –њ–Њ —Б—А–∞–≤–љ–µ–љ–Є—О —Б –њ–Њ–њ—Г–ї—П—Ж–Є–Њ–љ–љ—Л–Љ–Є –і–∞–љ–љ—Л–Љ–Є (—Г–Љ–µ—А–µ–љ–љ—Л–є —А–Є—Б–Ї), –љ–Њ –Є –∞—Б—Б–Њ—Ж–Є–Є—А—Г–µ—В—Б—П —Б –≤—Л—Б–Њ–Ї–Њ–є –ї–µ—В–∞–ї—М–љ–Њ—Б—В—М—О (–≤—Л—Б–Њ–Ї–Є–є —А–Є—Б–Ї) (—В–∞–±–ї. 3).

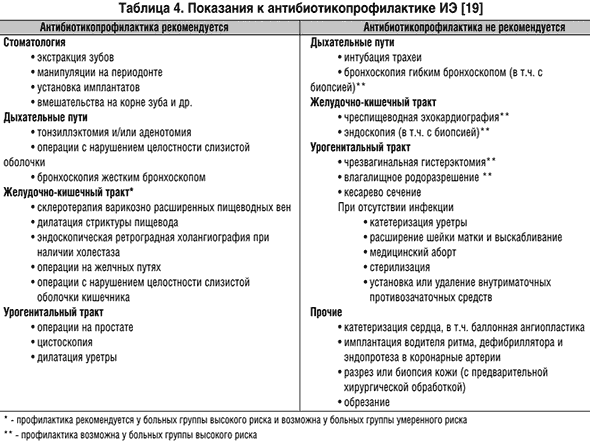
–Р–љ—В–Є–±–Є–Њ—В–Є–Ї–Њ–њ—А–Њ—Д–Є–ї–∞–Ї—В–Є–Ї–∞ –њ–Њ–Ї–∞–Ј–∞–љ–∞ —В–Њ–ї—М–Ї–Њ –њ—А–Є –Њ–њ—А–µ–і–µ–ї–µ–љ–љ—Л—Е –≤–Љ–µ—И–∞—В–µ–ї—М—Б—В–≤–∞—Е, —Б–Њ–њ—А–Њ–≤–Њ–ґ–і–∞—О—Й–Є—Е—Б—П –±–∞–Ї—В–µ—А–Є–µ–Љ–Є–µ–є, –≤—Л–Ј–≤–∞–љ–љ–Њ–є –њ–Њ—В–µ–љ—Ж–Є–∞–ї—М–љ—Л–Љ–Є –≤–Њ–Ј–±—Г–і–Є—В–µ–ї—П–Љ–Є –Ш–≠ (—В–∞–±–ї. 4).
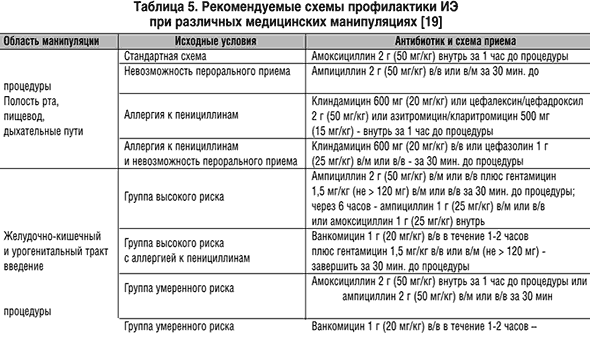
–Т —В–∞–±–ї–Є—Ж–µ 5 –њ—А–µ–і—Б—В–∞–≤–ї–µ–љ—Л —А–µ–Ї–Њ–Љ–µ–љ–і–∞—Ж–Є–Є –њ–Њ –∞–љ—В–Є–±–Є–Њ—В–Є–Ї–Њ–њ—А–Њ—Д–Є–ї–∞–Ї—В–Є–Ї–µ –њ—А–Є —А–∞–Ј–ї–Є—З–љ—Л—Е –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є—Е —Б–Є—В—Г–∞—Ж–Є—П—Е. –Ю–і–љ–∞–Ї–Њ —Н—В–Є —Б—Е–µ–Љ—Л –љ–µ —П–≤–ї—П—О—В—Б—П —Б—В–∞–љ–і–∞—А—В–∞–Љ–Є –ї–µ—З–µ–љ–Є—П –Є –љ–µ –Ј–∞–Љ–µ–љ—П—О—В –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Њ–≥–Њ –Љ—Л—И–ї–µ–љ–Є—П. –Т—А–∞—З –і–Њ–ї–ґ–µ–љ —А—Г–Ї–Њ–≤–Њ–і—Б—В–≤–Њ–≤–∞—В—М—Б—П —Б–Њ–±—Б—В–≤–µ–љ–љ—Л–Љ –Њ–њ—Л—В–Њ–Љ –≤ –≤—Л–±–Њ—А–µ –њ—А–µ–њ–∞—А–∞—В–∞ –Є –Њ–њ—А–µ–і–µ–ї–µ–љ–Є–Є –Ї—А–∞—В–љ–Њ—Б—В–Є –µ–≥–Њ –њ—А–Є–Љ–µ–љ–µ–љ–Є—П –≤ –Ј–∞–≤–Є—Б–Є–Љ–Њ—Б—В–Є –Њ—В –Њ—Б–Њ–±–µ–љ–љ–Њ—Б—В–µ–є —Б–ї—Г—З–∞—П.
–Т –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Њ–є –њ—А–∞–Ї—В–Є–Ї–µ –≤–Њ–Ј–Љ–Њ–ґ–љ—Л —Б–Є—В—Г–∞—Ж–Є–Є, –Ї–Њ–≥–і–∞ –±–Њ–ї—М–љ—Л–µ –Є–Ј –≥—А—Г–њ–њ —А–Є—Б–Ї–∞ —Г–ґ–µ –њ–Њ–ї—Г—З–∞—О—В –∞–љ—В–Є–±–∞–Ї—В–µ—А–Є–∞–ї—М–љ—Л–µ –њ—А–µ–њ–∞—А–∞—В—Л (–њ–Њ –Ї–∞–Ї–Є–Љ-–ї–Є–±–Њ –Є–љ—Л–Љ –њ–Њ–Ї–∞–Ј–∞–љ–Є—П–Љ), –Ї–Њ—В–Њ—А—Л–µ –Є—Б–њ–Њ–ї—М–Ј—Г—О—В—Б—П –і–ї—П –њ—А–Њ—Д–Є–ї–∞–Ї—В–Є–Ї–Є –Ш–≠. –Т –њ–Њ–і–Њ–±–љ—Л—Е —Б–ї—Г—З–∞—П—Е —Ж–µ–ї–µ—Б–Њ–Њ–±—А–∞–Ј–љ–Њ –љ–µ —Г–≤–µ–ї–Є—З–Є–≤–∞—В—М –і–Њ–Ј—Г –њ—А–Є–Љ–µ–љ—П–µ–Љ–Њ–≥–Њ –њ—А–µ–њ–∞—А–∞—В–∞, –∞ –љ–∞–Ј–љ–∞—З–∞—В—М –∞–љ—В–Є–±–Є–Њ—В–Є–Ї –і—А—Г–≥–Њ–є –≥—А—Г–њ–њ—Л. –Х—Б–ї–Є –њ–Њ–Ј–≤–Њ–ї—П—О—В –Њ–±—Б—В–Њ—П—В–µ–ї—М—Б—В–≤–∞, –њ—А–µ–і–њ–Њ–ї–∞–≥–∞–µ–Љ—Г—О, –≤ —З–∞—Б—В–љ–Њ—Б—В–Є, —Б—В–Њ–Љ–∞—В–Њ–ї–Њ–≥–Є—З–µ—Б–Ї—Г—О –њ—А–Њ—Ж–µ–і—Г—А—Г –ґ–µ–ї–∞—В–µ–ї—М–љ–Њ –њ—А–Њ–≤–µ—Б—В–Є —З–µ—А–µ–Ј 9-14 –і–љ–µ–є –њ–Њ—Б–ї–µ –Њ–Ї–Њ–љ—З–∞–љ–Є—П –∞–љ—В–Є–±–Є–Њ—В–Є–Ї–Њ—В–µ—А–∞–њ–Є–Є, —З—В–Њ –і–∞–µ—В –≤–Њ–Ј–Љ–Њ–ґ–љ–Њ—Б—В—М –≤–Њ—Б—Б—В–∞–љ–Њ–≤–ї–µ–љ–Є—П –Њ–±—Л—З–љ–Њ–є –Љ–Є–Ї—А–Њ—Д–ї–Њ—А—Л –њ–Њ–ї–Њ—Б—В–Є —А—В–∞.
–°–ї–µ–і—Г–µ—В –Њ—Б–Њ–±–Њ –њ–Њ–і—З–µ—А–Ї–љ—Г—В—М, —З—В–Њ —Б—Е–µ–Љ–∞ –њ—А–Є–µ–Љ–∞ –∞–љ—В–Є–±–Є–Њ—В–Є–Ї–Њ–≤, –љ–∞–Ј–љ–∞—З–∞–µ–Љ—Л—Е —Б —Ж–µ–ї—М—О –њ—А–Њ—Д–Є–ї–∞–Ї—В–Є–Ї–Є —А–µ—Ж–Є–і–Є–≤–Њ–≤ –Њ—Б—В—А–Њ–є —А–µ–≤–Љ–∞—В–Є—З–µ—Б–Ї–Њ–є –ї–Є—Е–Њ—А–∞–і–Ї–Є, –љ–µ —Б–Њ–Њ—В–≤–µ—В—Б—В–≤—Г–µ—В —В–∞–Ї–Њ–≤–Њ–є –і–ї—П –њ—А–µ–і—Г–њ—А–µ–ґ–і–µ–љ–Є—П –Ш–≠. –Ъ—А–Њ–Љ–µ —В–Њ–≥–Њ, —Г —Н—В–Є—Е –±–Њ–ї—М–љ—Л—Е, –Њ—Б–Њ–±–µ–љ–љ–Њ –њ—А–Є –і–ї–Є—В–µ–ї—М–љ–Њ–Љ –њ–µ—А–Њ—А–∞–ї—М–љ–Њ–Љ –њ—А–Є–µ–Љ–µ –њ–µ–љ–Є—Ж–Є–ї–ї–Є–љ–Њ–≤—Л—Е –њ—А–µ–њ–∞—А–∞—В–Њ–≤, —Б—Г—Й–µ—Б—В–≤—Г–µ—В –≤—Л—Б–Њ–Ї–∞—П –≤–µ—А–Њ—П—В–љ–Њ—Б—В—М –љ–Њ—Б–Є—В–µ–ї—М—Б—В–≤–∞ –Ј–µ–ї–µ–љ—П—Й–Є—Е —Б—В—А–µ–њ—В–Њ–Ї–Њ–Ї–Ї–Њ–≤, —П–≤–ї—П—О—Й–Є—Е—Б—П –Њ—В–љ–Њ—Б–Є—В–µ–ї—М–љ–Њ —Г—Б—В–Њ–є—З–Є–≤—Л–Љ–Є –Ї –∞–љ—В–Є–±–Є–Њ—В–Є–Ї–∞–Љ —Н—В–Њ–є –≥—А—Г–њ–њ—Л. –Т –њ–Њ–і–Њ–±–љ—Л—Е —Б–Є—В—Г–∞—Ж–Є—П—Е –і–ї—П –њ—А–Њ—Д–Є–ї–∞–Ї—В–Є–Ї–Є –Ш–≠ —А–µ–Ї–Њ–Љ–µ–љ–і—Г–µ—В—Б—П –љ–∞–Ј–љ–∞—З–∞—В—М –Ї–ї–Є–љ–і–∞–Љ–Є—Ж–Є–љ –Є–ї–Є –Љ–∞–Ї—А–Њ–ї–Є–і—Л (–∞–Ј–Є—В—А–Њ–Љ–Є—Ж–Є–љ, –Ї–ї–∞—А–Є—В—А–Њ–Љ–Є—Ж–Є–љ).
–Я—А–Є —Е–Є—А—Г—А–≥–Є—З–µ—Б–Ї–Є—Е –≤–Љ–µ—И–∞—В–µ–ї—М—Б—В–≤–∞—Е –љ–∞ –Є–љ—Д–Є—Ж–Є—А–Њ–≤–∞–љ–љ—Л—Е —В–Ї–∞–љ—П—Е –љ–µ—А–µ–і–Ї–Њ –≤–Њ–Ј–љ–Є–Ї–∞–µ—В –±–∞–Ї—В–µ—А–Є–µ–Љ–Є—П, –Њ–±—Г—Б–ї–Њ–≤–ї–µ–љ–љ–∞—П –≤–Њ–Ј–±—Г–і–Є—В–µ–ї—П–Љ–Є –њ–µ—А–≤–Є—З–љ–Њ–є –Є–љ—Д–µ–Ї—Ж–Є–Є. –Ф–ї—П –њ—А–Њ—Д–Є–ї–∞–Ї—В–Є–Ї–Є –Ш–≠ —Г —В–∞–Ї–Є—Е –±–Њ–ї—М–љ—Л—Е –Є—Б–њ–Њ–ї—М–Ј—Г—О—В –∞–љ—В–Є–±–Є–Њ—В–Є–Ї–Є —Б –Љ–∞–Ї—Б–Є–Љ–∞–ї—М–љ–Њ–є –∞–Ї—В–Є–≤–љ–Њ—Б—В—М—О –≤ –Њ—В–љ–Њ—И–µ–љ–Є–Є –≤–µ—А–Њ—П—В–љ—Л—Е –Є–љ—Д–µ–Ї—В–Њ–≥–µ–љ–Њ–≤. –Т —З–∞—Б—В–љ–Њ—Б—В–Є, –њ—А–Є –Є–љ—Д–µ–Ї—Ж–Є—П—Е –Љ—П–≥–Ї–Є—Е —В–Ї–∞–љ–µ–є, –Ї–Њ—Б—В–µ–є –Є–ї–Є —Б—Г—Б—В–∞–≤–Њ–≤ –њ–Њ–Ї–∞–Ј–∞–љ–Њ –љ–∞–Ј–љ–∞—З–µ–љ–Є–µ –∞–љ—В–Є—Б—В–∞—Д–Є–ї–Њ–Ї–Њ–Ї–Ї–Њ–≤—Л—Е –њ–µ–љ–Є—Ж–Є–ї–ї–Є–љ–Њ–≤ –Є–ї–Є —Ж–µ—Д–∞–ї–Њ—Б–њ–Њ—А–Є–љ–Њ–≤ I –њ–Њ–Ї–Њ–ї–µ–љ–Є—П, –∞ –њ—А–Є –Є–љ—Д–µ–Ї—Ж–Є—П—Е –Љ–Њ—З–µ–≤—Л—Е –њ—Г—В–µ–є - –∞–Љ–Є–љ–Њ–≥–ї–Є–Ї–Њ–Ј–Є–і–Њ–≤, —Ж–µ—Д–∞–ї–Њ—Б–њ–Њ—А–Є–љ–Њ–≤ III –њ–Њ–Ї–Њ–ї–µ–љ–Є—П –Є–ї–Є —Д—В–Њ—А—Е–Є–љ–Њ–ї–Њ–љ–Њ–≤.
–£—З–Є—В—Л–≤–∞—П —Б–њ–µ–Ї—В—А –њ–Њ—В–µ–љ—Ж–Є–∞–ї—М–љ—Л—Е –≤–Њ–Ј–±—Г–і–Є—В–µ–ї–µ–є –Ш–≠ –њ—А–Є –Њ–њ–µ—А–∞—Ж–Є—П—Е –љ–∞ –Њ—В–Ї—А—Л—В–Њ–Љ —Б–µ—А–і—Ж–µ (St. aureus, –Ї–Њ–∞–≥—Г–ї–∞–Ј–Њ–љ–µ–≥–∞—В–Є–≤–љ—Л–µ —Б—В–∞—Д–Є–ї–Њ–Ї–Њ–Ї–Ї–Є, –і–Є—Д—В–µ—А–Њ–Є–і—Л), –≤ –њ—А–Њ—Д–Є–ї–∞–Ї—В–Є—З–µ—Б–Ї–Є—Е —Ж–µ–ї—П—Е –Њ–±—Л—З–љ–Њ –њ—А–Є–Љ–µ–љ—П—О—В —Ж–µ—Д–∞–ї–Њ—Б–њ–Њ—А–Є–љ—Л I –њ–Њ–Ї–Њ–ї–µ–љ–Є—П. –Ю–і–љ–∞–Ї–Њ –±–Њ–ї—М—И–Њ–µ –≤–ї–Є—П–љ–Є–µ –љ–∞ –≤—Л–±–Њ—А –њ—А–µ–њ–∞—А–∞—В–∞ –Њ–Ї–∞–Ј—Л–≤–∞—О—В –і–∞–љ–љ—Л–µ –њ–Њ –∞–љ—В–Є–±–Є–Њ—В–Є–Ї–Њ—А–µ–Ј–Є—Б—В–µ–љ—В–љ–Њ—Б—В–Є –≤ –Ї–Њ–љ–Ї—А–µ—В–љ–Њ–Љ —Б—В–∞—Ж–Є–Њ–љ–∞—А–µ. –Я—А–Є –≤—Л—Б–Њ–Ї–Њ–є —А–∞—Б–њ—А–Њ—Б—В—А–∞–љ–µ–љ–љ–Њ—Б—В–Є –Љ–µ—В–Є—Ж–Є–ї–ї–Є–љ-—А–µ–Ј–Є—Б—В–µ–љ—В–љ—Л—Е —Б—В–∞—Д–Є–ї–Њ–Ї–Њ–Ї–Ї–Њ–≤ –і–ї—П –њ–µ—А–Є–Њ–њ–µ—А–∞—Ж–Є–Њ–љ–љ–Њ–є –њ—А–Њ—Д–Є–ї–∞–Ї—В–Є–Ї–Є —А–µ–Ї–Њ–Љ–µ–љ–і—Г–µ—В—Б—П –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞—В—М –≤–∞–љ–Ї–Њ–Љ–Є—Ж–Є–љ.
–Т –Ј–∞–Ї–ї—О—З–µ–љ–Є–µ —Е–Њ—В–µ–ї–Њ—Б—М –±—Л –Њ—В–Љ–µ—В–Є—В—М, —З—В–Њ –Ш–≠ –Љ–Њ–ґ–µ—В —А–∞–Ј–≤–Є—В—М—Б—П, –і–∞–ґ–µ –љ–µ—Б–Љ–Њ—В—А—П –љ–∞ —Б–Њ–Њ—В–≤–µ—В—Б—В–≤—Г—О—Й—Г—О –∞–љ—В–Є–±–Є–Њ—В–Є–Ї–Њ–њ—А–Њ—Д–Є–ї–∞–Ї—В–Є–Ї—Г. –Я–Њ—Н—В–Њ–Љ—Г –њ—А–Є –њ–Њ—П–≤–ї–µ–љ–Є–Є, –љ–∞ –њ–µ—А–≤—Л–є –≤–Ј–≥–ї—П–і, –Љ–∞–ї–Њ–Њ–±—К—П—Б–љ–Є–Љ–Њ–є –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Њ–є —Б–Є–Љ–њ—В–Њ–Љ–∞—В–Є–Ї–Є (—Б—Г–±—Д–µ–±—А–Є–ї–Є—В–µ—В, —Б–ї–∞–±–Њ—Б—В—М, –∞–њ–∞—В–Є—П, –љ–µ–і–Њ–Љ–Њ–≥–∞–љ–Є–µ), –њ–Њ—Б–ї–µ–і–Њ–≤–∞–≤—И–µ–є –Ј–∞ —Б—В–Њ–Љ–∞—В–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є–Љ–Є –Є–ї–Є —Е–Є—А—Г—А–≥–Є—З–µ—Б–Ї–Є–Љ–Є –њ—А–Њ—Ж–µ–і—Г—А–∞–Љ–Є —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –Ї–∞—А–і–Є–Њ–≥–µ–љ–љ—Л–Љ–Є —Д–∞–Ї—В–Њ—А–∞–Љ–Є —А–Є—Б–Ї–∞ –Ш–≠, –≤—А–∞—З –і–Њ–ї–ґ–µ–љ —Б–Њ—Е—А–∞–љ—П—В—М –≤—Л—Б–Њ–Ї–Є–є «–Є–љ–і–µ–Ї—Б –љ–∞—Б—В–Њ—А–Њ–ґ–µ–љ–љ–Њ—Б—В–Є» –≤ –Њ—В–љ–Њ—И–µ–љ–Є–Є —Н—В–Њ–≥–Њ –≥—А–Њ–Ј–љ–Њ–≥–Њ –Є –Ї–Њ–≤–∞—А–љ–Њ–≥–Њ –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П.
1. Wilson W.R., Karchmer A.W., Dajani A.S. et al. Antibiotic treatment of adults with infective endocarditis due to Streptococci, Enterococci, Staphylococci and HACEK microorganisms. JAMA 1995; 274 (21): 1706 - 1713.
2. Baldassarre J.S., Kaye D. Principles and overview of antibiotic therapy. In: Kaye D., editor, . Infective endocarditis. New York: Raven Press, 1992; 169-190.
3. Francioli P. Etienne J., Hoigne R. et al. Treatment of streptococcal endocarditis with a single daily dose of ceftriaxone sodium for 4 weeks: efficacy and outpatient treatment feasibility. JAMA 1992; 267: 264 - 267.
4. Francioli P., Ruch W., Stamboulian D. Et al. Treatment of streptococcal endocarditis with a single daily dose of ceftriaxone and netylmicin for 14 days: a prospective multicenter study. Clin. Infect. Dis. 1995; 21; 1406-1410.
5. Eliopoulos G.M. Aminoglycoside resistant enterococcal endocarditis. Mad. Clin. North Am. 1993; 17: 117 - 127.
6. Korzeniowski O., Sande M.A., the National Collaborative Endocarditis Study Group. Combination antimicrobial therapy for Staphylococcus aureus endocarditis in patient addicted to parenteral drugs and in nonaddicts: a prospective study. Ann. Intern. Med. 1982; 97: 496 - 503.
7. Karchmer A.W. Staphylococcus aureus and vancomycin: the sequel. Ann. Intern. Med. 1991; 115: 739 - 741.
8. Chambers H.F., Miller T., Newman M.D. Right-sided Staphylococcus aureus endocarditis in intravenous drug abusers: two-week combination therapy. Ann. Intern. Med. 1988; 109: 619 - 624.
9. Dworkin R.J., Lee B.L., Sande M.A., Chambers H.F. Treatment of right-sided Staphylococcus aureus endocarditis in intravenous drug users with ciprofloxacin and rifampicin. Lancet 1989; 2: 1071 - 1073.
10. Karchmer A.W., Archer G.L., Dismukes W.E. Staphylococcus epidermidis causing prosthetic valve endocarditis: microbiologic and clinical observations as guides to therapy. Ann. Intern. Med. 1983; 98: 447 - 455.
11. Karchmer A.W. Staphylococcal endocarditis. In: Kaye D., editor, . Infective endocarditis. New York: Raven Press, 1992; 225-249.
12. Andrade-Baiocchi S., Tognim M.C., Baiocchi O.C., Sader H.S. Endocarditis due to glycopeptides-intermediate Staphylococcus aureus: case report and strain characterization. Diagn. Microbiol. Infect.Dis. 2003; 45(2): 149-152.
13. Birmingham M.C., Rayner C.R., Meagher A.K. et al.Linezoliod for the treatment of multidrug-resistant, gram-positive infectious: experience from compassionable-use programm.// Clin. Infect. Dis. 2003; 36(2): 159-168.
14. Rao N., White G.J. Successful treatment of Enterococcus faecalis prosthetic valve endocarditis with linezolid. Clin. Infect. Dis. 2002; 35(7): 902-904.
15. Reyes M.P., Lerner A.M. Current problems in the treatment of infective endocarditis due to Pseudomonas aeruginosa. Rev. Infect. Dis. 1983; 5: 314 - 321.
16. Bayer A.S., Bolger A.F., Taubert K.A> et al. Diagnosis and management of infective endocarditis and its complications. Circulation. 1998; 98: 2936 - 2948.
17. Andriole V.T. Current and future antifungal therapy: new targets for antifungal therapy. Int. J. Antimicrob. Agents. 2000; 16: 317-321.
18. Sabo J.A., Abdel-Rahman S.M. Voriconazole: a new triazole antifungal. Ann. Pharmacother. 2000; 34: 1032-1043.
19. Dajani A.S., Taubert K.A., Wilson W. et al. Prevention of bacterial endocarditis: recommendations of American Heart Association. JAMA 1997; 277: 1794 - 1801.
20. Dajani A.S., Bawdon R.E., Berry M.C. Oral amoxicillin as prophylaxis for endocarditis: what is the optimal dose? Clin. Infect. Dis. 1994; 18: 157 - 160.
21. Dajani A.S., Bisno A.L., Chung K.J. et al. Prevention of bacterial endocarditis. JAMA 1990; 264: 2919-2922.












