–Ъ bвАУ–ї–∞–Ї—В–∞–Љ–љ—Л–Љ –∞–љ—В–Є–±–Є–Њ—В–Є–Ї–∞–Љ –Њ—В–љ–Њ—Б—П—В—Б—П –њ–µ–љ–Є—Ж–Є–ї–ї–Є–љ—Л, —Ж–µ—Д–∞–ї–Њ—Б–њ–Њ—А–Є–љ—Л, –Ї–∞—А–±–∞–њ–µ–љ–µ–Љ—Л. –Ю–±—Й–Є–Љ —Д—А–∞–≥–Љ–µ–љ—В–Њ–Љ –≤ —Е–Є–Љ–Є—З–µ—Б–Ї–Њ–є —Б—В—А—Г–Ї—В—Г—А–µ bвАУ–ї–∞–Ї—В–∞–Љ–љ—Л—Е –∞–љ—В–Є–±–Є–Њ—В–Є–Ї–Њ–≤ —П–≤–ї—П–µ—В—Б—П bвАУ–ї–∞–Ї—В–∞–Љ–љ–Њ–µ –Ї–Њ–ї—М—Ж–Њ, –Є–Љ–µ–љ–љ–Њ —Б –µ–≥–Њ –љ–∞–ї–Є—З–Є–µ–Љ —Б–≤—П–Ј–∞–љ–∞ –Љ–Є–Ї—А–Њ–±–Є–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–∞—П –∞–Ї—В–Є–≤–љ–Њ—Б—В—М —Н—В–Є—Е –њ—А–µ–њ–∞—А–∞—В–Њ–≤. –Ь–Є—И–µ–љ—М—О –і–µ–є—Б—В–≤–Є—П bвАУ–ї–∞–Ї—В–∞–Љ–љ—Л—Е –∞–љ—В–Є–±–Є–Њ—В–Є–Ї–Њ–≤ –≤ –Љ–Є–Ї—А–Њ–±–љ–Њ–є –Ї–ї–µ—В–Ї–µ —П–≤–ї—П—О—В—Б—П —Д–µ—А–Љ–µ–љ—В—Л —В—А–∞–љ—БвАУ –Є –Ї–∞—А–±–Њ¬≠–Ї—Б–Є–њ–µ–њ—В–Є–і–∞–Ј—Л, —Г—З–∞—Б—В–≤—Г—О—Й–Є–µ –≤ —Б–Є–љ—В–µ–Ј–µ –Њ—Б–љ–Њ–≤–љ–Њ–≥–Њ –Ї–Њ–Љ–њ–Њ–љ–µ–љ—В–∞ –љ–∞—А—Г–ґ–љ–Њ–є –Љ–µ–Љ–±—А–∞–љ—Л –Љ–Є–Ї—А–Њ–Њ—А–≥–∞–љ–Є–Ј–Љ–Њ–≤ вАУ –њ–µ–њ—В–Є–і–Њ–≥–ї–Є–Ї–∞–љ–∞. –≠—В–Є —Д–µ—А–Љ–µ–љ—В—Л —В–∞–Ї–ґ–µ –љ–∞–Ј—Л–≤–∞—О—В—Б—П ¬Ђ–њ–µ–љ–Є—Ж–Є–ї–ї–Є–љ—Б–≤—П–Ј—Л–≤–∞—О—Й–Є–µ –±–µ–ї–Ї–Є¬ї.
–Ю–±—Й–Є–Љ–Є —Б–≤–Њ–є—Б—В–≤–∞–Љ–Є –≤—Б–µ—Е bвАУ–ї–∞–Ї—В–∞–Љ–љ—Л—Е –∞–љ—В–Є–±–Є–Њ—В–Є–Ї–Њ–≤ —П–≤–ї—П–µ—В—Б—П –±—Л—Б—В—А–Њ–µ –±–∞–Ї—В–µ—А–Є—Ж–Є–і–љ–Њ–µ –і–µ–є—Б—В–≤–Є–µ –љ–∞ –Љ–Є–Ї—А–Њ–±–љ—Г—О –Ї–ї–µ—В–Ї—Г. –Т —В–Њ –ґ–µ –≤—А–µ–Љ—П, –Є–љ–і–Є–≤–Є–і—Г–∞–ї—М–љ—Л–µ —Б–≤–Њ–є—Б—В–≤–∞ –Њ—В–і–µ–ї—М–љ—Л—Е bвАУ–ї–∞–Ї—В–∞–Љ–Њ–≤ –Њ–њ—А–µ–і–µ–ї—П–µ—В—Б—П –Є—Е —Б–њ–Њ—Б–Њ–±–љ–Њ—Б—В—М—О –њ—А–Њ–љ–Є–Ї–∞—В—М —З–µ—А–µ–Ј –Ї–ї–µ—В–Њ—З–љ—Г—О —Б—В–µ–љ–Ї—Г –Љ–Є–Ї—А–Њ–Њ—А–≥–∞–љ–Є–Ј–Љ–Њ–≤, –∞—Д—Д–Є–љ–љ–Њ—Б—В—М—О –Ї –њ–µ–љ–Є—Ж–Є–ї–ї–Є–љ—Б–≤—П–Ј—Л–≤–∞—О—Й–Є–Љ –±–µ–ї–Ї–∞–Љ, —Г—Б—В–Њ–є—З–Є–≤–Њ—Б—В—М—О –Ї –≥–Є–і—А–Њ–ї–Є–Ј—Г bвАУ–ї–∞–Ї—В–∞–Љ–∞–Ј–∞–Љ–Є. –Т —Б–≤—П–Ј–Є —Б —Н—В–Є–Љ–Є –Њ—Б–Њ–±–µ–љ–љ–Њ—Б—В—П–Љ–Є –њ—А–µ–њ–∞—А–∞—В—Л –Ї–ї–∞—Б—Б–∞ bвАУ–ї–∞–Ї—В–∞–Љ–Њ–≤ —Б—Г—Й–µ—Б—В–≤–µ–љ–љ–Њ –Њ—В–ї–Є—З–∞—О—В—Б—П –Љ–µ–ґ–і—Г —Б–Њ–±–Њ–є –њ–Њ —Г—А–Њ–≤–љ—О –њ—А–Є—А–Њ–і–љ–Њ–є –∞–љ—В–Є–Љ–Є–Ї—А–Њ–±–љ–Њ–є –∞–Ї—В–Є–≤–љ–Њ—Б—В–Є, –њ—А–Є–Њ–±—А–µ—В–µ–љ–љ–Њ–є —Г—Б—В–Њ–є—З–Є–≤–Њ—Б—В–Є, —З—В–Њ –Њ–њ—А–µ–і–µ–ї—П–µ—В –Њ—Б–Њ–±—Л–µ –њ–Њ–Ї–∞–Ј–∞–љ–Є—П –Ї –њ—А–Є–Љ–µ–љ–µ–љ–Є—О –Ї–∞–ґ–і–Њ–≥–Њ –Є–Ј –њ—А–µ–њ–∞—А–∞—В–Њ–≤. –Т –љ–∞—Б—В–Њ—П—Й–µ–є —А–∞–±–Њ—В–µ –њ—А–Њ–∞–љ–∞–ї–Є–Ј–Є—А–Њ–≤–∞–љ—Л –∞–љ—В–Є–Љ–Є–Ї—А–Њ–±–љ—Л–µ —Б–≤–Њ–є—Б—В–≤–∞ bвАУ–ї–∞–Ї—В–∞–Љ–љ—Л—Е –∞–љ—В–Є–±–Є–Њ—В–Є–Ї–Њ–≤ –Є –Њ–њ—А–µ–і–µ–ї–µ–љ—Л –Њ—Б–љ–Њ–≤–љ—Л–µ –њ–Њ–Ј–Є—Ж–Є–Є –Ї–∞–ґ–і–Њ–≥–Њ –Є–Ј –њ—А–µ–њ–∞—А–∞—В–Њ–≤ –і–ї—П –ї–µ—З–µ–љ–Є—П –Є–љ—Д–µ–Ї—Ж–Є–є –≤ —Б—В–∞—Ж–Є–Њ–љ–∞—А–µ, —З—В–Њ –њ–Њ–Љ–Њ–ґ–µ—В —Б–њ–µ—Ж–Є–∞–ї–Є—Б—В–∞–Љ –§–Њ—А–Љ—Г–ї—П—А–љ–Њ–≥–Њ –Ъ–Њ–Љ–Є—В–µ—В–∞ –Њ–±–Њ—Б–љ–Њ–≤–∞—В—М –Є –њ–ї–∞–љ–Є—А–Њ–≤–∞—В—М –њ—А–Є–Љ–µ–љ–µ–љ–Є—П –∞–љ—В–Є–±–Є–Њ—В–Є–Ї–Њ–≤ –≤ –ї–µ—З–µ–±–љ–Њ–Љ —Г—З—А–µ–ґ–і–µ–љ–Є–Є.
–Ъ –≥—А—Г–њ–њ–µ –њ–µ–љ–Є—Ж–Є–ї–ї–Є–љ–Њ–≤ –Њ—В–љ–Њ—Б—П—В—Б—П –њ—А–Є—А–Њ–і–љ—Л–µ –∞–љ—В–Є–±–Є–Њ—В–Є–Ї–Є (–±–µ–љ–Ј–Є–ї–њ–µ–љ–Є—Ж–Є–ї–ї–Є–љ) –Є –њ–Њ–ї—Г—Б–Є–љ—В–µ—В–Є—З–µ—Б–Ї–Є–µ (–∞–Љ–Є–љ–Њ–њ–µ–љ–Є—Ж–Є–ї–ї–Є–љ—Л, –њ–µ–љ–Є—Ж–Є–ї–ї–Є–љ–∞–Ј–Њ—Б—В–∞–±–Є–ї—М–љ—Л–µ, –Ї–∞—А–±–Њ–Ї—Б–ЄвАУ –Є —Г—А–µ–Є–і–Њ–њ–µ–љ–Є—Ж–Є–ї–ї–Є–љ—Л, –Є–љ–≥–Є–±–Є—В–Њ—А–Ј–∞—Й–Є—Й–µ–љ–љ—Л–µ).
–С–µ–љ–Ј–Є–ї–њ–µ–љ–Є—Ж–Є–ї–ї–Є–љ
–Р–Ї—В–Є–≤–µ–љ –≥–ї–∞–≤–љ—Л–Љ –Њ–±—А–∞–Ј–Њ–Љ –њ—А–Њ—В–Є–≤ –≥—А–∞–Љ–њ–Њ–ї–Њ–ґ–Є—В–µ–ї—М–љ—Л—Е –Є –≥—А–∞–Љ–Њ—В—А–Є—Ж–∞—В–µ–ї—М–љ—Л—Е –Ї–Њ–Ї–Ї–Њ–≤: —Б—В–∞—Д–Є–ї–Њ–Ї–Њ–Ї–Ї–Њ–≤ (–Ї—А–Њ–Љ–µ –њ—А–Њ–і—Г—Ж–Є—А—Г—О—Й–Є—Е –њ–µ–љ–Є—Ж–Є–ї–ї–Є–љ–∞–Ј—Г), —Б—В—А–µ–њ—В–Њ–Ї–Њ–Ї–Ї–Њ–≤, –њ–љ–µ–≤–Љ–Њ–Ї–Њ–Ї–Ї–Њ–≤, E. faecalis (–≤ –Љ–µ–љ—М—И–µ–є —Б—В–µ–њ–µ–љ–Є), N. gonorrhoeae, N. meningitidis; –њ—А–Њ—П–≤–ї—П–µ—В –≤—Л—Б–Њ–Ї—Г—О –∞–Ї—В–Є–≤–љ–Њ—Б—В—М –њ—А–Њ—В–Є–≤ –∞–љ–∞—Н—А–Њ–±–Њ–≤, C. diphtheriae, L. monocytogenes , T. pallidum, B. burgdorferi, Leptospira. –Я–Њ –і–µ–є—Б—В–≤–Є—О –љ–∞ –Ї–Њ–Ї–Ї–Њ–≤—Г—О —Д–ї–Њ¬≠—А—Г –њ—А–µ–≤–Њ—Б—Е–Њ–і–Є—В –і—А—Г–≥–Є–µ –њ–µ–љ–Є—Ж–Є–ї–ї–Є–љ—Л –Є —Ж–µ—Д–∞–ї–Њ—Б–њ–Њ—А–Є–љ—Л IвАУII –њ–Њ–Ї–Њ–ї–µ–љ–Є—П. –Т —В–Њ –ґ–µ –≤—А–µ–Љ—П –њ—А–Є–Љ–µ–љ–µ–љ–Є–µ –±–µ–љ–Ј–Є–ї–њ–µ–љ–Є—Ж–Є–ї–ї–Є–љ–∞ –ї–Є–Љ–Є—В–Є—А–Њ–≤–∞–љ–Њ –≤—Л—Б–Њ–Ї–Є–Љ —Г—А–Њ–≤–љ–µ–Љ —А–µ–Ј–Є—Б—В–µ–љ—В–љ–Њ—Б—В–Є, –≥–ї–∞–≤–љ—Л–Љ –Њ–±—А–∞–Ј–Њ–Љ, —Б—В–∞—Д–Є–ї–Њ–Ї–Њ–Ї–Ї–Њ–≤ (–і–Њ 95%) –Є –њ–љ–µ–≤–Љ–Њ–Ї–Њ–Ї–Ї–Њ–≤ (10вАУ20%). –Ю—Б–љ–Њ–≤–љ–Њ–µ –њ–Њ–Ї–∞–Ј–∞–љ–Є–µ –і–ї—П –њ—А–Є–Љ–µ–љ–µ–љ–Є—П –±–µ–љ–Ј–Є–ї–њ–µ–љ–Є—Ж–Є–ї–ї–Є–љ–∞ –≤ —Б—В–∞—Ж–Є–Њ–љ–∞—А–µ —П–≤–ї—П—О—В—Б—П –љ–µ–Њ—Б–ї–Њ–ґ–љ–µ–љ–љ—Л–µ —Б—В—А–µ–њ—В–Њ–Ї–Њ–Ї–Ї–Њ–≤—Л–µ –Є–љ—Д–µ–Ї—Ж–Є–Є –Ї–Њ–ґ–Є –Є –Љ—П–≥–Ї–Є—Е —В–Ї–∞–љ–µ–є (—А–Њ–ґ–∞) –Є –Љ–µ–љ–Є–љ–≥–Њ–Ї–Њ–Ї–Ї–Њ–≤–∞—П –Є–љ—Д–µ–Ї—Ж–Є—П. –С–µ–љ¬≠–Ј–Є–ї¬≠–њ–µ¬≠–љ–Є¬≠—Ж–Є–ї¬≠–ї–Є–љ (–≤ —Б–Њ—З–µ—В–∞–љ–Є–Є —Б –Ї–ї–Є–љ–і–∞–Љ–Є—Ж–Є–љ–Њ–Љ) —В–∞–Ї–ґ–µ —П–≤–ї—П–µ—В—Б—П —Б—А–µ–і—Б—В–≤–Њ–Љ –≤—Л¬≠–±–Њ—А–∞ –ї–µ—З–µ–љ–Є—П –Ї–ї–Њ—Б—В—А–Є–і–Є–∞–ї—М–љ–Њ–є –Є–љ—Д–µ–Ї—Ж–Є–Є –Љ—П–≥–Ї–Є—Е —В–Ї–∞–љ–µ–є. –Т –і—А—Г¬≠–≥–Є—Е –њ–Њ—В–µ–љ—Ж–Є–∞–ї—М–љ–Њ –≤–Њ–Ј–Љ–Њ–ґ–љ—Л—Е —Б–Є—В—Г–∞—Ж–Є—П—Е (–Є–љ—Д–µ–Ї—Ж–Є–Є –і—Л—Е–∞—В–µ–ї—М–љ—Л—Е –њ—Г—В–µ–є, —Н–љ—В–µ—А–Њ–Ї–Њ–Ї–Ї–Њ–≤—Л–µ –Є–љ—Д–µ–Ї—Ж–Є–Є) –≤–Љ–µ—Б—В–Њ –±–µ–љ–Ј–Є–ї–њ–µ–љ–Є—Ж–Є–ї–ї–Є¬≠–љ–∞ –Љ–Њ–ґ¬≠–љ–Њ –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞—В—М –∞–Љ–Є–љ–Њ–њ–µ–љ–Є—Ж–Є–ї–ї–Є–љ—Л.
–Р–Љ–Є–љ–Њ–њ–µ–љ–Є—Ж–Є–ї–ї–Є–љ—Л (–∞–Љ–њ–Є—Ж–Є–ї–ї–Є–љ)
–°–њ–µ–Ї—В—А –∞–Ї—В–Є–≤–љ–Њ—Б—В–Є –±–ї–Є–Ј–Њ–Ї –Ї –±–µ–љ–Ј–Є–ї–њ–µ–љ–Є—Ж–Є–ї–ї–Є–љ—Г (–≥—А–∞–Љ–њ–Њ–ї–Њ–ґ–Є—В–µ–ї—М–љ—Л–µ –Є –≥—А–∞–Љ–Њ—В—А–Є—Ж–∞—В–µ–ї—М–љ—Л–µ –Ї–Њ–Ї–Ї–Є), –Ї—А–Њ–Љ–µ —В–Њ–≥–Њ, –∞–Ї—В–Є–≤–µ–љ –≤ –Њ—В–љ–Њ—И–µ–љ–Є–Є –≥—А–∞–Љ–Њ—В—А–Є—Ж–∞—В–µ–ї—М–љ—Л—Е –±–∞–Ї—В–µ—А–Є–є вАУ E. —Бoli –Є Proteus mirabilis. –Э–µ —Б—В–∞–±–Є–ї–µ–љ –Ї bвАУ–ї–∞–Ї—В–∞–Љ–∞–Ј–∞–Љ —Б—В–∞—Д–Є–ї–Њ–Ї–Њ–Ї–Ї–Њ–≤ –Є –≥—А–∞–Љ–Њ—В—А–Є—Ж–∞—В–µ–ї—М–љ—Л—Е –±–∞–Ї—В–µ—А–Є–є. –Я—А–µ–њ–∞—А–∞—В —Е–∞—А–∞–Ї—В–µ—А–Є–Ј—Г–µ—В—Б—П –љ–Є–Ј–Ї–Њ–є –±–Є–Њ–і–Њ—Б—В—Г–њ–љ–Њ—Б—В—М—О, –њ–Њ—Н—В–Њ–Љ—Г —Ж–µ–ї–µ—Б–Њ–Њ–±—А–∞–Ј–љ–Њ –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞—В—М —В–Њ–ї—М–Ї–Њ –њ–∞—А–µ–љ—В–µ—А–∞–ї—М–љ—Г—О —Д–Њ—А–Љ—Г.
–Ю—Б–љ–Њ–≤–љ—Л–µ –њ–Њ–Ї–∞–Ј–∞–љ–Є—П:
вАҐ –Ш–љ—Д–µ–Ї—Ж–Є–Є, –≤—Л–Ј–≤–∞–љ–љ—Л–µ Enterococcus faecalis (—Б—А–µ–і—Б—В–≤–Њ –≤—Л–±–Њ—А–∞). –£—Б—В–Њ–є—З–Є–≤–Њ—Б—В—М —Н–µ—В–µ—А–Њ–Ї–Њ–Ї–Ї–Њ–≤ –Ї –∞–Љ–њ–Є—Ж–Є–ї–ї–Є–љ—Г –≤ –†–§ –љ–µ –њ—А–µ–≤—Л—И–∞–µ—В 10%. –Я—А–Є –±–∞–Ї—В–µ—А–Є–µ–Љ–Є–Є/—Б–µ–њ—Б–Є—Б–µ —Б—Г—В–Њ—З–љ–∞—П –і–Њ–Ј–∞ –і–Њ–ї–ґ–љ–∞ –±—Л—В—М –љ–µ –љ–Є–ґ–µ 8 –≥.
вАҐ –Э–µ—В—П–ґ–µ–ї—Л–µ –≤–љ–µ–±–Њ–ї—М–љ–Є—З–љ—Л–µ –Є–љ—Д–µ–Ї—Ж–Є–Є –љ–Є–ґ–љ–Є—Е –і—Л—Е–∞—В–µ–ї—М–љ—Л—Е –њ—Г—В–µ–є вАУ –њ–љ–µ–≤–Љ–Њ–љ–Є–Є –Є –±—А–Њ–љ—Е–Є—В. –Я—А–Є –љ–µ—В—П–ґ–µ–ї–Њ–є –њ–љ–µ–≤–Љ–Њ–љ–Є–Є –љ–µ —Г—Б—В—Г–њ–∞–µ—В –≤ —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В–Є –Љ–∞–Ї—А–Њ–ї–Є–і–∞–Љ –Є —Ж–µ—Д–∞–ї–Њ—Б–њ–Њ—А–Є–љ–∞–Љ IIвАУIII –њ–Њ–Ї–Њ–ї–µ–љ–Є—П. –≠—Д—Д–µ–Ї—В–Є–≤–µ–љ –≤ —Б—Г—В–Њ—З–љ–Њ–є –і–Њ–Ј–µ 4 –≥.
вАҐ –Ш–љ—Д–µ–Ї—Ж–Є–Њ–љ–љ—Л–є —Н–љ–і–Њ–Ї–∞—А–і–Є—В –љ–∞—В–Є–≤–љ–Њ–≥–Њ –Ї–ї–∞–њ–∞–љ–∞ вАУ –≤ –Ї–∞—З–µ—Б—В–≤–µ —Б—А–µ–і—Б—В–≤–∞ —Н–Љ–њ–Є—А–Є—З–µ—Б–Ї–Њ–є —В–µ—А–∞–њ–Є–Є –Є–ї–Є –њ—А–Є —Г—Б—В–∞–љ–Њ–≤–ї–µ–љ–љ–Њ–є —Б—В—А–µ–њ—В–Њ–Ї–Њ–Ї–Ї–Њ–≤–Њ–є/—Н–љ—В–µ—А–Њ–Ї–Њ–Ї–Ї–Њ–≤–Њ–є —Н—В–Є–Њ–ї–Њ–≥–Є–Є.
–Р–Љ–њ–Є—Ж–Є–ї–ї–Є–љ –љ–µ —Ж–µ–ї–µ—Б–Њ–Њ–±—А–∞–Ј–љ–Њ –њ—А–Є–Љ–µ–љ—П—В—М –њ—А–Є –Є–љ—Д–µ–Ї—Ж–Є—П—Е –Љ–Њ—З–µ–≤—Л–≤–Њ–і—П—Й–Є—Е –њ—Г—В–µ–є –Є–ЈвАУ–Ј–∞ –≤—Л—Б–Њ–Ї–Њ–≥–Њ —Г—А–Њ–≤–љ—П —Г—Б—В–Њ–є—З–Є–≤–Њ—Б—В–Є E. coli.
–Я–µ–љ–Є—Ж–Є–ї–ї–Є–љ–∞–Ј–Њ—Б—В–∞–±–Є–ї—М–љ—Л–µ –њ–µ–љ–Є—Ж–Є–ї–ї–Є–љ—Л (–Њ–Ї—Б–∞—Ж–Є–ї–ї–Є–љ)
–Р–Ї—В–Є–≤–µ–љ –≥–ї–∞–≤–љ—Л–Љ –Њ–±—А–∞–Ј–Њ–Љ –≤ –Њ—В–љ–Њ—И–µ–љ–Є–Є –У—А–∞–Љ(+) –Ї–Њ–Ї–Ї–Њ–≤ (Staphylococcus spp., S. pyogenes, S. pneumoniae, S. viridans, S. agalactiae); –љ–µ –і–µ–є—Б—В–≤—Г–µ—В –љ–∞ —Н–љ—В–µ—А–Њ–Ї–Њ–Ї–Ї–Є. –Я–Њ –њ—А–Є—А–Њ–і–љ–Њ–є –∞–Ї—В–Є–≤–љ–Њ—Б—В–Є –њ—А–Њ—В–Є–≤ –≥—А–∞–Љ–њ–Њ–ї–Њ–ґ–Є—В–µ–ї—М–љ—Л—Е –Ї–Њ–Ї–Ї–Њ–≤ —Г—Б—В—Г–њ–∞–µ—В –њ—А–Є—А–Њ–і–љ—Л–Љ –њ–µ–љ–Є—Ж–Є–ї–ї–Є–љ–∞–Љ. –°—В–∞–±–Є–ї–µ–љ –Ї —Б—В–∞—Д–Є–ї–Њ–Ї–Њ–Ї–Ї–Њ–≤—Л–Љ bвАУ–ї–∞–Ї—В–∞–Љ–∞–Ј–∞–Љ.
–Ю—Б–љ–Њ–≤–љ—Л–µ –њ–Њ–Ї–∞–Ј–∞–љ–Є—П:
вАҐ –Ш–љ—Д–µ–Ї—Ж–Є–Є, –≤—Л–Ј–≤–∞–љ–љ—Л–µ S. aureus –≤ —Б–ї—Г—З–∞–µ –і–Њ–Ї—Г–Љ–µ–љ—В–Є—А–Њ–≤–∞–љ–љ–Њ–є —З—Г–≤—Б—В–≤–Є—В–µ–ї—М–љ–Њ—Б—В–Є –Ї –Њ–Ї—Б–∞—Ж–Є–ї–ї–Є–љ—Г (—Б—А–µ–і—Б—В–≤–Њ –≤—Л–±–Њ—А–∞). –Я—А–Є –ї–Њ–Ї–∞–ї–Є–Ј–Њ–≤–∞–љ–љ—Л—Е –Є–љ—Д–µ–Ї—Ж–Є—П—Е вАУ 4вАУ6 –≥/—Б—Г—В., –њ—А–Є –±–∞–Ї—В–µ—А–Є–µ–Љ–Є–Є/—Б–µ–њ—Б–Є—Б–µ вАУ 8вАУ12 –≥/—Б—Г—В.
вАҐ –Ш–љ—Д–µ–Ї—Ж–Є–Є —Б –њ—А–µ–і–њ–Њ–ї–∞–≥–∞–µ–Љ–Њ–є —Б—В–∞—Д–Є–ї–Њ–Ї–Њ–Ї–Ї–Њ–≤–Њ–є —Н—В–Є–Њ–ї–Њ–≥–Є–µ–є:
вАУ –Э–µ–Њ—Б–ї–Њ–ґ–љ–µ–љ–љ—Л–µ –Є–љ—Д–µ–Ї—Ж–Є–Є –Ї–Њ–ґ–Є –Є –Љ—П–≥–Ї–Є—Е —В–Ї–∞–љ–µ–є (—Д—Г—А—Г–љ–Ї—Г–ї, –Ї–∞—А–±—Г–љ–Ї—Г–ї, –њ–Є–Њ–і–µ—А–Љ–Є—П –Є –і—А.)
вАУ –Ь–∞—Б—В–Є—В
вАУ –Ш–љ—Д–µ–Ї—Ж–Є–Њ–љ–љ—Л–є —Н–љ–і–Њ–Ї–∞—А–і–Є—В —Г –≤/–≤ –љ–∞—А–Ї–Њ–Љ–∞–љ–Њ–≤ (—Б—А–µ–і—Б—В–≤–Њ –≤—Л–±–Њ—А–∞)
вАУ –Ю—Б—В—А—Л–є –≥–љ–Њ–є–љ—Л–є –∞—А—В—А–Є—В (—Б—А–µ–і—Б—В–≤–Њ –≤—Л–±–Њ—А–∞)
вАУ –Ъ–∞—В–µ—В–µ—АвАУ–∞—Б—Б–Њ—Ж–Є–Є—А–Њ–≤–∞–љ–љ–∞—П –∞–љ–≥–Є–Њ–≥–µ–љ–љ–∞—П –Є–љ—Д–µ–Ї—Ж–Є—П
–Ъ–∞—А–±–Њ–Ї—Б–Є–њ–µ–љ–Є—Ж–Є–ї–ї–Є–љ—Л (–Ї–∞—А–±–µ–љ–Є—Ж–Є–ї–ї–Є–љ)
–•–∞—А–∞–Ї—В–µ—А–Є–Ј—Г–µ—В—Б—П —И–Є—А–Њ–Ї–Є–Љ –∞–љ—В–Є–Љ–Є–Ї—А–Њ–±–љ—Л–Љ —Б–њ–µ–Ї—В—А–Њ–Љ, –≤–Ї–ї—О—З–∞—П Pseudomonas aeruginosa. –Т —Б–Њ–≤—А–µ–Љ–µ–љ–љ–Њ–є —Б–Є—В—Г–∞—Ж–Є–Є –Њ—В–Љ–µ—З–∞–µ—В—Б—П –≤—Л—Б–Њ–Ї–Є–є —Г—А–Њ–≤–µ–љ—М —Г—Б—В–Њ–є—З–Є–≤–Њ—Б—В–Є –љ–Њ–Ј–Њ–Ї–Њ–Љ–Є–∞–ї—М–љ—Л—Е —И—В–∞–Љ–Љ–Њ–≤ –≥—А–∞–Љ–Њ—В—А–Є—Ж–∞—В–µ–ї—М–љ—Л—Е –±–∞–Ї—В–µ—А–Є–є –Ї –Ї–∞—А–±–µ–љ–Є—Ж–Є–ї–ї–Є–љ—Г (–≤—Л—И–µ, —З–µ–Љ –Ї —Ж–µ—Д–∞–ї–Њ—Б–њ–Њ—А–Є–љ–∞–Љ IIIвАУIV –њ–Њ–Ї–Њ–ї–µ–љ–Є—П –Є —Д—В–Њ—А—Е–Є–љ–Њ–ї–Њ–љ–∞–Љ), –њ–Њ—Н—В–Њ–Љ—Г –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є–µ –њ—А–µ–њ–∞—А–∞—В–∞ –њ—А–µ–і—Б—В–∞–≤–ї—П–µ—В—Б—П –љ–µ —Ж–µ–ї–µ—Б–Њ–Њ–±—А–∞–Ј–љ—Л–Љ.
–£—А–µ–Є–і–Њ–њ–µ–љ–Є—Ж–Є–ї–ї–Є–љ—Л
(–∞–Ј–ї–Њ—Ж–Є–ї–ї–Є–љ, –њ–Є–њ–µ—А–∞—Ж–Є–ї–ї–Є–љ)
–Т –љ–∞—Б—В–Њ—П—Й–µ–µ –≤—А–µ–Љ—П –≤ –Љ–µ–і–Є—Ж–Є–љ—Б–Ї–Њ–є –њ—А–∞–Ї—В–Є–Ї–µ –њ—А–Є–Љ–µ–љ—П–µ—В—Б—П —В–Њ–ї—М–Ї–Њ –Ї–Є–Љ–±–Є–љ–Є—А–Њ–≤–∞–љ–љ—Л–є –њ—А–µ–њ–∞—А–∞—В –њ–Є–њ–µ—А–∞—Ж–Є–ї–ї–Є–љ–∞ —Б –Є–љ–≥–Є–±–Є—В–Њ—А–Њ–≤ bвАУ–ї–∞–Ї—В–∞–Љ–∞–Ј —В–∞–Ј–Њ–±–∞–Ї—В–∞–Љ–Њ–Љ.
–Ш–љ–≥–Є–±–Є—В–Њ—А–Њ–Ј–∞—Й–Є—Й–µ–љ–љ—Л–µ –њ–µ–љ–Є—Ж–Є–ї–ї–Є–љ—Л
–Ъ –Є–љ–≥–Є–±–Є—В–Њ—А–Ј–∞—Й–Є—Й–µ–љ–љ—Л–Љ –њ–µ–љ–Є—Ж–Є–ї–ї–Є–љ–∞–Љ –Њ—В–љ–Њ—Б—П—В: –∞–Љ–Њ–Ї—Б–Є—Ж–Є–ї¬≠–ї–Є–љ/–Ї–ї–∞–≤—Г–ї–∞–љ–∞—В, –∞–Љ–Њ–Ї—Б–Є—Ж–Є–ї–ї–Є–љ/—Б—Г–ї—М–±–∞–Ї—В–∞–Љ, –∞–Љ–њ–Є—Ж–Є–ї¬≠–ї–Є–љ/—Б—Г–ї—М¬≠¬≠–±–∞–Ї¬≠—В–∞–Љ, –њ–Є–њ–µ—А–∞—Ж–Є–ї–ї–Є–љ/—В–∞–Ј–Њ–±–∞–Ї—В–∞–Љ, —В–Є–Ї–∞—А—Ж–Є–ї¬≠–ї–Є–љ/–Ї–ї–∞¬≠–≤—Г–ї–∞–љ–∞—В. –≠—В–Є –∞–љ—В–Є–±–Є–Њ—В–Є–Ї–Є –њ—А–µ–і—Б—В–∞–≤–ї—П—О—В —Б–Њ–±–Њ–є —Д–Є–Ї—Б–Є—А–Њ–≤–∞–љ–љ—Л–µ –Ї–Њ–Љ–±–Є–љ–∞—Ж–Є–Є –њ–Њ–ї—Г—Б–Є–љ—В–µ—В–Є—З–µ—Б–Ї–Є—Е –њ–µ–љ–Є—Ж–Є–ї–ї–Є–љ–Њ–≤ (–∞–Љ–Є–љ–Њ–њ–µ–љ–Є—Ж–Є–ї–ї–Є–љ–Њ–≤, –Ї–∞—А–±–Њ–Ї—Б–Є–њ–µ–љ–Є—Ж–Є–ї–ї–Є–љ–Њ–≤ –Є–ї–Є —Г—А–µ–Є–і–Њ–њ–µ–љ–Є—Ж–Є–ї–ї–Є–љ–Њ–≤) —Б –Є–љ–≥–Є–±–Є—В–Њ—А–∞–Љ–Є bвАУ–ї–∞–Ї—В–∞–Љ–∞–Ј, –Ї–Њ—В–Њ—А—Л–µ –љ–µ–Њ–±—А–∞—В–Є–Љ–Њ —Б–≤—П–Ј—Л–≤–∞—О—В —А–∞–Ј–ї–Є—З–љ—Л–µ bвАУ–ї–∞–Ї—В–∞–Љ–∞–Ј—Л –Є —В–∞–Ї–Є–Љ –Њ–±—А–∞–Ј–Њ–Љ –Ј–∞—Й–Є—Й–∞—О—В –њ–µ–љ–Є—Ж–Є–ї–ї–Є–љ—Л –Њ—В —А–∞–Ј—А—Г—И–µ–љ–Є—П —Н—В–Є–Љ–Є —Д–µ—А–Љ–µ–љ—В–∞–Љ–Є. –Т —А–µ–Ј—Г–ї—М—В–∞—В–µ —А–µ–Ј–Є—Б—В–µ–љ—В–љ—Л–µ –Ї –њ–µ–љ–Є—Ж–Є–ї–ї–Є–љ–∞–Љ —И—В–∞–Љ–Љ—Л –Љ–Є–Ї—А–Њ–Њ—А–≥–∞–љ–Є–Ј–Љ–Њ–≤ —Б—В–∞–љ–Њ–≤—П—В—Б—П —З—Г–≤—Б—В–≤–Є—В–µ–ї—М–љ—Л–Љ–Є –Ї –Ї–Њ–Љ–±–Є–љ–∞—Ж–Є–Є –і–∞–љ–љ—Л—Е –њ—А–µ–њ–∞—А–∞—В–Њ–≤ —Б –Є–љ–≥–Є–±–Є—В–Њ—А–∞–Љ–Є. –°–њ–µ–Ї—В—А –њ—А–Є—А–Њ–і–љ–Њ–є –∞–Ї—В–Є–≤–љ–Њ—Б—В–Є –Є–љ–≥–Є–±–Є—В–Њ—А–Ј–∞—Й–Є—Й–µ–љ–љ—Л—Е bвАУ–ї–∞–Ї—В–∞–Љ–Њ–≤ —Б–Њ–Њ—В–≤–µ—В—Б—В–≤—Г–µ—В —Б–Њ–і–µ—А–ґ–∞—Й–Є–Љ—Б—П –≤ –Є—Е —Б–Њ—Б—В–∞–≤–µ –њ–µ–љ–Є—Ж–Є–ї–ї–Є–љ–∞–Љ; —А–∞–Ј–ї–Є—З–∞–µ—В—Б—П —В–Њ–ї—М–Ї–Њ —Г—А–Њ–≤–µ–љ—М –њ—А–Є–Њ–±—А–µ—В–µ–љ–љ–Њ–є —Г—Б—В–Њ–є—З–Є–≤–Њ—Б—В–Є. –Ъ–ї–Є–љ–Є—З–µ—Б–Ї–Є –Ј–љ–∞—З–Є–Љ–Њ–є —П–≤–ї—П–µ—В—Б—П –≤—Л—Б–Њ–Ї–∞—П –∞–Ї—В–Є–≤–љ–Њ—Б—В—М —Н—В–Є—Е –њ—А–µ–њ–∞—А–∞—В–Њ–≤ –≤ –Њ—В–љ–Њ—И–µ–љ–Є–Є –њ–љ–µ–≤–Љ–Њ–Ї–Њ–Ї–Ї–Њ–≤/—Б—В—А–µ–њ—В–Њ–Ї–Њ–Ї–Ї–Њ–≤, —Б—В–∞—Д–Є–ї–Њ–Ї–Њ–Ї–Ї–Њ–≤, –Ї–Є¬≠—И–µ—З¬≠–љ–Њ–є –њ–∞–ї–Њ—З–Ї–Є, –≥–µ–Љ–Њ—Д–Є–ї—М–љ–Њ–є –њ–∞–ї–Њ—З–Ї–Є. –Т –±–Њ–ї—М–љ–Є—З–љ—Л–є –§–Њ—А–Љ—Г–ї—П—А –Њ–±–Њ—Б–љ–Њ–≤–∞–љ–Њ –≤–Ї–ї—О—З–µ–љ–Є–µ –Њ–і–љ–Њ–≥–Њ –Є–Ј —В—А–µ—Е –Є–љ–≥–Є–±–Є—В–Њ—А–Њ–Ј–∞—Й–Є—Й–µ–љ–љ—Л—Е –∞–Љ–Є–љ–Њ–њ–µ–љ–Є—Ж–Є–ї–ї–Є–љ–Њ–≤.
–Р–Љ–Њ–Ї—Б–Є—Ж–Є–ї–ї–Є–љ/–Ї–ї–∞–≤—Г–ї–∞–љ–∞—В. –ѓ–≤–ї—П–µ—В—Б—П –љ–∞–Є–±–Њ–ї–µ–µ —Е–Њ—А–Њ¬≠—И–Њ –Є–Ј—Г—З–µ–љ–љ—Л–Љ –∞–љ—В–Є–±–Є–Њ—В–Є–Ї–Њ–Љ —Н—В–Њ–є –≥—А—Г–њ–њ—Л —Б –љ–∞–Є–±–Њ–ї–µ–µ —И–Є—А–Њ–Ї–Є–Љ–Є –њ–Њ–Ї–∞–Ј–∞–љ–Є—П–Љ–Є –Ї –њ—А–Є–Љ–µ–љ–µ–љ–Є—О. –С–Њ–ї—М¬≠—И–Є–љ¬≠—Б—В–≤–Њ –≤–љ–µ–±–Њ–ї—М–љ–Є—З–љ—Л—Е —И—В–∞–Љ–Љ–Њ–≤ S. aureus —З—Г–≤—Б—В–≤–Є—В–µ–ї—М–љ–Њ –Ї –∞–Љ–Њ–Ї—Б–Є—Ж–Є–ї–ї–Є–љ/–Ї–ї–∞–≤—Г–ї–∞–љ–∞—В—Г. –£—Б—В–Њ–є—З–Є–≤–Њ—Б—В—М S. pneumoniae, H. influenzae –≤ –†–§ –љ–µ–Ј–љ–∞—З–Є—В–µ–ї—М–љ–∞. –Т –њ–Њ—Б–ї–µ–і–љ–Є–µ –≥–Њ–і—Л –љ–∞–±–ї—О–і–∞–µ—В—Б—П —А–Њ—Б—В —Г—Б—В–Њ–є¬≠—З–Є–≤–Њ—Б—В–Є –≤–љ–µ–±–Њ–ї—М–љ–Є—З–љ—Л—Е —Г—А–Њ–њ–∞—В–Њ–≥–µ–љ–љ—Л—Е —И—В–∞–Љ–Љ–Њ–≤ E. coli, —Б–Њ—Б—В–∞–≤–ї—П—О—Й–Є–є –≤ –љ–∞—Б—В–Њ—П—Й–µ–µ –≤—А–µ–Љ—П –Њ–Ї–Њ–ї–Њ 20%. –£—Б—В–Њ–є—З–Є–≤–Њ—Б—В—М –У—А–∞–Љ(вАУ) –±–∞–Ї—В–µ—А–Є–є –Ї–Є—И–µ—З–љ–Њ–є –≥—А—Г–њ–њ—Л –≤–∞—А—М–Є—А—Г–µ—В вАУ –≤–љ–µ–±–Њ–ї—М–љ–Є—З–љ—Л–µ —И—В–∞–Љ–Љ—Л, –Ї–∞–Ї –њ—А–∞–≤–Є–ї–Њ, —З—Г–≤—Б—В–≤–Є—В–µ–ї—М–љ—Л, –∞ –≥–Њ—Б–њ–Є—В–∞–ї—М–љ—Л–µ вАУ —З–∞—Б—В–Њ —Г—Б—В–Њ–є—З–Є–≤—Л.
–Ю—Б–љ–Њ–≤–љ—Л–µ –њ–Њ–Ї–∞–Ј–∞–љ–Є—П:
вАҐ –Т–љ–µ–±–Њ–ї—М–љ–Є—З–љ—Л–µ —А–µ—Б–њ–Є—А–∞—В–Њ—А–љ—Л–µ –Є–љ—Д–µ–Ї—Ж–Є–Є, –њ—А–µ–ґ–і–µ –≤—Б–µ–≥–Њ
вАУ –Ю–±–Њ—Б—В—А–µ–љ–Є–µ —Е—А–Њ–љ–Є—З–µ—Б–Ї–Њ–≥–Њ –±—А–Њ–љ—Е–Є—В–∞ (—Б—А–µ–і—Б—В–≤–Њ –≤—Л–±–Њ—А–∞)
вАУ –Ю—Б–ї–Њ–ґ–љ–µ–љ–љ–∞—П –њ–љ–µ–≤–Љ–Њ–љ–Є—П вАУ –і–µ—Б—В—А—Г–Ї—Ж–Є—П, –∞–±—Б—Ж–µ—Б—Б (—Б—А–µ–і—Б—В–≤–Њ –≤—Л–±–Њ—А–∞)
вАУ –°–Є–љ—Г—Б–Є—В (—Б—А–µ–і—Б—В–≤–Њ –≤—Л–±–Њ—А–∞)
вАҐ –Т–љ–µ–±–Њ–ї—М–љ–Є—З–љ—Л–µ –∞–±–і–Њ–Љ–Є–љ–∞–ї—М–љ—Л–µ –Є–љ—Д–µ–Ї—Ж–Є–Є (—Б—А–µ–і—Б—В–≤–Њ –≤—Л–±–Њ—А–∞)
вАҐ –Т–Њ—Б–њ–∞–ї–Є—В–µ–ї—М–љ—Л–µ –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П –Њ—А–≥–∞–љ–Њ–≤ –Љ–∞–ї–Њ–≥–Њ —В–∞–Ј–∞
(–≤ —Б–Њ—З–µ—В–∞–љ–Є–Є —Б –і–Њ–Ї—Б–Є—Ж–Є–Ї–ї–Є–љ–Њ–Љ –Є–ї–Є –Љ–∞–Ї—А–Њ–ї–Є–і–Њ–Љ)
вАҐ –£–Ї—Г—И–µ–љ–љ—Л–µ —А–∞–љ—Л (—Б—А–µ–і—Б—В–≤–Њ –≤—Л–±–Њ—А–∞)
–Р–Љ–Њ–Ї—Б–Є—Ж–Є–ї–ї–Є–љ/—Б—Г–ї—М–±–∞–Ї—В–∞–Љ. –•–Њ—В—П —Б—Г–ї—М–±–∞–Ї—В–∞–Љ —Г—Б—В—Г–њ–∞–µ—В –Ї–ї–∞–≤—Г–ї–∞–љ–∞—В—Г –њ–Њ —Б—В–µ–њ–µ–љ–Є –Є–љ–≥–Є–±–Є—А–Њ–≤–∞–љ–Є—П bвАУ–ї–∞–Ї—В–∞–Љ–∞–Ј, –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є—Е —А–∞–Ј–ї–Є—З–Є–є –Љ–µ–ґ–і—Г –њ—А–µ–њ–∞—А–∞—В–∞–Љ–Є –љ–µ —Г—Б—В–∞–љ–Њ–≤–ї–µ–љ–Њ. –≠—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В—М –∞–Љ–Њ–Ї—Б–Є—Ж–Є–ї–ї–Є–љ/—Б—Г–ї—М–±–∞–Ї—В–∞–Љ–∞ –і–Њ–Ї—Г–Љ–µ–љ—В–Є—А–Њ–≤–∞–љ–∞ –њ—А–Є –≤–љ–µ–±–Њ–ї—М–љ–Є—З–љ—Л—Е —А–µ—Б–њ–Є—А–∞—В–Њ—А–љ—Л—Е –Є –∞–±–і–Њ–Љ–Є–љ–∞–ї—М–љ—Л—Е –Є–љ—Д–µ–Ї—Ж–Є—П—Е.
–Р–Љ–њ–Є—Ж–Є–ї–ї–Є–љ/—Б—Г–ї—М–±–∞–Ї—В–∞–Љ. –≠—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В—М –і–Њ–Ї—Г–Љ–µ–љ—В–Є—А–Њ–≤–∞–љ–∞ –њ—А–Є —Е–Є—А—Г—А–≥–Є—З–µ—Б–Ї–Є—Е –Є–љ—Д–µ–Ї—Ж–Є—П—Е (–њ–µ—А–Є—В–Њ–љ–Є—В, –Њ—Б–ї–Њ–ґ–љ–µ–љ–љ—Л–µ –Є–љ—Д–µ–Ї—Ж–Є–Є –Љ—П–≥–Ї–Є—Е —В–Ї–∞–љ–µ–є). –Ъ –љ–µ–і–Њ—Б—В–∞—В–Ї–∞–Љ –Љ–Њ–ґ–љ–Њ –Њ—В–љ–µ—Б—В–Є –љ–µ–Њ–±—Е–Њ–і–Є–Љ–Њ—Б—В—М —З–∞—Б—В—Л—Е –Є–љ—Д—Г–Ј–Є–є (–Ї–∞–ґ–і—Л–µ 6 —З–∞—Б–Њ–≤) –њ–Њ —Б—А–∞–≤–љ–µ–љ–Є—О —Б –њ–µ—А–≤—Л–Љ–Є –і–≤—Г–Љ—П –њ—А–µ–њ–∞—А–∞—В–∞–Љ–Є.
–¶–µ—Д–∞–ї–Њ—Б–њ–Њ—А–Є–љ—Л
–Т—Б–µ —Ж–µ—Д–∞–ї–Њ—Б–њ–Њ—А–Є–љ—Л —П–≤–ї—П—О—В—Б—П –њ—А–Њ–Є–Ј–≤–Њ–і–љ—Л–Љ–Є 7вАУ–∞–Љ–Є–љ–Њ—Ж–µ—Д–Њ–ї–∞—Б–њ–Њ—А–∞–љ–Њ–≤–Њ–є –Ї–Є—Б–ї–Њ—В—Л. –Т –Ј–∞–≤–Є—Б–Є–Љ–Њ—Б—В–Є –Њ—В —Б–њ–µ–Ї—В—А–∞ –∞–љ—В–Є–Љ–Є–Ї—А–Њ–±–љ–Њ–є –∞–Ї—В–Є–≤–љ–Њ—Б—В–Є —Ж–µ—Д–∞–ї–Њ—Б–њ–Њ—А–Є–љ—Л —А–∞–Ј–і–µ–ї—П—О—В –љ–∞ 4 –њ–Њ–Ї–Њ–ї–µ–љ–Є—П (–≥–µ–љ–µ—А–∞—Ж–Є–Є).
–¶–µ—Д–∞–ї–Њ—Б–њ–Њ—А–Є–љ—Л I –њ–Њ–Ї–Њ–ї–µ–љ–Є—П (—Ж–µ—Д–∞–Ј–Њ–ї–Є–љ) –∞–Ї—В–Є–≤–љ—Л –њ—А–µ–Є–Љ—Г—Й–µ—Б—В–≤–µ–љ–љ–Њ –њ—А–Њ—В–Є–≤ –≥—А–∞–Љ–њ–Њ–ї–Њ–ґ–Є—В–µ–ї—М–љ—Л—Е –Љ–Є–Ї—А–Њ¬≠–Њ—А–≥–∞¬≠–љ–Є–Ј¬≠–Љ–Њ–≤ (—Б—В–∞—Д–Є–ї–Њ–Ї–Њ–Ї–Ї–Є, —Б—В—А–µ–њ—В–Њ–Ї–Њ–Ї–Ї–Є, –њ–љ–µ–≤–Љ–Њ–Ї–Њ–Ї–Ї–Є). –Э–µ–Ї–Њ—В–Њ—А—Л–µ –≥—А–∞–Љ–Њ—В—А–Є—Ж–∞—В–µ–ї—М–љ—Л–µ —Н–љ—В–µ—А–Њ–±–∞–Ї—В–µ—А–Є–Є (E. coli, P. mirabilis) –њ—А–Є—А–Њ–і–љ–Њ —З—Г–≤—Б—В–≤–Є—В–µ–ї—М–љ—Л –Ї —Ж–µ—Д–∞–ї–Њ—Б–њ–Њ—А–Є–љ–∞–Љ I –њ–Њ–Ї–Њ–ї–µ–љ–Є—П, –љ–Њ –њ—А–Є–Њ–±—А–µ—В–µ–љ–љ–∞—П —Г—Б—В–Њ–є—З–Є–≤–Њ—Б—В—М –Ї –љ–Є–Љ –≤—Л—Б–Њ–Ї–∞—П. –Я—А–µ–њ–∞—А–∞—В—Л –ї–µ–≥–Ї–Њ –њ–Њ–і–≤–µ—А–≥–∞—О—В—Б—П –≥–Є–і—А–Њ–ї–Є–Ј—Г bвАУ–ї–∞–Ї—В–∞–Љ–∞–Ј–∞–Љ–Є.
–¶–µ—Д–∞–ї–Њ—Б–њ–Њ—А–Є–љ—Л II –њ–Њ–Ї–Њ–ї–µ–љ–Є—П (—Ж–µ—Д—Г—А–Њ–Ї—Б–Є–Љ, —Ж–µ—Д–∞–Љ–∞–љ–і–Њ–ї) –±–Њ–ї–µ–µ –∞–Ї—В–Є–≤–љ—Л –≤ –Њ—В–љ–Њ—И–µ–љ–Є–Є –≥—А–∞–Љ–Њ—В—А–Є—Ж–∞—В–µ–ї—М–љ—Л—Е –±–∞–Ї—В–µ—А–Є–є –њ–Њ —Б—А–∞–≤–љ–µ–љ–Є—О —Б —Ж–µ—Д–∞–ї–Њ—Б–њ–Њ—А–Є–љ–∞–Љ–Є I –њ–Њ–Ї–Њ–ї–µ–љ–Є—П –Є –±–Њ–ї–µ–µ —Г—Б—В–Њ–є—З–Є–≤—Л –Ї –і–µ–є—Б—В–≤–Є—О bвАУ–ї–∞–Ї—В–∞–Љ–∞–Ј (—Ж–µ—Д—Г—А–Њ–Ї—Б–Є–Љ –±–Њ–ї–µ–µ —Б—В–∞–±–Є–ї–µ–љ, —З–µ–Љ —Ж–µ—Д–∞–Љ–∞–љ–і–Њ–ї). –Я—А–µ–њ–∞—А–∞—В—Л —Б–Њ—Е—А–∞–љ—П—О—В –≤—Л—Б–Њ–Ї—Г—О –∞–Ї—В–Є–≤–љ–Њ—Б—В—М –≤ –Њ—В–љ–Њ—И–µ–љ–Є–Є –≥—А–∞–Љ–њ–Њ–ї–Њ–ґ–Є—В–µ–ї—М–љ—Л—Е –±–∞–Ї—В–µ—А–Є–є.
–¶–µ—Д–∞–ї–Њ—Б–њ–Њ—А–Є–љ—Л III –њ–Њ–Ї–Њ–ї–µ–љ–Є—П –њ—А–µ–Є–Љ—Г—Й–µ—Б—В–≤–µ–љ–љ–Њ –∞–Ї—В–Є–≤–љ—Л –≤ –Њ—В–љ–Њ—И–µ–љ–Є–Є –≥—А–∞–Љ–Њ—В—А–Є—Ж–∞—В–µ–ї—М–љ—Л—Е –Љ–Є–Ї—А–Њ–Њ—А–≥–∞–љ–Є–Ј–Љ–Њ–≤ –Є —Б—В—А–µ–њ—В–Њ–Ї–Њ–Ї–Ї–Њ–≤/–њ–љ–µ–≤–Љ–Њ–Ї–Њ–Ї–Ї–Њ–≤. –Р–љ—В–Є—Б—В–∞—Д–Є–ї–Њ¬≠–Ї–Њ–Ї¬≠–Ї–Њ¬≠–≤–∞—П –∞–Ї—В–Є–≤–љ–Њ—Б—В—М –љ–µ –≤—Л—Б–Њ–Ї–∞—П.
–°–ї–µ–і—Г–µ—В –≤—Л–і–µ–ї—П—В—М —Ж–µ—Д–∞–ї–Њ—Б–њ–Њ—А–Є–љ—Л –≥—А—Г–њ–њ—Л IIIa (—Ж–µ—Д–Њ—В–∞–Ї—Б–Є–Љ, —Ж–µ—Д—В—А–Є–∞–Ї—Б–Њ–љ), –Ї–Њ—В–Њ—А—Л–µ –њ—А–Њ—П–≤–ї—П—О—В –≤—Л—Б–Њ–Ї—Г—О –∞–Ї—В–Є–≤–љ–Њ—Б—В—М –≤ –Њ—В–љ–Њ—И–µ–љ–Є–Є Enterobacteriaceae –Є —Б—В—А–µ–њ—В–Њ¬≠–Ї–Њ–Ї¬≠–Ї–Њ–≤/–њ–љ–µ–≤–Љ–Њ–Ї–Њ–Ї¬≠–Ї–Њ–≤.
–¶–µ—Д–∞–ї–Њ—Б–њ–Њ—А–Є–љ—Л –≥—А—Г–њ–њ—Л IIIb (—Ж–µ—Д—В–∞–Ј–Є–і–Є–Љ, —Ж–µ—Д–Њ–њ–µ—А–∞–Ј–Њ–љ), –љ–∞—А—П–і—Г —Б Enterobacteriaceae, –∞–Ї—В–Є–≤–љ—Л –њ—А–Њ—В–Є–≤ P. aeruginosa –Є, –≤ –Љ–µ–љ—М—И–µ–є —Б—В–µ–њ–µ–љ–Є, Acinetobacter spp. –Т —В–Њ–ґ–µ –≤—А–µ–Љ—П –∞–љ—В–Є—Б—В—А–µ–њ—В–Њ–Ї–Њ–Ї–Ї–Њ–≤–∞—П –∞–Ї—В–Є–≤–љ–Њ—Б—В—М —Г –љ–Є—Е –љ–Є–Ј–Ї–∞—П.
–Т—Б–µ —Ж–µ—Д–∞–ї–Њ—Б–њ–Њ—А–Є–љ—Л III –њ–Њ–Ї–Њ–ї–µ–љ–Є—П –Њ–±–ї–∞–і–∞—О—В –±–Њ–ї–µ–µ –≤—Л—Б–Њ–Ї–Њ–є —Б—В–∞–±–Є–ї—М–љ–Њ—Б—В—М—О –Ї bвАУ–ї–∞–Ї—В–∞–Љ–∞–Ј–∞–Љ –њ–Њ —Б—А–∞–≤–љ–µ–љ–Є—О —Б —Ж–µ—Д–∞–ї–Њ—Б–њ–Њ—А–Є–љ–∞–Љ–Є IвАУII –њ–Њ–Ї–Њ–ї–µ–љ–Є–є, –љ–Њ —А–∞–Ј—А—Г—И–∞—О—В—Б—П bвАУ–ї–∞–Ї—В–∞–Љ–∞–Ј–∞–Љ–Є —А–∞—Б—И–Є—А–µ–љ–љ–Њ–≥–Њ —Б–њ–µ–Ї—В—А–∞ –Є —Е—А–Њ–Љ–Њ—Б–Њ–Љ–љ—Л–Љ–Є bвАУ–ї–∞–Ї—В–∞–Љ–∞–Ј–∞–Љ–Є –Ї–ї–∞—Б—Б–∞ –° (AmpC))
–¶–µ—Д–∞–ї–Њ—Б–њ–Њ—А–Є–љ—Л IV –њ–Њ–Ї–Њ–ї–µ–љ–Є—П (—Ж–µ—Д–µ–њ–Є–Љ) —Б–Њ—З–µ—В–∞—О—В –≤—Л—Б–Њ–Ї—Г—О –∞–Ї—В–Є–≤–љ–Њ—Б—В—М —Ж–µ—Д–∞–ї–Њ—Б–њ–Њ—А–Є–љ–Њ–≤ IвАУII –њ–Њ–Ї–Њ–ї–µ–љ–Є–є –≤ –Њ—В–љ–Њ—И–µ–љ–Є–Є —Б—В–∞—Д–Є–ї–Њ–Ї–Њ–Ї–Ї–Њ–≤ –Є —Ж–µ—Д–∞–ї–Њ—Б–њ–Њ—А–Є–љ–Њ–≤ III –њ–Њ–Ї–Њ–ї–µ–љ–Є—П вАУ –≤ –Њ—В–љ–Њ—И–µ–љ–Є–Є –≥—А–∞–Љ–Њ—В—А–Є—Ж–∞—В–µ–ї—М–љ—Л—Е –Љ–Є–Ї—А–Њ–Њ—А–≥–∞–љ–Є–Ј–Љ–Њ–≤. –Т –љ–∞—Б—В–Њ—П—Й–µ–µ –≤—А–µ–Љ—П —Ж–µ—Д–µ–њ–Є–Љ –Є–Љ–µ–µ—В –љ–∞–Є–±–Њ–ї–µ–µ —И–Є¬≠—А–Њ¬≠–Ї–Є–є —Б–њ–µ–Ї—В—А –∞–љ—В–Є–Љ–Є–Ї—А–Њ–±–љ–Њ–є –∞–Ї—В–Є–≤–љ–Њ—Б—В–Є —Б—А–µ–і–Є —Ж–µ—Д–∞–ї–Њ—Б–њ–Њ—А–Є–љ–Њ–≤—Л—Е –∞–љ—В–Є–±–Є–Њ—В–Є–Ї–Њ–≤. –¶–µ—Д–∞–ї–Њ—Б–њ–Њ—А–Є–љ—Л IV –њ–Њ–Ї–Њ–ї–µ–љ–Є—П –≤ –љ–µ–Ї–Њ—В–Њ—А—Л—Е —Б–ї—Г—З–∞—П—Е –њ—А–Њ—П–≤–ї—П—О—В –∞–Ї—В–Є–≤–љ–Њ—Б—В—М –≤ –Њ—В–љ–Њ—И–µ–љ–Є–Є —В–µ—Е —И—В–∞–Љ–Љ–Њ–≤ Enterobacteriaceae, –Ї–Њ—В–Њ—А—Л–µ —Г—Б—В–Њ–є—З–Є–≤—Л –Ї —Ж–µ—Д–∞–ї–Њ—Б–њ–Њ—А–Є–љ–∞–Љ III –њ–Њ–Ї–Њ–ї–µ–љ–Є—П.
–¶–µ—Д–µ–њ–Є–Љ –њ–Њ–ї–љ–Њ—Б—В—М—О —Г—Б—В–Њ–є—З–Є–≤ –Ї –≥–Є–і—А–Њ–ї–Є–Ј—Г AmpC bвАУ–ї–∞–Ї—В–∞–Љ–∞–Ј–∞–Љ–Є –Є —З–∞—Б—В–Є—З–љ–Њ –њ—А–Њ—В–Є–≤–Њ—Б—В–Њ–Є—В –≥–Є–і—А–Њ–ї–Є–Ј—Г –њ–ї–∞–Ј–Љ–Є–і–љ—Л–Љ–Є bвАУ–ї–∞–Ї—В–∞–Љ–∞–Ј–∞–Љ–Є —А–∞—Б—И–Є—А–µ–љ–љ–Њ–≥–Њ —Б–њ–µ–Ї—В—А–∞, –њ—А–Њ—П–≤–ї—П–µ—В –≤—Л—Б–Њ–Ї—Г—О –∞–Ї—В–Є–≤–љ–Њ—Б—В—М –≤ –Њ—В–љ–Њ—И–µ–љ–Є–Є P. aeruginosa (—Б—А–∞–≤–љ–Є–Љ—Г—О —Б —Ж–µ—Д—В–∞–Ј–Є–і–Є–Љ–Њ–Љ).
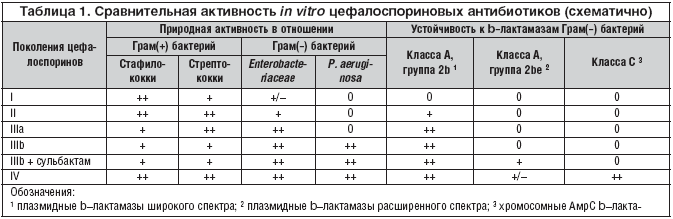
–Ґ–∞–Ї–Є–Љ –Њ–±—А–∞–Ј–Њ–Љ, —Г —Ж–µ—Д–∞–ї–Њ—Б–њ–Њ—А–Є–љ–Њ–≤ –Њ—В I –Ї IV –њ–Њ–Ї–Њ–ї–µ–љ–Є—О —Г–≤–µ–ї–Є—З–Є–≤–∞–µ—В—Б—П –∞–Ї—В–Є–≤–љ–Њ—Б—В—М –≤ –Њ—В–љ–Њ—И–µ–љ–Є–Є –≥—А–∞–Љ–Њ—В—А–Є—Ж–∞—В–µ–ї—М–љ—Л—Е –±–∞–Ї—В–µ—А–Є–є –Є –њ–љ–µ–≤–Љ–Њ–Ї–Њ–Ї–Ї–Њ–≤, –Є –љ–µ–Љ–љ–Њ–≥–Њ —Б–љ–Є–ґ–∞–µ—В—Б—П –∞–Ї—В–Є–≤–љ–Њ—Б—В—М –≤ –Њ—В–љ–Њ—И–µ–љ–Є–Є —Б—В–∞—Д–Є–ї–Њ–Ї–Њ–Ї–Ї–Њ–≤ –Њ—В I –Ї III –њ–Њ–Ї–Њ–ї–µ–љ–Є—О; –Њ—В I –Ї IV –њ–Њ–Ї–Њ–ї–µ–љ–Є—О —Г–≤–µ–ї–Є—З–Є–≤–∞–µ—В—Б—П —Г—Б—В–Њ–є—З–Є–≤–Њ—Б—В—М –Ї –і–µ–є—Б—В–≤–Є—О bвАУ–ї–∞–Ї—В–∞–Љ–∞–Ј –≥—А–∞–Љ–Њ—В—А–Є—Ж–∞—В–µ–ї—М–љ—Л—Е –±–∞–Ї—В–µ—А–Є–є (—В–∞–±–ї. 1).
–Т—Б–µ —Ж–µ—Д–∞–ї–Њ—Б–њ–Њ—А–Є–љ—Л –њ—А–∞–Ї—В–Є—З–µ—Б–Ї–Є –ї–Є—И–µ–љ—Л –∞–Ї—В–Є–≤–љ–Њ—Б—В–Є –њ—А–Њ—В–Є–≤ —Н–љ—В–µ—А–Њ–Ї–Њ–Ї–Ї–Њ–≤, –Љ–∞–ї–Њ–∞–Ї—В–Є–≤–љ—Л –њ—А–Њ—В–Є–≤ –≥—А–∞–Љ–њ–Њ–ї–Њ–ґ–Є—В–µ–ї—М–љ—Л—Е –∞–љ–∞—Н—А–Њ–±–Њ–≤ –Є —Б–ї–∞–±–Њ –∞–Ї—В–Є–≤–љ—Л –њ—А–Њ—В–Є–≤ –≥—А–∞–Љ–Њ—В—А–Є—Ж–∞—В–µ–ї—М–љ—Л—Е –∞–љ–∞—Н—А–Њ–±–Њ–≤.
–Т —Б–Њ–Њ—В–≤–µ—В—Б—В–≤–Є–µ —Б –Њ—Б–Њ–±–µ–љ–љ–Њ—Б—В—П–Љ–Є –∞–љ—В–Є–Љ–Є–Ї—А–Њ–±–љ–Њ–є –∞–Ї—В–Є–≤–љ–Њ—Б—В–Є, –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Њ–µ –њ–Њ–Ј–Є—Ж–Є–Њ–љ–Є—А–Њ–≤–∞–љ–Є–µ –≤ —А—П–і—Г —Ж–µ—Д–∞–ї–Њ—Б–њ–Њ—А–Є–љ–Њ–≤—Л—Е –∞–љ—В–Є–±–Є–Њ—В–Є–Ї–Њ–≤ —Б—Г—Й–µ—Б—В–≤–µ–љ–љ–Њ —А–∞–Ј–ї–Є—З–∞–µ—В—Б—П.
–¶–µ—Д–∞–Ј–Њ–ї–Є–љ
–¶–µ—Д–∞–ї–Њ—Б–њ–Њ—А–Є–љ I –њ–Њ–Ї–Њ–ї–µ–љ–Є—П –і–ї—П –њ–∞—А–µ–љ—В–µ—А–∞–ї—М–љ–Њ–≥–Њ –њ—А–Є–Љ–µ–љ–µ–љ–Є—П.
–Ю—Б–љ–Њ–≤–љ—Л–µ –њ–Њ–Ї–∞–Ј–∞–љ–Є—П:
вАҐ –Ш–љ—В—А–∞–Њ–њ–µ—А–∞—Ж–Є–Њ–љ–љ–∞—П –њ—А–Њ—Д–Є–ї–∞–Ї—В–Є–Ї–∞ –њ–Њ—Б–ї–µ–Њ–њ–µ—А–∞—Ж–Є–Њ–љ–љ–Њ–є —А–∞–љ–µ–≤–Њ–є –Є–љ—Д–µ–Ї—Ж–Є–Є (—Б—А–µ–і—Б—В–≤–Њ –≤—Л–±–Њ—А–∞).
вАҐ –°—В–∞—Д–Є–ї–Њ–Ї–Њ–Ї–Ї–Њ–≤—Л–µ –Є–љ—Д–µ–Ї—Ж–Є–Є —А–∞–Ј–ї–Є—З–љ–Њ–є –ї–Њ–Ї–∞–ї–Є–Ј–∞—Ж–Є–Є (–∞–ї—М—В–µ—А–љ–∞—В–Є–≤–∞ –Њ–Ї—Б–∞—Ж–Є–ї–ї–Є–љ—Г). –†–µ–ґ–Є–Љ –і–Њ–Ј–Є—А–Њ–≤–∞–љ–Є—П вАУ –њ–Њ 2 –≥ –Ї–∞–ґ–і—Л–µ 6вАУ8 —З–∞—Б–Њ–≤.
–¶–µ—Д—Г—А–Њ–Ї—Б–Є–Љ
–¶–µ—Д–∞–ї–Њ—Б–њ–Њ—А–Є–љ II –њ–Њ–Ї–Њ–ї–µ–љ–Є—П –і–ї—П –њ–∞—А–µ–љ—В–µ—А–∞–ї—М–љ–Њ–≥–Њ –њ—А–Є–Љ–µ–љ–µ–љ–Є—П.
–Ю—Б–љ–Њ–≤–љ—Л–µ –њ–Њ–Ї–∞–Ј–∞–љ–Є—П:
вАҐ –Ш–љ—Д–µ–Ї—Ж–Є–Є, –≤—Л–Ј–≤–∞–љ–љ—Л–µ –Њ–Ї—Б–∞—Ж–Є–ї–ї–Є–љ—З—Г–≤—Б—В–≤–Є—В–µ–ї—М–љ—Л–Љ–Є —Б—В–∞—Д–Є–ї–Њ–Ї–Њ–Ї–Ї–∞–Љ–Є (–∞–ї—М—В–µ—А–љ–∞—В–Є–≤–∞ –Њ–Ї—Б–∞—Ж–Є–ї–ї–Є–љ—Г –Є —Ж–µ—Д–∞–Ј–Њ–ї–Є–љ—Г)
вАҐ –Ш–љ—В—А–∞–Њ–њ–µ—А–∞—Ж–Є–Њ–љ–љ–∞—П –њ—А–Њ—Д–Є–ї–∞–Ї—В–Є–Ї–∞ –њ–Њ—Б–ї–µ–Њ–њ–µ—А–∞—Ж–Є–Њ–љ–љ–Њ–є —А–∞–љ–µ–≤–Њ–є –Є–љ—Д–µ–Ї—Ж–Є–Є (—Б—А–µ–і—Б—В–≤–Њ –≤—Л–±–Њ—А–∞). –Я–Њ —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В–Є —А–∞–≤–µ–љ —Ж–µ—Д–∞–Ј–Њ–ї–Є–љ—Г, –≤ –Њ—В–і–µ–ї—М–љ—Л—Е –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П—Е –њ–Њ–Ї–∞–Ј–∞–љ–Њ –њ—А–µ–Є–Љ—Г—Й–µ—Б—В–≤–Њ —Ж–µ—Д—Г—А–Њ–Ї—Б–Є–Љ–∞, –Њ—Б–Њ–±–µ–љ–љ–Њ —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –≤—Л—Б–Њ–Ї–Є–Љ —А–Є—Б–Ї–Њ–Љ –њ–Њ—Б–ї–µ–Њ–њ–µ—А–∞—Ж–Є–Њ–љ–љ—Л—Е –Њ—Б–ї–Њ–ґ–љ–µ–љ–Є–є.
вАҐ –Т–љ–µ–±–Њ–ї—М–љ–Є—З–љ—Л–µ –љ–µ–Њ—Б–ї–Њ–ґ–љ–µ–љ–љ—Л–µ –Є–љ—Д–µ–Ї—Ж–Є–Є –Ї–Њ–ґ–Є –Є –Љ—П–≥–Ї–Є—Е —В–Ї–∞–љ–µ–є
вАҐ –Т–љ–µ–±–Њ–ї—М–љ–Є—З–љ—Л–µ –Є–љ—В—А–∞–∞–±–і–Њ–Љ–Є–љ–∞–ї—М–љ—Л–µ –Є–љ—Д–µ–Ї—Ж–Є–Є (–≤ –Ї–Њ–Љ–±–Є–љ–∞—Ж–Є–Є —Б –Љ–µ—В—А–Њ–љ–Є–і–∞–Ј–Њ–ї–Њ–Љ –Є–ї–Є –Ї–ї–Є–љ–і–∞–Љ–Є—Ж–Є–љ–Њ–Љ)
–¶–µ—Д–Њ—В–∞–Ї—Б–Є–Љ, —Ж–µ—Д—В—А–Є–∞–Ї—Б–Њ–љ
–¶–µ—Д–∞–ї–Њ—Б–њ–Њ—А–Є–љ—Л III –њ–Њ–Ї–Њ–ї–µ–љ–Є—П, –≥—А—Г–њ–њ–∞ IIIa.
–Ю—Б–љ–Њ–≤–љ—Л–µ –њ–Њ–Ї–∞–Ј–∞–љ–Є—П:
вАҐ –Т–љ–µ–±–Њ–ї—М–љ–Є—З–љ–∞—П –њ–љ–µ–≤–Љ–Њ–љ–Є—П —В—П–ґ–µ–ї–Њ–≥–Њ —В–µ—З–µ–љ–Є—П вАУ –≤ —Б–Њ—З–µ—В–∞–љ–Є–Є —Б –Љ–∞–Ї—А–Њ–ї–Є–і–љ—Л–Љ –∞–љ—В–Є–±–Є–Њ—В–Є–Ї–Њ–Љ (—Б—А–µ–і—Б—В–≤–Њ –≤—Л–±–Њ—А–∞)
вАҐ –Ц–Є–Ј–љ–µ–Њ–њ–∞—Б–љ—Л–µ –Є–љ—Д–µ–Ї—Ж–Є–Є, –≤—Л–Ј–≤–∞–љ–љ—Л–µ H. influenzae (—Б–µ–њ—Б–Є—Б, —Н–њ–Є–≥–ї–Њ—В—В–Є—В), N. meningitidis (–Љ–µ–љ–Є–љ–≥–Є—В), S. pneumoniae (–њ–љ–µ–≤–Љ–Њ–љ–Є—П, –Љ–µ–љ–Є–љ–≥–Є—В), S. viridans (—Н–љ–і–Њ–Ї–∞—А–і–Є—В).
вАҐ –Т—В–Њ—А–Є—З–љ—Л–є –≥–љ–Њ–є–љ—Л–є –Љ–µ–љ–Є–љ–≥–Є—В —Г –≤–Ј—А–Њ—Б–ї—Л—Е –Є –і–µ—В–µ–є, —Г –љ–Њ–≤–Њ—А–Њ–ґ–і–µ–љ–љ—Л—Е вАУ –≤ –Ї–Њ–Љ–±–Є–љ–∞—Ж–Є–Є —Б –∞–Љ–њ–Є—Ж–Є–ї–ї–Є–љ–Њ–Љ (—Б—А–µ–і—Б—В–≤–Њ –≤—Л–±–Њ—А–∞)
вАҐ –Т–љ–µ–±–Њ–ї—М–љ–Є—З–љ—Л–µ –Є–љ—В—А–∞–∞–±–і–Њ–Љ–Є–љ–∞–ї—М–љ—Л–µ –Є–љ—Д–µ–Ї—Ж–Є–Є вАУ –≤ –Ї–Њ–Љ–±–Є–љ–∞—Ж–Є–Є —Б –Ї–ї–Є–љ–і–∞–Љ–Є—Ж–Є–љ–Њ–Љ –Є–ї–Є –Љ–µ—В—А–Њ–љ–Є–і–∞–Ј–Њ–ї–Њ–Љ (—Б—А–µ–і—Б—В–≤–Њ –≤—Л–±–Њ—А–∞)
вАҐ –У–Є–љ–µ–Ї–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є–µ –Є–љ—Д–µ–Ї—Ж–Є–Є (—Н–љ–і–Њ–Љ–µ—В—А–Є—В, —Б–∞–ї—М–њ–Є–љ–≥–Є—В, —В—Г–±–ЊвАУ–Њ–≤–∞—А–Є–∞–ї—М–љ—Л–є –∞–±—Б—Ж–µ—Б—Б) вАУ –≤ –Ї–Њ–Љ–±–Є–љ–∞—Ж–Є–Є —Б –і–Њ–Ї—Б–Є—Ж–Є–Ї–ї–Є–љ–Њ–Љ
вАҐ –Ю—Б–ї–Њ–ґ–љ–µ–љ–љ—Л–µ –Є–љ—Д–µ–Ї—Ж–Є–Є –Љ–Њ—З–µ–≤—Л–≤–Њ–і—П—Й–Є—Е –њ—Г—В–µ–є (—Б—А–µ–і—Б—В–≤–Њ –≤—Л–±–Њ—А–∞)
–Ъ–ї–Є–љ–Є—З–µ—Б–Ї–Є—Е —А–∞–Ј–ї–Є—З–Є–є –Љ–µ–ґ–і—Г —Ж–µ—Д–Њ—В–∞–Ї—Б–Є–Љ–Њ–Љ –Є —Ж–µ—Д—В—А–Є–∞–Ї—Б–Њ–љ–Њ–Љ –љ–µ —Г—Б—В–∞–љ–Њ–≤–ї–µ–љ–Њ.
–¶–µ—Д—В–∞–Ј–Є–і–Є–Љ, —Ж–µ—Д–Њ–њ–µ—А–∞–Ј–Њ–љ
–¶–µ—Д–∞–ї–Њ—Б–њ–Њ—А–Є–љ—Л III –њ–Њ–Ї–Њ–ї–µ–љ–Є—П, –≥—А—Г–њ–њ–∞ IIIb
–Ю—Б–љ–Њ–≤–љ—Л–µ –њ–Њ–Ї–∞–Ј–∞–љ–Є—П:
вАҐ –Ш–љ—Д–µ–Ї—Ж–Є–Є, –≤—Л–Ј–≤–∞–љ–љ—Л–µ P. aeruginosa
вАҐ –У–Њ—Б–њ–Є—В–∞–ї—М–љ–∞—П –њ–љ–µ–≤–Љ–Њ–љ–Є—П, –≤–Њ–Ј–љ–Є–Ї—И–∞—П –љ–∞ —Д–Њ–љ–µ –њ—А–Њ–≤–µ–і–µ–љ–Є—П –Ш–Т–Ы (–њ–Њ—Б–ї–µ 5 —Б—Г—В–Њ–Ї)
вАҐ –Я–Њ—Б–ї–µ–Њ–њ–µ—А–∞—Ж–Є–Њ–љ–љ—Л–є –њ–µ—А–Є—В–Њ–љ–Є—В –≤ —Б–ї—Г—З–∞–µ –≤—Л—Б–Њ–Ї–Њ–Ї–Њ —А–Є—Б–Ї–∞ –њ—Б–µ–≤–і–Њ–Љ–Њ–љ–∞–і–љ–Њ–є –Є–љ—Д–µ–Ї—Ж–Є–Є
вАҐ –Ю—Б—В—А—Л–є –і–µ—Б—В—А—Г–Ї—В–Є–≤–љ—Л–є –њ–∞–љ–Ї—А–µ–∞—В–Є—В
–Ъ–ї–Є–љ–Є—З–µ—Б–Ї–Є—Е —А–∞–Ј–ї–Є—З–Є–є –Љ–µ–ґ–і—Г —Ж–µ—Д—В–∞–Ј–Є–і–Є–Љ–Њ–Љ –Є —Ж–µ—Д–Њ–њ–µ—А–∞–Ј–Њ–љ–Њ–Љ –љ–µ —Г—Б—В–∞–љ–Њ–≤–ї–µ–љ–Њ, —Е–Њ—В—П —Ж–µ—Д—В–∞–Ј–Є–і–Є–Љ —Е–∞—А–∞–Ї—В–µ—А–Є–Ј—Г–µ—В—Б—П –±–Њ–ї–µ–µ –≤—Л—Б–Њ–Ї–Њ–є –њ—А–Є—А–Њ–і–љ–Њ–є –∞–љ—В–Є–њ—Б–µ–≤–і–Њ–Љ–Њ–љ–∞–і–љ–Њ–є –∞–Ї—В–Є–≤–љ–Њ—Б—В—М—О. –Я—А–Є –љ–Њ–Ј–Њ–Ї–Њ–Љ–Є–∞–ї—М–љ–Њ–є –њ–љ–µ–≤–Љ–Њ–љ–Є–Є, –≤–µ—А–Њ—П—В–љ–Њ, –њ—А–µ–і–њ–Њ—З—В–Є—В–µ–ї—М–љ–µ–µ –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞—В—М —Ж–µ—Д—В–∞–Ј–Є–і–Є–Љ, –њ—А–Є –∞–±–і–Њ–Љ–Є–љ–∞–ї—М–љ—Л—Е –Є–љ—Д–µ–Ї—Ж–Є—П—Е вАУ —Ж–µ—Д–Њ–њ–µ—А–∞–Ј–Њ–љ –Є–ЈвАУ–Ј–∞ –Њ—Б–Њ–±–µ–љ–љ–Њ—Б—В–µ–є —Д–∞—А–Љ–∞–Ї–Њ–Ї–Є–љ–µ—В–Є–Ї–Є –∞–љ—В–Є–±–Є–Њ—В–Є–Ї–∞. –Я—А–Є –њ—Б–µ–≤–і–Њ–Љ–Њ–љ–∞–і–љ—Л—Е –Є–љ—Д–µ–Ї—Ж–Є—П—Е –¶–Э–° –Љ–Њ–ґ–љ–Њ –њ—А–Є–Љ–µ–љ—П—В—М —В–Њ–ї—М–Ї–Њ —Ж–µ—Д—В–∞–Ј–Є–і–Є–Љ, —В–∞–Ї –Ї–∞–Ї —Ж–µ—Д–Њ–њ–µ—А–∞–Ј–Њ–љ –љ–µ –њ—А–Њ–љ–Є–Ї–∞–µ—В —З–µ—А–µ–Ј –≥–µ–Љ–∞—В–ЊвАУ—Н–љ—Ж–µ—Д–∞–ї–Є—З–µ—Б–Ї–Є–є –±–∞—А—М–µ—А.
–¶–µ—Д–µ–њ–Є–Љ
–¶–µ—Д–∞–ї–Њ—Б–њ–Њ—А–Є–љ IV –њ–Њ–Ї–Њ–ї–µ–љ–Є—П.
–Ю—Б–љ–Њ–≤–љ—Л–µ –њ–Њ–Ї–∞–Ј–∞–љ–Є—П:
вАҐ –Ш–љ—Д–µ–Ї—Ж–Є–Є, –≤—Л–Ј–≤–∞–љ–љ—Л–µ P. aeruginosa
вАҐ –У–Њ—Б–њ–Є—В–∞–ї—М–љ–∞—П –њ–љ–µ–≤–Љ–Њ–љ–Є—П, –≤ —В.—З. –љ–∞ –Ш–Т–Ы
вАҐ –Ю—Б–ї–Њ–ґ–љ–µ–љ–љ—Л–µ –Є–љ—В—А–∞–∞–±–і–Њ–Љ–Є–љ–∞–ї—М–љ—Л–µ –Є–љ—Д–µ–Ї—Ж–Є–Є вАУ –≤ –Ї–Њ–Љ–±–Є–љ–∞—Ж–Є–Є —Б –Љ–µ—В—А–Њ–љ–Є–і–∞–Ј–Њ–ї–Њ–Љ (—Б—А–µ–і—Б—В–≤–Њ –≤—Л–±–Њ—А–∞)
вАҐ –Ш–љ—Д–Є—Ж–Є—А–Њ–≤–∞–љ–љ—Л–є –њ–∞–љ–Ї—А–µ–Њ–љ–µ–Ї—А–Њ–Ј вАУ –≤ –Ї–Њ–Љ–±–Є–љ–∞—Ж–Є–Є —Б –Љ–µ—В—А–Њ–љ–Є–і–∞–Ј–Њ–ї–Њ–Љ
–¶–µ—Д–Њ–њ–µ—А–∞–Ј–Њ–љ/—Б—Г–ї—М–±–∞–Ї—В–∞–Љ
–¶–µ—Д–∞–ї–Њ—Б–њ–Њ—А–Є–љ III –њ–Њ–Ї–Њ–ї–µ–љ–Є—П –≤ –Ї–Њ–Љ–±–Є–љ–∞—Ж–Є–Є —Б –Є–љ–≥–Є–±–Є—В–Њ—А–Њ–Љ bвАУ–ї–∞–Ї—В–∞–Љ–∞–Ј.
–Ю–±–ї–∞—Б—В—М –њ—А–Є–Љ–µ–љ–µ–љ–Є—П —Н—В–Њ–≥–Њ –њ—А–µ–њ–∞—А–∞—В–∞ –Њ–њ—А–µ–і–µ–ї—П–µ—В—Б—П –љ–µ–≤—Л—Б–Њ–Ї–Њ–є —Г—Б—В–Њ–є—З–Є–≤–Њ—Б—В—М—О –љ–Њ–Ј–Њ–Ї–Њ–Љ–Є–∞–ї—М–љ—Л—Е —И—В–∞–Љ–Љ–Њ–≤ Enterobacteriaceae (–Љ–µ–љ—М—И–µ —З–µ–Љ —Г —Ж–µ—Д–∞–ї–Њ—Б–њ–Њ—А–Є–љ–Њ–≤ IIIвАУIV –њ–Њ–Ї–Њ–ї–µ–љ–Є–є) –Є –≤—Л—Б–Њ–Ї–Њ–є –њ—А–Є—А–Њ–і–љ–Њ–є —З—Г–≤—Б—В–≤–Є—В–µ–ї—М–љ–Њ—Б—В—М—О Acinetobacter spp. –Ї —Н—В–Њ–є –Ї–Њ–Љ–±–Є–љ–∞—Ж–Є–Є. –Т –Њ—В–ї–Є—З–Є–µ –Њ—В –і—А—Г–≥–Є—Е —Ж–µ—Д–∞–ї–Њ—Б–њ–Њ—А–Є–љ–Њ–≤—Л—Е –∞–љ—В–Є–±–Є–Њ—В–Є–Ї–Њ–≤ –Њ–±–ї–∞–і–∞–µ—В –≤—Л—Б–Њ–Ї–Њ–є –∞–Ї—В–Є–≤–љ–Њ—Б—В—М—О –њ—А–Њ—В–Є–≤ –∞–љ–∞—Н—А–Њ–±–љ—Л—Е –±–∞–Ї—В–µ—А–Є–є.
–Ю—Б–љ–Њ–≤–љ—Л–µ –њ–Њ–Ї–∞–Ј–∞–љ–Є—П:
вАҐ –Т –Ї–∞—З–µ—Б—В–≤–µ —Н–Љ–њ–Є—А–Є—З–µ—Б–Ї–Њ–є —В–µ—А–∞–њ–Є–Є:
вАУ –У–Њ—Б–њ–Є—В–∞–ї—М–љ—Л–µ –∞–±–і–Њ–Љ–Є–љ–∞–ї—М–љ—Л–µ –Є–љ—Д–µ–Ї—Ж–Є–Є вАУ –њ–µ—А–Є—В–Њ–љ–Є—В, –∞–±—Б—Ж–µ—Б—Б, –Є–љ—Д–Є—Ж–Є—А–Њ–≤–∞–љ–љ—Л–є –њ–∞–љ–Ї—А–µ–Њ–љ–µ–Ї—А–Њ–Ј, –Є–љ—Д–µ–Ї—Ж–Є–Є –њ–µ—З–µ–љ–Є –Є –ґ–µ–ї—З–µ–≤—Л–≤–Њ–і—П—Й–Є—Е –њ—Г—В–µ–є (—Б—А–µ–і—Б—В–≤–Њ –≤—Л–±–Њ—А–∞)
вАУ –°–µ–њ—Б–Є—Б (–Ї—А–Њ–Љ–µ –∞–љ–≥–Є–Њ–≥–µ–љ–љ–Њ–≥–Њ)
вАУ –Т–µ–љ—В–Є–ї—П—В–Њ—АвАУ–∞—Б—Б–Њ—Ж–Є–Є—А–Њ–≤–∞–љ–љ–∞—П –њ–љ–µ–≤–Љ–Њ–љ–Є—П (—Б—А–µ–і—Б—В–≤–Њ –≤—Л–±–Њ—А–∞)
–Ъ–∞—А–±–∞–њ–µ–љ–µ–Љ—Л
–Ъ —Н—В–Њ–є –≥—А—Г–њ–њ–µ –Њ—В–љ–Њ—Б—П—В—Б—П –Є–Љ–Є–њ–µ–љ–µ–Љ, –Љ–µ—А–Њ–њ–µ–љ–µ–Љ, —Н—А—В–∞–њ–µ–љ–µ–Љ. –Р–љ—В–Є–±–Є–Њ—В–Є–Ї–∞–Љ –≥—А—Г–њ–њ—Л –Ї–∞—А–±–∞–њ–µ–љ–µ–Љ–Њ–≤ —Б–≤–Њ–є—Б—В–≤–µ–љ –љ–∞–Є–±–Њ–ї–µ–µ —И–Є—А–Њ–Ї–Є–є —Б–њ–µ–Ї—В—А –∞–љ—В–Є–Љ–Є–Ї—А–Њ–±–љ–Њ–є –∞–Ї—В–Є–≤–љ–Њ—Б—В–Є —Б—А–µ–і–Є –≤—Б–µ—Е –њ—А–µ–њ–∞—А–∞—В–Њ–≤ –Ї–ї–∞—Б—Б–∞ bвАУ–ї–∞–Ї—В–∞–Љ–Њ–≤.
–Ъ–∞—А–±–∞–њ–µ–љ–µ–Љ—Л –Њ–±–ї–∞–і–∞—О—В —И–Є—А–Њ–Ї–Є–Љ —Б–њ–µ–Ї—В—А–Њ–Љ –∞–љ—В–Є–Љ–Є–Ї—А–Њ–±–љ–Њ–є –∞–Ї—В–Є–≤–љ–Њ—Б—В–Є, –≤ —В–Њ–Љ —З–Є—Б–ї–µ –њ—А–Њ—В–Є–≤ –∞—Н—А–Њ–±–љ—Л—Е –У—А–∞–Љ(+) –Є –У—А–∞–Љ(вАУ) –Љ–Є–Ї—А–Њ–Њ—А–≥–∞–љ–Є–Ј–Љ–Њ–≤, –∞ —В–∞–Ї–ґ–µ –∞–љ–∞—Н—А–Њ–±–Њ–≤. –Ш–Љ–Є–њ–µ–љ–µ–Љ –Є –Љ–µ—А–Њ–њ–µ–љ–µ–Љ, –≤ –Њ—В–ї–Є—З–Є–µ –Њ—В —Н—А—В–∞–њ–µ–љ–µ–Љ–∞, –њ—А–Њ—П–≤–ї—П—О—В –∞–Ї—В–Є–≤–љ–Њ—Б—В—М –≤ –Њ—В–љ–Њ—И–µ–љ–Є–Є –љ–µ—Д–µ—А–Љ–µ–љ—В–Є—А—Г—О—Й–Є—Е –Љ–Є–Ї—А–Њ–Њ—А–≥–∞–љ–Є–Ј–Љ–Њ–≤ (Pseudomonas aeruginosa, Acineto¬≠bacter spp.), —З—В–Њ –Њ–±—К—П—Б–љ—П–µ—В –Є—Б–Ї–ї—О—З–Є—В–µ–ї—М–љ–Њ ¬Ђ–≤–љ–µ–±–Њ–ї—М–љ–Є—З–љ—Л–µ –њ–Њ–Ї–∞–Ј–∞–љ–Є—П¬ї —Н—А—В–∞–њ–µ–љ–µ–Љ–∞, —В.–µ. –љ–µ–≤–Њ–Ј–Љ–Њ–ґ–љ–Њ—Б—В—М –ї–µ—З–µ–љ–Є—П –і–∞–љ–љ—Л–Љ –њ—А–µ–њ–∞—А–∞—В–Њ–Љ –≥–Њ—Б–њ–Є—В–∞–ї—М–љ—Л—Е –Є–љ—Д–µ–Ї—Ж–Є–є. –Я–Њ –њ—А–Є—А–Њ–і–љ–Њ–є –∞–Ї—В–Є–≤–љ–Њ—Б—В–Є –≤ –Њ—В–љ–Њ—И–µ–љ–Є–Є –≥—А–∞–Љ–њ–Њ–ї–Њ–ґ–Є—В–µ–ї—М–љ—Л—Е –±–∞–Ї—В–µ—А–Є–є –Є –≥—А–∞–Љ–Њ—В—А–Є—Ж–∞—В–µ–ї—М–љ—Л—Е —Н–љ—В–µ—А–Њ–±–∞–Ї—В–µ—А–Є–є (E. coli –Є –і—А.) —Б—Г—Й–µ—Б—В–≤–µ–љ–љ—Л—Е —А–∞–Ј–ї–Є—З–Є–є –Љ–µ–ґ–і—Г –Ї–∞—А–±–µ–њ–µ–љ–µ–Љ–∞–Љ–Є –љ–µ –Њ—В–Љ–µ—З–µ–љ–Њ. –Т –Њ—В–љ–Њ—И–µ–љ–Є–Є Acinetobacter spp. –Є–Љ–Є–њ–µ–љ–µ–Љ –Є –Љ–µ—А–Њ–њ–µ–љ–µ–Љ –њ—А–Њ—П–≤–ї—П—О—В —А–∞–≤–љ—Г—О –∞–Ї—В–Є–≤–љ–Њ—Б—В—М. –†–∞–Ј–ї–Є—З–Є—П –Љ–µ–ґ–і—Г —Н—В–Є–Љ–Є –∞–љ—В–Є–±–Є–Њ—В–Є–Ї–∞–Љ–Є –Ј–∞–Ї–ї—О—З–∞—О—В—Б—П –≤ –±–Њ–ї–µ–µ –≤—Л—Б–Њ–Ї–Њ–є –њ—А–Є—А–Њ–і–љ–Њ–є –∞–љ—В–Є–њ—Б–µ–≤–і–Њ–Љ–Њ–љ–∞–і–љ–Њ–є –∞–Ї—В–Є–≤–љ–Њ—Б—В–Є –Љ–µ—А–Њ–њ–µ–љ–µ–Љ–∞ (–Ь–µ—А–Њ–љ–µ–Љ) вАУ —Н—В–Њ—В –∞–љ—В–Є–±–Є–Њ—В–Є–Ї –њ–Њ–і–∞–≤–ї—П–µ—В —А–Њ—Б—В P. aeruginosa –≤ —Б—А–µ–і–љ–Є—Е –Ї–Њ–љ—Ж–µ–љ—В—А–∞—Ж–Є—П—Е 0,25вАУ0,5 –Љ–≥/–ї, –≤ —В–Њ –≤—А–µ–Љ—П –Ї–∞–Ї –Є–Љ–Є–њ–µ–љ–µ–Љ вАУ 1вАУ2 –Љ–≥/–ї. –≠—В–Є —А–∞–Ј–ї–Є—З–Є—П, –љ–µ –Њ—З–µ–љ—М –Ј–љ–∞—З–Є—В–µ–ї—М–љ—Л–µ in vitro, –Љ–Њ–≥—Г—В –Є–Љ–µ—В—М –Њ–њ—А–µ–і–µ–ї—П—О—Й–µ–µ –Ј–љ–∞—З–µ–љ–Є–µ –≤ –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Њ–є –њ—А–∞–Ї—В–Є–Ї–µ –≤ —Г—Б–ї–Њ–≤–Є—П—Е –Њ—В—З–µ—В–ї–Є–≤–Њ–≥–Њ —Б–љ–Є–ґ–µ–љ–Є—П —З—Г–≤—Б—В–≤–Є—В–µ–ї—М–љ–Њ—Б—В–Є –≥–Њ—Б–њ–Є—В–∞–ї—М–љ—Л—Е —И—В–∞–Љ–Љ–Њ–≤ P. aeruginosa –Ї –∞–љ—В–Є–±–Є–Њ—В–Є–Ї–∞–Љ. –Т —Н—В–Є—Е —Г—Б–ї–Њ–≤–Є—П—Е, –і–∞–ґ–µ –љ–µ–±–Њ–ї—М—И–Њ–µ –њ–Њ–≤—Л—И–µ–љ–Є–µ –Ь–Я–Ъ –Љ–Њ–ґ–µ—В –њ—А–Є–≤–Њ–і–Є—В –Ї –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Њ–є –љ–µ—Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В–Є –∞–љ—В–Є–±–Є–Њ—В–Є–Ї–∞ –њ—А–Є –µ–≥–Њ –њ—А–Є–Љ–µ–љ–µ–љ–Є–Є –≤ —В–µ—А–∞–њ–µ–≤—В–Є—З–µ—Б–Ї–Є—Е –і–Њ–Ј–∞—Е. –Т –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П—Е, –њ—А–Њ–≤–µ–і–µ–љ–љ—Л—Е –≤ –њ–Њ—Б–ї–µ–і–љ–Є–µ –≥–Њ–і—Л –њ–Њ–Ї–∞–Ј–∞–љ–Њ, —З—В–Њ –≤ —Б–ї—Г—З–∞–µ –љ–µ–≤—Л—Б–Њ–Ї–Њ–≥–Њ —Г—А–Њ–≤–љ—П —Г—Б—В–Њ–є—З–Є–≤–Њ—Б—В–Є P. aeruginosa –Љ–µ—А–Њ–њ–µ–љ–µ–Љ –≤ –≤—Л—Б–Њ–Ї–Є—Е –і–Њ–Ј–∞—Е (4вАУ6 –≥/—Б—Г—В.) –Љ–Њ–ґ–µ—В —Б–Њ—Е—А–∞–љ—П—В—М –Ї–ї–Є–љ–Є—З–µ—Б–Ї—Г—О —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В—М.
–Ю—Б–љ–Њ–≤–љ—Л–Љ –і–Њ—Б—В–Њ–Є–љ—Б—В–≤–Њ–Љ –Ї–∞—А–±–∞–њ–µ–љ–µ–Љ–Њ–≤, –Њ–њ—А–µ–і–µ–ї—П—О—Й–Є–Љ –Є—Е –≤–∞–ґ–љ–Њ–µ –Ј–љ–∞—З–µ–љ–Є–µ –≤ –Љ–µ–і–Є—Ж–Є–љ–µ, —П–≤–ї—П–µ—В—Б—П –љ–Є–Ј–Ї–Є–є —Г—А–Њ–≤–µ–љ—М —Г—Б—В–Њ–є—З–Є–≤–Њ—Б—В–Є –±–Њ–ї—М—И–Є–љ—Б—В–≤–∞ –≤–Њ–Ј–±—Г–і–Є—В–µ–ї–µ–є –≥–Њ—Б–њ–Є—В–∞–ї—М–љ—Л—Е –Є–љ—Д–µ–Ї—Ж–Є–є, –Ј–∞ –Є—Б–Ї–ї—О—З–µ–љ–Є–µ–Љ P. aeruginosa. –Ґ–∞–Ї, –і–Њ –љ–∞—Б—В–Њ—П—Й–µ–≥–Њ –≤—А–µ–Љ–µ–љ–Є –љ–µ –≤—Л—П–≤–ї–µ–љ–Њ —И—В–∞–Љ–Љ–Њ–≤ —Б—В—А–µ–њ—В–Њ¬≠–Ї–Њ–Ї¬≠–Ї–Њ–≤/–њ–љ–µ–≤–Љ–Њ–Ї–Њ–Ї–Ї–Њ–≤, E. coli, P. mirabilis, —Г—Б—В–Њ–є—З–Є–≤—Л—Е –Ї –Ї–∞—А¬≠–±–∞¬≠–њ–µ–љ–µ–Љ–∞–Љ. –Ъ–∞—А–±–∞–њ–µ–љ–µ–Љ—Л –љ–µ –њ–Њ–і–≤–µ—А–≥–∞—О—В—Б—П –≥–Є–і—А–Њ–ї–Є–Ј—Г bвАУ–ї–∞–Ї—В–∞–Љ–∞–Ј–∞–Љ–Є –Ї–ї–∞—Б—Б–∞ –Р, –≤ —В–Њ–Љ —З–Є—Б–ї–µ —А–∞—Б—И–Є—А–µ–љ–љ–Њ–≥–Њ —Б–њ–µ–Ї—В—А–∞, –∞ —В–∞–Ї–ґ–µ –Ї–ї–∞—Б—Б–∞ –°, —З—В–Њ —П–≤–ї—П–µ—В—Б—П –Њ–њ—А–µ–і–µ–ї—П—О—Й–Є–Љ —Д–∞–Ї—В–Њ—А–Њ–Љ –њ—А–µ–Є–Љ—Г—Й–µ—Б—В–≤–∞ –Ї–ї–∞—Б—Б–∞ –Ї–∞—А–±–Њ–њ–µ–љ–µ–Љ–Њ–≤ –њ–µ—А–µ–і —Ж–µ—Д–∞–ї–Њ—Б–њ–Њ—А–Є–љ–∞–Љ–Є (–∞–Ї—В–Є–≤–љ–Њ—Б—В—М –≤ —Б–ї—Г—З–∞–µ –С–Ы–†–°вАУ–њ—А–Њ–і—Г—Ж–Є—А—Г—О—Й–Є—Е –њ–∞—В–Њ–≥–µ–љ–Њ–≤ –і–Њ 99вАУ100%). –Т –Љ–Є—А–µ –≤—Л–і–µ–ї–µ–љ—Л –ї–Є—И—М –µ–і–Є–љ–Є—З–љ—Л–µ —И—В–∞–Љ–Љ—Л Klebsiella spp., Enterobacter spp., —Г—Б—В–Њ–є—З–Є–≤—Л–µ –Ї –Ї–∞—А–±–∞–њ–µ–љ–µ–Љ–∞–Љ. –С–Њ–ї—М—И–Є–љ—Б—В–≤–Њ —И—В–∞–Љ–Љ–Њ–≤ –∞—Ж–Є–љ–µ—В–Њ–±–∞–Ї—В–µ—А–Є–є —В–∞–Ї–ґ–µ —Б–Њ—Е—А–∞–љ—П—О—В —З—Г–≤—Б—В–≤–Є—В–µ–ї—М–љ–Њ—Б—В—М –Ї –Ї–∞—А–±–∞–њ–µ–љ–µ–Љ–∞–Љ. –≠—В–Є–Љ –Њ–±—К—П—Б–љ—П–µ—В—Б—П —В–Њ—В —Д–∞–Ї—В, —З—В–Њ –≤ –љ–∞—Б—В–Њ—П—Й–µ–µ –≤—А–µ–Љ—П –Ї–∞—А–±–∞–њ–µ–љ–µ–Љ—Л —А–∞—Б—Б–Љ–∞—В—А–Є–≤–∞—О—В—Б—П –Ї–∞–Ї —Б–∞–Љ—Л–µ –љ–∞–і–µ–ґ–љ—Л–µ —Б—А–µ–і—Б—В–≤–∞ —Н–Љ–њ–Є—А–Є—З–µ—Б–Ї–Њ–є —В–µ—А–∞–њ–Є–Є –≥–Њ—Б–њ–Є—В–∞–ї—М–љ—Л—Е –Є–љ—Д–µ–Ї—Ж–Є–є.
–£—Б—В–Њ–є—З–Є–≤–Њ—Б—В—М Enterobacteriaceae –Є Acinetobacter spp. –Ї –Ї–∞—А–±–∞–њ–µ–љ–µ–Љ–∞–Љ –њ–µ—А–µ–Ї—А–µ—Б—В–љ–∞—П, –≤ —В–Њ –ґ–µ –≤—А–µ–Љ—П —Г—Б—В–Њ–є—З–Є–≤–Њ—Б—В—М P. aeruginosa –Љ–Њ–ґ–µ—В —А–∞–Ј–ї–Є—З–∞—В—М—Б—П. –Ю—В—Б—Г—В¬≠—Б—В–≤–Є–µ –њ–Њ–ї–љ–Њ–є –њ–µ—А–µ–Ї—А–µ—Б—В–љ–Њ–є —Г—Б—В–Њ–є—З–Є–≤–Њ—Б—В–Є —Б–Є–љ–µ–≥–љ–Њ–є–љ–Њ–є –њ–∞–ї–Њ—З–Ї–Є –Љ–µ–ґ–і—Г –Љ–µ—А–Њ–њ–µ–љ–µ–Љ–Њ–Љ –Є –Є–Љ–Є–њ–µ–љ–µ–Љ–Њ–Љ –Њ–±—К—П—Б–љ—П–µ—В—Б—П —А–∞–Ј–љ—Л–Љ–Є –Љ–µ—Е–∞–љ–Є–Ј–Љ–∞–Љ–Є —Г—Б—В–Њ–є—З–Є–≤–Њ—Б—В–Є.
–Ю—Б–љ–Њ–≤–љ–Њ–є –Љ–µ—Е–∞–љ–Є–Ј–Љ —Г—Б—В–Њ–є—З–Є–≤–Њ—Б—В–Є P. aeruginosa –Ї –Є–Љ–Є–њ–µ–љ–µ–Љ—Г —Б–≤—П–Ј–∞–љ —Б –љ–∞—А—Г—И–µ–љ–Є–µ–Љ –њ—А–Њ–љ–Є—Ж–∞–µ–Љ–Њ—Б—В–Є –Љ–Є–Ї—А–Њ–±–љ–Њ–є –Ї–ї–µ—В–Ї–Є –і–ї—П –∞–љ—В–Є–±–Є–Њ—В–Є–Ї–∞ –≤—Б–ї–µ–і—Б—В–≤–Є–µ —Г—В—А–∞—В—Л –њ–Њ—А–Є–љ–Њ–≤–Њ–≥–Њ –Ї–∞–љ–∞–ї–∞ OprD –≤ —А–µ–Ј—Г–ї—М—В–∞—В–µ –Љ—Г—В–∞—Ж–Є–Є. –Э–∞ —Д–Њ–љ–µ –Є–Љ–Є–њ–µ–љ–µ–Љ–∞ –і–Њ—Б—В–∞—В–Њ—З–љ–Њ –±—Л—Б—В—А–Њ –њ—А–Њ–Є—Б—Е–Њ–і–Є—В —Б–µ–ї–µ–Ї—Ж–Є—П —В–∞–Ї–Є—Е –Љ—Г—В–∞–љ—В–Њ–≤. –І–∞—Б—В–Њ—В–∞ –Љ—Г—В–∞—Ж–Є–є, –њ—А–Є–≤–Њ–і—П—Й–Є—Е –Ї —Г—В—А–∞—В–µ OprD —Б–Њ—Б—В–∞–≤–ї—П–µ—В 10вАУ7, –њ—А–Є—З–µ–Љ —Н—В–Њ —З–∞—Б—В–Њ —Б–Њ—З–µ—В–∞–µ—В—Б—П —Б –≥–Є–њ–µ—А–њ—А–Њ–і—Г–Ї—Ж–Є–µ–є —Е—А–Њ–Љ–Њ—Б–Њ–Љ–љ—Л—Е AmpC bвАУ–ї–∞–Ї—В–∞–Љ–∞–Ј. –Т —А–µ–Ј—Г–ї—М—В–∞—В–µ –Ј–љ–∞—З–µ–љ–Є—П –Ь–Я–Ъ –Є–Љ–Є–њ–µ–љ–µ–Љ–∞ –≤–Њ–Ј—А–∞—Б—В–∞—О—В –і–Њ 8вАУ32 –Љ–Ї–≥/–Љ–ї, —З—В–Њ —Б–Њ–њ—А–Њ–≤–Њ–ґ–і–∞–µ—В—Б—П –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Њ–є –љ–µ—Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В—М—О –ї–µ—З–µ–љ–Є—П. –Я–Њ—В–µ—А—П –њ–Њ—А–Є–љ–∞ OprD –љ–µ –Ї—А–Є—В–Є—З–љ–∞ –і–ї—П –Љ–µ—А–Њ–њ–µ–љ–µ–Љ–∞, —В–∞–Ї –Ї–∞–Ї –∞–љ—В–Є–±–Є–Њ—В–Є–Ї –Є—Б–њ–Њ–ї—М–Ј—Г–µ—В –і–ї—П –њ—А–Њ–љ–Є–Ї–љ–Њ–≤–µ–љ–Є—П –≤ –Ї–ї–µ—В–Ї—Г –Є –і—А—Г–≥–Є–µ –њ–Њ—А–Є–љ–Њ–≤—Л–µ –Ї–∞–љ–∞–ї—Л. –Ъ—А–Њ–Љ–µ —В–Њ–≥–Њ, –Љ–µ—А–Њ–њ–µ–љ–µ–Љ (–Ь–µ—А–Њ–љ–µ–Љ) –њ—А–Њ—П–≤–ї—П–µ—В –±–Њ–ї—М—И—Г—О —Б—В–∞–±–Є–ї—М–љ–Њ—Б—В—М –Ї —Е—А–Њ–Љ–Њ—Б–Њ–Љ–љ—Л–Љ bвАУ–ї–∞–Ї—В–∞–Љ–∞–Ј–∞–Љ —З–µ–Љ –Є–Љ–Є–њ–µ–љ–µ–Љ, –њ–Њ—Н—В–Њ–Љ—Г —Г–Ї–∞–Ј–∞–љ–љ—Л–µ –≤—Л—И–µ –Љ—Г—В–∞—Ж–Є–Є –љ–µ –њ—А–Є–≤–Њ–і—П—В –Ї —А–Њ—Б—В—Г –Ь–Я–Ъ –і–ї—П –Љ–µ—А–Њ–њ–µ–љ–µ–Љ–∞.
–Ю—Б–љ–Њ–≤–љ–Њ–є –Љ–µ—Е–∞–љ–Є–Ј–Љ —Г—Б—В–Њ–є—З–Є–≤–Њ—Б—В–Є P. aeruginosa –Ї –Љ–µ—А–Њ–њ–µ–љ–µ–Љ—Г —Б–≤—П–Ј–∞–љ —Б –∞–Ї—В–Є–≤–∞—Ж–Є–µ–є —Б–Є—Б—В–µ–Љ —Н—Д—Д–ї—О–Ї—Б–љ–Њ–є –њ–Њ–Љ–њ—Л (MexAвАУMexBвАУOprM), –њ—А–Є—З–µ–Љ –≤ —А–µ–Ј—Г–ї—М—В–∞—В–µ —В–∞–Ї–Њ–є –Њ—В–і–µ–ї—М–љ–Њ–є –Љ—Г—В–∞—Ж–Є–Є –Ј–љ–∞—З–µ–љ–Є—П –Ь–Я–Ъ –Љ–µ—А–Њ–њ–µ–љ–µ–Љ–∞ –њ–Њ–≤—Л—И–∞—О—В—Б—П, –љ–Њ –љ–µ–Ј–љ–∞—З–Є—В–µ–ї—М–љ–Њ (–і–Њ 2вАУ4 –Љ–Ї–≥/–Љ–ї), –Є –Ї–ї–Є–љ–Є—З–µ—Б–Ї–∞—П —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В—М –∞–љ—В–Є–±–Є–Њ—В–Є–Ї–∞ –Љ–Њ–ґ–µ—В —Б–Њ—Е—А–∞–љ—П—В—М—Б—П. –Ф–ї—П —В–Њ–≥–Њ, —З—В–Њ–±—Л –Ј–љ–∞—З–µ–љ–Є—П –Ь–Я–Ъ –Љ–µ—А–Њ–њ–µ–љ–µ–Љ–∞ –≤—Л—А–Њ—Б–ї–Є –Ј–љ–∞—З–Є—В–µ–ї—М–љ–Њ, –љ–µ–Њ–±—Е–Њ–і–Є–Љ–Њ –Њ–і–љ–Њ–≤—А–µ–Љ–µ–љ–љ–Њ –і–≤–µ –Љ—Г—В–∞—Ж–Є–Є вАУ –∞–Ї—В–Є–≤–∞—Ж–Є—П —Н—Д—Д–ї—О–Ї—Б–љ–Њ–є –њ–Њ–Љ–њ—Л –Є —Г—В—А–∞—В–∞ –њ–Њ—А–Є–љ–Њ–≤–Њ–≥–Њ –Ї–∞–љ–∞–ї–∞, –Њ–і–љ–∞–Ї–Њ –≤–µ—А–Њ—П—В–љ–Њ—Б—В—М —В–∞–Ї–Њ–≥–Њ —Б–Њ–±—Л—В–Є—П –Ј–љ–∞—З–Є—В–µ–ї—М–љ–Њ –Љ–µ–љ—М—И–µ вАУ 10вАУ14. –£–Ї–∞–Ј–∞–љ–љ—Л–µ —А–∞–Ј–ї–Є—З–Є—П –≤ –Љ–µ—Е–∞–љ–Є–Ј–Љ–∞—Е —Г—Б—В–Њ–є—З–Є–≤–Њ—Б—В–Є –Њ–±—К—П—Б–љ—П—О—В, –њ–Њ—З–µ–Љ—Г —А–µ–Ј–Є—Б—В–µ–љ—В–љ–Њ—Б—В—М P. aeruginosa –Ї –Љ–µ—А–Њ–њ–µ–љ–µ–Љ—Г —А–∞–Ј–≤–Є–≤–∞–µ—В—Б—П –Љ–µ–і–ї–µ–љ–љ–µ–µ, —З–µ–Љ –Ї –Є–Љ–Є–њ–µ–љ–µ–Љ—Г, —З—В–Њ –љ–∞–≥–ї—П–і–љ–Њ –≤–Є–і–љ–Њ –Є–Ј –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П –∞–љ—В–Є–±–Є–Њ—В–Є–Ї–Њ—А–µ–Ј–Є—Б—В–µ–љ—В–љ–Њ—Б—В–Є MYSTIC (1997вАУ2005 –≥–≥.). –≠—В–Њ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ –њ–Њ–Ї–∞–Ј–∞–ї–Њ, —З—В–Њ –≤ —Б—В—А–∞–љ–∞—Е –Т–Њ—Б—В–Њ—З–љ–Њ–є –Х–≤—А–Њ–њ—Л —З–∞—Б—В–Њ—В–∞ –≤—Л—Б–Њ–Ї–Њ—З—Г–≤—Б—В–≤–Є—В–µ–ї—М–љ—Л—Е —И—В–∞–Љ–Љ–Њ–≤ P. aeruginosa (–Ь–Я–Ъ<1 –Љ–≥/–ї) –±—Л–ї–∞ –≤—Л—И–µ –і–ї—П –Љ–µ—А–Њ–њ–µ–љ–µ–Љ–∞ (38,7%), —З–µ–Љ –і–ї—П –Є–Љ–Є–њ–µ–љ–µ–Љ–∞ (12,4%). –Т –Њ—В–љ–Њ—И–µ–љ–Є–Є –Є–Љ–Є–њ–µ–љ–µ–ЉвАУ—А–µ–Ј–Є—Б—В–µ–љ—В–љ—Л—Е —И—В–∞–Љ–Љ–Њ–≤ –Љ–µ—А–Њ–њ–µ–љ–µ–Љ –њ—А–Њ—П–≤–ї—П–ї –∞–Ї—В–Є–≤–љ–Њ—Б—В—М –≤ 11,2вАУ31,3%, –≤ —В–Њ –≤—А–µ–Љ—П –Ї–∞–Ї –≤ –Њ—В–љ–Њ—И–µ–љ–Є–Є –Љ–µ—А–Њ–њ–µ–љ–µ–ЉвАУ—А–µ–Ј–Є—Б—В–µ–љ—В–љ—Л—Е —И—В–∞–Љ–Љ–Њ–≤ –Є–Љ–Є–њ–µ–љ–µ–Љ —Б–Њ—Е—А–∞–љ—П–ї –∞–Ї—В–Є–≤–љ–Њ—Б—В—М —В–Њ–ї—М–Ї–Њ –≤ 2,2вАУ7,4%. –≠—В–Є –і–∞–љ–љ—Л–µ –њ–Њ–Ї–∞–Ј—Л–≤–∞—О—В, —З—В–Њ –≤ –Њ—В–і–µ–ї–µ–љ–Є—П—Е —А–µ–∞–љ–Є–Љ–∞—Ж–Є–Є –Є –Є–љ—В–µ–љ—Б–Є–≤–љ–Њ–є —В–µ—А–∞–њ–Є–Є –њ—А–Є –њ—А–Њ–≤–µ–і–µ–љ–Є–Є —Н–Љ–њ–Є—А–Є—З–µ—Б–Ї–Њ–є —В–µ—А–∞–њ–Є–Є –љ–Њ–Ј–Њ–Ї–Њ–Љ–Є–∞–ї—М–љ–Њ–є –њ–љ–µ–≤–Љ–Њ–љ–Є–Є, –≤–µ–і—Г—Й–Є–Љ –≤–Њ–Ј–±—Г–і–Є—В–µ–ї–µ–Љ –Ї–Њ—В–Њ—А–Њ–є —П–≤–ї—П–µ—В—Б—П —Б–Є–љ–µ–≥–љ–Њ–є–љ–∞—П –њ–∞–ї–Њ—З–Ї–∞, –±–Њ–ї–µ–µ —Ж–µ–ї–µ—Б–Њ–Њ–±—А–∞–Ј–љ–Њ –љ–∞–Ј–љ–∞—З–µ–љ–Є–µ –Љ–µ—А–Њ–њ–µ–љ–µ–Љ–∞. –Т —Е–Є—А—Г—А–≥–Є—З–µ—Б–Ї–Є—Е –Њ—В–і–µ–ї–µ–љ–Є—П—Е, –≥–і–µ –Ј–љ–∞—З–µ–љ–Є–µ —Б–Є–љ–µ–≥–љ–Њ–є–љ–Њ–є –њ–∞–ї–Њ—З–Ї–Є –љ–Є–ґ–µ, –њ—А–Њ–≥–љ–Њ–Ј–Є—А—Г–µ—В—Б—П –Њ–і–Є–љ–∞–Ї–Њ–≤–∞—П —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В—М —Н—В–Є—Е –∞–љ—В–Є–±–Є–Њ—В–Є–Ї–Њ–≤.
–Ь–µ—А–Њ–њ–µ–љ–µ–Љ
–Ю—Б–љ–Њ–≤–љ—Л–µ –њ–Њ–Ї–∞–Ј–∞–љ–Є—П:
вАҐ –Ґ—П–ґ–µ–ї—Л–µ –≥–Њ—Б–њ–Є—В–∞–ї—М–љ—Л–µ –Є–љ—Д–µ–Ї—Ж–Є–Є, –≤—Л–Ј–≤–∞–љ–љ—Л–µ –У—А–∞–Љ(вАУ) –±–∞–Ї—В–µ—А–Є—П–Љ–Є, —А–µ–Ј–Є—Б—В–µ–љ—В–љ—Л–Љ–Є –Ї —Ж–µ—Д–∞–ї–Њ—Б–њ–Њ—А–Є–љ–∞–Љ IIIвАУIV –њ–Њ–Ї–Њ–ї–µ–љ–Є–є –Є —Д—В–Њ—А—Е–Є–љ–Њ–ї–Њ–љ–∞–Љ (—Б—А–µ–і—Б—В–≤–Њ –≤—Л–±–Њ—А–∞).
вАҐ –Ш–љ—Д–µ–Ї—Ж–Є–Є, –≤—Л–Ј–≤–∞–љ–љ—Л–µ E. coli –Є Klebsiella spp. —Б –њ—А–Њ–і—Г–Ї—Ж–Є–µ–є bвАУ–ї–∞–Ї—В–∞–Љ–∞–Ј —А–∞—Б—И–Є—А–µ–љ–љ–Њ–≥–Њ —Б–њ–µ–Ї—В—А–∞ (—Б—А–µ–і—Б—В–≤–Њ –≤—Л–±–Њ—А–∞)
вАҐ –Ш–љ—Д–µ–Ї—Ж–Є–Є, –≤—Л–Ј–≤–∞–љ–љ—Л–µ P. aeruginosa, Acinetobacter spp.
вАҐ –Т –Ї–∞—З–µ—Б—В–≤–µ —Б—А–µ–і—Б—В–≤–∞ —Н–Љ–њ–Є—А–Є—З–µ—Б–Ї–Њ–є —В–µ—А–∞–њ–Є–Є:
вАУ –У–Њ—Б–њ–Є—В–∞–ї—М–љ–∞—П –њ–љ–µ–≤–Љ–Њ–љ–Є—П, –≤ —В.—З. –≤–µ–љ—В–Є–ї—П—В–Њ—АвАУ–∞—Б—Б–Њ—Ж–Є–Є—А–Њ–≤–∞–љ–љ–∞—П (—Б—А–µ–і—Б—В–≤–Њ –≤—Л–±–Њ—А–∞)
вАУ –Ы–µ–≥–Њ—З–љ—Л–µ –љ–∞–≥–љ–Њ–µ–љ–Є—П (–∞–±—Б—Ж–µ—Б—Б, —Н–Љ–њ–Є–µ–Љ–∞)
вАУ –С—А–Њ–љ—Е–ЊвАУ–ї–µ–≥–Њ—З–љ—Л–µ –Є–љ—Д–µ–Ї—Ж–Є–Є —Г –±–Њ–ї—М–љ—Л—Е –Љ—Г–Ї–Њ–≤–Є—Б—Ж–Є–і–Њ–Ј–Њ–Љ (—Б—А–µ–і—Б—В–≤–Њ –≤—Л–±–Њ—А–∞)
вАУ –Ш–љ—В—А–∞–∞–±–і–Њ–Љ–Є–љ–∞–ї—М–љ—Л–µ –Є–љ—Д–µ–Ї—Ж–Є–Є вАУ –њ–µ—А–Є—В–Њ–љ–Є—В, –∞–±—Б—Ж–µ—Б—Б—Л
вАУ –Ш–љ—Д–Є—Ж–Є—А–Њ–≤–∞–љ–љ—Л–є –њ–∞–љ–Ї—А–µ–Њ–љ–µ–Ї—А–Њ–Ј (–њ—А–Є —В—П–ґ–µ–ї–Њ–Љ —В–µ—З–µ–љ–Є–Є вАУ —Б—А–µ–і—Б—В–≤–Њ –≤—Л–±–Њ—А–∞)
вАУ –Ь–µ–љ–Є–љ–≥–Є—В, –≤ —В.—З. –њ–Њ—Б–ї–µ–Њ–њ–µ—А–∞—Ж–Є–Њ–љ–љ—Л–є, –њ–Њ—Б—В—В—А–∞–≤–Љ–∞—В–Є—З–µ—Б–Ї–Є–є.
вАУ –Ґ—П–ґ–µ–ї—Л–є —Б–µ–њ—Б–Є—Б –љ–µ—Г—Б—В–∞–љ–Њ–≤–ї–µ–љ–љ–Њ–є —Н—В–Є–Њ–ї–Њ–≥–Є–Є (—Б—А–µ–і—Б—В–≤–Њ –≤—Л–±–Њ—А–∞)
вАУ –Ш–љ—Д–µ–Ї—Ж–Є–Є —Г –±–Њ–ї—М–љ—Л—Е —Б –љ–µ–є—В—А–Њ–њ–µ–љ–Є–µ–є (—Б—А–µ–і—Б—В–≤–Њ –≤—Л–±–Њ—А–∞)
–†–µ–Ї–Њ–Љ–µ–љ–і—Г–µ–Љ—Л–µ —Б—Г—В–Њ—З–љ—Л–µ –і–Њ–Ј—Л:
1. –Я–љ–µ–≤–Љ–Њ–љ–Є–Є, –Є–љ—Д–µ–Ї—Ж–Є–Є –Љ–Њ—З–µ–≤—Л–≤–Њ–і—П—Й–Є—Е –њ—Г—В–µ–є, –Є–љ—Д–µ–Ї—Ж–Є–Є –≤ –∞–Ї—Г—И–µ—А—Б—В–≤–µ –Є –≥–Є–љ–µ–Ї–Њ–ї–Њ–≥–Є–Є (—Н–љ–і–Њ–Љ–µ—В—А–Є—В –Є –і—А.), –Є–љ—Д–µ–Ї—Ж–Є–Є –Ї–Њ–ґ–Є вАУ 500 –Љ–≥ –≤/–≤ –Ї–∞–ґ–і—Л–µ 8 —З;
2. –У–Њ—Б–њ–Є—В–∞–ї—М–љ—Л–µ –њ–љ–љ–µ–≤–Љ–Њ–љ–Є–Є, –њ–µ—А–Є—В–Њ–љ–Є—В, –њ–Њ–і–Њ–Ј—А–µ–љ–Є–µ –љ–∞ –±–∞–Ї—В–µ—А–Є–∞–ї—М–љ—Г—О –Є–љ—Д–µ–Ї—Ж–Є—О —Г –±–Њ–ї—М–љ—Л—Е —Б —Б–Є–Љ–њ—В–Њ–Љ–∞–Љ–Є –љ–µ–є—В—А–Њ–њ–µ–љ–Є–Є, –∞ —В–∞–Ї–ґ–µ —Б–µ–њ—В–Є—Ж–µ–Љ–Є–Є вАУ 1 –≥ –≤/–≤ –Ї–∞–ґ–і—Л–µ 8 —З;
3. –Ь–µ–љ–Є–љ–≥–Є—В вАУ 2 –≥ –Ї–∞–ґ–і—Л–µ 8 —З;
4. –Ф–Њ–Ј–Є—А–Њ–≤–Ї–∞ —Г –Њ—Б–Њ–±—Л—Е –Ї–∞—В–µ–≥–Њ—А–Є–є –њ–∞—Ж–Є–µ–љ—В–Њ–≤ вАУ —Б–Љ. –њ–Њ–ї–љ—Г—О –Є–љ—Б—В—А—Г–Ї—Ж–Є—О –њ–Њ –њ—А–Є–Љ–µ–љ–µ–љ–Є—О –њ—А–µ–њ–∞—А–∞—В–∞.
–Ш–Љ–Є–њ–µ–љ–µ–Љ
–Ю—Б–љ–Њ–≤–љ—Л–µ –њ–Њ–Ї–∞–Ј–∞–љ–Є—П:
вАҐ –Ґ—П–ґ–µ–ї—Л–µ –≥–Њ—Б–њ–Є—В–∞–ї—М–љ—Л–µ –Є–љ—Д–µ–Ї—Ж–Є–Є, –≤—Л–Ј–≤–∞–љ–љ—Л–µ –У—А–∞–Љ(вАУ) –±–∞–Ї—В–µ—А–Є—П–Љ–Є, —А–µ–Ј–Є—Б—В–µ–љ—В–љ—Л–Љ–Є –Ї —Ж–µ—Д–∞–ї–Њ—Б–њ–Њ—А–Є–љ–∞–Љ IIIвАУIV –њ–Њ–Ї–Њ–ї–µ–љ–Є–є –Є —Д—В–Њ—А—Е–Є–љ–Њ–ї–Њ–љ–∞–Љ (—Б—А–µ–і—Б—В–≤–Њ –≤—Л–±–Њ—А–∞).
вАҐ –Ш–љ—Д–µ–Ї—Ж–Є–Є, –≤—Л–Ј–≤–∞–љ–љ—Л–µ E. coli –Є Klebsiella spp. —Б –њ—А–Њ–і—Г–Ї—Ж–Є–µ–є bвАУ–ї–∞–Ї—В–∞–Љ–∞–Ј —А–∞—Б—И–Є—А–µ–љ–љ–Њ–≥–Њ —Б–њ–µ–Ї—В—А–∞ (—Б—А–µ–і—Б—В–≤–Њ –≤—Л–±–Њ—А–∞).
вАҐ –Ш–љ—Д–µ–Ї—Ж–Є–Є, –≤—Л–Ј–≤–∞–љ–љ—Л–µ P. aeruginosa, Acinetobacter spp.
вАҐ –Т –Ї–∞—З–µ—Б—В–≤–µ —Б—А–µ–і—Б—В–≤–∞ —Н–Љ–њ–Є—А–Є—З–µ—Б–Ї–Њ–є —В–µ—А–∞–њ–Є–Є:
вАУ –У–Њ—Б–њ–Є—В–∞–ї—М–љ–∞—П –њ–љ–µ–≤–Љ–Њ–љ–Є—П, –≤ —В.—З. –≤–µ–љ—В–Є–ї—П—В–Њ—АвАУ–∞—Б—Б–Њ—Ж–Є–Є—А–Њ–≤–∞–љ–љ–∞—П
вАУ –Ы–µ–≥–Њ—З–љ—Л–µ –љ–∞–≥–љ–Њ–µ–љ–Є—П (–∞–±—Б—Ж–µ—Б—Б, —Н–Љ–њ–Є–µ–Љ–∞)
вАУ –С—А–Њ–љ—Е–ЊвАУ–ї–µ–≥–Њ—З–љ—Л–µ –Є–љ—Д–µ–Ї—Ж–Є–Є —Г –±–Њ–ї—М–љ—Л—Е –Љ—Г–Ї–Њ–≤–Є—Б—Ж–Є–і–Њ–Ј–Њ–Љ (—Б—А–µ–і—Б—В–≤–Њ –≤—Л–±–Њ—А–∞)
вАУ –Ш–љ—В—А–∞–∞–±–і–Њ–Љ–Є–љ–∞–ї—М–љ—Л–µ –Є–љ—Д–µ–Ї—Ж–Є–Є вАУ –њ–µ—А–Є—В–Њ–љ–Є—В, –∞–±—Б—Ж–µ—Б—Б—Л
вАУ –Ш–љ—Д–Є—Ж–Є—А–Њ–≤–∞–љ–љ—Л–є –њ–∞–љ–Ї—А–µ–Њ–љ–µ–Ї—А–Њ–Ј
вАУ –Ґ—П–ґ–µ–ї—Л–є —Б–µ–њ—Б–Є—Б –љ–µ—Г—Б—В–∞–љ–Њ–≤–ї–µ–љ–љ–Њ–є —Н—В–Є–Њ–ї–Њ–≥–Є–Є (—Б—А–µ–і—Б—В–≤–Њ –≤—Л–±–Њ—А–∞)
вАУ –Ш–љ—Д–µ–Ї—Ж–Є–Є —Г –±–Њ–ї—М–љ—Л—Е —Б –љ–µ–є—В—А–Њ–њ–µ–љ–Є–µ–є
–≠—А—В–∞–њ–µ–љ–µ–Љ
–Ю—Б–љ–Њ–≤–љ—Л–µ –њ–Њ–Ї–∞–Ј–∞–љ–Є—П:
вАҐ –Ґ—П–ґ–µ–ї—Л–µ –≤–љ–µ–±–Њ–ї—М–љ–Є—З–љ—Л–µ –Є–ї–Є —А–∞–љ–љ–Є–µ –њ–Њ—Б–ї–µ–Њ–њ–µ—А–∞—Ж–Є–Њ–љ–љ—Л–µ –∞–±–і–Њ–Љ–Є–љ–∞–ї—М–љ—Л–µ –Є–љ—Д–µ–Ї—Ж–Є–Є
вАҐ –Ю—Б–ї–Њ–ґ–љ–µ–љ–љ—Л–µ –Є–љ—Д–µ–Ї—Ж–Є–Є –Љ—П–≥–Ї–Є—Е —В–Ї–∞–љ–µ–є, –і–Є–∞–±–µ—В–Є—З–µ—Б–Ї–∞—П —Б—В–Њ–њ–∞ –Є –і—А.)
вАҐ –Ю—Б–ї–Њ–ґ–љ–µ–љ–љ–∞—П –≤–љ–µ–±–Њ–ї—М–љ–Є—З–љ–∞—П –њ–љ–µ–≤–Љ–Њ–љ–Є—П