–Ф–ї—П –Њ–њ—В–Є–Љ–∞–ї—М–љ–Њ–≥–Њ –≤—Л–±–Њ—А–∞ –∞–љ—В–Є–±–Є–Њ—В–Є–Ї–∞ –љ–µ–Њ–±—Е–Њ–і–Є–Љ–Њ —Г—З–Є—В—Л–≤–∞—В—М —Б–њ–µ–Ї—В—А –∞–Ї—В–Є–≤–љ–Њ—Б—В–Є –њ—А–µ–њ–∞—А–∞—В–Њ–≤, –Є—Е —Д–∞—А–Љ–∞–Ї–Њ–Ї–Є–љ–µ—В–Є—З–µ—Б–Ї–Є–µ —Е–∞—А–∞–Ї—В–µ—А–Є—Б—В–Є–Ї–Є, –±–µ–Ј–Њ–њ–∞—Б–љ–Њ—Б—В—М, –њ–µ—А–µ–љ–Њ—Б–Є–Љ–Њ—Б—В—М –Є —Б—В–Њ–Є–Љ–Њ—Б—В—М.
–Я–Њ—Б–ї–µ–і–љ–Є–є —Д–∞–Ї—В–Њ—А –≤ —Б–Њ–≤—А–µ–Љ–µ–љ–љ—Л—Е —Г—Б–ї–Њ–≤–Є—П—Е –њ—А–Є–Њ–±—А–µ—В–∞–µ—В –≤—Б–µ –±–Њ–ї—М—И–µ–µ –Ј–љ–∞—З–µ–љ–Є–µ. –Т —Б—В–∞—В—М–µ —А–∞—Б—Б–Љ–Њ—В—А–µ–љ—Л –њ—Г—В–Є —Б–љ–Є–ґ–µ–љ–Є—П –Ј–∞—В—А–∞—В –љ–∞ –∞–љ—В–Є–±–∞–Ї—В–µ—А–Є–∞–ї—М–љ—Г—О —В–µ—А–∞–њ–Є—О –≤ —Б—В–∞—Ж–Є–Њ–љ–∞—А–µ.
–Т—Б–µ –њ—А–µ–ї–∞–≥–∞–µ–Љ—Л–µ —А–µ—И–µ–љ–Є—П —П–≤–ї—П—О—В—Б—П –љ–∞—Г—З–љ–Њ –Њ–±–Њ—Б–љ–Њ–≤–∞–љ–љ—Л–Љ–Є, –Є—Е —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В—М –њ–Њ–і—В–≤–µ—А–ґ–і–µ–љ–∞ —А–µ–Ј—Г–ї—М—В–∞—В–∞–Љ–Є –њ—А–Њ—Б–њ–µ–Ї—В–Є–≤–љ—Л—Е —А–∞–љ–і–Њ–Љ–Є–Ј–Є—А–Њ–≤–∞–љ–љ—Л—Е –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є—Е –Є—Б–њ—Л—В–∞–љ–Є–є.
For optimal choice of an antibiotic, it is necessary to take into account the spectrum of activities of drugs, their pharmacokinetic characteristics, safety, tolerance, and cost. The latter is of greater importance under the present-day conditions. The paper considers the ways of reducing the cost of antibiotic therapy in the inpatient setting. All the decisions presented are scientifically grounded, their efficiency has been confirmed by the results of prospective randomized clinical trials.
–Ю.–Ы. –†–Њ–Ј–µ–љ—Б–Њ–љ, –Ы.–°. –°—В—А–∞—З—Г–љ—Б–Ї–Є–є – –Ї–∞—Д–µ–і—А–∞ –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Њ–є —Д–∞—А–Љ–∞–Ї–Њ–ї–Њ–≥–Є–Є –Є –∞–љ—В–Є–Љ–Є–Ї—А–Њ–±–љ–Њ–є —Е–Є–Љ–Є–Њ—В–µ—А–∞–њ–Є–Є. –°–Љ–Њ–ї–µ–љ—Б–Ї–∞—П –≥–Њ—Б—Г–і–∞—А—Б—В–≤–µ–љ–љ–∞—П –Љ–µ–і–Є—Ж–Є–љ—Б–Ї–∞—П –∞–Ї–∞–і–µ–Љ–Є—П
O.L. Rozenson, L.S. Strachunsky – department of Clinical Pharmacology and Antimicrobial Chemotherapy, Smolensk State Medical Academy
–Я—А–Њ–±–ї–µ–Љ–∞ –≤—Л–±–Њ—А–∞ –∞–љ—В–Є–±–Є–Њ—В–Є–Ї–∞ –±—Г–і–µ—В —Б—Г—Й–µ—Б—В–≤–Њ–≤–∞—В—М, –њ–Њ–Ї–∞ –њ–Њ—П–≤–ї—П—О—В—Б—П –љ–Њ–≤—Л–µ –∞–љ—В–Є–±–∞–Ї—В–µ—А–Є–∞–ї—М–љ—Л–µ –њ—А–µ–њ–∞—А–∞—В—Л –Є –њ—А–Њ–і–Њ–ї–ґ–∞–µ—В –Љ–µ–љ—П—В—М—Б—П —З—Г–≤—Б—В–≤–Є—В–µ–ї—М–љ–Њ—Б—В—М –±–∞–Ї—В–µ—А–Є–є –Ї –љ–Є–Љ. –Я—А–Є–љ–Є–Љ–∞—П —А–µ—И–µ–љ–Є–µ –Њ –≤—Л–±–Њ—А–µ –∞–љ—В–Є–±–Є–Њ—В–Є–Ї–∞, –Ї–∞–Ї –њ—А–∞–≤–Є–ї–Њ, –≤—А–∞—З –њ–Њ—Б–ї–µ–і–Њ–≤–∞—В–µ–ї—М–љ–Њ –Њ—Ж–µ–љ–Є–≤–∞–µ—В —Б–ї–µ–і—Г—О—Й–Є–µ —Д–∞–Ї—В–Њ—А—Л:
—Б–њ–µ–Ї—В—А –∞–Ї—В–Є–≤–љ–Њ—Б—В–Є;
- —Д–∞—А–Љ–∞–Ї–Њ–Ї–Є–љ–µ—В–Є—З–µ—Б–Ї–Є–µ —Е–∞—А–∞–Ї—В–µ—А–Є—Б—В–Є–Ї–Є;
- –±–µ–Ј–Њ–њ–∞—Б–љ–Њ—Б—В—М –Є –њ–µ—А–µ–љ–Њ—Б–Є–Љ–Њ—Б—В—М;
- —Б—В–Њ–Є–Љ–Њ—Б—В—М –∞–љ—В–Є–±–Є–Њ—В–Є–Ї–∞.
–Х—Б–ї–Є –Њ –њ–µ—А–≤—Л—Е —В—А–µ—Е —Д–∞–Ї—В–Њ—А–∞—Е –і–∞–љ–љ—Л—Е –≤ –Љ–µ–і–Є—Ж–Є–љ—Б–Ї–Њ–є –ї–Є—В–µ—А–∞—В—Г—А–µ –і–Њ—Б—В–∞—В–Њ—З–љ–Њ –Љ–љ–Њ–≥–Њ, —В–Њ —Н–Ї–Њ–љ–Њ–Љ–Є—З–µ—Б–Ї–Є–µ –њ–Њ–Ї–∞–Ј–∞—В–µ–ї–Є –∞–љ—В–Є–±–∞–Ї—В–µ—А–Є–∞–ї—М–љ–Њ–є —В–µ—А–∞–њ–Є–Є —Б—В–∞–ї–Є –њ—А–Є–≤–ї–µ–Ї–∞—В—М –Ї —Б–µ–±–µ –њ—А–Є—Б—В–∞–ї—М–љ–Њ–µ –≤–љ–Є–Љ–∞–љ–Є–µ –Њ—В–љ–Њ—Б–Є—В–µ–ї—М–љ–Њ –љ–µ–і–∞–≤–љ–Њ, —З—В–Њ –≤—Л–Ј–≤–∞–љ–Њ –њ–Њ—Б—В–Њ—П–љ–љ—Л–Љ —А–Њ—Б—В–Њ–Љ —А–∞—Б—Е–Њ–і–Њ–≤ –љ–∞ –Ј–і—А–∞–≤–Њ–Њ—Е—А–∞–љ–µ–љ–Є–µ, –µ–≥–Њ –љ–µ–і–Њ—Б—В–∞—В–Њ—З–љ—Л–Љ —Д–Є–љ–∞–љ—Б–Є—А–Њ–≤–∞–љ–Є–µ–Љ, —Б–∞–Љ–Њ—Б—В–Њ—П—В–µ–ї—М–љ—Л–Љ –њ–ї–∞–љ–Є—А–Њ–≤–∞–љ–Є–µ–Љ —Д–Є–љ–∞–љ—Б–Њ–≤–Њ–є –і–µ—П—В–µ–ї—М–љ–Њ—Б—В–Є –ї–µ—З–µ–±–љ—Л—Е —Г—З—А–µ–ґ–і–µ–љ–Є–є, —Г–≤–µ–ї–Є—З–µ–љ–Є–µ–Љ –Ї–Њ–ї–Є—З–µ—Б—В–≤–∞ –∞–љ—В–Є–±–Є–Њ—В–Є–Ї–Њ–≤ –љ–∞ —А—Л–љ–Ї–µ.
–Т –њ–Њ—Б–ї–µ–і–љ–µ–µ –≤—А–µ–Љ—П –Ј–∞ —А—Г–±–µ–ґ–Њ–Љ –њ—Г–±–ї–Є–Ї—Г–µ—В—Б—П –±–Њ–ї—М—И–Њ–µ –Ї–Њ–ї–Є—З–µ—Б—В–≤–Њ —Д–∞—А–Љ–∞–Ї–Њ—Н–Ї–Њ–љ–Њ–Љ–Є—З–µ—Б–Ї–Є—Е –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–є –∞–љ—В–Є–±–∞–Ї—В–µ—А–Є–∞–ї—М–љ—Л—Е –њ—А–µ–њ–∞—А–∞—В–Њ–≤. –Ю—В –Ї–ї–∞—Б—Б–Є—З–µ—Б–Ї–Є—Е –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є—Е –Є—Б–њ—Л—В–∞–љ–Є–є –Є—Е –Њ—В–ї–Є—З–∞–µ—В —В–Њ, —З—В–Њ –њ–Њ–Љ–Є–Љ–Њ –Њ—Ж–µ–љ–Ї–Є —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В–Є –Є –±–µ–Ј–Њ–њ–∞—Б–љ–Њ—Б—В–Є –њ—А–µ–њ–∞—А–∞—В–Њ–≤ –њ—А–Њ–≤–Њ–і–Є—В—Б—П –Њ—Ж–µ–љ–Ї–∞ –≤—Б–µ—Е —А–∞—Б—Е–Њ–і–Њ–≤, —Б–≤—П–Ј–∞–љ–љ—Л—Е —Б –ї–µ—З–µ–љ–Є–µ–Љ –і–∞–љ–љ–Њ–є –Є–љ—Д–µ–Ї—Ж–Є–Є, –њ—А–Є—З–µ–Љ –і–ї—П –≤—Л–±–Њ—А–∞ –Њ–њ—В–Є–Љ–∞–ї—М–љ–Њ–≥–Њ —А–µ–ґ–Є–Љ–∞ –∞–љ—В–Є–±–Є–Њ—В–Є–Ї–Њ—В–µ—А–∞–њ–Є–Є —Н—В–Є –њ–Њ–Ї–∞–Ј–∞—В–µ–ї–Є —А–∞—Б—Б–Љ–∞—В—А–Є–≤–∞—О—В—Б—П –≤ –љ–µ—А–∞–Ј—А—Л–≤–љ–Њ–є —Б–≤—П–Ј–Є –і—А—Г–≥ —Б –і—А—Г–≥–Њ–Љ.
–Ю–±—Й–µ–њ—А–Є–љ—П—В—Л–Љ –њ—А–Є –њ—А–Њ–≤–µ–і–µ–љ–Є–Є —Д–∞—А–Љ–∞–Ї–Њ—Н–Ї–Њ–љ–Њ–Љ–Є—З–µ—Б–Ї–Є—Е –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–є —Б—З–Є—В–∞–µ—В—Б—П —Г—З–µ—В —В—А–µ—Е –Њ—Б–љ–Њ–≤–љ—Л—Е —Б–Њ—Б—В–∞–≤–ї—П—О—Й–Є—Е —Б—В–Њ–Є–Љ–Њ—Б—В–Є –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П: –њ—А—П–Љ–Њ–є (–Љ–µ–і–Є—Ж–Є–љ—Б–Ї–Њ–є), –Ї–Њ—Б–≤–µ–љ–љ–Њ–є (–Ј–∞—В—А–∞—В—Л –≤ —Б–≤—П–Ј–Є —Б –≤—А–µ–Љ–µ–љ–љ–Њ–є –Є–ї–Є –њ–Њ—Б—В–Њ—П–љ–љ–Њ–є —Г—В—А–∞—В–Њ–є —В—А—Г–і–Њ—Б–њ–Њ—Б–Њ–±–љ–Њ—Б—В–Є) –Є —В–∞–Ї –љ–∞–Ј—Л–≤–∞–µ–Љ–Њ–є –љ–µ–Љ–∞—В–µ—А–Є–∞–ї—М–љ–Њ–є ( —Б–Њ–Њ—В–љ–Њ—Б–Є–Љ–Њ–є —Б–Њ —Б–љ–Є–ґ–µ–љ–Є–µ–Љ –Ї–∞—З–µ—Б—В–≤–∞ –ґ–Є–Ј–љ–Є) —Б—В–Њ–Є–Љ–Њ—Б—В–Є.
–Ґ–∞–±–ї–Є—Ж–∞ 1. –Ю—Б–љ–Њ–≤–љ—Л–µ –Ї–Њ–Љ–њ–Њ–љ–µ–љ—В—Л —Б—В–Њ–Є–Љ–Њ—Б—В–Є –∞–љ—В–Є–±–∞–Ї—В–µ—А–Є–∞–ї—М–љ–Њ–є —В–µ—А–∞–њ–Є–Є
| –Ч–∞–Ї—Г–њ–Њ—З–љ–∞—П —Б—В–Њ–Є–Љ–Њ—Б—В—М –∞–љ—В–Є–±–Є–Њ—В–Є–Ї–∞. –°—В–Њ–Є–Љ–Њ—Б—В—М –≤–≤–µ–і–µ–љ–Є—П: – —Б–њ–µ—Ж–Є–∞–ї—М–љ—Л–µ –Љ–µ–і–Є—Ж–Є–љ—Б–Ї–Є–µ –њ—А–Є–љ–∞–і–ї–µ–ґ–љ–Њ—Б—В–Є (—И–њ—А–Є—Ж—Л, –Є–≥–ї—Л, —Б–Є—Б—В–µ–Љ—Л –і–ї—П –≤–≤–µ–і–µ–љ–Є—П –Є–љ—Д—Г–Ј–Є–Њ–љ–љ—Л—Е —А–∞—Б—В–≤–Њ—А–Њ–≤, –њ–µ—А—З–∞—В–Ї–Є, –і–µ–Ј–Є–љ—Д–µ–Ї—В–∞–љ—В—Л –Є –і—А.); – —Б—В–µ—А–Є–ї–Є–Ј–∞—Ж–Є—П; – –Ј–∞—В—А–∞—В—Л —А–∞–±–Њ—З–µ–≥–Њ –≤—А–µ–Љ–µ–љ–Є —Б—А–µ–і–љ–µ–≥–Њ –Љ–µ–і–Є—Ж–Є–љ—Б–Ї–Њ–≥–Њ –њ–µ—А—Б–Њ–љ–∞–ї–∞; – —Г—В–Є–ї–Є–Ј–∞—Ж–Є—П —И–њ—А–Є—Ж–Њ–≤, –Є–≥–ї –Є –і—А—Г–≥–Є—Е —А–∞—Б—Е–Њ–і—Г–µ–Љ—Л—Е –Љ–∞—В–µ—А–Є–∞–ї–Њ–≤. –°—В–Њ–Є–Љ–Њ—Б—В—М –њ—А–µ–±—Л–≤–∞–љ–Є—П –њ–∞—Ж–Є–µ–љ—В–∞ –≤ —Б—В–∞—Ж–Є–Њ–љ–∞—А–µ –њ–Њ –њ–Њ–≤–Њ–і—Г –Є–љ—Д–µ–Ї—Ж–Є–Њ–љ–љ–Њ–≥–Њ –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П, –µ–≥–Њ –Њ—Б–ї–Њ–ґ–љ–µ–љ–Є–є. –°—В–Њ–Є–Љ–Њ—Б—В—М –Ї–Њ–љ—Б—Г–ї—М—В–∞—Ж–Є–є —Б–њ–µ—Ж–Є–∞–ї–Є—Б—В–Њ–≤ (—Е–Є—А—Г—А–≥, —В–µ—А–∞–њ–µ–≤—В, –≥–Є–љ–µ–Ї–Њ–ї–Њ–≥ –Є –і—А.). –°—В–Њ–Є–Љ–Њ—Б—В—М –і–Њ–њ–Њ–ї–љ–Є—В–µ–ї—М–љ–Њ–≥–Њ –ї–µ—З–µ–љ–Є—П –њ—А–Є –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Њ–є –љ–µ—Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В–Є. –°—В–Њ–Є–Љ–Њ—Б—В—М –і–Њ–њ–Њ–ї–љ–Є—В–µ–ї—М–љ–Њ–≥–Њ –ї–µ—З–µ–љ–Є—П –њ—А–Є –≤–Њ–Ј–љ–Є–Ї–љ–Њ–≤–µ–љ–Є–Є –љ–µ–ґ–µ–ї–∞—В–µ–ї—М–љ—Л—Е —А–µ–∞–Ї—Ж–Є–є. –°—В–Њ–Є–Љ–Њ—Б—В—М –ї–∞–±–Њ—А–∞—В–Њ—А–љ—Л—Е –Є –і–Є–∞–≥–љ–Њ—Б—В–Є—З–µ—Б–Ї–Є—Е –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–є: – –Љ–Є–Ї—А–Њ–±–Є–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є–µ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П (–≤—Л–і–µ–ї–µ–љ–Є–µ –Є –Є–і–µ–љ—В–Є—Д–Є–Ї–∞—Ж–Є—П –≤–Њ–Ј–±—Г–і–Є—В–µ–ї—П, –Њ–њ—А–µ–і–µ–ї–µ–љ–Є–µ —З—Г–≤—Б—В–≤–Є—В–µ–ї—М–љ–Њ—Б—В–Є –Ї –∞–љ—В–Є–±–Є–Њ—В–Є–Ї–∞–Љ) – —В–µ—А–∞–њ–µ–≤—В–Є—З–µ—Б–Ї–Є–є –ї–µ–Ї–∞—А—Б—В–≤–µ–љ–љ—Л–є –Љ–Њ–љ–Є—В–Њ—А–Є–љ–≥ (–њ—А–Є –њ—А–Є–Љ–µ–љ–µ–љ–Є–Є –∞–Љ–Є–љ–Њ–≥–ї–Є–Ї–Њ–Ј–Є–і–Њ–≤, –≤–∞–љ–Ї–Њ–Љ–Є—Ж–Є–љ–∞, —Е–ї–Њ—А–∞–Љ—Д–µ–љ–Є–Ї–Њ–ї–∞) – –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є–µ –Є –±–Є–Њ—Е–Є–Љ–Є—З–µ—Б–Ї–Є–µ –∞–љ–∞–ї–Є–Ј—Л – –Є–љ—Б—В—А—Г–Љ–µ–љ—В–∞–ї—М–љ—Л–µ –Љ–µ—В–Њ–і—Л –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П. –°—В–Њ–Є–Љ–Њ—Б—В—М –ї–µ—З–µ–љ–Є—П (–і–Њ–ї–µ—З–Є–≤–∞–љ–Є—П) –њ–∞—Ж–Є–µ–љ—В–∞ –≤ –∞–Љ–±—Г–ї–∞—В–Њ—А–љ—Л—Е —Г—Б–ї–Њ–≤–Є—П—Е. |
–Ґ–∞–±–ї–Є—Ж–∞ 2. –Я—Г—В–Є —Б–љ–Є–ґ–µ–љ–Є—П —А–∞—Б—Е–Њ–і–Њ–≤ –љ–∞ –∞–љ—В–Є–±–∞–Ї—В–µ—А–Є–∞–ї—М–љ—Г—О —В–µ—А–∞–њ–Є—О –≤ —Б—В–∞—Ж–Є–Њ–љ–∞—А–µ
| –Я–Њ–≤—Л—И–µ–љ–Є–µ –Ї–≤–∞–ї–Є—Д–Є–Ї–∞—Ж–Є–Є –≤—А–∞—З–µ–є –≤ –Њ–±–ї–∞—Б—В–Є –∞–љ—В–Є–Љ–Є–Ї—А–Њ–±–љ–Њ–є —Е–Є–Љ–Є–Њ—В–µ—А–∞–њ–Є–Є –£—З–µ—В –ї–Њ–Ї–∞–ї—М–љ–Њ–є —Б—В—А—Г–Ї—В—Г—А—Л –∞–љ—В–Є–±–Є–Њ—В–Є–Ї–Њ—А–µ–Ј–Є—Б—В–µ–љ—В–љ–Њ—Б—В–Є –£–ї—Г—З—И–µ–љ–Є–µ –Ї–∞—З–µ—Б—В–≤–∞ —А–∞–±–Њ—В—Л –ї–∞–±–Њ—А–∞—В–Њ—А–Є–Є –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Њ–є –Љ–Є–Ї—А–Њ–±–Є–Њ–ї–Њ–≥–Є–Є –Я–µ—А–Њ—А–∞–ї—М–љ–∞—П –∞–љ—В–Є–±–Є–Њ—В–Є–Ї–Њ—В–µ—А–∞–њ–Є—П –°—В—Г–њ–µ–љ—З–∞—В–∞—П —В–µ—А–∞–њ–Є—П –Ъ–Њ—А–Њ—В–Ї–Є–µ –Ї—Г—А—Б—Л –∞–љ—В–Є–±–Є–Њ—В–Є–Ї–Њ—В–µ—А–∞–њ–Є–Є –Р–љ—В–Є–±–Є–Њ—В–Є–Ї–Њ–њ—А–Њ—Д–Є–ї–∞–Ї—В–Є–Ї–∞ –≤ —Е–Є—А—Г—А–≥–Є–Є –Я—А–Є–Љ–µ–љ–µ–љ–Є–µ –≥–µ–љ–µ—А–Є–Ї–Њ–≤ –§–Њ—А–Љ—Г–ї—П—А –∞–љ—В–Є–±–Є–Њ—В–Є–Ї–Њ–≤ –°–Є—Б—В–µ–Љ–∞ "–Њ–≥—А–∞–љ–Є—З–µ–љ–Є—П" –њ—А–Є–Љ–µ–љ–µ–љ–Є—П –∞–љ—В–Є–±–Є–Њ—В–Є–Ї–Њ–≤ –Я–∞—А–µ–љ—В–µ—А–∞–ї—М–љ–∞—П –∞–љ—В–Є–±–Є–Њ—В–Є–Ї–Њ—В–µ—А–∞–њ–Є—П –≤–љ–µ —Б—В–∞—Ж–Є–Њ–љ–∞—А–∞ –Т—Л–±–Њ—А –∞–љ—В–Є–±–Є–Њ—В–Є–Ї–Њ–≤ —Б –і–ї–Є—В–µ–ї—М–љ—Л–Љ –Є–љ—В–µ—А–≤–∞–ї–Њ–Љ –і–Њ–Ј–Є—А–Њ–≤–∞–љ–Є—П –Ь–Њ–љ–Њ—В–µ—А–∞–њ–Є—П |
–°–ї–µ–і—Г–µ—В —А–∞–Ј–ї–Є—З–∞—В—М –њ–Њ–љ—П—В–Є—П —Б—В–Њ–Є–Љ–Њ—Б—В—М –∞–љ—В–Є–±–Є–Њ—В–Є–Ї–∞ –Є —Б—В–Њ–Є–Љ–Њ—Б—В—М –∞–љ—В–Є–±–∞–Ї—В–µ—А–Є–∞–ї—М–љ–Њ–є —В–µ—А–∞–њ–Є–Є. –Я–Њ–і —Б—В–Њ–Є–Љ–Њ—Б—В—М—О –∞–љ—В–Є–±–Є–Њ—В–Є–Ї–∞ –њ–Њ–і—А–∞–Ј—Г–Љ–µ–≤–∞–µ—В—Б—П –µ–≥–Њ –Ј–∞–Ї—Г–њ–Њ—З–љ–∞—П —Ж–µ–љ–∞ (—Ж–µ–љ—Л –љ–∞ –∞–љ—В–Є–±–∞–Ї—В–µ—А–Є–∞–ї—М–љ—Л–µ –њ—А–µ–њ–∞—А–∞—В—Л —Г –Њ—А–≥–∞–љ–Є–Ј–∞—Ж–Є–є –њ–Њ –Њ–њ—В–Њ–≤–Њ–є –њ—А–Њ–і–∞–ґ–µ –ї–µ–Ї–∞—А—Б—В–≤–µ–љ–љ—Л—Е –њ—А–µ–њ–∞—А–∞—В–Њ–≤, –≤ –∞–њ—В–µ–Ї–∞—Е). –Я–Њ–љ—П—В–Є–µ "—Б—В–Њ–Є–Љ–Њ—Б—В—М –∞–љ—В–Є–±–∞–Ї—В–µ—А–Є–∞–ї—М–љ–Њ–є —В–µ—А–∞–њ–Є–Є" –≥–Њ—А–∞–Ј–і–Њ —И–Є—А–µ, –Њ–љ–Њ –≤–Ї–ї—О—З–∞–µ—В –≤ —Б–µ–±—П –љ–µ—Б–Ї–Њ–ї—М–Ї–Њ —Б—В–Њ–Є–Љ–Њ—Б—В–µ–є: —Б–∞–Љ–Њ–≥–Њ –∞–љ—В–Є–±–Є–Њ—В–Є–Ї–∞, –µ–≥–Њ –≤–≤–µ–і–µ–љ–Є—П, –і–Њ–њ–Њ–ї–љ–Є—В–µ–ї—М–љ–Њ–≥–Њ –∞–љ—В–Є–±–∞–Ї—В–µ—А–Є–∞–ї—М–љ–Њ–≥–Њ –ї–µ—З–µ–љ–Є—П –њ—А–Є –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Њ–є –љ–µ—Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В–Є –Є/–Є–ї–Є —А–∞–Ј–≤–Є—В–Є–Є –љ–µ–ґ–µ–ї–∞—В–µ–ї—М–љ—Л—Е —А–µ–∞–Ї—Ж–Є–є, –њ—А–µ–±—Л–≤–∞–љ–Є—П –њ–∞—Ж–Є–µ–љ—В–∞ –≤ —Б—В–∞—Ж–Є–Њ–љ–∞—А–µ –Є —В. –і. (—В–∞–±–ї. 1).
–§–∞—А–Љ–∞–Ї–Њ—Н–Ї–Њ–љ–Њ–Љ–Є—З–µ—Б–Ї–Є–µ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П —П–≤–ї—П—О—В—Б—П –Њ–±—И–Є—А–љ—Л–Љ –њ–Њ–ї–µ–Љ –і–µ—П—В–µ–ї—М–љ–Њ—Б—В–Є, –њ–Њ—Б–Ї–Њ–ї—М–Ї—Г —А–∞—Б—Е–Њ–і—Л —Б—В–∞—Ж–Є–Њ–љ–∞—А–Њ–≤ –љ–∞ –ї–µ–Ї–∞—А—Б—В–≤–µ–љ–љ—Л–µ —Б—А–µ–і—Б—В–≤–∞ –≤ —Б—А–µ–і–љ–µ–Љ —Б–Њ—Б—В–∞–≤–ї—П—О—В 15 – 20% –Њ—В –Є—Е –±—О–і–ґ–µ—В–∞, –њ—А–Є—З–µ–Љ –љ–∞ –і–Њ–ї—О –∞–љ—В–Є–Є–љ—Д–µ–Ї—Ж–Є–Њ–љ–љ—Л—Е –њ—А–µ–њ–∞—А–∞—В–Њ–≤ –њ—А–Є—Е–Њ–і–Є—В—Б—П 50 – 60% [1, 2]. –°—Г—Й–µ—Б—В–≤—Г–µ—В —А—П–і —А–µ—И–µ–љ–Є–є, –њ–Њ–Ј–≤–Њ–ї—П—О—Й–Є—Е —Б–Њ–Ї—А–∞—В–Є—В—М –Ј–∞—В—А–∞—В—Л –љ–∞ –њ—А–Њ–≤–µ–і–µ–љ–Є–µ –∞–љ—В–Є–±–∞–Ї—В–µ—А–Є–∞–ї—М–љ–Њ–є —В–µ—А–∞–њ–Є–Є –≤ —Б—В–∞—Ж–Є–Њ–љ–∞—А–µ –њ—А–Є —Б–Њ—Е—А–∞–љ–µ–љ–Є–Є –≤—Л—Б–Њ–Ї–Њ–є –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Њ–є —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В–Є (—В–∞–±–ї. 2).
–Я–Њ–≤—Л—И–µ–љ–Є–µ –Ї–≤–∞–ї–Є—Д–Є–Ї–∞—Ж–Є–Є –≤—А–∞—З–µ–є –≤ –Њ–±–ї–∞—Б—В–Є –∞–љ—В–Є–Љ–Є–Ї—А–Њ–±–љ–Њ–є —Е–Є–Љ–Є–Њ—В–µ—А–∞–њ–Є–Є, —Г—З–µ—В –ї–Њ–Ї–∞–ї—М–љ–Њ–є —Б—В—А—Г–Ї—В—Г—А—Л –∞–љ—В–Є–±–Є–Њ—В–Є–Ї–Њ—А–µ–Ј–Є—Б—В–µ–љ—В–љ–Њ—Б—В–Є, —Г–ї—Г—З—И–µ–љ–Є–µ –Ї–∞—З–µ—Б—В–≤–∞ —А–∞–±–Њ—В—Л –ї–∞–±–Њ—А–∞—В–Њ—А–Є–Є –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Њ–є –Љ–Є–Ї—А–Њ–±–Є–Њ–ї–Њ–≥–Є–Є
–Ь—Л —Б–Њ–Ј–љ–∞—В–µ–ї—М–љ–Њ –Њ–±—К–µ–і–Є–љ–Є–ї–Є —В—А–Є —Н—В–Є –њ–Њ–і—Е–Њ–і–∞ –Ї —Б–љ–Є–ґ–µ–љ–Є—О –Ј–∞—В—А–∞—В –њ—А–Є –њ—А–Њ–≤–µ–і–µ–љ–Є–Є –∞–љ—В–Є–±–∞–Ї—В–µ—А–Є–∞–ї—М–љ–Њ–є —В–µ—А–∞–њ–Є–Є –≤ —Б—В–∞—Ж–Є–Њ–љ–∞—А–µ, —В–∞–Ї –Ї–∞–Ї –Њ–љ–Є –љ–∞—Е–Њ–і—П—В—Б—П –≤ –љ–µ—А–∞–Ј—А—Л–≤–љ–Њ–є —Б–≤—П–Ј–Є –і—А—Г–≥ —Б –і—А—Г–≥–Њ–Љ.
–Э–∞–Ј–љ–∞—З–µ–љ–Є–µ –∞–љ—В–Є–±–Є–Њ—В–Є–Ї–Њ–≤ –љ–µ –њ–Њ –њ–Њ–Ї–∞–Ј–∞–љ–Є—П–Љ –Љ–Њ–ґ–љ–Њ –Њ–±—К—П—Б–љ–Є—В—М –њ–Њ –Ї—А–∞–є–љ–µ–є –Љ–µ—А–µ —В—А–µ–Љ—П –њ—А–Є—З–Є–љ–∞–Љ–Є [3]:
- –≤–ї–Є—П–љ–Є–µ–Љ —А–µ–Ї–ї–∞–Љ–љ–Њ–є –Ї–∞–Љ–њ–∞–љ–Є–Є —Д–∞—А–Љ–∞—Ж–µ–≤—В–Є—З–µ—Б–Ї–Є—Е —Д–Є—А–Љ;
- –љ–µ–і–Њ—Б—В–∞—В–Њ—З–љ–Њ–є –њ–Њ–і–≥–Њ—В–Њ–≤–Ї–Њ–є –≤—А–∞—З–∞ –≤ –Њ–±–ї–∞—Б—В–Є —Е–Є–Љ–Є–Њ—В–µ—А–∞–њ–Є–Є;
- —З—А–µ–Ј–Љ–µ—А–љ—Л–Љ–Є —В—А–µ–±–Њ–≤–∞–љ–Є—П–Љ–Є –њ–∞—Ж–Є–µ–љ—В–∞ –Ї –њ—А–Њ–≤–Њ–і–Є–Љ–Њ–Љ—Г –ї–µ—З–µ–љ–Є—О.
–Э–∞ –њ–µ—А–≤–Њ–µ –Љ–µ—Б—В–Њ —Б–ї–µ–і—Г–µ—В –њ–Њ—Б—В–∞–≤–Є—В—М –≤—В–Њ—А–Њ–є —Д–∞–Ї—В–Њ—А, —В–∞–Ї –Ї–∞–Ї –≤—А–∞—З—Г, –Њ–±–ї–∞–і–∞—О—Й–µ–Љ—Г —Б–Њ–≤—А–µ–Љ–µ–љ–љ—Л–Љ–Є –Ј–љ–∞–љ–Є—П–Љ–Є –≤ –Њ–±–ї–∞—Б—В–Є –∞–љ—В–Є–Љ–Є–Ї—А–Њ–±–љ–Њ–є —Е–Є–Љ–Є–Њ—В–µ—А–∞–њ–Є–Є –Є –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Њ–є –Љ–Є–Ї—А–Њ–±–Є–Њ–ї–Њ–≥–Є–Є, –≥–Њ—А–∞–Ј–і–Њ –ї–µ–≥—З–µ –њ—А–Њ—В–Є–≤–Њ—Б—В–Њ—П—В—М –і–∞–≤–ї–µ–љ–Є—О –Ї–∞–Ї —А–µ–Ї–ї–∞–Љ—Л, —В–∞–Ї –Є –њ–∞—Ж–Є–µ–љ—В–Њ–≤.
–Ч–љ–∞–љ–Є–µ —Н–њ–Є–і–µ–Љ–Є–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Њ–є —Б–Є—В—Г–∞—Ж–Є–Є –≤ —Б—В–∞—Ж–Є–Њ–љ–∞—А–µ –њ–Њ–Љ–Њ–≥–∞–µ—В —А–∞–Ј—Г–Љ–љ–Њ –њ–Њ–і–Њ–є—В–Є –Ї –њ—А–Є–Љ–µ–љ–µ–љ–Є—О –∞–љ—В–Є–±–∞–Ї—В–µ—А–Є–∞–ї—М–љ–Њ–є —В–µ—А–∞–њ–Є–Є, —З—В–Њ –њ–Њ–Ј–≤–Њ–ї—П–µ—В —Г–Љ–µ–љ—М—И–Є—В—М —Б–µ–ї–µ–Ї—Ж–Є—О —А–µ–Ј–Є—Б—В–µ–љ—В–љ—Л—Е —И—В–∞–Љ–Љ–Њ–≤, —Б–љ–Є–Ј–Є—В—М —З–Є—Б–ї–Њ —Б–ї—Г—З–∞–µ–≤ –љ–µ–Њ–њ—А–∞–≤–і–∞–љ–љ–Њ–≥–Њ –љ–∞–Ј–љ–∞—З–µ–љ–Є—П –∞–љ—В–Є–±–Є–Њ—В–Є–Ї–Њ–≤ –Є —А–∞—Б—Е–Њ–і—Л –љ–∞ –љ–Є—Е, –њ–Њ–≤—Л—Б–Є—В—М –Ї–Њ–љ—В—А–Њ–ї—М –Ј–∞ –њ—А–Є–Љ–µ–љ–µ–љ–Є–µ–Љ –∞–љ—В–Є–±–Є–Њ—В–Є–Ї–Њ–≤.
–Ґ–∞–±–ї–Є—Ж–∞ 3. –°—В–Њ–Є–Љ–Њ—Б—В—М –Њ—В–і–µ–ї—М–љ—Л—Е –∞–љ—В–Є–±–Є–Њ—В–Є–Ї–Њ–≤, –Є—Б–њ–Њ–ї—М–Ј—Г–µ–Љ—Л—Е –њ—А–Є –њ—А–Њ–≤–µ–і–µ–љ–Є–Є —Б—В—Г–њ–µ–љ—З–∞—В–Њ–є —В–µ—А–∞–њ–Є–Є [4]
|
–Р–љ—В–Є–±–Є–Њ—В–Є–Ї |
–†–∞–Ј–Њ–≤–∞—П –і–Њ–Ј–∞, –Љ–≥ |
–Ч–∞–Ї—Г–њ–Њ—З–љ–∞—П —Б—В–Њ–Є–Љ–Њ—Б—В—М, $ |
* |
| –Р–Љ–њ–Є—Ж–Є–ї–ї–Є–љ –љ–∞—В—А–Є—П (–†–Њ—Б—Б–Є—П) | 500 (–≤/–≤, –≤/–Љ) | 0,20 | + 39 |
| –Р–Љ–њ–Є—Ж–Є–ї–ї–Є–љ —В—А–Є–≥–Є–і—А–∞—В (–†–Њ—Б—Б–Є—П) | 500 (–≤–љ—Г—В—А—М) | 0,17 | |
| –¶–µ—Д—Г—А–Њ–Ї—Б–Є–Љ –љ–∞—В—А–Є—П (GW) | 750 (–≤/–≤, –≤/–Љ) | 3,12 | + 28 |
| –¶–µ—Д—Г—А–Њ–Ї—Б–Є–Љ –∞–Ї—Б–µ—В–Є–ї (GW) |
500 (–≤–љ—Г—В—А—М) |
2,26 |
|
| –¶–Є–њ—А–Њ—Д–ї–Њ–Ї—Б–∞—Ж–Є–љ (KRKA) |
400 (–≤/–≤) |
2,44 |
+ 78 |
|
500 (–≤–љ—Г—В—А—М) |
0,54 |
||
| –Ъ–ї–Є–љ–і–∞–Љ–Є—Ж–Є–љ–∞ —Д–Њ—Б—Д–∞—В (Upjohn) |
600 (–≤/–≤, –≤/–Љ) |
8,62 |
+ 86 |
| –Ъ–ї–Є–љ–і–∞–Љ–Є—Ж–Є–љ–∞ –≥–Є–і—А–Њ—Е–ї–Њ—А–Є–і (Upjohn) |
600 (–≤–љ—Г—В—А—М) |
1,24 |
|
| –Ь–µ—В—А–Њ–љ–Є–і–∞–Ј–Њ–ї (RPR) |
500 (–≤/–≤) |
3,95 |
+ 95 |
|
500 (–≤–љ—Г—В—А—М) |
0,18 |
||
| –°—Г–ї—М—Д–∞–Љ–µ—В–Њ–Ї—Б–∞–Ј–Њ–ї |
800/160 (–≤/–≤) |
1,97 |
+ 95 |
| –Ґ—А–Є–Љ–µ—В–Њ–њ—А–Є–Љ (Polfa) |
800/160 (–≤–љ—Г—В—А—М) |
0,1 |
|
| –§–ї—Г–Ї–Њ–љ–∞–Ј–Њ–ї (Pfizer) |
100 (–≤/–≤) |
15,99 |
+ 55 |
|
100 (–≤–љ—Г—В—А—М) |
7,22 |
||
|
*–†–∞–Ј–љ–Є—Ж–∞ –≤ —Б—В–Њ–Є–Љ–Њ—Б—В–Є –њ–∞—А–µ–љ—В–µ—А–∞–ї—М–љ—Л—Е –Є –Њ—А–∞–ї—М–љ—Л—Е –њ—А–µ–њ–∞—А–∞—В–Њ–≤ –Ј–∞ —А–∞–Ј–Њ–≤—Г—О –і–Њ–Ј—Г. |
|||
–Ч–љ–∞–љ–Є–µ —Н–њ–Є–і–µ–Љ–Є–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Њ–є —Б–Є—В—Г–∞—Ж–Є–Є –≤ —Б—В–∞—Ж–Є–Њ–љ–∞—А–µ –љ–µ–≤–Њ–Ј–Љ–Њ–ґ–љ–Њ –±–µ–Ј –Ї–∞—З–µ—Б—В–≤–µ–љ–љ–Њ–є —А–∞–±–Њ—В—Л –ї–∞–±–Њ—А–∞—В–Њ—А–Є–Є –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Њ–є –Љ–Є–Ї—А–Њ–±–Є–Њ–ї–Њ–≥–Є–Є. –І—В–Њ–±—Л —А–µ–Ј—Г–ї—М—В–∞—В—Л –Љ–Є–Ї—А–Њ–±–Є–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є—Е –∞–љ–∞–ї–Є–Ј–Њ–≤ –±—Л–ї–Є –і–Њ—Б—В–Њ–≤–µ—А–љ—Л–Љ–Є, –љ–µ–Њ–±—Е–Њ–і–Є–Љ–Њ –њ—А–Є–Љ–µ–љ—П—В—М –Љ–Є–Ї—А–Њ–±–Є–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є–µ –Љ–∞—В–µ—А–Є–∞–ї—Л –≤—Л—Б–Њ–Ї–Њ–≥–Њ –Ї–∞—З–µ—Б—В–≤–∞, —Б—В–∞–љ–і–∞—А—В–Є–Ј–Є—А–Њ–≤–∞—В—М –Љ–µ—В–Њ–і—Л –∞–љ–∞–ї–Є–Ј–∞ –≤ —Б–Њ–Њ—В–≤–µ—В—Б—В–≤–Є–Є —Б –Љ–µ–ґ–і—Г–љ–∞—А–Њ–і–љ—Л–Љ–Є —В—А–µ–±–Њ–≤–∞–љ–Є—П–Љ–Є, –њ—А–Њ–≤–Њ–і–Є—В—М –≤–љ—Г—В—А–µ–љ–љ–Є–є –Є –≤–љ–µ—И–љ–Є–є –Ї–Њ–љ—В—А–Њ–ї—М –Ї–∞—З–µ—Б—В–≤–∞.
–Я–µ—А–Њ—А–∞–ї—М–љ–∞—П –∞–љ—В–Є–±–Є–Њ—В–Є–Ї–Њ—В–µ—А–∞–њ–Є—П
–С–Њ–ї—М—И–Є–љ—Б—В–≤–Њ —Б–Њ–≤—А–µ–Љ–µ–љ–љ—Л—Е –њ–µ—А–Њ—А–∞–ї—М–љ—Л—Е –∞–љ—В–Є–±–Є–Њ—В–Є–Ї–Њ–≤ —Е–∞—А–∞–Ї—В–µ—А–Є–Ј—Г—О—В—Б—П —И–Є—А–Њ–Ї–Є–Љ —Б–њ–µ–Ї—В—А–Њ–Љ –і–µ–є—Б—В–≤–Є—П, –≤—Л—Б–Њ–Ї–Њ–є –±–Є–Њ–і–Њ—Б—В—Г–њ–љ–Њ—Б—В—М—О, –∞ —В–∞–Ї–ґ–µ –Љ–∞–ї–Њ–є –Ї—А–∞—В–љ–Њ—Б—В—М—О –њ—А–Є–µ–Љ–∞, —З—В–Њ –њ–Њ–Ј–≤–Њ–ї—П–µ—В –Є—Е –љ–∞–Ј–љ–∞—З–∞—В—М –Є–Ј–љ–∞—З–∞–ї—М–љ–Њ –њ—А–Є –ї–µ—З–µ–љ–Є–Є —А—П–і–∞ –Є–љ—Д–µ–Ї—Ж–Є–Њ–љ–љ—Л—Е –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є–є. –°–љ–Є–ґ–µ–љ–Є–µ —А–∞—Б—Е–Њ–і–Њ–≤ –≤ —Н—В–Њ–Љ —Б–ї—Г—З–∞–µ –Њ–±—Г—Б–ї–Њ–≤–ї–µ–љ–Њ —А–∞–Ј–љ–Є—Ж–µ–є –≤ —Б—В–Њ–Є–Љ–Њ—Б—В–Є –њ–µ—А–Њ—А–∞–ї—М–љ—Л—Е –Є –њ–∞—А–µ–љ—В–µ—А–∞–ї—М–љ—Л—Е –∞–љ—В–Є–±–Є–Њ—В–Є–Ї–Њ–≤, –Ј–љ–∞—З–Є—В–µ–ї—М–љ—Л–Љ —Б–љ–Є–ґ–µ–љ–Є–µ–Љ —Б—В–Њ–Є–Љ–Њ—Б—В–Є –≤–≤–µ–і–µ–љ–Є—П –∞–љ—В–Є–±–Є–Њ—В–Є–Ї–∞, –≤–Њ–Ј–Љ–Њ–ґ–љ–Њ—Б—В—М—О —А–∞–љ–љ–µ–є –≤—Л–њ–Є—Б–Ї–Є –њ–∞—Ж–Є–µ–љ—В–∞ –Є–Ј —Б—В–∞—Ж–Є–Њ–љ–∞—А–∞, —Б–љ–Є–ґ–µ–љ–Є–µ–Љ —А–Є—Б–Ї–∞ —А–∞–Ј–≤–Є—В–Є—П –љ–Њ–Ј–Њ–Ї–Њ–Љ–Є–∞–ї—М–љ–Њ–є –Є–љ—Д–µ–Ї—Ж–Є–Є. –Ъ—А–Њ–Љ–µ —В–Њ–≥–Њ, –ї–µ—З–µ–љ–Є–µ –і–ї—П –њ–∞—Ж–Є–µ–љ—В–∞ —Б—В–∞–љ–Њ–≤–Є—В—Б—П –±–Њ–ї–µ–µ –Ї–Њ–Љ—Д–Њ—А—В–љ—Л–Љ.
–Я—А–Є–Љ–µ—А–∞–Љ–Є –і–∞–љ–љ–Њ–≥–Њ –њ–Њ–і—Е–Њ–і–∞ –Љ–Њ–≥—Г—В —П–≤–ї—П—В—М—Б—П –њ—А–Є–Љ–µ–љ–µ–љ–Є–µ –Ї–Њ–∞–Љ–Њ–Ї—Б–Є–Ї–ї–∞–≤–∞, —Ж–µ—Д—Г—А–Њ–Ї—Б–Є–Љ–∞ –∞–Ї—Б–µ—В–Є–ї–∞ –њ—А–Є –Є–љ—Д–µ–Ї—Ж–Є—П—Е –і—Л—Е–∞—В–µ–ї—М–љ—Л—Е –њ—Г—В–µ–є, —Д—В–Њ—А—Е–Є–љ–Њ–ї–Њ–љ–Њ–≤ –њ—А–Є –Є–љ—Д–µ–Ї—Ж–Є—П—Е –Љ–Њ—З–µ–≤—Л–≤–Њ–і—П—Й–Є—Е –њ—Г—В–µ–є, –Љ–∞–Ї—А–Њ–ї–Є–і–Њ–≤, —Ж–µ—Д—Г—А–Њ–Ї—Б–Є–Љ–∞ –∞–Ї—Б–µ—В–Є–ї–∞, –Ї–Њ–∞–Љ–Њ–Ї—Б–Є–Ї–ї–∞–≤–∞ –њ—А–Є –Є–љ—Д–µ–Ї—Ж–Є—П—Е –Ы–Ю–†-–Њ—А–≥–∞–љ–Њ–≤.
–°—В—Г–њ–µ–љ—З–∞—В–∞—П —В–µ—А–∞–њ–Є—П
–°—В—Г–њ–µ–љ—З–∞—В–∞—П —В–µ—А–∞–њ–Є—П – –і–≤—Г—Е—Н—В–∞–њ–љ–Њ–µ –њ—А–Є–Љ–µ–љ–µ–љ–Є–µ –∞–љ—В–Є–Љ–Є–Ї—А–Њ–±–љ—Л—Е –њ—А–µ–њ–∞—А–∞—В–Њ–≤ —Б –њ–µ—А–µ—Е–Њ–і–Њ–Љ –Њ—В –њ–∞—А–µ–љ—В–µ—А–∞–ї—М–љ–Њ–≥–Њ –љ–∞ –љ–µ–њ–∞—А–µ–љ—В–µ—А–∞–ї—М–љ—Л–є (–Ї–∞–Ї –њ—А–∞–≤–Є–ї–Њ, –њ–µ—А–Њ—А–∞–ї—М–љ—Л–є) –њ—Г—В—М –≤–≤–µ–і–µ–љ–Є—П –≤ –≤–Њ–Ј–Љ–Њ–ґ–љ–Њ –Ї–Њ—А–Њ—В–Ї–Є–µ —Б—А–Њ–Ї–Є, –Њ–њ—А–µ–і–µ–ї—П–µ–Љ—Л–µ –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є–Љ —Б–Њ—Б—В–Њ—П–љ–Є–µ–Љ –њ–∞—Ж–Є–µ–љ—В–∞.
–Ґ–∞–±–ї–Є—Ж–∞ 4. –°—А–∞–≤–љ–Є—В–µ–ї—М–љ–∞—П —Б—В–Њ–Є–Љ–Њ—Б—В—М —Г–њ–∞–Ї–Њ–≤–Ї–Є (10 —В–∞–±–ї–µ—В–Њ–Ї –њ–Њ 250 –Љ–≥) –Є–љ–љ–Њ–≤–∞—Ж–Є–Њ–љ–љ–Њ–≥–Њ —Ж–Є–њ—А–Њ—Д–ї–Њ–Ї—Б–∞—Ж–Є–љ–∞ (—Ж–Є–њ—А–Њ–±–∞–є) –Є –µ–≥–Њ –≥–µ–љ–µ—А–Є–Ї–Њ–≤ [4]
| –Р–љ—В–Є–±–Є–Њ—В–Є–Ї, —Д–Є—А–Љ–∞, —Б—В—А–∞–љ–∞ | –Ч–∞–Ї—Г–њ–Њ—З–љ–∞—П —Б—В–Њ–Є–Љ–Њ—Б—В—М, $ |
| –¶–Є–њ—А–Њ–±–∞–є, –Т–∞—Г–µr, –У–µ—А–Љ–∞–љ–Є—П |
10,06 |
| –¶–Є–њ—А–Њ—Ж–Є–љ–∞–ї, Zdravle, –Ѓ–≥–Њ—Б–ї–∞–≤–Є—П |
4,00 |
| –¶–Є–њ—А–Є–љ–Њ–ї, KRKA, –°–ї–Њ–≤–µ–љ–Є—П |
2,72 |
| –¶–Є–њ—А–Њ–ї–µ—В, Dr. Reddy`s Laboratories, –Ш–љ–і–Є—П |
2,31 |
| –Ъ–≤–Є–љ—В–Њ—А, Torrent, –Ш–љ–і–Є—П |
1,70 |
–Ю—Б–љ–Њ–≤–љ–∞—П –Є–і–µ—П —Б—В—Г–њ–µ–љ—З–∞—В–Њ–є —В–µ—А–∞–њ–Є–Є –Ј–∞–Ї–ї—О—З–∞–µ—В—Б—П –≤ —В–Њ–Љ, —З—В–Њ, –µ—Б–ї–Є –њ–∞—Ж–Є–µ–љ—В–∞ –Љ–Њ–ґ–љ–Њ —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ –ї–µ—З–Є—В—М –Ї–Њ—А–Њ—В–Ї–Є–Љ –Ї—Г—А—Б–Њ–Љ –њ–∞—А–µ–љ—В–µ—А–∞–ї—М–љ–Њ–≥–Њ –∞–љ—В–Є–Љ–Є–Ї—А–Њ–±–љ–Њ–≥–Њ –њ—А–µ–њ–∞—А–∞—В–∞ —Б –њ–Њ—Б–ї–µ–і—Г—О—Й–Є–Љ –њ–µ—А–µ–≤–Њ–і–Њ–Љ –љ–∞ –њ–µ—А–Њ—А–∞–ї—М–љ—Л–є –њ—А–Є–µ–Љ, —В–Њ —Н—В–Њ –Љ–Њ–ґ–µ—В –Ј–љ–∞—З–Є—В–µ–ї—М–љ–Њ —Г–Љ–µ–љ—М—И–Є—В—М —Б—В–Њ–Є–Љ–Њ—Б—В—М –ї–µ—З–µ–љ–Є—П, —Б–Њ–Ї—А–∞—В–Є—В—М —Б—А–Њ–Ї –њ—А–µ–±—Л–≤–∞–љ–Є—П –њ–∞—Ж–Є–µ–љ—В–∞ –≤ —Б—В–∞—Ж–Є–Њ–љ–∞—А–µ –њ—А–Є –≤—Л—Б–Њ–Ї–Њ–є –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Њ–є —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В–Є —В–µ—А–∞–њ–Є–Є. –Э–∞–Ї–Њ–њ–ї–µ–љ –Њ–њ—Л—В –њ—А–Є–Љ–µ–љ–µ–љ–Є—П —Б—В—Г–њ–µ–љ—З–∞—В–Њ–є —В–µ—А–∞–њ–Є–Є –њ—А–Є –≥–Њ—Б–њ–Є—В–∞–ї—М–љ–Њ–є –њ–љ–µ–≤–Љ–Њ–љ–Є–Є, –Є–љ—Д–µ–Ї—Ж–Є–Є —Г—А–Њ–≥–µ–љ–Є—В–∞–ї—М–љ–Њ–≥–Њ —В—А–∞–Ї—В–∞, —Б–µ–њ—В–Є—Ж–µ–Љ–Є–Є, –Є–љ—Д–µ–Ї—Ж–Є–Є –Ї–Њ–ґ–Є –Є –Љ—П–≥–Ї–Є—Е —В–Ї–∞–љ–µ–є, –Є–љ—В—А–∞–∞–±–і–Њ–Љ–Є–љ–∞–ї—М–љ–Њ–є –Є–љ—Д–µ–Ї—Ж–Є–Є [1, 2].
–Ґ–∞–±–ї–Є—Ж–∞ 5. –Ъ—А–Є—В–µ—А–Є–Є –і–ї—П –њ—А–Њ–≤–µ–і–µ–љ–Є—П –њ–∞—А–µ–љ—В–µ—А–∞–ї—М–љ–Њ–є –∞–љ—В–±–Є–Њ—В–Є–Ї–Њ—В–µ—А–∞–њ–Є–Є –љ–∞ –і–Њ–Љ—Г [22]
| –Я–∞—Ж–Є–µ–љ—В
– —Б–Њ–≥–ї–∞—Б–Є–µ –њ–∞—Ж–Є–µ–љ—В–∞ –Ч–∞–±–Њ–ї–µ–≤–∞–љ–Є–µ – —Б—В–∞–±–Є–ї–Є–Ј–∞—Ж–Є—П –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Њ–≥–Њ —Б–Њ—Б—В–Њ—П–љ–Є—П –Ґ–µ—А–∞–њ–Є—П – –≤–Њ–Ј–Љ–Њ–ґ–љ–Њ—Б—В—М —Г—Б—В–∞–љ–Њ–≤–Є—В—М —Б–Є—Б—В–µ–Љ—Г –і–ї—П |
–°—В—Г–њ–µ–љ—З–∞—В–∞—П —В–µ—А–∞–њ–Є—П –Є–Љ–µ–µ—В –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є–µ –Є —Н–Ї–Њ–љ–Њ–Љ–Є—З–µ—Б–Ї–Є–µ –њ—А–µ–Є–Љ—Г—Й–µ—Б—В–≤–∞ –Ї–∞–Ї –і–ї—П –њ–∞—Ж–Є–µ–љ—В–∞, —В–∞–Ї –Є –і–ї—П –ї–µ—З–µ–±–љ–Њ–≥–Њ —Г—З—А–µ–ґ–і–µ–љ–Є—П. –Я—А–µ–Є–Љ—Г—Й–µ—Б—В–≤–∞ –і–ї—П –њ–∞—Ж–Є–µ–љ—В–∞ –Ј–∞–Ї–ї—О—З–∞—О—В—Б—П, –≤–Њ-–њ–µ—А–≤—Л—Е, –≤ —Г–Љ–µ–љ—М—И–µ–љ–Є–Є –Ї–Њ–ї–Є—З–µ—Б—В–≤–∞ –Є–љ—К–µ–Ї—Ж–Є–є, —З—В–Њ –і–µ–ї–∞–µ—В –ї–µ—З–µ–љ–Є–µ –±–Њ–ї–µ–µ –Ї–Њ–Љ—Д–Њ—А—В–љ—Л–Љ –Є —Б–љ–Є–ґ–∞–µ—В —А–Є—Б–Ї –≤–Њ–Ј–љ–Є–Ї–љ–Њ–≤–µ–љ–Є—П –њ–Њ—Б—В–Є–љ—К–µ–Ї—Ж–Є–Њ–љ–љ—Л—Е –Њ—Б–ї–Њ–ґ–љ–µ–љ–Є–є (—Д–ї–µ–±–Є—В—Л, –њ–Њ—Б—В–Є–љ—К–µ–Ї—Ж–Є–Њ–љ—Л–µ –∞–±—Б—Ж–µ—Б—Б—Л, –Ї–∞—В–µ—В–µ—А-–∞—Б—Б–Њ—Ж–Є–Є—А–Њ–≤–∞–љ–љ—Л–µ –Є–љ—Д–µ–Ї—Ж–Є–Є). –Т–Њ-–≤—В–Њ—А—Л—Е, –њ—А–Є –њ–Њ–ї–Њ–ґ–Є—В–µ–ї—М–љ–Њ–є –і–Є–љ–∞–Љ–Є–Ї–µ –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П –Є –Њ—В—Б—Г—В—Б—В–≤–Є–Є –њ–Њ–Ї–∞–Ј–∞–љ–Є–є –і–ї—П –њ—А–µ–±—Л–≤–∞–љ–Є—П –њ–∞—Ж–Є–µ–љ—В–∞ –≤ —Б—В–∞—Ж–Є–Њ–љ–∞—А–µ –Њ–љ –Љ–Њ–ґ–µ—В –±—Л—В—М –≤—Л–њ–Є—Б–∞–љ —А–∞–љ—М—И–µ –Є –њ—А–Њ–і–Њ–ї–ґ–∞—В—М –ї–µ—З–µ–љ–Є–µ –≤ –і–Њ–Љ–∞—И–љ–Є—Е —Г—Б–ї–Њ–≤–Є—П—Е, —З—В–Њ –±—Г–і–µ—В –±–ї–∞–≥–Њ–њ—А–Є—П—В–љ–Њ —Б–Ї–∞–Ј—Л–≤–∞—В—М—Б—П –љ–∞ –µ–≥–Њ –њ—Б–Є—Е–Њ—Н–Љ–Њ—Ж–Є–Њ–љ–∞–ї—М–љ–Њ–Љ —Б–Њ—Б—В–Њ—П–љ–Є–Є, –∞ —В–∞–Ї–ґ–µ –њ–Њ–Ј–≤–Њ–ї–Є—В —Б–љ–Є–Ј–Є—В—М —А–Є—Б–Ї –љ–Њ–Ј–Њ–Ї–Њ–Љ–Є–∞–ї—М–љ–Њ–є –Є–љ—Д–µ–Ї—Ж–Є–Є.
–Ґ–∞–±–ї–Є—Ж–∞ 6. –Ъ–ї–Є–љ–Є—З–µ—Б–Ї–∞—П —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В—М (–Ъ–≠) –Є–Љ–Є–њ–µ–љ–µ–Љ–∞ –њ–Њ —Б—А–∞–≤–љ–µ–љ–Є—О —Б –Ї–Њ–Љ–±–Є–љ–Є—А–Њ–≤–∞–љ–љ–Њ–є —В–µ—А–∞–њ–Є–µ–є –њ—А–Є –љ–µ–є—В—А–Њ–њ–µ–љ–Є—З–µ—Б–Ї–Њ–є –ї–Є—Е–Њ—А–∞–і–Ї–µ –≤ —Б—А–∞–≤–љ–Є—В–µ–ї—М–љ—Л—Е —А–∞–љ–і–Њ–Љ–Є–Ј–Є—А–Њ–≤–∞–љ–љ—Л—Е –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П—Е [24]
|
–Ъ–≠ |
–Я—А–µ–њ–µ—А–∞—В —Б—А–∞–≤–љ–µ–љ–Є—П –Я–°,% |
–Ъ–≠(–Я–°) |
|
91 |
–У–µ–љ—В–∞–Љ–Є—Ж–Є–љ+—Ж–µ—Д—Г—А–Њ–Ї—Б–Є–Љ (–Є–ї–Є —Ж–µ—Д–∞–ї–Њ—В–Є–љ) |
74 |
|
79 |
–Р–Љ–Є–Ї–∞—Ж–Є–љ+–њ–Є–њ–µ—А–∞–ї–Є–ї–ї–Є–љ |
69 |
|
82 |
–¶—Н—Д—В–∞–Ј–Є–і–Є–Љ+–≤–∞–љ–Ї–Њ–Љ–Є—Ж–Є–љ |
59 |
|
88 |
–Ґ–Њ–±—А–∞–Љ–Є—Ж–Є–љ+–њ–Є–њ–µ—А–∞—Ж–Є–ї–ї–Є–љ |
87 |
|
82 |
–Ы–∞—В–∞–Љ–Њ–Ї—Б–µ—Д+—В–Њ–±—А–∞–Љ–Є—Ж–Є–љ |
80 |
|
93 |
–¶–µ—Д–Њ–њ–µ—А–∞–Ј–Њ–љ+–Љ–µ–Ј–ї–Њ—Ж–Є–ї–ї–Є–љ |
95 |
|
72 |
–¶–µ—Д—В–∞–Ј–Є–і–Є–Љ+–∞–Љ–Є–Ї–∞—Ж–Є–љ |
71 |
–Ґ–∞–±–ї–Є—Ж–∞ 7. –Ъ–ї–Є–љ–Є—З–µ—Б–Ї–∞—П (–Ъ–≠) —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В—М –Є–Љ–Є–њ–µ–љ–µ–Љ–∞ –њ–Њ —Б—А–∞–≤–љ–µ–љ–Є—О —Б –Ї–Њ–Љ–±–Є–љ–Є—А–Њ–≤–∞–љ–љ–Њ–є —В–µ—А–∞–њ–Є–µ–є –њ—А–Є –ї–µ—З–µ–љ–Є–Є –Є–љ—В—А–∞–∞–±–і–Њ–Љ–Є–љ–∞–ї—М–љ—Л—Е –Є–љ—Д–µ–Ї—Ж–Є–є –≤ —Б—А–∞–≤–љ–Є—В–µ–ї—М–љ—Л—Е, —А–∞–љ–і–Њ–Љ–Є–Ј–Є—А–Њ–≤–∞–љ–љ—Л—Е –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П—Е [24]
|
–Ъ–≠ |
–Я—А–µ–њ–µ—А–∞—В —Б—А–∞–≤–љ–µ–љ–Є—П –Я–°,% |
–Ъ–≠(–Я–°) |
|
100 |
–¶–µ—Д—В–∞–Ј–Є–і–Є–Љ,—Ж–µ—Д—В–∞–Ј–Є–і–Є–Љ+–Љ–µ—В—А–Њ–љ–Є–і–∞–Ј–Њ–ї |
84 |
|
79 |
–Ґ–Њ–Љ–±—А–∞–Љ–Є—Ж–Є–љ+–Ї–ї–Є–љ–і–∞–Љ–Є—Ж–Є–љ/–Љ–µ—В—А–Њ–љ–Є–і–∞–Ј–Њ–ї |
67 |
|
83 |
–Ґ–Њ–±—А–∞–Љ–Є—Ж–Є–љ+–Ї–ї–Є–љ–і–∞–Љ–Є—Ж–Є–љ ± –≤–∞–љ–Ї–Њ–Љ–Є—Ж–Є–љ |
70 |
|
94 |
–Ъ–ї–Є–љ–і–∞–Љ–Є—Ж–Є–љ + –љ–µ—В–Є–ї–Љ–Є—Ж–Є–љ |
89 |
|
100 |
–Ь–µ—А–Њ–њ–µ–љ–µ–Љ |
100 |
|
97 |
–Ъ–ї–Є–љ–і–∞–Љ–Є—Ж–Є–љ + –≥–µ–љ—В–∞–Љ–Є—Ж–Є–љ |
100 |
|
85 |
–Р–Љ–Њ–Ї—Б–Є—Ж–Є–ї–ї–Є–љ + –Ї–ї–Є–љ–і–∞–Љ–Є—Ж–Є–љ + –љ–µ—В–Є–ї–Љ–Є—Ж–Є–љ |
83 |
|
84 |
–Р–Љ–њ–Є—Ж–Є–ї–ї–Є–љ + –Љ–µ—В—А–Њ–і–Є–љ–∞–Ј–Њ–ї + –≥–µ–љ—В–∞–Љ–Є—Ж–Є–љ |
92 |
–Я—А–µ–Є–Љ—Г—Й–µ—Б—В–≤–∞ –і–ї—П —Б—В–∞—Ж–Є–Њ–љ–∞—А–∞, –≥–і–µ –њ—А–Њ–≤–Њ–і–Є—В—Б—П —Б—В—Г–њ–µ–љ—З–∞—В–∞—П —В–µ—А–∞–њ–Є—П, —Б–Ї–ї–∞–і85—Л–≤–∞—О—В—Б—П –Є–Ј —Б–ї–µ–і—Г—О—Й–Є—Е —Д–∞–Ї—В–Њ—А–Њ–≤:
- —Б–љ–Є–ґ–µ–љ–Є—П –Ј–∞—В—А–∞—В –≤ —Б–≤—П–Ј–Є —Б –Љ–µ–љ—М—И–µ–є —Б—В–Њ–Є–Љ–Њ—Б—В—М—О –Њ—А–∞–ї—М–љ—Л—Е –∞–љ—В–Є–±–Є–Њ—В–Є–Ї–Њ–≤ (—В–∞–±–ї. 3);
- —Б–љ–Є–ґ–µ–љ–Є–µ —А–∞—Б—Е–Њ–і–Њ–≤ –њ—А–Є –њ—А–Є–Љ–µ–љ–µ–љ–Є–Є –Њ—А–∞–ї—М–љ—Л—Е –∞–љ—В–Є–±–Є–Њ—В–Є–Ї–Њ–≤, —З—В–Њ —Б–≤—П–Ј–∞–љ–Њ —Б –і–Њ–њ–Њ–ї–љ–Є—В–µ–ї—М–љ—Л–Љ–Є –Ј–∞—В—А–∞—В–∞–Љ–Є –љ–∞ –≤–≤–µ–і–µ–љ–Є–µ –њ–∞—А–µ–љ—В–µ—А–∞–ї—М–љ—Л—Е –∞–љ—В–Є–±–∞–Ї—В–µ—А–Є–∞–ї—М–љ—Л—Е –њ—А–µ–њ–∞—А–∞—В–Њ–≤ (—Б–Љ. —В–∞–±–ї. 1);
- –≤–Њ–Ј–Љ–Њ–ґ–љ–Њ—Б—В—М –±–Њ–ї–µ–µ —А–∞–љ–љ–µ–є –≤—Л–њ–Є—Б–Ї–Є –±–Њ–ї—М–љ–Њ–≥–Њ, —В–∞–Ї –Ї–∞–Ї –њ—А–Є–µ–Љ –Њ—А–∞–ї—М–љ—Л—Е –∞–љ—В–Є–±–Є–Њ—В–Є–Ї–Њ–≤, –Ї–∞–Ї –њ—А–∞–≤–Є–ї–Њ, –љ–µ —В—А–µ–±—Г–µ—В –њ—А–µ–±—Л–≤–∞–љ–Є—П –њ–∞—Ж–Є–µ–љ—В–∞ –≤ —Б—В–∞—Ж–Є–Њ–љ–∞—А–µ;
- —Б–љ–Є–ґ–µ–љ–Є–µ —А–Є—Б–Ї–∞ –≤–Њ–Ј–љ–Є–Ї–љ–Њ–≤–µ–љ–Є—П –љ–Њ–Ј–Њ–Ї–Њ–Љ–Є–∞–ї—М–љ–Њ–є –Є–љ—Д–µ–Ї—Ж–Є–Є, –≤–Ї–ї—О—З–∞—П –њ–Њ—Б—В–Є–љ—К–µ–Ї—Ж–Є–Њ–љ—Л–µ –Њ—Б–ї–Њ–ґ–љ–µ–љ–Є—П.
–Ъ–Њ—А–Њ—В–Ї–Є–µ –Ї—Г—А—Б—Л –∞–љ—В–Є–±–Є–Њ—В–Є–Ї–Њ—В–µ—А–∞–њ–Є–Є
–°—В–∞–љ–і–∞—А—В–љ—Л–µ —Б—Е–µ–Љ—Л –∞–љ—В–Є–±–∞–Ї—В–µ—А–Є–∞–ї—М–љ–Њ–є —В–µ—А–∞–њ–Є–Є –њ–µ—А–Є–Њ–і–Є—З–µ—Б–Ї–Є –њ–µ—А–µ—Б–Љ–∞—В—А–Є–≤–∞—О—В—Б—П –≤ —Б–≤—П–Ј–Є —Б —А–Њ—Б—В–Њ–Љ —А–µ–Ј–Є—Б—В–µ–љ—В–љ–Њ—Б—В–Є –≤–Њ–Ј–±—Г–і–Є—В–µ–ї–µ–є –Є –њ–Њ—П–≤–ї–µ–љ–Є–µ–Љ –љ–Њ–≤—Л—Е –њ—А–µ–њ–∞—А–∞—В–Њ–≤, –Є–Љ–µ—О—Й–Є—Е —Г–ї—Г—З—И–µ–љ–љ—Л–µ —Д–∞—А–Љ–∞–Ї–Њ–Ї–Є–љ–µ—В–Є—З–µ—Б–Ї–Є–µ –њ–Њ–Ї–∞–Ј–∞—В–µ–ї–Є, –њ—А–µ–ґ–і–µ –≤—Б–µ–≥–Њ –±–Њ–ї–µ–µ –і–ї–Є—В–µ–ї—М–љ—Л–є –њ–µ—А–Є–Њ–і –њ–Њ–ї—Г–≤—Л–≤–µ–і–µ–љ–Є—П –Є –ї—Г—З—И—Г—О –±–Є–Њ–і–Њ—Б—В—Г–њ–љ–Њ—Б—В—М. –Я—А–Є–Љ–µ—А–Њ–Љ –љ–Њ–≤–Њ–≥–Њ –њ–Њ–і—Е–Њ–і–∞ –Ї —Е–Є–Љ–Є–Њ—В–µ—А–∞–њ–Є–Є —П–≤–ї—П—О—В—Б—П –Ї–Њ—А–Њ—В–Ї–Є–µ –Ї—Г—А—Б—Л –њ—А–Є–Љ–µ–љ–µ–љ–Є—П –∞–љ—В–Є–±–Є–Њ—В–Є–Ї–Њ–≤. –Ъ–∞–Ї –њ–Њ–Ї–∞–Ј–∞–ї–Є —А–µ–Ј—Г–ї—М—В–∞—В—Л –њ—А–Њ—Б–њ–µ–Ї—В–Є–≤–љ—Л—Е –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є—Е –Є—Б–њ—Л—В–∞–љ–Є–є, –Є—Е –Љ–Њ–ґ–љ–Њ —Г—Б–њ–µ—И–љ–Њ –њ—А–Є–Љ–µ–љ—П—В—М –њ—А–Є –Є–љ—Д–µ–Ї—Ж–Є—П—Е –Ы–Ю–†-–Њ—А–≥–∞–љ–Њ–≤ (–Њ—Б—В—А—Л–є —Б—А–µ–і–љ–Є–є –Њ—В–Є—В, –Њ—Б—В—А—Л–є —Б–Є–љ—Г—Б–Є—В, —В–Њ–љ–Ј–Є–ї–ї–Њ—Д–∞—А–Є–љ–≥–Є—В) [5 – 7], –Є–љ—Д–µ–Ї—Ж–Є—П—Е –і—Л—Е–∞—В–µ–ї—М–љ—Л—Е (–Њ–±–Њ—Б—В—А–µ–љ–Є–µ —Е—А–Њ–љ–Є—З–µ—Б–Ї–Њ–≥–Њ –±—А–Њ–љ—Е–Є—В–∞, –≤–љ–µ–±–Њ–ї—М–љ–Є—З–љ—Л–µ –њ–љ–µ–≤–Љ–Њ–љ–Є–Є) [8, 9] –Є –Љ–Њ—З–µ–≤—Л–≤–Њ–і—П—Й–Є—Е [10, 11] –њ—Г—В–µ–є.
–Ґ–∞–±–ї–Є—Ж–∞ 8. –Ю—Б–Њ–±–µ–љ–љ–Њ—Б—В–Є —А–∞–Ј–ї–Є—З–љ—Л—Е –њ–Њ–і—Е–Њ–і–Њ–≤, –љ–∞–њ—А–∞–≤–ї–µ–љ–љ—Л—Е –љ–∞ —Б–љ–Є–ґ–µ–љ–Є–µ –Ј–∞—В—А–∞—В –њ—А–Є –њ—А–Њ–≤–µ–і–µ–љ–Є–Є –∞–љ—В–Є–±–∞–Ї—В–µ—А–Є–∞–ї—М–љ–Њ–є —В–µ—А–∞–њ–Є–Є
| –Я–Њ–і—Е–Њ–і | –°–љ–Є–ґ–µ–љ–Є–µ —Б—В–Є–Љ–Њ—Б—В–Є –Р–С | –°–љ–Є–ґ–µ–љ–Є–µ —Б—В–Њ–Є–Љ–Њ—Б—В–Є –≤–≤–µ–і–µ–љ–Є—П –Р–С | –£–Љ–µ–љ—М—И–µ–љ–Є–µ —З–Є—Б–ї–∞ –њ–Њ—Б—В–Є–љ—К–µ–Ї—Ж–Є–Њ–љ–љ—Л—Е –Њ—Б–ї–Њ–ґ–љ–µ–љ–Є–є | –Я–Њ–≤—Л—И–µ–љ–Є–µ –Ї–Њ–Љ—Д–Њ—А—В–∞ –ї–µ—З–µ–љ–Є—П | –°–љ–Є–ґ–µ–љ–Є–µ —А–Є—Б–Ї–∞ –љ–Њ–Ј–Њ–Ї–Њ–Љ–Є–∞–ї—М–љ–Њ–є –Є–љ—Д–µ–Ї—Ж–Є–Є | –£–ї—Г—З—И–µ–љ–Є–µ –њ—Б–Є—Е–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Њ–є –Є —Б–Њ—Ж–Є–∞–ї—М–љ–Њ–є –∞–і–∞–њ—В–∞—Ж–Є–Є | –£–Љ–µ–љ—М—И–µ–љ–Є–µ —Б—А–Њ–Ї–∞ –≥–Њ—Б–њ–Є—В–∞–ї–Є–Ј–∞—Ж–Є–Є | –£–ї—Г—З—И–µ–љ–Є–µ —Б–Њ–±–ї—О–і–µ–љ–Є—П —А–µ–ґ–Є–Љ–∞ –ї–µ—З–µ–љ–Є—П | –£–Љ–µ–љ—М—И–µ–љ–Є–µ —З–Є—Б–ї–∞ –њ–Њ—Б–ї–µ–Њ–њ–µ—А–∞—Ж–Є–Њ–љ–љ—Л—Е —А–∞–љ–µ–≤—Л—Е –Є–љ—Д–µ–Ї—Ж–Є–є | –£–ї—Г—З—И–µ–љ–Є–µ –Ї–Њ–љ—В—А–Њ–ї—П –њ—А–Є–Љ–µ–љ–µ–љ–Є—П –Р–С | –£–ї—Г—З—И–µ–љ–Є–µ —Н–њ–Є–і–Є–Љ–Є–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Њ–є —Б–Є—В—Г–∞—Ж–Є–Є |
| –°—В—Г–њ–µ–љ—З–∞—В–∞—П —В–µ—А–∞–њ–Є—П |
+ |
+ |
+ |
+ |
+ |
+ |
+/- |
- |
- |
- |
- |
| –Ъ–Њ—А–Њ—В–Ї–Є–µ –Ї—Г—А—Б—Л |
+ |
+ |
+ |
+ |
- |
+/- |
+/- |
+ |
- |
- |
- |
| –Р–љ—В–Є–±–Є–Њ—В–Є–Ї–Њ-–њ—А–Њ—Д–Є–ї–∞–Ї—В–Є–Ї–∞ |
+ |
+ |
+ |
+/- |
+ |
- |
+ |
+/- |
+ |
- |
- |
| –Я—А–Є–Љ–µ–љ–µ–љ–Є–µ –≥–µ–љ–µ—А–Є–Ї–Њ–≤ |
+ |
- |
- |
- |
- |
- |
- |
- |
- |
- |
- |
| –§–Њ—А–Љ—Г–ї—П—А |
+ |
+ |
- |
- |
+ |
- |
- |
- |
- |
+ |
+ |
| –°–Є—Б—В–µ–Љ–∞ "–Њ–≥—А–∞–љ–Є—З–µ–љ–Є—П" |
+ |
+ |
- |
- |
+ |
- |
- |
- |
- |
+ |
+ |
| –Я–∞—А–µ–љ—В–µ—А–∞–ї—М–љ–∞—П —В–µ—А–∞–њ–Є—П –≤–љ–µ —Б—В–∞—Ж–Є–Њ–љ–∞—А–∞ |
- |
- |
- |
+ |
+ |
+ |
+ |
- |
- |
- |
- |
| –Р–С —Б –і–ї–Є—В–µ–ї—М–љ—Л–Љ –Є–љ—В–µ—А–≤–∞–ї–Њ–Љ –і–Њ–Ј–Є—А–Њ–≤–∞–љ–Є—П |
+/- |
+ |
+ |
+ |
- |
- |
- |
- |
- |
- |
- |
| –Ь–Њ–љ–Њ—В–µ—А–∞–њ–Є—П |
+/- |
+ |
+ |
+ |
- |
- |
- |
- |
- |
- |
- |
| –Я–µ—А–Њ—А–∞–ї—М–љ—Л–µ –∞–љ—В–Є–±–Є–Њ—В–Є–Ї–Є |
+ |
+ |
+ |
+ |
+ |
+ |
+/- |
- |
- |
- |
- |
| –Я —А –Є –Љ –µ —З –∞ –љ –Є –µ. –Р–С – –∞–љ—В–Є–±–Є–Њ—В–Є–Ї, "+" – –µ—Б—В—М, "-" - –Њ—В—Б—Г—В—Б—В–≤—Г–µ—В, "+/-" – –њ—А–Є—Б—Г—В—Б—В–≤—Г–µ—В –љ–µ –≤—Б–µ–≥–і–∞ –Є–ї–Є –њ—А–Є–Ј–љ–∞–Ї –Њ–њ–Њ—Б—А–µ–і–Њ–≤–∞–љ –Ї–Њ—Б–≤–µ–љ–љ–Њ. | |||||||||||
–†–∞—Б—Б–Љ–Њ—В—А–Є–Љ –≤ –Ї–∞—З–µ—Б—В–≤–µ –њ—А–Є–Љ–µ—А–∞ –њ—А–Є–Љ–µ–љ–µ–љ–Є–µ –Ї–Њ—А–Њ—В–Ї–Њ–≥–Њ –Ї—Г—А—Б–∞ –∞–љ—В–Є–±–Є–Њ—В–Є–Ї–Њ—В–µ—А–∞–њ–Є–Є –њ—А–Є —Б—В—А–µ–њ—В–Њ–Ї–Њ–Ї–Ї–Њ–≤–Њ–Љ —В–Њ–љ–Ј–Є–ї–ї–Њ—Д–∞—А–Є–љ–≥–Є—В–µ. 10-–і–љ–µ–≤–љ—Л–є –Ї—Г—А—Б –њ–µ–љ–Є—Ж–Є–ї–ї–Є–љ–∞ —П–≤–ї—П–µ—В—Б—П –Ј–Њ–ї–Њ—В—Л–Љ —Б—В–∞–љ–і–∞—А—В–Њ–Љ –і–ї—П –ї–µ—З–µ–љ–Є—П —Б—В—А–µ–њ—В–Њ–Ї–Њ–Ї–Ї–Њ–≤–Њ–≥–Њ —В–Њ–љ–Ј–Є–ї–ї–Њ—Д–∞—А–Є–љ–≥–Є—В–∞ —Б 1951 –≥. –Э–µ—Б–Љ–Њ—В—А—П –љ–∞ —В–Њ, —З—В–Њ —Н—В–Њ—В –∞–љ—В–Є–±–Є–Њ—В–Є–Ї –≤—Л–і–µ—А–ґ–∞–ї –Є—Б–њ—Л—В–∞–љ–Є–µ –≤—А–µ–Љ–µ–љ–µ–Љ –Є –Њ—Б—В–∞–µ—В—Б—П —Н—Д—Д–µ–Ї—В–Є–≤–љ—Л–Љ —Г –±–Њ–ї—М—И–Є–љ—Б—В–≤–∞ –њ–∞—Ж–Є–µ–љ—В–Њ–≤, –љ–Њ—Б–Є—В–µ–ї—М—Б—В–≤–Њ b-–≥–µ–Љ–Њ–ї–Є—В–Є—З–µ—Б–Ї–Њ–≥–Њ —Б—В—А–µ–њ—В–Њ–Ї–Њ–Ї–Ї–∞ –≥—А—Г–њ–њ—Л –Р —Б–Њ—Е—А–∞–љ—П–µ—В—Б—П –≤ 5 – 35% —Б–ї—Г—З–∞–µ–≤, —З—В–Њ –≥–Њ–≤–Њ—А–Є—В –Њ –±–∞–Ї—В–µ—А–Є–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Њ–є –љ–µ—Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В–Є –њ–µ–љ–Є—Ж–Є–ї–ї–Є–љ–∞ [12].
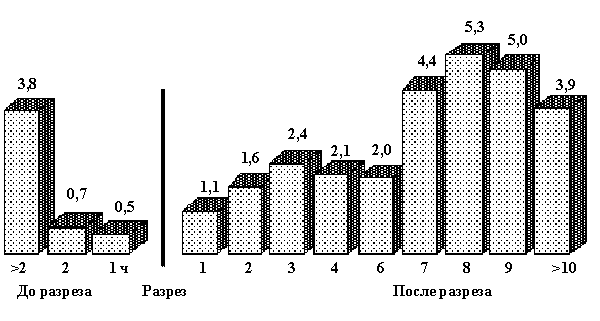
–†–Є—Б. 1. –І–∞—Б—В–Њ—В–∞ –њ–Њ—Б–ї–µ–Њ–њ–µ—А–∞—Ж–Є–Њ–љ–љ–Њ–є —А–∞–љ–µ–≤–Њ–є –Є–љ—Д–µ–Ї—Ж–Є–Є (–≤ %) –≤ –Ј–∞–≤–Є—Б–Є–Љ–Њ—Б—В–Є –Њ—В –≤—А–µ–Љ–µ–љ–Є –Љ–µ–ґ–і—Г –≤–≤–µ–і–µ–љ–Є–µ–Љ –∞–љ—В–Є–±–Є–Њ—В–Є–Ї–∞ –Є –љ–∞—З–∞–ї–Њ–Љ –Њ–њ–µ—А–∞—Ж–Є–Є [18].
–Т–Њ–Ј–Љ–Њ–ґ–љ—Л–Љ–Є –њ—А–Є—З–Є–љ–∞–Љ–Є –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Њ–є –љ–µ—Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В–Є —Б—В–∞–љ–і–∞—А—В–љ–Њ–≥–Њ 10-–і–љ–µ–≤–љ–Њ–≥–Њ –Ї—Г—А—Б–∞ –њ–µ–љ–Є—Ж–Є–ї–ї–Є–љ–∞ —П–≤–ї—П—О—В—Б—П: –љ–Є–Ј–Ї–Є–є —Г—А–Њ–≤–µ–љ—М —Б–Њ–±–ї—О–і–µ–љ–Є—П –њ–∞—Ж–Є–µ–љ—В–∞–Љ–Є —А–µ–ґ–Є–Љ–∞ –ї–µ—З–µ–љ–Є—П, –Ї–Њ–ї–Њ–љ–Є–Ј–∞—Ж–Є—П –Ї–Њ-–њ–∞—В–Њ–≥–µ–љ–∞–Љ–Є, —Н—А–∞–і–Є–Ї–∞—Ж–Є—П –љ–µ–њ–∞—В–Њ–≥–µ–љ–љ–Њ–є "–Ј–∞—Й–Є—В–љ–Њ–є" –Љ–Є–Ї—А–Њ—Д–ї–Њ—А—Л —А–Њ—В–Њ–≥–ї–Њ—В–Ї–Є, –Њ—Б–ї–∞–±–ї–µ–љ–Є–µ –Є–Љ–Љ—Г–љ–љ–Њ–≥–Њ –Њ—В–≤–µ—В–∞ –њ—А–Є —А–∞–љ–љ–µ–Љ –љ–∞—З–∞–ї–µ –∞–љ—В–Є–±–Є–Њ—В–Є–Ї–Њ—В–µ—А–∞–њ–Є–Є, –њ–µ—А–µ—Е–Њ–і –≤ –љ–Њ—Б–Є—В–µ–ї—М—Б—В–≤–Њ [13]. –Ъ–ї–Є–љ–Є—З–µ—Б–Ї–Є –і–Њ–Ї–∞–Ј–∞–љ–љ–Њ–є –∞–ї—М—В–µ—А–љ–∞—В–Є–≤–Њ–є —В—А–∞–і–Є—Ж–Є–Њ–љ–љ–Њ–Љ—Г 10-–і–љ–µ–≤–љ–Њ–Љ—Г –Ї—Г—А—Б—Г –њ–µ–љ–Є—Ж–Є–ї–ї–Є–љ–∞ –њ—А–Є —Б—В—А–µ–њ—В–Њ–Ї–Њ–Ї–Ї–Њ–≤–Њ–Љ —В–Њ–љ–Ј–Є–ї–ї–Њ—Д–∞—А–Є–љ–≥–Є—В–µ —П–≤–ї—П—О—В—Б—П, –љ–∞–њ—А–Є–Љ–µ—А, –Ї–Њ—А–Њ—В–Ї–Є–µ –Ї—Г—А—Б—Л —Ж–µ—Д–∞–ї–Њ—Б–њ–Њ—А–Є–љ–∞ II –њ–Њ–Ї–Њ–ї–µ–љ–Є—П —Ж–µ—Д—Г—А–Њ–Ї—Б–Є–Љ–∞ –∞–Ї—Б–µ—В–Є–ї–∞ (4 –і–љ—П) [14], –∞ —В–∞–Ї–ґ–µ –∞–љ—В–Є–±–Є–Њ—В–Є–Ї–Њ–≤ –Є–Ј –≥—А—Г–њ–њ—Л –Љ–∞–Ї—А–Њ–ї–Є–і–Њ–≤ – –∞–Ј–Є—В—А–Њ–Љ–Є—Ж–Є–љ–∞ [15], —Б–њ–Є—А–∞–Љ–Є—Ж–Є–љ–∞ [16].
–Ъ–Њ—А–Њ—В–Ї–Є–µ –Ї—Г—А—Б—Л –∞–љ—В–Є–±–Є–Њ—В–Є–Ї–Њ—В–µ—А–∞–њ–Є–Є –њ—А–Є –≤—Л—Б–Њ–Ї–Њ–Љ —Г—А–Њ–≤–љ–µ –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Њ–є —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В–Є –Њ–±–ї–∞–і–∞—О—В —Б–ї–µ–і—Г—О—Й–Є–Љ–Є –њ—А–µ–Є–Љ—Г—Й–µ—Б—В–≤–∞–Љ–Є:
- —Г–ї—Г—З—И–∞–µ—В—Б—П —Б–Њ–±–ї—О–і–µ–љ–Є–µ –њ–∞—Ж–Є–µ–љ—В–∞–Љ–Є —А–µ–ґ–Є–Љ–∞ –ї–µ—З–µ–љ–Є—П;
- —Б–љ–Є–ґ–∞–µ—В—Б—П —Б—В–Њ–Є–Љ–Њ—Б—В—М –ї–µ—З–µ–љ–Є—П –Ј–∞ —Б—З–µ—В —Г–Љ–µ–љ—М—И–µ–љ–Є—П —А–∞—Б—Е–Њ–і–Њ–≤ –љ–∞ –∞–љ—В–Є–±–Є–Њ—В–Є–Ї –Є –µ–≥–Њ –≤–≤–µ–і–µ–љ–Є–µ, –∞ —В–∞–Ї–ґ–µ –≤–Њ–Ј–Љ–Њ–ґ–љ–Њ–≥–Њ —Б–Њ–Ї—А–∞—Й–µ–љ–Є—П —Б—А–Њ–Ї–∞ –≥–Њ—Б–њ–Є—В–∞–ї–Є–Ј–∞—Ж–Є–Є;
- —Б–љ–Є–ґ–∞–µ—В—Б—П —А–Є—Б–Ї —А–∞–Ј–≤–Є—В–Є—П –љ–Њ–Ј–Њ–Ї–Њ–Љ–Є–∞–ї—М–љ–Њ–є –Є–љ—Д–µ–Ї—Ж–Є–Є, –≤–Ї–ї—О—З–∞—П –њ–Њ—Б—В–Є–љ—К–µ–Ї—Ж–Є–Њ–љ–љ—Л–µ –Њ—Б–ї–Њ–ґ–љ–µ–љ–Є—П.
–Р–љ—В–Є–±–Є–Њ—В–Є–Ї–Њ–њ—А–Њ—Д–Є–ї–∞–Ї—В–Є–Ї–∞ –≤ —Е–Є—А—Г—А–≥–Є–Є
–Я–Њ –Ј–∞—А—Г–±–µ–ґ–љ—Л–Љ –і–∞–љ–љ—Л–Љ, —А–∞–Ј–≤–Є—В–Є–µ —А–∞–љ–µ–≤–Њ–є –Є–љ—Д–µ–Ї—Ж–Є–Є —Б–њ–Њ—Б–Њ–±—Б—В–≤—Г–µ—В —Г–і–ї–Є–љ–µ–љ–Є—О —Б—А–Њ–Ї–Њ–≤ –њ—А–µ–±—Л–≤–∞–љ–Є—П –±–Њ–ї—М–љ–Њ–≥–Њ –≤ —Б—В–∞—Ж–Є–Њ–љ–∞—А–µ –љ–∞ 1 –љ–µ–і, —З—В–Њ –њ—А–Є–≤–Њ–і–Є—В –Ї —Г–≤–µ–ї–Є—З–µ–љ–Є—О —Б—В–Њ–Є–Љ–Њ—Б—В–Є –ї–µ—З–µ–љ–Є—П –љ–∞ 10–20% [17]. –Т –љ–∞—Б—В–Њ—П—Й–µ–µ –≤—А–µ–Љ—П –љ–Є–Ї—В–Њ –љ–µ —Б—В–∞–≤–Є—В –њ–Њ–і —Б–Њ–Љ–љ–µ–љ–Є–µ –њ—А–µ–Є–Љ—Г—Й–µ—Б—В–≤–∞ –њ–µ—А–Є–Њ–њ–µ—А–∞—Ж–Є–Њ–љ–љ–Њ–є –∞–љ—В–Є–±–Є–Њ—В–Є–Ї–Њ–њ—А–Њ—Д–Є–ї–∞–Ї—В–Є–Ї–Є. –Т –ї–Є—В–µ—А–∞—В—Г—А–µ –і–Є—Б–Ї—Г—В–Є—А—Г—О—В—Б—П –≤–Њ–њ—А–Њ—Б—Л –љ–µ –Њ —В–Њ–Љ, –љ—Г–ґ–µ–љ –ї–Є –∞–љ—В–Є–±–Є–Њ—В–Є–Ї –≤–Њ–Њ–±—Й–µ, –∞ –Ї–∞–Ї–Њ–є –њ—А–µ–њ–∞—А–∞—В –≤—Л–±—А–∞—В—М, —З—В–Њ–±—Л –і–Њ–±–Є—В—М—Б—П –Љ–∞–Ї—Б–Є–Љ–∞–ї—М–љ–Њ–є –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Њ–є –Є —Д–∞—А–Љ–∞–Ї–Њ—Н–Ї–Њ–љ–Њ–Љ–Є—З–µ—Б–Ї–Њ–є —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В–Є. –Т —В–Њ –ґ–µ –≤—А–µ–Љ—П –Љ–љ–Њ–≥–Є–µ —А–Њ—Б—Б–Є–є—Б–Ї–Є–µ —Е–Є—А—Г—А–≥–Є –љ–µ –њ–Њ—З—Г–≤—Б—В–≤–Њ–≤–∞–ї–Є –њ—А–µ–Є–Љ—Г—Й–µ—Б—В–≤ –∞–љ—В–Є–±–Є–Њ—В–Є–Ї–Њ–њ—А–Њ—Д–Є–ї–∞–Ї—В–Є–Ї–Є. –Т–Њ –Љ–љ–Њ–≥–Њ–Љ —Н—В–Њ —Б–≤—П–Ј–∞–љ–Њ —Б —В–µ–Љ, —З—В–Њ "–∞–љ—В–Є–±–Є–Њ—В–Є–Ї–Њ–њ—А–Њ—Д–Є–ї–∞–Ї—В–Є–Ї–∞" –љ–∞—З–Є–љ–∞–µ—В—Б—П –њ–Њ—Б–ї–µ –Њ–Ї–Њ–љ—З–∞–љ–Є—П –Њ–њ–µ—А–∞—Ж–Є–Є, –Ї–Њ–≥–і–∞ –±–Њ–ї—М–љ–Њ–є –њ–Њ—Б—В—Г–њ–∞–µ—В –≤ –њ–∞–ї–∞—В—Г. –Ю–±—Л—З–љ—Л–є –µ–µ –Ї—Г—А—Б —Б–Њ—Б—В–∞–≤–ї—П–µ—В 5–7 –і–љ–µ–є –Є –≤–Ї–ї—О—З–∞–µ—В –≤ —Б–µ–±—П –љ–∞–Є–±–Њ–ї–µ–µ –і–Њ—Б—В—Г–њ–љ—Л–µ –∞–љ—В–Є–±–Є–Њ—В–Є–Ї–Є, —В–∞–Ї–Є–µ –Ї–∞–Ї –±–µ–љ–Ј–Є–ї–њ–µ–љ–Є—Ж–Є–ї–ї–Є–љ, –њ–Њ–ї—Г—Б–Є–љ—В–µ—В–Є—З–µ—Б–Ї–Є–µ –њ–µ–љ–Є—Ж–Є–ї–ї–Є–љ—Л, –∞–Љ–Є–љ–Њ–≥–ї–Є–Ї–Њ–Ј–Є–і—Л. –Ы–Є—И—М –≤ –Њ—В–і–µ–ї—М–љ—Л—Е —Б—В–∞—Ж–Є–Њ–љ–∞—А–∞—Е –Є—Б–њ–Њ–ї—М–Ј—Г—О—В—Б—П –њ—А–Њ—В–Њ–Ї–Њ–ї—Л –њ–µ—А–Є–Њ–њ–µ—А–∞—Ж–Є–Њ–љ–љ–Њ–є –њ—А–Њ—Д–Є–ї–∞–Ї—В–Є–Ї–Є —Б –≤–≤–µ–і–µ–љ–Є–µ–Љ –њ–µ—А–≤–Њ–є –і–Њ–Ј—Л –њ—А–µ–њ–∞—А–∞—В–∞ –њ–µ—А–µ–і –љ–∞—З–∞–ї–Њ–Љ –Њ–њ–µ—А–∞—Ж–Є–Є.
–≠–Ї—Б–њ–µ—А–Є–Љ–µ–љ—В–∞–ї—М–љ—Л–µ —А–∞–±–Њ—В—Л –±—Л–ї–Є –њ–Њ–і—В–≤–µ—А–ґ–і–µ–љ—Л —А–µ–Ј—Г–ї—М—В–∞—В–∞–Љ–Є —А–∞–љ–і–Њ–Љ–Є–Ј–Є—А–Њ–≤–∞–љ–љ—Л—Е –Ї–Њ–љ—В—А–Њ–ї–Є—А–Њ–≤–∞–љ–љ—Л—Е –њ—А–Њ—Б–њ–µ–Ї—В–Є–≤–љ—Л—Е –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є—Е –Є—Б–њ—Л—В–∞–љ–Є–є. –Т —А–∞–±–Њ—В–µ D. Classen [18] –њ–Њ–Ї–∞–Ј–∞–љ–Њ, —З—В–Њ, –µ—Б–ї–Є –∞–љ—В–Є–±–∞–Ї—В–µ—А–Є–∞–ї—М–љ–∞—П —В–µ—А–∞–њ–Є—П –љ–∞—З–Є–љ–∞–µ—В—Б—П –±–Њ–ї–µ–µ —З–µ–Љ –Ј–∞ 2 —З –і–Њ –Љ–Њ–Љ–µ–љ—В–∞ —А–∞–Ј—А–µ–Ј–∞, —В–Њ –њ–Њ—Б–ї–µ–Њ–њ–µ—А–∞—Ж–Є–Њ–љ–љ–∞—П –Є–љ—Д–µ–Ї—Ж–Є—П —А–∞–Ј–≤–Є–≤–∞–µ—В—Б—П –≤ 3,8% —Б–ї—Г—З–∞–µ–≤ –њ–Њ —Б—А–∞–≤–љ–µ–љ–Є—О —Б 0,5% –њ—А–Є –≤–≤–µ–і–µ–љ–Є–Є –∞–љ—В–Є–±–Є–Њ—В–Є–Ї–∞ –Ј–∞ 1 —З (—А–Є—Б. 1).
–Х—Б–ї–Є –ґ–µ –∞–љ—В–Є–±–Є–Њ—В–Є–Ї –≤–≤–Њ–і–Є—В—Б—П –њ–Њ—Б–ї–µ –љ–∞—З–∞–ї–∞ –Њ–њ–µ—А–∞—Ж–Є–Є, —З–∞—Б—В–Њ—В–∞ —А–∞–Ј–≤–Є—В–Є—П –Є–љ—Д–µ–Ї—Ж–Є–Є –љ–∞—З–Є–љ–∞–µ—В –≤–Њ–Ј—А–∞—Б—В–∞—В—М, –і–Њ—Б—В–Є–≥–∞—П 5% –њ—А–Є –≤–≤–µ–і–µ–љ–Є–Є —З–µ—А–µ–Ј 8 – 9 —З –њ–Њ—Б–ї–µ —А–∞–Ј—А–µ–Ј–∞, –њ—А–Є—З–µ–Љ —З–µ–Љ –њ–Њ–Ј–ґ–µ –њ–Њ—Б–ї–µ –љ–∞—З–∞–ї–∞ –Њ–њ–µ—А–∞—Ж–Є–Є –љ–∞—З–∞—В–∞ –∞–љ—В–Є–±–Є–Њ—В–Є–Ї–Њ–њ—А–Њ—Д–Є–ї–∞–Ї—В–Є–Ї–∞, —В–µ–Љ –≤—Л—И–µ –≤–µ—А–Њ—П—В–љ–Њ—Б—В—М —А–∞–Ј–≤–Є—В–Є—П –Є–љ—Д–µ–Ї—Ж–Є–Є.
–Т 1995 –≥. –≤ –Њ–і–љ–Њ–Љ –Є–Ј —Б—В–∞—Ж–Є–Њ–љ–∞—А–Њ–≤ –°–Љ–Њ–ї–µ–љ—Б–Ї–∞ –Љ—Л –њ—А–Њ–≤–µ–ї–Є —А–µ—В—А–Њ—Б–њ–µ–Ї—В–Є–≤–љ—Л–є –∞–љ–∞–ї–Є–Ј 495 –Є—Б—В–Њ—А–Є–є –±–Њ–ї–µ–Ј–љ–Є –њ–∞—Ж–Є–µ–љ—В–Њ–≤, –≥–Њ—Б–њ–Є—В–∞–ї–Є–Ј–Є—А–Њ–≤–∞–љ–љ—Л—Е –≤ —В—А–∞–≤–Љ–∞—В–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Њ–µ, –Њ–љ–Ї–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Њ–µ –Њ—В–і–µ–ї–µ–љ–Є—П –Є –Њ—В–і–µ–ї–µ–љ–Є–µ —З–Є—Б—В–Њ–є —Е–Є—А—Г—А–≥–Є–Є. –Э–Є –≤ –Њ–і–љ–Њ–Љ —Б–ї—Г—З–∞–µ –њ–µ—А–Є–Њ–њ–µ—А–∞—Ж–Є–Њ–љ–љ–∞—П –∞–љ—В–Є–±–Є–Њ—В–Є–Ї–Њ–њ—А–Њ—Д–Є–ї–∞–Ї—В–Є–Ї–∞ –љ–µ –њ—А–Њ–≤–Њ–і–Є–ї–∞—Б—М. –Т–Љ–µ—Б—В–Њ —Н—В–Њ–≥–Њ, –Ї–∞–Ї –њ—А–∞–≤–Є–ї–Њ, –≤ –њ–Њ—Б–ї–µ–Њ–њ–µ—А–∞—Ж–Є–Њ–љ–љ–Њ–Љ –њ–µ—А–Є–Њ–і–µ —Б "–њ—А–Њ—Д–Є–ї–∞–Ї—В–Є—З–µ—Б–Ї–Њ–є —Ж–µ–ї—М—О" –љ–∞–Ј–љ–∞—З–∞–ї–Є—Б—М –∞–љ—В–Є–±–Є–Њ—В–Є–Ї–Є –Ї—Г—А—Б–Њ–Љ 5 – 10 –і–љ–µ–є. –°—А–µ–і–љ—П—П —Б—В–Њ–Є–Љ–Њ—Б—В—М –Ї—Г—А—Б–∞ —Б–Њ—Б—В–∞–≤–ї—П–ї–∞ –љ–∞ 1995 –≥. 30 000 —А—Г–±. –≤ —В–Њ –≤—А–µ–Љ—П –Ї–∞–Ї –њ—А–Њ–≤–µ–і–µ–љ–Є–µ –њ–µ—А–Є–Њ–њ–µ—А–∞—Ж–Є–Њ–љ–љ–Њ–є –∞–љ—В–Є–±–Є–Њ—В–Є–Ї–Њ–њ—А–Њ—Д–Є–ї–∞–Ї—В–Є–Ї–Є —Ж–µ—Д–∞–Ј–Њ–ї–Є–љ–Њ–Љ —Б—В–Њ–Є–ї–Њ 12 500 —А—Г–±.
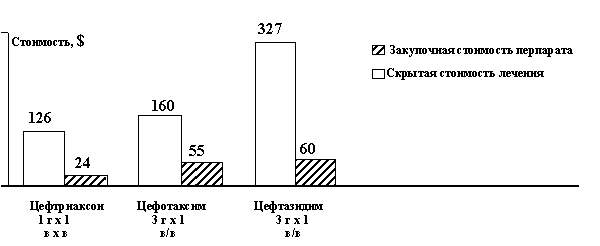
–†–Є—Б. 2 –°—А–∞–≤–љ–Є—В–µ–ї—М–љ—Л–є –∞–љ–∞–ї–Є–Ј —Б—В–Њ–Є–Љ–Њ—Б—В–Є 7-–і–љ–µ–≤–љ–Њ–≥–Њ –Ї—Г—А—Б–∞ –ї–µ—З–µ–љ–Є—П —Ж–µ—Д–∞–ї–Њ—Б–њ–Њ—А–Є–љ–∞–Љ–Є III –њ–Њ–Ї–Њ–ї–µ–љ–Є—П [23]
–Т–≤–µ–і–µ–љ–Є–µ –∞–љ—В–Є–±–Є–Њ—В–Є–Ї–Њ–≤ —Б –њ—А–Њ—Д–Є–ї–∞–Ї—В–Є—З–µ—Б–Ї–Њ–є —Ж–µ–ї—М—О –≤ –њ–µ—А–Є–Њ–њ–µ—А–∞—Ж–Є–Њ–љ–љ–Њ–Љ –њ–µ—А–Є–Њ–і–µ –њ—А–Є —Г—Б–ї–Њ–≤–љ–Њ-—З–Є—Б—В—Л—Е –Є —Г—Б–ї–Њ–≤–љ–Њ-–Ј–∞–≥—А—П–Ј–љ–µ–љ–љ—Л—Е –Њ–њ–µ—А–∞—В–Є–≤–љ—Л—Е –≤–Љ–µ—И–∞—В–µ–ї—М—Б—В–≤–∞—Е –њ–Њ–Ј–≤–Њ–ї—П–µ—В:
- —Б–љ–Є–Ј–Є—В—М —З–∞—Б—В–Њ—В—Г –њ–Њ—Б–ї–µ–Њ–њ–µ—А–∞—Ж–Є–Њ–љ–љ—Л—Е –Є–љ—Д–µ–Ї—Ж–Є–Њ–љ–љ—Л—Е –Њ—Б–ї–Њ–ґ–љ–µ–љ–Є–є;
- —Б–љ–Є–Ј–Є—В—М —А–∞—Б—Е–Њ–і—Л –Ј–∞ —Б—З–µ—В —Б–Њ–Ї—А–∞—Й–µ–љ–Є—П —З–Є—Б–ї–∞ –њ—Б–ї–µ–Њ–њ–µ—А–∞—Ж–Є–Њ–љ–љ—Л—Е –Є–љ—Д–µ–Ї—Ж–Є–Њ–љ–љ—Л—Е –Њ—Б–ї–Њ–ґ–љ–µ–љ–Є–є, –Њ—В–Љ–µ–љ—Л –і–ї–Є—В–µ–ї—М–љ—Л—Е –Ї—Г—А—Б–Њ–≤ "–∞–љ—В–Є–±–Є–Њ—В–Є–Ї–Њ–њ—А–Њ—Д–Є–ї–∞–Ї—В–Є–Ї–Є" –≤ –њ–Њ—Б–ї–µ–Њ–њ–µ—А–∞—Ж–Є–Њ–љ–љ–Њ–Љ –њ–µ—А–Є–Њ–і–µ;
- —Б–љ–Є–Ј–Є—В—М —З–∞—Б—В–Њ—В—Г –љ–Њ–Ј–Њ–Ї–Њ–Љ–Є–∞–ї—М–љ–Њ–є –Є–љ—Д–µ–Ї—Ж–Є–Є;
- —Б–Њ–Ї—А–∞—В–Є—В—М —Б—А–Њ–Ї –≥–Њ—Б–њ–Є—В–∞–ї–Є–Ј–∞—Ж–Є–Є –њ–∞—Ж–Є–µ–љ—В–Њ–≤.
–Я—А–Є–Љ–µ–љ–µ–љ–Є–µ –≥–µ–љ–µ—А–Є–Ї–Њ–≤
–Ш—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є–µ –∞–љ—В–Є–±–Є–Њ—В–Є–Ї–Њ–≤-–≥–µ–љ–µ—А–Є–Ї–Њ–≤ —Б–њ–Њ—Б–Њ–±–љ–Њ —Б–Њ–Ї—А–∞—В–Є—В—М —А–∞—Б—Е–Њ–і—Л –Ј–∞ —Б—З–µ—В —А–∞–Ј–љ–Є—Ж—Л –≤ —Б—В–Њ–Є–Љ–Њ—Б—В–Є –Љ–µ–ґ–і—Г –љ–Є–Љ–Є –Є –Є–љ–љ–Њ–≤–∞—Ж–Є–Њ–љ–љ—Л–Љ–Є –∞–љ—В–Є–±–∞–Ї—В–µ—А–Є–∞–ї—М–љ—Л–Љ–Є –њ—А–µ–њ–∞—А–∞—В–∞–Љ–Є (—В–∞–±–ї. 4).
–Э–∞ –њ–µ—А–≤—Л–є –≤–Ј–≥–ї—П–і –≥–µ–љ–µ—А–Є–Ї–∞ –Ї–∞–ґ–µ—В—Б—П –њ—А–Њ—Б—В–Њ–є –Ј–∞–і–∞—З–µ–є –њ—А–Є –љ—Л–љ–µ—И–љ–µ–Љ –Є–Ј–Њ–±–Є–ї–Є–Є –љ–∞ —Д–∞—А–Љ–∞—Ж–µ–≤—В–Є—З–µ—Б–Ї–Њ–Љ —А—Л–љ–Ї–µ –∞–љ—В–Є–±–∞–Ї—В–µ—А–Є–∞–ї—М–љ—Л—Е –њ—А–µ–њ–∞—А–∞—В–Њ–≤. –Ю–і–љ–∞–Ї–Њ –љ–µ –≤—Б–µ –≥–µ–љ–µ—А–Є–Ї–Є —А–∞–≤–љ–Њ—Ж–µ–љ–љ—Л –≤ –Ї–∞—З–µ—Б—В–≤–µ–љ–љ–Њ–Љ –Њ—В–љ–Њ—И–µ–љ–Є–Є. –Т –њ–µ—А–≤—Г—О –Њ—З–µ—А–µ–і—М —Н—В–Њ –Њ—В–љ–Њ—Б–Є—В—Б—П –Ї –њ–µ—А–Њ—А–∞–ї—М–љ—Л–Љ –њ—А–µ–њ–∞—А–∞—В–∞–Љ, —В–∞–Ї –Ї–∞–Ї –≥–µ–љ–µ—А–Є–Ї–Є –і–Њ–ї–ґ–љ—Л –±—Л—В—М –±–Є–Њ—Н–Ї–≤–Є–≤–∞–ї–µ–љ—В–љ—Л–Љ–Є –Њ—А–Є–≥–Є–љ–∞–ї—М–љ–Њ–Љ—Г –њ—А–µ–њ–∞—А–∞—В—Г, —Е–Њ—В—П —Б–ї–µ–і—Г–µ—В —Г–і–µ–ї—П—В—М –њ–Њ–≤—Л—И–µ–љ–љ–Њ–µ –≤–љ–Є–Љ–∞–љ–Є–µ –Є –Ї–∞—З–µ—Б—В–≤—Г –њ—А–µ–њ–∞—А–∞—В–Њ–≤ –і–ї—П –њ–∞—А–µ–љ—В–µ—А–∞–ї—М–љ–Њ–≥–Њ –≤–≤–µ–і–µ–љ–Є—П [19].
–Я—А–Є –≤—Л–±–Њ—А–µ –≥–µ–љ–µ—А–Є—З–µ—Б–Ї–Њ–≥–Њ –∞–љ—В–Є–±–Є–Њ—В–Є–Ї–∞ –Љ—Л –і–Њ–ї–ґ–љ—Л –±—Л—В—М —Г–≤–µ—А–µ–љ—Л –≤ –µ–≥–Њ —Б–Њ–Њ—В–≤–µ—В—Б—В–≤–Є–Є –Њ–±—Й–µ–њ—А–Є–љ—П—В—Л–Љ —Б—В–∞–љ–і–∞—А—В–∞–Љ –њ–Њ —Б–Њ–і–µ—А–ґ–∞–љ–Є—О –∞–Ї—В–Є–≤–љ–Њ–≥–Њ –≤–µ—Й–µ—Б—В–≤–∞, –Ї–Њ–љ—Ж–µ–љ—В—А–∞—Ж–Є–Є –њ—А–Є–Љ–µ—Б–µ–є, –∞ –і–ї—П –Њ—А–∞–ї—М–љ—Л—Е –њ—А–µ–њ–∞—А–∞—В–Њ–≤ –Є –њ–Њ –њ–Њ–Ї–∞–Ј–∞—В–µ–ї—О –±–Є–Њ–і–Њ—Б—В—Г–њ–љ–Њ—Б—В–Є.
–§–Њ—А–Љ—Г–ї—П—А –∞–љ—В–Є–±–Є–Њ—В–Є–Ї–Њ–≤
–Я–Њ–і —Д–Њ—А–Љ—Г–ї—П—А–Њ–Љ –њ—А–Є–љ—П—В–Њ –њ–Њ–љ–Є–Љ–∞—В—М –њ–µ—А–µ—З–µ–љ—М –ї–µ–Ї–∞—А—Б—В–≤–µ–љ–љ—Л—Е –њ—А–µ–њ–∞—А–∞—В–Њ–≤, —А–µ–Ї–Њ–Љ–µ–љ–і—Г–µ–Љ—Л—Е –Њ—А–≥–∞–љ–∞–Љ–Є –≥–Њ—Б—Г–і–∞—А—Б—В–≤–µ–љ–љ–Њ–≥–Њ –Ј–і—А–∞–≤–Њ–Њ—Е—А–∞–љ–µ–љ–Є—П, –Љ–µ–і–Є—Ж–Є–љ—Б–Ї–Њ–≥–Њ —Б—В—А–∞—Е–Њ–≤–∞–љ–Є—П –Є–ї–Є –њ—А–µ–і–њ–Њ—З—В–Є—В–µ–ї—М–љ—Л—Е –≤ –і–∞–љ–љ–Њ–Љ –ї–µ—З–µ–±–љ–Њ–Љ —Г—З—А–µ–ґ–і–µ–љ–Є–Є. –§–Њ—А–Љ—Г–ї—П—А –Њ–і–љ–Њ–є –Ї–ї–Є–љ–Є–Ї–Є –Љ–Њ–ґ–µ—В –Њ—В–ї–Є—З–∞—В—М—Б—П –Њ—В —Д–Њ—А–Љ—Г–ї—П—А–∞ –і—А—Г–≥–Њ–є, –Њ–і–љ–∞–Ї–Њ –њ–Њ–і—Е–Њ–і—Л –Ї –µ–≥–Њ —Б–Њ—Б—В–∞–≤–ї–µ–љ–Є—О –Њ—Б—В–∞—О—В—Б—П –Њ–і–Є–љ–∞–Ї–Њ–≤—Л–Љ–Є.
–Т —Б–Њ—Б—В–∞–≤–ї–µ–љ–Є–Є —Д–Њ—А–Љ—Г–ї—П—А–∞ –∞–љ—В–Є–±–∞–Ї—В–µ—А–Є–∞–ї—М–љ—Л—Е –њ—А–µ–њ–∞—А–∞—В–Њ–≤ –њ—А–Є–љ–Є–Љ–∞—О—В —Г—З–∞—Б—В–Є–µ –≤—А–∞—З–Є —А–∞–Ј–љ—Л—Е —Б–њ–µ—Ж–Є–∞–ї—М–љ–Њ—Б—В–µ–є – –Є–љ—Д–µ–Ї—Ж–Є–Њ–љ–Є—Б—В—Л, –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є–µ —Д–∞—А–Љ–∞–Ї–Њ–ї–Њ–≥–Є, –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є–µ –Љ–Є–Ї—А–Њ–±–Є–Њ–ї–Њ–≥–Є, —Е–Є—А—Г—А–≥–Є –Є –і—А—Г–≥–Є–µ –Ї–ї–Є–љ–Є—Ж–Є—Б—В—Л. –§–Њ—А–Љ—Г–ї—П—А —Б–ї–µ–і—Г–µ—В —Б–Є—Б—В–µ–Љ–∞—В–Є—З–µ—Б–Ї–Є (1 – 2 —А–∞–Ј–∞ –≤ –≥–Њ–і) –њ–µ—А–µ—Б–Љ–∞—В—А–Є–≤–∞—В—М —Б —Г—З–µ—В–Њ–Љ —Н–њ–Є–і–µ–Љ–Є–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є—Е –і–∞–љ–љ—Л—Е, –њ–Њ—П–≤–ї–µ–љ–Є—П –љ–Њ–≤—Л—Е –∞–љ—В–Є–±–Є–Њ—В–Є–Ї–Њ–≤, –Є–Ј–Љ–µ–љ–µ–љ–Є—П –њ–Њ–і—Е–Њ–і–Њ–≤ –Ї –ї–µ—З–µ–љ–Є—О –Є –њ—А–Њ—Д–Є–ї–∞–Ї—В–Є–Ї–µ –Є–љ—Д–µ–Ї—Ж–Є–Њ–љ–љ—Л—Е –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є–є. –°—Г—Й–µ—Б—В–≤—Г—О—В –Њ–њ—А–µ–і–µ–ї–µ–љ–љ—Л–µ –њ—А–Є–љ—Ж–Є–њ—Л –Њ—В–±–Њ—А–∞ –∞–љ—В–Є–±–Є–Њ—В–Є–Ї–∞ –≤ —Д–Њ—А–Љ—Г–ї—П—А, –љ–∞–њ—А–Є–Љ–µ—А, –Є–Ј –љ–µ—Б–Ї–Њ–ї—М–Ї–Є—Е –њ—А–µ–і—Б—В–∞–≤–Є—В–µ–ї–µ–є –Њ–і–љ–Њ–≥–Њ –Ї–ї–∞—Б—Б–∞ –∞–љ—В–Є–±–∞–Ї—В–µ—А–Є–∞–ї—М–љ—Л—Е –њ—А–µ–њ–∞—А–∞—В–Њ–≤ —Б–ї–µ–і—Г–µ—В –Њ—В–і–∞–≤–∞—В—М –њ—А–µ–і–њ–Њ—З—В–µ–љ–Є–µ –Ї–∞–Ї–Њ–Љ—Г-–ї–Є–±–Њ –Њ–і–љ–Њ–Љ—Г –њ—А–µ–њ–∞—А–∞—В—Г. –Ґ–∞–Ї, –љ–µ –Є–Љ–µ–µ—В —Б–Љ—Л—Б–ї–∞ –њ—А–Є–Љ–µ–љ—П—В—М –≤ —Б—В–∞—Ж–Є–Њ–љ–∞—А–µ –љ–µ—Б–Ї–Њ–ї—М–Ї–Њ –∞–Љ–Є–љ–Њ–≥–ї–Є–Ї–Њ–Ј–Є–і–Њ–≤, –љ–∞–њ—А–Є–Љ–µ—А –≥–µ–љ—В–∞–Љ–Є—Ж–Є–љ, —В–Њ–±—А–∞–Љ–Є—Ж–Є–љ, –љ–µ—В–Є–ї–Љ–Є—Ж–Є–љ, –∞–Љ–Є–Ї–∞—Ж–Є–љ. –Ю–±—Л—З–љ–Њ –≤—Л–±–Є—А–∞—О—В –Њ–і–Є–љ-–і–≤–∞ –Є–Ј –љ–Є—Е.
–§–Њ—А–Љ—Г–ї—П—А–љ–∞—П —Б—Е–µ–Љ–∞ –∞–љ—В–Є–±–∞–Ї—В–µ—А–Є–∞–ї—М–љ—Л—Е –њ—А–µ–њ–∞—А–∞—В–Њ–≤ –Є–Љ–µ–µ—В —Б–ї–µ–і—Г—О—Й–Є–µ —Д–∞—А–Љ–∞–Ї–Њ—Н–Ї–Њ–љ–Њ–Љ–Є—З–µ—Б–Ї–Є–µ –њ—А–µ–Є–Љ—Г—Й–µ—Б—В–≤–∞:
- –Њ–≥—А–∞–љ–Є—З–µ–љ–љ–Њ–µ —З–Є—Б–ї–Њ –∞–љ—В–Є–±–Є–Њ—В–Є–Ї–Њ–≤, –Є—Б–њ–Њ–ї—М–Ј—Г–µ–Љ—Л—Е –≤ –Ї–ї–Є–љ–Є–Ї–µ;
- –±–Њ–ї–µ–µ –і–µ—В–∞–ї—М–љ–Њ–µ –Ј–љ–∞–љ–Є–µ –≤—А–∞—З–∞–Љ–Є —Н—В–Њ–≥–Њ –Њ–≥—А–∞–љ–Є—З–µ–љ–љ–Њ–≥–Њ —З–Є—Б–ї–∞ –∞–љ—В–Є–±–Є–Њ—В–Є–Ї–Њ–≤;
- –њ–Њ–≤—Л—И–µ–љ–Є–µ –Ї–Њ–љ—В—А–Њ–ї—П –Ј–∞ –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є–µ–Љ –∞–љ—В–Є–±–∞–Ї—В–µ—А–Є–∞–ї—М–љ—Л—Е –њ—А–µ–њ–∞—А–∞—В–Њ–≤;
- —Б–љ–Є–ґ–µ–љ–Є–µ —А–Є—Б–Ї–∞ –њ–Њ—П–≤–ї–µ–љ–Є—П —А–µ–Ј–Є—Б—В–µ–љ—В–љ—Л—Е —И—В–∞–Љ–Љ–Њ–≤ –≤–Њ–Ј–±—Г–і–Є—В–µ–ї–µ–є, —Г–ї—Г—З—И–µ–љ–Є–µ —Н–њ–Є–і–µ–Љ–Є–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Њ–є —Б–Є—В—Г–∞—Ж–Є–Є –≤ –Ї–ї–Є–љ–Є–Ї–µ;
- —Б–љ–Є–ґ–µ–љ–Є–µ –Ј–∞—В—А–∞—В –љ–∞ –Ј–∞–Ї—Г–њ–Ї—Г –∞–љ—В–Є–±–∞–Ї—В–µ—А–Є–∞–ї—М–љ—Л—Е –њ—А–µ–њ–∞—А–∞—В–Њ–≤ –Ј–∞ —Б—З–µ—В –Њ–≥—А–∞–љ–Є—З–µ–љ–љ–Њ–≥–Њ –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є—П –∞–љ—В–Є–±–Є–Њ—В–Є–Ї–Њ–≤, –Њ–≥—А–∞–љ–Є—З–µ–љ–Є—П –њ–µ—А–µ—З–љ—П –∞–љ—В–Є–±–Є–Њ—В–Є–Ї–Њ–≤, –≤–Њ–Ј–Љ–Њ–ґ–љ–Њ—Б—В–Є –њ—А–µ–і–Њ—Б—В–∞–≤–ї–µ–љ–Є—П —Б–Ї–Є–і–Њ–Ї –њ–Њ—Б—В–∞–≤—Й–Є–Ї–Њ–Љ –њ—А–Є –њ—А–Є–Њ–±—А–µ—В–µ–љ–Є–Є –Ї—А—Г–њ–љ—Л—Е –њ–∞—А—В–Є–є –њ—А–µ–њ–∞—А–∞—В–Њ–≤ –Њ–і–љ–Њ–≥–Њ –Ї–ї–∞—Б—Б–∞, –≤—Л–±–Њ—А–∞ –≤ —А–∞–Љ–Ї–∞—Е –≥—А—Г–њ–њ—Л –њ—А–µ–њ–∞—А–∞—В–∞ —Б –љ–∞–Є–ї—Г—З—И–Є–Љ –њ–Њ–Ї–∞–Ј–∞—В–µ–ї–µ–Љ —Б—В–Њ–Є–Љ–Њ—Б—В—М – —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В—М.
–°–Є—Б—В–µ–Љ–∞ –Њ–≥—А–∞–љ–Є—З–µ–љ–Є—П –њ—А–Є–Љ–µ–љ–µ–љ–Є—П –∞–љ—В–Є–±–Є–Њ—В–Є–Ї–Њ–≤
–°–Є—Б—В–µ–Љ–∞ –Њ–≥—А–∞–љ–Є—З–µ–љ–Є—П –њ—А–Є–Љ–µ–љ–µ–љ–Є—П –∞–љ—В–Є–±–Є–Њ—В–Є–Ї–Њ–≤ –Љ–Њ–ґ–µ—В –Є–Љ–µ—В—М –і–≤–∞ –≤–∞—А–Є–∞–љ—В–∞.
–Я–µ—А–≤—Л–є –Є–Ј –љ–Є—Е —Б–Њ—Б—В–Њ–Є—В –≤ —В–Њ–Љ, —З—В–Њ –≤ –Ї–ї–Є–љ–Є–Ї–µ —Б–Њ–Ј–і–∞–µ—В—Б—П —В–∞–Ї –љ–∞–Ј—Л–≤–∞–µ–Љ—Л–є —Б–њ–Є—Б–Њ–Ї —А–µ–Ј–µ—А–≤–љ—Л—Е, –Њ–≥—А–∞–љ–Є—З–µ–љ–љ—Л—Е –Ї –њ—А–Є–Љ–µ–љ–µ–љ–Є—О –∞–љ—В–Є–±–∞–Ї—В–µ—А–Є–∞–ї—М–љ—Л—Е –њ—А–µ–њ–∞—А–∞—В–Њ–≤.
–Э–∞–Ј–љ–∞—З–∞—П –њ–∞—Ж–Є–µ–љ—В—Г –∞–љ—В–Є–±–Є–Њ—В–Є–Ї –Є–Ј —А–µ–Ј–µ—А–≤–љ–Њ–≥–Њ —Б–њ–Є—Б–Ї–∞, –≤—А–∞—З –њ–Њ–ї—Г—З–∞–µ—В –Є–Ј –∞–њ—В–µ–Ї–Є –њ—А–µ–њ–∞—А–∞—В —В–Њ–ї—М–Ї–Њ –і–ї—П –љ–∞—З–∞–ї–∞ —В–µ—А–∞–њ–Є–Є (–љ–∞ 1 – 2 –і–љ—П), –і–ї—П –њ—А–Њ–і–Њ–ї–ґ–µ–љ–Є—П –Ї—Г—А—Б–∞ –Њ–љ –Ј–∞–њ–Њ–ї–љ—П–µ—В –њ–Є—Б—М–Љ–µ–љ–љ–Њ–µ —В—А–µ–±–Њ–≤–∞–љ–Є–µ —Б –Њ–±–Њ—Б–љ–Њ–≤–∞–љ–Є–µ–Љ –≤—Л–±–Њ—А–∞ –∞–љ—В–Є–±–Є–Њ—В–Є–Ї–∞. –Т —Б–ї—Г–∞—З–µ, –µ—Б–ї–Є –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є–µ–є —Д–∞—А–Љ–∞–Ї–Њ–ї–Њ–≥ –њ—А–Є–Ј–љ–∞–µ—В –љ–∞–Ј–љ–∞—З–µ–љ–Є–µ –∞–љ—В–Є–±–Є–Њ—В–Є–Ї–∞ –Њ–њ—А–∞–≤–і–∞–љ–љ—Л–Љ, –њ–∞—Ж–Є–µ–љ—В –њ—А–Њ–і–Њ–ї–ґ–∞–µ—В –њ–Њ–ї—Г—З–∞—В—М –љ–∞–Ј–љ–∞—З–µ–љ–љ—Л–є –њ—А–µ–њ–∞—А–∞—В. –Т –њ—А–Њ—В–Є–≤–љ–Њ–Љ —Б–ї—Г—З–∞–µ –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є–є —Д–∞—А–Љ–∞–Ї–Њ–ї–Њ–≥ –Є–ї–Є —Е–Є–Љ–Є–Њ—В–µ—А–∞–њ–µ–≤—В –Њ–±—Б—Г–ґ–і–∞–µ—В –Њ–±–Њ—Б–љ–Њ–≤–∞–љ–љ–Њ—Б—В—М –≤—Л–±–Њ—А–∞ –∞–љ—В–Є–±–Є–Њ—В–Є–Ї–∞ —Б –ї–µ—З–∞—Й–Є–Љ –≤—А–∞—З–Њ–Љ.
–Т—В–Њ—А–Њ–є –≤–∞—А–Є–∞–љ—В –Њ–≥—А–∞–љ–Є—З–µ–љ–Є—П –њ—А–Є–Љ–µ–љ–µ–љ–Є—П –∞–љ—В–Є–±–Є–Њ—В–Є–Ї–Њ–≤ –Ј–∞–Ї–ї—О—З–∞–µ—В—Б—П –≤ –њ—А–µ–і–≤–∞—А–Є—В–µ–ї—М–љ–Њ–є –Ї–Њ–љ—Б—Г–ї—М—В–∞—Ж–Є–Є –ї–µ—З–∞—Й–µ–≥–Њ –≤—А–∞—З–∞ —Б–Њ —Б–њ–µ—Ж–Є–∞–ї–Є—Б—В–Њ–Љ –њ–Њ –Є–љ—Д–µ–Ї—Ж–Є–Њ–љ–љ—Л–Љ –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П–Љ (–Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є–є —Д–∞—А–Љ–∞–Ї–Њ–ї–Њ–≥, —Е–Є–Љ–Є–Њ—В–µ—А–∞–њ–µ–≤—В) –њ–µ—А–µ–і —В–µ–Љ, –Ї–∞–Ї –љ–∞–Ј–љ–∞—З–Є—В—М –њ—А–µ–њ–∞—А–∞—В –Є–Ј —А–µ–Ј–µ—А–≤–љ–Њ–≥–Њ —Б–њ–Є—Б–Ї–∞.
–§–∞—А–Љ–∞–Ї–Њ—Н–Ї–Њ–љ–Њ–Љ–Є—З–µ—Б–Ї–Є–µ –њ—А–µ–Є–Љ—Г—Й–µ—Б—В–≤–∞, –Ї–Њ—В–Њ—А—Л–µ –Є–Љ–µ–µ—В —Б–Є—Б—В–µ–Љ–∞ –Њ–≥—А–∞–љ–Є—З–µ–љ–Є—П –њ—А–Є–Љ–µ–љ–µ–љ–Є—П –∞–љ—В–Є–±–Є–Њ—В–Є–Ї–Њ–≤, —В–∞–Ї–Є–µ –ґ–µ, –Ї–∞–Ї –Є –њ—А–Є –њ—А–Є–Љ–µ–љ–µ–љ–Є–Є —Д–Њ—А–Љ—Г–ї—П—А–љ–Њ–є —Б–Є—Б—В–µ–Љ—Л, –Њ–і–љ–∞–Ї–Њ –њ—А–Є —Н—В–Њ–Љ –Њ–±–µ—Б–њ–µ—З–Є–≤–∞–µ—В—Б—П –±–Њ–ї–µ–µ —Б—В—А–Њ–≥–Є–є –Ї–Њ–љ—В—А–Њ–ї—М –Ј–∞ –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є–µ–Љ –∞–љ—В–Є–±–Є–Њ—В–Є–Ї–Њ–≤.
–Т —А—П–і–µ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–є –њ–Њ–Ї–∞–Ј–∞–љ–Њ, —З—В–Њ —Б–Є—Б—В–µ–Љ–∞ –Њ–≥—А–∞












