–°–Њ–≥–ї–∞—Б–љ–Њ –Њ–њ—А–µ–і–µ–ї–µ–љ–Є—О –Т–Ю–Ч, —А–∞—Ж–Є–Њ–љ–∞–ї—М–љ–Њ–µ –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є–µ –Ы–° – —Н—В–Њ –њ—А–∞–≤–Є–ї—М–љ–Њ–µ, —Б–Њ–Њ—В–≤–µ—В—Б—В–≤—Г—О—Й–µ–µ –Є –љ–∞–і–ї–µ–ґ–∞—Й–µ–µ –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є–µ –Ы–°. –†–∞—Ж–Є–Њ–љ–∞–ї—М–љ–Њ–µ –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є–µ –Њ–Ј–љ–∞—З–∞–µ—В, —З—В–Њ –њ–∞—Ж–Є–µ–љ—В—Л –њ–Њ–ї—Г—З–∞—О—В –љ–∞–і–ї–µ–ґ–∞—Й–Є–µ –ї–µ–Ї–∞—А—Б—В–≤–µ–љ–љ—Л–µ –њ—А–µ–њ–∞—А–∞—В—Л –≤ –њ—А–∞–≤–Є–ї—М–љ—Л—Е –і–Њ–Ј–Є—А–Њ–≤–Ї–∞—Е, –љ–∞ —Б–Њ–Њ—В–≤–µ—В—Б—В–≤—Г—О—Й–Є–є –њ–µ—А–Є–Њ–і –≤—А–µ–Љ–µ–љ–Є –Є —Б –љ–∞–Є–Љ–µ–љ—М—И–Є–Љ–Є –Ј–∞—В—А–∞—В–∞–Љ–Є –і–ї—П —Б–µ–±—П –Є –Њ–±—Й–µ—Б—В–≤–∞ [8]. –І—В–Њ –Ї–∞—Б–∞–µ—В—Б—П –Р–Ь–Я, —В–Њ –Т–Ю–Ч –Њ–њ—А–µ–і–µ–ї—П–µ—В —А–∞–Ј—Г–Љ–љ–Њ–µ –њ—А–Є–Љ–µ–љ–µ–љ–Є–µ –∞–љ—В–Є–±–Є–Њ—В–Є–Ї–Њ–≤ –Ї–∞–Ї «–Њ–њ—В–Є–Љ–∞–ї—М–љ—Л–є –≤—Л–±–Њ—А –Р–Ь–Я —Б —В–Њ—З–Ї–Є –Ј—А–µ–љ–Є—П —Б–Њ–Њ—В–љ–Њ—И–µ–љ–Є—П —Б—В–Њ–Є–Љ–Њ—Б—В—М/—Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В—М, –Ї–Њ—В–Њ—А—Л–є –Њ–±–µ—Б–њ–µ—З–Є–≤–∞–µ—В –Љ–∞–Ї—Б–Є–Љ–∞–ї—М–љ—Л–є —В–µ—А–∞–њ–µ–≤—В–Є—З–µ—Б–Ї–Є–є —Н—Д—Д–µ–Ї—В, –Є –Љ–Є–љ–Є–Љ–∞–ї—М–љ—Л–µ —В–Њ–Ї—Б–Є—З–љ–Њ—Б—В—М, —Б–≤—П–Ј–∞–љ–љ—Г—О —Б –њ—А–Є–Љ–µ–љ–µ–љ–Є–µ–Љ –Ы–°, –Є —А–∞–Ј–≤–Є—В–Є–µ –∞–љ—В–Є–Љ–Є–Ї—А–Њ–±–љ–Њ–є —А–µ–Ј–Є—Б—В–µ–љ—В–љ–Њ—Б—В–Є [9]».
–°–ї–µ–і—Г–µ—В –Њ—В–Љ–µ—В–Є—В—М, —З—В–Њ –Є–Љ–µ–љ–љ–Њ –∞–љ—В–Є–±–Є–Њ—В–Є–Ї–Є —П–≤–ї—П—О—В—Б—П –њ—А–∞–Ї—В–Є—З–µ—Б–Ї–Є –µ–і–Є–љ—Б—В–≤–µ–љ–љ–Њ–є –≥—А—Г–њ–њ–Њ–є –Ы–°, –Ї–Њ—В–Њ—А–∞—П –њ–Њ—З—В–Є –≤ 50% —Б–ї—Г—З–∞–µ–≤ –њ—А–Є–Љ–µ–љ—П–µ—В—Б—П –љ–µ—А–∞—Ж–Є–Њ–љ–∞–ї—М–љ–Њ –Є –љ–µ–Њ–±–Њ—Б–љ–Њ–≤–∞–љ–љ–Њ [7]. –Х—Й–µ –≤ 1970 –≥. –Ш.–Р. –Ъ–∞—Б—Б–Є—А—Б–Ї–Є–є –њ–Є—Б–∞–ї –Њ –њ—А–Њ–±–ї–µ–Љ–µ —А–µ–Ј–Є—Б—В–µ–љ—В–љ–Њ—Б—В–Є –Љ–Є–Ї—А–Њ–Њ—А–≥–∞–љ–Є–Ј–Љ–Њ–≤: «…–Р–љ—В–Є–±–Є–Њ—В–Є–Ї–Є –њ—А–Њ–і–Њ–ї–ґ–∞—О—В –і–µ–є—Б—В–≤–Њ–≤–∞—В—М. –І–∞—Й–µ –≤—Б–µ–≥–Њ –≤ —А–µ–Ј–Є—Б—В–µ–љ—В–љ–Њ—Б—В–Є –≤–Є–љ–Њ–≤–∞—В—Л –±–Њ–ї—М–љ—Л–µ –Є–ї–Є –≤—А–∞—З–Є – –љ–∞–і–Њ —Г–Љ–µ—В—М –њ—А–Є–Љ–µ–љ—П—В—М –∞–љ—В–Є–±–Є–Њ—В–Є–Ї–Є…» [11].
–Ф–µ–є—Б—В–≤–Є—В–µ–ї—М–љ–Њ, –љ–µ—А–∞—Ж–Є–Њ–љ–∞–ї—М–љ–Њ–µ –Є –љ–µ–Њ–±–Њ—Б–љ–Њ–≤–∞–љ–љ–Њ–µ –љ–∞–Ј–љ–∞—З–µ–љ–Є–µ –Р–Ь–Я –Љ–Њ–ґ–µ—В –Є—Б—Е–Њ–і–Є—В—М –Њ—В —Б–∞–Љ–Є—Е –њ–∞—Ж–Є–µ–љ—В–Њ–≤, –Ї–Њ–≥–і–∞ –Њ–љ–Є –њ—А–Є–Љ–µ–љ—П—О—В –∞–љ—В–Є–±–Є–Њ—В–Є–Ї–Є —Г —Б–µ–±—П, —Б–≤–Њ–Є—Е –і–µ—В–µ–є –Є–ї–Є —А–Њ–і—Б—В–≤–µ–љ–љ–Є–Ї–Њ–≤ —Б–∞–Љ–Њ—Б—В–Њ—П—В–µ–ї—М–љ–Њ, –±–µ–Ј –њ—А–µ–і—И–µ—Б—В–≤—Г—О—Й–µ–є –≤—А–∞—З–µ–±–љ–Њ–є –Ї–Њ–љ—Б—Г–ї—М—В–∞—Ж–Є–Є. –Э–µ—А–µ–і–Ї–Њ –≤ —В–∞–Ї–Є—Е —Б–ї—Г—З–∞—П—Е –њ–∞—Ж–Є–µ–љ—В—Л –Ї–Њ–њ–Є—А—Г—О—В –≤—А–∞—З–µ–±–љ—Г—О —В–∞–Ї—В–Є–Ї—Г –Є –њ—А–Є–Љ–µ–љ—П—О—В –Р–Ь–Я –њ–Њ —В–µ–Љ –ґ–µ –њ–Њ–Ї–∞–Ј–∞–љ–Є—П–Љ, –њ–Њ –Ї–Њ—В–Њ—А—Л–Љ –Є—Е —А–∞–љ–µ–µ –љ–∞–Ј–љ–∞—З–∞–ї –≤—А–∞—З. –Я–∞—Ж–Є–µ–љ—В—Л –≤ –±–Њ–ї—М—И–Є–љ—Б—В–≤–µ —Б–ї—Г—З–∞–µ–≤ –Є—Б–њ–Њ–ї—М–Ј—Г—О—В —Б–∞–Љ–Њ–ї–µ—З–µ–љ–Є–µ –∞–љ—В–Є–±–Є–Њ—В–Є–Ї–∞–Љ–Є –њ—А–Є —Б–Њ—Б—В–Њ—П–љ–Є—П—Е, –љ–µ —В—А–µ–±—Г—О—Й–Є—Е –Є—Е –њ—А–Є–Љ–µ–љ–µ–љ–Є—П, –∞ –Є–Љ–µ–љ–љ–Њ –њ—А–Є –Њ—Б—В—А—Л—Е —А–µ—Б–њ–Є—А–∞—В–Њ—А–љ—Л—Е –Є–љ—Д–µ–Ї—Ж–Є—П—Е, –Ї–Њ—В–Њ—А—Л–µ —З–∞—Й–µ –≤—Б–µ–≥–Њ –Є–Љ–µ—О—В –≤–Є—А—Г—Б–љ—Г—О —Н—В–Є–Њ–ї–Њ–≥–Є—О, –њ—А–Є –Ї–∞—И–ї–µ, —А–∞—Б—Б—В—А–Њ–є—Б—В–≤–µ –Ї–Є—И–µ—З–љ–Є–Ї–∞, –≤ –Ї–∞—З–µ—Б—В–≤–µ –њ—А–Њ—В–Є–≤–Њ–≤–Њ—Б–њ–∞–ї–Є—В–µ–ї—М–љ—Л—Е –Є –ґ–∞—А–Њ–њ–Њ–љ–Є–ґ–∞—О—Й–Є—Е –њ—А–µ–њ–∞—А–∞—В–Њ–≤, –њ—А–Є –±–Њ–ї—П—Е –≤ –≥–Њ—А–ї–µ –Є –ґ–Є–≤–Њ—В–µ –Є —В. –і. [12].
–Э–µ—А–µ–і–Ї–Њ –Р–Ь–Я –њ—А–Є–Љ–µ–љ—П—О—В—Б—П –њ–Њ —Б–Њ–≤–µ—В—Г –њ—А–Њ–≤–Є–Ј–Њ—А–Њ–≤, –Ї–Њ–≥–і–∞ —А–∞–±–Њ—В–љ–Є–Ї–Є –∞–њ—В–µ–Ї –і–∞—О—В —А–µ–Ї–Њ–Љ–µ–љ–і–∞—Ж–Є–Є –њ–Њ –њ—А–Є–Њ–±—А–µ—В–µ–љ–Є—О –љ–µ —В–Њ–ї—М–Ї–Њ –±–µ–Ј—А–µ—Ж–µ–њ—В—Г—А–љ—Л—Е –њ—А–µ–њ–∞—А–∞—В–Њ–≤, –љ–Њ –Є –∞–љ—В–Є–±–Є–Њ—В–Є–Ї–Њ–≤, –Њ—В–љ–Њ—Б—П—Й–Є—Е—Б—П –Ї —Б—В—А–Њ–≥–Њ —А–µ—Ж–µ–њ—В—Г—А–љ—Л–Љ –Ы–° [13]. –≠—В–∞ –њ—А–Њ–±–ї–µ–Љ–∞ –љ–µ —П–≤–ї—П–µ—В—Б—П –Є—Б–Ї–ї—О—З–Є—В–µ–ї—М–љ–Њ —А–Њ—Б—Б–Є–є—Б–Ї–Њ–є. –Т –і—А—Г–≥–Є—Е —Б—В—А–∞–љ–∞—Е –Є–Љ–µ–љ–љ–Њ —Д–∞—А–Љ–∞—Ж–µ–≤—В–Є—З–µ—Б–Ї–Є–µ —А–∞–±–Њ—В–љ–Є–Ї–Є – –Њ–і–Є–љ –Є–Ј –Њ—Б–љ–Њ–≤–љ—Л—Е –Є—Б—В–Њ—З–љ–Є–Ї–Њ–≤ –њ–Њ–ї—Г—З–µ–љ–Є—П –њ–∞—Ж–Є–µ–љ—В–∞–Љ–Є –∞–љ—В–Є–±–Є–Њ—В–Є–Ї–Њ–≤ –±–µ–Ј –љ–∞–Ј–љ–∞—З–µ–љ–Є—П –≤—А–∞—З–∞: 31% —Б–ї—Г—З–∞–µ–≤ –≤ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є –Ь. McKee [14], 41% —Б–ї—Г—З–∞–µ–≤ –≤ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є M.H. Väänänen [16], 53,6% —Б–ї—Г—З–∞–µ–≤ –≤ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є F.A. Sawair [15].
–Э–µ—А–∞—Ж–Є–Њ–љ–∞–ї—М–љ–Њ–µ –Є –љ–µ–Њ–±–Њ—Б–љ–Њ–≤–∞–љ–љ–Њ–µ –љ–∞–Ј–љ–∞—З–µ–љ–Є–µ –Р–Ь–Я –Љ–Њ–ґ–µ—В –Є—Б—Е–Њ–і–Є—В—М –Њ—В –≤—А–∞—З–µ–є –≤ —В–µ—Е —Б–ї—Г—З–∞—П—Е, –Ї–Њ–≥–і–∞ –∞–љ—В–Є–±–Є–Њ—В–Є–Ї–Є –љ–∞–Ј–љ–∞—З–∞—О—В—Б—П –њ—А–Є –Њ—В—Б—Г—В—Б—В–≤–Є–Є –њ–Њ–Ї–∞–Ј–∞–љ–Є–є; –Ї–Њ–≥–і–∞ —Б–Њ—Б—В–Њ—П–љ–Є–µ –њ–∞—Ж–Є–µ–љ—В–∞ —В—А–µ–±—Г–µ—В –љ–∞–Ј–љ–∞—З–µ–љ–Є—П –∞–љ—В–Є–±–∞–Ї—В–µ—А–Є–∞–ї—М–љ–Њ–є —В–µ—А–∞–њ–Є–Є (–Р–С–Ґ), –љ–Њ –љ–µ–њ—А–∞–≤–Є–ї—М–љ–Њ –≤—Л–±–Є—А–∞—О—В—Б—П –њ—А–µ–њ–∞—А–∞—В, —Б–њ–Њ—Б–Њ–± –Є –Ї—А–∞—В–љ–Њ—Б—В—М –≤–≤–µ–і–µ–љ–Є—П, –љ–∞–Ј–љ–∞—З–∞—О—В—Б—П –љ–µ–Ї–Њ—А—А–µ–Ї—В–љ—Л–µ –і–Њ–Ј—Л –Є–ї–Є –і–ї–Є—В–µ–ї—М–љ–Њ—Б—В—М —В–µ—А–∞–њ–Є–Є, –љ–µ —Г—З–Є—В—Л–≤–∞—О—В—Б—П –≤–Њ–Ј–Љ–Њ–ґ–љ—Л–µ –ї–µ–Ї–∞—А—Б—В–≤–µ–љ–љ—Л–µ –≤–Ј–∞–Є–Љ–Њ–і–µ–є—Б—В–≤–Є—П, –љ–µ–њ—А–∞–≤–Є–ї—М–љ–Њ –Њ—Ж–µ–љ–Є–≤–∞–µ—В—Б—П —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В—М —В–µ—А–∞–њ–Є–Є –Є —В. –і. –Э–µ–Љ–∞–ї–Њ–≤–∞–ґ–љ–Њ–µ –Ј–љ–∞—З–µ–љ–Є–µ –Є–Љ–µ–µ—В –Њ—В–љ–Њ—И–µ–љ–Є–µ –љ–∞—Б–µ–ї–µ–љ–Є—П: –≤—А–∞—З –Љ–Њ–ґ–µ—В –≥—А–∞–Љ–Њ—В–љ–Њ –≤—Л–±—А–∞—В—М –Є –њ—А–µ–њ–∞—А–∞—В, –Є –Ї–Њ—А—А–µ–Ї—В–љ—Г—О –і–Њ–Ј—Г, –Є –љ–µ–Њ–±—Е–Њ–і–Є–Љ—Г—О –і–ї–Є—В–µ–ї—М–љ–Њ—Б—В—М —В–µ—А–∞–њ–Є–Є, –љ–Њ –њ–∞—Ж–Є–µ–љ—В—Л –љ–µ —Б–ї–µ–і—Г—О—В —Н—В–Є–Љ –љ–∞–Ј–љ–∞—З–µ–љ–Є—П–Љ –≤—А–∞—З–∞.
–Т–Њ –Љ–љ–Њ–≥–Є—Е —Б–ї—Г—З–∞—П—Е –Њ—И–Є–±–Ї–Є –њ—А–Є –љ–∞–Ј–љ–∞—З–µ–љ–Є–Є –Р–С–Ґ –Њ–±—Г—Б–ї–Њ–≤–ї–µ–љ—Л —А–∞—Б–њ—А–Њ—Б—В—А–∞–љ–µ–љ–љ—Л–Љ–Є —Б—А–µ–і–Є –≤—А–∞—З–µ–є –Љ–Є—Д–∞–Љ–Є –Є –Ј–∞–±–ї—Г–ґ–і–µ–љ–Є—П–Љ–Є –≤ –Њ—В–љ–Њ—И–µ–љ–Є–Є –Р–Ь–Я –≤ —Ж–µ–ї–Њ–Љ.
–Я—А–Є–≤–µ–і–µ–Љ –љ–µ–Ї–Њ—В–Њ—А—Л–µ –љ–∞–Є–±–Њ–ї–µ–µ –њ–Њ–њ—Г–ї—П—А–љ—Л–µ –Ј–∞–±–ї—Г–ґ–і–µ–љ–Є—П –Њ—В–љ–Њ—Б–Є—В–µ–ї—М–љ–Њ –∞–љ—В–Є–±–Є–Њ—В–Є–Ї–Њ–≤.
–Ь–Є—Д 1. –Ф–ї–Є—В–µ–ї—М–љ–Њ—Б—В—М –Р–С —В–µ—А–∞–њ–Є–Є –і–Њ–ї–ґ–љ–∞ —Б–Њ—Б—В–∞–≤–ї—П—В—М –љ–µ –Љ–µ–љ–µ–µ 10–14 –і–љ–µ–є
–°–Њ–≤—А–µ–Љ–µ–љ–љ—Л–є –∞—А—Б–µ–љ–∞–ї –Р–Ь–Я –≤–Ї–ї—О—З–∞–µ—В –њ—А–µ–њ–∞—А–∞—В—Л, –Є—Б–њ–Њ–ї—М–Ј—Г–µ–Љ—Л–µ –Ї–Њ—А–Њ—В–Ї–Є–Љ–Є –Ї—Г—А—Б–∞–Љ–Є –Є –і–∞–ґ–µ –Њ–і–љ–Њ–Ї—А–∞—В–љ–Њ (3–5-–і–љ–µ–≤–љ—Л–µ –Ї—Г—А—Б—Л –∞–Ј–Є—В—А–Њ–Љ–Є—Ж–Є–љ–∞ –њ—А–Є –≤–љ–µ–±–Њ–ї—М–љ–Є—З–љ—Л—Е –Є–љ—Д–µ–Ї—Ж–Є—П—Е –і—Л—Е–∞—В–µ–ї—М–љ—Л—Е –њ—Г—В–µ–є, –∞ –Є–Љ–µ–љ–љ–Њ –њ—А–Є –Њ—Б—В—А–Њ–Љ —Б—В—А–µ–њ—В–Њ–Ї–Њ–Ї–Ї–Њ–≤–Њ–Љ —В–Њ–љ–Ј–Є–ї–ї–Њ—Д–∞—А–Є–љ–≥–Є—В–µ [17–19], –Њ—Б—В—А–Њ–Љ —Б—А–µ–і–љ–µ–Љ –Њ—В–Є—В–µ [20, 21], –Њ—Б—В—А–Њ–Љ –±–∞–Ї—В–µ—А–Є–∞–ї—М–љ–Њ–Љ —А–Є–љ–Њ—Б–Є–љ—Г—Б–Є—В–µ [23–25], –≤–љ–µ–±–Њ–ї—М–љ–Є—З–љ–Њ–є –њ–љ–µ–≤–Љ–Њ–љ–Є–Є [26–28]; –Њ–і–љ–Њ–Ї—А–∞—В–љ–Њ–µ –њ—А–Є–Љ–µ–љ–µ–љ–Є–µ —Д–Њ—Б—Д–Њ–Љ–Є—Ж–Є–љ–∞ —В—А–Њ–Љ–µ—В–∞–Љ–Њ–ї–∞ –Є–ї–Є –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є–µ —Д—В–Њ—А—Е–Є–љ–Њ–ї–Њ–љ–Њ–≤ –≤ —В–µ—З–µ–љ–Є–µ 3-—Е –і–љ–µ–є –њ—А–Є –ї–µ—З–µ–љ–Є–Є –Њ—Б—В—А–Њ–≥–Њ –љ–µ–Њ—Б–ї–Њ–ґ–љ–µ–љ–љ–Њ–≥–Њ —Ж–Є—Б—В–Є—В–∞ [32], –Њ–і–љ–Њ–Ї—А–∞—В–љ–Њ–µ –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є–µ –∞–Ј–Є—В—А–Њ–Љ–Є—Ж–Є–љ–∞ –і–ї—П –ї–µ—З–µ–љ–Є—П –љ–µ–Њ—Б–ї–Њ–ґ–љ–µ–љ–љ–Њ–є —Е–ї–∞–Љ–Є–і–Є–є–љ–Њ–є –Є–љ—Д–µ–Ї—Ж–Є–Є [33–35], –∞–Ј–Є—В—А–Њ–Љ–Є—Ж–Є–љ–∞ –Є–ї–Є —Ж–µ—Д—В—А–Є–∞–Ї—Б–Њ–љ–∞ –њ—А–Є –љ–µ–Њ—Б–ї–Њ–ґ–љ–µ–љ–љ–Њ–є –≥–Њ–љ–Њ—А–µ–µ [36], –Ї–Њ—А–Њ—В–Ї–Є–µ (1–3 –і–љ—П) –Ї—Г—А—Б—Л —Ж–µ—Д—В—А–Є–∞–Ї—Б–Њ–љ–∞ –њ—А–Є –Њ—Б—В—А–Њ–Љ —Б—А–µ–і–љ–µ–Љ –Њ—В–Є—В–µ [37] –Є —В. –і.).
–Т —В–Њ –ґ–µ –≤—А–µ–Љ—П —Б—Г—Й–µ—Б—В–≤—Г—О—В –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П –Є —Б–Њ—Б—В–Њ—П–љ–Є—П, –њ—А–Є –Ї–Њ—В–Њ—А—Л—Е –і–ї–Є—В–µ–ї—М–љ–Њ—Б—В—М –Р–С–Ґ –Ј–љ–∞—З–Є—В–µ–ї—М–љ–Њ –њ—А–µ–≤—Л—И–∞–µ—В —Б—В–∞–љ–і–∞—А—В–љ—Л–µ 10–14 –і–љ–µ–є –Є –Љ–Њ–ґ–µ—В —Б–Њ—Б—В–∞–≤–ї—П—В—М –љ–µ—Б–Ї–Њ–ї—М–Ї–Њ –љ–µ–і–µ–ї—М –Є –і–∞–ґ–µ –Љ–µ—Б—П—Ж–µ–≤: –љ–∞–њ—А–Є–Љ–µ—А, —В—Г–±–µ—А–Ї—Г–ї–µ–Ј, —Е—А–Њ–љ–Є—З–µ—Б–Ї–Є–є –Њ—Б—В–µ–Њ–Љ–Є–µ–ї–Є—В, —Е—А–Њ–љ–Є—З–µ—Б–Ї–Є–є –њ—А–Њ—Б—В–∞—В–Є—В, –≥–љ–Њ–є–љ—Л–є –њ–µ—А–Є–Ї–∞—А–і–Є—В, –±–∞–Ї—В–µ—А–Є–∞–ї—М–љ—Л–є —Н–љ–і–Њ–Ї–∞—А–і–Є—В –Є –і—А. [38].
–Э–µ —Б–ї–µ–і—Г–µ—В –њ—А–Њ–і–Њ–ї–ґ–∞—В—М –Ї—Г—А—Б –Р–С —В–µ—А–∞–њ–Є–Є –і–Њ –њ–Њ–ї–љ–Њ–≥–Њ –Ї—Г–њ–Є—А–Њ–≤–∞–љ–Є—П —Б–Є–Љ–њ—В–Њ–Љ–Њ–≤ –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П, –љ–Њ—А–Љ–∞–ї–Є–Ј–∞—Ж–Є–Є —Б–Ї–Њ—А–Њ—Б—В–Є –Њ—Б–µ–і–∞–љ–Є—П —Н—А–Є—В—А–Њ—Ж–Є—В–Њ–≤ (–°–Ю–≠), —А–µ–љ—В–≥–µ–љ–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Њ–є –Ї–∞—А—В–Є–љ—Л, –Ј–∞–ґ–Є–≤–ї–µ–љ–Є—П —А–∞–љ—Л –Є —В. –і. –Э–∞–њ—А–Є–Љ–µ—А, –њ—А–Є –Њ—Б—В—А–Њ–Љ –љ–µ–Њ—Б–ї–Њ–ґ–љ–µ–љ–љ–Њ–Љ —Ж–Є—Б—В–Є—В–µ –ї–µ–є–Ї–Њ—Ж–Є—В—Г—А–Є—П –Є –і–Є–Ј—Г—А–Є—П —Б–Њ—Е—А–∞–љ—П—О—В—Б—П –љ–∞ 3-–є –і–µ–љ—М –ї–µ—З–µ–љ–Є—П –љ–Њ—А—Д–ї–Њ–Ї—Б–∞—Ж–Є–љ–Њ–Љ —Г 78 –Є 52,5% –њ–∞—Ж–Є–µ–љ—В–Њ–Ї —Б–Њ–Њ—В–≤–µ—В—Б—В–≤–µ–љ–љ–Њ. –Ю–і–љ–∞–Ї–Њ —Н—В–Њ –љ–µ —П–≤–ї—П–µ—В—Б—П –њ–Њ–Ї–∞–Ј–∞–љ–Є–µ–Љ –і–ї—П –љ–∞–Ј–љ–∞—З–µ–љ–Є—П –±–Њ–ї–µ–µ –і–ї–Є—В–µ–ї—М–љ–Њ–≥–Њ –Ї—Г—А—Б–∞ –Р–Ь–Я, –њ–Њ—Б–Ї–Њ–ї—М–Ї—Г –Њ—Б–љ–Њ–≤–љ–Њ–є –Ї—А–Є—В–µ—А–Є–є —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В–Є –ї–µ—З–µ–љ–Є—П – –±–∞–Ї—В–µ—А–Є—Г—А–Є—П –Ї—Г–њ–Є—А—Г–µ—В—Б—П –Ї —Н—В–Њ–Љ—Г –≤—А–µ–Љ–µ–љ–Є —Г 94% –њ–∞—Ж–Є–µ–љ—В–Њ–Ї [39]. –°–Ю–≠ –≤–Њ–Њ–±—Й–µ —П–≤–ї—П–µ—В—Б—П –љ–µ—Б–њ–µ—Ж–Є—Д–Є—З–µ—Б–Ї–Є–Љ –њ–Њ–Ї–∞–Ј–∞—В–µ–ї–µ–Љ, –љ–µ –њ–Њ–Ј–≤–Њ–ї—П—О—Й–Є–Љ –Њ—Ж–µ–љ–Є–≤–∞—В—М –љ–∞–ї–Є—З–Є–µ, –≤—Л—А–∞–ґ–µ–љ–љ–Њ—Б—В—М –Є –і–Є–љ–∞–Љ–Є–Ї—Г –Є–љ—Д–µ–Ї—Ж–Є–Њ–љ–љ–Њ–≥–Њ –њ—А–Њ—Ж–µ—Б—Б–∞ [40]. –Я—А–Є –≤–љ–µ–±–Њ–ї—М–љ–Є—З–љ–Њ–є –њ–љ–µ–≤–Љ–Њ–љ–Є–Є —Б—Г–±—Д–µ–±—А–Є–ї—М–љ–∞—П —В–µ–Љ–њ–µ—А–∞—В—Г—А–∞ (37,0–37,5°–°) –њ—А–Є –Њ—В—Б—Г—В—Б—В–≤–Є–Є –і—А—Г–≥–Є—Е –њ—А–Є–Ј–љ–∞–Ї–Њ–≤ –±–∞–Ї—В–µ—А–Є–∞–ї—М–љ–Њ–є –Є–љ—Д–µ–Ї—Ж–Є–Є –Љ–Њ–ґ–µ—В –±—Л—В—М –њ—А–Њ—П–≤–ї–µ–љ–Є–µ–Љ –љ–µ–Є–љ—Д–µ–Ї—Ж–Є–Њ–љ–љ–Њ–≥–Њ –≤–Њ—Б–њ–∞–ї–µ–љ–Є—П –Є–ї–Є –њ–Њ—Б—В–Є–љ—Д–µ–Ї—Ж–Є–Њ–љ–љ–Њ–є –∞—Б—В–µ–љ–Є–Є (–≤–µ–≥–µ—В–∞—В–Є–≤–љ–Њ–є –і–Є—Б—Д—Г–љ–Ї—Ж–Є–Є) –Є –љ–µ —П–≤–ї—П–µ—В—Б—П –њ–Њ–Ї–∞–Ј–∞–љ–Є–µ–Љ –і–ї—П –њ—А–Њ–і–Њ–ї–ґ–µ–љ–Є—П –Р–С–Ґ –Є–ї–Є –Ј–∞–Љ–µ–љ—Л –Р–Ь–Я [31]. –Ю—Б—В–∞—В–Њ—З–љ—Л–µ –Є–Ј–Љ–µ–љ–µ–љ–Є—П –љ–∞ —А–µ–љ—В–≥–µ–љ–Њ–≥—А–∞–Љ–Љ–µ –Љ–Њ–≥—Г—В —Б–Њ—Е—А–∞–љ—П—В—М—Б—П –≤ —В–µ—З–µ–љ–Є–µ 1–2 –Љ–µ—Б., —Е—А–Є–њ—Л –њ—А–Є –∞—Г—Б–Ї—Г–ї—М—В–∞—Ж–Є–Є – –≤ —В–µ—З–µ–љ–Є–µ 3–4 –љ–µ–і., —Б—Г—Е–Њ–є –Ї–∞—И–µ–ї—М, –Њ—Б–Њ–±–µ–љ–љ–Њ —Г –Ї—Г—А—П—Й–Є—Е, –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б —Е—А–Њ–љ–Є—З–µ—Б–Ї–Њ–є –Њ–±—Б—В—А—Г–Ї—В–Є–≤–љ–Њ–є –±–Њ–ї–µ–Ј–љ—М—О –ї–µ–≥–Ї–Є—Е (–•–Ю–С–Ы) – –≤ —В–µ—З–µ–љ–Є–µ 1–2 –Љ–µ—Б. [31].
–Ь–Є—Д 2. –Р–Ь–Я –љ–µ–Њ–±—Е–Њ–і–Є–Љ–Њ –Љ–µ–љ—П—В—М –Ї–∞–ґ–і—Л–µ 5–7 –і–љ–µ–є, —З—В–Њ–±—Л —Г –≤–Њ–Ј–±—Г–і–Є—В–µ–ї—П –љ–µ –≤–Њ–Ј–љ–Є–Ї–ї–∞ —А–µ–Ј–Є—Б—В–µ–љ—В–љ–Њ—Б—В—М
–Я–Њ—П–≤–ї–µ–љ–Є–µ –Є —А–∞—Б–њ—А–Њ—Б—В—А–∞–љ–µ–љ–Є–µ —Г—Б—В–Њ–є—З–Є–≤–Њ—Б—В–Є –Љ–Є–Ї—А–Њ–Њ—А–≥–∞–љ–Є–Ј–Љ–Њ–≤ –Ї –∞–љ—В–Є–±–Є–Њ—В–Є–Ї–∞–Љ – –∞–љ—В–Є–±–Є–Њ—В–Є–Ї–Њ—А–µ–Ј–Є—Б—В–µ–љ—В–љ–Њ—Б—В–Є –і–µ–є—Б—В–≤–Є—В–µ–ї—М–љ–Њ –њ—А–µ–і—Б—В–∞–≤–ї—П–µ—В —Б–Њ–±–Њ–є —Б–µ—А—М–µ–Ј–љ—Г—О –њ—А–Њ–±–ї–µ–Љ—Г –і–ї—П –њ—А–Њ–≤–µ–і–µ–љ–Є—П —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ–є –Р–С–Ґ. –Ю—Ж–µ–љ–Ї—Г –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Њ–є —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В–Є –ї–µ—З–µ–љ–Є—П —Б–ї–µ–і—Г–µ—В –њ—А–Њ–≤–Њ–і–Є—В—М —З–µ—А–µ–Ј 48–72 —З –њ–Њ—Б–ї–µ –љ–∞–Ј–љ–∞—З–µ–љ–Є—П –Р–Ь–Я [31, 38], –Є –њ—А–Є –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Њ–є –љ–µ—Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В–Є –љ–µ–Ј–∞–Љ–µ–і–ї–Є—В–µ–ї—М–љ–Њ –Љ–µ–љ—П—В—М –∞–љ—В–Є–±–Є–Њ—В–Є–Ї, –љ–µ –і–Њ–ґ–Є–і–∞—П—Б—М 5–7-–≥–Њ –і–љ—П —В–µ—А–∞–њ–Є–Є. –Х—Б–ї–Є –њ—А–µ–њ–∞—А–∞—В —Н—Д—Д–µ–Ї—В–Є–≤–µ–љ, —В–Њ –≤ –Ј–∞–Љ–µ–љ–µ –µ–≥–Њ –љ–∞ 5–7-–є –і–µ–љ—М –љ–µ—В –љ–µ–Њ–±—Е–Њ–і–Є–Љ–Њ—Б—В–Є, –∞ –њ—А–Є —В–∞–Ї–Њ–є —Б–Љ–µ–љ–µ –Р–Ь–Я –Є–ї–Є –љ–µ–Ј–∞–≤–µ—А—И–µ–љ–љ–Њ–Љ –Ї—Г—А—Б–µ –Р–С–Ґ –Ї–∞–Ї —А–∞–Ј –Є –њ–Њ–≤—Л—И–∞–µ—В—Б—П —А–Є—Б–Ї —Д–Њ—А–Љ–Є—А–Њ–≤–∞–љ–Є—П –∞–љ—В–Є–±–Є–Њ—В–Є–Ї–Њ—А–µ–Ј–Є—Б—В–µ–љ—В–љ–Њ—Б—В–Є —Г –Љ–Є–Ї—А–Њ–Њ—А–≥–∞–љ–Є–Ј–Љ–Њ–≤ [41]. –Э–µ—Б–Њ–Љ–љ–µ–љ–љ–Њ, —Б—Г—Й–µ—Б—В–≤—Г—О—В –Є –і—А—Г–≥–Є–µ –њ–Њ–Ї–∞–Ј–∞–љ–Є—П –і–ї—П –Ј–∞–Љ–µ–љ—Л –Р–Ь–Я –і–∞–ґ–µ –љ–∞ —Д–Њ–љ–µ —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ–є —В–µ—А–∞–њ–Є–Є, –љ–∞–њ—А–Є–Љ–µ—А, —А–∞–Ј–≤–Є—В–Є–µ —В—П–ґ–µ–ї—Л—Е –љ–µ–ґ–µ–ї–∞—В–µ–ї—М–љ—Л—Е –ї–µ–Ї–∞—А—Б—В–≤–µ–љ–љ—Л—Е —А–µ–∞–Ї—Ж–Є–є, —В—А–µ–±—Г—О—Й–Є—Е –Њ—В–Љ–µ–љ—Л –њ—А–µ–њ–∞—А–∞—В–∞, –ї–Є–±–Њ –≤—Л—Б–Њ–Ї–∞—П –њ–Њ—В–µ–љ—Ж–Є–∞–ї—М–љ–∞—П —В–Њ–Ї—Б–Є—З–љ–Њ—Б—В—М –∞–љ—В–Є–±–Є–Њ—В–Є–Ї–∞, –Њ–≥—А–∞–љ–Є—З–Є–≤–∞—О—Й–∞—П –і–ї–Є—В–µ–ї—М–љ–Њ—Б—В—М –µ–≥–Њ –њ—А–Є–Љ–µ–љ–µ–љ–Є—П, –Њ–і–љ–∞–Ї–Њ –і–∞–љ–љ—Л–µ —Б–Є—В—Г–∞—Ж–Є–Є –≤–Њ–Ј–љ–Є–Ї–∞—О—В –≤ –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Њ–є –њ—А–∞–Ї—В–Є–Ї–µ —А–µ–і–Ї–Њ –Є —П–≤–ї—П—О—В—Б—П —Б–Ї–Њ—А–µ–µ –Є—Б–Ї–ї—О—З–µ–љ–Є–µ–Љ, —З–µ–Љ –њ—А–∞–≤–Є–ї–Њ–Љ.
–Ь–Є—Д 3. –Х—Б—В—М —Б–Є–ї—М–љ—Л–µ –Є —Б–ї–∞–±—Л–µ –∞–љ—В–Є–±–Є–Њ—В–Є–Ї–Є
–Ь–љ–Њ–≥–Є–µ –≤—А–∞—З–Є –њ–Њ–ї–∞–≥–∞—О—В, —З—В–Њ –±–µ—Б–њ–Њ–ї–µ–Ј–љ–Њ –њ—А–Є–Љ–µ–љ—П—В—М –њ–µ–љ–Є—Ж–Є–ї–ї–Є–љ—Л, –њ–Њ—Б–Ї–Њ–ї—М–Ї—Г —Н—В–Њ «—Г—Б—В–∞—А–µ–≤—И–Є–µ» –Є «—Б–ї–∞–±—Л–µ» –Р–Ь–Я, –Ї –Ї–Њ—В–Њ—А—Л–Љ –Ј–∞ 60 –ї–µ—В –≤—Б–µ –Љ–Є–Ї—А–Њ–Њ—А–≥–∞–љ–Є–Ј–Љ—Л —Б—В–∞–ї–Є —Г—Б—В–Њ–є—З–Є–≤—Л–Љ–Є. –Э–µ—Б–Њ–Љ–љ–µ–љ–љ–Њ, –њ—А–Њ–±–ї–µ–Љ–∞ –∞–љ—В–Є–±–Є–Њ—В–Є–Ї–Њ—А–µ–Ј–Є—Б—В–µ–љ—В–љ–Њ—Б—В–Є –Њ—З–µ–љ—М –∞–Ї—В—Г–∞–ї—М–љ–∞ –Ї–∞–Ї –і–ї—П –†–Њ—Б—Б–Є–Є, —В–∞–Ї –Є –і–ї—П –≤—Б–µ–≥–Њ –Љ–Є—А–∞. –Т —В–Њ –ґ–µ –≤—А–µ–Љ—П β-–≥–µ–Љ–Њ–ї–Є—В–Є—З–µ—Б–Ї–Є–є —Б—В—А–µ–њ—В–Њ–Ї–Њ–Ї–Ї –≥—А—Г–њ–њ—Л –Р (–С–У–°–Р) Streptococcus (S.) pyogenes – –≤–Њ–Ј–±—Г–і–Є—В–µ–ї—М —В–Њ–љ–Ј–Є–ї–ї–Њ—Д–∞—А–Є–љ–≥–Є—В–∞, —Б–Ї–∞—А–ї–∞—В–Є–љ—Л, —А–Њ–ґ–Є—Б—В–Њ–≥–Њ –≤–Њ—Б–њ–∞–ї–µ–љ–Є—П, —Б—В—А–µ–њ—В–Њ–і–µ—А–Љ–Є–є –Њ—В–ї–Є—З–∞–µ—В—Б—П –≤—Л—Б–Њ–Ї–Њ–є —З—Г–≤—Б—В–≤–Є—В–µ–ї—М–љ–Њ—Б—В—М—О –Ї β-–ї–∞–Ї—В–∞–Љ–∞–Љ (–њ–µ–љ–Є—Ж–Є–ї–ї–Є–љ–∞–Љ –Є —Ж–µ—Д–∞–ї–Њ—Б–њ–Њ—А–Є–љ–∞–Љ). –≠—В–Є –∞–љ—В–Є–±–Є–Њ—В–Є–Ї–Є –Њ—Б—В–∞—О—В—Б—П –µ–і–Є–љ—Б—В–≤–µ–љ–љ—Л–Љ –Ї–ї–∞—Б—Б–Њ–Љ –Р–Ь–Я, –Ї –Ї–Њ—В–Њ—А—Л–Љ —Г S. pyogenes –љ–µ –њ–Њ—П–≤–Є–ї–∞—Б—М —А–µ–Ј–Є—Б—В–µ–љ—В–љ–Њ—Б—В—М. –Ш—Б—Е–Њ–і—П –Є–Ј —Н—В–Њ–≥–Њ –≤—Б–µ —А—Г–Ї–Њ–≤–Њ–і—Б—В–≤–∞ –њ–Њ –ї–µ—З–µ–љ–Є—О –Њ—Б—В—А–Њ–≥–Њ —Б—В—А–µ–њ—В–Њ–Ї–Њ–Ї–Ї–Њ–≤–Њ–≥–Њ —В–Њ–љ–Ј–Є–ї–ї–Њ—Д–∞—А–Є–љ–≥–Є—В–∞ –≤ –Ї–∞—З–µ—Б—В–≤–µ «–Ј–Њ–ї–Њ—В–Њ–≥–Њ —Б—В–∞–љ–і–∞—А—В–∞» —А–µ–Ї–Њ–Љ–µ–љ–і—Г—О—В –њ–µ–љ–Є—Ж–Є–ї–ї–Є–љ—Л (—Д–µ–љ–Њ–Ї—Б–Є–Љ–µ—В–Є–ї–њ–µ–љ–Є—Ж–Є–ї–ї–Є–љ –Є–ї–Є –∞–Љ–Њ–Ї—Б–Є—Ж–Є–ї–ї–Є–љ) [18, 19, 42, 43].
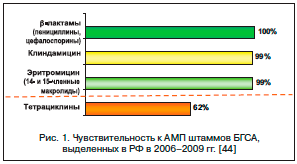
–Я–Њ –і–∞–љ–љ—Л–Љ –Љ–љ–Њ–≥–Њ—Ж–µ–љ—В—А–Њ–≤–Њ–≥–Њ –њ—А–Њ—Б–њ–µ–Ї—В–Є–≤–љ–Њ–≥–Њ –Љ–Є–Ї—А–Њ–±–Є–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Њ–≥–Њ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П –Я–µ–У–Р–° «–Ь–Њ–љ–Є—В–Њ—А–Є–љ–≥ –∞–љ—В–Є–±–Є–Њ—В–Є–Ї–Њ—А–µ–Ј–Є—Б—В–µ–љ—В–љ–Њ—Б—В–Є –њ–љ–µ–≤–Љ–Њ–Ї–Њ–Ї–Ї–Њ–≤, –≥–µ–Љ–Њ—Д–Є–ї –Є –њ–Є–Њ–≥–µ–љ–љ—Л—Е —Б—В—А–µ–њ—В–Њ–Ї–Њ–Ї–Ї–Њ–≤ –≤ —А–∞–Ј–ї–Є—З–љ—Л—Е —А–µ–≥–Є–Њ–љ–∞—Е –†–Њ—Б—Б–Є–Є» –Ј–∞ –њ–µ—А–Є–Њ–і —Б 1999 –њ–Њ 2009 –≥. [44], –≤—Б–µ —И—В–∞–Љ–Љ—Л –С–У–°–Р –Њ–±–ї–∞–і–∞–ї–Є –≤—Л—Б–Њ–Ї–Њ–є —З—Г–≤—Б—В–≤–Є—В–µ–ї—М–љ–Њ—Б—В—М—О –Ї –њ–µ–љ–Є—Ж–Є–ї–ї–Є–љ—Г. –Т —В–Њ –ґ–µ –≤—А–µ–Љ—П –љ–∞ –њ—А–Њ—В—П–ґ–µ–љ–Є–Є –≤—Б–µ–≥–Њ —Н—В–Њ–≥–Њ 10-–ї–µ—В–љ–µ–≥–Њ –њ–µ—А–Є–Њ–і–∞ —Б–Њ—Е—А–∞–љ—П–ї—Б—П –≤—Л—Б–Њ–Ї–Є–є —Г—А–Њ–≤–µ–љ—М —А–µ–Ј–Є—Б—В–µ–љ—В–љ–Њ—Б—В–Є S. pyogenes –Ї —В–µ—В—А–∞—Ж–Є–Ї–ї–Є–љ—Г (45,8% –≤ 1999–2003 –≥–≥. –Є 33,9% –≤ 2007–2009 –≥–≥.) (—А–Є—Б. 1).
–Ъ—А–∞–є–љ–µ –≤–∞–ґ–љ–Њ —Г—З–Є—В—Л–≤–∞—В—М —А–µ–≥–Є–Њ–љ–∞–ї—М–љ—Л–µ –і–∞–љ–љ—Л–µ –њ–Њ –∞–љ—В–Є–±–Є–Њ—В–Є–Ї–Њ—А–µ–Ј–Є—Б—В–µ–љ—В–љ–Њ—Б—В–Є —А–∞–Ј–ї–Є—З–љ—Л—Е –≤–Њ–Ј–±—Г–і–Є—В–µ–ї–µ–є. –Ґ–∞–Ї, –≤ –Х–≤—А–Њ–њ–µ –≤–µ—Б—М–Љ–∞ –∞–Ї—В—Г–∞–ї—М–љ–∞ –њ—А–Њ–±–ї–µ–Љ–∞ —А–µ–Ј–Є—Б—В–µ–љ—В–љ–Њ—Б—В–Є –њ–љ–µ–≤–Љ–Њ–Ї–Њ–Ї–Ї–Њ–≤ (S. pneumoniae) –Ї –њ–µ–љ–Є—Ж–Є–ї–ї–Є–љ—Г, –Ї–Њ—В–Њ—А–∞—П, –њ–Њ –і–∞–љ–љ—Л–Љ –Х–≤—А–Њ–њ–µ–є—Б–Ї–Њ–є —Б–Є—Б—В–µ–Љ—Л –њ–Њ –љ–∞–і–Ј–Њ—А—Г –Ј–∞ –∞–љ—В–Є–Љ–Є–Ї—А–Њ–±–љ–Њ–є —А–µ–Ј–Є—Б—В–µ–љ—В–љ–Њ—Б—В—М—О (European Antimicrobial Resistance Surveillance System – EARSS), –≤ 2012 –≥. –≤ 9 –Є–Ј 29 —Б—В—А–∞–љ – —Г—З–∞—Б—В–љ–Є—Ж –і–∞–љ–љ–Њ–є —Б–Є—Б—В–µ–Љ—Л –Љ–Њ–љ–Є—В–Њ—А–Є–љ–≥–∞ –≤–∞—А—М–Є—А–Њ–≤–∞–ї–∞ –Њ—В 10 –і–Њ 25%, –∞ –≤ 4 —Б—В—А–∞–љ–∞—Е —Б–Њ—Б—В–∞–≤–ї—П–ї–∞ 25–50% [45]. –Т —В–Њ –ґ–µ –≤—А–µ–Љ—П, —Б–Њ–≥–ї–∞—Б–љ–Њ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—О –Я–µ–У–Р–°-III, –њ—А–Њ–≤–µ–і–µ–љ–љ–Њ–Љ—Г –≤ 2006–2009 –≥–≥., —Б—А–µ–і–Є —И—В–∞–Љ–Љ–Њ–≤ –њ–љ–µ–≤–Љ–Њ–Ї–Њ–Ї–Ї–∞, –≤—Л–і–µ–ї–µ–љ–љ—Л—Е –љ–∞ —В–µ—А—А–Є—В–Њ—А–Є–Є –†–§ –Ј–∞ —Г–Ї–∞–Ј–∞–љ–љ—Л–є –њ–µ—А–Є–Њ–і, –Є–Ј–Њ–ї—П—В—Л —Б –њ—А–Њ–Љ–µ–ґ—Г—В–Њ—З–љ—Л–Љ —Г—А–Њ–≤–љ–µ–Љ —А–µ–Ј–Є—Б—В–µ–љ—В–љ–Њ—Б—В–Є –Ї –њ–µ–љ–Є—Ж–Є–ї–ї–Є–љ—Г —Б–Њ—Б—В–∞–≤–Є–ї–Є 9,1%, –∞ —Б –≤—Л—Б–Њ–Ї–Є–Љ —Г—А–Њ–≤–љ–µ–Љ – 2,1%, —В. –µ. –Њ–±—Й–∞—П –і–Њ–ї—П –љ–µ—З—Г–≤—Б—В–≤–Є—В–µ–ї—М–љ—Л—Е —И—В–∞–Љ–Љ–Њ–≤ –і–Њ—Б—В–Є–≥–ї–∞ 11,2% (—А–Є—Б. 2) [46].
–Ґ–∞–Ї–Є–Љ –Њ–±—А–∞–Ј–Њ–Љ, –њ–µ–љ–Є—Ж–Є–ї–ї–Є–љ—Л –Є –∞–Љ–Є–љ–Њ–њ–µ–љ–Є—Ж–Є–ї–ї–Є–љ—Л (–њ–µ–љ–Є—Ж–Є–ї–ї–Є–љ, –∞–Љ–Њ–Ї—Б–Є—Ж–Є–ї–ї–Є–љ, –∞–Љ–Њ–Ї—Б–Є—Ж–Є–ї–ї–Є–љ/–Ї–ї–∞–≤—Г–ї–∞–љ–∞—В) —Б–Њ—Е—А–∞–љ—П—О—В –∞–Ї—В–Є–≤–љ–Њ—Б—В—М –≤ –Њ—В–љ–Њ—И–µ–љ–Є–Є S. pneumoniae –Є –љ–µ —Г—В—А–∞—В–Є–ї–Є —Б–≤–Њ–µ–≥–Њ –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Њ–≥–Њ –Ј–љ–∞—З–µ–љ–Є—П.
–Э–µ–Њ–±—Е–Њ–і–Є–Љ–Њ –њ–Њ–Љ–љ–Є—В—М, —З—В–Њ –љ–µ–Њ–њ—А–∞–≤–і–∞–љ–љ–Њ —И–Є—А–Њ–Ї–Њ–µ –љ–∞–Ј–љ–∞—З–µ–љ–Є–µ «–љ–Њ–≤—Л—Е» –Р–Ь–Я –њ—А–Є —Б–Њ—Е—А–∞–љ–µ–љ–Є–Є —З—Г–≤—Б—В–≤–Є—В–µ–ї—М–љ–Њ—Б—В–Є –Ї «—Б—В–∞—А—Л–Љ» –њ—А–µ–њ–∞—А–∞—В–∞–Љ –Љ–Њ–ґ–µ—В –њ—А–Є–≤–µ—Б—В–Є –Ї –љ–µ–±–ї–∞–≥–Њ–њ—А–Є—П—В–љ—Л–Љ –њ–Њ—Б–ї–µ–і—Б—В–≤–Є—П–Љ —Б —В–Њ—З–Ї–Є –Ј—А–µ–љ–Є—П –≤–Њ–Ј–љ–Є–Ї–љ–Њ–≤–µ–љ–Є—П –Є —А–∞—Б–њ—А–Њ—Б—В—А–∞–љ–µ–љ–Є—П –∞–љ—В–Є–±–Є–Њ—В–Є–Ї–Њ—А–µ–Ј–Є—Б—В–µ–љ—В–љ–Њ—Б—В–Є. –Ґ–∞–Ї, —А–µ–Ј—Г–ї—М—В–∞—В—Л —Ж–µ–ї–Њ–≥–Њ —А—П–і–∞ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–є –њ—А–Њ–і–µ–Љ–Њ–љ—Б—В—А–Є—А–Њ–≤–∞–ї–Є –љ–µ–Њ–і–Є–љ–∞–Ї–Њ–≤—Г—О —Б–њ–Њ—Б–Њ–±–љ–Њ—Б—В—М —А–∞–Ј–ї–Є—З–љ—Л—Е –Р–Ь–Я –≤—Л–Ј—Л–≤–∞—В—М –њ–Њ—П–≤–ї–µ–љ–Є–µ –Є —А–∞—Б–њ—А–Њ—Б—В—А–∞–љ–µ–љ–Є–µ –Ї –љ–Є–Љ —А–µ–Ј–Є—Б—В–µ–љ—В–љ–Њ—Б—В–Є —Б—А–µ–і–Є —А–∞–Ј–ї–Є—З–љ—Л—Е –≤–Њ–Ј–±—Г–і–Є—В–µ–ї–µ–є. –Т —З–∞—Б—В–љ–Њ—Б—В–Є, —А–∞—Б–њ—А–Њ—Б—В—А–∞–љ–µ–љ–Є–µ –њ–µ–љ–Є—Ж–Є–ї–ї–Є–љ–Њ—А–µ–Ј–Є—Б—В–µ–љ—В–љ—Л—Е —И—В–∞–Љ–Љ–Њ–≤ S. pneumoniae –Ї–Њ—А—А–µ–ї–Є—А—Г–µ—В —Б —А–Њ—Б—В–Њ–Љ –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є—П –њ–µ—А–Њ—А–∞–ї—М–љ—Л—Е —Ж–µ—Д–∞–ї–Њ—Б–њ–Њ—А–Є–љ–Њ–≤ –і–ї—П –ї–µ—З–µ–љ–Є—П —А–µ—Б–њ–Є—А–∞—В–Њ—А–љ—Л—Е –Є–љ—Д–µ–Ї—Ж–Є–є, –њ—А–Є —Н—В–Њ–Љ –њ—А–Є–Љ–µ–љ–µ–љ–Є–µ –њ—А–µ–њ–∞—А–∞—В–Њ–≤ –њ–µ–љ–Є—Ж–Є–ї–ї–Є–љ–Њ–≤–Њ–≥–Њ —А—П–і–∞ –Њ–±—Л—З–љ–Њ –љ–µ –≤—Л–Ј—Л–≤–∞–µ—В —В–∞–Ї–Њ–≥–Њ —Н—Д—Д–µ–Ї—В–∞ [47].
–Т –Э–Є–і–µ—А–ї–∞–љ–і–∞—Е –њ—А–µ–Є–Љ—Г—Й–µ—Б—В–≤–µ–љ–љ–Њ–µ –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є–µ –і–ї—П –ї–µ—З–µ–љ–Є—П «—Б—В–∞—А—Л—Е» –њ—А–µ–њ–∞—А–∞—В–Њ–≤ —Б —Г–Ј–Ї–Є–Љ —Б–њ–µ–Ї—В—А–Њ–Љ –∞–љ—В–Є–Љ–Є–Ї—А–Њ–±–љ–Њ–≥–Њ –і–µ–є—Б—В–≤–Є—П –Љ–љ–Њ–≥–Є–µ –≥–Њ–і—Л —В—Й–∞—В–µ–ї—М–љ–Њ –Є–Ј—Г—З–∞–ї–Њ—Б—М –≤ –љ–µ—Б–Ї–Њ–ї—М–Ї–Є—Е –Љ–µ–і–Є—Ж–Є–љ—Б–Ї–Є—Е —Г—З—А–µ–ґ–і–µ–љ–Є—П—Е, –Є –і–∞–љ–љ–∞—П —Б—В—А–∞—В–µ–≥–Є—П —Б—В–∞–ї–∞ –Њ—Б–љ–Њ–≤–Њ–є –њ—А–Є–љ—Ж–Є–њ–Њ–≤ —А–∞—Ж–Є–Њ–љ–∞–ї—М–љ–Њ–≥–Њ –њ—А–Є–Љ–µ–љ–µ–љ–Є—П –∞–љ—В–Є–±–Є–Њ—В–Є–Ї–Њ–≤ [48]. –Т –Ф–∞–љ–Є–Є, —П–≤–ї—П—О—Й–µ–є—Б—П –Њ–і–љ–Њ–є –Є–Ј —Б—В—А–∞–љ —Б –љ–∞–Є–±–Њ–ї–µ–µ –љ–Є–Ј–Ї–Є–Љ —Г—А–Њ–≤–љ–µ–Љ –∞–љ—В–Є–±–Є–Њ—В–Є–Ї–Њ—А–µ–Ј–Є—Б—В–µ–љ—В–љ–Њ—Б—В–Є, –≤ –±–Њ–ї—М—И–Є–љ—Б—В–≤–µ —Б–ї—Г—З–∞–µ–≤ –њ—А–µ–і–њ–Њ—З—В–µ–љ–Є–µ –Њ—В–і–∞–µ—В—Б—П —Н—В–Є–Љ –ґ–µ –њ—А–µ–њ–∞—А–∞—В–∞–Љ [49].
–Ь–Є—Д 4. 16-—З–ї–µ–љ–љ—Л–µ –Љ–∞–Ї—А–Њ–ї–Є–і—Л –Њ–±–ї–∞–і–∞—О—В –њ—А–µ–Є–Љ—Г—Й–µ—Б—В–≤–∞–Љ–Є —Б –Љ–Є–Ї—А–Њ–±–Є–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Њ–є —В–Њ—З–Ї–Є –Ј—А–µ–љ–Є—П –љ–∞–і 14- –Є 15-—З–ї–µ–љ–љ—Л–Љ–Є –Љ–∞–Ї—А–Њ–ї–Є–і–∞–Љ–Є –≤ –Њ—В–љ–Њ—И–µ–љ–Є–Є S. pyogenes –Є S. pneumoniae
16-—З–ї–µ–љ–љ—Л–µ –Љ–∞–Ї—А–Њ–ї–Є–і—Л –і–µ–є—Б—В–≤–Є—В–µ–ї—М–љ–Њ –Љ–Њ–≥—Г—В —Б–Њ—Е—А–∞–љ—П—В—М –∞–Ї—В–Є–≤–љ–Њ—Б—В—М in vitro –њ—А–Њ—В–Є–≤ –љ–µ–Ї–Њ—В–Њ—А—Л—Е —И—В–∞–Љ–Љ–Њ–≤ S. pyogenes –Є S. pneumoniae, —А–µ–Ј–Є—Б—В–µ–љ—В–љ—Л—Е –Ї 14- –Є 15-—З–ї–µ–љ–љ—Л–Љ –Љ–∞–Ї—А–Њ–ї–Є–і–∞–Љ. –Ф–µ–ї–Њ –≤ —В–Њ–Љ, —З—В–Њ –Њ–њ–Є—Б–∞–љ—Л 2 –Њ—Б–љ–Њ–≤–љ—Л—Е –Љ–µ—Е–∞–љ–Є–Ј–Љ–∞ –њ—А–Є–Њ–±—А–µ—В–µ–љ–љ–Њ–є —А–µ–Ј–Є—Б—В–µ–љ—В–љ–Њ—Б—В–Є –і–∞–љ–љ—Л—Е –Љ–Є–Ї—А–Њ–Њ—А–≥–∞–љ–Є–Ј–Љ–Њ–≤ –Ї –Љ–∞–Ї—А–Њ–ї–Є–і–∞–Љ: 1) –Љ–Њ–і–Є—Д–Є–Ї–∞—Ж–Є—П (–Љ–µ—В–Є–ї–Є—А–Њ–≤–∞–љ–Є–µ –Є–ї–Є –Љ—Г—В–∞—Ж–Є—П) –Љ–Є—И–µ–љ–Є –і–µ–є—Б—В–≤–Є—П (50S-—Б—Г–±—К–µ–і–Є–љ–Є—Ж—Л –±–∞–Ї—В–µ—А–Є–∞–ї—М–љ–Њ–є —А–Є–±–Њ—Б–Њ–Љ—Л), —З—В–Њ –љ–∞—А—Г—И–∞–µ—В —Б–≤—П–Ј—Л–≤–∞–љ–Є–µ —Б –љ–µ–є –Љ–∞–Ї—А–Њ–ї–Є–і–љ—Л—Е –∞–љ—В–Є–±–Є–Њ—В–Є–Ї–Њ–≤, –Є 2) –∞–Ї—В–Є–≤–љ–Њ–µ –≤—Л–≤–µ–і–µ–љ–Є–µ (—Н—Д—Д–ї—О–Ї—Б) –∞–љ—В–Є–±–Є–Њ—В–Є–Ї–∞ –Є–Ј –±–∞–Ї—В–µ—А–Є–∞–ї—М–љ–Њ–є –Ї–ї–µ—В–Ї–Є [50, 51].
–Я–µ—А–≤—Л–є –Љ–µ—Е–∞–љ–Є–Ј–Љ –Њ–±—Г—Б–ї–Њ–≤–ї–µ–љ –Љ–µ—В–Є–ї–Є—А–Њ–≤–∞–љ–Є–µ–Љ 23S-—А–Є–±–Њ—Б–Њ–Љ–∞–ї—М–љ–Њ–є –†–Э–Ъ –њ–Њ–і –і–µ–є—Б—В–≤–Є–µ–Љ –Њ—Б–Њ–±—Л—Е —Д–µ—А–Љ–µ–љ—В–Њ–≤ – –±–∞–Ї—В–µ—А–Є–∞–ї—М–љ—Л—Е –Љ–µ—В–Є–ї–∞–Ј, –Ї–Њ–і–Є—А—Г–µ–Љ—Л—Е erm-–≥–µ–љ–∞–Љ–Є, –Є –Њ–±–Њ–Ј–љ–∞—З–∞–µ—В—Б—П –Ї–∞–Ї MLSB-—В–Є–њ —А–µ–Ј–Є—Б—В–µ–љ—В–љ–Њ—Б—В–Є. –≠—В–Њ—В —В–Є–њ —А–µ–Ј–Є—Б—В–µ–љ—В–љ–Њ—Б—В–Є –Њ–±—Г—Б–ї–Њ–≤–ї–Є–≤–∞–µ—В —Г—Б—В–Њ–є—З–Є–≤–Њ—Б—В—М –±–∞–Ї—В–µ—А–Є–Є –Ї–Њ –≤—Б–µ–Љ –Љ–∞–Ї—А–Њ–ї–Є–і–∞–Љ (14-, 15- –Є 16-—З–ї–µ–љ–љ—Л–Љ) –Є, –Ї—А–Њ–Љ–µ —В–Њ–≥–Њ, –Ї –ї–Є–љ–Ї–Њ–Ј–∞–Љ–Є–і–∞–Љ. –Т—В–Њ—А–Њ–є –Љ–µ—Е–∞–љ–Є–Ј–Љ —А–µ–Ј–Є—Б—В–µ–љ—В–љ–Њ—Б—В–Є – —Н—Д—Д–ї—О–Ї—Б, –њ–Њ–ї—Г—З–Є–≤—И–Є–є –љ–∞–Ј–≤–∞–љ–Є–µ –Ь-—Д–µ–љ–Њ—В–Є–њ–∞, —Е–∞—А–∞–Ї—В–µ—А–µ–љ –њ—А–µ–ґ–і–µ –≤—Б–µ–≥–Њ –і–ї—П —Б—В—А–µ–њ—В–Њ–Ї–Њ–Ї–Ї–Њ–≤ (–С–У–°–Р, –њ–љ–µ–≤–Љ–Њ–Ї–Њ–Ї–Ї–Є). –°—Г—Й–µ—Б—В–≤–µ–љ–љ–Њ, —З—В–Њ –≤—Л–≤–µ–і–µ–љ–Є—О –Є–Ј –Ї–ї–µ—В–Ї–Є –њ–Њ–і–≤–µ—А–≥–∞—О—В—Б—П —В–Њ–ї—М–Ї–Њ 14- –Є 15-—З–ї–µ–љ–љ—Л–µ –Љ–∞–Ї—А–Њ–ї–Є–і—Л, –∞ 16-—З–ї–µ–љ–љ—Л–µ —Б–Њ—Е—А–∞–љ—П—О—В —Б–≤–Њ—О –∞–Ї—В–Є–≤–љ–Њ—Б—В—М. –†–∞—Б–њ—А–Њ—Б—В—А–∞–љ–µ–љ–љ–Њ—Б—В—М —А–∞–Ј–ї–Є—З–љ—Л—Е —Д–µ–љ–Њ—В–Є–њ–Њ–≤ —А–µ–Ј–Є—Б—В–µ–љ—В–љ–Њ—Б—В–Є —Б—А–µ–і–Є —А–∞–Ј–љ—Л—Е –≤–Є–і–Њ–≤ –Љ–Є–Ї—А–Њ–Њ—А–≥–∞–љ–Є–Ј–Љ–Њ–≤ –Љ–Њ–ґ–µ—В –Ј–љ–∞—З–Є—В–µ–ї—М–љ–Њ –≤–∞—А—М–Є—А–Њ–≤–∞—В—М –≤ —А–∞–Ј–ї–Є—З–љ—Л—Е —Б—В—А–∞–љ–∞—Е –Є —А–µ–≥–Є–Њ–љ–∞—Е. –Т —З–∞—Б—В–љ–Њ—Б—В–Є, –Є–Ј–≤–µ—Б—В–љ–Њ, —З—В–Њ –≤ –°–®–Р –±–Њ–ї–µ–µ —А–∞—Б–њ—А–Њ—Б—В—А–∞–љ–µ–љ –Ь-—Д–µ–љ–Њ—В–Є–њ —А–µ–Ј–Є—Б—В–µ–љ—В–љ–Њ—Б—В–Є (—Б–Њ—Б—В–∞–≤–ї—П–µ—В –Њ–Ї–Њ–ї–Њ 60% —Б—А–µ–і–Є —А–µ–Ј–Є—Б—В–µ–љ—В–љ—Л—Е —И—В–∞–Љ–Љ–Њ–≤), –∞ –≤ –±–Њ–ї—М—И–Є–љ—Б—В–≤–µ —Б—В—А–∞–љ –Х–≤—А–Њ–њ—Л – MLSB-—В–Є–њ [52]. –≠—В–Є –Љ–µ—Е–∞–љ–Є–Ј–Љ—Л –Љ–Њ–≥—Г—В –≤—Б—В—А–µ—З–∞—В—М—Б—П –Ї–∞–Ї –њ–Њ –Њ—В–і–µ–ї—М–љ–Њ—Б—В–Є, —В–∞–Ї –Є –≤ –Ї–Њ–Љ–±–Є–љ–∞—Ж–Є–Є, –Є —Н—В–Є –і–∞–љ–љ—Л–µ —Б–ї–µ–і—Г–µ—В —Г—З–Є—В—Л–≤–∞—В—М –њ—А–Є –≤—Л–±–Њ—А–µ –Р–Ь–Я –Є –њ—А–Њ–≥–љ–Њ–Ј–Є—А–Њ–≤–∞–љ–Є–Є —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В–Є –ї–µ—З–µ–љ–Є—П.
–Х—Б–ї–Є –≥–Њ–≤–Њ—А–Є—В—М –Њ –љ–∞—И–µ–є —Б—В—А–∞–љ–µ, —В–Њ, –њ–Њ –і–∞–љ–љ—Л–Љ –њ–Њ—Б–ї–µ–і–љ–µ–≥–Њ –Љ–љ–Њ–≥–Њ—Ж–µ–љ—В—А–Њ–≤–Њ–≥–Њ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П –Я–µ–У–Р–°-III (2006–2009 –≥–≥.), —А–µ–Ј–Є—Б—В–µ–љ—В–љ–Њ—Б—В—М —И—В–∞–Љ–Љ–Њ–≤ S. pneumoniae –Ї –ї–Є–љ–Ї–Њ–Ј–∞–Љ–Є–і–∞–Љ –Є –Ї 14-, 15-, 16-—З–ї–µ–љ–љ—Л–Љ –Љ–∞–Ї—А–Њ–ї–Є–і–∞–Љ —Б–Њ—Б—В–∞–≤–ї—П–µ—В –Њ–Ї–Њ–ї–Њ 5% [46]. –Ґ–∞–Ї–Є–Љ –Њ–±—А–∞–Ј–Њ–Љ, –љ–∞ –љ–∞—Б—В–Њ—П—Й–Є–є –Љ–Њ–Љ–µ–љ—В —А–µ–Ј–Є—Б—В–µ–љ—В–љ–Њ—Б—В—М –њ–љ–µ–≤–Љ–Њ–Ї–Њ–Ї–Ї–Њ–≤ –Ї –Љ–∞–Ї—А–Њ–ї–Є–і–∞–Љ –љ–µ —П–≤–ї—П–µ—В—Б—П –њ—А–Њ–±–ї–µ–Љ–Њ–є –і–ї—П –љ–∞—И–µ–є —Б—В—А–∞–љ—Л, –Ї—А–Њ–Љ–µ —В–Њ–≥–Њ, —Б—Г–і—П –њ–Њ —Д–µ–љ–Њ—В–Є–њ—Г —А–µ–Ј–Є—Б—В–µ–љ—В–љ–Њ—Б—В–Є, –љ–∞ —В–µ—А—А–Є—В–Њ—А–Є–Є –†–§ —Г S. pneumoniae –њ—А–µ–≤–∞–ї–Є—А—Г–µ—В MLSB-—В–Є–њ —А–µ–Ј–Є—Б—В–µ–љ—В–љ–Њ—Б—В–Є.
–І—В–Њ –Ї–∞—Б–∞–µ—В—Б—П –і–∞–љ–љ—Л—Е –Њ —З—Г–≤—Б—В–≤–Є—В–µ–ї—М–љ–Њ—Б—В–Є S. pyogenes, —В–Њ –њ–Њ —А–µ–Ј—Г–ї—М—В–∞—В–∞–Љ —В–Њ–≥–Њ –ґ–µ –њ—А–Њ—Б–њ–µ–Ї—В–Є–≤–љ–Њ–≥–Њ –Љ–Є–Ї—А–Њ–±–Є–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Њ–≥–Њ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П –Я–µ–У–Р–° –±—Л–ї–Є –Њ—В–Љ–µ—З–µ–љ—Л –і–Њ—Б—В–∞—В–Њ—З–љ–Њ —Б—Г—Й–µ—Б—В–≤–µ–љ–љ—Л–µ —А–∞–Ј–ї–Є—З–Є—П –≤ —З—Г–≤—Б—В–≤–Є—В–µ–ї—М–љ–Њ—Б—В–Є S. pyogenes –Ї –Љ–∞–Ї—А–Њ–ї–Є–і–∞–Љ –≤ —А–∞–Ј–ї–Є—З–љ—Л–µ –≤—А–µ–Љ–µ–љ–љ—Л–µ –Є–љ—В–µ—А–≤–∞–ї—Л (—В–∞–±–ї. 1). –Ю–і–љ–∞–Ї–Њ –њ–Њ –і–∞–љ–љ—Л–Љ –њ–Њ—Б–ї–µ–і–љ–µ–≥–Њ —Н—В–∞–њ–∞ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П –Я–µ–У–Р–°-III (2006–2009 –≥–≥.) 99% —И—В–∞–Љ–Љ–Њ–≤ –С–У–°–Р –±—Л–ї–Є —З—Г–≤—Б—В–≤–Є—В–µ–ї—М–љ—Л –Ї —Н—А–Є—В—А–Њ–Љ–Є—Ж–Є–љ—Г –Є –Ї–ї–Є–љ–і–∞–Љ–Є—Ж–Є–љ—Г [44].
–Я—А–Є–љ–Є–Љ–∞—П –≤–Њ –≤–љ–Є–Љ–∞–љ–Є–µ –Њ—В—Б—Г—В—Б—В–≤–Є–µ —А–∞–Ј–ї–Є—З–Є–є –≤ —З—Г–≤—Б—В–≤–Є—В–µ–ї—М–љ–Њ—Б—В–Є –Ї –Љ–∞–Ї—А–Њ–ї–Є–і–∞–Љ –Є –ї–Є–љ–Ї–Њ–Ј–∞–Љ–Є–і–∞–Љ –≤ –†–§ –≤ 2006–2009 –≥–≥., –Љ–Њ–ґ–љ–Њ —Б–і–µ–ї–∞—В—М –љ–µ—Б–Ї–Њ–ї—М–Ї–Њ –Њ—Б–љ–Њ–≤–љ—Л—Е –≤—Л–≤–Њ–і–Њ–≤:
1. –†–µ–Ј–Є—Б—В–µ–љ—В–љ–Њ—Б—В—М –Ї –Љ–∞–Ї—А–Њ–ї–Є–і–∞–Љ —Г –њ–љ–µ–≤–Љ–Њ–Ї–Њ–Ї–Ї–Њ–≤ –Є –С–У–°–Р –≤ –†–§ –љ–µ —П–≤–ї—П–µ—В—Б—П –њ—А–Њ–±–ї–µ–Љ–Њ–є.
2. –Э–∞ –Њ—Б–љ–Њ–≤–∞–љ–Є–Є –њ–Њ–ї—Г—З–µ–љ–љ—Л—Е –і–∞–љ–љ—Л—Е –Є –њ—А–µ–і–њ–Њ–ї–∞–≥–∞–µ–Љ—Л—Е –Љ–µ—Е–∞–љ–Є–Ј–Љ–Њ–≤ —А–µ–Ј–Є—Б—В–µ–љ—В–љ–Њ—Б—В–Є –ї–Є–љ–Ї–Њ–Ј–∞–Љ–Є–і—Л –Є 16-—З–ї–µ–љ–љ—Л–µ –Љ–∞–Ї—А–Њ–ї–Є–і—Л (–і–ґ–Њ–Ј–∞–Љ–Є—Ж–Є–љ, –Љ–Є–і–µ–Ї–∞–Љ–Є—Ж–Є–љ) –љ–µ –Є–Љ–µ—О—В –љ–Є–Ї–∞–Ї–Є—Е –Љ–Є–Ї—А–Њ–±–Є–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є—Е –њ—А–µ–Є–Љ—Г—Й–µ—Б—В–≤ –њ–µ—А–µ–і 14- –Є 15-—З–ї–µ–љ–љ—Л–Љ–Є –Љ–∞–Ї—А–Њ–ї–Є–і–∞–Љ–Є –≤ –Њ—В–љ–Њ—И–µ–љ–Є–Є S. pneumoniae –Є S. pyogenes.
–Ь–Є—Д 5. –Р–љ—В–Є–±–Є–Њ—В–Є–Ї–Є –Њ—З–µ–љ—М —В–Њ–Ї—Б–Є—З–љ—Л,
–Є –Є—Е –њ—А–Є–Љ–µ–љ–µ–љ–Є–µ —В—А–µ–±—Г–µ—В –Њ–±—П–Ј–∞—В–µ–ї—М–љ–Њ–≥–Њ –љ–∞–Ј–љ–∞—З–µ–љ–Є—П «–њ—А–µ–њ–∞—А–∞—В–Њ–≤ –њ—А–Є–Ї—А—Л—В–Є—П»
–Ъ–∞–Ї —Б—А–µ–і–Є –≤—А–∞—З–µ–є, —В–∞–Ї –Є —Б—А–µ–і–Є –љ–∞—Б–µ–ї–µ–љ–Є—П –±—Л—В—Г–µ—В –Љ–љ–µ–љ–Є–µ, —З—В–Њ –∞–љ—В–Є–±–Є–Њ—В–Є–Ї–Є —В–Њ–Ї—Б–Є—З–љ—Л, –≤—Л–Ј—Л–≤–∞—О—В –∞–ї–ї–µ—А–≥–Є—О –Є —Г–≥–љ–µ—В–∞—О—В –Є–Љ–Љ—Г–љ–Є—В–µ—В, –њ–Њ—Н—В–Њ–Љ—Г –Њ—А–≥–∞–љ–Є–Ј–Љ—Г —В—А–µ–±—Г–µ—В—Б—П –љ–µ—Б–Ї–Њ–ї—М–Ї–Њ –Љ–µ—Б—П—Ж–µ–≤ –і–ї—П «–≤–Њ—Б—Б—В–∞–љ–Њ–≤–ї–µ–љ–Є—П» –љ–Њ—А–Љ–∞–ї—М–љ–Њ–≥–Њ —Б–Њ—Б—В–Њ—П–љ–Є—П –Є –љ–µ–Њ–±—Е–Њ–і–Є–Љ–Њ –љ–∞–Ј–љ–∞—З–µ–љ–Є–µ –∞–љ—В–Є–≥–Є—Б—В–∞–Љ–Є–љ–љ—Л—Е, –Є–Љ–Љ—Г–љ–Њ—Б—В–Є–Љ—Г–ї–Є—А—Г—О—Й–Є—Е/–Є–Љ–Љ—Г–љ–Њ–Ї–Њ—А—А–Є–≥–Є—А—Г—О—Й–Є—Е, –Њ–±—Й–µ—Г–Ї—А–µ–њ–ї—П—О—Й–Є—Е, –≤–Є—В–∞–Љ–Є–љ–љ—Л—Е –Є —А—П–і–∞ –і—А—Г–≥–Є—Е —Б–Њ–њ—Г—В—Б—В–≤—Г—О—Й–Є—Е –њ—А–µ–њ–∞—А–∞—В–Њ–≤.
–Т–Њ–Ј–Љ–Њ–ґ–љ–Њ, –і–∞–љ–љ–Њ–µ –Ј–∞–±–ї—Г–ґ–і–µ–љ–Є–µ –≤–Њ–Ј–љ–Є–Ї–ї–Њ –≤ «—А–∞–љ–љ—О—О —Н—А—Г» –Р–С–Ґ, –Ї–Њ–≥–і–∞ –Є—Б–њ–Њ–ї—М–Ј—Г–µ–Љ—Л–µ –Р–Ь–Я (—Е–ї–Њ—А–∞–Љ—Д–µ–љ–Є–Ї–Њ–ї, –∞–Љ–Є–љ–Њ–≥–ї–Є–Ї–Њ–Ј–Є–і—Л, —Б—Г–ї—М—Д–∞–љ–Є–ї–∞–Љ–Є–і—Л, —В–µ—В—А–∞—Ж–Є–Ї–ї–Є–љ—Л) –і–µ–є—Б—В–≤–Є—В–µ–ї—М–љ–Њ –±—Л–ї–Є —В–Њ–Ї—Б–Є—З–љ—Л –Є –љ–µ—А–µ–і–Ї–Њ –≤—Л–Ј—Л–≤–∞–ї–Є –љ–µ–ґ–µ–ї–∞—В–µ–ї—М–љ—Л–µ –ї–µ–Ї–∞—А—Б—В–≤–µ–љ–љ—Л–µ —А–µ–∞–Ї—Ж–Є–Є. –Т –љ–∞—Б—В–Њ—П—Й–µ–µ –≤—А–µ–Љ—П –≤ —А–∞—Б–њ–Њ—А—П–ґ–µ–љ–Є–Є –≤—А–∞—З–µ–є –Є–Љ–µ—О—В—Б—П —Н—Д—Д–µ–Ї—В–Є–≤–љ—Л–µ –њ—А–µ–њ–∞—А–∞—В—Л —Б –±–ї–∞–≥–Њ–њ—А–Є—П—В–љ—Л–Љ –њ—А–Њ—Д–Є–ї–µ–Љ –±–µ–Ј–Њ–њ–∞—Б–љ–Њ—Б—В–Є. –Т—Б–µ –Р–Ь–Я, —Б–њ–Њ—Б–Њ–±–љ—Л–µ –≤—Л–Ј–≤–∞—В—М –Є–Љ–Љ—Г–љ–Њ—Б—Г–њ—А–µ—Б—Б–Є—О —Г —З–µ–ї–Њ–≤–µ–Ї–∞, –Њ—В—Б–µ–Є–≤–∞—О—В—Б—П –µ—Й–µ –љ–∞ —Б—В–∞–і–Є–Є –і–Њ–Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є—Е –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–є [53]. –С–Њ–ї–µ–µ —В–Њ–≥–Њ, —Г –љ–µ–Ї–Њ—В–Њ—А—Л—Е –≥—А—Г–њ–њ –Р–Ь–Я (–љ–∞–њ—А–Є–Љ–µ—А, —Г –∞–Ј–Є—В—А–Њ–Љ–Є—Ж–Є–љ–∞), –љ–∞–Њ–±–Њ—А–Њ—В, –Њ–±–љ–∞—А—Г–ґ–µ–љ–Њ –±–ї–∞–≥–Њ–њ—А–Є—П—В–љ–Њ–µ –і–µ–є—Б—В–≤–Є–µ –љ–∞ –Є–Љ–Љ—Г–љ–љ—Г—О —Б–Є—Б—В–µ–Љ—Г: –≤–Њ–Ј–і–µ–є—Б—В–≤–Є–µ –љ–∞ —Б–Є–љ—В–µ–Ј —Ж–Є—В–Њ–Ї–Є–љ–Њ–≤/—Е–µ–Љ–Њ–Ї–Є–љ–Њ–≤, –≤–ї–Є—П–љ–Є–µ –љ–∞ –љ–µ–є—В—А–Њ—Д–Є–ї—Л, —Д–∞–≥–Њ—Ж–Є—В–Њ–Ј, —Е–µ–Љ–Њ—В–∞–Ї—Б–Є—Б, —Г—Б–Є–ї–µ–љ–Є–µ –∞–Ї—В–Є–≤–љ–Њ—Б—В–Є –љ–Њ—А–Љ–∞–ї—М–љ—Л—Е –Ї–Є–ї–ї–µ—А–љ—Л—Е –Ї–ї–µ—В–Њ–Ї, —Г—Б–Є–ї–µ–љ–Є–µ –∞–њ–Њ–њ—В–Њ–Ј–∞ –Є –Љ—Г–Ї–Њ—Ж–Є–ї–Є–∞—А–љ–Њ–≥–Њ –Ї–ї–Є—А–µ–љ—Б–∞, —Б–љ–Є–ґ–µ–љ–Є–µ —Б–µ–Ї—А–µ—Ж–Є–Є —Б–ї–Є–Ј–Є –±–Њ–Ї–∞–ї–Њ–≤–Є–і–љ—Л–Љ–Є –Ї–ї–µ—В–Ї–∞–Љ–Є, —Г–Љ–µ–љ—М—И–µ–љ–Є–µ –≤—Л—А–∞–ґ–µ–љ–љ–Њ—Б—В–Є –±—А–Њ–љ—Е–Є–∞–ї—М–љ–Њ–є –Њ–±—Б—В—А—Г–Ї—Ж–Є–Є [54–56].
–Э–µ—А–µ–і–Ї–Њ –≤—А–∞—З–Є –њ–Њ–ї–∞–≥–∞—О—В, —З—В–Њ –љ–∞ —Д–Њ–љ–µ –Р–С–Ґ –љ–µ–Њ–±—Е–Њ–і–Є–Љ–Њ –љ–∞–Ј–љ–∞—З–µ–љ–Є–µ —Б–Њ–њ—Г—В—Б—В–≤—Г—О—Й–Є—Е –Ы–°, –∞ –Є–Љ–µ–љ–љ–Њ —В–∞–Ї –љ–∞–Ј—Л–≤–∞–µ–Љ—Л—Е «–њ—А–µ–њ–∞—А–∞—В–Њ–≤ –њ—А–Є–Ї—А—Л—В–Є—П» – «–і–µ—Б–µ–љ—Б–Є–±–Є–ї–Є–Ј–Є—А—Г—О—Й–µ–є» —В–µ—А–∞–њ–Є–Є (–∞–љ—В–Є–≥–Є—Б—В–∞–Љ–Є–љ–љ—Л—Е –њ—А–µ–њ–∞—А–∞—В–Њ–≤, —В–Є–Њ—Б—Г–ї—М—Д–∞—В–∞ –љ–∞—В—А–Є—П, –Ї–∞–ї—М—Ж–Є—П –≥–ї—О–Ї–Њ–љ–∞—В–∞, –Ї–∞–ї—М—Ж–Є—П —Е–ї–Њ—А–Є–і–∞), –њ—А–Њ—В–Є–≤–Њ–≥—А–Є–±–Ї–Њ–≤—Л—Е –њ—А–µ–њ–∞—А–∞—В–Њ–≤ (–љ–Є—Б—В–∞—В–Є–љ –≤–љ—Г—В—А—М –і–ї—П –њ—А–Њ—Д–Є–ї–∞–Ї—В–Є–Ї–Є —А–∞–Ј–≤–Є—В–Є—П –Ї–∞–љ–і–Є–і–Њ–Ј–∞) –Є –Є–Љ–Љ—Г–љ–Њ—Б—В–Є–Љ—Г–ї–Є—А—Г—О—Й–µ–є/–Є–Љ–Љ—Г–љ–Њ–Ї–Њ—А—А–Є–≥–Є—А—Г—О—Й–µ–є —В–µ—А–∞–њ–Є–Є. –Ґ–∞–Ї, –≤ 5 –≥–Њ—А–Њ–і–∞—Е –†–Њ—Б—Б–Є–Є –≤ 2000 –≥. –±—Л–ї–Є –њ—А–Њ–∞–љ–Ї–µ—В–Є—А–Њ–≤–∞–љ—Л —Г—З–∞—Б—В–Ї–Њ–≤—Л–µ —В–µ—А–∞–њ–µ–≤—В—Л –Є –њ—Г–ї—М–Љ–Њ–љ–Њ–ї–Њ–≥–Є –≥–Њ—А–Њ–і—Б–Ї–Є—Е –њ–Њ–ї–Є–Ї–ї–Є–љ–Є–Ї. –Ю—В–≤–µ—З–∞—П –љ–∞ –≤–Њ–њ—А–Њ—Б –Њ –і—А—Г–≥–Є—Е –≥—А—Г–њ–њ–∞—Е –Ы–° –і–ї—П –ї–µ—З–µ–љ–Є—П –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –≤–љ–µ–±–Њ–ї—М–љ–Є—З–љ–Њ–є –њ–љ–µ–≤–Љ–Њ–љ–Є–µ–є, –±–Њ–ї–µ–µ –њ–Њ–ї–Њ–≤–Є–љ—Л –≤—А–∞—З–µ–є –Њ—В–Љ–µ—З–∞–ї–Є —Ж–µ–ї–µ—Б–Њ–Њ–±—А–∞–Ј–љ—Л–Љ –љ–∞–Ј–љ–∞—З–µ–љ–Є–µ –Њ–і–љ–Њ–≤—А–µ–Љ–µ–љ–љ–Њ —Б –∞–љ—В–Є–±–Є–Њ—В–Є–Ї–∞–Љ–Є –≤–Є—В–∞–Љ–Є–љ–Њ–≤ (59%) –Є –∞–љ—В–Є–≥–Є—Б—В–∞–Љ–Є–љ–љ—Л—Е –њ—А–µ–њ–∞—А–∞—В–Њ–≤ (56%); 48% – –њ—А–Њ—В–Є–≤–Њ–≥—А–Є–±–Ї–Њ–≤—Л—Е –Ы–°, —В–∞–Ї–Є—Е –Ї–∞–Ї –љ–Є—Б—В–∞—В–Є–љ, 34,4% – –Є–Љ–Љ—Г–љ–Њ–Љ–Њ–і—Г–ї—П—В–Њ—А–Њ–≤, 11,2% – –љ–µ—Б—В–µ—А–Њ–Є–і–љ—Л—Е –њ—А–Њ—В–Є–≤–Њ–≤–Њ—Б–њ–∞–ї–Є—В–µ–ї—М–љ—Л—Е –њ—А–µ–њ–∞—А–∞—В–Њ–≤ [57]. –Р–љ—В–Є–≥–Є—Б—В–∞–Љ–Є–љ–љ—Л–µ –њ—А–µ–њ–∞—А–∞—В—Л –њ–Њ–ї—Г—З–∞–ї–Є 16,9% –њ–∞—Ж–Є–µ–љ—В–Њ–≤ –њ—А–Є –Њ–±–Њ—Б—В—А–µ–љ–Є–Є –•–Ю–С–Ы (–њ—А–Њ–∞–љ–∞–ї–Є–Ј–Є—А–Њ–≤–∞–љ–Њ 1116 —Б–ї—Г—З–∞–µ–≤ –∞–Љ–±—Г–ї–∞—В–Њ—А–љ–Њ–≥–Њ –ї–µ—З–µ–љ–Є—П), –њ—А–Є –Њ—Б—В—А–Њ–Љ —Б—А–µ–і–љ–µ–Љ –Њ—В–Є—В–µ – 44,1% (n=1489), –∞ –њ—А–Є –Њ—Б—В—А–Њ–Љ —Б–Є–љ—Г—Б–Є—В–µ – 59,2% (n=1529) [58]. –Т —В–Њ –ґ–µ –≤—А–µ–Љ—П –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є—Е –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–є, –і–Њ–Ї–∞–Ј—Л–≤–∞—О—Й–Є—Е —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В—М –њ—А–Є–Љ–µ–љ–µ–љ–Є—П –∞–љ—В–Є–≥–Є—Б—В–∞–Љ–Є–љ–љ—Л—Е –њ—А–µ–њ–∞—А–∞—В–Њ–≤ —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –Њ—Б—В—А—Л–Љ —А–Є–љ–Њ—Б–Є–љ—Г—Б–Є—В–Њ–Љ, –љ–µ—В [59, 60]. –Р–љ—В–Є—Е–Њ–ї–Є–љ–µ—А–≥–Є—З–µ—Б–Ї–Є–є —Н—Д—Д–µ–Ї—В –∞–љ—В–Є–≥–Є—Б—В–∞–Љ–Є–љ–љ—Л—Е –њ—А–µ–њ–∞—А–∞—В–Њ–≤ I –њ–Њ–Ї–Њ–ї–µ–љ–Є—П –Љ–Њ–ґ–µ—В –љ–∞—А—Г—И–∞—В—М –µ—Б—В–µ—Б—В–≤–µ–љ–љ—Л–є –Љ—Г–Ї–Њ—Ж–Є–ї–Є–∞—А–љ—Л–є –Ї–ї–Є—А–µ–љ—Б –Є–Ј-–Ј–∞ —Б–≥—Г—Й–µ–љ–Є—П —Б–ї–Є–Ј–Є, –≤—Л–Ј—Л–≤–∞—В—М —Б—Г—Е–Њ—Б—В—М —Б–ї–Є–Ј–Є—Б—В–Њ–є –Њ–±–Њ–ї–Њ—З–Ї–Є –њ–Њ–ї–Њ—Б—В–Є –љ–Њ—Б–∞ –Є –Њ–Ї–Њ–ї–Њ–љ–Њ—Б–Њ–≤—Л—Е —Б–Є–љ—Г—Б–Њ–≤. –Р–љ—В–Є–≥–Є—Б—В–∞–Љ–Є–љ–љ—Л–µ –њ—А–µ–њ–∞—А–∞—В—Л II –њ–Њ–Ї–Њ–ї–µ–љ–Є—П, –ї–Є—И–µ–љ–љ—Л–µ –∞–љ—В–Є—Е–Њ–ї–Є–љ–µ—А–≥–Є—З–µ—Б–Ї–Њ–≥–Њ —Н—Д—Д–µ–Ї—В–∞, –Љ–Њ–≥—Г—В –±—Л—В—М —А–µ–Ї–Њ–Љ–µ–љ–і–Њ–≤–∞–љ—Л –і–ї—П –ї–µ—З–µ–љ–Є—П –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –∞–ї–ї–µ—А–≥–Є–µ–є –Є–ї–Є —Е—А–Њ–љ–Є—З–µ—Б–Ї–Є–Љ —Б–Є–љ—Г—Б–Є—В–Њ–Љ, –љ–Њ –љ–µ –і–ї—П —В–µ—А–∞–њ–Є–Є –Њ—Б—В—А–Њ–≥–Њ –±–∞–Ї—В–µ—А–Є–∞–ї—М–љ–Њ–≥–Њ —А–Є–љ–Њ—Б–Є–љ—Г—Б–Є—В–∞ [29, 61]. –Ґ–Њ –ґ–µ —Б–∞–Љ–Њ–µ –Ї–∞—Б–∞–µ—В—Б—П –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є—П –∞–љ—В–Є–≥–Є—Б—В–∞–Љ–Є–љ–љ—Л—Е –њ—А–µ–њ–∞—А–∞—В–Њ–≤ –њ—А–Є –Њ–±–Њ—Б—В—А–µ–љ–Є–Є –•–Ю–С–Ы: –і–∞–љ–љ—Л–µ –Ы–° –Њ–Ї–∞–Ј—Л–≤–∞—О—В —Б–Ї–Њ—А–µ–µ –љ–µ–≥–∞—В–Є–≤–љ—Л–є, —З–µ–Љ –њ–Њ–Ј–Є—В–Є–≤–љ—Л–є —Н—Д—Д–µ–Ї—В, –њ–Њ—Б–Ї–Њ–ї—М–Ї—Г –њ–Њ–≤—Л—И–∞—О—В –≤—П–Ј–Ї–Њ—Б—В—М –±—А–Њ–љ—Е–Є–∞–ї—М–љ–Њ–≥–Њ —Б–µ–Ї—А–µ—В–∞ –Є –Ј–∞—В—А—Г–і–љ—П—О—В –µ–≥–Њ –Њ—В—Е–Њ–ґ–і–µ–љ–Є–µ.
–Э–∞ –љ–∞—Б—В–Њ—П—Й–Є–є –Љ–Њ–Љ–µ–љ—В —Г–±–µ–і–Є—В–µ–ї—М–љ—Л—Е –і–Њ–Ї–∞–Ј–∞—В–µ–ї—М—Б—В–≤ —В–Њ–≥–Њ, —З—В–Њ –∞–љ—В–Є–≥–Є—Б—В–∞–Љ–Є–љ–љ—Л–µ –њ—А–µ–њ–∞—А–∞—В—Л –њ—А–µ–і–Њ—В–≤—А–∞—Й–∞—О—В —А–∞–Ј–≤–Є—В–Є–µ –∞–ї–ї–µ—А–≥–Є—З–µ—Б–Ї–Є—Е —А–µ–∞–Ї—Ж–Є–є –њ—А–Є –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є–Є –і—А—Г–≥–Є—Е –Ы–°, –≤ —З–∞—Б—В–љ–Њ—Б—В–Є, –∞–љ—В–Є–±–Є–Њ—В–Є–Ї–Њ–≤, –љ–µ—В, –∞ –њ—А–Є —Б–Њ–≤–Љ–µ—Б—В–љ–Њ–Љ –љ–∞–Ј–љ–∞—З–µ–љ–Є–Є –љ–µ—Б–Ї–Њ–ї—М–Ї–Є—Е –њ—А–µ–њ–∞—А–∞—В–Њ–≤ —Г–≤–µ–ї–Є—З–Є–≤–∞–µ—В—Б—П —А–Є—Б–Ї –љ–µ–±–ї–∞–≥–Њ–њ—А–Є—П—В–љ–Њ–≥–Њ –ї–µ–Ї–∞—А—Б—В–≤–µ–љ–љ–Њ–≥–Њ –≤–Ј–∞–Є–Љ–Њ–і–µ–є—Б—В–≤–Є—П, –љ–µ–ґ–µ–ї–∞—В–µ–ї—М–љ—Л—Е –ї–µ–Ї–∞—А—Б—В–≤–µ–љ–љ—Л—Е —А–µ–∞–Ї—Ж–Є–є –Є —Б—Г—Й–µ—Б—В–≤–µ–љ–љ–Њ –≤–Њ–Ј—А–∞—Б—В–∞–µ—В —Б—В–Њ–Є–Љ–Њ—Б—В—М –ї–µ—З–µ–љ–Є—П [62, 63]. –§–∞—А–Љ–∞–Ї–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–∞—П –њ—А–Њ—Д–Є–ї–∞–Ї—В–Є–Ї–∞ –і–Њ–ї–ґ–љ–∞ –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞—В—М—Б—П —В–Њ–ї—М–Ї–Њ –і–ї—П –њ—А–µ–і–Њ—В–≤—А–∞—Й–µ–љ–Є—П —А–∞–Ј–≤–Є—В–Є—П –∞–љ–∞—Д–Є–ї–∞–Ї—В–Њ–Є–і–љ—Л—Е —А–µ–∞–Ї—Ж–Є–є –≤ –Њ—В–≤–µ—В –љ–∞ –±—Л—Б—В—А–Њ–µ –≤/–≤ –≤–≤–µ–і–µ–љ–Є–µ –≤–∞–љ–Ї–Њ–Љ–Є—Ж–Є–љ–∞ (–Є—Б–њ–Њ–ї—М–Ј—Г—О—В—Б—П –∞–љ—В–Є–≥–Є—Б—В–∞–Љ–Є–љ–љ—Л–µ –њ—А–µ–њ–∞—А–∞—В—Л I –њ–Њ–Ї–Њ–ї–µ–љ–Є—П –≤/–≤) [64] –Є –љ–∞ —А–µ–љ—В–≥–µ–љ–Њ–Ї–Њ–љ—В—А–∞—Б—В–љ—Л–µ –≤–µ—Й–µ—Б—В–≤–∞ –Є —Б—А–µ–і—Б—В–≤–∞ –і–ї—П —Д–ї—О–Њ—А–µ—Б—Ж–µ–љ—В–љ–Њ–є –∞–љ–≥–Є–Њ–≥—А–∞—Д–Є–Є – –≤ –і–∞–љ–љ–Њ–Љ —Б–ї—Г—З–∞–µ —А–µ–Ї–Њ–Љ–µ–љ–і—Г–µ—В—Б—П –њ—А–µ–≤–µ–љ—В–Є–≤–љ–Њ–µ –љ–∞–Ј–љ–∞—З–µ–љ–Є–µ –≥–ї—О–Ї–Њ–Ї–Њ—А—В–Є–Ї–Њ–Є–і–Њ–≤ –Є –∞–љ—В–Є–≥–Є—Б—В–∞–Љ–Є–љ–љ—Л—Е –њ—А–µ–њ–∞—А–∞—В–Њ–≤; –≤–Њ –≤—Б–µ—Е –і—А—Г–≥–Є—Е —Б–ї—Г—З–∞—П—Е –њ—А–Њ—Д–Є–ї–∞–Ї—В–Є—З–µ—Б–Ї–Њ–µ –љ–∞–Ј–љ–∞—З–µ–љ–Є–µ –∞–љ—В–Є–≥–Є—Б—В–∞–Љ–Є–љ–љ—Л—Е –њ—А–µ–њ–∞—А–∞—В–Њ–≤ —Б –і—А—Г–≥–Є–Љ–Є –Ы–° –љ–µ –њ–Њ–Ї–∞–Ј–∞–љ–Њ [65].
–Ю–і–љ–Њ–є –Є–Ј —А–∞—Б–њ—А–Њ—Б—В—А–∞–љ–µ–љ–љ—Л—Е –Њ—И–Є–±–Њ–Ї –њ—А–Є –њ—А–Њ–≤–µ–і–µ–љ–Є–Є –Р–С–Ґ —П–≤–ї—П–µ—В—Б—П –љ–∞–Ј–љ–∞—З–µ–љ–Є–µ –Њ–і–љ–Њ–≤—А–µ–Љ–µ–љ–љ–Њ —Б –∞–љ—В–Є–±–Є–Њ—В–Є–Ї–Њ–Љ –њ—А–Њ—В–Є–≤–Њ–≥—А–Є–±–Ї–Њ–≤—Л—Е —Б—А–µ–і—Б—В–≤ —Б —Ж–µ–ї—М—О –њ—А–Њ—Д–Є–ї–∞–Ї—В–Є–Ї–Є –≥—А–Є–±–Ї–Њ–≤—Л—Е –Њ—Б–ї–Њ–ґ–љ–µ–љ–Є–є. –°–ї–µ–і—Г–µ—В –њ–Њ–і—З–µ—А–Ї–љ—Г—В—М, —З—В–Њ –њ—А–Є –љ–µ–і–ї–Є—В–µ–ї—М–љ–Њ–Љ –њ—А–Є–Љ–µ–љ–µ–љ–Є–Є —Б–Њ–≤—А–µ–Љ–µ–љ–љ—Л—Е –Р–Ь–Я —Г –Є–Љ–Љ—Г–љ–Њ–Ї–Њ–Љ–њ–µ—В–µ–љ—В–љ—Л—Е –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —А–Є—Б–Ї –≥—А–Є–±–Ї–Њ–≤–Њ–є —Б—Г–њ–µ—А–Є–љ—Д–µ–Ї—Ж–Є–Є –Љ–Є–љ–Є–Љ–∞–ї–µ–љ, –Є –Њ–і–љ–Њ–≤—А–µ–Љ–µ–љ–љ–Њ–µ –љ–∞–Ј–љ–∞—З–µ–љ–Є–µ –∞–љ—В–Є–Љ–Є–Ї–Њ—В–Є–Ї–Њ–≤ –љ–µ –Њ–њ—А–∞–≤–і–∞–љ–љ–Њ [66]. –Ъ–Њ–Љ–±–Є–љ–∞—Ж–Є—П –∞–љ—В–Є–±–Є–Њ—В–Є–Ї–∞ —Б –њ—А–Њ—В–Є–≤–Њ–≥—А–Є–±–Ї–Њ–≤—Л–Љ —Б—А–µ–і—Б—В–≤–Њ–Љ –≤–Њ–Ј–Љ–Њ–ґ–љ–∞ —В–Њ–ї—М–Ї–Њ —Г –±–Њ–ї—М–љ—Л—Е, –њ–Њ–ї—Г—З–∞—О—Й–Є—Е —Ж–Є—В–Њ—Б—В–∞—В–Є—З–µ—Б–Ї—Г—О –Є–ї–Є –њ—А–Њ—В–Є–≤–Њ–Њ–њ—Г—Е–Њ–ї–µ–≤—Г—О —В–µ—А–∞–њ–Є—О, –Є–ї–Є —Г –Т–Ш–І-–Є–љ—Д–Є—Ж–Є—А–Њ–≤–∞–љ–љ—Л—Е –њ–∞—Ж–Є–µ–љ—В–Њ–≤ [67–69]. –Т —Н—В–Є—Е —Б–ї—Г—З–∞—П—Е –Њ–њ—А–∞–≤–і–∞–љ–љ–Њ –њ—А–Њ—Д–Є–ї–∞–Ї—В–Є—З–µ—Б–Ї–Њ–µ –љ–∞–Ј–љ–∞—З–µ–љ–Є–µ –∞–љ—В–Є–Љ–Є–Ї–Њ—В–Є–Ї–Њ–≤ —Б–Є—Б—В–µ–Љ–љ–Њ–≥–Њ –і–µ–є—Б—В–≤–Є—П (–Ї–µ—В–Њ–Ї–Њ–љ–∞–Ј–Њ–ї, –Є—В—А–∞–Ї–Њ–љ–∞–Ј–Њ–ї, —Д–ї—Г–Ї–Њ–љ–∞–Ј–Њ–ї), –љ–Њ –љ–µ –љ–Є—Б—В–∞—В–Є–љ–∞ [70, 71]. –Я–Њ—Б–ї–µ–і–љ–Є–є –њ—А–∞–Ї—В–Є—З–µ—Б–Ї–Є –љ–µ –≤—Б–∞—Б—Л–≤–∞–µ—В—Б—П –≤ –Ц–Ъ–Ґ –Є –љ–µ —Б–њ–Њ—Б–Њ–±–µ–љ –њ—А–µ–і–Њ—В–≤—А–∞—В–Є—В—М –≥—А–Є–±–Ї–Њ–≤—Г—О —Б—Г–њ–µ—А–Є–љ—Д–µ–Ї—Ж–Є—О –Є–љ–Њ–є –ї–Њ–Ї–∞–ї–Є–Ј–∞—Ж–Є–Є – –њ–Њ–ї–Њ—Б—В–Є —А—В–∞, –і—Л—Е–∞—В–µ–ї—М–љ—Л—Е –њ—Г—В–µ–є, –њ–Њ–ї–Њ–≤—Л—Е –Њ—А–≥–∞–љ–Њ–≤, –≥—А–Є–±–Ї–Њ–≤—Л–є —Б–µ–њ—Б–Є—Б [72].
–Ф–ї—П –Љ–љ–Њ–≥–Є—Е —А–Њ—Б—Б–Є–є—Б–Ї–Є—Е –≤—А–∞—З–µ–є —Е–∞—А–∞–Ї—В–µ—А–љ–∞ –Њ—Б–Њ–±–∞—П «–њ—А–Є–≤—П–Ј–∞–љ–љ–Њ—Б—В—М» –Ї –љ–∞–Ј–љ–∞—З–µ–љ–Є—О –Њ–±—Й–µ—Г–Ї—А–µ–њ–ї—П—О—Й–Є—Е –Є –Є–Љ–Љ—Г–љ–Њ—Б—В–Є–Љ—Г–ї–Є—А—Г—О—Й–Є—Е –њ—А–µ–њ–∞—А–∞—В–Њ–≤. –Я—А–Є —Н—В–Њ–Љ –≤ –†–Њ—Б—Б–Є–Є —И–Є—А–Њ–Ї–Њ –њ—А–Є–Љ–µ–љ—П—О—В—Б—П —В–∞–Ї–Є–µ –њ—А–µ–њ–∞—А–∞—В—Л, –Ї–∞–Ї –њ–Њ–ї–Є–Њ–Ї—Б–Є–і–Њ–љ–Є–є, –≥–ї—Г—В–∞–Љ–Є–ї-—В—А–Є–њ—В–Њ—Д–∞–љ, –і–Є–Њ–Ї—Б–Њ–Љ–µ—В–Є–ї—В–µ—В—А–∞–≥–Є–і—А–Њ–њ–Є—А–Є–Љ–Є–і–Є–љ, —В–Є–ї–Њ—А–Њ–љ –Є –і—А. –Ф–∞–љ–љ–∞—П –≥—А—Г–њ–њ–∞ –њ—А–µ–њ–∞—А–∞—В–Њ–≤ –Њ—В—Б—Г—В—Б—В–≤—Г–µ—В –≤ –Љ–µ–ґ–і—Г–љ–∞—А–Њ–і–љ—Л—Е —А–µ–Ї–Њ–Љ–µ–љ–і–∞—Ж–Є—П—Е –њ–Њ —В–µ—А–∞–њ–Є–Є –Є–љ—Д–µ–Ї—Ж–Є–Њ–љ–љ—Л—Е –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є–є, –∞ —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В—М –Є –љ–µ–Њ–±—Е–Њ–і–Є–Љ–Њ—Б—В—М –Є—Е –њ—А–Є–Љ–µ–љ–µ–љ–Є—П –љ–µ –і–Њ–Ї–∞–Ј–∞–љ—Л –≤ –Ї–Њ–љ—В—А–Њ–ї–Є—А—Г–µ–Љ—Л—Е –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є—Е –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П—Е [73].
–Ь–Є—Д 6. –Р–љ—В–Є–±–Є–Њ—В–Є–Ї–Є –≤—Л–Ј—Л–≤–∞—О—В –і–Є—Б–±–∞–Ї—В–µ—А–Є–Њ–Ј, –њ–Њ—Н—В–Њ–Љ—Г –њ–Њ—Б–ї–µ –Ї—Г—А—Б–∞ –∞–љ—В–Є–±–Є–Њ—В–Є–Ї–Њ–≤ –љ–µ–Њ–±—Е–Њ–і–Є–Љ–Њ –≤–Њ—Б—Б—В–∞–љ–∞–≤–ї–Є–≤–∞—В—М –Ї–Є—И–µ—З–љ—Г—О –Љ–Є–Ї—А–Њ—Д–ї–Њ—А—Г
–Ф–µ–є—Б—В–≤–Є—В–µ–ї—М–љ–Њ, –љ–∞–Є–±–Њ–ї–µ–µ —З–∞—Б—В—Л–Љ–Є –ґ–∞–ї–Њ–±–∞–Љ–Є —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ –љ–∞ —Д–Њ–љ–µ –њ—А–Є–Љ–µ–љ–µ–љ–Є—П –∞–љ—В–Є–±–Є–Њ—В–Є–Ї–Њ–≤ —П–≤–ї—П—О—В—Б—П –і–Є—Б–њ–µ–њ—Б–Є—З–µ—Б–Ї–Є–µ —А–∞—Б—Б—В—А–Њ–є—Б—В–≤–∞ (—В–Њ—И–љ–Њ—В–∞, —А–≤–Њ—В–∞, –і–Є–∞—А–µ—П). –Э–µ–ґ–µ–ї–∞—В–µ–ї—М–љ—Л–µ –ї–µ–Ї–∞—А—Б—В–≤–µ–љ–љ—Л–µ —А–µ–∞–Ї—Ж–Є–Є —Б–Њ —Б—В–Њ—А–Њ–љ—Л –Ц–Ъ–Ґ –Љ–Њ–≥—Г—В –±—Л—В—М –Ї–∞–Ї –њ–µ—А–≤–Є—З–љ—Л–Љ–Є, –Њ–±—Г—Б–ї–Њ–≤–ї–µ–љ–љ—Л–Љ–Є –љ–µ–њ–Њ—Б—А–µ–і—Б—В–≤–µ–љ–љ—Л–Љ –≤–Њ–Ј–і–µ–є—Б—В–≤–Є–µ–Љ –Р–Ь–Я –љ–∞ —Б—В—А—Г–Ї—В—Г—А—Л –њ–Є—Й–µ–≤–∞—А–Є—В–µ–ї—М–љ–Њ–≥–Њ —В—А–∞–Ї—В–∞, —В–∞–Ї –Є –Њ–њ–Њ—Б—А–µ–і–Њ–≤–∞–љ–љ—Л–Љ–Є – –≤ —А–µ–Ј—Г–ї—М—В–∞—В–µ –љ–∞—А—Г—И–µ–љ–Є—П –љ–Њ—А–Љ–∞–ї—М–љ–Њ–≥–Њ –±–Є–Њ—Ж–µ–љ–Њ–Ј–∞ (–љ–∞–њ—А–Є–Љ–µ—А, –љ–∞—А—Г—И–µ–љ–Є—П –≤–Ї—Г—Б–∞ –њ—А–Є –Њ—А–Њ—Д–∞—А–Є–љ–≥–µ–∞–ї—М–љ–Њ–Љ –Ї–∞–љ–і–Є–і–Њ–Ј–µ –Є–ї–Є —А–∞–Ј–≤–Є—В–Є–µ –∞–љ—В–Є–±–Є–Њ—В–Є–Ї-–∞—Б—Б–Њ—Ж–Є–Є—А–Њ–≤–∞–љ–љ–Њ–є –і–Є–∞—А–µ–Є (–Р–Р–Ф)). –Ь–љ–Њ–≥–Є–µ –∞–љ—В–Є–±–Є–Њ—В–Є–Ї–Є –Љ–Њ–≥—Г—В –Њ–Ї–∞–Ј—Л–≤–∞—В—М –≤–ї–Є—П–љ–Є–µ –љ–∞ –љ–Њ—А–Љ–∞–ї—М–љ—Г—О –Љ–Є–Ї—А–Њ—Д–ї–Њ—А—Г –Њ—А–≥–∞–љ–Є–Ј–Љ–∞, –њ—А–Є—З–µ–Љ –≤ –±–Њ–ї—М—И–µ–є —Б—В–µ–њ–µ–љ–Є —Б—В—А–∞–і–∞–µ—В –Љ–Є–Ї—А–Њ—Д–ї–Њ—А–∞ –њ–Њ–ї–Њ—Б—В–Є —А—В–∞ –Є –Ї–Є—И–µ—З–љ–Є–Ї–∞. –Ю–і–љ–∞–Ї–Њ –≤ –њ–Њ–і–∞–≤–ї—П—О—Й–µ–Љ –±–Њ–ї—М—И–Є–љ—Б—В–≤–µ —Б–ї—Г—З–∞–µ–≤ –њ—А–Є –њ—А–Є–Љ–µ–љ–µ–љ–Є–Є –∞–љ—В–Є–±–Є–Њ—В–Є–Ї–Њ–≤ –Є–Ј–Љ–µ–љ–µ–љ–Є—П –Ї–Њ–ї–Є—З–µ—Б—В–≤–µ–љ–љ–Њ–≥–Њ –Є –Ї–∞—З–µ—Б—В–≤–µ–љ–љ–Њ–≥–Њ —Б–Њ—Б—В–∞–≤–∞ –Љ–Є–Ї—А–Њ—Д–ї–Њ—А—Л –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є –љ–µ –њ—А–Њ—П–≤–ї—П—О—В—Б—П, –љ–µ —В—А–µ–±—Г—О—В –Ї–Њ—А—А–µ–Ї—Ж–Є–Є –Є –њ—А–Њ—Е–Њ–і—П—В —Б–∞–Љ–Њ—Б—В–Њ—П—В–µ–ї—М–љ–Њ.
–І–∞—Б—В–Њ—В–∞ –і–Є–∞—А–µ–Є –љ–∞ —Д–Њ–љ–µ –њ—А–Є–µ–Љ–∞ —А–∞–Ј–ї–Є—З–љ—Л—Е –Р–Ь–Я –≤–∞—А—М–Є—А—Г–µ—В –≤ —И–Є—А–Њ–Ї–Є—Е –њ—А–µ–і–µ–ї–∞—Е –Є —Б–Њ—Б—В–∞–≤–ї—П–µ—В 2–6% –њ—А–Є –њ—А–Є–Љ–µ–љ–µ–љ–Є–Є —Д—В–Њ—А—Е–Є–љ–Њ–ї–Њ–љ–Њ–≤ [74], –Њ–Ї–Њ–ї–Њ 15% –њ—А–Є —В–µ—А–∞–њ–Є–Є –∞–Љ–Њ–Ї—Б–Є—Ж–Є–ї–ї–Є–љ–Њ–Љ/–Ї–ї–∞–≤—Г–ї–∞–љ–∞—В–Њ–Љ [75] –Є –і–Њ 25% –њ—А–Є –љ–∞–Ј–љ–∞—З–µ–љ–Є–Є —Н—А–Є—В—А–Њ–Љ–Є—Ж–Є–љ–∞ [76]. –Ю–і–љ–∞–Ї–Њ —Б—А–µ–і–Є –≤—Б–µ—Е —Б–ї—Г—З–∞–µ–≤ –і–Є–∞—А–µ–Є –љ–∞ —Д–Њ–љ–µ —В–µ—А–∞–њ–Є–Є –Р–Ь–Я –љ–µ –±–Њ–ї–µ–µ 10–20% —Б–≤—П–Ј–∞–љ—Л —Б –Є–љ—Д–µ–Ї—Ж–Є–µ–є Clostridium (–°.) difficile. –Ґ–µ—А–∞–њ–Є—П –∞–љ—В–Є–±–Є–Њ—В–Є–Ї–∞–Љ–Є —И–Є—А–Њ–Ї–Њ–≥–Њ —Б–њ–µ–Ї—В—А–∞ –і–µ–є—Б—В–≤–Є—П –Љ–Њ–ґ–µ—В –≤—Л–Ј–≤–∞—В—М –њ–Њ–і–∞–≤–ї–µ–љ–Є–µ –љ–Њ—А–Љ–∞–ї—М–љ–Њ–є –љ–µ—Б–њ–Њ—А–Њ–Њ–±—А–∞–Ј—Г—О—Й–µ–є –∞–љ–∞—Н—А–Њ–±–љ–Њ–є –Љ–Є–Ї—А–Њ—Д–ї–Њ—А—Л —В–Њ–ї—Б—В–Њ–≥–Њ –Ї–Є—И–µ—З–љ–Є–Ї–∞, —З—В–Њ –њ—А–Є–≤–Њ–і–Є—В –Ї –Є–Ј–±—Л—В–Њ—З–љ–Њ–Љ—Г —А–Њ—Б—В—Г C. difficile –Є –њ–Њ—Б–ї–µ–і—Г—О—Й–µ–Љ—Г –≤—Л—Б–≤–Њ–±–Њ–ґ–і–µ–љ–Є—О —В–Њ–Ї—Б–Є–љ–Њ–≤ –Р –Є –Т –Є —А–∞–Ј–≤–Є—В–Є—О –Р–Р–Ф. –°–ї—Г—З–∞–Є –≤–Њ–Ј–љ–Є–Ї–љ–Њ–≤–µ–љ–Є—П –њ—Б–µ–≤–і–Њ–Љ–µ–Љ–±—А–∞–љ–Њ–Ј–љ–Њ–≥–Њ –Ї–Њ–ї–Є—В–∞ –Є –Р–Р–Ф –Њ–њ–Є—Б–∞–љ—Л –њ—А–Є –њ—А–Є–Љ–µ–љ–µ–љ–Є–Є –±–Њ–ї—М—И–Є–љ—Б—В–≤–∞ –Р–Ь–Я, –Њ–і–љ–∞–Ї–Њ —Б—З–Є—В–∞–µ—В—Б—П, —З—В–Њ –љ–∞–Є–±–Њ–ї–µ–µ —З–∞—Б—В–Њ —Н—В–Є —Б–Њ—Б—В–Њ—П–љ–Є—П –≤–Њ–Ј–љ–Є–Ї–∞—О—В –њ—А–Є –њ—А–Є–Љ–µ–љ–µ–љ–Є–Є –ї–Є–љ–Ї–Њ–Ј–∞–Љ–Є–і–Њ–≤, –њ–µ–љ–Є—Ж–Є–ї–ї–Є–љ–Њ–≤, —Ж–µ—Д–∞–ї–Њ—Б–њ–Њ—А–Є–љ–Њ–≤ –Є —Д—В–Њ—А—Е–Є–љ–Њ–ї–Њ–љ–Њ–≤ [77]. –Ъ–ї–Є–љ–Є—З–µ—Б–Ї–Є–µ –њ—А–Њ—П–≤–ї–µ–љ–Є—П –Р–Р–Ф –Љ–Њ–≥—Г—В –≤–∞—А—М–Є—А–Њ–≤–∞—В—М –Њ—В –ї–µ–≥–Ї–Њ–≥–Њ —Б–∞–Љ–Њ–Ї—Г–њ–Є—А—Г—О—Й–µ–≥–Њ—Б—П –і–Є–∞—А–µ–є–љ–Њ–≥–Њ —Б–Є–љ–і—А–Њ–Љ–∞ –і–Њ —В—П–ґ–µ–ї–µ–є—И–µ–≥–Њ –њ—Б–µ–≤–і–Њ–Љ–µ–Љ–±—А–∞–љ–Њ–Ј–љ–Њ–≥–Њ –Ї–Њ–ї–Є—В–∞, —В–Њ–Ї—Б–Є—З–µ—Б–Ї–Њ–≥–Њ –Љ–µ–≥–∞–Ї–Њ–ї–Њ–љ–∞, –њ–µ—А—Д–Њ—А–∞—Ж–Є–Є –Ї–Є—И–µ—З–љ–Є–Ї–∞, —Б–µ–њ—Б–Є—Б–∞ –Є –і–∞–ґ–µ –ї–µ—В–∞–ї—М–љ–Њ–≥–Њ –Є—Б—Е–Њ–і–∞ [78]. –†–∞–Ј–≤–Є—В–Є–µ –њ—Б–µ–≤–і–Њ–Љ–µ–Љ–±—А–∞–љ–Њ–Ј–љ–Њ–≥–Њ –Ї–Њ–ї–Є—В–∞ –љ–∞ —Д–Њ–љ–µ –Р–С–Ґ – –Њ–њ–∞—Б–љ–Њ–µ –Њ—Б–ї–Њ–ґ–љ–µ–љ–Є–µ, —В—А–µ–±—Г—О—Й–µ–µ –њ–Њ—Б—В–Њ—П–љ–љ–Њ–є –љ–∞—Б—В–Њ—А–Њ–ґ–µ–љ–љ–Њ—Б—В–Є –≤—А–∞—З–µ–є. –£ –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –ї–µ–≥–Ї–Њ–є –Р–Р–Ф –Њ—В–Љ–µ–љ–∞ –њ—А–Є—З–Є–љ–љ–Њ-–Ј–љ–∞—З–Є–Љ–Њ–≥–Њ –њ—А–µ–њ–∞—А–∞—В–∞ –Њ–±—Л—З–љ–Њ –±—Л–≤–∞–µ—В –і–Њ—Б—В–∞—В–Њ—З–љ–Њ–є –і–ї—П –Ї—Г–њ–Є—А–Њ–≤–∞–љ–Є—П —Б–Є–Љ–њ—В–Њ–Љ–Њ–≤, –≤ —В–Њ –≤—А–µ–Љ—П –Ї–∞–Ї –њ—А–Є —Б—А–µ–і–љ–µ—В—П–ґ–µ–ї—Л—Е –Є —В—П–ґ–µ–ї—Л—Е —Д–Њ—А–Љ–∞—Е –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П –њ–Њ–Љ–Є–Љ–Њ –Њ—В–Љ–µ–љ—Л –∞–љ—В–Є–±–∞–Ї—В–µ—А–Є–∞–ї—М–љ—Л—Е –њ—А–µ–њ–∞—А–∞—В–Њ–≤ (–Р–С–Я) –љ–µ–Њ–±—Е–Њ–і–Є–Љ–Њ –љ–∞–Ј–љ–∞—З–µ–љ–Є–µ –Љ–µ—В—А–Њ–љ–Є–і–∞–Ј–Њ–ї–∞ –Є–ї–Є –≤–∞–љ–Ї–Њ–Љ–Є—Ж–Є–љ–∞ –≤–љ—Г—В—А—М [78].
–Ю—Б—В–∞–ї—М–љ—Л–µ —Б–ї—Г—З–∞–Є –њ–Њ—А–∞–ґ–µ–љ–Є—П –Ц–Ъ–Ґ –≤—Л–Ј–≤–∞–љ—Л —Д—Г–љ–Ї—Ж–Є–Њ–љ–∞–ї—М–љ—Л–Љ–Є –љ–∞—А—Г—И–µ–љ–Є—П–Љ–Є –Љ–µ—В–∞–±–Њ–ї–Є–Ј–Љ–∞ —Г–≥–ї–µ–≤–Њ–і–Њ–≤ –Є–ї–Є –ґ–µ–ї—З–љ—Л—Е –Ї–Є—Б–ї–Њ—В –≤ –Ї–Є—И–µ—З–љ–Є–Ї–µ, –∞–ї–ї–µ—А–≥–Є—З–µ—Б–Ї–Є–Љ–Є –Є–ї–Є —В–Њ–Ї—Б–Є—З–µ—Б–Ї–Є–Љ–Є —Н—Д—Д–µ–Ї—В–∞–Љ–Є –Р–С–Я –Є–ї–Є —Д–∞—А–Љ–∞–Ї–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є–Љ –і–µ–є—Б—В–≤–Є–µ–Љ –Р–С–Я –љ–∞ –Љ–Њ—В–Њ—А–Є–Ї—Г –Ц–Ъ–Ґ. –Ъ–ї–∞–≤—Г–ї–∞–љ–Њ–≤–∞—П –Ї–Є—Б–ї–Њ—В–∞ –Є –µ–µ –Љ–µ—В–∞–±–Њ–ї–Є—В—Л —Г—Б–Є–ї–Є–≤–∞—О—В –Љ–Њ—В–Њ—А–Є–Ї—Г —В–Њ–љ–Ї–Њ–є –Ї–Є—И–Ї–Є [76].
–Э–µ–ї—М–Ј—П –љ–µ –њ–Њ–і—З–µ—А–Ї–љ—Г—В—М, —З—В–Њ –і–Є—Б–њ–µ–њ—Б–Є—З–µ—Б–Ї–Є–µ —А–∞—Б—Б—В—А–Њ–є—Б—В–≤–∞ –њ—А–Є –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є–Є –Љ–∞–Ї—А–Њ–ї–Є–і–Њ–≤ —Б–≤—П–Ј–∞–љ—Л —Б–Њ —Б—В–Є–Љ—Г–ї—П—Ж–Є–µ–є –њ–µ—А–Є—Б—В–∞–ї—М—В–Є–Ї–Є –Ї–Є—И–µ—З–љ–Є–Ї–∞ –Є–Ј-–Ј–∞ –∞–Ї—В–Є–≤–∞—Ж–Є–Є –Љ–Њ—В–Є–ї–Є–љ–Њ–≤—Л—Е —А–µ—Ж–µ–њ—В–Њ—А–Њ–≤ (—В–∞–Ї –љ–∞–Ј—Л–≤–∞–µ–Љ—Л–є –њ—А–Њ–Ї–Є–љ–µ—В–Є—З–µ—Б–Ї–Є–є —Н—Д—Д–µ–Ї—В), –Ї–Њ—В–Њ—А–∞—П –≤–Њ–Ј–љ–Є–Ї–∞–µ—В —Г –Ј–љ–∞—З–Є—В–µ–ї—М–љ–Њ–≥–Њ —З–Є—Б–ї–∞ –њ–∞—Ж–Є–µ–љ—В–Њ–≤ –њ—А–Є –њ—А–Є–Љ–µ–љ–µ–љ–Є–Є –≤ –Њ—Б–љ–Њ–≤–љ–Њ–Љ —Н—А–Є—В—А–Њ–Љ–Є—Ж–Є–љ–∞ [79]. «–Э–Њ–≤—Л–µ» –Љ–∞–Ї—А–Њ–ї–Є–і—Л, —В–∞–Ї–Є–µ –Ї–∞–Ї –∞–Ј–Є—В—А–Њ–Љ–Є—Ж–Є–љ (–°—Г–Љ–∞–Љ–µ–і®), —Е–∞—А–∞–Ї—В–µ—А–Є–Ј—Г—О—В—Б—П —Б—Г—Й–µ—Б—В–≤–µ–љ–љ–Њ –ї—Г—З—И–µ–є –њ–µ—А–µ–љ–Њ—Б–Є–Љ–Њ—Б—В—М—О, —З—В–Њ —Б–≤—П–Ј–∞–љ–Њ —Б –Љ–µ–љ–µ–µ –≤—Л—А–∞–ґ–µ–љ–љ—Л–Љ –њ—А–Њ–Ї–Є–љ–µ—В–Є—З–µ—Б–Ї–Є–Љ —Н—Д—Д–µ–Ї—В–Њ–Љ [80]. –Ґ–∞–Ї–Є–Љ –Њ–±—А–∞–Ј–Њ–Љ, –і–Є–∞—А–µ—П —П–≤–ї—П–µ—В—Б—П –Њ—З–µ–љ—М —З–∞—Б—В–Њ–є –ґ–∞–ї–Њ–±–Њ–є –њ—А–Є —В–µ—А–∞–њ–Є–Є –Љ–∞–Ї—А–Њ–ї–Є–і–∞–Љ–Є –Є –∞–Љ–Њ–Ї—Б–Є—Ж–Є–ї–ї–Є–љ–Њ–Љ/–Ї–ї–∞–≤—Г–ї–∞–љ–∞—В–Њ–Љ, –Њ–і–љ–∞–Ї–Њ –Њ–љ–∞, –Ї–∞–Ї –њ—А–∞–≤–Є–ї–Њ, –љ–µ –њ—А–µ–і—Б—В–∞–≤–ї—П–µ—В –Њ–њ–∞—Б–љ–Њ—Б—В–Є –і–ї—П –њ–∞—Ж–Є–µ–љ—В–∞, –∞ –Р–Р–Ф –љ–∞ —Д–Њ–љ–µ –ї–µ—З–µ–љ–Є—П –Љ–∞–Ї—А–Њ–ї–Є–і–∞–Љ–Є —А–∞–Ј–≤–Є–≤–∞–µ—В—Б—П –Ї—А–∞–є–љ–µ —А–µ–і–Ї–Њ.
–Ь–Є—Д 7. –Р–љ—В–Є–±–Є–Њ—В–Є–Ї–Є –љ–µ–Њ–±—Е–Њ–і–Є–Љ–Њ –њ—А–Є–Љ–µ–љ—П—В—М –і–ї—П —Б–∞–љ–∞—Ж–Є–Є –Њ—З–∞–≥–Њ–≤ –Є–љ—Д–µ–Ї—Ж–Є–Є
–Т–∞–ґ–љ–Њ –Ј–љ–∞—В—М, —З—В–Њ –≤—Л–і–µ–ї–µ–љ–Є–µ –Ј–Њ–ї–Њ—В–Є—Б—В—Л—Е —Б—В–∞—Д–Є–ї–Њ–Ї–Њ–Ї–Ї–Њ–≤ —Б –Ј–∞–і–љ–µ–є —Б—В–µ–љ–Ї–Є –≥–ї–Њ—В–Ї–Є –Є–ї–Є –Є–Ј –њ–Њ–ї–Њ—Б—В–Є –љ–Њ—Б–∞ –Є–ї–Є —Б –Ї–Њ–ґ–љ—Л—Е –њ–Њ–Ї—А–Њ–≤–Њ–≤ –љ–µ —П–≤–ї—П–µ—В—Б—П –њ–Њ–Ї–∞–Ј–∞–љ–Є–µ–Љ –Ї –љ–∞–Ј–љ–∞—З–µ–љ–Є—О –∞–љ—В–Є–±–Є–Њ—В–Є–Ї–Њ–≤ [81, 82]. –Т –љ–∞—Б—В–Њ—П—Й–µ–µ –≤—А–µ–Љ—П –µ—Б—В—М –µ–і–Є–љ—Б—В–≤–µ–љ–љ–Њ–µ –њ–Њ–Ї–∞–Ј–∞–љ–Є–µ –і–ї—П –ї–µ—З–µ–љ–Є—П –љ–Њ—Б–Є—В–µ–ї–µ–є –і–∞–љ–љ–Њ–≥–Њ –Љ–Є–Ї—А–Њ–Њ—А–≥–∞–љ–Є–Ј–Љ–∞ – –≤ —В–Њ–Љ —Б–ї—Г—З–∞–µ, –Ї–Њ–≥–і–∞ —Г—Б—В–∞–љ–Њ–≤–ї–µ–љ–Њ, —З—В–Њ –љ–Њ—Б–Є—В–µ–ї—М –Љ–µ—В–Є—Ж–Є–ї–ї–Є–љ–Њ—А–µ–Ј–Є—Б—В–µ–љ—В–љ–Њ–≥–Њ —И—В–∞–Љ–Љ–∞ S. aureus (–њ–∞—Ж–Є–µ–љ—В –Є–ї–Є —Б–Њ—В—А—Г–і–љ–Є–Ї —Б–њ–µ—Ж–Є–∞–ї–Є–Ј–Є—А–Њ–≤–∞–љ–љ–Њ–≥–Њ –Њ—В–і–µ–ї–µ–љ–Є—П, –љ–∞–њ—А–Є–Љ–µ—А, —Е–Є—А—Г—А–≥–Є—З–µ—Б–Ї–Њ–≥–Њ, —А–µ–∞–љ–Є–Љ–∞—Ж–Є–Є –Є –Є–љ—В–µ–љ—Б–Є–≤–љ–Њ–є —В–µ—А–∞–њ–Є–Є, —В—А–∞–љ—Б–њ–ї–∞–љ—В–Њ–ї–Њ–≥–Є–Є –Є –і—А.) —П–≤–Є–ї—Б—П –Є—Б—В–Њ—З–љ–Є–Ї–Њ–Љ –≤—Б–њ—Л—И–Ї–Є –љ–Њ–Ј–Њ–Ї–Њ–Љ–Є–∞–ї—М–љ–Њ–є –Є–љ—Д–µ–Ї—Ж–Є–Є –≤ –і–∞–љ–љ–Њ–Љ –Њ—В–і–µ–ї–µ–љ–Є–Є [84, 83]. –Ґ–Њ –ґ–µ —Б–∞–Љ–Њ–µ –Њ—В–љ–Њ—Б–Є—В—Б—П –Ї –±–µ—Б—Б–Є–Љ–њ—В–Њ–Љ–љ–Њ–є –±–∞–Ї—В–µ—А–Є—Г—А–Є–Є, –Ї–Њ—В–Њ—А–∞—П –љ–µ —В—А–µ–±—Г–µ—В –љ–∞–Ј–љ–∞—З–µ–љ–Є—П –Р–С–Ґ (–Є—Б–Ї–ї—О—З–µ–љ–Є–µ —Б–Њ—Б—В–∞–≤–ї—П—О—В –ї–Є—И—М –±–µ—А–µ–Љ–µ–љ–љ—Л–µ –њ–∞—Ж–Є–µ–љ—В–Ї–Є —Б –±–µ—Б—Б–Є–Љ–њ—В–Њ–Љ–љ–Њ–є –±–∞–Ї—В–µ—А–Є—Г—А–Є–µ–є –Є –њ–∞—Ж–Є–µ–љ—В—Л —Б –±–∞–Ї—В–µ—А–Є—Г—А–Є–µ–є –њ–µ—А–µ–і –Є–љ–≤–∞–Ј–Є–≤–љ—Л–Љ —Г—А–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є–Љ –≤–Љ–µ—И–∞—В–µ–ї—М—Б—В–≤–Њ–Љ – –Є–Љ –љ–µ–Њ–±—Е–Њ–і–Є–Љ–Њ –љ–∞–Ј–љ–∞—З–µ–љ–Є–µ –Р–Ь–Я) [85].
–І–∞—Б—В–Њ –≤—А–∞—З–Є –љ–∞–Ј–љ–∞—З–∞—О—В –љ–Є—Б—В–∞—В–Є–љ –Є–ї–Є –і—А—Г–≥–Њ–є –∞–љ—В–Є–Љ–Є–Ї–Њ—В–Є–Ї –≤ —Б–ї—Г—З–∞–µ –Њ–±–љ–∞—А—Г–ґ–µ–љ–Є—П –≤ –њ–Њ–ї–Њ—Б—В–Є —А—В–∞, –Љ–Њ—З–µ –Є–ї–Є –≤–∞–≥–Є–љ–∞–ї—М–љ–Њ–Љ –Љ–∞–Ј–Ї–µ –≥—А–Є–±–Њ–≤ —А–Њ–і–∞ –°andida, –Њ—А–Є–µ–љ—В–Є—А—Г—П—Б—М –њ—А–Є —Н—В–Њ–Љ –ї–Є—И—М –љ–∞ –і–∞–љ–љ—Л–µ –Љ–Є–Ї—А–Њ–±–Є–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Њ–≥–Њ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П –Є –љ–µ —Г—З–Є—В—Л–≤–∞—П –љ–∞–ї–Є—З–Є—П –Є–ї–Є –Њ—В—Б—Г—В—Б—В–≤–Є—П —Б–Є–Љ–њ—В–Њ–Љ–Њ–≤ –Ї–∞–љ–і–Є–і–Њ–Ј–∞ –Є —Д–∞–Ї—В–Њ—А–Њ–≤ —А–Є—Б–Ї–∞ —А–∞–Ј–≤–Є—В–Є—П –≥—А–Є–±–Ї–Њ–≤–Њ–є –Є–љ—Д–µ–Ї—Ж–Є–Є (—В—П–ґ–µ–ї—Л–є –Є–Љ–Љ—Г–љ–Њ–і–µ—Д–Є—Ж–Є—В –Є –і—А.). –Т—Л–і–µ–ї–µ–љ–Є–µ –≥—А–Є–±–Њ–≤ —А–Њ–і–∞ –°andida –Є–Ј –њ–Њ–ї–Њ—Б—В–Є —А—В–∞, –≤–ї–∞–≥–∞–ї–Є—Й–∞ –Є–ї–Є –Љ–Њ—З–µ–≤—Л—Е –њ—Г—В–µ–є –њ–∞—Ж–Є–µ–љ—В–Њ–≤ –≤ –±–Њ–ї—М—И–Є–љ—Б—В–≤–µ —Б–ї—Г—З–∞–µ–≤ (—Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ –±–µ–Ј —Д–∞–Ї—В–Њ—А–Њ–≤ —А–Є—Б–Ї–∞ —А–∞–Ј–≤–Є—В–Є—П –Њ—Б—В—А–Њ–≥–Њ –і–Є—Б—Б–µ–Љ–Є–љ–Є—А–Њ–≤–∞–љ–љ–Њ–≥–Њ –Ї–∞–љ–і–Є–і–Њ–Ј–∞) –Њ—В—А–∞–ґ–∞–µ—В –±–µ—Б—Б–Є–Љ–њ—В–Њ–Љ–љ—Г—О –Ї–Њ–ї–Њ–љ–Є–Ј–∞—Ж–Є—О, –љ–µ —В—А–µ–±—Г—О—Й—Г—О –љ–∞–Ј–љ–∞—З–µ–љ–Є—П —Б–Є—Б—В–µ–Љ–љ–Њ–є –њ—А–Њ—В–Є–≤–Њ–≥—А–Є–±–Ї–Њ–≤–Њ–є —В–µ—А–∞–њ–Є–Є, – –љ–µ–Њ–±—Е–Њ–і–Є–Љ–Њ –ї–Є—И—М —Г—Б—В—А–∞–љ–µ–љ–Є–µ –Є–ї–Є —Г–Љ–µ–љ—М—И–µ–љ–Є–µ –≤–ї–Є—П–љ–Є—П —Д–∞–Ї—В–Њ—А–Њ–≤ —А–Є—Б–Ї–∞ [66, 86, 87].
–Ь–Є—Д 8. –Ф–ї—П –і–Њ—Б—В–Є–ґ–µ–љ–Є—П –љ–∞–Є–ї—Г—З—И–µ–≥–Њ —Н—Д—Д–µ–Ї—В–∞ –∞–љ—В–Є–±–Є–Њ—В–Є–Ї —Б–ї–µ–і—Г–µ—В –і–Њ—Б—В–∞–≤–ї—П—В—М –љ–µ–њ–Њ—Б—А–µ–і—Б—В–≤–µ–љ–љ–Њ –≤ –Њ—З–∞–≥ –Є–љ—Д–µ–Ї—Ж–Є–Є, –Є—Б–њ–Њ–ї—М–Ј—Г—П –≤–љ—Г—В—А–Є–њ–Њ–ї–Њ—Б—В–љ–Њ–µ, –Є–љ—В—А–∞–∞—А—В–µ—А–Є–∞–ї—М–љ–Њ–µ, —Н–љ–і–Њ–ї–Є–Љ—Д–∞—В–Є—З–µ—Б–Ї–Њ–µ –≤–≤–µ–і–µ–љ–Є–µ –њ—А–µ–њ–∞—А–∞—В–∞
–Э–µ—Б–Њ–Љ–љ–µ–љ–љ–Њ, –њ—А–Є –љ–µ—В—П–ґ–µ–ї—Л—Е –Є–љ—Д–µ–Ї—Ж–Є—П—Е –≤–Њ –Љ–љ–Њ–≥–Є—Е —Б–ї—Г—З–∞—П—Е –љ–µ—В –љ–µ–Њ–±—Е–Њ–і–Є–Љ–Њ—Б—В–Є –≤ —Б–Є—Б—В–µ–Љ–љ–Њ–Љ –њ—А–Є–Љ–µ–љ–µ–љ–Є–Є –Р–Ь–Я. –Ґ–∞–Ї, –Љ–µ—Б—В–љ–Њ–µ –њ—А–Є–Љ–µ–љ–µ–љ–Є–µ –∞–љ—В–Є–±–Є–Њ—В–Є–Ї–Њ–≤ –Њ–њ—А–∞–≤–і–∞–љ–љ–Њ –њ—А–Є –њ–Њ–≤–µ—А—Е–љ–Њ—Б—В–љ—Л—Е –±–∞–Ї—В–µ—А–Є–∞–ї—М–љ—Л—Е –Є –≥—А–Є–±–Ї–Њ–≤—Л—Е –Є–љ—Д–µ–Ї—Ж–Є—П—Е –Ї–Њ–ґ–Є (–љ–∞–њ—А–Є–Љ–µ—А, –њ—А–Є–Љ–µ–љ–µ–љ–Є–µ –Ї—А–µ–Љ–∞ —Б –Ї–ї–Є–љ–і–∞–Љ–Є—Ж–Є–љ–Њ–Љ –њ—А–Є —Н—А–Є—В—А–∞–Ј–Љ–µ –Є–ї–Є –Љ–µ—Б—В–љ–Њ–µ –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є–µ –њ—А–Њ—В–Є–≤–Њ–≥—А–Є–±–Ї–Њ–≤—Л—Е –њ—А–µ–њ–∞—А–∞—В–Њ–≤ –њ—А–Є –њ–Њ–≤–µ—А—Е–љ–Њ—Б—В–љ—Л—Е –Љ–Є–Ї–Њ–Ј–∞—Е), –±–∞–Ї—В–µ—А–Є–∞–ї—М–љ–Њ–Љ –≤–∞–≥–Є–љ–Њ–Ј–µ, –Ї–∞–љ–і–Є–і–Њ–Ј–љ–Њ–Љ –≤—Г–ї—М–≤–Њ–≤–∞–≥–Є–љ–Є—В–µ, –Ї–Њ–љ—К—О–љ–Ї—В–Є–≤–Є—В–µ, –љ–∞—А—Г–ґ–љ–Њ–Љ –Њ—В–Є—В–µ [88–90]. –Ш–Љ–µ—О—В—Б—П –і–∞–љ–љ—Л–µ –Њ –≤—Л—Б–Њ–Ї–Њ–є —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В–Є –Љ–µ—Б—В–љ–Њ–≥–Њ –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є—П —Г—И–љ—Л—Е –Ї–∞–њ–µ–ї—М —Б —Д—В–Њ—А—Е–Є–љ–Њ–ї–Њ–љ–∞–Љ–Є (–Њ—Д–ї–Њ–Ї—Б–∞—Ж–Є–љ–Њ–Љ) –і–ї—П –ї–µ—З–µ–љ–Є—П –љ–∞—А—Г–ґ–љ–Њ–≥–Њ –Њ—В–Є—В–∞ –Є–ї–Є –Њ—Б—В—А–Њ–≥–Њ —Б—А–µ–і–љ–µ–≥–Њ –Њ—В–Є—В–∞ —Б –Њ—В–Њ—А–µ–µ–є (—В. –µ. –њ—А–Є —Г—Б–ї–Њ–≤–Є–Є –љ–∞–ї–Є—З–Є—П –њ–µ—А—Д–Њ—А–∞—Ж–Є–Є –±–∞—А–∞–±–∞–љ–љ–Њ–є –њ–µ—А–µ–њ–Њ–љ–Ї–Є, —З—В–Њ –Њ–±–µ—Б–њ–µ—З–Є–≤–∞–µ—В –і–Њ—Б—В–∞—В–Њ—З–љ–Њ–µ –њ—А–Њ–љ–Є–Ї–љ–Њ–≤–µ–љ–Є–µ –∞–љ—В–Є–±–Є–Њ—В–Є–Ї–∞ –≤ –њ–Њ–ї–Њ—Б—В—М —Б—А–µ–і–љ–µ–≥–Њ —Г—Е–∞) [20]. –Т —В–Њ –ґ–µ –≤—А–µ–Љ—П –њ—А–Є –±–Њ–ї–µ–µ –≥–ї—Г–±–Њ–Ї–Є—Е –Є —В—П–ґ–µ–ї—Л—Е –њ–Њ—А–∞–ґ–µ–љ–Є—П—Е, —Б–Є—Б—В–µ–Љ–љ—Л—Е –Є–љ—Д–µ–Ї—Ж–Є–Њ–љ–љ—Л—Е –њ—А–Њ—Ж–µ—Б—Б–∞—Е –Љ–µ—Б—В–љ–Њ–є –∞–љ—В–Є–Љ–Є–Ї—А–Њ–±–љ–Њ–є —В–µ—А–∞–њ–Є–Є –±—Г–і–µ—В –љ–µ–і–Њ—Б—В–∞—В–Њ—З–љ–Њ.
–Ш—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є–µ –∞–љ—В–Є–±–Є–Њ—В–Є–Ї–Њ–≤ –Љ–µ—Б—В–љ–Њ —З–∞—Б—В–Њ –Њ–Ї–∞–Ј—Л–≤–∞–µ—В—Б—П —Н—Д—Д–µ–Ї—В–Є–≤–љ—Л–Љ –њ—А–Є –ї–µ—З–µ–љ–Є–Є –Є–љ—Д–Є—Ж–Є—А–Њ–≤–∞–љ–љ—Л—Е —А–∞–љ. –Ґ–µ–Љ –љ–µ –Љ–µ–љ–µ–µ –Ї–Њ–Љ–±–Є–љ–∞—Ж–Є—П –Љ–µ—Б—В–љ–Њ–≥–Њ –Є —Б–Є—Б—В–µ–Љ–љ–Њ–≥–Њ –њ—А–Є–Љ–µ–љ–µ–љ–Є—П –Р–Ь–Я –љ–µ –Њ–±–ї–∞–і–∞–µ—В –±–Њ–ї—М—И–µ–є —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В—М—О, —З–µ–Љ –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є–µ —В–Њ–ї—М–Ї–Њ —Б–Є—Б—В–µ–Љ–љ—Л—Е –Є–ї–Є —В–Њ–ї—М–Ї–Њ –Љ–µ—Б—В–љ—Л—Е –∞–љ—В–Є–±–Є–Њ—В–Є–Ї–Њ–≤. –С–Њ–ї–µ–µ —В–Њ–≥–Њ, –Є–Ј–Њ–ї–Є—А–Њ–≤–∞–љ–љ–Њ–µ –Љ–µ—Б—В–љ–Њ–µ –њ—А–Є–Љ–µ–љ–µ–љ–Є–µ –∞–љ—В–Є–±–Є–Њ—В–Є–Ї–Њ–≤ –Ј–љ–∞—З–Є—В–µ–ї—М–љ–Њ —Г—Б—В—Г–њ–∞–µ—В –њ–Њ —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В–Є —Б–Є—Б—В–µ–Љ–љ–Њ–Љ—Г –њ—А–Є–Љ–µ–љ–µ–љ–Є—О. –Я—А–Є –Љ–µ—Б—В–љ–Њ–Љ –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є–Є –∞–љ—В–Є–±–Є–Њ—В–Є–Ї–Њ–≤ —Б–ї–µ–і—Г–µ—В —Б–Њ–±–ї—О–і–∞—В—М —Б–ї–µ–і—Г—О—Й–Є–µ –њ—А–Є–љ—Ж–Є–њ—Л:
1) –љ–µ –њ—А–Є–Љ–µ–љ—П—В—М –Љ–µ—Б—В–љ–Њ –≤ —А–∞–љ–µ –∞–љ—В–Є–±–Є–Њ—В–Є–Ї–Є, –Ї–Њ—В–Њ—А—Л–µ –≤ –і–∞–љ–љ–Њ–є —Б–Є—В—Г–∞—Ж–Є–Є –љ–µ –±—Л–ї–Є –±—Л –њ–Њ–Ї–∞–Ј–∞–љ—Л –Є –і–ї—П —Б–Є—Б—В–µ–Љ–љ–Њ–≥–Њ –њ—А–Є–Љ–µ–љ–µ–љ–Є—П;
2) –љ–µ –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞—В—М –±–Њ–ї—М—И–µ–µ —З–Є—Б–ї–Њ –∞–љ—В–Є–±–Є–Њ—В–Є–Ї–Њ–≤, —З–µ–Љ —Н—В–Њ –±—Л–ї–Њ –±—Л –љ–µ–Њ–±—Е–Њ–і–Є–Љ–Њ –њ—А–Є –Є—Е —Б–Є—Б—В–µ–Љ–љ–Њ–Љ –њ—А–Є–Љ–µ–љ–µ–љ–Є–Є –≤ –і–∞–љ–љ–Њ–є —Б–Є—В—Г–∞—Ж–Є–Є.
–Я—А–Є —А–∞—Б—З–µ—В–µ –Њ–±—Й–µ–є –і–Њ–Ј—Л —Б–ї–µ–і—Г–µ—В —Б—Г–Љ–Љ–Є—А–Њ–≤–∞—В—М –і–Њ–Ј—Л –њ—А–µ–њ–∞—А–∞—В–∞, –≤–≤–µ–і–µ–љ–љ–Њ–≥–Њ –њ–∞—А–µ–љ—В–µ—А–∞–ї—М–љ–Њ –Є –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–љ–Њ–≥–Њ –Љ–µ—Б—В–љ–Њ –≤ —А–∞–љ–µ. –Я—А–µ–њ–∞—А–∞—В—Л –і–ї—П –Љ–µ—Б—В–љ–Њ–≥–Њ –њ—А–Є–Љ–µ–љ–µ–љ–Є—П, –Є—Б–њ–Њ–ї—М–Ј—Г–µ–Љ—Л–µ —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –Њ–ґ–Њ–≥–Њ–≤—Л–Љ–Є —А–∞–љ–∞–Љ–Є, –Љ–Њ–≥—Г—В –њ—А–Є–Љ–µ–љ—П—В—М—Б—П –Є —Г –Њ—В–і–µ–ї—М–љ—Л—Е –Ї–∞—В–µ–≥–Њ—А–Є–є –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –Њ–±—И–Є—А–љ—Л–Љ–Є –Њ—В–Ї—А—Л—В—Л–Љ–Є —А–∞–љ–∞–Љ–Є.
–°–ї–µ–і—Г–µ—В –њ–Њ–Љ–љ–Є—В—М, —З—В–Њ –Љ–µ—Б—В–љ–Њ–µ –њ—А–Є–Љ–µ–љ–µ–љ–Є–µ –Р–Ь–Я, –њ—А–µ–і–љ–∞–Ј–љ–∞—З–µ–љ–љ—Л—Е –і–ї—П —Б–Є—Б—В–µ–Љ–љ–Њ–≥–Њ –≤–≤–µ–і–µ–љ–Є—П (–Њ–±–Ї–∞–ї—Л–≤–∞–љ–Є–µ —А–∞–љ—Л, –≤–≤–µ–і–µ–љ–Є–µ –≤ –і—А–µ–љ–∞–ґ–љ—Л–µ —В—А—Г–±–Ї–Є, –Њ—А–Њ—И–µ–љ–Є–µ –њ–Њ–ї–Њ—Б—В–µ–є –≤–Њ –≤—А–µ–Љ—П –Њ–њ–µ—А–∞—Ж–Є–Є) —Б —Ж–µ–ї—М—О –њ—А–Њ—Д–Є–ї–∞–Ї—В–Є–Ї–Є –Є–ї–Є –ї–µ—З–µ–љ–Є—П –Є–љ—Д–µ–Ї—Ж–Є–є –≤ –Њ–±–ї–∞—Б—В–Є —Е–Є—А—Г—А–≥–Є—З–µ—Б–Ї–Њ–≥–Њ –≤–Љ–µ—И–∞—В–µ–ї—М—Б—В–≤–∞ —П–≤–ї—П–µ—В—Б—П –љ–µ—Ж–µ–ї–µ—Б–Њ–Њ–±—А–∞–Ј–љ—Л–Љ –Є –љ–µ –Љ–Њ–ґ–µ—В —Б—А–∞–≤–љ–Є–≤–∞—В—М—Б—П –њ–Њ —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В–Є —Б –њ–∞—А–µ–љ—В–µ—А–∞–ї—М–љ—Л–Љ –љ–∞–Ј–љ–∞—З–µ–љ–Є–µ–Љ –∞–љ—В–Є–±–Є–Њ—В–Є–Ї–Њ–≤. –Т –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П—Е —Г—Б—В–∞–љ–Њ–≤–ї–µ–љ–Њ, —З—В–Њ –±–Њ–ї—М—И–Є–љ—Б—В–≤–Њ –Р–Ь–Я —А–∞–Ј—А—Г—И–∞–µ—В—Б—П –≤ —А–µ–Ј—Г–ї—М—В–∞—В–µ –≤–Ј–∞–Є–Љ–Њ–і–µ–є—Б—В–≤–Є—П —Б –њ—А–Њ–і—Г–Ї—В–∞–Љ–Є —А–∞—Б–њ–∞–і–∞ —В–Ї–∞–љ–µ–є, –±–∞–Ї—В–µ—А–Є–∞–ї—М–љ—Л–Љ–Є —В–Њ–Ї—Б–Є–љ–∞–Љ–Є –Є —Д–µ—А–Љ–µ–љ—В–∞–Љ–Є. –Ь–µ—Б—В–љ–Њ–µ –њ—А–Є–Љ–µ–љ–µ–љ–Є–µ —Б–Є—Б—В–µ–Љ–љ—Л—Е –∞–љ—В–Є–±–Є–Њ—В–Є–Ї–Њ–≤ –љ–µ –њ–Њ–Ј–≤–Њ–ї—П–µ—В —Б–Њ–Ј–і–∞—В—М –Њ–њ—В–Є–Љ–∞–ї—М–љ—Л–µ –±–∞–Ї—В–µ—А–Є—Ж–Є–і–љ—Л–µ –Ї–Њ–љ—Ж–µ–љ—В—А–∞—Ж–Є–Є –њ—А–µ–њ–∞—А–∞—В–∞ –≤ –Њ—З–∞–≥–µ –Є–љ—Д–µ–Ї—Ж–Є–Є –Є –Њ–Ї—А—Г–ґ–∞—О—Й–Є—Е —В–Ї–∞–љ—П—Е, —З—В–Њ –њ—А–Є–≤–Њ–і–Є—В –Ї —Д–Њ—А–Љ–Є—А–Њ–≤–∞–љ–Є—О –∞–љ—В–Є–±–Є–Њ—В–Є–Ї–Њ—А–µ–Ј–Є—Б—В–µ–љ—В–љ–Њ—Б—В–Є —Г –Љ–Є–Ї—А–Њ–Њ—А–≥–∞–љ–Є–Ј–Љ–Њ–≤. –Ъ—А–Њ–Љ–µ —В–Њ–≥–Њ, –њ—А–Є –Љ–µ—Б—В–љ–Њ–Љ –њ—А–Є–Љ–µ–љ–µ–љ–Є–Є –∞–љ—В–Є–±–Є–Њ—В–Є–Ї–Њ–≤ –њ—А–Њ–Є—Б—Е–Њ–і–Є—В —Б–µ–ї–µ–Ї—Ж–Є—П —А–µ–Ј–Є—Б—В–µ–љ—В–љ—Л—Е —И—В–∞–Љ–Љ–Њ–≤, –≤ —Б–≤—П–Ј–Є —Б —З–µ–Љ –љ–µ–ґ–µ–ї–∞—В–µ–ї—М–љ–Њ –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞—В—М –і–ї—П –Љ–µ—Б—В–љ–Њ–є —В–µ—А–∞–њ–Є–Є –њ—А–µ–њ–∞—А–∞—В—Л, –Є—Б–њ–Њ–ї—М–Ј—Г—О—Й–Є–µ—Б—П –Є –і–ї—П —Б–Є—Б—В–µ–Љ–љ–Њ–є —В–µ—А–∞–њ–Є–Є (–љ–∞–њ—А–Є–Љ–µ—А, –Љ–∞–Ј—М —Б –≥–µ–љ—В–∞–Љ–Є—Ж–Є–љ–Њ–Љ). –Я—А–µ–і–њ–Њ—З—В–µ–љ–Є–µ —Б–ї–µ–і—Г–µ—В –Њ—В–і–∞—В—М –∞–љ—В–Є—Б–µ–њ—В–Є–Ї–∞–Љ –ї–Є–±–Њ –∞–љ—В–Є–±–Є–Њ—В–Є–Ї–∞–Љ, –љ–µ –њ—А–Є–Љ–µ–љ—П—О—Й–Є–Љ—Б—П (–Є–ї–Є —А–µ–і–Ї–Њ –њ—А–Є–Љ–µ–љ—П—О—Й–Є–Љ—Б—П) —Б–Є—Б—В–µ–Љ–љ–Њ, —В–∞–Ї–Є–Љ –Ї–∞–Ї –Љ—Г–њ–Є—А–Њ—Ж–Є–љ –Є –њ–Њ–ї–Є–Љ–Є–Ї—Б–Є–љ. –Ґ–∞–Ї–Є–Љ –Њ–±—А–∞–Ј–Њ–Љ, –Љ–Њ–ґ–љ–Њ –Ј–∞–Ї–ї—О—З–Є—В—М, —З—В–Њ –Љ–µ—Б—В–љ–∞—П –∞–љ—В–Є–±–Є–Њ—В–Є–Ї–Њ—В–µ—А–∞–њ–Є—П, –±–µ–Ј—Г—Б–ї–Њ–≤–љ–Њ, –Њ–њ—А–∞–≤–і–∞–љ–љ–∞, –љ–Њ –ї–Є—И—М –њ–Њ –Њ–њ—А–µ–і–µ–ї–µ–љ–љ—Л–Љ –њ–Њ–Ї–∞–Ј–∞–љ–Є—П–Љ –Є —Б –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є–µ–Љ –Њ–њ—А–µ–і–µ–ї–µ–љ–љ—Л—Е –њ—А–µ–њ–∞—А–∞—В–Њ–≤.
–ѓ–≤–ї—П–µ—В—Б—П –љ–µ–Њ–±–Њ—Б–љ–Њ–≤–∞–љ–љ—Л–Љ –≤–љ—Г—В—А–Є–њ–Њ–ї–Њ—Б—В–љ–Њ–µ –≤–≤–µ–і–µ–љ–Є–µ –∞–љ—В–Є–±–Є–Њ—В–Є–Ї–Њ–≤, –≤ —З–∞—Б—В–љ–Њ—Б—В–Є, –≤ –њ–Њ–ї–Њ—Б—В–Є –Њ–Ї–Њ–ї–Њ–љ–Њ—Б–Њ–≤—Л—Е –њ–∞–Ј—Г—Е –њ—А–Є —Б–Є–љ—Г—Б–Є—В–µ [92], –≤–љ—Г—В—А–Є–њ–ї–µ–≤—А–∞–ї—М–љ–Њ–µ –≤–≤–µ–і–µ–љ–Є–µ –њ—А–Є –љ–∞–ї–Є—З–Є–Є –њ–ї–µ–≤—А–Є—В–∞ [73], —Н–љ–і–Њ–ї—О–Љ–±–∞–ї—М–љ–Њ–µ –≤–≤–µ–і–µ–љ–Є–µ –∞–љ—В–Є–±–Є–Њ—В–Є–Ї–Њ–≤ (—Е–ї–Њ—А–∞–Љ—Д–µ–љ–Є–Ї–Њ–ї + –њ–µ–љ–Є—Ж–Є–ї–ї–Є–љ, —Б—В—А–µ–њ—В–Њ–Љ–Є—Ж–Є–љ) –њ—А–Є –Є–љ—Д–µ–Ї—Ж–Є—П—Е –¶–Э–° [93], –њ—А–Є–Љ–µ–љ–µ–љ–Є–µ –∞–Љ–Є–љ–Њ–≥–ї–Є–Ї–Њ–Ј–Є–і–Њ–≤ –≤–љ—Г—В—А—М –і–ї—П –ї–µ—З–µ–љ–Є—П –Ї–Є—И–µ—З–љ—Л—Е –Є–љ—Д–µ–Ї—Ж–Є–є [94].
–Х—Й–µ –Њ–і–љ–∞ —А–∞–Ј–љ–Њ–≤–Є–і–љ–Њ—Б—В—М –Љ–µ—Б—В–љ–Њ–≥–Њ –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є—П –∞–љ—В–Є–±–Є–Њ—В–Є–Ї–Њ–≤ – –∞—Н—А–Њ–Ј–Њ–ї—М–љ—Л–є –њ—Г—В—М –≤–≤–µ–і–µ–љ–Є—П. –≠—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В—М –і–∞–љ–љ–Њ–≥–Њ –њ—Г—В–Є –≤–≤–µ–і–µ–љ–Є—П —П–≤–ї—П–µ—В—Б—П –Ї—А–∞–є–љ–µ —Б–Њ–Љ–љ–Є—В–µ–ї—М–љ–Њ–є. –Х–і–Є–љ—Б—В–≤–µ–љ–љ–Њ–µ –њ–Њ–Ї–∞–Ј–∞–љ–Є–µ –і–ї—П –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є—П —Н—В–Њ–≥–Њ —Б–њ–Њ—Б–Њ–±–∞ –≤–≤–µ–і–µ–љ–Є—П – —Н—В–Њ –ї–µ—З–µ–љ–Є–µ –Є–љ—Д–µ–Ї—Ж–Є–є –і—Л—Е–∞—В–µ–ї—М–љ—Л—Е –њ—Г—В–µ–є, –≤—Л–Ј–≤–∞–љ–љ—Л—Е Pseudomonas aeruginosa, –њ—А–Є –Љ—Г–Ї–Њ–≤–Є—Б—Ж–Є–і–Њ–Ј–µ (–Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є–µ –Ї–Њ–ї–Є—Б—В–Є–Љ–µ—В–∞—В–∞ –љ–∞—В—А–Є—П –Є–љ–≥–∞–ї—П—Ж–Є–Њ–љ–љ–Њ) [95]. –Р—Н—А–Њ–Ј–Њ–ї—М–љ—Л–є –њ—Г—В—М –≤–≤–µ–і–µ–љ–Є—П –Љ–Њ–ґ–µ—В –њ—А–Є–Љ–µ–љ—П—В—М—Б—П –≤ –Ї–∞—З–µ—Б—В–≤–µ –і–Њ–њ–Њ–ї–љ–Є—В–µ–ї—М–љ–Њ–є —В–µ—А–∞–њ–Є–Є —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –љ–Њ–Ј–Њ–Ї–Њ–Љ–Є–∞–ї—М–љ–Њ–є –њ–љ–µ–≤–Љ–Њ–љ–Є–µ–є, –≤—Л–Ј–≤–∞–љ–љ–Њ–є –њ–Њ–ї–Є—А–µ–Ј–Є—Б—В–µ–љ—В–љ—Л–Љ–Є –≥—А–∞–Љ–Њ—В—А–Є—Ж–∞—В–µ–ї—М–љ—Л–Љ–Є –Љ–Є–Ї—А–Њ–Њ—А–≥–∞–љ–Є–Ј–Љ–∞–Љ–Є –≤ —Б–ї—Г—З–∞–µ –љ–µ–і–Њ—Б—В–∞—В–Њ—З–љ–Њ–є —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В–Є —Б–Є—Б—В–µ–Љ–љ–Њ–є –Р–С–Ґ; —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В—М –Є –±–µ–Ј–Њ–њ–∞—Б–љ–Њ—Б—В—М –њ—А–Є–Љ–µ–љ–µ–љ–Є—П –љ–µ–Ї–Њ—В–Њ—А—Л—Е –Р–Ь–Я –∞—Н—А–Њ–Ј–Њ–ї—М–љ–Њ (–≤ —З–∞—Б—В–љ–Њ—Б—В–Є, –∞–Љ–Є–љ–Њ–≥–ї–Є–Ї–Њ–Ј–Є–і–Њ–≤) –≤ –љ–∞—Б—В–Њ—П—Й–µ–µ –≤—А–µ–Љ—П –Є–Ј—Г—З–∞—О—В—Б—П –≤ –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є—Е –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П—Е [95].
–С–Њ–ї—М—И–Є–љ—Б—В–≤–Њ —Б–Њ–≤—А–µ–Љ–µ–љ–љ—Л—Е –Р–Ь–Я (–њ–µ–љ–Є—Ж–Є–ї–ї–Є–љ—Л, —Ж–µ—Д–∞–ї–Њ—Б–њ–Њ—А–Є–љ—Л, –Ї–∞—А–±–∞–њ–µ–љ–µ–Љ—Л, —Д—В–Њ—А—Е–Є–љ–Њ–ї–Њ–љ—Л –Є –і—А.) –њ—А–Є –≤/–≤ –≤–≤–µ–і–µ–љ–Є–Є –≤ –∞–і–µ–Ї–≤–∞—В–љ—Л—Е –і–Њ–Ј–∞—Е –Є –њ—А–Є —Б–Њ–Њ—В–≤–µ—В—Б—В–≤—Г—О—Й–µ–є –і–ї—П –Ї–∞–ґ–і–Њ–≥–Њ –њ—А–µ–њ–∞—А–∞—В–∞ –Ї—А–∞—В–љ–Њ—Б—В–Є –≤–≤–µ–і–µ–љ–Є—П —Е–Њ—А–Њ—И–Њ –њ—А–Њ–љ–Є–Ї–∞—О—В –≤ –Њ—А–≥–∞–љ—Л –Є —В–Ї–∞–љ–Є –Є —Б–Њ–Ј–і–∞—О—В –≤ –љ–Є—Е –і–Њ—Б—В–∞—В–Њ—З–љ—Л–µ —В–µ—А–∞–њ–µ–≤—В–Є—З–µ—Б–Ї–Є–µ –Ї–Њ–љ—Ж–µ–љ—В—А–∞—Ж–Є–Є, –њ–Њ—Н—В–Њ–Љ—Г –≤–≤–µ–і–µ–љ–Є—П –Є—Е –љ–µ–њ–Њ—Б—А–µ–і—Б—В–≤–µ–љ–љ–Њ –≤ –Њ—З–∞–≥ –Є–љ—Д–µ–Ї—Ж–Є–Є –љ–µ —В—А–µ–±—Г–µ—В—Б—П.
–°–Њ–≤—А–µ–Љ–µ–љ–љ—Л–µ –Љ–∞–Ї—А–Њ–ї–Є–і—Л —Б —Г–ї—Г—З—И–µ–љ–љ—Л–Љ–Є —Д–∞—А–Љ–∞–Ї–Њ–Ї–Є–љ–µ—В–Є—З–µ—Б–Ї–Є–Љ–Є —Б–≤–Њ–є—Б—В–≤–∞–Љ–Є, —В–∞–Ї–Є–µ –Ї–∞–Ї –∞–Ј–Є—В—А–Њ–Љ–Є—Ж–Є–љ (–°—Г–Љ–∞–Љ–µ–і®), –Њ–±–ї–∞–і–∞—О—В —Г–љ–Є–Ї–∞–ї—М–љ–Њ–є —В–Ї–∞–љ–µ–≤–Њ–є –љ–∞–њ—А–∞–≤–ї–µ–љ–љ–Њ—Б—В—М—О –Є —Б–њ–Њ—Б–Њ–±–љ–Њ—Б—В—М—О —Д–Њ—А–Љ–Є—А–Њ–≤–∞—В—М –Љ–∞–Ї—Б–Є–Љ–∞–ї—М–љ—Л–µ –Ї–Њ–љ—Ж–µ–љ—В—А–∞—Ж–Є–Є –≤ –Њ—З–∞–≥–∞—Е –Є–љ—Д–µ–Ї—Ж–Є–Є. –Ъ –њ—А–µ–Є–Љ—Г—Й–µ—Б—В–≤–∞–Љ —Д–∞—А–Љ–∞–Ї–Њ–Ї–Є–љ–µ—В–Є–Ї–Є –∞–Ј–Є—В—А–Њ–Љ–Є—Ж–Є–љ–∞ –Њ—В–љ–Њ—Б–Є—В—Б—П –љ–Є–Ј–Ї–Є–є —Г—А–Њ–≤–µ–љ—М —Б–≤—П–Ј—Л–≤–∞–љ–Є—П —Б –±–µ–ї–Ї–∞–Љ–Є –њ–ї–∞–Ј–Љ—Л (7–51%), —З—В–Њ –њ–Њ–Ј–≤–Њ–ї—П–µ—В –њ—А–µ–њ–∞—А–∞—В—Г –±—Л—Б—В—А–µ–µ –њ–µ—А–µ–Љ–µ—Й–∞—В—М—Б—П –Є–Ј —Б–Њ—Б—Г–і–Є—Б—В–Њ–≥–Њ —А—Г—Б–ї–∞ –≤ —В–Ї–∞–љ–Є. –Т—Л—Б–Њ–Ї–∞—П –ї–Є–њ–Њ—Д–Є–ї—М–љ–Њ—Б—В—М –∞–Ј–Є—В—А–Њ–Љ–Є—Ж–Є–љ–∞ —В–∞–Ї–ґ–µ —Б–њ–Њ—Б–Њ–±—Б—В–≤—Г–µ—В –µ–≥–Њ —Е–Њ—А–Њ—И–µ–Љ—Г –њ—А–Њ–љ–Є–Ї–љ–Њ–≤–µ–љ–Є—О –≤ —В–Ї–∞–љ–Є –Є –љ–∞–Ї–Њ–њ–ї–µ–љ–Є—О –≤ –љ–Є—Е, –Њ —З–µ–Љ —Б–≤–Є–і–µ—В–µ–ї—М—Б—В–≤—Г–µ—В –±–Њ–ї—М—И–Њ–є –Њ–±—К–µ–Љ —А–∞—Б–њ—А–µ–і–µ–ї–µ–љ–Є—П – 31,1 –ї/–Ї–≥. –Т—Б–µ —Н—В–Њ –≤–µ–і–µ—В –Ї —В–Њ–Љ—Г, —З—В–Њ –Ї–Њ–љ—Ж–µ–љ—В—А–∞—Ж–Є–Є –∞–Ј–Є—В—А–Њ–Љ–Є—Ж–Є–љ–∞ –≤ —В–Ї–∞–љ—П—Е –≤ –і–µ—Б—П—В–Ї–Є –Є —Б–Њ—В–љ–Є —А–∞–Ј –њ—А–µ–≤—Л—И–∞—О—В —Б—Л–≤–Њ—А–Њ—В–Њ—З–љ—Л–µ (–љ–∞–њ—А–Є–Љ–µ—А, –≤ —Б–ї–Є–Ј–Є—Б—В–Њ–є –Њ–±–Њ–ї–Њ—З–Ї–µ –±—А–Њ–љ—Е–Њ–≤ – –і–Њ 240 —А–∞–Ј, –∞ –≤ –ґ–Є–і–Ї–Њ—Б—В–Є –∞–ї—М–≤–µ–Њ–ї—П—А–љ–Њ–≥–Њ —Н–њ–Є—В–µ–ї–Є—П – –і–Њ 80 —А–∞–Ј) –Є –њ–Њ–і–і–µ—А–ґ–Є–≤–∞—О—В—Б—П –љ–∞ –≤—Л—Б–Њ–Ї–Њ–Љ —Г—А–Њ–≤–љ–µ –≤ —В–µ—З–µ–љ–Є–µ 5–7 –і–љ–µ–є –њ–Њ—Б–ї–µ –µ–≥–Њ –Њ—В–Љ–µ–љ—Л.
–Р–Ј–Є—В—А–Њ–Љ–Є—Ж–Є–љ —Е–Њ—А–Њ—И–Њ –њ—А–Њ–љ–Є–Ї–∞–µ—В –≤–љ—Г—В—А—М –Ї–ї–µ—В–Њ–Ї (–≤–Ї–ї—О—З–∞—П —Н–њ–Є—В–µ–ї–Є–Њ—Ж–Є—В—Л, –Љ–∞–Ї—А–Њ—Д–∞–≥–Є, —Д–Є–±—А–Њ–±–ї–∞—Б—В—Л –Є –і—А.) –Є —Б–Њ–Ј–і–∞–µ—В –і–ї–Є—В–µ–ї—М–љ–Њ —Б–Њ—Е—А–∞–љ—П—О—Й–Є–µ—Б—П –≤—Л—Б–Њ–Ї–Є–µ –≤–љ—Г—В—А–Є–Ї–ї–µ—В–Њ—З–љ—Л–µ –Ї–Њ–љ—Ж–µ–љ—В—А–∞—Ж–Є–Є, –і–Њ 1200 —А–∞–Ј –њ—А–µ–≤—Л—И–∞—О—Й–Є–µ –Ї–Њ–љ—Ж–µ–љ—В—А–∞—Ж–Є—О –≤ –Ї—А–Њ–≤–Є. –Э–∞–Є–±–Њ–ї—М—И–µ–µ –љ–∞–Ї–Њ–њ–ї–µ–љ–Є–µ –Њ—В–Љ–µ—З–∞–µ—В—Б—П –≤ —Д–Њ—Б—Д–Њ–ї–Є–њ–Є–і–љ–Њ–Љ —Б–ї–Њ–µ –Љ–µ–Љ–±—А–∞–љ –ї–Є–Ј–Њ—Б–Њ–Љ —Д–∞–≥–Њ—Ж–Є—В–Є—А—Г—О—Й–Є—Е –Ї–ї–µ—В–Њ–Ї –Ї—А–Њ–≤–Є (–љ–µ–є—В—А–Њ—Д–Є–ї–Њ–≤, –Љ–Њ–љ–Њ—Ж–Є—В–Њ–≤) –Є —В–Ї–∞–љ–µ–є (–∞–ї—М–≤–µ–Њ–ї—П—А–љ—Л—Е –Љ–∞–Ї—А–Њ—Д–∞–≥–Њ–≤). –§–∞–≥–Њ—Ж–Є—В—Л, –љ–∞—Б—Л—Й–µ–љ–љ—Л–µ –∞–Ј–Є—В—А–Њ–Љ–Є—Ж–Є–љ–Њ–Љ, —В—А–∞–љ—Б–њ–Њ—А—В–Є—А—Г—О—В –µ–≥–Њ –≤ –Њ—З–∞–≥ –Є–љ—Д–µ–Ї—Ж–Є–Њ–љ–љ–Њ–≥–Њ –≤–Њ—Б–њ–∞–ї–µ–љ–Є—П –Ј–∞ —Б—З–µ—В –Љ–Є–≥—А–∞—Ж–Є–Є –њ–Њ–і –≤–ї–Є—П–љ–Є–µ–Љ —Б–µ–Ї—А–µ—В–Є—А—Г–µ–Љ—Л—Е –±–∞–Ї—В–µ—А–Є—П–Љ–Є —Е–µ–Љ–Њ—В–∞–Ї—Б–Є—З–µ—Б–Ї–Є—Е —Д–∞–Ї—В–Њ—А–Њ–≤, —Б–Њ–Ј–і–∞–≤–∞—П –≤ –љ–µ–Љ –Ї–Њ–љ—Ж–µ–љ—В—А–∞—Ж–Є—О –∞–љ—В–Є–±–Є–Њ—В–Є–Ї–∞ –≤—Л—И–µ, —З–µ–Љ –≤ –Ј–і–Њ—А–Њ–≤—Л—Е —В–Ї–∞–љ—П—Е, –њ—А–Є—З–µ–Љ —Б—В–µ–њ–µ–љ—М –Ї–Њ–љ—Ж–µ–љ—В—А–∞—Ж–Є–Є –Ї–Њ—А—А–µ–ї–Є—А—Г–µ—В —Б –≤—Л—А–∞–ґ–µ–љ–љ–Њ—Б—В—М—О –≤–Њ—Б–њ–∞–ї–Є—В–µ–ї—М–љ–Њ–≥–Њ –Њ—В–µ–Ї–∞. –Т—Л—Б–≤–Њ–±–Њ–ґ–і–µ–љ–Є–µ –Є–Ј –Љ–∞–Ї—А–Њ—Д–∞–≥–Њ–≤, –љ–µ–є—В—А–Њ—Д–Є–ї–Њ–≤ –Є –Љ–Њ–љ–Њ—Ж–Є—В–Њ–≤ –њ—А–Њ–Є—Б—Е–Њ–і–Є—В –≤ –њ—А–Њ—Ж–µ—Б—Б–µ —Д–∞–≥–Њ—Ж–Є—В–Њ–Ј–∞ –њ–Њ–і –і–µ–є—Б—В–≤–Є–µ–Љ –±–∞–Ї—В–µ—А–Є–∞–ї—М–љ—Л—Е —Б—В–Є–Љ—Г–ї–Њ–≤ [96, 97]. –Ґ–∞–Ї–∞—П –љ–∞–њ—А–∞–≤–ї–µ–љ–љ–∞—П –і–Њ—Б—В–∞–≤–Ї–∞ –∞–љ—В–Є–±–Є–Њ—В–Є–Ї–∞ –Є–Љ–µ–µ—В –Њ—Б–Њ–±–Њ–µ –Ј–љ–∞—З–µ–љ–Є–µ –≤ —Б–ї—Г—З–∞–µ –Є–љ—Д–µ–Ї—Ж–Є–Є –≤ –Њ–≥—А–∞–љ–Є—З–µ–љ–љ—Л—Е –ї–Њ–Ї—Г—Б–∞—Е. –Ъ—А–Њ–Љ–µ —В–Њ–≥–Њ, –љ–∞–Ї–Њ–њ–ї–µ–љ–Є–µ –∞–Ј–Є—В—А–Њ–Љ–Є—Ж–Є–љ–∞ –≤ –ї–Є–Ј–Њ—Б–Њ–Љ–∞—Е —Д–∞–≥–Њ—Ж–Є—В–Є—А—Г—О—Й–Є—Е –Ї–ї–µ—В–Њ–Ї –Њ–±–µ—Б–њ–µ—З–Є–≤–∞–µ—В —В–µ—А–∞–њ–µ–≤—В–Є—З–µ—Б–Ї–Є–µ –Ї–Њ–љ—Ж–µ–љ—В—А–∞—Ж–Є–Є –њ—А–µ–њ–∞—А–∞—В–Њ–≤ –≤ —Д–∞–≥–Њ–ї–Є–Ј–Њ—Б–Њ–Љ–∞—Е –Є —Ж–Є—В–Њ–њ–ї–∞–Ј–Љ–µ, —З—В–Њ –Њ—Б–Њ–±–µ–љ–љ–Њ –≤–∞–ґ–љ–Њ —Б —В–Њ—З–Ї–Є –Ј—А–µ–љ–Є—П –≤–Њ–Ј–і–µ–є—Б—В–≤–Є—П –љ–∞ –≤–љ—Г—В—А–Є–Ї–ї–µ—В–Њ—З–љ—Л—Е –≤–Њ–Ј–±—Г–і–Є—В–µ–ї–µ–є (Chlamydophila spp., Legionella spp., Mycoplasma spp.) –Є –Њ–±—Л—З–љ—Л—Е –њ–∞—В–Њ–≥–µ–љ–Њ–≤, –Ї–Њ—В–Њ—А—Л–µ –≤ –љ–µ–Ї–Њ—В–Њ—А—Л—Е —Б–Є—В—Г–∞—Ж–Є—П—Е –Љ–Њ–≥—Г—В –љ–∞—Е–Њ–і–Є—В—М—Б—П –≤–љ—Г—В—А–Є –Ї–ї–µ—В–Њ–Ї (–љ–∞–њ—А–Є–Љ–µ—А, Streptococcus pyogenes).
–Я—А–Є –≤–љ—Г—В—А–Є–њ–Њ–ї–Њ—Б—В–љ–Њ–Љ –Є–ї–Є —Н–љ–і–Њ–ї–Є–Љ—Д–∞—В–Є—З–µ—Б–Ї–Њ–Љ –≤–≤–µ–і–µ–љ–Є–Є –∞–љ—В–Є–±–Є–Њ—В–Є–Ї–Њ–≤ –љ–µ–≤–Њ–Ј–Љ–Њ–ґ–љ–Њ –њ—А–Њ–≥–љ–Њ–Ј–Є—А–Њ–≤–∞—В—М –Є—Е —Д–∞—А–Љ–∞–Ї–Њ–Ї–Є–љ–µ—В–Є–Ї—Г, –Є –Ї–Њ–љ—Ж–µ–љ—В—А–∞—Ж–Є–Є –њ—А–µ–њ–∞—А–∞—В–∞ –≤ –Њ—З–∞–≥–µ –Є–љ—Д–µ–Ї—Ж–Є–Є –Є —Б—Л–≤–Њ—А–Њ—В–Ї–µ –Ї—А–Њ–≤–Є –Њ–Ї–∞–Ј—Л–≤–∞—О—В—Б—П –Ї—А–∞–є–љ–µ –≤–∞—А–Є–∞–±–µ–ї—М–љ—Л–Љ–Є —Г —А–∞–Ј–ї–Є—З–љ—Л—Е –њ–∞—Ж–Є–µ–љ—В–Њ–≤. –Я—А–Є —Н—В–Њ–Љ –Ї–Њ–љ—Ж–µ–љ—В—А–∞—Ж–Є–Є –Љ–Њ–≥—Г—В –±—Л—В—М –Ї–∞–Ї —Б—Г–±—В–µ—А–∞–њ–µ–≤—В–Є—З–µ—Б–Ї–Є–Љ–Є (—З—В–Њ –њ—А–Є–≤–Њ–і–Є—В –Ї –љ–µ—Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В–Є —В–µ—А–∞–њ–Є–Є –Є —А–Є—Б–Ї—Г —А–∞–Ј–≤–Є—В–Є—П —А–µ–Ј–Є—Б—В–µ–љ—В–љ–Њ—Б—В–Є —Г –≤–Њ–Ј–±—Г–і–Є—В–µ–ї–µ–є), —В–∞–Ї –Є —В–Њ–Ї—Б–Є—З–µ—Б–Ї–Є–Љ–Є (—Б —А–∞–Ј–≤–Є—В–Є–µ–Љ —В—П–ґ–µ–ї—Л—Е –љ–µ–ґ–µ–ї–∞—В–µ–ї—М–љ—Л—Е —А–µ–∞–Ї—Ж–Є–є —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤). –Ъ—А–Њ–Љ–µ —В–Њ–≥–Њ, —Б–∞–Љ–Њ –њ–Њ —Б–µ–±–µ –≤–љ—Г—В—А–Є–њ–Њ–ї–Њ—Б—В–љ–Њ–µ, –Є–љ—В—А–∞–∞—А—В–µ—А–Є–∞–ї—М–љ–Њ–µ –Є —Н–љ–і–Њ–ї–Є–Љ—Д–∞—В–Є—З–µ—Б–Ї–Њ–µ –≤–≤–µ–і–µ–љ–Є–µ –њ—А–µ–њ–∞—А–∞—В–Њ–≤ —П–≤–ї—П–µ—В—Б—П –і–Њ—Б—В–∞—В–Њ—З–љ–Њ —Б–ї–Њ–ґ–љ–Њ–є –Є–љ–≤–∞–Ј–Є–≤–љ–Њ–є –њ—А–Њ—Ж–µ–і—Г—А–Њ–є, —Б–њ–Њ—Б–Њ–±–љ–Њ–є –њ—А–Є–≤–µ—Б—В–Є –Ї —Ж–µ–ї–Њ–Љ—Г —А—П–і—Г —Б–µ—А—М–µ–Ј–љ—Л—Е –Њ—Б–ї–Њ–ґ–љ–µ–љ–Є–є —Г –њ–∞—Ж–Є–µ–љ—В–∞. –Я—А–Є–љ–Є–Љ–∞—П –≤–Њ –≤–љ–Є–Љ–∞–љ–Є–µ –Њ—Б–љ–Њ–≤–Њ–њ–Њ–ї–∞–≥–∞—О—Й–Є–є –њ—А–Є–љ—Ж–Є–њ –Љ–µ–і–Є—Ж–Є–љ—Л «Non nocere» – «–Э–µ –љ–∞–≤—А–µ–і–Є», –Њ—В —В–∞–Ї–Є—Е –Љ–µ—В–Њ–і–Њ–≤ –і–Њ—Б—В–∞–≤–Ї–Є –∞–љ—В–Є–±–Є–Њ—В–Є–Ї–Њ–≤ –≤ –Њ—З–∞–≥ –Є–љ—Д–µ–Ї—Ж–Є–Є —Б–ї–µ–і—Г–µ—В –Њ—В–Ї–∞–Ј–∞—В—М—Б—П –≤–Њ–Њ–±—Й–µ.
–Ч–∞–Ї–ї—О—З–µ–љ–Є–µ: –≤ –і–∞–љ–љ–Њ–є –њ—Г–±–ї–Є–Ї–∞—Ж–Є–Є –Љ—Л –њ–Њ—Б—В–∞—А–∞–ї–Є—Б—М —А–∞—Б—Б–Љ–Њ—В—А–µ—В—М –љ–∞–Є–±–Њ–ї–µ–µ —А–∞—Б–њ—А–Њ—Б—В—А–∞–љ–µ–љ–љ—Л–µ –Ј–∞–±–ї—Г–ґ–і–µ–љ–Є—П, –Ї–∞—Б–∞—О—Й–Є–µ—Б—П –њ—А–Є–Љ–µ–љ–µ–љ–Є—П –Р–С–Я –≤ –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Њ–є –њ—А–∞–Ї—В–Є–Ї–µ. –Т–µ—А–Њ—П—В–љ–Њ, –±–Њ–ї—М—И–Є–љ—Б—В–≤—Г —З–Є—В–∞—В–µ–ї–µ–є –љ–∞—И–Є —А–∞—Б—Б—Г–ґ–і–µ–љ–Є—П –њ–Њ–Ї–∞–ґ—Г—В—Б—П –∞–Ј–±—Г—З–љ—Л–Љ–Є –Є—Б—В–Є–љ–∞–Љ–Є. –Т —В–Њ –ґ–µ –≤—А–µ–Љ—П –µ—Б–ї–Є –њ—А–∞–Ї—В–Є—З–µ—Б–Ї–Є–Љ –≤—А–∞—З–∞–Љ –њ—А–Є –љ–∞–Ј–љ–∞—З–µ–љ–Є–Є –Р–С–Ґ –њ–∞—Ж–Є–µ–љ—В–∞–Љ —Г–і–∞—Б—В—Б—П –Є–Ј–±–µ–ґ–∞—В—М –њ–Њ–і–Њ–±–љ—Л—Е –Њ—И–Є–±–Њ—З–љ—Л—Е —Б—Г–ґ–і–µ–љ–Є–є, —Н—В–Њ –њ—А–Є–≤–µ–і–µ—В –Ї –љ–µ—Б–Њ–Љ–љ–µ–љ–љ–Њ–Љ—Г —Г–ї—Г—З—И–µ–љ–Є—О –Ї–∞—З–µ—Б—В–≤–∞, –њ–Њ–≤—Л—И–µ–љ–Є—О —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В–Є –Є –±–µ–Ј–Њ–њ–∞—Б–љ–Њ—Б—В–Є –ї–µ—З–µ–љ–Є—П –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –Є–љ—Д–µ–Ї—Ж–Є—П–Љ–Є –≤ –њ–Њ–≤—Б–µ–і–љ–µ–≤–љ–Њ–є –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Њ–є –њ—А–∞–Ї—В–Є–Ї–µ.
C—В–∞—В—М—П –њ–Њ–і–≥–Њ—В–Њ–≤–ї–µ–љ–∞ –њ—А–Є –њ–Њ–і–і–µ—А–ґ–Ї–µ –Ю–Ю–Ю «–Ґ–µ–≤–∞» –†–Њ—Б—Б–Є—П, –Ь–Њ—Б–Ї–≤–∞, 119049, —Г–ї. –®–∞–±–Њ–ї–Њ–≤–Ї–∞,10, –Ї–Њ—А–њ. 1, –±–Є–Ј–љ–µ—Б-—Ж–µ–љ—В—А «–Ъ–Њ–љ–Ї–Њ—А–і», —Б–µ–Ї—В–Њ—А –Р, 3 —Н—В–∞–ґ


–Ы–Є—В–µ—А–∞—В—Г—А–∞
1. –†–µ—И–µ–і—М–Ї–Њ –У.–Ъ., –Ъ–Њ–Ј–ї–Њ–≤ –†.–°. –°–Њ—Б—В–Њ—П–љ–Є–µ —А–µ–Ј–Є—Б—В–µ–љ—В–љ–Њ—Б—В–Є –Ї –∞–љ—В–Є–Є–љ—Д–µ–Ї—Ж–Є–Њ–љ–љ—Л–Љ —Е–Є–Љ–Є–Њ–њ—А–µ–њ–∞—А–∞—В–∞–Љ –≤ –†–Њ—Б—Б–Є–Є. –Я—А–∞–Ї—В–Є—З–µ—Б–Ї–Њ–µ —А—Г–Ї–Њ–≤–Њ–і—Б—В–≤–Њ –њ–Њ –∞–љ—В–Є–Є–љ—Д–µ–Ї—Ж–Є–Њ–љ–Њ–є —Е–Є–Љ–Є–Њ—В–µ—А–∞–њ–Є–Є / –њ–Њ–і —А–µ–і. –Ы.–°. –°—В—А–∞—З—Г–љ—Б–Ї–Њ–≥–Њ, –Ѓ.–С. –С–µ–ї–Њ—Г—Б–Њ–≤–∞, –°.–Э. –Ъ–Њ–Ј–ї–Њ–≤–∞ –Ь.: –†–¶ «–§–∞—А–Љ–µ–і–Є–љ—Д–Њ», 2007. –°. 32–46.
2. Levy S.B. Starting life resistance-free // N Engl J Med. 1990. Vol. 323. –†. 335–337.
3. Rudholm N. Economic implications of antibiotic resistance in a global economy // J Health Econ. 2002. Vol. 21. –†. 1071–1083.
4. Howard D.H., Scott R.D., Packard R., Jones D. The global impact of drug resistance // Clin Infect Dis. 2000. Vol. 36 (Suppl. 1). –†. 4–10.
5. Jacoby G.A., Archer G.L. New mechanisms of bacterial resistance to antimicrobial agents // N Engl J Med. 1991. Vol. 324. –†. 601–612.
6. Hoiby N. Ecological antibiotic policy // J Antimicrob Chemother. 2000. Vol. 46 (Suppl. 1). –†. 59–62.
7. Wenzel R.P., Edmond M.B. Managing antibiotic resistance // N Engl J Med. 2000. Vol. 343. –†. 1961–1963.
8. –Ы–µ–Ї–∞—А—Б—В–≤–µ–љ–љ—Л–µ —Б—А–µ–і—Б—В–≤–∞ –Є –Є—Е —А–∞—Ж–Є–Њ–љ–∞–ї—М–љ–Њ–µ –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є–µ. –Ш–љ—Д–Њ—А–Љ–∞—Ж–Є–Њ–љ–љ—Л–є –±—О–ї–ї–µ—В–µ–љ—М –Т–Ю–Ч. вДЦ 338. M–∞–є 2010 –≥. Available from: http://www.who.int/mediacentre/factsheets/fs338/ru.
9. World Health Organization. WHO Global Strategy for Containment of Antimicrobial Resistance. 11 September 2001. Available at: http://www.who.int/csr/drugresist/WHO_Global_Strategy_English.pdf.
10. Antibiotics Still Overprescribed for Sore Throats, Bronchitis ID Week 2013: Abstracts 962 and 963. Presented October 3, 2013.
11. –Ъ–∞—Б—Б–Є—А—Б–Ї–Є–є –Ш.–Р. –Ю –≤—А–∞—З–µ–≤–∞–љ–Є–Є. –Ь.: –Ь–µ–і–Є—Ж–Є–љ–∞. 1970. 272 —Б.
12. –°—В—А–∞—З—Г–љ—Б–Ї–Є–є –Ы. –°., –Р–љ–і—А–µ–µ–≤–∞ –Ш. –Т. –°–∞–Љ–Њ–ї–µ—З–µ–љ–Є–µ –∞–љ—В–Є–±–Є–Њ—В–Є–Ї–∞–Љ–Є –≤ –†–Њ—Б—Б–Є–Є // –†–µ–Љ–µ–і–Є—Г–Љ. 2004. вДЦ 12. –°. 19–25.
13. –Р–љ–і—А–µ–µ–≤–∞ –Ш.–Т., –Ъ–Њ–Ј–ї–Њ–≤ –°.–Э., –Ъ–Њ—А–Њ–ї–µ–≤ –°.–Т. —Б —Б–Њ–∞–≤—В. –Ю—В 2004 –і–Њ 2009 –≥–Њ–і–∞: –Є–Ј–Љ–µ–љ–Є–ї–Є—Б—М –ї–Є –Ј–∞ –њ—П—В—М –ї–µ—В —А–µ–Ї–Њ–Љ–µ–љ–і–∞—Ж–Є–Є —Д–∞—А–Љ–∞—Ж–µ–≤—В–Њ–≤ –Љ—Г–ґ—З–Є–љ–∞–Љ —Б —Б–Є–Љ–њ—В–Њ–Љ–∞–Љ–Є –Њ—Б—В—А–Њ–≥–Њ —Г—А–µ—В—А–Є—В–∞? // –Ъ–ї–Є–љ–Є—З–µ—Б–Ї–∞—П –Љ–Є–Ї—А–Њ–±–Є–Њ–ї–Њ–≥–Є—П –Є –∞–љ—В–Є–Љ–Є–Ї—А–Њ–±–љ–∞—П —Е–Є–Љ–Є–Њ—В–µ—А–∞–њ–Є—П. 2009. вДЦ 11 (3). –°. 253–263.
14. McKee M., Mills L., Mainous A. Antibiotic use for the treatment of upper respiratory infections in a diverse community // J Fam Pract. 1999. Vol. 48. –†. 993–996.
15. Sawair F.A., Baqain Z.H., Abu Karaky A. et al. Assessment of self-medication of antibiotics in a Jordanian population // Med Princ Pract. 2009. Vol. 18 (1). –†. 21–25.
16. Väänänen M.H., Pietilä K., Airaksinen M. Self-medication with antibiotics - does it really happen in Europe? // Health Policy. 2006. Vol. 77 (2). –†. 166–171.
17. Chiappini E., Regoli M., Bonsignori F. et al. Analysis of different recommendations from international guidelines for the management of acute pharyngitis in adults and children // Clin Ther. 2011. Vol. 33 (1). –†. 48–58.
18. Pelucchi C., Grigoryan L., Galeone C. et al. ESCMID Guideline for the management of acute sore throat // Clin Microbiol Infect. 2012. Vol. 18 (Suppl 1). –†. 1–28.
19. Shulman S.T., Bisno A.L., Clegg H.W. et al. Infectious Diseases Society of America. Clinical practice guideline for the diagnosis and management of group A streptococcal pharyngitis: 2012 update by the Infectious Diseases Society of America // Clin Infect Dis. 2012. Vol. 55 (10). –†. 86–102.
20. Gulani A., Sachdev H.P., Qazi S.A. Efficacy of short course (<4 days) of antibiotics for treatment of acute otitis media in children: a systematic review of randomized controlled trials // Indian Pediatr. 2010. Vol. 47 (1). –†. 74–87.
21. Kozyrskyj A., Klassen T.P., Moffatt M., Harvey K. Short-course antibiotics for acute otitis media. Cochrane Database Syst Rev. 2010. Vol. 9: CD001095.
22. American Academy of Pediatrics and American Academy of Family Physicians. Subcommittee on management of acute otitis media: clinical practice guideline: diagnosis and management of acute otitis media // Pediatrics. 2004. Vol. 113. –†. 1451–1465.
23. Alagić-Smailbegović J., Saracević E., Sutalo K. Azythromicin versus amoxicillin-clavulanate in the treatment of acute sinusitis in children // Bosn J Basic Med Sci. 2006. Vol. 6 (4). –†. 76–78.
24. Ng D.K., Chow P.Y., Leung L. et al. A randomized controlled trial of azithromycin and amoxycillin/ clavulanate in the management of subacute childhood rhinosinusitis // J Paediatr Child Health. 2000. Vol. 36 (4). –†. 378–381.
25. –°–≤–Є—Б—В—Г—И–Ї–Є–љ –Т.–Ь., –Р–љ–і—А–µ–µ–≤–∞ –Ш.–Т., –°—В–µ—Ж—О–Ї –Ю.–£. —Б —Б–Њ–∞–≤—В. –Ю–±–Ј–Њ—А —Б–Њ–≤—А–µ–Љ–µ–љ–љ—Л—Е —А–µ–Ї–Њ–Љ–µ–љ–і–∞—Ж–Є–є –њ–Њ —В–∞–Ї—В–Є–Ї–µ –≤–µ–і–µ–љ–Є—П –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –Њ—Б—В—А—Л–Љ –±–∞–Ї—В–µ—А–Є–∞–ї—М–љ—Л–Љ —А–Є–љ–Њ—Б–Є–љ—Г—Б–Є—В–Њ–Љ –≤ –њ–µ–і–Є–∞—В—А–Є—З–µ—Б–Ї–Њ–є –њ—А–∞–Ї—В–Є–Ї–µ // –Ъ–ї–Є–љ–Є—З–µ—Б–Ї–∞—П –Љ–Є–Ї—А–Њ–±–Є–Њ–ї–Њ–≥–Є—П –Є –∞–љ—В–Є–Љ–Є–Ї—А–Њ–±–љ–∞—П —Е–Є–Љ–Є–Њ—В–µ—А–∞–њ–Є—П. 2012. вДЦ 14 (3). –°. 176–190.
26. Bradley J.S., Byington C.L., Shah S.S. et al. The management of community-acquired pneumonia in infants and children older than 3 months of age: clinical practice guidelines by the Pediatric Infectious Diseases Society and the Infectious Diseases Society of America // Clin Infect Dis. 2011. Vol. 53 (7). –†. 25–76.
27. Harris M., Clark J., Coote N. et al. British Thoracic Society Standards of Care Committee. British Thoracic Society guidelines for the management of community acquired pneumonia in children: update 2011 // Thorax. 2011. Vol. 66. Suppl 2. –†. 1–23.
28. –Т–љ–µ–±–Њ–ї—М–љ–Є—З–љ–∞—П –њ–љ–µ–≤–Љ–Њ–љ–Є—П —Г –і–µ—В–µ–є: —А–∞—Б–њ—А–Њ—Б—В—А–∞–љ–µ–љ–љ–Њ—Б—В—М, –і–Є–∞–≥–љ–Њ—Б—В–Є–Ї–∞, –ї–µ—З–µ–љ–Є–µ –Є –њ—А–Њ—Д–Є–ї–∞–Ї—В–Є–Ї–∞. –Ь., 2011. 64 —Б.
29. Scheid D.C., Hamm R.M. Acute bacterial rhinosinusitis in adults: part II. Treatment // Am Fam Physician. 2004. Vol. 70 (9). –†. 1697–1704.
30. Slavin R.G., Spector S.L., Bernstein I.L. et al. American Academy of Allergy, Asthma and Immunology; American College of Allergy, Asthma and Immunology; Joint Council of Allergy, Asthma and Immunology. The diagnosis and management of sinusitis: a practice parameter update // J Allergy Clin Immunol. 2005. Vol. 116 (6 Suppl). –†. 13–47.
31. –І—Г—З–∞–ї–Є–љ –Р.–У., –°–Є–љ–Њ–њ–∞–ї—М–љ–Є–Ї–Њ–≤ –Р.–Ш., –Ъ–Њ–Ј–ї–Њ–≤ –†.–°. —Б —Б–Њ–∞–≤—В. –Т–љ–µ–±–Њ–ї—М–љ–Є—З–љ–∞—П –њ–љ–µ–≤–Љ–Њ–љ–Є—П —Г –≤–Ј—А–Њ—Б–ї—Л—Е. –Я—А–∞–Ї—В–Є—З–µ—Б–Ї–Є–µ —А–µ–Ї–Њ–Љ–µ–љ–і–∞—Ж–Є–Є –њ–Њ –і–Є–∞–≥–љ–Њ—Б—В–Є–Ї–µ, –ї–µ—З–µ–љ–Є—О –Є –њ—А–Њ—Д–Є–ї–∞–Ї—В–Є–Ї–µ // –Ъ–ї–Є–љ–Є—З–µ—Б–Ї–∞—П –Љ–Є–Ї—А–Њ–±–Є–Њ–ї–Њ–≥–Є—П –Є –∞–љ—В–Є–Љ–Є–Ї—А–Њ–±–љ–∞—П —Е–Є–Љ–Є–Њ—В–µ—А–∞–њ–Є—П. 2010. вДЦ 12 (3). –°. 186–222.
32. Gupta K., Hooton T.M., Naber K.G. et al. Infectious Diseases Society of America; European Society for Microbiology and Infectious Diseases. International clinical practice guidelines for the treatment of acute uncomplicated cystitis and pyelonephritis in women: A 2010 update by the Infectious Diseases Society of America and the European Society for Microbiology and Infectious Diseases // Clin Infect Dis. 2011. Vol. 52 (5). –†. 103–120.
33. Geisler W.M. Diagnosis and management of uncomplicated Chlamydia trachomatis infections in adolescents and adults: summary of evidence reviewed for the 2010 Centers for Disease Control and Prevention Sexually Transmitted Diseases Treatment Guidelines // Clin Infect Dis. 2011. Vol. 53. Suppl 3. –†. 92–98.
34. Lanjouw E., Ossewaarde J.M., Stary A. et al. European guideline for the management of Chlamydia trachomatis infections // Int. J. STD AIDS. 2010. Vol. 21 (11). –†. 729–737.
35. –Я—А–Њ—В–Њ–Ї–Њ–ї –≤–µ–і–µ–љ–Є—П –±–Њ–ї—М–љ—Л—Е «–Ш–љ—Д–µ–Ї—Ж–Є–Є, –њ–µ—А–µ–і–∞–≤–∞–µ–Љ—Л–µ –њ–Њ–ї–Њ–≤—Л–Љ –њ—Г—В–µ–Љ». «–£—А–Њ–≥–µ–љ–Є—В–∞–ї—М–љ–∞—П —Е–ї–∞–Љ–Є–і–Є–є–љ–∞—П –Є–љ—Д–µ–Ї—Ж–Є—П» / –њ–Њ–і —А–µ–і. –Т.–Ш. –Ъ–Є—Б–Є–љ–Њ–є. –Ь.: –Э—М—О–і–Є–∞–Љ–µ–і. 2011. –°. 164–191.
36. Centers for Disease Control and Prevention (CDC). Update to CDC's Sexually transmitted diseases treatment guidelines, 2010: oral cephalosporins no longer a recommended treatment for gonococcal infections. MMWR Morb Mortal Wkly Rep. 2012. Vol. 61 (31). –†. 590–594.
37. Lieberthal A.S., Carroll A.E., Chonmaitree T. et al. The diagnosis and management of acute otitis media // Pediatrics. 2014. Vol. 133 (2). –†. 346–347.
38. –Ъ—А–∞—В–Ї–Є–є —Б–њ—А–∞–≤–Њ—З–љ–Є–Ї –њ–Њ –∞–љ—В–Є–Љ–Є–Ї—А–Њ–±–љ–Њ–є —В–µ—А–∞–њ–Є–Є / –њ–Њ–і —А–µ–і. –†.–°. –Ъ–Њ–Ј–ї–Њ–≤–∞. –°–Љ–Њ–ї–µ–љ—Б–Ї, –Ь–Р–Ъ–Ь–Р–•, 2012. 460 —Б.
39. –Ш—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ UTIAP-I, 1998–1999 –≥–≥., –љ–µ–Њ–њ—Г–±–ї–Є–Ї–Њ–≤–∞–љ–љ—Л–µ –і–∞–љ–љ—Л–µ.
40. Jurado R.L. Why Shouldn't We Determine the Erythrocyte Sedimentation Rate? // Clinical Infectious Diseases, 2001. Vol. 33. –†. 548–549.
41. Rubinstein E., Ronald A. Toronto declaration to combat antimicrobial resistance. Proceedings of the Global Resistance Day, 40th Interscience Conference on Antimicrobial Agents and Chemotherapy, September 16, 2000, Toronto, Ontario, Canada.
42. Gerber M.A., Baltimore R.S., Eaton C.B. et al. Prevention of rheumatic fever and diagnosis and treatment of acute streptococcal pharyngitis: A scientific statement from the American Heart Association Rheumatic Fever, Endocarditis and Kawasaki Disease Committee of the Council on Cardiovascular Disease in the Young, the Interdisciplinary Council on Functional Genomics and Translational Biology, and the Interdisciplinary Council on Quality of Care and Outcomes Research: Endorsed by the American Academy of Pediatrics // Circulation. 2009. Vol. 119. –†. 1541–1551.
43. American Academy of Pediatrics, Committee on Infectious Diseases. Red Book: Report of the Committee on Infectious Diseases. 28th ed. Elk Grove Village, Ill: American Academy of Pediatrics; 2009.
44. –Р–Ј–Њ–≤—Б–Ї–Њ–≤–∞ –Ю.–Т., –Ш–≤–∞–љ—З–Є–Ї –Э.–Т., –Ф–µ—Е–љ–Є—З –Р.–Т., –Ъ—А–µ—З–Є–Ї–Њ–≤–∞ –Ю.–Ш., –Ъ–Њ–Ј–ї–Њ–≤ –†.–°., –Є—Б—Б–ї–µ–і–Њ–≤–∞—В–µ–ї—М—Б–Ї–∞—П –≥—А—Г–њ–њ–∞ «–Я–µ–У–Р–°». –Ф–Є–љ–∞–Љ–Є–Ї–∞ –∞–љ—В–Є–±–Є–Њ—В–Є–Ї–Њ—А–µ–Ј–Є—Б—В–µ–љ—В–љ–Њ—Б—В–Є —А–µ—Б–њ–Є—А–∞—В–Њ—А–љ—Л—Е —И—В–∞–Љ–Љ–Њ–≤ Streptococcus pyogenes –≤ –†–Њ—Б—Б–Є–Є –Ј–∞ –њ–µ—А–Є–Њ–і 1999–2009 –≥–≥. // –Ъ–ї–Є–љ–Є—З–µ—Б–Ї–∞—П –Љ–Є–Ї—А–Њ–±–Є–Њ–ї–Њ–≥–Є—П –Є –∞–љ—В–Є–Љ–Є–Ї—А–Њ–±–љ–∞—П —Е–Є–Љ–Є–Њ—В–µ—А–∞–њ–Є—П. 2012. вДЦ 14 (4). –°. 309–321.
45. European Centre for Disease Prevention and Control. Antimicrobial resistance surveillance in Europe 2012. Annual Report of the European Antimicrobial Resistance Surveillance Network (EARS-Net). Stockholm: ECDC; 2013.
46. –Ъ–Њ–Ј–ї–Њ–≤ –†.–°., –°–Є–≤–∞—П –Ю.–Т., –Ъ—А–µ—З–Є–Ї–Њ–≤–∞ –Ю.–Ш. –Є —Б–Њ–∞–≤—В. –Ф–Є–љ–∞–Љ–Є–Ї–∞ —А–µ–Ј–Є—Б—В–µ–љ—В–љ–Њ—Б—В–Є Streptococcus pneumoniae –Ї –∞–љ—В–Є–±–Є–Њ—В–Є–Ї–∞–Љ –≤ –†–Њ—Б—Б–Є–Є –Ј–∞ –њ–µ—А–Є–Њ–і 1999–2009 –≥–≥. –Ъ–ї–Є–љ–Є—З–µ—Б–Ї–∞—П –Љ–Є–Ї—А–Њ–±–Є–Њ–ї–Њ–≥–Є—П –Є –∞–љ—В–Є–Љ–Є–Ї—А–Њ–±–љ–∞—П —Е–Є–Љ–Є–Њ—В–µ—А–∞–њ–Є—П. 2010. вДЦ 12 (4). –°. 329–341.
47. Granizo J.J., Aguilar L., Casal J. et al. Streptococcus pneumoniae resistance to erythromycin and penicillin in relation to macrolide and beta-lactam consumption in Spain (1979–1997) // J Antimicrob Chemother. 2000. Vol. 46. –†. 767–773.
48. Van der Meer J.W.M., Gyssens I.C. Considerations in providing antibiotic therapy. The APUA Newsletter 1992; winter. –†. 3–5.
49. Frimodt-Moller N., Espersen F., Jacobsen B. et al. Problems with antibiotic resistance in Spain and their relation to antibiotic use in humans elsewhere // Clin Infect Dis. 1997. Vol. 25. –†. 939–941.
50. Bryskier A., Butzler J.-P. Macrolides. In: Antibiotic and Chemotherapy. Finch R.G., e.a.: eds. Churchill Livingstone, 2003. P. 310–325.
51. Robinson D.A., Sutcliffe J.A., Tewodros W. et al. Evolution and global dissemination of macrolide-resistant group A streptococci // Antimicrob. Agents Chemother. 2006. Vol. 50 (9). –†. 2903–2911.
52. Thornsberry C., Brown N.P., Draghi D.C. et al. Antimicrobial activity against multidrug-resistant S.pneumoniae isolated in United States, 2001–2005 // Postgrad Med. 2008. Vol. 120 (Suppl. 3). –†. 32–38.
53. –Ъ–Њ–Ј–ї–Њ–≤ –†.–°., –°—В—А–∞—З—Г–љ—Б–Ї–Є–є –Ы.–°. –Ю–±—Й–Є–µ –Њ—Б–Њ–±–µ–љ–љ–Њ—Б—В–Є –∞–љ—В–Є–Є–љ—Д–µ–Ї—Ж–Є–Њ–љ–љ—Л—Е —Е–Є–Љ–Є–Њ–њ—А–µ–њ–∞—А–∞—В–Њ–≤. –Я—А–∞–Ї—В–Є—З–µ—Б–Ї–Њ–µ —А—Г–Ї–Њ–≤–Њ–і—Б—В–≤–Њ –њ–Њ –∞–љ—В–Є–Є–љ—Д–µ–Ї—Ж–Є–Њ–љ–Њ–є —Е–Є–Љ–Є–Њ—В–µ—А–∞–њ–Є–Є / –њ–Њ–і —А–µ–і. –Ы.–°. –°—В—А–∞—З—Г–љ—Б–Ї–Њ–≥–Њ, –Ѓ.–С. –С–µ–ї–Њ—Г—Б–Њ–≤–∞, –°.–Э. –Ъ–Њ–Ј–ї–Њ–≤–∞ –Ь.: –†–¶ «–§–∞—А–Љ–µ–і–Є–љ—Д–Њ», 2007. –°. 64–68.
54. Culic O., Erakovic V., Parnham M.J. Anti-inflammatory effects of macrolide antibiotics // Eur J Pharmacol. 2001. Vol. 429 (1–3). –†. 209–229.
55. Amsden G.W. Anti-inflammatory effects of macrolides - an underappreciated benefit in the treatment of community-acquired respiratory tract infections and chronic inflammatory pulmonary conditions? // J Antimicrob Chemother. 2005. Vol. 55 (1). –†. 10–21.
56. –Ш–Љ–Љ—Г–љ–Њ–Љ–Њ–і—Г–ї–Є—А—Г—О—Й–∞—П –∞–Ї—В–Є–≤–љ–Њ—Б—В—М –Љ–∞–Ї—А–Њ–ї–Є–і–Њ–≤ — —Д–∞—А–Љ–∞–Ї–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Њ–µ —Б–≤–Њ–є—Б—В–≤–Њ –Є–ї–Є —А–µ–∞–ї—М–љ—Л–є –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є–є —Н—Д—Д–µ–Ї—В? // –Ъ–ї–Є–љ–Є—З–µ—Б–Ї–∞—П —Д–∞—А–Љ–∞–Ї–Њ–ї–Њ–≥–Є—П –Є —В–µ—А–∞–њ–Є—П. 2005. вДЦ 14 (2). –°. 5–9.
57. –†–∞—З–Є–љ–∞ –°.–Р., –Ъ–Њ–Ј–ї–Њ–≤ –°.–Э., –Ш–і–µ–ї–µ–≤–Є—З –Х.–Р. —Б —Б–Њ–∞–≤—В. –Я—А–µ–і—Б—В–∞–≤–ї–µ–љ–Є—П –≤—А–∞—З–µ–є –њ–Њ–ї–Є–Ї–ї–Є–љ–Є–Ї –Њ–± —Н—В–Є–Њ–ї–Њ–≥–Є–Є –Є —В–∞–Ї—В–Є–Ї–µ –ї–µ—З–µ–љ–Є—П –≤–љ–µ–±–Њ–ї—М–љ–Є—З–љ–Њ–є –њ–љ–µ–≤–Љ–Њ–љ–Є–Є –≤ –∞–Љ–±—Г–ї–∞—В–Њ—А–љ—Л—Е —Г—Б–ї–Њ–≤–Є—П—Е // –Я—Г–ї—М–Љ–Њ–љ–Њ–ї–Њ–≥–Є—П. 2004. вДЦ 2. –°. 6–12.
58. –Ъ–Њ–Ј–ї–Њ–≤ –°.–Э. –§–∞—А–Љ–∞–Ї–Њ—Н–њ–Є–і–µ–Љ–Є–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є–µ –њ–Њ–і—Е–Њ–і—Л –Ї –Њ–њ—В–Є–Љ–Є–Ј–∞—Ж–Є–Є –ї–µ–Ї–∞—А—Б—В–≤–µ–љ–љ–Њ–є —В–µ—А–∞–њ–Є–Є –≤–љ–µ–±–Њ–ї—М–љ–Є—З–љ—Л—Е –Є–љ—Д–µ–Ї—Ж–Є–є –≤ –∞–Љ–±—Г–ї–∞—В–Њ—А–љ—Л—Е —Г—Б–ї–Њ–≤–Є—П—Е;:
–Ф–Є—Б. –і–Њ–Ї—В. –Љ–µ–і. –љ–∞—Г–Ї. –°–Љ–Њ–ї–µ–љ—Б–Ї, 2004.
59. Braun J.J., Alabert J.P., Michel F.B. et al. Adjunct effect of loratadine in the treatment of acute sinusitis in patients with allergic rhinitis // Allergy. 1997. Vol. 52. –†. 650–655.
60. McCormick D.P., John S.D., Swischuk L.E. et al. A double-blind, placebo-controlled trial of decongestant-antihistamine for the treatment of sinusitis in children // Clin Pediatr (Phila). 1996. Vol. 35 (9). –†. 457–460.
61. Thomas M., Yawn B.P., Price D. et al. EPOS Primary Care Guidelines: European Position Paper on the Primary Care Diagnosis and Management of Rhinosinusitis and Nasal Polyps 2007 - a summary // Prim Care Respir J. 2008. Vol. 17 (2). –†. 79–89.
62. Patterson R., Grammer L.C., Greenberger P.A. Allergic Diseases: Diagnosis and Management. Lippincott Williams & Wilkins; 5th edition, 1997. 634 p.
63. Babe K.S., Serafin W.E. Histamine bradykinin and their antagonists. In: Hardman J.G., Limbird L.E., Molinoff P.–Т., Ruddon R.W. eds. Goodman and Gilman's the pharmacological basis of therapeutics. 9th ed. New York: McGraw-Hill, 1996. –†. 581–600.
64. Renz C.L., Thurn J.D., Finn H.A. et al. Antihistamine prophylaxis permits rapid vancomycin infusion // Crit Care Med. 1999. Vol. 27 (9). –†. 1732–1737.
65. The diagnosis and management of anaphylaxis: an updated practice parameter // J Allergy Clin Immunol. 2005. Vol. 115 (3 Suppl). –†. 483–523.
66. –Ф–≤–Њ—А–µ—Ж–Ї–Є–є –Ы.–Ш., –ѓ–Ї–Њ–≤–ї–µ–≤ –°.–Т. –Ю—И–Є–±–Ї–Є –∞–љ—В–Є–±–∞–Ї—В–µ—А–Є–∞–ї—М–љ–Њ–є —В–µ—А–∞–њ–Є–Є –Є–љ—Д–µ–Ї—Ж–Є–є –і—Л—Е–∞—В–µ–ї—М–љ—Л—Е –њ—Г—В–µ–є –≤ –∞–Љ–±—Г–ї–∞—В–Њ—А–љ–Њ–є –њ—А–∞–Ї—В–Є–Ї–µ // –Ш–љ—Д–µ–Ї—Ж–Є–Є –Є –∞–љ—В–Є–Љ–Є–Ї—А–Њ–±–љ–∞—П —В–µ—А–∞–њ–Є—П. 2001. вДЦ 3 (2). –°. 49–54.
67. Cornely O.A., Böhme A., Buchheidt D. et al. Infectious Diseases Working Party (AGIHO) of the German Society of Hematology and Oncology (DGHO). Prophylaxis of invasive fungal infections in patients with hematological malignancies and solid tumors - guidelines of the Infectious Diseases Working Party (AGIHO) of the German Society of Hematology and Oncology (DGHO) // Ann Hematol. 2003. Vol. 82. Suppl 2. –†. 186–200.
68. Ship J.A., Vissink A., Challacom be S.J. Use of prophylactic antifungals in the immunocompromised host // Oral Surg Oral Med Oral Pathol Oral Radiol Endod. 2007. Vol. 103.(6). –†. 1–14.
69. Cruciani M., Mengoli C., Malena M. et al. Antifungal prophylaxis in liver transplant patients: a systematic review and meta-analysis // Liver Transpl. 2006. Vol. 12 (5). –†. 850–885.
70. DeGregorio M.W., Lee W.M., Ries C.A. Candida infections in patients with acute leukemia: ineffectiveness of nystatin prophylaxis and relationship between oropharyngeal and systemic candidiasis // Cancer. 1982. Vol. 50 (12). –†. 2780–2784.
71. Philpott-Howard J.N., Wade J.J., Mufti G.J. et al. Randomized comparison of oral fluconazole versus oral polyenes for the prevention of fungal infection in patients at risk of neutropenia // J Antimicrob Chemother. 1993. Vol. 31 (6). –†. 973–984.
72. –Ъ–ї–Є–Љ–Ї–Њ –Э.–Э., –Т–µ—Б–µ–ї–Њ–≤ –Р.–Т. –Я—А–Њ—В–Є–≤–Њ–≥—А–Є–±–Ї–Њ–≤—Л–µ —Е–Є–Љ–Є–Њ–њ—А–µ–њ–∞—А–∞—В—Л. –Я—А–∞–Ї—В–Є—З–µ—Б–Ї–Њ–µ —А—Г–Ї–Њ–≤–Њ–і—Б—В–≤–Њ –њ–Њ –∞–љ—В–Є–Є–љ—Д–µ–Ї—Ж–Є–Њ–љ–Њ–є —Е–Є–Љ–Є–Њ—В–µ—А–∞–њ–Є–Є / –њ–Њ–і —А–µ–і. –Ы.–°. –°—В—А–∞—З—Г–љ—Б–Ї–Њ–≥–Њ, –Ѓ.–С. –С–µ–ї–Њ—Г—Б–Њ–≤–∞, –°.–Э. –Ъ–Њ–Ј–ї–Њ–≤–∞. –Ь.: –†–¶ «–§–∞—А–Љ–µ–і–Є–љ—Д–Њ», 2007. –°. 157–175.
73. –Я–љ–µ–≤–Љ–Њ–љ–Є—П —Г –і–µ—В–µ–є. –Ъ–ї–Є–љ–Є—З–µ—Б–Ї–Є–µ —А–µ–Ї–Њ–Љ–µ–љ–і–∞—Ж–Є–Є / –њ–Њ–і —А–µ–і. –Р.–Р. –С–∞—А–∞–љ–Њ–≤–∞ –Ь.: –У–≠–Ю–Ґ–Р–†-–Ь–µ–і–Є–∞, 2005. 28 —Б.
74. Owens R.C. Jr., Ambrose P.G. Antimicrobial safety: focus on fluoroquinolones // Clin Infect Dis. 2005. Vol. 41 (Suppl. 2). –†. 144–157.
75. Salvo F., De Sarro A., Caputi A.P. et al. Amoxicillin and amoxicillin plus clavulanate: a safety review // Expert Opin Drug Saf. 2009. Vol. 8 (1). –†. 111–118.
76. Högenauer C., Hammer H.F., Krejs G.J. et al. Mechanisms and management of antibiotic-associated diarrhea // Clin Infect Dis. 1998. Vol. 27 (4). –†. 702–710.
77. Bartlett J.G. Antibiotic-associated diarrhea // Clin Infect Dis. 1992. Vol. 15. –†. 573–581.
78. Makins R, Ballinger A. Gastrointestinal side effects of drugs // Expert Opin Drug Saf. 2003. Vol. 2 (4). –†. 421–429.
79. Peeters T.L., Matthys G., Depootere I. et al. Erythromycin is a motilin receptor agonist // Am J Physiol. 1989. Vol. 257. –†. 470–474.
80. Caron F., Bouaniche M., Delatour F. et al. B. Effects of two oral erythromycin ethylsuccinate formulations on the motility of the small intestine in human beings // Antimicrob Agents Chemother. 1996. Vol. 40. –†. 1796–1800.
81. Waldvogel F.A. Staphylococcus aureus. In: Mandell G.L., Bennett J.E., Dolin R. Principles and Practice of Infectious Diseases. 5th ed. Philadelphia: Churchill Livingstone, 2000. –†. 2069–2092.
82. Archer G.L. Staphylococcus epidermidis and other coagulase-negative staphylococci. In: Mandell G.L., Bennett J.E., Dolin R. Principles and Practice of Infectious Diseases. 5th ed. Philadelphia: Churchill Livingstone, 2000. –†. 2092–2100.
83. Eltringham I. Mupirocin resistance and methicillin-resistant Staphylococcus aureus (MRSA) // J Hosp Infect. 1997. Vol. 35. –†. 1–8.
84. Reagan D.R., Bradley N., Doebbeling N. et al. Elimination of coincident Staphylococcus aureus nasal and hand carriage with intranasal application of mupirocin calcium ointment // Ann Intern Med. 1991. Vol. 114. –†. 101–106.
85. Nicolle L.E., Bradley S., Colgan R. et al. Infectious Diseases Society of America guidelines for the diagnosis and treatment of asymptomatic bacteriuria in adults // Clin Infect Dis. 2005. Vol. 40. –†. 643–654.
86. –Ъ–ї–Є–Љ–Ї–Њ –Э.–Э., –Т–µ—Б–µ–ї–Њ–≤ –Р.–Т. –Т—Л–±–Њ—А –∞–љ—В–Є–Љ–Є–Ї—А–Њ–±–љ—Л—Е —Е–Є–Љ–Є–Њ–њ—А–µ–њ–∞—А–∞—В–Њ–≤ –њ—А–Є –≥—А–Є–±–Ї–Њ–≤—Л—Е –Є–љ—Д–µ–Ї—Ж–Є—П—Е. –Я—А–∞–Ї—В–Є—З–µ—Б–Ї–Њ–µ —А—Г–Ї–Њ–≤–Њ–і—Б—В–≤–Њ –њ–Њ –∞–љ—В–Є–Є–љ—Д–µ–Ї—Ж–Є–Њ–љ–Њ–є —Е–Є–Љ–Є–Њ—В–µ—А–∞–њ–Є–Є. –Я–Њ–і —А–µ–і. –Ы.–°. –°—В—А–∞—З—Г–љ—Б–Ї–Њ–≥–Њ, –Ѓ.–С. –С–µ–ї–Њ—Г—Б–Њ–≤–∞, –°.–Э. –Ъ–Њ–Ј–ї–Њ–≤–∞ –Ь.: –†–¶ «–§–∞—А–Љ–µ–і–Є–љ—Д–Њ», 2007. –°. 340–355.
87. –†–∞—Д–∞–ї—М—Б–Ї–Є–є –Т.–Т. –Ъ–ї–Є–љ–Є—З–µ—Б–Ї–Њ–µ –Ј–љ–∞—З–µ–љ–Є–µ –Є —В–µ—А–∞–њ–Є—П –Ї–∞–љ–і–Є–і—Г—А–Є–Є // –Ъ–ї–Є–љ–Є—З–µ—Б–Ї–∞—П –Љ–Є–Ї—А–Њ–±–Є–Њ–ї–Њ–≥–Є—П –Є –∞–љ—В–Є–Љ–Є–Ї—А–Њ–±–љ–∞—П —Е–Є–Љ–Є–Њ—В–µ—А–∞–њ–Є—П. 2001. вДЦ 3(1). –°. 22–27.
88. Kaye E.T. Topical antibacterial agents: role in prophylaxis and treatment of bacterial infections. In: Remington J.S., Swartz M.N., editors. Current Clinical Topics in Infectious Diseases. 20th ed. Malden: Blackwell Sciens, 2000. –†. 43–63.
89. Tunkel A. Topical antibacterials. In: Mandell G.L., Bennett J.E., Dolin R., editors. 5th ed. Philadelphia: Churchill Livingstone, 2000. –†. 428–436.
90. –С–Њ–≥–і–∞–љ–Њ–≤–Є—З –Ґ.–Ь., –°—В—А–∞—З—Г–љ—Б–Ї–Є–є –Ы.–°. –Ь—Г–њ–Є—А–Њ—Ж–Є–љ: —Г–љ–Є–Ї–∞–ї—М–љ—Л–є –∞–љ—В–Є–±–Є–Њ—В–Є–Ї –і–ї—П –Љ–µ—Б—В–љ–Њ–≥–Њ –њ—А–Є–Љ–µ–љ–µ–љ–Є—П // –Ъ–ї–Є–љ–Є—З–µ—Б–Ї–∞—П –Љ–Є–Ї—А–Њ–±–Є–Њ–ї–Њ–≥–Є—П –Є –∞–љ—В–Є–Љ–Є–Ї—А–Њ–±–љ–∞—П —Е–Є–Љ–Є–Њ—В–µ—А–∞–њ–Є—П. 1999. вДЦ 1 (1). –°. 57–65.
91. Goldblatt E.L. Efficacy of ofloxacin and other otic preparations for acute otitis media in patients with tympanostomy tubes // Pediatr Infect Dis J. 2001. Vol. 20 (1). –†. 116–119.
92. –ѓ–љ–Њ–≤ –Ѓ.–Ъ., –†—П–Ј–∞–љ—Ж–µ–≤ –°.–Т. –Ю—Б—В—А—Л–є —А–Є–љ–Њ—Б–Є–љ—Г—Б–Є—В –≤ –њ—А–∞–Ї—В–Є–Ї–µ –≤—А–∞—З–∞-—В–µ—А–∞–њ–µ–≤—В–∞ // Consilium medicum. 2003. вДЦ 5 (10). –°. 557–563.
93. –Ы–Њ–±–Ј–Є–љ –Ѓ.–С., –Я–Є–ї–Є–њ–µ–љ–Ї–Њ –Т.–Т., –°—В–µ—Ж—О–Ї –Ю.–£. –Ш–љ—Д–µ–Ї—Ж–Є–Є —Ж–µ–љ—В—А–∞–ї—М–љ–Њ–є –љ–µ—А–≤–љ–Њ–є —Б–Є—Б—В–µ–Љ—Л. –Я—А–∞–Ї—В–Є—З–µ—Б–Ї–Њ–µ —А—Г–Ї–Њ–≤–Њ–і—Б—В–≤–Њ –њ–Њ –∞–љ—В–Є–Є–љ—Д–µ–Ї—Ж–Є–Њ–љ–Њ–є —Е–Є–Љ–Є–Њ—В–µ—А–∞–њ–Є–Є / –њ–Њ–і —А–µ–і. –Ы.–°. –°—В—А–∞—З—Г–љ—Б–Ї–Њ–≥–Њ, –Ѓ.–С. –С–µ–ї–Њ—Г—Б–Њ–≤–∞, –°.–Э. –Ъ–Њ–Ј–ї–Њ–≤–∞ –Ь.: –†–¶ «–§–∞—А–Љ–µ–і–Є–љ—Д–Њ», 2007. –°. 300–310.
94. –†–µ—И–µ–і—М–Ї–Њ –У.–Ъ., –•–∞–є–Ї–Є–љ–∞ –Х.–Т. –У—А—Г–њ–њ–∞ –∞–Љ–Є–љ–Њ–≥–ї–Є–Ї–Њ–Ј–Є–і–Њ–≤. –Я—А–∞–Ї—В–Є—З–µ—Б–Ї–Њ–µ —А—Г–Ї–Њ–≤–Њ–і—Б—В–≤–Њ –њ–Њ –∞–љ—В–Є–Є–љ—Д–µ–Ї—Ж–Є–Њ–љ–Њ–є —Е–Є–Љ–Є–Њ—В–µ—А–∞–њ–Є–Є. –Я–Њ–і —А–µ–і. –Ы.–°. –°—В—А–∞—З—Г–љ—Б–Ї–Њ–≥–Њ, –Ѓ.–С. –С–µ–ї–Њ—Г—Б–Њ–≤–∞, –°.–Э. –Ъ–Њ–Ј–ї–Њ–≤–∞ –Ь.: –†–¶ «–§–∞—А–Љ–µ–і–Є–љ—Д–Њ», 2007. –°. 88–93.
95. –І—Г—З–∞–ї–Є–љ –Р.–У., –°–Є–љ–Њ–њ–∞–ї—М–љ–Є–Ї–Њ–≤ –Р.–Ш., –Ъ–Њ–Ј–ї–Њ–≤ –†.–°., –†–∞—З–Є–љ–∞ –°.–Р. –Ш–љ—Д–µ–Ї—Ж–Є–Є –љ–Є–ґ–љ–Є—Е –і—Л—Е–∞—В–µ–ї—М–љ—Л—Е –њ—Г—В–µ–є. –Я—А–∞–Ї—В–Є—З–µ—Б–Ї–Њ–µ —А—Г–Ї–Њ–≤–Њ–і—Б—В–≤–Њ –њ–Њ –∞–љ—В–Є–Є–љ—Д–µ–Ї—Ж–Є–Њ–љ–Њ–є —Е–Є–Љ–Є–Њ—В–µ—А–∞–њ–Є–Є / –њ–Њ–і —А–µ–і. –Ы.–°. –°—В—А–∞—З—Г–љ—Б–Ї–Њ–≥–Њ, –Ѓ.–С. –С–µ–ї–Њ—Г—Б–Њ–≤–∞, –°.–Э. –Ъ–Њ–Ј–ї–Њ–≤–∞ –Ь.: –†–¶ «–§–∞—А–Љ–µ–і–Є–љ—Д–Њ», 2007. –°. 258–266.
96. Gladue R.P., Bright G.M., Isaacson R.E., et al. In vitro and in vivo uptake of azithromycin (CP-62,993) by phagocytic cells: possible mechanism of delivery and release at sites of infection // Antimicrob Agents Chemother. 1989. Vol. 33. P. 277–282.
97. Hand W.L., Hand D.L. Characteristics and mechanisms of azithromycin accumulation and efflux in human polymorphonuclear leukocytes // Int Antimicrob Agents. 2001. Vol. 18. P. 419–425.












