–Ъ–∞—А–±–∞–њ–µ–љ–µ–Љ—Л (–Є–Љ–Є–њ–µ–љ–µ–Љ, –Љ–µ—А–Њ–њ–µ–љ–µ–Љ –Є —Н—А—В–∞–њ–µ–љ–µ–Љ)1 —П–≤–ї—П—О—В—Б—П –∞–љ—В–Є–±–Є–Њ—В–Є–Ї–∞–Љ–Є —Б –љ–∞–Є–±–Њ–ї–µ–µ —И–Є—А–Њ–Ї–Є–Љ —Б–њ–µ–Ї—В—А–Њ–Љ –∞–Ї—В–Є–≤–љ–Њ—Б—В–Є, —З—В–Њ –≤—Л–≥–Њ–і–љ–Њ –Њ—В–ї–Є—З–∞–µ—В –Є—Е –Њ—В –Љ–љ–Њ–≥–Є—Е –і—А—Г–≥–Є—Е –Ї–ї–∞—Б—Б–Њ–≤ –∞–љ—В–Є–Љ–Є–Ї—А–Њ–±–љ—Л—Е –њ—А–µ–њ–∞—А–∞—В–Њ–≤. –Ю–љ–Є –њ—А–Њ—П–≤–ї—П—О—В –±—Л—Б—В—А–Њ–µ –±–∞–Ї—В–µ—А–Є—Ж–Є–і–љ–Њ–µ –і–µ–є—Б—В–≤–Є–µ –≤ –Њ—В–љ–Њ—И–µ–љ–Є–Є –≥—А–∞–Љ–њ–Њ–ї–Њ–ґ–Є—В–µ–ї—М–љ—Л—Е –Є –≥—А–∞–Љ–Њ—В—А–Є—Ж–∞—В–µ–ї—М–љ—Л—Е –∞—Н—А–Њ–±–љ—Л—Е –Є –∞–љ–∞—Н—А–Њ–±–љ—Л—Е –±–∞–Ї—В–µ—А–Є–є. –Я—А–Є—А–Њ–і–љ–Њ–є —Г—Б—В–Њ–є—З–Є–≤–Њ—Б—В—М—О –Ї –Ї–∞—А–±–∞–њ–µ–љ–µ–Љ–∞–Љ –Њ–±–ї–∞–і–∞—О—В –Љ–µ—В–Є—Ж–Є–ї–ї–Є–љ—А–µ–Ј–Є—Б—В–µ–љ—В–љ—Л–µ —Б—В–∞—Д–Є–ї–Њ–Ї–Њ–Ї–Ї–Є, Enterococcus faecium, Stenotrophomonas maltophilia. –£ –Є–Љ–Є–њ–µ–љ–µ–Љ–∞ –≤ 2–4 —А–∞–Ј–∞ –≤—Л—И–µ –∞–Ї—В–Є–≤–љ–Њ—Б—В—М in vitro –њ—А–Њ—В–Є–≤ –Љ–µ—В–Є—Ж–Є–ї–ї–Є–љ—З—Г–≤—Б—В–≤–Є—В–µ–ї—М–љ—Л—Е —Б—В–∞—Д–Є–ї–Њ–Ї–Њ–Ї–Ї–Њ–≤, Streptococcus pneumoniae –Є Enterococcus faecalis, –∞ –Љ–µ—А–Њ–њ–µ–љ–µ–Љ –≤ 4–64 —А–∞–Ј–∞ –њ—А–µ–≤–Њ—Б—Е–Њ–і–Є—В –Є–Љ–Є–њ–µ–љ–µ–Љ –њ–Њ –і–µ–є—Б—В–≤–Є—О –љ–∞ –≥—А–∞–Љ–Њ—В—А–Є—Ж–∞—В–µ–ї—М–љ—Л–µ –±–∞–Ї—В–µ—А–Є–Є, —З—В–Њ –Є–Љ–µ–µ—В –Њ—Б–Њ–±–Њ–µ –Ј–љ–∞—З–µ–љ–Є–µ –≤ –Њ—В–љ–Њ—И–µ–љ–Є–Є Pseudomonas aeruginosa – —Б–∞–Љ–Њ–≥–Њ —З–∞—Б—В–Њ–≥–Њ –≤–Њ–Ј–±—Г–і–Є—В–µ–ї—П –Є–љ—Д–µ–Ї—Ж–Є–є –≤ –Њ—В–і–µ–ї–µ–љ–Є—П—Е —А–µ–∞–љ–Є–Љ–∞—Ж–Є–Є –Є –Є–љ—В–µ–љ—Б–Є–≤–љ–Њ–є —В–µ—А–∞–њ–Є–Є (–Ю–†–Ш–Ґ) [1,2]. –Ъ–∞—А–±–∞–њ–µ–љ–µ–Љ—Л –њ—А–Њ—П–≤–ї—П—О—В —А–∞–≤–љ—Г—О –∞–љ—В–Є–∞–љ–∞—Н—А–Њ–±–љ—Г—О –∞–Ї—В–Є–≤–љ–Њ—Б—В—М, –±–Њ–ї–µ–µ –≤—Л—Б–Њ–Ї—Г—О –њ–Њ —Б—А–∞–≤–љ–µ–љ–Є—О —Б –Љ–µ—В—А–Њ–љ–Є–і–∞–Ј–Њ–ї–Њ–Љ, –Ї–ї–Є–љ–і–∞–Љ–Є—Ж–Є–љ–Њ–Љ, —Ж–µ—Д–Њ–Ї—Б–Є—В–Є–љ–Њ–Љ [3]. –≠—А—В–∞–њ–µ–љ–µ–Љ –≤ –Њ—В–ї–Є—З–Є–µ –Њ—В –Є–Љ–Є–њ–µ–љ–µ–Љ–∞ –Є –Љ–µ—А–Њ–њ–µ–љ–µ–Љ–∞ –љ–µ –і–µ–є—Б—В–≤—Г–µ—В –љ–∞ –љ–µ—Д–µ—А–Љ–µ–љ—В–Є—А—Г—О—Й–Є–µ –±–∞–Ї—В–µ—А–Є–Є (P. aeruginosa –Є Acinetobacter spp.) [4] –Є —Е–∞—А–∞–Ї—В–µ—А–Є–Ј—Г–µ—В—Б—П –≤—Л—Б–Њ–Ї–Є–Љ —Б–≤—П–Ј—Л–≤–∞–љ–Є–µ–Љ —Б –±–µ–ї–Ї–∞–Љ–Є —Б—Л–≤–Њ—А–Њ—В–Ї–Є –Ї—А–Њ–≤–Є, —З—В–Њ —Г–≤–µ–ї–Є—З–Є–≤–∞–µ—В –њ–µ—А–Є–Њ–і –µ–≥–Њ –њ–Њ–ї—Г–≤—Л–≤–µ–і–µ–љ–Є—П –і–Њ 4 —З–∞—Б–Њ–≤ –њ–Њ —Б—А–∞–≤–љ–µ–љ–Є—О —Б 1 —З–∞—Б–Њ–Љ —Г –∞–љ—В–Є—Б–Є–љ–µ–≥–љ–Њ–є–љ—Л—Е –Ї–∞—А–±–∞–њ–µ–љ–µ–Љ–Њ–≤ [5].
–Э–µ—А–∞—Ж–Є–Њ–љ–∞–ї—М–љ–Њ–µ –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є–µ –Ї–∞—А–±–∞–њ–µ–љ–µ–Љ–Њ–≤ –≤ —А—Г—В–Є–љ–љ–Њ–є –њ—А–∞–Ї—В–Є–Ї–µ –±–µ–Ј —Г—З–µ—В–∞ –Њ–±—К–µ–Ї—В–Є–≤–љ—Л—Е –њ–Њ–Ї–∞–Ј–∞–љ–Є–є, –њ–Њ–Љ–Є–Љ–Њ —Н–Ї–Њ–љ–Њ–Љ–Є—З–µ—Б–Ї–Њ–є –љ–µ—Ж–µ–ї–µ—Б–Њ–Њ–±—А–∞–Ј–љ–Њ—Б—В–Є, –Љ–Њ–ґ–µ—В —Б–Њ–њ—А–Њ–≤–Њ–ґ–і–∞—В—М—Б—П —Д–Њ—А–Љ–Є—А–Њ–≤–∞–љ–Є–µ–Љ –Є —Б–µ–ї–µ–Ї—Ж–Є–µ–є –њ–Њ–ї–Є—А–µ–Ј–Є—Б—В–µ–љ—В–љ—Л—Е —И—В–∞–Љ–Љ–Њ–≤ –±–∞–Ї—В–µ—А–Є–є, –Ї–Њ–≥–і–∞ –ї—О–±—Л–µ –∞–љ—В–Є–Љ–Є–Ї—А–Њ–±–љ—Л–µ –њ—А–µ–њ–∞—А–∞—В—Л —Б—В–∞–љ–Њ–≤—П—В—Б—П –љ–µ—Н—Д—Д–µ–Ї—В–Є–≤–љ—Л–Љ–Є. –Я–Њ—Н—В–Њ–Љ—Г –њ—А–Є –љ–∞–Ј–љ–∞—З–µ–љ–Є–Є —Н–Љ–њ–Є—А–Є—З–µ—Б–Ї–Њ–є —В–µ—А–∞–њ–Є–Є –њ—А–Є —В—П–ґ–µ–ї—Л—Е –Є–љ—Д–µ–Ї—Ж–Є—П—Е –≤–Њ–Ј–љ–Є–Ї–∞–µ—В –і–Є–ї–µ–Љ–Љ–∞ –Љ–µ–ґ–і—Г –љ–µ–Њ–±—Е–Њ–і–Є–Љ–Њ—Б—В—М—О –Љ–∞–Ї—Б–Є–Љ–∞–ї—М–љ–Њ —И–Є—А–Њ–Ї–Њ–≥–Њ –Њ—Е–≤–∞—В–∞ –њ–Њ—В–µ–љ—Ж–Є–∞–ї—М–љ—Л—Е –≤–Њ–Ј–±—Г–і–Є—В–µ–ї–µ–є –і–ї—П –Њ–±–µ—Б–њ–µ—З–µ–љ–Є—П –∞–і–µ–Ї–≤–∞—В–љ–Њ–≥–Њ –ї–µ—З–µ–љ–Є—П, —Б –Њ–і–љ–Њ–є —Б—В–Њ—А–Њ–љ—Л, –Є –Љ–Є–љ–Є–Љ–Є–Ј–∞—Ж–Є–µ–є —Б–µ–ї–µ–Ї—Ж–Є–Є –∞–љ—В–Є–±–Є–Њ—В–Є–Ї–Њ—А–µ–Ј–Є—Б—В–µ–љ—В–љ—Л—Е —И—В–∞–Љ–Љ–Њ–≤, —Б –і—А—Г–≥–Њ–є —Б—В–Њ—А–Њ–љ—Л. –°–ї–µ–і—Г–µ—В —В–∞–Ї–ґ–µ —Г—З–Є—В—Л–≤–∞—В—М —А–µ–≥–Є–Њ–љ–∞–ї—М–љ—Л–µ –Є –ї–Њ–Ї–∞–ї—М–љ—Л–µ –і–∞–љ–љ—Л–µ –Љ–Њ–љ–Є—В–Њ—А–Є–љ–≥–∞ –њ—А–Є–Њ–±—А–µ—В–µ–љ–љ–Њ–є —Г—Б—В–Њ–є—З–Є–≤–Њ—Б—В–Є –≤–µ–і—Г—Й–Є—Е –≤–Њ–Ј–±—Г–і–Є—В–µ–ї–µ–є –≤–љ–µ–±–Њ–ї—М–љ–Є—З–љ—Л—Е –Є –≥–Њ—Б–њ–Є—В–∞–ї—М–љ—Л—Е –Є–љ—Д–µ–Ї—Ж–Є–є, –Є –≤ –њ–µ—А–≤—Г—О –Њ—З–µ—А–µ–і—М —Г—А–Њ–≤–µ–љ—М –њ—А–Њ–і—Г—Ж–µ–љ—В–Њ–≤ b––ї–∞–Ї—В–∞–Љ–∞–Ј —А–∞—Б—И–Є—А–µ–љ–љ–Њ–≥–Њ —Б–њ–µ–Ї—В—А–∞ (–С–Ы–†–°) —Б—А–µ–і–Є –≥—А–∞–Љ–Њ—В—А–Є—Ж–∞—В–µ–ї—М–љ—Л—Е –њ–∞—В–Њ–≥–µ–љ–Њ–≤, –њ—А–µ–і—Б—В–∞–≤–ї—П—О—Й–Є—Е –љ–∞–Є–±–Њ–ї—М—И—Г—О —Г–≥—А–Њ–Ј—Г, —В–∞–Ї –Ї–∞–Ї –Њ–љ–Є –≥–Є–і—А–Њ–ї–Є–Ј—Г—О—В –њ—А–∞–Ї—В–Є—З–µ—Б–Ї–Є –≤—Б–µ —Ж–µ—Д–∞–ї–Њ—Б–њ–Њ—А–Є–љ—Л –Є —И–Є—А–Њ–Ї–Њ —А–∞—Б–њ—А–Њ—Б—В—А–∞–љ–µ–љ—Л –≤ –†–Њ—Б—Б–Є–Є. –Ъ —З–Є—Б–ї—Г –њ—А–Њ–±–ї–µ–Љ–љ—Л—Е –Љ–Є–Ї—А–Њ–Њ—А–≥–∞–љ–Є–Ј–Љ–Њ–≤ –Њ—В–љ–Њ—Б—П—В—Б—П P. aeruginosa –Є Acinetobacter spp., –Ї–Њ—В–Њ—А—Л–µ –Љ–Њ–≥—Г—В –њ—А–Є–Њ–±—А–µ—В–∞—В—М —Г—Б—В–Њ–є—З–Є–≤–Њ—Б—В—М –Ї –Є–Љ–Є–њ–µ–љ–µ–Љ—Г –Є —А–µ–ґ–µ – –Ї –Љ–µ—А–Њ–њ–µ–љ–µ–Љ—Г. –Т–∞–ґ–љ–∞—П —А–Њ–ї—М –≤ –і–Њ—Б—В–Є–ґ–µ–љ–Є–Є –Љ–∞–Ї—Б–Є–Љ–∞–ї—М–љ–Њ–є –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Њ–є –Є –Љ–Є–Ї—А–Њ–±–Є–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Њ–є —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В–Є –Ї–∞—А–±–∞–њ–µ–љ–µ–Љ–Њ–≤ –њ—А–Є–љ–∞–і–ї–µ–ґ–Є—В —А–∞—Ж–Є–Њ–љ–∞–ї—М–љ–Њ–Љ—Г –Є—Е –і–Њ–Ј–Є—А–Њ–≤–∞–љ–Є—О —Б —Г—З–µ—В–Њ–Љ —Д–∞—А–Љ–∞–Ї–Њ–Ї–Є–љ–µ—В–Є—З–µ—Б–Ї–Є—Е –Є —Д–∞—А–Љ–∞–Ї–Њ–і–Є–љ–∞–Љ–Є—З–µ—Б–Ї–Є—Е (–§–Ъ/–§–Ф) –њ–∞—А–∞–Љ–µ—В—А–Њ–≤, –Њ —З–µ–Љ –љ–∞–≥–ї—П–і–љ–Њ —Б–≤–Є–і–µ—В–µ–ї—М—Б—В–≤—Г—О—В —А–µ–Ј—Г–ї—М—В–∞—В—Л –Є–Ј—Г—З–µ–љ–Є—П –Љ–µ—А–Њ–њ–µ–љ–µ–Љ–∞ —Б –њ–Њ–Љ–Њ—Й—М—О –Љ–∞—В–µ–Љ–∞—В–Є—З–µ—Б–Ї–Њ–≥–Њ –Љ–Њ–і–µ–ї–Є—А–Њ–≤–∞–љ–Є—П. –†–∞—Б—Б–Љ–Њ—В—А–µ–љ–Є—О —Н—В–Є—Е –Є —Б–Љ–µ–ґ–љ—Л—Е –≤–Њ–њ—А–Њ—Б–Њ–≤ —Б –∞–Ї—Ж–µ–љ—В–Њ–Љ –љ–∞ –Љ–µ—А–Њ–њ–µ–љ–µ–Љ –њ–Њ—Б–≤—П—Й–µ–љ–∞ –љ–∞—Б—В–Њ—П—Й–∞—П –њ—Г–±–ї–Є–Ї–∞—Ж–Є—П.
–•–∞—А–∞–Ї—В–µ—А–Є—Б—В–Є–Ї–∞ –±–µ—В–∞––ї–∞–Ї—В–∞–Љ–∞–Ј (–С–Ы)
–Є —А–µ–Ї–Њ–Љ–µ–љ–і–∞—Ж–Є–Є –њ–Њ –≤—Л—П–≤–ї–µ–љ–Є—О –С–Ы–†–°
–Я—А–Њ–і—Г–Ї—Ж–Є—П –С–Ы —П–≤–ї—П–µ—В—Б—П –≤–µ–і—Г—Й–Є–Љ –Љ–µ—Е–∞–љ–Є–Ј–Љ–Њ–Љ —Д–Њ—А–Љ–Є—А–Њ–≤–∞–љ–Є—П —А–µ–Ј–Є—Б—В–µ–љ—В–љ–Њ—Б—В–Є –Ї b––ї–∞–Ї—В–∞–Љ–љ—Л–Љ –∞–љ—В–Є–±–Є–Њ—В–Є–Ї–∞–Љ —Г –≥—А–∞–Љ–Њ—В—А–Є—Ж–∞—В–µ–ї—М–љ—Л—Е –±–∞–Ї—В–µ—А–Є–є. –Т—Б–µ –Є–Ј–≤–µ—Б—В–љ—Л–µ –≤ –љ–∞—Б—В–Њ—П—Й–µ–µ –≤—А–µ–Љ—П –С–Ы (–±–Њ–ї–µ–µ 300 —А–∞–Ј–љ–Њ–≤–Є–і–љ–Њ—Б—В–µ–є) –і–µ–ї—П—В –љ–∞ 4 –Љ–Њ–ї–µ–Ї—Г–ї—П—А–љ—Л—Е –Ї–ї–∞—Б—Б–∞, –≤ –њ—А–µ–і–µ–ї–∞—Е –Ї–Њ—В–Њ—А—Л—Е —Д–µ—А–Љ–µ–љ—В—Л —Е–∞—А–∞–Ї—В–µ—А–Є–Ј—Г—О—В—Б—П –Њ–±—Й–љ–Њ—Б—В—М—О —Б–≤–Њ–є—Б—В–≤ –Є –≤—Л—А–∞–ґ–µ–љ–љ–Њ–є –≥–Њ–Љ–Њ–ї–Њ–≥–Є–µ–є, –∞ —В–∞–Ї–ґ–µ —З—Г–≤—Б—В–≤–Є—В–µ–ї—М–љ–Њ—Б—В—М—О –Є–ї–Є —А–µ–Ј–Є—Б—В–µ–љ—В–љ–Њ—Б—В—М—О –Ї –і–µ–є—Б—В–≤–Є—О –Є–љ–≥–Є–±–Є—В–Њ—А–Њ–≤ – –Ї–ї–∞–≤—Г–ї–∞–љ–Њ–≤–Њ–є –Ї–Є—Б–ї–Њ—В—Л, —Б—Г–ї—М–±–∞–Ї—В–∞–Љ–∞, —В–∞–Ј–Њ–±–∞–Ї—В–∞–Љ–∞ [6]. –§–µ—А–Љ–µ–љ—В—Л –Ї–ї–∞—Б—Б–∞ –Т –Њ—В–љ–Њ—Б—П—В—Б—П –Ї –Љ–µ—В–∞–ї–ї–Њ—Н–љ–Ј–Є–Љ–∞–Љ, –њ–Њ—Б–Ї–Њ–ї—М–Ї—Г –≤ –Ї–∞—З–µ—Б—В–≤–µ –Ї–Њ—Д–µ—А–Љ–µ–љ—В–∞ –≤ –љ–Є—Е –њ—А–Є—Б—Г—В—Б—В–≤—Г–µ—В –∞—В–Њ–Љ —Ж–Є–љ–Ї–∞. –С–Ы –Ї–ї–∞—Б—Б–Њ–≤ –Р, –°, D –Њ—В–љ–Њ—Б—П—В—Б—П –Ї —Д–µ—А–Љ–µ–љ—В–∞–Љ «—Б–µ—А–Є–љ–Њ–≤–Њ–≥–Њ» —В–Є–њ–∞ (–њ–Њ –∞–Љ–Є–љ–Њ–Ї–Є—Б–ї–Њ—В–µ, –љ–∞—Е–Њ–і—П—Й–µ–є—Б—П –≤ –∞–Ї—В–Є–≤–љ–Њ–Љ —Ж–µ–љ—В—А–µ —Д–µ—А–Љ–µ–љ—В–∞).
–Т–љ—Г—В—А–Є –Ї–ї–∞—Б—Б–∞ –Р –≤—Л–і–µ–ї–µ–љ—Л 7 –≥—А—Г–њ–њ [6], –Є–Ј –Ї–Њ—В–Њ—А—Л—Е –њ–Њ–≤—Л—И–µ–љ–љ–Њ–µ –≤–љ–Є–Љ–∞–љ–Є–µ –≤ –љ–∞—Б—В–Њ—П—Й–µ–µ –≤—А–µ–Љ—П —Г–і–µ–ї—П—О—В –≥—А—Г–њ–њ–µ 2be, –≥–і–µ —Б–Њ—Б—А–µ–і–Њ—В–Њ—З–µ–љ–∞ –±–Њ–ї—М—И–∞—П —З–∞—Б—В—М —Д–µ—А–Љ–µ–љ—В–Њ–≤, –Њ–±–Њ–Ј–љ–∞—З–µ–љ–љ—Л—Е –њ–Њ–і —В–µ—А–Љ–Є–љ–Њ–Љ «–±–µ—В–∞––ї–∞–Ї—В–∞–Љ–∞–Ј—Л —А–∞—Б—И–Є—А–µ–љ–љ–Њ–≥–Њ —Б–њ–µ–Ї—В—А–∞» (–С–Ы–†–°). –Т –Њ—В–ї–Є—З–Є–µ –Њ—В —А–∞–љ–µ–µ –Є–Ј–≤–µ—Б—В–љ—Л—Е «–±–µ—В–∞––ї–∞–Ї—В–∞–Љ–∞–Ј —И–Є—А–Њ–Ї–Њ–≥–Њ —Б–њ–µ–Ї—В—А–∞», –≥–Є–і—А–Њ–ї–Є–Ј–Є—А—Г—О—Й–Є—Е –њ—А–Є—А–Њ–і–љ—Л–µ –Є –њ–Њ–ї—Г—Б–Є–љ—В–µ—В–Є—З–µ—Б–Ї–Є–µ –њ–µ–љ–Є—Ж–Є–ї–ї–Є–љ—Л, —Ж–µ—Д–∞–ї–Њ—Б–њ–Њ—А–Є–љ—Л I –Є –Њ—В—З–∞—Б—В–Є II –њ–Њ–Ї–Њ–ї–µ–љ–Є—П, –С–Ы–†–° –і–Њ–њ–Њ–ї–љ–Є—В–µ–ї—М–љ–Њ –≥–Є–і—А–Њ–ї–Є–Ј—Г—О—В —Ж–µ—Д–∞–ї–Њ—Б–њ–Њ—А–Є–љ—Л III –Є IV –њ–Њ–Ї–Њ–ї–µ–љ–Є–є (–љ–µ –Ј–∞—В—А–∞–≥–Є–≤–∞—П —Ж–µ—Д–∞–Љ–Є—Ж–Є–љ—Л2). –Ю–љ–Є —Б–Њ—Е—А–∞–љ—П—О—В —З—Г–≤—Б—В–≤–Є—В–µ–ї—М–љ–Њ—Б—В—М –Ї –і–µ–є—Б—В–≤–Є—О –Є–љ–≥–Є–±–Є—В–Њ—А–Њ–≤, –∞ –њ—А–Њ–і—Г—Ж–Є—А—Г—О—Й–Є–µ –Є—Е –±–∞–Ї—В–µ—А–Є–Є (—З–∞—Й–µ K. pneumoniae –Є E. coli) –Њ—В–ї–Є—З–∞—О—В—Б—П –∞—Б—Б–Њ—Ж–Є–Є—А–Њ–≤–∞–љ–љ–Њ–є —А–µ–Ј–Є—Б—В–µ–љ—В–љ–Њ—Б—В—М—О –Ї –і—А—Г–≥–Є–Љ –∞–љ—В–Є–±–Є–Њ—В–Є–Ї–∞–Љ: –≥–µ–љ—В–∞–Љ–Є—Ж–Є–љ—Г – –і–Њ 80%, —Ж–Є–њ—А–Њ—Д–ї–Њ–Ї—Б–∞—Ж–Є–љ—Г – 40–60% [7]. –Ю—В–≤–µ—В—Б—В–≤–µ–љ–љ—Л–µ –Ј–∞ —Б–Є–љ—В–µ–Ј –С–Ы–†–° –≥–µ–љ—Л –ї–Њ–Ї–∞–ї–Є–Ј–Њ–≤–∞–љ—Л –љ–∞ –њ–ї–∞–Ј–Љ–Є–і–∞—Е, –Ї–Њ—В–Њ—А—Л–µ —А–µ–њ–ї–Є—Ж–Є—А—Г—О—В—Б—П –∞–≤—В–Њ–љ–Њ–Љ–љ–Њ –≤ —Ж–Є—В–Њ–њ–ї–∞–Ј–Љ–µ –±–∞–Ї—В–µ—А–Є–∞–ї—М–љ–Њ–є –Ї–ї–µ—В–Ї–Є –Є —Б–њ–Њ—Б–Њ–±–љ—Л –њ–µ—А–µ–і–∞–≤–∞—В—М—Б—П –±–Њ–ї—М—И–Њ–Љ—Г —З–Є—Б–ї—Г –і—А—Г–≥–Є—Е –Њ—Б–Њ–±–µ–є –Ї–∞–Ї –≤–љ—Г—В—А–Є –≤–Є–і–∞, —В–∞–Ї –Є –њ—Г—В–µ–Љ –Љ–µ–ґ–≤–Є–і–Њ–≤–Њ–є –Є –Љ–µ–ґ—А–Њ–і–Њ–≤–Њ–є –њ–µ—А–µ–і–∞—З–Є. –≠—В–Њ—В –њ—А–Њ—Ж–µ—Б—Б –љ–Њ—Б–Є—В —Н–њ–Є–і–µ–Љ–Є—З–µ—Б–Ї–Є–є —Е–∞—А–∞–Ї—В–µ—А, –∞ –∞–љ—В–Є–±–Є–Њ—В–Є–Ї–Є —Б–њ–Њ—Б–Њ–±—Б—В–≤—Г—О—В —Б–µ–ї–µ–Ї—Ж–Є–Є —А–µ–Ј–Є—Б—В–µ–љ—В–љ—Л—Е –Ї–ї–Њ–љ–Њ–≤ –±–∞–Ї—В–µ—А–Є–є. –§–∞–Ї—В–Њ—А–∞–Љ–Є —А–Є—Б–Ї–∞ —А–∞—Б–њ—А–Њ—Б—В—А–∞–љ–µ–љ–Є—П –С–Ы–†–° —П–≤–ї—П—О—В—Б—П:
• –њ—А–µ–і—И–µ—Б—В–≤—Г—О—Й–∞—П —В–µ—А–∞–њ–Є—П —Ж–µ—Д–∞–ї–Њ—Б–њ–Њ—А–Є–љ–∞–Љ–Є III –њ–Њ–Ї–Њ–ї–µ–љ–Є—П [8] (–Є—Е —З—А–µ–Ј–Љ–µ—А–љ–Њ–µ –њ–Њ—В—А–µ–±–ї–µ–љ–Є–µ –≤ —В–µ—З–µ–љ–Є–µ –і–ї–Є—В–µ–ї—М–љ–Њ–≥–Њ –≤—А–µ–Љ–µ–љ–Є —В–∞–Ї–ґ–µ –≤–µ–і–µ—В –Ї –≤—Б–њ—Л—И–Ї–∞–Љ –Є–љ—Д–µ–Ї—Ж–Є–є, –Њ–±—Г—Б–ї–Њ–≤–ї–µ–љ–љ—Л—Е –Љ–µ—В–Є—Ж–Є–ї–ї–Є–љ—А–µ–Ј–Є—Б—В–µ–љ—В–љ—Л–Љ–Є —Б—В–∞—Д–Є–ї–Њ–Ї–Њ–Ї–Ї–∞–Љ–Є [9]);
• –њ—А–Є–Љ–µ–љ–µ–љ–Є–µ –∞—А—В–µ—А–Є–∞–ї—М–љ—Л—Е, —Ж–µ–љ—В—А–∞–ї—М–љ—Л—Е –≤–µ–љ–Њ–Ј–љ—Л—Е –Є –Љ–Њ—З–µ–≤—Л—Е –Ї–∞—В–µ—В–µ—А–Њ–≤;
• –Њ–Ї–∞–Ј–∞–љ–Є–µ –Љ–µ–і–Є—Ж–Є–љ—Б–Ї–Њ–є –њ–Њ–Љ–Њ—Й–Є –≤ –Ю–†–Ш–Ґ, –Ї—А—Г–њ–љ—Л—Е –±–Њ–ї—М–љ–Є—Ж–∞—Е (–±–Њ–ї–µ–µ 500 –Ї–Њ–µ–Ї), —Г—З—А–µ–ґ–і–µ–љ–Є—П—Е —Б–Њ—Ж–Є–∞–ї—М–љ–Њ–є –Ј–∞—Й–Є—В—Л.
–Я–Њ –і–∞–љ–љ—Л–Љ –Љ–љ–Њ–≥–Њ—Ж–µ–љ—В—А–Њ–≤–Њ–≥–Њ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П MYSTIC, —Б—А–µ–і–Є —Б—В—А–∞–љ –Х–≤—А–Њ–њ—Л –љ–∞–Є–±–Њ–ї—М—И—Г—О —З–∞—Б—В–Њ—В—Г —А–∞—Б–њ—А–Њ—Б—В—А–∞–љ–µ–љ–Є—П –С–Ы–†–° —Б—В–∞–±–Є–ї—М–љ–Њ –Њ—В–Љ–µ—З–∞—О—В –≤ –†–Њ—Б—Б–Є–Є –Є –Я–Њ–ї—М—И–µ (–і–Њ 40% —Б—А–µ–і–Є –≤—Б–µ—Е –Є–Ј—Г—З–µ–љ–љ—Л—Е —Н–љ—В–µ—А–Њ–±–∞–Ї—В–µ—А–Є–є) [10]. –Т –Њ—В–і–µ–ї—М–љ—Л—Е –ї–µ—З–µ–±–љ—Л—Е —Г—З—А–µ–ґ–і–µ–љ–Є—П—Е –†–§ —З–∞—Б—В–Њ—В–∞ –њ—А–Њ–і—Г–Ї—Ж–Є–Є –С–Ы–†–° —Б—А–µ–і–Є Klebsiella spp. –њ—А–µ–≤—Л—И–∞–µ—В 90% [11].
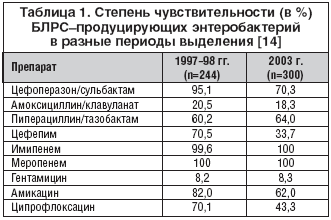
–°–Њ–≥–ї–∞—Б–љ–Њ –Ј–∞—А—Г–±–µ–ґ–љ—Л–Љ –њ—Г–±–ї–Є–Ї–∞—Ж–Є—П–Љ –Є–Љ–Є–њ–µ–љ–µ–Љ –Є –Љ–µ—А–Њ–њ–µ–љ–µ–Љ –≤ —А–∞–≤–љ–Њ–є —Б—В–µ–њ–µ–љ–Є —Б–Њ—Е—А–∞–љ—П—О—В –∞–Ї—В–Є–≤–љ–Њ—Б—В—М –њ—А–Њ—В–Є–≤ —Н–љ—В–µ—А–Њ–±–∞–Ї—В–µ—А–Є–є, –њ—А–Њ–і—Г—Ж–Є—А—Г—О—Й–Є—Е –С–Ы–†–° [12, 13], —З—В–Њ –њ–Њ–і—В–≤–µ—А–ґ–і–∞—О—В –Є —А–Њ—Б—Б–Є–є—Б–Ї–Є–µ –Є—Б—Б–ї–µ–і–Њ–≤–∞—В–µ–ї–Є [14] (—В–∞–±–ї. 1).
–°–Њ–≥–ї–∞—Б–љ–Њ —А–µ–Ї–Њ–Љ–µ–љ–і–∞—Ж–Є—П–Љ NCCLS, —И—В–∞–Љ–Љ—Л E. coli –Є Klebsiella spp., –њ—А–Њ–і—Г—Ж–Є—А—Г—О—Й–Є–µ –С–Ы–†–°, –і–Њ–ї–ґ–љ—Л —А–∞—Б—Б–Љ–∞—В—А–Є–≤–∞—В—М—Б—П –Ї–∞–Ї —Г—Б—В–Њ–є—З–Є–≤—Л–µ –Ї –њ–µ–љ–Є—Ж–Є–ї–ї–Є–љ–∞–Љ, —Ж–µ—Д–∞–ї–Њ—Б–њ–Њ—А–Є–љ–∞–Љ (–Ї—А–Њ–Љ–µ —Ж–µ—Д–∞–Љ–Є—Ж–Є–љ–Њ–≤), –∞–Ј—В—А–µ–Њ–љ–∞–Љ—Г [15], –∞ –ї–µ—З–µ–љ–Є–µ —Б–Њ–Њ—В–≤–µ—В—Б—В–≤—Г—О—Й–Є—Е –Є–љ—Д–µ–Ї—Ж–Є–є —Ж–µ—Д–∞–ї–Њ—Б–њ–Њ—А–Є–љ–∞–Љ–Є III–IV –њ–Њ–Ї–Њ–ї–µ–љ–Є—П –љ–µ—Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ –Є –≤–µ–і–µ—В –Ї –і–∞–ї—М–љ–µ–є—И–µ–Љ—Г —А–∞—Б–њ—А–Њ—Б—В—А–∞–љ–µ–љ–Є—О –С–Ы–†–°.
–Т—Л—П–≤–ї–µ–љ–Є–µ —И—В–∞–Љ–Љ–Њ–≤, –њ—А–Њ–і—Г—Ж–Є—А—Г—О—Й–Є—Е –С–Ы–†–°, –љ–µ–≤–Њ–Ј–Љ–Њ–ґ–љ–Њ –Њ—Б—Г—Й–µ—Б—В–≤–Є—В—М —А—Г—В–Є–љ–љ—Л–Љ–Є –Љ–µ—В–Њ–і–∞–Љ–Є –Њ—Ж–µ–љ–Ї–Є –∞–љ—В–Є–±–Є–Њ—В–Є–Ї–Њ—З—Г–≤—Б—В–≤–Є—В–µ–ї—М–љ–Њ—Б—В–Є, –њ–Њ—Н—В–Њ–Љ—Г —З–∞—Б—В–Њ –њ–Њ–ї—М–Ј—Г—О—В—Б—П –Ї–Њ—Б–≤–µ–љ–љ—Л–Љ–Є –њ—А–Є–Ј–љ–∞–Ї–∞–Љ–Є. –Х—Б–ї–Є –≤—Л–і–µ–ї–µ–љ –≥–Њ—Б–њ–Є—В–∞–ї—М–љ—Л–є —И—В–∞–Љ–Љ –Ї–ї–µ–±—Б–Є–µ–ї–ї—Л –Є–ї–Є –Ї–Є—И–µ—З–љ–Њ–є –њ–∞–ї–Њ—З–Ї–Є, —Г—Б—В–Њ–є—З–Є–≤—Л–є –њ—А–Є –Њ–њ—А–µ–і–µ–ї–µ–љ–Є–Є –і–Є—Б–Ї–Њ––і–Є—Д—Д—Г–Ј–Є–Њ–љ–љ—Л–Љ –Љ–µ—В–Њ–і–Њ–Љ —Е–Њ—В—П –±—Л –Ї –Њ–і–љ–Њ–Љ—Г –Є–Ј —В—А–µ—Е –∞–љ—В–Є–±–Є–Њ—В–Є–Ї–Њ–≤ – —Ж–µ—Д–Њ—В–∞–Ї—Б–Є–Љ—Г, —Ж–µ—Д—В—А–Є–∞–Ї—Б–Њ–љ—Г –Є–ї–Є —Ж–µ—Д—В–∞–Ј–Є–і–Є–Љ—Г, —В–Њ –љ–µ —Б–ї–µ–і—Г–µ—В –љ–∞–Ј–љ–∞—З–∞—В—М —Ж–µ—Д–∞–ї–Њ—Б–њ–Њ—А–Є–љ—Л, –∞ –љ–∞–Є–±–Њ–ї–µ–µ –љ–∞–і–µ–ґ–љ—Л–Љ–Є —Б—А–µ–і—Б—В–≤–∞–Љ–Є –≤ —Н—В–Њ–Љ —Б–ї—Г—З–∞–µ —П–≤–ї—П—О—В—Б—П –Ї–∞—А–±–∞–њ–µ–љ–µ–Љ—Л.
–Т —В–∞–±–ї–Є—Ж–µ 2 –њ—А–µ–і—Б—В–∞–≤–ї–µ–љ—Л –Ї—А–Є—В–µ—А–Є–Є —З—Г–≤—Б—В–≤–Є—В–µ–ї—М–љ–Њ—Б—В–Є K. pneumoniae –Є E. coli –Ї —Ж–µ—Д–∞–ї–Њ—Б–њ–Њ—А–Є–љ–∞–Љ, –њ–Њ–Ј–≤–Њ–ї—П—О—Й–Є–µ —А–∞—Б—Б–Љ–∞—В—А–Є–≤–∞—В—М —И—В–∞–Љ–Љ—Л —Н—В–Є—Е –Љ–Є–Ї—А–Њ–Њ—А–≥–∞–љ–Є–Ј–Љ–Њ–≤ –Ї–∞–Ї –њ–Њ–і–Њ–Ј—А–Є—В–µ–ї—М–љ—Л–µ –љ–∞ –њ—А–Њ–і—Г–Ї—Ж–Є—О –С–Ы–†–°.
–Т –Ї–∞—З–µ—Б—В–≤–µ –њ–Њ–і—В–≤–µ—А–ґ–і–∞—О—Й–Є—Е —В–µ—Б—В–Њ–≤ –Є—Б–њ–Њ–ї—М–Ј—Г—О—В —Б—В–∞–љ–і–∞—А—В–љ—Л–µ –і–Є—Б–Ї–Є —Б –Њ–±—Л—З–љ—Л–Љ —Б–Њ–і–µ—А–ґ–∞–љ–Є–µ–Љ —Ж–µ—Д–Њ—В–∞–Ї—Б–Є–Љ–∞ –Є —Ж–µ—Д—В–∞–Ј–Є–і–Є–Љ–∞ (–њ–Њ 30 –Љ–Ї–≥ –љ–∞ –і–Є—Б–Ї) –Є –і–Є—Б–Ї–Є, —Б–Њ–і–µ—А–ґ–∞—Й–Є–µ –Ї–Њ–Љ–±–Є–љ–∞—Ж–Є–Є –Ї–∞–ґ–і–Њ–≥–Њ –Є–Ј —Н—В–Є—Е –∞–љ—В–Є–±–Є–Њ—В–Є–Ї–Њ–≤ —Б –Ї–ї–∞–≤—Г–ї–∞–љ–Њ–≤–Њ–є –Ї–Є—Б–ї–Њ—В–Њ–є (30 –Љ–Ї–≥ —Ж–µ—Д–∞–ї–Њ—Б–њ–Њ—А–Є–љ–∞ + 10 –Љ–Ї–≥ –Ї–ї–∞–≤—Г–ї–∞–љ–∞—В–∞). –Ь–Є–Ї—А–Њ–Њ—А–≥–∞–љ–Є–Ј–Љ —Б—З–Є—В–∞–µ—В—Б—П –њ—А–Њ–і—Г—Ж–µ–љ—В–Њ–Љ –С–Ы–†–°, –µ—Б–ї–Є –Ј–Њ–љ–∞ –Ј–∞–і–µ—А–ґ–Ї–Є —А–Њ—Б—В–∞ –≤–Њ–Ї—А—Г–≥ –і–Є—Б–Ї–∞ —Б –Ї–Њ–Љ–±–Є–љ–∞—Ж–Є–µ–є —Ж–µ—Д–∞–ї–Њ—Б–њ–Њ—А–Є–љ–∞ –Є –Ї–ї–∞–≤—Г–ї–∞–љ–∞—В–∞ –љ–∞ 5 –Љ–Љ –Є –±–Њ–ї–µ–µ –њ—А–µ–≤—Л—И–∞–µ—В –і–Є–∞–Љ–µ—В—А –Ј–Њ–љ—Л –≤–Њ–Ї—А—Г–≥ –і–Є—Б–Ї–∞ —Б —Ж–µ—Д–∞–ї–Њ—Б–њ–Њ—А–Є–љ–Њ–Љ. –Ф–ї—П –њ–Њ–ї–Њ–ґ–Є—В–µ–ї—М–љ–Њ–≥–Њ —А–µ–Ј—Г–ї—М—В–∞—В–∞ –і–Њ—Б—В–∞—В–Њ—З–љ–Њ –≤—Л—П–≤–Є—В—М —А–∞–Ј–ї–Є—З–Є—П —Е–Њ—В—П –±—Л –і–ї—П –Њ–і–љ–Њ–є –њ–∞—А—Л –і–Є—Б–Ї–Њ–≤.
–Т –Љ–µ—В–Њ–і–µ —Б–µ—А–Є–є–љ—Л—Е —А–∞–Ј–≤–µ–і–µ–љ–Є–є –≤ –±—Г–ї—М–Њ–љ–µ –Љ–Є–Ї—А–Њ–Њ—А–≥–∞–љ–Є–Ј–Љ —Б—З–Є—В–∞–µ—В—Б—П –њ—А–Њ–і—Г—Ж–µ–љ—В–Њ–Љ –С–Ы–†–°, –µ—Б–ї–Є –Ј–љ–∞—З–µ–љ–Є–µ –Ь–Я–Ъ –≤ –њ—А–Є—Б—Г—В—Б—В–≤–Є–Є –Ї–ї–∞–≤—Г–ї–∞–љ–∞—В–∞ –љ–∞ 3 –Є –±–Њ–ї—М—И–µ —А–∞–Ј–≤–µ–і–µ–љ–Є–є —Г—Б—В—Г–њ–∞–µ—В —Б–Њ–Њ—В–≤–µ—В—Б—В–≤—Г—О—Й–µ–Љ—Г –Ј–љ–∞—З–µ–љ–Є—О –Ь–Я–Ъ —Ж–µ—Д–∞–ї–Њ—Б–њ–Њ—А–Є–љ–∞ –±–µ–Ј –Ї–ї–∞–≤—Г–ї–∞–љ–∞—В–∞.
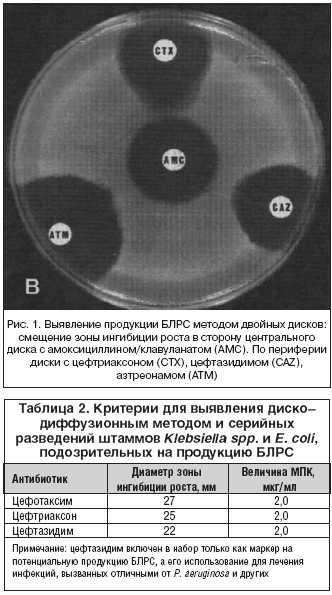
–Ф–Њ—Б—В–∞—В–Њ—З–љ–Њ –і–µ–Љ–Њ–љ—Б—В—А–∞—В–Є–≤–љ—Л–Љ —П–≤–ї—П–µ—В—Б—П –Љ–µ—В–Њ–і –і–≤—Г—Е –і–Є—Б–Ї–Њ–≤. –Э–∞ —З–∞—И–Ї—Г –Я–µ—В—А–Є —Б –∞–≥–∞—А–Њ–Љ Mueller–Hinton, –њ—А–µ–і–≤–∞—А–Є—В–µ–ї—М–љ–Њ –Ј–∞—Б–µ—П–љ–љ—Л–Љ –Є—Б—Б–ї–µ–і—Г–µ–Љ—Л–Љ –Љ–Є–Ї—А–Њ–Њ—А–≥–∞–љ–Є–Ј–Љ–Њ–Љ, –љ–∞–Ї–ї–∞–і—Л–≤–∞—О—В –і–Є—Б–Ї —Б –∞–Љ–Њ–Ї—Б–Є—Ж–Є–ї–ї–Є–љ–Њ–Љ/–Ї–ї–∞–≤—Г–ї–∞–љ–∞—В–Њ–Љ, –∞ –љ–∞ —А–∞—Б—Б—В–Њ—П–љ–Є–Є 30 –Љ–Љ –Њ—В –љ–µ–≥–Њ – –і–Є—Б–Ї —Б –Њ–і–љ–Є–Љ –Є–Ј —Ж–µ—Д–∞–ї–Њ—Б–њ–Њ—А–Є–љ–Њ–≤ III –њ–Њ–Ї–Њ–ї–µ–љ–Є—П (—А–∞—Б—Б—В–Њ—П–љ–Є–µ –Є–Ј–Љ–µ—А—П–µ—В—Б—П –Њ—В —Ж–µ–љ—В—А–∞ –і–Є—Б–Ї–Њ–≤). –Т–Њ–Ј–Љ–Њ–ґ–љ—Л –≤–∞—А–Є–∞–љ—В—Л –љ–∞–ї–Њ–ґ–µ–љ–Є—П 2 –Є 3 –і–Є—Б–Ї–Њ–≤ —Б —А–∞–Ј–ї–Є—З–љ—Л–Љ–Є —Ж–µ—Д–∞–ї–Њ—Б–њ–Њ—А–Є–љ–∞–Љ–Є (–Є –∞–Ј—В—А–µ–Њ–љ–∞–Љ–Њ–Љ) –≤–Њ–Ї—А—Г–≥ –і–Є—Б–Ї–∞ —Б –∞–Љ–Њ—Б–Ї–Є—Ж–Є–ї–ї–Є–љ–Њ–Љ/–Ї–ї–∞–≤—Г–ї–∞–љ–∞—В–Њ–Љ. –Х—Б–ї–Є –Љ–Є–Ї—А–Њ–Њ—А–≥–∞–љ–Є–Ј–Љ –њ—А–Њ–і—Г—Ж–Є—А—Г–µ—В –С–Ы–†–°, –Ј–Њ–љ–∞ –Є–љ–≥–Є–±–Є—Ж–Є–Є —А–Њ—Б—В–∞ –≤–Њ–Ї—А—Г–≥ –і–Є—Б–Ї–∞ —Б —Ж–µ—Д–∞–ї–Њ—Б–њ–Њ—А–Є–љ–Њ–Љ –Њ–Ї–∞–ґ–µ—В—Б—П «–≤—Л—В—П–љ—Г—В–Њ–є» –≤ —Б—В–Њ—А–Њ–љ—Г –і–Є—Б–Ї–∞ —Б –∞–Љ–Њ–Ї—Б–Є—Ж–Є–ї–ї–Є–љ–Њ–Љ/–Ї–ї–∞–≤—Г–ї–∞–љ–∞—В–Њ–Љ –Є–ї–Є –њ—А–Њ–Є—Б—Е–Њ–і–Є—В —Б–ї–Є—П–љ–Є–µ –Ј–Њ–љ. –Я—А–Є—З–Є–љ–Њ–є –љ–∞–±–ї—О–і–∞–µ–Љ–Њ–≥–Њ —Н—Д—Д–µ–Ї—В–∞ —П–≤–ї—П–µ—В—Б—П –њ–Њ–і–∞–≤–ї–µ–љ–Є–µ —А–Њ—Б—В–∞ –Љ–Є–Ї—А–Њ–Њ—А–≥–∞–љ–Є–Ј–Љ–∞ –≤ —В–Њ–є –Ј–Њ–љ–µ, –Ї—Г–і–∞ –і–Є—Д—Д—Г–љ–і–Є—А—Г—О—В –Є –Ї–ї–∞–≤—Г–ї–∞–љ–∞—В, –Є —Ж–µ—Д–∞–ї–Њ—Б–њ–Њ—А–Є–љ (—А–Є—Б. 1).
–С–Ы –Ї–ї–∞—Б—Б–∞ –° –Њ—В–љ–Њ—Б—П—В—Б—П –Ї –љ–∞–Є–±–Њ–ї–µ–µ —А–∞—Б–њ—А–Њ—Б—В—А–∞–љ–µ–љ–љ—Л–Љ —Д–µ—А–Љ–µ–љ—В–∞–Љ —Б —Е—А–Њ–Љ–Њ—Б–Њ–Љ–љ–Њ–є –ї–Њ–Ї–∞–ї–Є–Ј–∞—Ж–Є–µ–є –≥–µ–љ–Њ–≤ (AmpC), –Ї–Њ—В–Њ—А—Л–µ –Њ–±–љ–∞—А—Г–ґ–Є–≤–∞—О—В—Б—П –њ—А–∞–Ї—В–Є—З–µ—Б–Ї–Є —Г –≤—Б–µ—Е –≥—А–∞–Љ–Њ—В—А–Є—Ж–∞—В–µ–ї—М–љ—Л—Е –±–∞–Ї—В–µ—А–Є–є. –Т –Њ—В–ї–Є—З–Є–µ –Њ—В –њ–ї–∞–Ј–Љ–Є–і–љ—Л—Е –С–Ы–†–° –Њ–љ–Є –љ–µ –њ–µ—А–µ–і–∞—О—В—Б—П –і—А—Г–≥–Є–Љ —Н–љ—В–µ—А–Њ–±–∞–Ї—В–µ—А–Є—П–Љ –Є —Е–∞—А–∞–Ї—В–µ—А–Є–Ј—Г—О—В—Б—П –Є–љ–і—Г—Ж–Є–±–µ–ї—М–љ–Њ—Б—В—М—О –Є –≥–Є–њ–µ—А–њ—А–Њ–і—Г–Ї—Ж–Є–µ–є, –≤–Њ–Ј–љ–Є–Ї–∞—О—Й–µ–є –љ–∞ —Д–Њ–љ–µ –ї–µ—З–µ–љ–Є—П. –Ю–±—Й–Є–Љ–Є —Б–≤–Њ–є—Б—В–≤–∞–Љ–Є —Н—В–Є—Е —Д–µ—А–Љ–µ–љ—В–Њ–≤ —П–≤–ї—П—О—В—Б—П: —Б–њ–Њ—Б–Њ–±–љ–Њ—Б—В—М –≥–Є–і—А–Њ–ї–Є–Ј–Њ–≤–∞—В—М –њ–µ–љ–Є—Ж–Є–ї–ї–Є–љ—Л –Є —Ж–µ—Д–∞–ї–Њ—Б–њ–Њ—А–Є–љ—Л I–III –њ–Њ–Ї–Њ–ї–µ–љ–Є—П; —Г—Б—В–Њ–є—З–Є–≤–Њ—Б—В—М –Ї –і–µ–є—Б—В–≤–Є—О –Є–љ–≥–Є–±–Є—В–Њ—А–Њ–≤; —З—Г–≤—Б—В–≤–Є—В–µ–ї—М–љ–Њ—Б—В—М –Ї —Ж–µ—Д–∞–ї–Њ—Б–њ–Њ—А–Є–љ–∞–Љ IV –њ–Њ–Ї–Њ–ї–µ–љ–Є—П –Є –Ї–∞—А–±–∞–њ–µ–љ–µ–Љ–∞–Љ.
–Ф–ї—П –±–∞–Ї—В–µ—А–Є–є –≥—А—Г–њ–њ—Л Enterobacter, Serratia, Morganella, P. aeruginosa —Е–∞—А–∞–Ї—В–µ—А–µ–љ –Є–љ–і—Г—Ж–Є–±–µ–ї—М–љ—Л–є —В–Є–њ —Н–Ї—Б–њ—А–µ—Б—Б–Є–Є –≥–µ–љ–Њ–≤. –Я—А–Є –Њ—В—Б—Г—В—Б—В–≤–Є–Є –≤ —Б—А–µ–і–µ –∞–љ—В–Є–±–Є–Њ—В–Є–Ї–Њ–≤ —Д–µ—А–Љ–µ–љ—В –њ—А–∞–Ї—В–Є—З–µ—Б–Ї–Є –љ–µ –≤—Л—А–∞–±–∞—В—Л–≤–∞–µ—В—Б—П, –љ–Њ –њ–Њ—Б–ї–µ –Ї–Њ–љ—В–∞–Ї—В–∞ —Б –љ–µ–Ї–Њ—В–Њ—А—Л–Љ–Є b––ї–∞–Ї—В–∞–Љ–∞–Љ–Є, –≤ —З–∞—Б—В–љ–Њ—Б—В–Є, —Б —Ж–µ—Д—В–∞–Ј–Є–і–Є–Љ–Њ–Љ, —Б–Ї–Њ—А–Њ—Б—В—М —Б–Є–љ—В–µ–Ј–∞ —А–µ–Ј–Ї–Њ –≤–Њ–Ј—А–∞—Б—В–∞–µ—В [16], —З—В–Њ –Љ–Њ–ґ–µ—В —Б–Њ–њ—А–Њ–≤–Њ–ґ–і–∞—В—М—Б—П —Б–µ–ї–µ–Ї—Ж–Є–µ–є –≤–∞–љ–Ї–Њ–Љ–Є—Ж–Є–љ—А–µ–Ј–Є—Б—В–µ–љ—В–љ—Л—Е —Н–љ—В–µ—А–Њ–Ї–Њ–Ї–Ї–Њ–≤ [17]. –Я—А–Є –љ–∞—А—Г—И–µ–љ–Є–Є —А–µ–≥—Г–ї—П—В–Њ—А–љ—Л—Е –Љ–µ—Е–∞–љ–Є–Ј–Љ–Њ–≤ –≤–Њ–Ј–Љ–Њ–ґ–љ–∞ –њ–Њ—Б—В–Њ—П–љ–љ–∞—П –≥–Є–њ–µ—А–њ—А–Њ–і—Г–Ї—Ж–Є—П —Д–µ—А–Љ–µ–љ—В–∞. –Ь–Њ—Й–љ—Л–Љ –Є–љ–і—Г–Ї—В–Њ—А–Њ–Љ —Е—А–Њ–Љ–Њ—Б–Њ–Љ–љ—Л—Е –С–Ы –Ї–ї–∞—Б—Б–∞ –° —П–≤–ї—П–µ—В—Б—П –Є–Љ–Є–њ–µ–љ–µ–Љ [18], –њ–Њ—Н—В–Њ–Љ—Г –µ–≥–Њ –њ—А–Є–Љ–µ–љ–µ–љ–Є–µ –љ–µ—А–µ–і–Ї–Њ –≤–µ–і–µ—В –Ї —Б–µ–ї–µ–Ї—Ж–Є–Є —И—В–∞–Љ–Љ–Њ–≤, —Г—Б—В–Њ–є—З–Є–≤—Л—Е –Ї —Ж–µ—Д–∞–ї–Њ—Б–њ–Њ—А–Є–љ–∞–Љ III –њ–Њ–Ї–Њ–ї–µ–љ–Є—П. –°–Њ–≥–ї–∞—Б–љ–Њ –Љ–µ–ґ–і—Г–љ–∞—А–Њ–і–љ–Њ–Љ—Г –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—О MYSTIC —А–∞—Б–њ—А–Њ—Б—В—А–∞–љ–µ–љ–љ–Њ—Б—В—М –Є–љ–і—Г—Ж–Є–±–µ–ї—М–љ—Л—Е AmpC —И—В–∞–Љ–Љ–Њ–≤ –≤ –†–Њ—Б—Б–Є–Є –Є –Я–Њ–ї—М—И–µ –Њ–і–Є–љ–∞–Ї–Њ–≤–Њ –≤—Л—Б–Њ–Ї–∞ –Є –і–Њ—Б—В–Є–≥–∞–µ—В 30% (–≤ –і—А—Г–≥–Є—Е —Б—В—А–∞–љ–∞—Е –Х–≤—А–Њ–њ—Л —Н—В–Њ—В –њ–Њ–Ї–∞–Ј–∞—В–µ–ї—М –љ–∞—Е–Њ–і–Є—В—Б—П –≤ –њ—А–µ–і–µ–ї–∞—Е 5–9%) [19].
–Ч–љ–∞—З–µ–љ–Є–µ –њ—А–µ–і—Б—В–∞–≤–Є—В–µ–ї–µ–є –і—А—Г–≥–Є—Е –Ї–ї–∞—Б—Б–Њ–≤ –С–Ы –љ–µ —Б—В–Њ–ї—М —Б—Г—Й–µ—Б—В–≤–µ–љ–љ–Њ, –њ–Њ—Б–Ї–Њ–ї—М–Ї—Г —Ж–µ—Д–∞–ї–Њ—Б–њ–Њ—А–Є–љ—Л III–IV –њ–Њ–Ї–Њ–ї–µ–љ–Є–є –љ–∞—А—П–і—Г —Б –Ї–∞—А–±–∞–њ–µ–љ–µ–Љ–∞–Љ–Є –≤ –њ–Њ–і–∞–≤–ї—П—О—Й–µ–Љ –±–Њ–ї—М—И–Є–љ—Б—В–≤–µ —Б–ї—Г—З–∞–µ–≤ —Б–Њ—Е—А–∞–љ—П—О—В —Б–≤–Њ—О –∞–Ї—В–Є–≤–љ–Њ—Б—В—М.
–Ь–µ—Е–∞–љ–Є–Ј–Љ—Л —Д–Њ—А–Љ–Є—А–Њ–≤–∞–љ–Є—П
—А–µ–Ј–Є—Б—В–µ–љ—В–љ–Њ—Б—В–Є –Ї –Ї–∞—А–±–∞–њ–µ–љ–µ–Љ–∞–Љ
–Ь–µ—Е–∞–љ–Є–Ј–Љ—Л —А–µ–Ј–Є—Б—В–µ–љ—В–љ–Њ—Б—В–Є –Љ–Є–Ї—А–Њ–Њ—А–≥–∞–љ–Є–Ј–Љ–Њ–≤ –Ї –Ї–∞—А–±–∞—А–µ–љ–µ–Љ–∞–Љ —Б—Е–Њ–і–љ—Л–µ, –Є—Б–Ї–ї—О—З–µ–љ–Є–µ–Љ —П–≤–ї—П–µ—В—Б—П P. aeruginosa. –Ъ–∞—А–±–∞–њ–µ–љ–µ–Љ—Л –њ—А–Њ–љ–Є–Ї–∞—О—В –≤ –Ї–ї–µ—В–Ї—Г —З–µ—А–µ–Ј –Њ—Б–Њ–±—Л–µ –±–µ–ї–Ї–Њ–≤—Л–µ —Б—В—А—Г–Ї—В—Г—А—Л –≤–љ–µ—И–љ–µ–є –Љ–µ–Љ–±—А–∞–љ—Л – –њ–Њ—А–Є–љ–Њ–≤—Л–µ –Ї–∞–љ–∞–ї—Л. –Э–∞–Є–±–Њ–ї–µ–µ —З–∞—Б—В—Л–Љ –Љ–µ—Е–∞–љ–Є–Ј–Љ–Њ–Љ —Г—Б—В–Њ–є—З–Є–≤–Њ—Б—В–Є —Б–Є–љ–µ–≥–љ–Њ–є–љ–Њ–є –њ–∞–ї–Њ—З–Ї–Є –Ї –Є–Љ–Є–њ–µ–љ–µ–Љ—Г —П–≤–ї—П–µ—В—Б—П —Г—В—А–∞—В–∞ –њ–Њ—А–Є–љ–Њ–≤–Њ–≥–Њ –±–µ–ї–Ї–∞ OprD (–Є–ї–Є —Б–љ–Є–ґ–µ–љ–Є–µ –µ–≥–Њ —Н–Ї—Б–њ—А–µ—Б—Б–Є–Є) –≤ —А–µ–Ј—Г–ї—М—В–∞—В–µ –Љ—Г—В–∞—Ж–Є–є, –њ—А–Њ–Є—Б—Е–Њ–і—П—Й–Є—Е —Б —З–∞—Б—В–Њ—В–Њ–є 10–7, —З—В–Њ –≤–µ–і–µ—В –Ї –љ–∞—А—Г—И–µ–љ–Є—О –њ—А–Њ–љ–Є–Ї–љ–Њ–≤–µ–љ–Є—П –∞–љ—В–Є–±–Є–Њ—В–Є–Ї–∞ –≤ –Ї–ї–µ—В–Ї—Г [20]. –Я—А–Є —Н—В–Њ–Љ –Ь–Я–Ъ —Г–≤–µ–ї–Є—З–Є–≤–∞–µ—В—Б—П —Б 1–2 –Љ–Ї–≥/–Љ–ї –і–Њ 8–32 –Љ–Ї–≥/–Љ–ї, —З—В–Њ —Б–Њ–њ—А–Њ–≤–Њ–ґ–і–∞–µ—В—Б—П –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Њ–є –љ–µ—Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В—М—О –њ—А–µ–њ–∞—А–∞—В–∞. –≠—В–Њ—В –Љ–µ—Е–∞–љ–Є–Ј–Љ —А–µ–Ј–Є—Б—В–µ–љ—В–љ–Њ—Б—В–Є –љ–µ –Ј–∞—В—А–∞–≥–Є–≤–∞–µ—В –Љ–µ—А–Њ–њ–µ–љ–µ–Љ, —В–∞–Ї –Ї–∞–Ї –µ–≥–Њ —В—А–∞–љ—Б–њ–Њ—А—В –≤ –Ї–ї–µ—В–Ї—Г –Љ–Њ–ґ–µ—В –Њ—Б—Г—Й–µ—Б—В–≤–ї—П—В—М—Б—П –Є —З–µ—А–µ–Ј –і—А—Г–≥–Є–µ –њ–Њ—А–Є–љ—Л.
–†–µ–Ј–Є—Б—В–µ–љ—В–љ–Њ—Б—В—М –Љ–µ—А–Њ–њ–µ–љ–µ–Љ–∞ —Б–≤—П–Ј–∞–љ–∞ —Б –∞–Ї—В–Є–≤–∞—Ж–Є–µ–є —Б–Є—Б—В–µ–Љ –∞–Ї—В–Є–≤–љ–Њ–≥–Њ –≤—Л–≤–µ–і–µ–љ–Є—П –∞–љ—В–Є–±–Є–Њ—В–Є–Ї–∞ –Ј–∞ –њ—А–µ–і–µ–ї—Л –Љ–Є–Ї—А–Њ–Њ—А–≥–∞–љ–Є–Ј–Љ–∞ (—Н—Д—Д–ї—О–Ї—Б). –Ф–∞–љ–љ—Л–є –Љ–µ—Е–∞–љ–Є–Ј–Љ —Г—Б—В–Њ–є—З–Є–≤–Њ—Б—В–Є –Ј–∞–≤–Є—Б–Є—В –Њ—В –і–µ—П—В–µ–ї—М–љ–Њ—Б—В–Є –њ—А–Њ—В–µ–Є–љ–Њ–≤ MexA– MexB–OprM, –њ—А–Є—З–µ–Љ MexB –њ—А–µ–і—Б—В–∞–≤–ї—П–µ—В —Б–Њ–±–Њ–є –ї–Њ–Ї–∞–ї–Є–Ј–Њ–≤–∞–љ–љ—Л–є –љ–∞ —Ж–Є—В–Њ–њ–ї–∞–Ј–Љ–∞—В–Є—З–µ—Б–Ї–Њ–є –Љ–µ–Љ–±—А–∞–љ–µ —Н—Д—Д–ї—О–Ї—Б–љ—Л–є –љ–∞—Б–Њ—Б, OprM –Њ–±—А–∞–Ј—Г–µ—В –њ–Њ—А—Л, —З–µ—А–µ–Ј –Ї–Њ—В–Њ—А—Л–µ —Г–і–∞–ї—П–µ—В—Б—П –∞–љ—В–Є–±–Є–Њ—В–Є–Ї, –∞ MexA —Б–≤—П–Ј—Л–≤–∞–µ—В –Є—Е –≤–Њ–µ–і–Є–љ–Њ [21] (—А–Є—Б. 2). –Я—А–Є —Н—В–Њ–Љ –Ь–Я–Ъ —Г–≤–µ–ї–Є—З–Є–≤–∞–µ—В—Б—П –љ–µ–Ј–љ–∞—З–Є—В–µ–ї—М–љ–Њ (—Б 0,12–0,5 –Љ–Ї–≥/–Љ–ї –і–Њ 2–4 –Љ–Ї–≥/–Љ–ї3), –∞ –Ї–ї–Є–љ–Є—З–µ—Б–Ї–∞—П —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В—М –Љ–µ—А–Њ–њ–µ–љ–µ–Љ–∞ —Б–Њ—Е—А–∞–љ—П–µ—В—Б—П –њ—А–Є –µ–≥–Њ –љ–∞–Ј–љ–∞—З–µ–љ–Є–Є –≤ —Б—Г—В–Њ—З–љ–Њ–є –і–Њ–Ј–µ 3 –≥. –Ы–Є—И—М —Б–Њ—З–µ—В–∞–љ–Є–µ –Њ–±–Њ–Є—Е –Љ–µ—Е–∞–љ–Є–Ј–Љ–Њ–≤ – –∞–Ї—В–Є–≤–љ–Њ–≥–Њ –≤—Л–≤–µ–і–µ–љ–Є—П –Є —Г—В—А–∞—В—Л –њ–Њ—А–Є–љ–∞ OprD (—З—В–Њ –≤–Њ–Ј–Љ–Њ–ґ–љ–Њ –њ—А–Є –і–≤—Г—Е –Њ–і–љ–Њ–≤—А–µ–Љ–µ–љ–љ—Л—Е –≥–µ–љ–љ—Л—Е –Љ—Г—В–∞—Ж–Є—П—Е, –≤–µ—А–Њ—П—В–љ–Њ—Б—В—М –Ї–Њ—В–Њ—А—Л—Е –Ї—А–∞–є–љ–µ –љ–Є–Ј–Ї–∞—П – 10–14), –њ—А–Є–≤–Њ–і–Є—В –Ї —А–∞–Ј–≤–Є—В–Є—О —А–µ–Ј–Є—Б—В–µ–љ—В–љ–Њ—Б—В–Є –Є –љ–µ—Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В–Є —В–µ—А–∞–њ–Є–Є [22].
–Т –Х–≤—А–Њ–њ–µ–є—Б–Ї–Є—Е —Б—В—А–∞–љ–∞—Е –љ–∞–Є–±–Њ–ї–µ–µ –≤—Л—Б–Њ–Ї—Г—О –∞–Ї—В–Є–≤–љ–Њ—Б—В—М –њ—А–Њ—В–Є–≤ P. aeruginosa —Б–Њ—Е—А–∞–љ—П—О—В –Љ–µ—А–Њ–њ–µ–љ–µ–Љ, –∞–Љ–Є–Ї–∞—Ж–Є–љ –Є –њ–Є–њ–µ—А–∞—Ж–Є–ї–ї–Є–љ/—В–∞–Ј–Њ–±–∞–Ї—В–∞–Љ [23] (—А–Є—Б. 3–Р). –Т –†–Њ—Б—Б–Є–Є –≤ –Ю–†–Ш–Ґ –љ–∞–Є–Љ–µ–љ—М—И–Є–є —Г—А–Њ–≤–µ–љ—М —Г—Б—В–Њ–є—З–Є–≤–Њ—Б—В–Є —Б–Є–љ–µ–≥–љ–Њ–є–љ–Њ–є –њ–∞–ї–Њ—З–Ї–Є –Њ—В–Љ–µ—З–∞–µ—В—Б—П –Ї –Љ–µ—А–Њ–њ–µ–љ–µ–Љ—Г, –∞–Љ–Є–Ї–∞—Ж–Є–љ—Г –Є —Ж–µ—Д—В–∞–Ј–Є–і–Є–Љ—Г, –≤ —В–Њ –≤—А–µ–Љ—П –Ї–∞–Ї —А–µ–Ј–Є—Б—В–µ–љ—В–љ–Њ—Б—В—М –Ї –Є–Љ–Є–њ–µ–љ–µ–Љ—Г, —Ж–Є–њ—А–Њ—Д–ї–Њ–Ї—Б–∞—Ж–Є–љ—Г, –њ–Є–њ–µ—А–∞—Ж–Є–ї–ї–Є–љ—Г/—В–∞–Ј–Њ–±–∞–Ї—В–∞–Љ—Г –Є –Њ—Б–Њ–±–µ–љ–љ–Њ –≥–µ–љ—В–∞–Љ–Є—Ж–Є–љ—Г –≤—Л—И–µ [24] (—А–Є—Б 3–С).
–Я–Њ –і–∞–љ–љ—Л–Љ –Њ—В–і–µ–ї—М–љ—Л—Е –∞–≤—В–Њ—А–Њ–≤, –і–Њ 44% —И—В–∞–Љ–Љ–Њ–≤ P. aeruginosa, —А–µ–Ј–Є—Б—В–µ–љ—В–љ—Л—Е –Ї –Є–Љ–Є–њ–µ–љ–µ–Љ—Г, —Б–Њ—Е—А–∞–љ—П–ї–Є —З—Г–≤—Б—В–≤–Є—В–µ–ї—М–љ–Њ—Б—В—М –Ї –Љ–µ—А–Њ–њ–µ–љ–µ–Љ—Г [25]. –Т –Љ–љ–Њ–≥–Њ—Ж–µ–љ—В—А–Њ–≤–Њ–Љ –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Њ–Љ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є, –њ—А–Њ–≤–µ–і–µ–љ–љ–Њ–Љ –≤ –†–Њ—Б—Б–Є–Є, 92% –Є–Ј–Њ–ї—П—В–Њ–≤ P. aeruginosa –Њ—В –±–Њ–ї—М–љ—Л—Е —Б —В—П–ґ–µ–ї—Л–Љ–Є –Є–љ—Д–µ–Ї—Ж–Є—П–Љ–Є –≤ –Ю–†–Ш–Ґ –±—Л–ї–Є —З—Г–≤—Б—В–≤–Є—В–µ–ї—М–љ—Л –Ї –Љ–µ—А–Њ–њ–µ–љ–µ–Љ—Г [26].
–Я–Њ—В—А–µ–±–ї–µ–љ–Є–µ –Є–Љ–Є–њ–µ–љ–µ–Љ–∞ –Ї–Њ—А—А–µ–ї–Є—А—Г–µ—В —Б —А–Њ—Б—В–Њ–Љ —А–µ–Ј–Є—Б—В–µ–љ—В–љ–Њ—Б—В–Є –Ї –љ–µ–Љ—Г –Є –∞–љ—В–Є—Б–Є–љ–µ–≥–љ–Њ–є–љ—Л–Љ —Ж–µ—Д–∞–ї–Њ—Б–њ–Њ—А–Є–љ–∞–Љ —Г P. aeruginosa [27]. –Э–∞–њ—А–Њ—В–Є–≤, –њ—А–Є–Љ–µ–љ–µ–љ–Є–µ –Љ–µ—А–Њ–њ–µ–љ–µ–Љ–∞ –љ–µ –≤–µ–і–µ—В –Ї —Б–µ–ї–µ–Ї—Ж–Є–Є AmpC —И—В–∞–Љ–Љ–Њ–≤ P. aeruginosa – –≥–Є–њ–µ—А–њ—А–Њ–і—Г—Ж–µ–љ—В–Њ–≤ —Е—А–Њ–Љ–Њ—Б–Њ–Љ–љ—Л—Е –С–Ы, —В–∞–Ї –Ї–∞–Ї –њ—А–µ–њ–∞—А–∞—В –њ–Њ–і–∞–≤–ї—П–µ—В –Є –і–µ—А–µ–њ—А–µ—Б—Б–Є—А–Њ–≤–∞–љ–љ—Л–µ —И—В–∞–Љ–Љ—Л––Љ—Г—В–∞–љ—В—Л [28].
–≠—Д—Д–µ–Ї—В –Є–љ–Њ–Ї—Г–ї—О–Љ–∞
–Ш–љ–Њ–Ї—Г–ї—О–Љ–—Н—Д—Д–µ–Ї—В –Ј–∞–Ї–ї—О—З–∞–µ—В—Б—П –≤ –Ј–љ–∞—З–Є—В–µ–ї—М–љ–Њ–Љ (–≤ 4 —А–∞–Ј–∞ –Є –≤—Л—И–µ) —Г–≤–µ–ї–Є—З–µ–љ–Є–Є –Ь–Я–Ъ –њ—А–Є –њ–Њ–≤—Л—И–µ–љ–Є–Є –њ–ї–Њ—В–љ–Њ—Б—В–Є –±–∞–Ї—В–µ—А–Є–∞–ї—М–љ–Њ–є –њ–Њ–њ—Г–ї—П—Ж–Є–Є –≤ 100 —А–∞–Ј. –≠—В–Њ –њ–Њ–Ї–∞–Ј–∞—В–µ–ї—М in vitro, –Ї–Њ—В–Њ—А—Л–є –Є—Б–њ–Њ–ї—М–Ј—Г–µ—В—Б—П –і–ї—П –њ—А–µ–і—Б–Ї–∞–Ј–∞–љ–Є—П —А–Є—Б–Ї–∞ –љ–µ—Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В–Є —В–µ—А–∞–њ–Є–Є –≤ —Б–ї—Г—З–∞—П—Е —В—П–ґ–µ–ї—Л—Е –Є–љ—Д–µ–Ї—Ж–Є–є —Б –≤—Л—Б–Њ–Ї–Њ–є –±–∞–Ї—В–µ—А–Є–∞–ї—М–љ–Њ–є –љ–∞–≥—А—Г–Ј–Ї–Њ–є [30]. –Я—А–Є –∞–±—Б—Ж–µ—Б—Б–∞—Е, –Љ–µ–љ–Є–љ–≥–Є—В–∞—Е, —Н–љ–і–Њ–Ї–∞—А–і–Є—В–∞—Е, –љ–Њ–Ј–Њ–Ї–Њ–Љ–Є–∞–ї—М–љ—Л—Е –њ–љ–µ–≤–Љ–Њ–љ–Є—П—Е –Ї–Њ–љ—Ж–µ–љ—В—А–∞—Ж–Є—П –≤–Њ–Ј–±—Г–і–Є—В–µ–ї—П –≤ –Њ—З–∞–≥–µ –Є–љ—Д–µ–Ї—Ж–Є–Є –Љ–Њ–ґ–µ—В –і–Њ—Б—В–Є–≥–∞—В—М 109 –Ъ–Ю–Х/–Љ–ї, —З—В–Њ –≤–µ–і–µ—В –Ї –љ–µ—Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В–Є —Ж–µ—Д–∞–ї–Њ—Б–њ–Њ—А–Є–љ–Њ–≤, –љ–µ—Б–Љ–Њ—В—А—П –љ–∞ —З—Г–≤—Б—В–≤–Є—В–µ–ї—М–љ–Њ—Б—В—М –Ї –љ–Є–Љ –Љ–Є–Ї—А–Њ–Њ—А–≥–∞–љ–Є–Ј–Љ–Њ–≤ in vitro [30–32]. –≠—Д—Д–µ–Ї—В—Г –Є–љ–Њ–Ї—Г–ї—О–Љ–∞ –Њ—Б–Њ–±–µ–љ–љ–Њ –њ–Њ–і–≤–µ—А–ґ–µ–љ—Л –∞–љ—В–Є—Б–Є–љ–µ–≥–љ–Њ–є–љ—Л–µ b––ї–∞–Ї—В–∞–Љ—Л – –њ–Є–њ–µ—А–∞—Ж–Є–ї–ї–Є–љ, –њ–Є–њ–µ—А–∞—Ж–Є–ї–ї–Є–љ/—В–∞–Ј–Њ–±–∞–Ї—В–∞–Љ, —Ж–µ—Д—В–∞–Ј–Є–і–Є–Љ –Є —Ж–µ—Д–µ–њ–Є–Љ [33, 34].
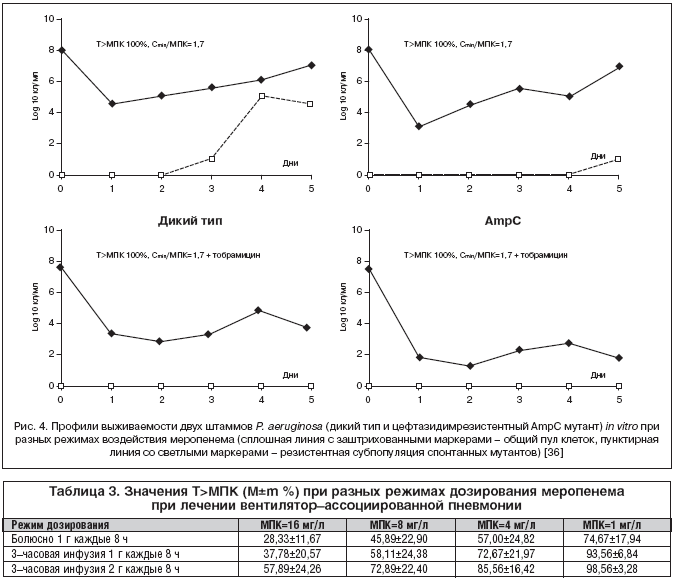
–Я—А–Є –Ї–Њ–ї–Є—З–µ—Б—В–≤–µ –Љ–Є–Ї—А–Њ–±–Њ–≤ –≤—Л—И–µ 107–108 –Ъ–Ю–Х/–Љ–ї —А–∞—Б—В–µ—В —З–∞—Б—В–Њ—В–∞ —Б–њ–Њ–љ—В–∞–љ–љ—Л—Е —Е—А–Њ–Љ–Њ—Б–Њ–Љ–љ—Л—Е –Љ—Г—В–∞—Ж–Є–є, –≤–µ–і—Г—Й–Є—Е –Ї –і–µ—А–µ–њ—А–µ—Б—Б–Є–Є –≥–µ–љ–∞ AmpC –Є –≥–Є–њ–µ—А–њ—А–Њ–і—Г–Ї—Ж–Є–Є –С–Ы, –≥–Є–і—А–Њ–ї–Є–Ј—Г—О—Й–Є—Е –њ–µ–љ–Є—Ж–Є–ї–ї–Є–љ—Л, —Ж–µ—Д–∞–ї–Њ—Б–њ–Њ—А–Є–љ—Л, –Є –љ–µ —З—Г–≤—Б—В–≤–Є—В–µ–ї—М–љ—Л—Е –Ї –і–µ–є—Б—В–≤–Є—О –Є–љ–≥–Є–±–Є—В–Њ—А–Њ–≤. –Ш—Е —Б–µ–ї–µ–Ї—Ж–Є—О –Љ–Њ–ґ–љ–Њ –њ–Њ–і–∞–≤–Є—В—М –њ—Г—В–µ–Љ –≤—Л–±–Њ—А–∞ –Њ–њ—В–Є–Љ–∞–ї—М–љ–Њ–≥–Њ —А–µ–ґ–Є–Љ–∞ –≤–Њ–Ј–і–µ–є—Б—В–≤–Є—П –Љ–µ—А–Њ–њ–µ–љ–µ–Љ–∞. –Ь–µ—В–Њ–і–Њ–Љ –Ї–Њ–Љ–њ—М—О—В–µ—А–љ–Њ–≥–Њ –Љ–Њ–і–µ–ї–Є—А–Њ–≤–∞–љ–Є—П —В—П–ґ–µ–ї–Њ–є –љ–Њ–Ј–Њ–Ї–Њ–Љ–Є–∞–ї—М–љ–Њ–є –њ–љ–µ–≤–Љ–Њ–љ–Є–Є –њ—А–Є –≤—Л—Б–Њ–Ї–Њ–є –і–Њ–Ј–µ –Є–љ–Њ–Ї—Г–ї—О–Љ–∞ (15 –Љ–ї 1—Е108 –Ъ–Ю–Х/–Љ–ї) in vitro –њ–Њ–Ї–∞–Ј–∞–љ–Њ, —З—В–Њ –њ—А–Є –Ї–Њ–љ—Ж–µ–љ—В—А–∞—Ж–Є–Є –∞–љ—В–Є–±–Є–Њ—В–Є–Ї–∞ –≤ –њ–ї–∞–Ј–Љ–µ (–°), —Б–Њ–Њ—В–≤–µ—В—Б—В–≤—Г—О—Й–µ–є –°min/–Ь–Я–Ъ=1,7 (–µ–µ –Љ–Њ–ґ–љ–Њ –і–Њ—Б—В–Є—З—М –њ—Г—В–µ–Љ 3–—З–∞—Б–Њ–≤–Њ–є –Є–љ—Д—Г–Ј–Є–Є 500 –Љ–≥ –Љ–µ—А–Њ–њ–µ–љ–µ–Љ–∞ [35]), –≤ —Б–Њ—З–µ—В–∞–љ–Є–Є —Б —В–Њ–±—А–∞–Љ–Є—Ж–Є–љ–Њ–Љ –њ–Њ–і–∞–≤–ї—П–µ—В—Б—П —А–Њ—Б—В P. aeruginosa –і–Є–Ї–Њ–≥–Њ —В–Є–њ–∞ –Є —Ж–µ—Д—В–∞–Ј–Є–і–Є–Љ—А–µ–Ј–Є—Б—В–µ–љ—В–љ–Њ–≥–Њ —И—В–∞–Љ–Љ–∞ –Є –њ–Њ–ї–љ–Њ—Б—В—М—О –Є–љ–≥–Є–±–Є—А—Г–µ—В—Б—П —Д–Њ—А–Љ–Є—А–Њ–≤–∞–љ–Є–µ AmpC –Љ—Г—В–∞–љ—В–Њ–≤ –љ–∞ –њ—А–Њ—В—П–ґ–µ–љ–Є–Є –≤—Б–µ–≥–Њ —Б—А–Њ–Ї–∞ –љ–∞–±–ї—О–і–µ–љ–Є—П (5 –і–љ–µ–є), –≤ —В–Њ –≤—А–µ–Љ—П –Ї–∞–Ї –≤ –Њ—В—Б—Г—В—Б—В–≤–Є–µ –∞–Љ–Є–љ–Њ–≥–ї–Є–Ї–Њ–Ј–Є–і–∞ –Ї –Ї–Њ–љ—Ж—Г 24 —З –≤–Њ–Ј–Њ–±–љ–Њ–≤–ї—П–µ—В—Б—П —А–Њ—Б—В –±–∞–Ї—В–µ—А–Є–∞–ї—М–љ—Л—Е –њ–Њ–њ—Г–ї—П—Ж–Є–є –Њ–±–Њ–Є—Е —И—В–∞–Љ–Љ–Њ–≤, –∞ –њ–Њ—Б–ї–µ –і–≤—Г—Е —Б—Г—В–Њ–Ї –њ—А–Њ–Є—Б—Е–Њ–і–Є—В —Б–µ–ї–µ–Ї—Ж–Є—П AmpC –Љ—Г—В–∞–љ—В–Њ–≤ –і–Є–Ї–Њ–≥–Њ —В–Є–њ–∞ –њ—А–Є —В–Њ–є –ґ–µ –Ї–Њ–љ—Ж–µ–љ—В—А–∞—Ж–Є–Є –Љ–µ—А–Њ–њ–µ–љ–µ–Љ–∞ [36] (—А–Є—Б. 4). –С–ї–∞–≥–Њ–і–∞—А—П —Н—В–Њ–є —Б—В—А–∞—В–µ–≥–Є–Є (–Ї–Њ–Љ–±–Є–љ–∞—Ж–Є—П –Љ–µ—А–Њ–њ–µ–љ–µ–Љ–∞ —Б –∞–Љ–Є–љ–Њ–≥–ї–Є–Ї–Њ–Ј–Є–і–∞–Љ–Є) –Љ–Њ–ґ–љ–Њ –њ–Њ–і–∞–≤–Є—В—М –Њ–±—А–∞–Ј–Њ–≤–∞–љ–Є–µ —Б–њ–Њ–љ—В–∞–љ–љ—Л—Е –Љ—Г—В–∞–љ—В–Њ–≤ P. aeruginosa —Г –Є–Љ–Љ—Г–љ–Њ–Ї–Њ–Љ–њ–µ—В–µ–љ—В–љ—Л—Е –њ–∞—Ж–Є–µ–љ—В–Њ–≤ –њ—А–Є —Г—Б–ї–Њ–≤–Є–Є, —З—В–Њ –Ґ>–Ь–Я–Ъ = 100%, —В–Њ –µ—Б—В—М —А–µ—З—М –Є–і–µ—В –Њ –њ–Њ—Б—В–Њ—П–љ–љ–Њ–є –Є–љ—Д—Г–Ј–Є–Є –∞–љ—В–Є–±–Є–Њ—В–Є–Ї–∞.
–Ю–њ—В–Є–Љ–Є–Ј–∞—Ж–Є—П —А–µ–ґ–Є–Љ–Њ–≤
–і–Њ–Ј–Є—А–Њ–≤–∞–љ–Є—П –Љ–µ—А–Њ–њ–µ–љ–µ–Љ–∞
–Ъ–∞—А–±–∞–њ–µ–љ–µ–Љ—Л –Њ—В–љ–Њ—Б—П—В—Б—П –Ї –Ј–∞–≤–Є—Б–Є–Љ—Л–Љ –Њ—В –≤—А–µ–Љ–µ–љ–Є –∞–љ—В–Є–±–Є–Њ—В–Є–Ї–∞–Љ. –°—В–∞–±–Є–ї—М–љ—Л–є –±–∞–Ї—В–µ—А–Є—Ж–Є–і–љ—Л–є –Є –∞–і–µ–Ї–≤–∞—В–љ—Л–є –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є–є —Н—Д—Д–µ–Ї—В –њ—А–Є –Є—Е –њ—А–Є–Љ–µ–љ–µ–љ–Є–Є –Љ–Њ–ґ–µ—В –±—Л—В—М –і–Њ—Б—В–Є–≥–љ—Г—В, –µ—Б–ї–Є –Ї–Њ–љ—Ж–µ–љ—В—А–∞—Ж–Є–Є –њ—А–µ–њ–∞—А–∞—В–∞ –≤ –Ї—А–Њ–≤–Є –≤ 2–4 —А–∞–Ј–∞ –њ—А–µ–≤—Л—И–∞—О—В –Ј–љ–∞—З–µ–љ–Є—П –Ь–Я–Ъ –≤ —В–µ—З–µ–љ–Є–µ 40–50% –Є–љ—В–µ—А–≤–∞–ї–∞ –≤—А–µ–Љ–µ–љ–Є –Љ–µ–ґ–і—Г –і–Њ–Ј–∞–Љ–Є (%–Ґ>–Ь–Я–Ъ –±–Њ–ї–µ–µ 40% –Ї–Њ—А—А–µ–ї–Є—А—Г–µ—В —Б –±–∞–Ї—В–µ—А–Є–∞–ї—М–љ—Л–Љ –Ї–Є–ї–ї–Є–љ–≥–Њ–Љ) [37]. –Ф–ї—П –Љ–µ—А–Њ–њ–µ–љ–µ–Љ–∞ —Н—В–Њ—В –њ–µ—А–Є–Њ–і –і–ї–Є—В—Б—П 4 —З. –≠—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В—М –∞–љ—В–Є–±–Є–Њ—В–Є–Ї–∞ –Љ–Њ–ґ–љ–Њ –њ–Њ–≤—Л—Б–Є—В—М –њ—Г—В–µ–Љ —Г–≤–µ–ї–Є—З–µ–љ–Є—П –і–Њ–Ј—Л, –Ї—А–∞—В–љ–Њ—Б—В–Є –њ—А–Є–Љ–µ–љ–µ–љ–Є—П (3–4 —А–∞–Ј–∞ –≤ —Б—Г—В–Ї–Є) –Є/–Є–ї–Є –њ—А–Њ–і–Њ–ї–ґ–Є—В–µ–ї—М–љ–Њ—Б—В–Є –Є–љ—Д—Г–Ј–Є–Є [38].
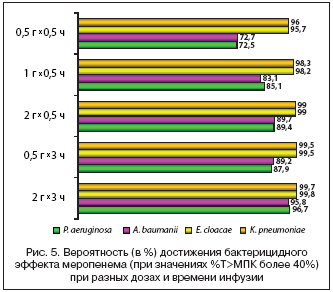
–Э–∞ –њ—А–Є–Љ–µ—А–µ –Љ–µ—А–Њ–њ–µ–љ–µ–Љ–∞ –і–Њ—Б—В–∞—В–Њ—З–љ–Њ —Е–Њ—А–Њ—И–Њ –Є–Ј—Г—З–µ–љ–Њ –њ—А–Є–Љ–µ–љ–µ–љ–Є–µ b––ї–∞–Ї—В–∞–Љ–Њ–≤ –≤ —А–µ–ґ–Є–Љ–µ –њ—А–Њ–і–ї–µ–љ–љ–Њ–є –Є–љ—Д—Г–Ј–Є–Є, –Ї–Њ–≥–і–∞ —А–∞–Ј–Њ–≤–∞—П –і–Њ–Ј–∞ –њ—А–µ–њ–∞—А–∞—В–∞ –≤–≤–Њ–і–Є—В—Б—П –≤ —В–µ—З–µ–љ–Є–µ 3–—Е —З–∞—Б–Њ–≤. –≠—В–Њ–Љ—Г –≤–Њ –Љ–љ–Њ–≥–Њ–Љ —Б–њ–Њ—Б–Њ–±—Б—В–≤–Њ–≤–∞–ї–Њ –њ—А–Є–Љ–µ–љ–µ–љ–Є–µ –Љ–µ—В–Њ–і–∞ —Б–Є–Љ—Г–ї—П—Ж–Є–Є Monte Carlo, —А–∞–Ј—А–∞–±–Њ—В–∞–љ–љ–Њ–≥–Њ –љ–∞ –Њ—Б–љ–Њ–≤–µ –Ї–Њ–Љ–њ—М—О—В–µ—А–љ–Њ–≥–Њ –Љ–Њ–і–µ–ї–Є—А–Њ–≤–∞–љ–Є—П, –њ–Њ–Ј–≤–Њ–ї—П—О—Й–µ–≥–Њ –∞–љ–∞–ї–Є–Ј–Є—А–Њ–≤–∞—В—М –≤–µ—А–Њ—П—В–љ–Њ—Б—В—М –і–Њ—Б—В–Є–ґ–µ–љ–Є—П –Њ–њ—А–µ–і–µ–ї–µ–љ–љ—Л—Е —Д–∞—А–Љ–∞–Ї–Њ–і–Є–љ–∞–Љ–Є—З–µ—Б–Ї–Є—Е —Ж–µ–ї–µ–є —Б —Г—З–µ—В–Њ–Љ –≤—Л—И–µ–њ–µ—А–µ—З–Є—Б–ї–µ–љ–љ—Л—Е —Д–∞–Ї—В–Њ—А–Њ–≤ [39]. –Ш—Б—Е–Њ–і—П –Є–Ј –њ–∞—А–∞–Љ–µ—В—А–∞ 40%–Ґ>–Ь–Я–Ъ –Љ–µ—В–Њ–і–Њ–Љ Monte Carlo –±—Л–ї–Њ –њ–Њ–Ї–∞–Ј–∞–љ–Њ, —З—В–Њ –њ—А–Є –Є–љ—Д—Г–Ј–Є–Є 500 –Љ–≥ –Љ–µ—А–Њ–њ–µ–љ–µ–Љ–∞ –≤ —В–µ—З–µ–љ–Є–µ 30 –Љ–Є–љ –Ї–∞–ґ–і—Л–µ 8 —З –і–Њ—Б—В–Є–≥–∞–µ—В—Б—П –≤—Л—А–∞–ґ–µ–љ–љ—Л–є –±–∞–Ї—В–µ—А–Є—Ж–Є–і–љ—Л–є —Н—Д—Д–µ–Ї—В –≤ –Њ—В–љ–Њ—И–µ–љ–Є–Є E. coli –Є K. pneumoniae, –љ–Њ –љ–µ–і–Њ—Б—В–∞—В–Њ—З–љ—Л–є –і–ї—П Acinetobacter baumanii –Є P. aeruginosa. –£–і–ї–Є–љ–µ–љ–Є–µ —Б—А–Њ–Ї–Њ–≤ –Є–љ—Д—Г–Ј–Є–Є –∞–љ—В–Є–±–Є–Њ—В–Є–Ї–∞ –≤ —В–Њ–є –ґ–µ –і–Њ–Ј–µ –і–Њ 3 —З —Б–Њ–њ—А–Њ–≤–Њ–ґ–і–∞–µ—В—Б—П –Ј–∞–Љ–µ—В–љ—Л–Љ –њ–Њ–≤—Л—И–µ–љ–Є–µ–Љ –µ–≥–Њ —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В–Є, —Б–Њ–њ–Њ—Б—В–∞–≤–Є–Љ–Њ–є —Б –∞–Ї—В–Є–≤–љ–Њ—Б—В—М—О –Љ–µ—А–Њ–њ–µ–љ–µ–Љ–∞ –њ—А–Є –±–Њ–ї—О—Б–љ–Њ–Љ –≤–≤–µ–і–µ–љ–Є–Є –≤ –і–Њ–Ј–µ 2 –≥ [40] (—А–Є—Б. 5). –Ґ–∞–Ї–ґ–µ –±—Л–ї–Њ –њ–Њ–Ї–∞–Ј–∞–љ–Њ, —З—В–Њ –њ—А–Є –Ј–∞–і–∞–љ–љ—Л—Е –Ј–љ–∞—З–µ–љ–Є—П—Е –Ь–Я–Ъ 16 –Љ–Ї–≥/–Љ–ї 3–—З–∞—Б–Њ–≤–∞—П –Є–љ—Д—Г–Ј–Є—П 2 –≥ –Љ–µ—А–Њ–њ–µ–љ–µ–Љ–∞ –њ–Њ–Ј–≤–Њ–ї—П–µ—В –і–Њ—Б—В–Є—З—М –њ–Њ–Ї–∞–Ј–∞—В–µ–ї—П 48%–Ґ>–Ь–Я–Ъ, –∞ —Н—В–Њ —Б–≤–Є–і–µ—В–µ–ї—М—Б—В–≤—Г–µ—В –Њ –≤–Њ–Ј–Љ–Њ–ґ–љ–Њ—Б—В–Є —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ–≥–Њ –≤–Њ–Ј–і–µ–є—Б—В–≤–Є—П –љ–∞ —И—В–∞–Љ–Љ—Л, —Б—З–Є—В–∞—О—Й–Є–µ—Б—П —А–µ–Ј–Є—Б—В–µ–љ—В–љ—Л–Љ–Є –Ї –Љ–µ—А–Њ–њ–µ–љ–µ–Љ—Г –љ–∞ –Њ—Б–љ–Њ–≤–∞–љ–Є–Є –і–∞–љ–љ—Л—Е –Ь–Я–Ъ [41]. –Я–Њ–ї—Г—З–µ–љ–љ—Л–µ —А–µ–Ј—Г–ї—М—В–∞—В—Л –±—Л–ї–Є –њ–Њ–і—В–≤–µ—А–ґ–і–µ–љ—Л –≤ –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Њ–Љ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є —Г –±–Њ–ї—М–љ—Л—Е —Б –≤–µ–љ—В–Є–ї—П—В–Њ—А––∞—Б—Б–Њ—Ж–Є–Є—А–Њ–≤–∞–љ–љ–Њ–є –њ–љ–µ–≤–Љ–Њ–љ–Є–µ–є (–Т–Р–Я), –≥–і–µ –њ—А–Є 3–—З–∞—Б–Њ–≤–Њ–є –Є–љ—Д—Г–Ј–Є–Є 2 –≥ –Љ–µ—А–Њ–њ–µ–љ–µ–Љ–∞ –Ї–∞–ґ–і—Л–µ 8 —З —Б–Њ–Ј–і–∞–≤–∞–ї–Є—Б—М –Ї–Њ–љ—Ж–µ–љ—В—А–∞—Ж–Є–Є –≤ –њ–ї–∞–Ј–Љ–µ, –њ—А–µ–≤—Л—И–∞—О—Й–Є–µ –Ь–Я–Ъ 16 –Љ–Ї–≥/–Љ–ї –≤ —В–µ—З–µ–љ–Є–µ –њ–Њ—З—В–Є 60% 8–—З–∞—Б–Њ–≤–Њ–≥–Њ –Є–љ—В–µ—А–≤–∞–ї–∞ [42] (—В–∞–±–ї. 3). –Т –і—А—Г–≥–Њ–Љ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є –њ—А–Є –ї–µ—З–µ–љ–Є–Є –Т–Р–Я –Љ–µ—А–Њ–њ–µ–љ–µ–Љ–Њ–Љ –≤ —В–µ—З–µ–љ–Є–µ 14 –і–љ–µ–є (1 –≥ –Ї–∞–ґ–і—Л–µ 6 —З) –Ї–ї–Є–љ–Є—З–µ—Б–Ї–∞—П —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В—М –≤ —А–µ–ґ–Є–Љ–µ –њ—А–Њ–і–ї–µ–љ–љ–Њ–є –Є–љ—Д—Г–Ј–Є–Є (15 –±–Њ–ї—М–љ—Л—Е) –±—Л–ї–∞ –≤—Л—И–µ –≤ —Б—А–∞–≤–љ–µ–љ–Є–Є —Б –±–Њ–ї—О—Б–љ—Л–Љ –≤–≤–µ–і–µ–љ–Є–µ–Љ (18 –±–Њ–ї—М–љ—Л—Е) –њ—А–µ–њ–∞—А–∞—В–∞ (93,3% –њ—А–Њ—В–Є–≤ 63,3%; —А=0,038), –∞ –∞—В—А–Є–±—Г—В–Є–≤–љ–∞—П –ї–µ—В–∞–ї—М–љ–Њ—Б—В—М –±—Л–ї–∞ –љ–Є–ґ–µ (—Б–Њ–Њ—В–≤–µ—В—Б—В–≤–µ–љ–љ–Њ, 6,7% –Є 23,3%; —А=0,236) [43]. –†–µ–ґ–Є–Љ –і–Њ–Ј–Є—А–Њ–≤–∞–љ–Є—П –Љ–µ—А–Њ–њ–µ–љ–µ–Љ–∞ –≤ –≤–Є–і–µ –њ—А–Њ–і–ї–µ–љ–љ—Л—Е –Є–љ—Д—Г–Ј–Є–є, –љ–∞—А—П–і—Г —Б —Д–∞—А–Љ–∞–Ї–Њ–і–Є–љ–∞–Љ–Є—З–µ—Б–Ї–Є–Љ–Є –њ—А–µ–Є–Љ—Г—Й–µ—Б—В–≤–∞–Љ–Є (–і–Њ—Б—В–Є–ґ–µ–љ–Є–µ –±–Њ–ї–µ–µ –≤—Л—Б–Њ–Ї–Є—Е –Ї–Њ–љ—Ж–µ–љ—В—А–∞—Ж–Є–є –њ—А–µ–њ–∞—А–∞—В–∞ –≤ –Њ—З–∞–≥–µ –≤–Њ—Б–њ–∞–ї–µ–љ–Є—П, –њ—А–µ–Њ–і–Њ–ї–µ–љ–Є–µ —А–µ–Ј–Є—Б—В–µ–љ—В–љ–Њ—Б—В–Є –≤–Њ–Ј–±—Г–і–Є—В–µ–ї–µ–є) –Є–Љ–µ–µ—В —Д–∞—А–Љ–∞–Ї–Њ—Н–Ї–Њ–љ–Њ–Љ–Є—З–µ—Б–Ї–Є–µ –њ—А–µ–Є–Љ—Г—Й–µ—Б—В–≤–∞, –Њ–±–µ—Б–њ–µ—З–Є–≤–∞—О—Й–Є–µ —Б–љ–Є–ґ–µ–љ–Є–µ –Ї—Г—А—Б–Њ–≤–Њ–є —Б—В–Њ–Є–Љ–Њ—Б—В–Є –ї–µ—З–µ–љ–Є—П [44,45].
–Ъ–∞—А–±–∞–њ–µ–љ–µ–Љ—Л –Ї–∞–Ї –њ—А–µ–њ–∞—А–∞—В—Л –≤—Л–±–Њ—А–∞ –њ—А–Є —Н–Љ–њ–Є—А–Є—З–µ—Б–Ї–Њ–є —В–µ—А–∞–њ–Є–Є —В—П–ґ–µ–ї—Л—Е –Є–љ—Д–µ–Ї—Ж–Є–є
–І–∞—Б—В–Њ–є –Њ—И–Є–±–Ї–Њ–є –≤ –ї–µ—З–µ–љ–Є–Є –≤–љ–Њ–≤—М –≤–Њ–Ј–љ–Є–Ї–∞—О—Й–Є—Е –Є–љ—Д–µ–Ї—Ж–Є–є —Г –≥–Њ—Б–њ–Є—В–∞–ї–Є–Ј–Є—А–Њ–≤–∞–љ–љ—Л—Е –±–Њ–ї—М–љ—Л—Е —П–≤–ї—П–µ—В—Б—П –љ–µ–і–Њ–Њ—Ж–µ–љ–Ї–∞ –≤—Л—Б–Њ–Ї–Њ–є –≤–µ—А–Њ—П—В–љ–Њ—Б—В–Є –љ–∞–ї–Є—З–Є—П —А–µ–Ј–Є—Б—В–µ–љ—В–љ—Л—Е –≤–Њ–Ј–±—Г–і–Є—В–µ–ї–µ–є –Є –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є–µ –љ–∞ –љ–∞—З–∞–ї—М–љ–Њ–Љ —Н—В–∞–њ–µ —Н–Љ–њ–Є—А–Є—З–µ—Б–Ї–Њ–є —В–µ—А–∞–њ–Є–Є «–њ—А–Њ—Б—В—Л—Е» –∞–љ—В–Є–±–Є–Њ—В–Є–Ї–Њ–≤, —А–µ–Ј–µ—А–≤–Є—А—Г—П –Љ–Њ—Й–љ—Л–µ –њ—А–µ–њ–∞—А–∞—В—Л —И–Є—А–Њ–Ї–Њ–≥–Њ —Б–њ–µ–Ї—В—А–∞ –і–ї—П –њ–∞—Ж–Є–µ–љ—В–Њ–≤, —Б–Њ—Б—В–Њ—П–љ–Є–µ –Ї–Њ—В–Њ—А—Л—Е –њ—А–Њ–≥—А–µ—Б—Б–Є–≤–љ–Њ —Г—Е—Г–і—И–∞–µ—В—Б—П –Є/–Є–ї–Є —Г –Ї–Њ—В–Њ—А—Л—Е —Г–ґ–µ –≤—Л—Б–µ—П–љ—Л —А–µ–Ј–Є—Б—В–µ–љ—В–љ—Л–µ –Љ–Є–Ї—А–Њ–Њ—А–≥–∞–љ–Є–Ј–Љ—Л. –Ґ–∞–Ї–Њ–є –њ–Њ–і—Е–Њ–і –Љ–Њ–ґ–µ—В –±—Л—В—М –њ—А–Є–µ–Љ–ї–µ–Љ –њ—А–Є –љ–µ—В—П–ґ–µ–ї—Л—Е –Є —Б—А–µ–і–љ–µ–є —В—П–ґ–µ—Б—В–Є –≤–љ–µ–±–Њ–ї—М–љ–Є—З–љ—Л—Е –Є–љ—Д–µ–Ї—Ж–Є—П—Е, –љ–Њ, –Ї–∞–Ї —Б–≤–Є–і–µ—В–µ–ї—М—Б—В–≤—Г—О—В –Љ–љ–Њ–≥–Њ—З–Є—Б–ї–µ–љ–љ—Л–µ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П, –њ—А–Є –љ–Њ–Ј–Њ–Ї–Њ–Љ–Є–∞–ї—М–љ—Л—Е –Є–љ—Д–µ–Ї—Ж–Є—П—Е –Ї—А–Њ–≤–Њ—В–Њ–Ї–∞ –Є –Т–Р–Я –љ–µ–∞–і–µ–Ї–≤–∞—В–љ–∞—П —Б—В–∞—А—В–Њ–≤–∞—П –∞–љ—В–Є–Љ–Є–Ї—А–Њ–±–љ–∞—П —В–µ—А–∞–њ–Є—П —Б–Њ–њ—А–Њ–≤–Њ–ґ–і–∞–µ—В—Б—П –і–Њ—Б—В–Њ–≤–µ—А–љ—Л–Љ —Г–≤–µ–ї–Є—З–µ–љ–Є–µ–Љ –ї–µ—В–∞–ї—М–љ–Њ—Б—В–Є, –∞ –њ–Њ—Б–ї–µ–і—Г—О—Й–∞—П –µ–µ –Ї–Њ—А—А–µ–Ї—Ж–Є—П (–њ–Њ—Б–ї–µ –њ–Њ–ї—Г—З–µ–љ–Є—П —А–µ–Ј—Г–ї—М—В–∞—В–Њ–≤ –Љ–Є–Ї—А–Њ–±–Є–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Њ–≥–Њ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П) –љ–µ —Г–ї—Г—З—И–∞–µ—В –Є—Б—Е–Њ–і–Њ–≤ –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П [46–48] (—А–Є—Б. 6). Kollef M.H. –Є —Б–Њ–∞–≤—В. [49] –њ–Њ–Ї–∞–Ј–∞–ї–Є, —З—В–Њ –њ—А–Є –љ–Њ–Ј–Њ–Ї–Њ–Љ–Є–∞–ї—М–љ—Л—Е –Є–љ—Д–µ–Ї—Ж–Є—П—Е —В–µ—А–∞–њ–Є—П –Њ–Ї–∞–Ј—Л–≤–∞–µ—В—Б—П –љ–µ–∞–і–µ–Ї–≤–∞—В–љ–Њ–є –≤ 2 —А–∞–Ј–∞ —З–∞—Й–µ, —З–µ–Љ –њ—А–Є –≤–љ–µ–±–Њ–ї—М–љ–Є—З–љ—Л—Е –Є–љ—Д–µ–Ї—Ж–Є—П—Е (34% –њ—А–Њ—В–Є–≤ 17%), –∞ –њ—А–µ–і—И–µ—Б—В–≤—Г—О—Й–µ–µ –њ—А–Є–Љ–µ–љ–µ–љ–Є–µ –∞–љ—В–Є–±–Є–Њ—В–Є–Ї–Њ–≤, —П–≤–ї—П—П—Б—М —Д–∞–Ї—В–Њ—А–Њ–Љ —А–Є—Б–Ї–∞ –≤—Л—Б–Њ–Ї–Њ–є —А–µ–Ј–Є—Б—В–µ–љ—В–љ–Њ—Б—В–Є –≤–Њ–Ј–±—Г–і–Є—В–µ–ї—П, –µ—Й–µ –≤ 1,5 —А–∞–Ј–∞ –њ–Њ–≤—Л—И–∞–µ—В –≤–µ—А–Њ—П—В–љ–Њ—Б—В—М –њ—А–Њ–≤–µ–і–µ–љ–Є—П –љ–µ–∞–і–µ–Ї–≤–∞—В–љ–Њ–є —В–µ—А–∞–њ–Є–Є (45%).
–Э–∞–Ї–Њ–њ–ї–µ–љ–Њ –Љ–љ–Њ–≥–Њ –і–∞–љ–љ—Л—Е –Њ —В–Њ–Љ, —З—В–Њ —А–∞–љ–љ–µ–µ –њ—А–Є–Љ–µ–љ–µ–љ–Є–µ –Ї–∞—А–±–∞–њ–µ–љ–µ–Љ–Њ–≤ –≤ —А–µ–ґ–Є–Љ–µ –і–µ—Н—Б–Ї–∞–ї–∞—Ж–Є–Њ–љ–љ–Њ–є —Н–Љ–њ–Є—А–Є—З–µ—Б–Ї–Њ–є —В–µ—А–∞–њ–Є–Є —Б—Г—Й–µ—Б—В–≤–µ–љ–љ–Њ –њ–Њ–≤—Л—И–∞–µ—В —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В—М –ї–µ—З–µ–љ–Є—П. –°–Њ–≥–ї–∞—Б–љ–Њ —А–µ–Ј—Г–ї—М—В–∞—В–∞–Љ —А–Њ—Б—Б–Є–є—Б–Ї–Њ–≥–Њ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П –Р–°–≠–Ґ [50] –Љ–Њ–љ–Њ—В–µ—А–∞–њ–Є—П —В—П–ґ–µ–ї—Л—Е –љ–Њ–Ј–Њ–Ї–Њ–Љ–Є–∞–ї—М–љ—Л—Е –Є–љ—Д–µ–Ї—Ж–Є–є (–њ–љ–µ–≤–Љ–Њ–љ–Є–Є, —А–∞—Б–њ—А–Њ—Б—В—А–∞–љ–µ–љ–љ–Њ–≥–Њ –њ–µ—А–Є—В–Њ–љ–Є—В–∞, –Є–љ—Д–Є—Ж–Є—А–Њ–≤–∞–љ–љ–Њ–≥–Њ –њ–∞–љ–Ї—А–µ–Њ–љ–µ–Ї—А–Њ–Ј–∞) –Љ–µ—А–Њ–њ–µ–љ–µ–Љ–Њ–Љ –њ–Њ –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Њ–є –Є –±–∞–Ї—В–µ—А–Є–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Њ–є —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В–Є –њ—А–µ–≤–Њ—Б—Е–Њ–і–Є—В —Б—В–∞–љ–і–∞—А—В–љ—Г—О —В–µ—А–∞–њ–Є—О b––ї–∞–Ї—В–∞–Љ–∞–Љ–Є –Є —Д—В–Њ—А—Е–Є–љ–Њ–ї–Њ–љ–∞–Љ–Є –≤ –Ї–Њ–Љ–±–Є–љ–∞—Ж–Є–Є —Б –∞–Љ–Є–љ–Њ–≥–ї–Є–Ї–Њ–Ј–Є–і–∞–Љ–Є –Є/–Є–ї–Є –Љ–µ—В—А–Њ–љ–Є–і–∞–Ј–Њ–ї–Њ–Љ –Є/–Є–ї–Є –≤–∞–љ–Ї–Њ–Љ–Є—Ж–Є–љ–Њ–Љ.
–Ю—В–µ—З–µ—Б—В–≤–µ–љ–љ—Л–Љ–Є –∞–≤—В–Њ—А–∞–Љ–Є [51] –њ—А–Њ–≤–µ–і–µ–љ —Б—А–∞–≤–љ–Є—В–µ–ї—М–љ—Л–є –∞–љ–∞–ї–Є–Ј —А–∞–Ј–ї–Є—З–љ—Л—Е —Б—Е–µ–Љ –∞–љ—В–Є–±–∞–Ї—В–µ—А–Є–∞–ї—М–љ–Њ–є —В–µ—А–∞–њ–Є–Є –њ—А–Є –љ–Њ–Ј–Њ–Ї–Њ–Љ–Є–∞–ї—М–љ—Л—Е –њ–µ—А–Є—В–Њ–љ–Є—В–∞—Е –Є –∞–±–і–Њ–Љ–Є–љ–∞–ї—М–љ–Њ–Љ —Б–µ–њ—Б–Є—Б–µ. –Э–∞–Є–±–Њ–ї–µ–µ –≤—Л—Б–Њ–Ї–∞—П —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В—М –±—Л–ї–∞ –і–Њ—Б—В–Є–≥–љ—Г—В–∞ –њ—А–Є –Љ–Њ–љ–Њ—В–µ—А–∞–њ–Є–Є –Ї–∞—А–±–∞–њ–µ–љ–µ–Љ–Њ–Љ, –≤ –і–≤–∞ —А–∞–Ј–∞ –љ–Є–ґ–µ –±—Л–ї–∞ —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В—М –њ—А–Є –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є–Є –Ї–Њ–Љ–±–Є–љ–∞—Ж–Є–Є —Ж–µ—Д–µ–њ–Є–Љ–∞ –Є –Љ–µ—В—А–Њ–љ–Є–і–∞–Ј–Њ–ї–∞ –Є —Б–∞–Љ–∞—П –љ–Є–Ј–Ї–∞—П –Њ—В–Љ–µ—З–∞–ї–∞—Б—М –њ—А–Є –Љ–Њ–љ–Њ—В–µ—А–∞–њ–Є–Є –Ј–∞—Й–Є—Й–µ–љ–љ—Л–Љ –њ–µ–љ–Є—Ж–Є–ї–ї–Є–љ–Њ–Љ. –Э–∞–Ј–љ–∞—З–µ–љ–Є–µ –Ї–∞—А–±–∞–њ–µ–љ–µ–Љ–Њ–≤ –њ—А–Є —А–∞—Б–њ—А–Њ—Б—В—А–∞–љ–µ–љ–љ–Њ–Љ –њ–µ—А–Є—В–Њ–љ–Є—В–µ –Є –Є–љ—Д–Є—Ж–Є—А–Њ–≤–∞–љ–љ–Њ–Љ –њ–∞–љ–Ї—А–µ–Њ–љ–µ–Ї—А–Њ–Ј–µ, —В—А–µ–±—Г—О—Й–µ–Љ –Њ–±—П–Ј–∞—В–µ–ї—М–љ–Њ–≥–Њ –Њ–њ–µ—А–∞—В–Є–≤–љ–Њ–≥–Њ –ї–µ—З–µ–љ–Є—П, —П–≤–ї—П–µ—В—Б—П –љ–∞–Є–±–Њ–ї–µ–µ —Н—Д—Д–µ–Ї—В–Є–≤–љ—Л–Љ —А–µ–ґ–Є–Љ–Њ–Љ –∞–љ—В–Є–±–Є–Њ—В–Є–Ї–Њ—В–µ—А–∞–њ–Є–Є, –∞ —Б—А–µ–і–љ—П—П –њ—А–Њ–і–Њ–ї–ґ–Є—В–µ–ї—М–љ–Њ—Б—В—М –Љ–Њ–љ–Њ—В–µ—А–∞–њ–Є–Є –Љ–Њ–ґ–µ—В –і–Њ—Б—В–Є–≥–∞—В—М 3 –љ–µ–і [52]. –Я–Њ–Ї–∞–Ј–∞–љ–Њ –і–Њ—Б—В–Њ–≤–µ—А–љ–Њ–µ —Б–љ–Є–ґ–µ–љ–Є–µ –ї–µ—В–∞–ї—М–љ–Њ—Б—В–Є –≤ 3 —А–∞–Ј–∞ –њ—А–Є –њ–∞–љ–Ї—А–µ–∞—В–Њ–≥–µ–љ–љ–Њ–Љ —Б–µ–њ—Б–Є—Б–µ, –ї–µ—З–µ–љ–љ–Њ–Љ –Ї–∞—А–±–∞–њ–µ–љ–µ–Љ–∞–Љ–Є –≤ —Б—А–∞–≤–љ–µ–љ–Є–Є —Б –і—А—Г–≥–Є–Љ–Є –∞–љ—В–Є–Љ–Є–Ї—А–Њ–±–љ—Л–Љ–Є –њ—А–µ–њ–∞—А–∞—В–∞–Љ–Є [49]. –°—З–Є—В–∞–µ—В—Б—П, —З—В–Њ —В—П–ґ–µ—Б—В—М —Б–Њ—Б—В–Њ—П–љ–Є—П –±–Њ–ї—М–љ–Њ–≥–Њ –њ–Њ —И–Ї–∞–ї–µ –Р–†–Р–°–Э–Х II —Б–≤—Л—И–µ 13 –±–∞–ї–ї–Њ–≤ –Є –њ–Њ —И–Ї–∞–ї–µ Ranson –±–Њ–ї–µ–µ 4 –±–∞–ї–ї–Њ–≤ —П–≤–ї—П–µ—В—Б—П –∞–±—Б–Њ–ї—О—В–љ—Л–Љ –њ–Њ–Ї–∞–Ј–∞–љ–Є–µ–Љ –Ї –љ–∞–Ј–љ–∞—З–µ–љ–Є—О –Ї–∞—А–±–∞–њ–µ–љ–µ–Љ–Њ–≤ –њ—А–Є –њ–∞–љ–Ї—А–µ–Њ–љ–µ–Ї—А–Њ–Ј–µ –љ–µ–Ј–∞–≤–Є—Б–Є–Љ–Њ –Њ—В –љ–∞–ї–Є—З–Є—П —А–µ–Ј—Г–ї—М—В–∞—В–Њ–≤ –Љ–Є–Ї—А–Њ–±–Є–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Њ–≥–Њ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П, –њ–Њ–і—В–≤–µ—А–ґ–і–∞—О—Й–Є—Е —Д–∞–Ї—В –Є–љ—Д–Є—Ж–Є—А–Њ–≤–∞–љ–Є—П –њ–Њ–і–ґ–µ–ї—Г–і–Њ—З–љ–Њ–є –ґ–µ–ї–µ–Ј—Л –Є –Ј–∞–±—А—О—И–Є–љ–љ–Њ–є –Ї–ї–µ—В—З–∞—В–Ї–Є [53]. –Т –њ—А–Њ—Б–њ–µ–Ї—В–Є–≤–љ–Њ–Љ —А–∞–љ–і–Њ–Љ–Є–Ј–Є—А–Њ–≤–∞–љ–љ–Њ–Љ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є [54] —Б—А–∞–≤–љ–Є–≤–∞–ї–Є —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В—М –Љ–µ—А–Њ–њ–µ–љ–µ–Љ–∞ —Б –Є–Љ–Є–њ–µ–љ–µ–Љ–Њ–Љ –≤ –њ—А–Њ—Д–Є–ї–∞–Ї—В–Є–Ї–µ —Б–µ–њ—В–Є—З–µ—Б–Ї–Є—Е –Њ—Б–ї–Њ–ґ–љ–µ–љ–Є–Є –њ—А–Є —В—П–ґ–µ–ї–Њ–є —Д–Њ—А–Љ–µ –њ–∞–љ–Ї—А–µ–Њ–љ–µ–Ї—А–Њ–Ј–∞ (–≤ –Ї–∞–ґ–і–Њ–є –≥—А—Г–њ–њ–µ –њ–Њ 88 –њ–∞—Ж–Є–µ–љ—В–Њ–≤). –І–∞—Б—В–Њ—В–∞ –≤–Њ–Ј–љ–Є–Ї–љ–Њ–≤–µ–љ–Є—П –њ–∞–љ–Ї—А–µ–∞—В–Њ–≥–µ–љ–љ—Л—Е –Є –≤–љ–µ–њ–∞–љ–Ї—А–µ–∞—В–Є—З–µ—Б–Ї–Є—Е –Є–љ—Д–µ–Ї—Ж–Є–є –±—Л–ї–∞ –њ—А–∞–Ї—В–Є—З–µ—Б–Ї–Є –Њ–і–Є–љ–∞–Ї–Њ–≤–Њ–є (11,4% –њ—А–Њ—В–Є–≤ 13,6% –Є 21,6% –њ—А–Њ—В–Є–≤ 23,9% —Б–Њ–Њ—В–≤–µ—В—Б—В–≤–µ–љ–љ–Њ), –љ–µ –±—Л–ї–Њ –Њ—В–ї–Є—З–Є–є –њ–Њ —Б—А–Њ–Ї–∞–Љ –≥–Њ—Б–њ–Є—В–∞–ї–Є–Ј–∞—Ж–Є–Є –Є –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є–Љ –Є—Б—Е–Њ–і–∞–Љ.
–Я—А–Є —Б—А–∞–≤–љ–µ–љ–Є–Є –Љ–µ—А–Њ–њ–µ–љ–µ–Љ–∞ –Є –Є–Љ–Є–њ–µ–љ–µ–Љ–∞ –њ–Њ —А–µ–Ј—Г–ї—М—В–∞—В–∞–Љ –Љ–µ—В–∞––∞–љ–∞–ї–Є–Ј–∞ 27 —А–∞–Ј–љ—Л—Е –Є—Б—В–Њ—З–љ–Є–Ї–Њ–≤ –љ–µ –≤—Л—П–≤–ї–µ–љ—Л —А–∞–Ј–ї–Є—З–Є—П –≤ —Б–Љ–µ—А—В–љ–Њ—Б—В–Є –њ–∞—Ж–Є–µ–љ—В–Њ–≤ –њ—А–Є –ї–µ—З–µ–љ–Є–Є —В—П–ґ–µ–ї—Л—Е –≤–љ–µ–±–Њ–ї—М–љ–Є—З–љ—Л—Е –Є –љ–Њ–Ј–Њ–Ї–Њ–Љ–Є–∞–ї—М–љ—Л—Е –Є–љ—Д–µ–Ї—Ж–Є–є –љ–Є–ґ–љ–Є—Е –Њ—В–і–µ–ї–Њ–≤ –і—Л—Е–∞—В–µ–ї—М–љ–Њ–≥–Њ —В—А–∞–Ї—В–∞, –Њ—А–≥–∞–љ–Њ–≤ –±—А—О—И–љ–Њ–є –њ–Њ–ї–Њ—Б—В–Є –Є –Љ–∞–ї–Њ–≥–Њ —В–∞–Ј–∞, –∞ —В–∞–Ї–ґ–µ —Б–µ–њ—Б–Є—Б–∞ (–Ю–® 0,98; 95% –Ф–Ш 0,71–1,35). –Ю–і–љ–∞–Ї–Њ —Г –Љ–µ—А–Њ–њ–µ–љ–µ–Љ–∞ –Њ—В–Љ–µ—З–µ–љ–∞ –±–Њ–ї–µ–µ –≤—Л—Б–Њ–Ї–∞—П –Ї–ї–Є–љ–Є—З–µ—Б–Ї–∞—П (–Ю–® 1,04; 95% –Ф–Ш 1,01–1,06) –Є –±–∞–Ї—В–µ—А–Є–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–∞—П (–Ю–® 1,05; 95% –Ф–Ш 1,01–1,08) —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В—М –Є –љ–∞–±–ї—О–і–∞–ї–Њ—Б—М –Љ–µ–љ—М—И–µ –Њ—Б–ї–Њ–ґ–љ–µ–љ–Є–є, –≤—Л—П–≤–ї–µ–љ–љ—Л—Е —Б –њ–Њ–Љ–Њ—Й—М—О –ї–∞–±–Њ—А–∞—В–Њ—А–љ—Л—Е —В–µ—Б—В–Њ–≤ (—В—А–Њ–Љ–±–Њ—Ж–Є—В–Њ–Ј, –њ–Њ–≤—Л—И–µ–љ–Є–µ —Г—А–Њ–≤–љ—П –њ–µ—З–µ–љ–Њ—З–љ—Л—Е —Д–µ—А–Љ–µ–љ—В–Њ–≤) –ї–Є–±–Њ –њ–Њ –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Њ–є —Б–Є–Љ–њ—В–Њ–Љ–∞—В–Є–Ї–µ [55]. –Ь–µ—А–Њ–њ–µ–љ–µ–Љ –±–µ–Ј–Њ–њ–∞—Б–љ–µ–µ –Є–Љ–Є–њ–µ–љ–µ–Љ–∞ –њ—А–Є –ї–µ—З–µ–љ–Є–Є –±–Њ–ї—М–љ—Л—Е —Б —Б–Њ–њ—Г—В—Б—В–≤—Г—О—Й–Є–Љ–Є –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П–Љ–Є —Ж–µ–љ—В—А–∞–ї—М–љ–Њ–є –љ–µ—А–≤–љ–Њ–є —Б–Є—Б—В–µ–Љ—Л –Є –љ–∞—А—Г—И–µ–љ–љ–Њ–є —Д—Г–љ–Ї—Ж–Є–µ–є –њ–Њ—З–µ–Ї –Є –Љ–Њ–ґ–µ—В –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞—В—М—Б—П –і–ї—П —В–µ—А–∞–њ–Є–Є –±–∞–Ї—В–µ—А–Є–∞–ї—М–љ—Л—Е –Љ–µ–љ–Є–љ–≥–Є—В–Њ–≤.
–Ч–∞–Ї–ї—О—З–µ–љ–Є–µ
–Ь–∞—Б—Б–Њ–≤–Њ–µ —Н–Љ–њ–Є—А–Є—З–µ—Б–Ї–Њ–µ –љ–∞–Ј–љ–∞—З–µ–љ–Є–µ –Ї–∞—А–±–∞–њ–µ–љ–µ–Љ–Њ–≤ —Б–≤—П–Ј–∞–љ–Њ —Б–Њ –Ј–љ–∞—З–Є—В–µ–ї—М–љ—Л–Љ–Є —Д–Є–љ–∞–љ—Б–Њ–≤—Л–Љ–Є –Ј–∞—В—А–∞—В–∞–Љ–Є –Є —Б–њ–Њ—Б–Њ–±—Б—В–≤—Г–µ—В —Б–µ–ї–µ–Ї—Ж–Є–Є –њ–Њ–ї–Є—А–µ–Ј–Є—Б—В–µ–љ—В–љ—Л—Е —И—В–∞–Љ–Љ–Њ–≤ –≥—А–∞–Љ–Њ—В—А–Є—Ж–∞—В–µ–ї—М–љ—Л—Е –±–∞–Ї—В–µ—А–Є–є, –њ–Њ—Н—В–Њ–Љ—Г –Є—Е —Б–ї–µ–і—Г–µ—В –њ—А–Є–Љ–µ–љ—П—В—М —Б—В—А–Њ–≥–Њ –њ–Њ –њ–Њ–Ї–∞–Ј–∞–љ–Є—П–Љ.
–° –њ–Њ–Ј–Є—Ж–Є–Є –і–Њ–Ї–∞–Ј–∞—В–µ–ї—М–љ–Њ–є –Љ–µ–і–Є—Ж–Є–љ—Л (–Љ–µ—В–∞––∞–љ–∞–ї–Є–Ј –Є –і–∞–љ–љ—Л–µ –Љ—Г–ї—М—В–Є—Ж–µ–љ—В—А–Њ–≤—Л—Е –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–є) –Ї–∞—А–±–∞–њ–µ–љ–µ–Љ—Л –љ–∞–Є–±–Њ–ї–µ–µ –љ–∞–і–µ–ґ–љ—Л –≤ –Ї–∞—З–µ—Б—В–≤–µ —Б—А–µ–і—Б—В–≤ —Б—В–∞—А—В–Њ–≤–Њ–є —Н–Љ–њ–Є—А–Є—З–µ—Б–Ї–Њ–є —В–µ—А–∞–њ–Є–Є —В—П–ґ–µ–ї—Л—Е –≥–Њ—Б–њ–Є—В–∞–ї—М–љ—Л—Е –Є–љ—Д–µ–Ї—Ж–Є–є. –Ю–љ–Є —П–≤–ї—П—О—В—Б—П –њ—А–µ–њ–∞—А–∞—В–∞–Љ–Є –њ–µ—А–≤–Њ–≥–Њ —А—П–і–∞ –њ—А–Є –Є–љ—Д–µ–Ї—Ж–Є—П—Е —Г –±–Њ–ї—М–љ—Л—Е –≤ –Ї—А–Є—В–Є—З–µ—Б–Ї–Њ–Љ —Б–Њ—Б—В–Њ—П–љ–Є–Є (–њ–Њ —И–Ї–∞–ї–µ –Р–†–Р–°–Э–Х II –±–Њ–ї–µ–µ 13 –±–∞–ї–ї–Њ–≤), –њ—А–Є –њ–Њ–Ј–і–љ–µ–є (–±–Њ–ї–µ–µ 5 —Б—Г—В–Њ–Ї) –Т–Р–Я, –Є–љ—Д–Є—Ж–Є—А–Њ–≤–∞–љ–љ–Њ–Љ –њ–∞–љ–Ї—А–µ–Њ–љ–µ–Ї—А–Њ–Ј–µ, –њ–Њ—Б–ї–µ–Њ–њ–µ—А–∞—Ж–Є–Њ–љ–љ–Њ–Љ –Љ–µ–љ–Є–љ–≥–Є—В–µ (–Љ–µ—А–Њ–њ–µ–љ–µ–Љ, –љ–Њ –љ–µ –Є–Љ–Є–њ–µ–љ–µ–Љ!), –њ—А–Є –Є–љ—Д–µ–Ї—Ж–Є—П—Е —Г –±–Њ–ї—М–љ—Л—Е —Б –љ–µ–є—В—А–Њ–њ–µ–љ–Є–µ–є, –њ—А–Є –≥–љ–Њ–є–љ—Л—Е –њ—А–Њ—Ж–µ—Б—Б–∞—Е –≤ –ї–µ–≥–Ї–Є—Е –љ–∞ —Д–Њ–љ–µ –Є–Љ–Љ—Г–љ–Њ–і–µ—Д–Є—Ж–Є—В–∞. –£ —Н—В–Є—Е –њ–∞—Ж–Є–µ–љ—В–Њ–≤ –Љ–Њ–ґ–љ–Њ –Њ–ґ–Є–і–∞—В—М —Б–љ–Є–ґ–µ–љ–Є—П —Б–Љ–µ—А—В–љ–Њ—Б—В–Є –њ—А–Є –њ—А–Њ–≤–µ–і–µ–љ–Є–Є –і–µ—Н—Б–Ї–∞–ї–∞—Ж–Є–Њ–љ–љ–Њ–є —В–µ—А–∞–њ–Є–Є.
–Т –Ї–∞—З–µ—Б—В–≤–µ –њ—А–µ–њ–∞—А–∞—В–Њ–≤ –≤—В–Њ—А–Њ–≥–Њ —А—П–і–∞ –Ї–∞—А–±–∞–њ–µ–љ–µ–Љ—Л –њ—А–Є–Љ–µ–љ—П—О—В—Б—П –њ—А–Є –љ–µ—Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В–Є —В–µ—А–∞–њ–Є–Є –њ–µ—А–≤–Њ–љ–∞—З–∞–ї—М–љ–Њ –≤—Л–±—А–∞–љ–љ—Л–Љ–Є –∞–љ—В–Є–±–Є–Њ—В–Є–Ї–∞–Љ–Є, —З—В–Њ —П–≤–Є–ї–Њ—Б—М –њ—А–Є—З–Є–љ–Њ–є –њ–µ—А–µ–≤–Њ–і–∞ –њ–∞—Ж–Є–µ–љ—В–∞ –≤ –Ю–†–Ш–Ґ –Є–Ј –і—А—Г–≥–Њ–≥–Њ –Њ—В–і–µ–ї–µ–љ–Є—П –±–Њ–ї—М–љ–Є—Ж—Л, –Є –њ—А–Є –∞–љ–∞–Љ–љ–µ—Б—В–Є—З–µ—Б–Ї–Є—Е —Г–Ї–∞–Ј–∞–љ–Є—П—Е –љ–∞ –љ–µ–і–∞–≤–љ—О—О —В–µ—А–∞–њ–Є—О –љ–µ—Б–Ї–Њ–ї—М–Ї–Є–Љ–Є –∞–љ—В–Є–±–Є–Њ—В–Є–Ї–∞–Љ–Є. –Ф–ї–Є—В–µ–ї—М–љ–Њ—Б—В—М –ї–µ—З–µ–љ–Є—П –Њ–±—Л—З–љ–Њ —Б–Њ—Б—В–∞–≤–ї—П–µ—В –Њ—В 3–5 –і–Њ 14 —Б—Г—В–Њ–Ї –Є –Њ–њ—А–µ–і–µ–ї—П–µ—В—Б—П –Ї–Њ–љ–Ї—А–µ—В–љ–Њ–є –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Њ–є —Б–Є—В—Г–∞—Ж–Є–µ–є.
–¶–µ–ї–µ–љ–∞–њ—А–∞–≤–ї–µ–љ–љ–∞—П —В–µ—А–∞–њ–Є—П –∞–љ—В–Є—Б–Є–љ–µ–≥–љ–Њ–є–љ—Л–Љ–Є –Ї–∞—А–±–∞–њ–µ–љ–µ–Љ–∞–Љ–Є –њ—А–Њ–≤–Њ–і–Є—В—Б—П –њ—А–Є –і–Њ–Ї—Г–Љ–µ–љ—В–Є—А–Њ–≤–∞–љ–љ—Л—Е –Є–љ—Д–µ–Ї—Ж–Є—П—Е, –≤—Л–Ј–≤–∞–љ–љ—Л—Е –њ—А–Њ–і—Г—Ж–µ–љ—В–∞–Љ–Є –С–Ы–†–°, –≥–і–µ –≤—Л–±–Њ—А –њ—А–µ–њ–∞—А–∞—В–Њ–≤ –Ј–∞ —А–µ–і–Ї–Є–Љ –Є—Б–Ї–ї—О—З–µ–љ–Є–µ–Љ –Њ–≥—А–∞–љ–Є—З–µ–љ –Љ–µ—А–Њ–њ–µ–љ–µ–Љ–Њ–Љ –Є –Є–Љ–Є–њ–µ–љ–µ–Љ–Њ–Љ. –Я—А–Є —Б–Є–љ–µ–≥–љ–Њ–є–љ–Њ–є –Є–љ—Д–µ–Ї—Ж–Є–Є –Љ–µ—А–Њ–њ–µ–љ–µ–Љ –њ—А–µ–≤–Њ—Б—Е–Њ–і–Є—В –Є–Љ–Є–њ–µ–љ–µ–Љ –њ–Њ —Б—В–µ–њ–µ–љ–Є –∞–Ї—В–Є–≤–љ–Њ—Б—В–Є, –∞ –і–ї—П –њ—А–µ–Њ–і–Њ–ї–µ–љ–Є—П –њ—А–Є–Њ–±—А–µ—В–µ–љ–љ–Њ–є —А–µ–Ј–Є—Б—В–µ–љ—В–љ–Њ—Б—В–Є P. aeruginosa –њ–µ—А—Б–њ–µ–Ї—В–Є–≤–љ—Л–Љ —П–≤–ї—П–µ—В—Б—П –њ—А–Є–Љ–µ–љ–µ–љ–Є–µ –∞–љ—В–Є–±–Є–Њ—В–Є–Ї–∞ –≤ —А–µ–ґ–Є–Љ–µ –њ—А–Њ–і–ї–µ–љ–љ–Њ–є –Є–љ—Д—Г–Ј–Є–Є.


–Ы–Є—В–µ—А–∞—В—Г—А–∞
1. Pfaller M.A., Jones R.N. A review of the in vitro activity of meropenem and comparative antimicrobial agents tested against 30,254 aerobic and anaerobic pathogens isolated world wide. Diagn Microbiol Infect Dis 1997; 28:157–163.
2. Fish D.N., Singletary T.J. Meropenem: a new carbapenem antibiotic. Pharmacotherapy 1997; 17(4):644–669.
3. Blumer J.I. Meropenem: evaluation of a new generation carbapenem. Intern J Antimicrob Agent 1997: 8(2):73–92.
4. Jones R.N. In vitro evaluation of ertapenem (MK–0826), a long acting carbapenem, tested against selected resistant strains 2001; 13:363–376.
5. Mouton J.W., Touzw D.J., Horrevorts A.M., Vinks A.A. Comparative pharmacokinetics of the carbapenems: clinical implications. Clin Pharmacokinet 2000; 39:185–201.
6. Bush K., Jacoby G.A., Medeiros A.A. A functional classification scheme for beta–lactamases and its correlation with molecular structure. Antimicrob Agents Chemother 1995; 39: 1211–1233.
7. Andes D., Craig W.A. Impact of extended spectrum beta–lactamase (ESBL) production on the activity of cefepime in a murine–thigh infection model. Abstracts of the 41th Interscience Conference on Antimicrobial Agents and Chemotherapy, Desember 2001.
8. Kollef M. Appropriatr empirical antibacterial therapy for nosocomial infections. Drugs 2003 ; 63(2): 2157–2168.
9. McGowan J.E., Tenover F.C. Control of antimicrobial resistance in the health care system. Infect Dis Clin North Am 1997; 11: 297–311.
10. Jones R.N., Pfaller M.A., and the MYSTIC Study Group. Antimicrobial activity of selected agents against strains of Escherichia coli, Klebsiella spp. And Proteus mirabilis with resistance phenotypes consistent with an extended spectrum beta–lactamase: report from the MYSTIC programme in Europe (1997–2000). Clin Microbiol Infect 2001; 7(Suppl 1):P438.
11. –°–Є–і–Њ—А–µ–љ–Ї–Њ –°.–Т. –Р–љ—В–Є–±–∞–Ї—В–µ—А–Є–∞–ї—М–љ–∞—П —В–µ—А–∞–њ–Є—П. –Я—А–∞–Ї—В–Є—З–µ—Б–Ї–Њ–µ —А—Г–Ї–Њ–≤–Њ–і—Б—В–≤–Њ. –Я–Њ–і —А–µ–і. –Ы.–°.–°—В—А–∞—З—Г–љ—Б–Ї–Њ–≥–Њ, –Ѓ.–С.–С–µ–ї–Њ—Г—Б–Њ–≤–∞, –°.–Э.–Ъ–Њ–Ј–ї–Њ–≤–∞. –Ь., 2000; 1–6.
12. Jacoby G.A. Extended–spectrum beta–lactamases and other enzymes providing resistance to oxyimino–beta–lactams. Infect Dis Clin North Amer 1997; 11:875–87.
13. Patterson J.E., Recb M., Jorgensen J.H. Extended–spectrum–beta–lactamases: dilemmas in detection and therapy. Antimicrob Infect Dis Newsletter 1998; 16:57–61.
14. –≠–є–і–µ–ї—М—И—В–µ–є–љ –Ь.–Т., –°—В—А–∞—З—Г–љ—Б–Ї–Є–є –Ы.–°. –Ф–Є–љ–∞–Љ–Є–Ї–∞ —А–∞—Б–њ—А–Њ—Б—В—А–∞–љ–µ–љ–љ–Њ—Б—В–Є –Є —З—Г–≤—Б—В–≤–Є—В–µ–ї—М–љ–Њ—Б—В–Є –С–Ы–†–°––њ—А–Њ–і—Г—Ж–Є—А—Г—О—Й–Є—Е —И—В–∞–Љ–Љ–Њ–≤ —Н–љ—В–µ—А–Њ–±–∞–Ї—В–µ—А–Є–є –Ї —А–∞–Ј–ї–Є—З–љ—Л–Љ –∞–љ—В–Є–Љ–Є–Ї—А–Њ–±–љ—Л–Љ –њ—А–µ–њ–∞—А–∞—В–∞–Љ –≤ –Ю–†–Ш–Ґ –†–Њ—Б—Б–Є–Є. –Ъ–ї–Є–љ –Ь–Є–Ї—А–Њ–±–Є–Њ–ї –Р–љ—В–Є–Љ–Є–Ї—А–Њ–± –•–Є–Љ–Є–Њ—В–µ—А. 2005; 7(4):323–336.
15. NCCLS 2000. Methods for dilution antimicrobial susceptibility tests for bacteria that grow aerobically. Approved standard M7–A5, 5th ed. National Committee for Clinical Laboratory Standards, Wayne, Pa.
16. Jones R.N. Resistance patterns among nosocomial pathogens: trends over the past few years. Chest 2001; 119: 397S–404S.
17. Quale G., Landman D., Saurina G. et al. Molecular epidemiology of a sitywide outbreak of extended–spectrum beta–lactamase producing Klebsiella pneumoniae infection. Clin Infect Dis 2002;35:834–841.
18. Shah P.M. Parenteral carbapenems. Clin Microbiol Infect 2008; 14(Suppl 1): 175–180.
19. Pfaller M.A., Jones R.N., and the MYSTIC Study Group. Antimicrobial susceptibility of inducible AmpC beta–lactamase produsing Gram–negative bacilli from the European Meropenem Yearly Susceptibility Test Information Collection (MYSTIC) programme 1997–2000. Clin Microbiol Infect 2001; 7(Suppl 1):P439.
20. Edwards J. Meropenem: a microbiological overview. J Antimicrob Chemother 1995; 36(Suppl A): 1–17.
21. Livermore D.M. Of Pseudomonas, porins, pumps and carbapenems. J Antimicrob Chemother 2001; 47:247–250.
22. Livermore D.M. Bacterial resistance: origins, epidemiology and impact. Clin Infect Dis 2003; 36(Suppl 1); S11–S23.
23. Turner P.J. Trends in antimicrobial susceptibilities among bacterial pathogens isolated from patients hospitalized in European medical centers: 6–year report of the MYSTIC surveillance study (1997–2002). Diagn Microbiol Infect Dis 2005; 51: 281–289.
24. –°—В—А–∞—З—Г–љ—Б–Ї–Є–є –Ы.–°., –†–µ—И–µ–і—М–Ї–Њ –У.–Ъ., –°—В–µ—Ж—О–Ї –Ю.–£. –Є –і—А. –°—А–∞–≤–љ–Є—В–µ–ї—М–љ–∞—П –∞–Ї—В–Є–≤–љ–Њ—Б—В—М–∞–љ—В–Є—Б–Є–љ–µ–≥–љ–Њ–є–љ—Л—Е –∞–љ—В–Є–±–Є–Њ—В–Є–Ї–Њ–≤ –≤ –Њ—В–љ–Њ—И–µ–љ–Є–Є –љ–Њ–Ј–Њ–Ї–Њ–Љ–Є–∞–ї—М–љ—Л—Е —И—В–∞–Љ–Љ–Њ–≤ P.aeruginosa, –≤—Л–і–µ–ї–µ–љ–љ—Л—Е –≤ –Њ—В–і–µ–ї–µ–љ–Є—П—Е —А–µ–∞–љ–Є–Љ–∞—Ж–Є–Є –Є –Є–љ—В–µ–љ—Б–Є–≤–љ–Њ–є —В–µ—А–∞–њ–Є–Є. –Ъ–ї–Є–љ –Ь–Є–Ї—А–Њ–±–Є–Њ–ї –Р–љ—В–Є–Љ–Є–Ї—А–Њ–± –•–Є–Љ–Є–Њ—В–µ—А 2003; 5(1): 35–46.
25. Iaconis J.P., Pitkin D.H., Skeikb W., et al. Comparison of antibacterial activities of meropenem and six other antimicrobials agents Pseudomonas aeruginosa isolates from North American studies and clinical trials. Clin Infect Dis 1997; 24(Suppl 2):S191–7.
26. –ѓ–Ї–Њ–≤–ї–µ–≤ –°.–Т., –ѓ–Ї–Њ–≤–ї–µ–≤ –Т.–Я., –Ф–µ—А–µ–≤—П–љ–Ї–Њ –Ш.–Ш. –Є –і—А. –Ь–љ–Њ–≥–Њ—Ж–µ–љ—В—А–Њ–≤–Њ–µ –Њ—В–Ї—А—Л—В–Њ–µ —А–∞–љ–і–Њ–Љ–Є–Ј–Є—А–Њ–≤–∞–љ–љ–Њ–µ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ –Љ–µ—А–Њ–њ–µ–љ–µ–Љ–∞ –≤ —Б—А–∞–≤–љ–µ–љ–Є–Є —Б –Ї–Њ–Љ–±–Є–љ–∞—Ж–Є–µ–є —Ж–µ—Д—В–∞–Ј–Є–і–Є–Љ–∞ –Є –∞–Љ–Є–Ї–∞—Ж–Є–љ–∞ –њ—А–Є —В—П–ґ–µ–ї—Л—Е –≥–Њ—Б–њ–Є—В–∞–ї—М–љ—Л—Е –Є–љ—Д–µ–Ї—Ж–Є—П—Е. –Р–љ—В–Є–±–Є–Њ—В–Є–Ї–Є –Є —Е–Є–Љ–Є–Њ—В–µ—А–∞–њ–Є—П. 1998; 43(1):15–23.
27. Lepper P.M., Grusa E., Reichl H., et al. Consumption of imipenem correlates with beta–lactam resistance in Pseudomonas aeruginosa. Antimicrob Agents Chemother 2002; 46: 2920–2925.
28. –°–Є–і–Њ—А–µ–љ–Ї–Њ –°.–Т., –†–µ–Ј–≤–∞–љ –°.–Я., –°—В–µ—А–µ—Е–Њ–≤–∞ –У.–Р., –У—А—Г–і–Є–љ–Є–љ–∞ –°.–Р. –У–Њ—Б–њ–Є—В–∞–ї—М–љ—Л–µ –Є–љ—Д–µ–Ї—Ж–Є–Є, –≤—Л–Ј–≤–∞–љ–љ—Л–µ Pseudomonas aeruginosa. –†–∞—Б–њ—А–Њ—Б—В—А–∞–љ–µ–љ–љ–Њ—Б—В—М –Є –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Њ–µ –Ј–љ–∞—З–µ–љ–Є–µ –∞–љ—В–Є–±–Є–Њ—В–Є–Ї–Њ—А–µ–Ј–Є—Б—В–µ–љ—В–љ–Њ—Б—В–Є. –Р–љ—В–Є–±–Є–Њ—В–Є–Ї–Є –Є —Е–Є–Љ–Є–Њ—В–µ—А–∞–њ–Є—П. 1999; 44(3):25–34.
29. –†–µ—И–µ–і—М–Ї–Њ –У.–Ъ., –†—П–±–Ї–Њ–≤–∞ –Х.–Ы., –§–∞—А–∞—Й—Г–Ї –Р.–Э., –Є—Б—Б–ї–µ–і–Њ–≤–∞—В–µ–ї—М—Б–Ї–∞—П –≥—А—Г–њ–њ–∞ –†–Ю–°–Э–Х–Ґ. –Э–µ—Д–µ—А–Љ–µ–љ—В–Є—А—Г—О—Й–Є–µ –≥—А–∞–Љ–Њ—В—А–Є—Ж–∞—В–µ–ї—М–љ—Л–µ –≤–Њ–Ј–±—Г–і–Є—В–µ–ї–Є –љ–Њ–Ј–Њ–Ї–Њ–Љ–Є–∞–ї—М–љ—Л—Е –Є–љ—Д–µ–Ї—Ж–Є–є –≤ –Ю–†–Ш–Ґ –†–Њ—Б—Б–Є–Є: –њ—А–Њ–±–ї–µ–Љ—Л –∞–љ—В–Є–±–Є–Њ—В–Є–Ї–Њ—А–µ–Ј–Є—Б—В–µ–љ—В–љ–Њ—Б—В–Є. –Ъ–ї–Є–љ –Ь–Є–Ї—А–Њ–±–Є–Њ–ї –Р–љ—В–Є–Љ–Є–Ї—А–Њ–± –•–Є–Љ–Є–Њ—В–µ—А. 2006; 8(3):243–259.
30. Queenan A.M., Foleno B., Gownley C., et al. Effects of inoculum and beta–lactamase activity in AmpC– and extended–spectrum beta–lactamase (ESBL)–producing Escherichia coli and Klebsiella pneumoniae clinical isolates tested by using NCCLS ESBL methodology. J Clin Microbiol 2004; 42: 269–275.
31. Burgess D.S., Hall R.G. In vitro killing of parenteral beta–lactams agains standart and high inocula of extended–spectrum beta–lactamase and non–ESBL producing Klebsiella pneumoniae. Diagn Microbiol Infect Dis 2004;49:41–46.
32. Kang C.L., Pai H., Kin S.H., et al. Cefepime and the inoculum effect in tests with Klebsiella pneumoniae produsing plasmid–mediated AmpC–type beta–lactamase. J Antimicrob Chemother 2004; 54:1130–1133.
33. Tam V.H., Schilling A.N., Melnick D.A., Coyle E.A. Comparison of beta–lactams in counter selecting resistance of Pseudomonas aeruginosa. Diagn Microbiol Infect Dis 2005; 52:145–151.
34. Thomson K.S., Moland E.S. Cefepime, piperacillin–tazobactam, and the inoculum effect in tests with extended–spectrum beta–lactamase–roducing Enterobacteriaceae. Antimicrob Agents Chemother 2001; 45: 3548–3554.
35. Danekar P.K., Maglio D., Sutherland C.A., et al. Pharmacokinetics of meropenem 0,5 and 2 g every 8 hours as a 3–hour infusion. Pharmacother 2003; 23:988–991.
36. Tam V.H., Schilling A.N., Neshat S., et al. Optimization of meropenem minimum concentration/MIC ratio to suppress in vitro resistance of Pseudomonas aeruginosa. Antimicrob Agents Chemother 2005; 49:4920–4927.
37. Drusano G.L. Pharmacokinetics of meropenem. Antiinfect Drugs Chemother 1996; 14(1):48.
38. Mouton J., van den Anker J. Meropenem clinical pharmacokinetics. Clin Pharmacokinet 1995; 28:275–286.
39. Jumbe N., Louie A., Leafy R., et al. Application of a mathematical model to prevent in vivo amplification of antibiotic–resistant bacterial population during therapy. J Clin Invest 2003; 112: 275–285.
40. Drusano G.L. Carbapenem monotherapy, novel strategies to minimize ICU resistance. 41st ICAAC 2001 December 16. Special Report 2002.
41. Drusano G.L. Prevention of resistance: a goal for dose selection for antimicrobial agents. Clin Infect Dis 2003; 36(Suppl 1):S42–S50.
42. Jaruratanasirikul S., Sriwiriyajan S., Punyo J. Comparison of the pharmacodynamics of meropenem in patients with ventilator–associated pneumonia following administration by 3–hour infusion or bolus injection. Antimicrob Agents Chemother 2005; 49:1337–1339.
43. Lorente L., Huidobro S., Martin M., Mora M. Meropenem administration by intermittent infusion versus continuous infusion for the treatment of nosocomial pneumonia. Critical Care 2005; 9(Suppl 1):P38.
44. Kuri J., Maglio D., Nightingale C., Nicolau D. Economic benefits of a meropenem dosage strategy based on pharmacodynamic concepts. Am J Health Syst Pharm 2003; 60:565–568.
45. Kotapati S., Nicolau D., Nightingale C., et al. Clinical and economic benefits of a meropenem dosage strategy based on pharmacodynamic concepts in a large teaching hospital. Am J Health Syst Pharm 2004; 61:1264–1270.
46. Alvarez–Lerma F. Modification of empiric antibiotic treatment in patients with pneumonia acquired in the intensive care unit: ICU–Acquired Pneumonia Study Group. Intensive Care Med 1996;22:387–394.
47. Rello J., Sa–Borges M., Correa H., et al. The value of routine microbial investigation in ventilator–associated pneumonia. Am J Respir Crit Care Med. 1997;156:196–200
48. Ibrahim E.H., Sherman G., Ward S., et al. The Influence of Inadequate Antimicrobial Treatment of Bloodstream Infections on Patient Outcomes in the ICU Setting Chest 2000;118:146–155.
49. Kollef M.H., Sherman G., Ward S., Fraser V.J. Inadequate antimicrobial treatment of infections: a risk factor for hospital mortality among critically ill patients. Chest 1999; 115:462–474.
50. –ѓ–Ї–Њ–≤–ї–µ–≤ –°.–Т., –С–µ–ї–Њ–±–Њ—А–Њ–і–Њ–≤ –Т.–С., –°–Є–і–Њ—А–µ–љ–Ї–Њ –°.–Т. –Є –і—А. –Р–љ–∞–ї–Є–Ј –∞–і–µ–Ї–≤–∞—В–љ–Њ—Б—В–Є —Б—В–∞—А—В–Њ–≤—Л—Е —Н–Љ–њ–Є—А–Є—З–µ—Б–Ї–Є—Е –†–µ–ґ–Є–Љ–Њ–≤ –∞–љ—В–Є–±–∞–Ї—В–µ—А–Є–∞–ї—М–љ–Њ–є —В–µ—А–∞–њ–Є–Є –њ—А–Є —В—П–ґ–µ–ї—Л—Е –љ–Њ–Ј–Њ–Ї–Њ–Љ–Є–∞–ї—М–љ—Л—Е –Є–љ—Д–µ–Ї—Ж–Є—П—Е (–Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ –Р–°–≠–Ґ). –Ъ–ї–Є–љ –§–∞—А–Љ–∞–Ї–Њ–ї –Ґ–µ—А 2006; 15:14–21.
51. –°–∞–≤–µ–ї—М–µ–≤ –Т.–°., –У–µ–ї—М—Д–∞–љ–і –С.–†. (—А–µ–і). –Р–љ—В–Є–±–∞–Ї—В–µ—А–Є–∞–ї—М–љ–∞—П —В–µ—А–∞–њ–Є—П –∞–±–і–Њ–Љ–Є–љ–∞–ї—М–љ–Њ–є —Е–Є—А—Г—А–≥–Є—З–µ—Б–Ї–Њ–є –Є–љ—Д–µ–Ї—Ж–Є–Є. –Ь. 2003; –Ш–Ј–і.3: 185 —Б.
52. Tellado J.M., Christou N.V. Intra–abdominal infections. – Madrid. “Harcourt” 2000; 219–246.
53. –У–µ–ї—М—Д–∞–љ–і –С.–†., –С—Г—А–љ–µ–≤–Є—З –°.–Ч., –У–µ–ї—М—Д–∞–љ–і –Х.–С. –Є –і—А. –≠—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В—М –њ–µ—Д–ї–Њ–Ї—Б–∞—Ж–Є–љ–∞ (–∞–±–∞–Ї—В–∞–ї–∞) –≤ –Ї–Њ–Љ–њ–ї–µ–Ї—Б–љ–Њ–Љ –ї–µ—З–µ–љ–Є–Є –±–Њ–ї—М–љ—Л—Е —Б –њ–∞–љ–Ї—А–µ–Њ–љ–µ–Ї—А–Њ–Ј–Њ–Љ. –Р–љ—В–Є–±–Є–Њ—В–Є–Ї–Є –Є —Е–Є–Љ–Є–Њ—В–µ—А–∞–њ–Є—П 2001; 46(5): 24–27.
54. Manes G., Rabitti P.G., Menchise A., et al. Prophylaxis with meropenem of septic complications in acute pancreatitis: a randomized, controlled trial versus imipenem. Pancreas 2003; 27:79–83.
55. Edwards S.J., Emmas C.E., Campbell H.E. Systematic review comparing meropenem with imipenem plus cilastatin in the treatment of severe infections. Cur Med Research Opinion 2005; 21:785–794.












