Ни для кого не новость, что мужчина и женщина – две большие разницы. Еще в 1871 г. Чарльз Дарвин писал: «Мужчина храбрее, драчливее и энергичнее женщины и обладает более изобретательным умом… по своим умственным способностям мужчина, очевидно, превосходит женщину».
Почему же сегодня именно мужчина в центре внимания? К сожалению, статистика неумолима: по данным ВОЗ, в 2002 году средняя продолжительность жизни мужчин была выше, чем у женщин только в 6 странах мира: Непале, Ботсване, Зимбабве, Лесото, Бангладеш и Свазиленде. В 2005 году профессором Дэнни Дорлингом (Великобритания) установлено, что в мире больше не осталось стран, где мужчины жили бы дольше женщин. Российские данные еще более удручающие: средняя продолжительность жизни мужчин в нашей стране наименьшая среди развитых стран и составляет 60,2 года, что на 9 лет меньше, чем у женщин.
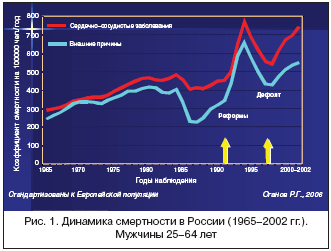
И причин этому несколько. Безусловно, общий низкий уровень жизни в стране, реформы середины 80–х гг. прошлого века, дефолт конца 90–х способствовали резкому увеличению смертности (прежде всего – от сердечно–сосудистых заболеваний – ССЗ), при этом в большей степени – у мужчин (рис. 1).
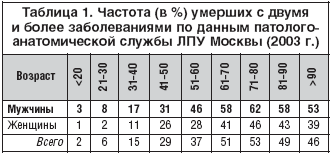
Другой факт – с возрастом растет число сочетанных хронических заболеваний. При этом частота полипатий (по данным аутопсий) у мужчин во всех возрастных группах существенно превышает таковую у женщин (табл. 1).
Значительный вклад в столь высокую заболеваемость и смертность вносит злоупотребление алкоголем. По нашим данным, в структуре летальных исходов в многопрофильном стационаре Москвы обусловленные алкоголем заболевания составляют 14,3%, в том числе 2/3 умерших – это мужчины [А.Л. Верткин, В.Г. Москвичев, 2007].
Итак, среднестатистический мужчина в России – это, как правило, больной человек, скорее всего, употребляющий алкоголь, и, как следствие, имеющий низкое качество и продолжительность жизни.
До настоящего времени факт как половых, так и социальных различий мало кто учитывает, определяя диагностическую и лечебную тактику. Между тем в последнее время появляется все больше данных о том, что одни и те же болезни имеют свои половые (гендерные) особенности и что лечить мужчин и женщин исходя из этого надо по–разному.
У мужчин больше ИМТ, больше размер внутренних органов, меньше относительное количество жира. Имеются различия в активности ферментов системы цитохрома Р450 у мужчин и женщин (у мужчин более высокая активность ферментов CYP1A2, CYP2D6, CYP2E1, у женщин более высокая активность фермента CYP3A4). Известно, что у женщин частота нежелательных лекарственных действий на 50–70% выше, чем у мужчин.
Но главное, что отличает мужчину от женщины – это половые гормоны, и прежде всего – тестостерон. С возрастом репродуктивная система мужчины претерпевает определенные изменения, которые, несмотря на проводимые аналогии с менопаузой, существенно отличаются от происходящих у женщин.
У мужчин не наблюдается резкого окончания репродуктивной функции, но происходит постепенное (начиная с 30–40 лет) снижение уровня тестостерона – около 2% в год и в 80 лет его уровень составляет 40% от уровня у 25–летнего мужчины [Harman S.M. et al., 2001].
Не вызывает сомнений взаимосвязь пола, гормонального статуса и развития ССЗ, в связи с этим гендерная кардиология представляет особый интерес. В трех крупных проспективных исследованиях (Framingham Study – изучены 1234 женщины в возрасте 53–83 лет, Nurses’ Health Study – 32 317 женщин 30–50 лет, Lipid Research Clinic Study – 2269 женщин 40–69 лет) получены убедительные сведения о связи между сердечно–сосудистой заболеваемостью, в первую очередь ИБС, у женщин, и уровнем эстрогенов, антиатеросклеротическое действие которых реализуется до наступления менопаузы [Sullivan J.M. et al., 1996].
Этим, вероятно, и обусловливается более низкий уровень заболеваемости ССЗ среди женщин, ИБС у которых развивается на 10–15 лет позже, чем у мужчин. Результаты Фрамингемского исследования продемонстрировали, что у женщин с гипертензией прогноз лучше, чем у мужчин, и что у них реже развивается ИБС. В рамках этого же исследования впервые было показано, что ожирение и метаболический синдром значимо и независимо увеличивают частоту ССЗ и сердечно–сосудистых осложнений, прежде всего у мужчин с избыточным весом (ИМТ от 25,0 до 29,9 кг /м2), у которых АГ выявлялась на 75%, а у женщин – только на 46% чаще по сравнению с лицами без избыточного веса.
В то же время сахарный диабет (СД) ассоциируется с более тяжелыми последствиями у женщин, чем у мужчин. Мета–анализ 10 проспективных исследований, преимущественно больных СД 2 типа, показал: риск ССЗ для женщин составляет 2,58, а для мужчин – 1,85. Этот фактор крайне неблагоприятен для женщин и сводит на нет положительное влияние эстрогенов.
Имеются данные о гендерных особенностях метаболического синдрома. Так, мета–анализ нескольких исследований показал, что высокий уровень тощаковой гликемии чаще встречается у мужчин, тогда как нарушение толерантности к углеводам – у женщин.
Характер распределения жировой ткани также имеет половые и инволютивные особенности. Так, у женщин в пременопаузе развивается периферический тип ожирения с подкожным отложением жировой ткани, тогда как у мужчин и постменопаузальных женщин – центральный тип, который ассоциирован с риском сердечно–сосудистой смертности [Regitz–Zagrosek V. et al., 2006].
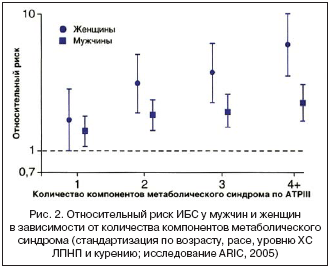
По данным исследования ARIC, риск ИБС линейно возрастает с увеличением количества компонентов метаболического синдрома. Для любого количества компонентов метаболического синдрома этот риск все–таки выше у женщин, чем у мужчин (рис. 2).
Таким образом, доказательства взаимосвязи половой принадлежности и механизмов развития метаболического синдрома очевидны.
Специфическими факторами риска развития ССЗ у женщин являются АГ и метаболические нарушения при беременности, гормональная контрацепция, менопауза, гистеровариэктомия. Результаты исследования Nurses` Health Study (NHS) показали определенную дозозависимую связь между коронарным риском среди женщин и потреблением никотина. Наряду с изменениями в стенке сосудов и свертывающей системе крови, характерными для обоих полов, курение оказывает ряд специфических эффектов на организм женщины. Они заключаются в более раннем наступлении менопаузы [Stampfer, 1990] и специфическом антиэстрогенном эффекте никотина [Khaw, 1988]. Курение дополнительно усиливает гипоэстрогенемию, являющуюся мощным фактором риска сердечно–сосудистой заболеваемости у женщин.
И хотя на протяжении последних лет летальность от ССЗ у женщин растет (в основном за счет роста числа курящих женщин), но все–таки она ниже, чем у мужчин, особенно молодого и среднего возраста [Goodman–Gruen and Barrett–Connor, 1996]. Именно мужской пол справедливо считается самостоятельным фактором кардиоваскулярного риска.
Однако пока еще недостаточно сведений о роли дефицита тестостерона у мужчин, его вкладе в развитие ССЗ и возможностях андрогенотерапии.
Тем не менее результаты некоторых работ свидетельствуют о наличии взаимосвязи между сниженным уровнем тестостерона, выраженностью атеросклероза и кардиоваскулярной патологией у мужчин [Phillips et al., 1994; English et al., 2000; L. Sieminska et al., 2003]. В работе Phillips et al. (1994 г.) была получена корреляция между уровнем свободного тестостерона и степени окклюзии коронарных артерий. L. Sieminska et al. (2003 г.) доказали, что уровень свободного тестостерона достоверно ниже у мужчин с коронарным атеросклерозом, а в исследовании M. Muller et al. (2004 г.) было выявлено, что концентрация свободного тестостерона находится в обратном соотношении с увеличением толщины «интима–медиа» сонной артерии.
При наличии АГ, ожирения, ишемической болезни сердца уровень тестостерона на 10–15% ниже, чем у здоровых людей того же возраста [А.Л. Верткин и соавт., 2006; A. Gray et al., 1991; C.A. Allan et al., 2006].
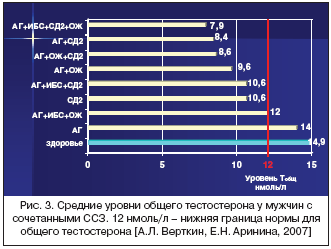
По нашим данным, андрогенный дефицит был выявлен у большинства из обследованных пациентов с ССЗ (в отличие от здоровых мужчин того же возраста). При этом сочетанная сосудистая патология (АГ в сочетании с висцеральным ожирением, АГ и СД 2 типа, АГ, висцеральное ожирение и СД 2 типа) независимо от возраста была ассоциирована со снижением уровня как общего, так и свободного тестостерона (рис. 3).
В ряде крупных исследований показана тесная взаимосвязь андрогенного дефицита и метаболического синдрома у мужчин [D. Simon et al., 1997; R.Y. Chen et al., 2006]. Низкий уровень тестостерона следует считать одним из компонентов метаболического синдрома (МС) наряду с инсулинорезистентностью, гиперинсулинемией, ожирением, дислипидемией, артериальной гипертензией, нарушением толерантности к глюкозе и нарушениями в свертывающей системе крови, то есть самостоятельным фактором кардиоваскулярного риска у мужчин.
По данным многочисленных исследований, ожирение, МС и атерогенез ассоциированы с хроническим воспалением [S.G. Wannamethee et al., 2005; H. Staiger et al., 2005; N. Paquot et al., 2005; M. Recasens, et al., 2004; K. Kobayashi et al., 2005]. В исследовании D. Aronson et al. была проанализирована взаимосвязь между уровнем С–реактивного протеина (CRP) и различными характеристиками МС. Было выявлено линейное возрастание уровня СRP при увеличении числа метаболических нарушений (p<0,0001), которые уменьшались при снижении индекса массы тела (ИМТ). При этом было также показано, что ИМТ, содержание триглицеридов, холестерина липопротеидов низкой плотности и глюкозы независимо взаимосвязаны с уровнем CRP [D. Aronson et al., 2004]. Сходные результаты были получены и другими исследователями. К примеру, H. Florez et al. также выявили положительную корреляцию уровня CRP и окружности талии, ИМТ, однако взаимосвязь инсулинорезистентности и CRP обнаружена только у мужчин, тогда как зависимость между уровнем последнего и содержанием свободных жирных кислот – только у женщин [H. Florez et al., 2005].
В свою очередь, ряд авторов продемонстрировали наличие тесной корреляции между уровнями различных цитокинов и содержанием тестостерона у мужчин. Так, M. Maggio et al. при обследовании 467 мужчин старше 65 лет выявили статистически значимую отрицательную корреляцию между уровнем IL–6 и содержанием как общего, так и свободного тестостерона [M. Maggio et al., 2006].
Проведенное в Китае (2002–2004 гг.) исследование показало, что уровни CRP, IL–6, IL–8, а также маркеров sICAM–1 (soluble intracellular adhesion molecule–1) и sVCAM–1 (soluble vascular cell adhesion molecule–1) достоверно выше у мужчин с андрогенным дефицитом, при этом корреляционный анализ показал тесную отрицательную взаимосвязь (r=–0,678) уровней свободного тестостерона и этих маркеров [Y.M. Yang et al., 2005].
Таким образом, суммируя приведенные факты, следует полагать, что низкая концентрация свободного тестостерона, приводя к повышению маркеров воспаления, способствует развитию и прогрессированию ожирения и атеросклероза, многократно повышая кардиоваскулярный риск у мужчин. Исходя из этого можно предположить, что нормализация уровня тестостерона может способствовать регрессу метаболических нарушений не только за счет усиления липолиза, повышения физической активности, повышения чувствительности тканей к инсулину, но также и посредством подавления воспалительного ответа.
За период с 1991 по 2002 г. проведен ряд экспериментальных исследований [Araneo et al., 1991; Li et al., 1993; Chao et al., 1995; Kanda et al., 1996; Dalal et al., 1997; D Agostino et al., 1999; Gornstein et al., 1999; Hatakeyama et al., 2002], выявивших снижение уровней воспалительных маркеров (фактора некроза опухолей–альфа – TNF–a, интерлейкинов: IL–6, IL–1, ?–интерферона) при введении андрогенов (тестостерона, дигидротестостерона и дигидроэпиандростерона).
В частности, исследование Chris J. Malkin et al. продемонстрировало положительное влияние заместительной терапии эфирами тестостерона в отношении маркеров воспаления. При этом уровни провоспалительных цитокинов – TNF–? и IL–1b на фоне лечения достоверно снижались, а концентрация противовоспалительного маркера IL–10, напротив, повышалась [C.J. Malkin, 2003].
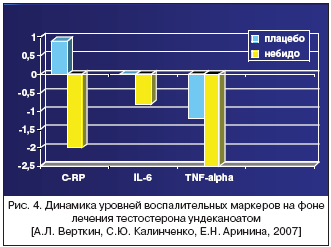
Прогнозируя позитивную роль нормализации уровня тестостерона у мужчин на течение сердечно–сосудистой патологии, маркером которой является в том числе увеличение воспалительных цитокинов, мы предприняли изучение влияния тестостерона ундеканоата (Небидо) в рамках двойного слепого плацебо–контролируемого исследования на эти маркеры (рис. 4).
Медианы исходных средних значений CRP составляли 4,0 мг/л в группе плацебо и 3,8 мг/л в группе активной терапии (p=1,0). По данным Health Professionals Follow–up study, концентрация CRP выше 3 мг/л ассоциируется с увеличением риска ИБС в 1,8 раза [P. Jennifer et al., 2004; S. Malik, 2005]. Использование же тестостерона ундеканоата привело к снижению CRP в 2,1 раза (p=0,01).
Исходные уровни IL–6 достоверно не различались, составив 3,2 [2,8–3,2] пг/мл и 3,7 [3,0–3,8] пг/мл, соответственно, в группе плацебо и активного лечения (p=1,0). Согласно результатам широкомасштабного исследования Health, Aging, and Body Composition study (Health ABC Study), концентрация IL–6?2,11 пг/мл независимо от других факторов риска тесно связана с развитием ИБС, инсульта и сердечной недостаточности [M. Cesari et al., 2003]. Кроме того, по данным J. Tzoulaki, уровень IL–6?3,3 мг/л является значимым предиктором развития периферического атеросклероза в ближайшие 5 лет [J. Tzoulaki et al., 2005]. На фоне терапии тестостерона ундеканоатом уровень IL–6 достоверно снизился до 3,1 [2,8–3,0] пг/мл (p=0,01). В группе плацебо статистической разницы показателей получено не было.
В уже цитируемом исследовании Health ABC Study выявлено возрастание риска кардиоваскулярных событий в 1,6 раза при увеличении концентрации TNF–??3,5 пг/мл. У пациентов в нашем исследовании исходные уровни TNF–? более чем в 4 раза превышали нормальные показатели и достоверно (p=0,005) снижались на фоне андрогенотерапии.
Кроме того, у пациентов, получавших тестостерона ундеканоат, достоверно снизился ИМТ (в среднем на 1,7 кг/м2, p<0,001), уровень общего холестерина и триглицеридов (в среднем соответственно на 1,8 и 0,6 ммоль/л, p<0,001), а уровень ХС ЛПВП – достоверно вырос (в среднем на 0,32 ммоль/л, p=0,16).
Таким образом, было продемонстрировано: терапия тестостерона ундеканоатом влияет на основные факторы кардиоваскулярного риска у мужчин, что следует учитывать при планировании научных исследований и разработке практических рекомендаций по профилактике и лечению сердечно–сосудистых заболеваний.
Подобный гендерспецифический подход пока был реализован только у женщин в Рекомендациях по профилактике сердечно–сосудистых заболеваний, основанных на доказательных исследованиях [AHA Scientific Statement, Evidence–Based Guidelines for Cardiovascular Disease Prevention in Women, 2004].
Вероятно, можно надеяться, что в скором времени терапия, направленная на коррекцию уровня тестостерона у мужчин, также войдет в рекомендации по лечению сердечно–сосудистых заболеваний.
Литература
1. Дедов И.И., Калинченко С.Ю. Возрастной андрогенный дефицит у мужчин. – М.: Практическая медицина, 2006. – 240 с.
2. Зайратьянц О.В., Ковальский Г.Б., Рыбакова М.Г. и соавт. Медико–демографические показатели: Россия, Москва, Санкт–Петербург. – Москва: МГМСУ, 2006.
3. Aronson D, Bartha P, Zinder O, Kerner A, Markiewicz W, Avizohar O, Brook GJ, Levy Y. Obesity is the major determinant of elevated C–reactive protein in subjects with the metabolic syndrome. // Int J Obes Relat Metab Disord. 2004 May;28(5):674–9.
4. Chen RY, Wittert GA, Andrews GR. Relative androgen deficiency in relation to obesity and metabolic status in older men. // Diabetes Obes Metab. 2006 Jul;8(4):429–35.
5. Chao TC, Van Alten PJ, Greager JA, Walter RJ. Steroid sex hormones regulate the release of tumor necrosis factor by macrophages. // Cell Immunol. – 1995. – Jan;160(1):43–9.
6. Cesari M., MD; Brenda W.J.H. Penninx, Anne B. Newman, Stephen B., Kritchevsky, Barbara J. Nicklas, Kim Sutton–Tyrrell, Susan M. Rubin, Jingzhong Ding, Eleanor M. Simonsick, Tamara B. Harris, Marco Pahor Inflammatory Markers and Onset of Cardiovascular Events Results From the Health ABC Study. // Circulation. – 2003. – November 11. – 108:2317–2322.
7. Florez H, Castillo–Florez S, Mende z A., Larreal–Urdaneta C, Lee D, Goldberg R. C–reactive protein is elevated in obese patients with the metabolic syndrome Diabetes Res Clin Pract. 2006 Jan;71(1):92–100. Epub 2005 Jul 5.
8. Gustiene O, Slapikas R, Marcinkeviciene J, Petrauskiene I, Milasauskiene Z, Griskeviciute R, Plepyte J, Zaliunas R. Relationship between the metabolic syndrome, endothelial function and intima–media thickness in asymptomatic middle–aged individuals. // Medicina (Kaunas). 2005;41(10):825–36.
9. Hutley L, Prins JB. Fat as an endocrine organ: relationship to the metabolic syndrome. // Am J Med Sci. 2005 Dec;330(6):280–9.
10. Kobayashi K. Adipokines: therapeutic targets for metabolic syndrome. // Curr Drug Targets. 2005 Jun;6(4):525–9.
11. Lambert CP, Sullivan DH, Evans WJ. Effects of testosterone replacement and/or resistance training on interleukin–6, tumor necrosis factor alpha, and leptin in elderly men ingesting megestrol acetate: a randomized controlled trial. // J Gerontol A Biol Sci Med Sci. 2003 Feb;58(2):165–70.
12. Maggio M, Basaria S, Ble A, Lauretani F, Bandinelli S, Ceda GP, Valenti G, Ling SM, Ferrucci L. Correlation between testosterone and the inflammatory marker soluble interleukin–6 receptor in older men. // J Clin Endocrinol Metab. 2006 Jan;91(1):345–7. Epub 2005 Nov 1.
13. Malkin C J, Pugh P J, Jones R D, Jones T H, Channer K S. // Testosterone as a protective factor against atherosclerosis –immunomodulation and influence upon plaque development and Stability. // Journal of Endocrinology 2003: 178, 373–380.
14. Malkin C.J., Pugh P.J., Richard D.J., Kapoor D., Channer K.S. The Effect of Testosterone Replacement on Endogenous Inflammatory Cytokines and Lipid Profiles in Hypogonadal Men. // The Journal of Clinical Endocrinology & Metabolism 89(7):3313–331.
15. Paquot N, Tappy L. Adipocytokines: link between obesity, type 2 diabetes and atherosclerosis. // Rev Med Liege. 2005 May–Jun;60(5–6):369–73.
16. Phillips G.B., Pinkernell B.H., Jing T.Y. The association of hypotestosteronemia with coronary artery disease in men. // Arterioscler. Thromb. – 1994. – Vol. 14, № 5. – P. 701–705.
17. Regitz–Zagrosek V, Lehmkuhl E, Weickert MO Gender differences in the metabolic syndrome and their role for cardiovascular disease. // Clin Res Cardiol. 2006 Mar;95(3):136–47. Epub 2006 Jan 30.
18. Staiger H, Haring HU. Adipocytokines: fat–derived humoral mediators of metabolic homeostasis. // Exp Clin Endocrinol Diabetes. 2005 Feb;113(2):67–79.
19. Stellato RK, Feldman HA, Hamdy O, Horton ES, McKinlay JB. Testosterone, sex hormone–binding globulin, and the development of type 2 diabetes in middle–aged men: prospective results from the Massachusetts male aging study. // Diabetes Care. 2000 Apr;23(4):490–4.
20. Yang YM et al., J Zhejiang Univ Sci B. 2005 Sep;6(9):931–5.
21. Wannamethee SG, Lowe GD, Shaper AG, Rumley A, Lennon L, Whincup PH. The metabolic syndrome and insulin resistance: relationship to haemostatic and inflammatory markers in older non–diabetic men. // Atherosclerosis. 2005 Jul;181(1):101–8.












