«Спондилогенные дорсалгии: источники, клиника, терапия»
«Спондилогенные дорсалгии: источники, клиника, терапия» К.А. Садоха, к.м.н., доцент кафедры неврологии и нейрохирургии БелМАПО (Минск)
Дорсалгия – болевой синдром в различных отделах спины и конечностей невисцеральной этиологии вследствие рефлекторных и/или компрессионных осложнений, дистрофических и функциональных изменений позвоночника, проксимальных суставов, а также миофасциального синдрома или фибромиалгии.
Распространенность боли в спине достигает степени пандемии, являясь серьезной медицинской и социально-экономической проблемой. Боль в спине – вторая по частоте после температурных заболеваний причина обращений к врачу, третья – по частоте госпитализации, а также частая причина инвалидизации. Тревожит тот факт, что 12–26% детей и подростков жалуются на боль в пояснице.
Распространенность заболеваний позвоночника в популяции составляет от 40 до 80% со стойкой тенденцией к росту. Почти 15% работающего населения ежегодно в большинстве регионов признаются нетрудоспособными по этой причине.
Болевой синдром может быть обусловлен изменениями тел позвонков, межпозвоночных дисков, суставов, связок, повреждениями и заболеваниями мышц; поражением спинного мозга, периферических нервов, нервных корешков, патологией внутренних органов, а также психическими расстройствами. Локальную боль в спине наиболее часто вызывают повреждения мышц, связок и дегенеративные изменения позвоночника.
Боли в спине, или дорсалгии, подразделяются на первичные, или спондилогенные, которые связаны с поражением позвоночно-двигательного сегмента, и вторичные, которые обусловлены другими причинами: травмами, опухолью, инфекционными процессами и заболеваниями внутренних органов.
К числу дегенеративно-дистрофических поражений позвоночника, или спондилопатий, относятся остеохондроз, спондилоартроз, спондилез. Это определенные этапы единого патологического процесса. При повышенных нагрузках образуются трещины в области фиброзного кольца, через которые выпячиваются элементы измененного диска с раздражением соседних нервных образований, что провоцирует боль в спине.
При анализе первичной обращаемости к врачам общей практики по поводу острой боли в пояснично-крестцовой области у 85% пациентов выявляются скелетно-мышечные боли. «Дискогенная» дорсалгия, которую гипердиагностируют врачи, боль, связанная с дисфункцией фасеточных суставов, отмечается не более чем в 10% случаев. Компрессионная радикулопатия на пояснично-крестцовом уровне встречается не более чем в 4–5% случаев, спондилолистез – в 2%.
Выделяют также основные вертеброгенные причины боли в спине (около 1% случаев), такие как первичная или метастатическая опухоль позвоночника, спондилоартриты, спондилиты, инфекционные, воспалительные процессы, дисциты.
У 2% пациентов боли в спине возникают вследствие заболеваний внутренних органов (невертеброгенные причины).
Существуют так называемые симптомы опасности, обычно указывающие на вторичный (симптоматический) характер дорсалгии:
1) впервые возникшие и быстро нарастающие боли;
2) значительная интенсивность боли;
3) независимость интенсивности боли от положения тела и движений;
4) усиление боли ночью;
5) лихорадка и/или резкое похудение;
6) недавняя травма, возникновение болей в связи с травмой;
7) очаговые неврологические нарушения, которые выходят за рамки типичной радикулопатии;
8) признаки злокачественного новообразования, онкологическое заболевание в анамнезе;
9) общая слабость;
10) дебют острого болевого синдрома в возрасте моложе 20 или старше 55 лет.
Среди причин первичных, или спондилогенных, дорсалгий выделяют так называемый диск-вертебральный синдром, или синдром мигрирующего диска, с раздражением соседних нервных образований вследствие сегментарной нестабильности в позвоночно-двигательном сегменте. К числу причин спондилогенной дорсалгии также относят дискорадикулярный конфликт. Выпячивание диска считается клинически значимым, если превышает 25% переднезаднего диаметра позвоночного канала или сужает его до критического уровня (10 мм) при ширине канала 18–20 мм. Еще одной причиной спондилогенной дорсалгии является синдром межпозвонкового отверстия, когда болевые ощущения обусловлены протрузией пульпозного ядра, раздражением нервных окончаний фиброзного кольца и задней продольной связки, спинального ганглия.
При патологических разрастаниях в области межпозвонкового отверстия возможно раздражение соседних нервных образований, что провоцирует спондилогенную дорсалгию.
Причинами боли в спине могут быть: дископаравертебральный синдром, связанный с напряжением околопозвоночных мышц; суставной синдром, или синовиальная боль, которая появляется при сближении суставных отростков и растяжении суставных капсул; синдром межостистых отростков, обусловленный фиброзным перерождением капсульно-связочных структур позвоночника; дискомедуллярный синдром, или компрессионно-ишемические поражения нервных корешков и структур спинного мозга.
Таким образом, при возникновении сдавления на уровне L4–L5 возможно раздражение не только корешковых артерий, но и соседних структур. В результате вначале возникает боль в спине с иррадиацией в обе ноги; затем на фоне распространения болевого синдрома появляются симптомы выпадения, т. е. парез нижних конечностей и нарушение функций тазовых органов.
Функция позвоночника обеспечивается структурной и функциональной полноценностью следующих структур: 1) межпозвонковых дисков; 2) апофизарных, крестцово-подвздошных, тазобедренных, коленных и голеностопных суставов; 3) связочного аппарата; 4) мышц спины, живота и нижних конечностей. Развитию биомеханического дисбаланса, увеличивающего нагрузку на те или иные структуры позвоночного столба, способствуют врожденные структурные несоответствия: асимметрия длины ног и/или тазового кольца, приводящая к формированию косого или скрученного таза, дисфункции крестцово-подвздошных сочленений, односторонняя сакрализация или люмбализация, асимметричная ориентация дугоотростчатых суставов и др.
Неспецифическая боль в спине – боль, которая связана со скелетно-мышечными расстройствами, без признаков поражения шейных, грудных, поясничных и крестцовых корешков и «специфических» повреждений позвоночника, таких как спондилолистез, остеопороз, опухоли, спондилоартропатии и др.
Мышечно-тонический синдром (МТС) – это наиболее часто встречающийся в практике рефлекторный болевой синдром, возникающий в ответ на раздражение рецепторов спинновертебрального нерва, причем не только при компрессии корешков, но и при других функциональных нарушениях в позвоночно-двигательном сегменте. Боль провоцируется движениями с участием соответствующей спазмированной мышцы. Симптомы натяжения вызывают локальную, или «короткую», боль, при пальпации мышца болезненна и напряжена.
Миофасциальный болевой синдром – проявление первичной дисфункции миофасциальных тканей, которая провоцируется активацией триггерных точек в фокусах повышенной болевой раздраженности мышцы или ее фракции. Например, причиной острой локализованной боли в пояснично-крестцовой области может быть миофасциальный болевой синдром в квадратной мышце поясницы, мышце, выпрямляющей позвоночник, многораздельных мышцах и мышцах-вращателях поясницы. Патогномоничным признаком миофасциальных болевых синдромов являются миофасциальные триггерные зоны. Для каждой триггерной зоны характерна своя строго определенная область отраженной боли и парестезии.
Факторы, которые способствуют формированию миофасциальных болевых синдромов, – это острое перерастяжение мышц при неподготовленном движении, антифизиологические длительные позы, воздействие высокой или низкой температуры, избыточная мышечная нагрузка, аномалии стопы, нарушение питания и обмена веществ.
Выделяют «большие» и «малые» диагностические критерии миофасциальных болевых синдромов:
• «Большие» критерии (необходимо наличие всех 5-ти):
– жалобы на региональную боль;
– пальпируемый тугой тяж в мышце;
– участок повышенной чувствительности в пределах тугого тяжа;
– характерный паттерн отраженной боли или чувствительных расстройств;
– ограничение объема движений.
• «Малые» критерии (необходимо наличие 1-го из 3-х):
– воспроизводимость боли или чувствительных нарушений при стимуляции триггерных точек;
– локальное вздрагивание при пальпации триггерной точки заинтересованной мышцы или при инъекции в триггерную точку;
– уменьшение боли при растяжении или инъекции в мышцу.
Вертеброгенная радикулопатия встречается не более чем в 5% случаев. Это обычно стреляющая, прокалывающая, реже жгучая боль, которая распространяется на нижнюю конечность вплоть до пальцев стопы, т. е. это «длинная» боль. Рефлекторные симптомы натяжения вызывают «длинную», «лампасную» боль в зоне пораженного нервного корешка и в первые дни – симптомы раздражения, т. е. болевой синдром, затем симптомы выпадения функций заинтересованного нервного корешка. При пальпации выявляется напряжение околопозвоночных мышц, а при МРТ – значимый дискомедуллярный конфликт (его уровень должен соответствовать клиническим проявлениям заболевания).
В межпозвонковом отверстии 1/3 объема занимают корешковые артерии и нервный корешок, 2/3 объема – венозное сплетение, поэтому нарушение венозного оттока, как правило, возникает с первых минут обострения заболеваний позвоночника.
Для лечения острых спондилогенных дорсалгий традиционно назначают нестероидные противовоспалительные препараты (НПВП), анальгетики, миорелаксанты, венотонизирующие, структурно-модифицирующие средства, а также дифференцированную физиотерапию. В настоящее время предпочитают применять препараты, которые оказывают комплексное действие на различные звенья патогенеза острой спондилогенной дорсалгии.
На протяжении последних лет широко применяется L-лизина эсцинат – венотропный препарат, имеющийся в инъекционной форме. Его основное действующее вещество – водорастворимая соль сапонина эсцина из плодов конского каштана и аминокислоты L–лизина (0,1% раствор для инъекций); ампулы по 5 мл содержат 4,4 г эсцина. Препарат действует на 3-х уровнях: эндотелия, просвета сосуда, сосудистой стенки. На уровне эндотелия препятствует высвобождению активного кислорода и продуктов его обмена, повышает энергетический статус эндотелия. В просвете сосуда оказывает антиагрегантный эффект, улучшая реологические свойства крови; в сосудистой стенке улучшает капиллярное кровообращение, микроциркуляцию, угнетает перекисное окисление липидов и защищает от оксидантного стресса.
Таким образом, препарат оказывает противоотечный, обезболивающий, противовоспалительный, мембранопротекторный эффекты, улучшает микроциркуляцию, снижает патологическую проницаемость сосудистой стенки за счет улучшения ее упруго-эластических свойств и венотонизирующего действия, восстанавливает эндотелиальную функцию, реологические показатели, снижает агрегационную активность тромбоцитов, применяется также с целью иммунокоррекции, т. к. воздействует на Т-клеточное звено иммунной системы.
Показано строго в/в введение препарата, лучше в/в капельно. Разовая доза L-лизина эсцината – 10 мл на 100 мл физиологического раствора в/в капельно 1 р./сут, 10 дней. Целесообразно начинать лечение как можно раньше, т. к. это позволит значительно сократить сроки лечения и избежать осложнений.
С момента появления L-лизина эсцината на фармрынке Белоруссии его эффективность и безопасность начали изучать во всех ведущих научных учреждениях республики, в т. ч. и на кафедре неврологии и нейрохирургии Белорусской медицинской академии постдипломного образования (Минск).
Под наблюдением находились 110 пациентов в возрасте от 26 до 58 лет (средний возраст – 42,0±2,2 года); 44 женщины и 66 мужчин. У 42 пациентов диагностирована люмбоишиалгия, у 36 – дискогенная радикулопатия с заинтересованностью первого крестцового корешка, у 32 – бирадикулярная дискогенная (L4–L5 и L5–S1) радикулопатия. Во всех случаях диагнозы соответствовали клинической классификации заболеваний периферической нервной системы [Антонов И.П., 1985], адаптированной к Международной классификации болезней 10-го пересмотра (МКБ-10). Продолжительность заболевания составляла 10,4±3,6 года. Длительность обострения до поступления в клинику колебалась от 1 до 5 нед., в среднем – 21,6±1,4 дня.
Распределение пациентов по группам было проведено методом случайной выборки. В основной группе (55 пациентов) на фоне общепринятого лечебного комплекса назначался L-лизина эсцинат (10 мл на 100 мл физиологического раствора в/в капельно 1 р./сут, 10 дней). В контрольной группе (55 пациентов, сопоставимых с основной группой по возрасту, полу, клиническим формам и другим параметрам) применялась общепринятая схема лечения (НПВП, миорелаксанты, традиционная физиотерапия), но без L-лизина эсцината.
Дизайн исследования включал клинико-неврологическую оценку пациентов с традиционным объективным осмотром, заполнением специально разработанной анкеты, определением степени выраженности боли по специальным шкалам до и после лечения, мануальное тестирование отдельных мышц с использованием дозированных нагрузочных проб, динамические общеклинические анализы, спондилографию с рентгенометрией позвоночника в 2-х проекциях, при необходимости – функциональную спондилографию, реовазографию нижних конечностей для определения состояния венозного оттока, электромиографию отдельных мышц, компьютерную, магнитно-резонансную томографию пояснично-крестцового отдела для подтверждения диагноза, исключения вторичного характера дорсалгии. Длительность наблюдения составила 14 дней.
Эффективность проводимого лечения оценивалась по следующим критериям: 1) интенсивность болевого синдрома по визуальной аналоговой шкале (ВАШ – 100 баллов); 2) объем движений в позвоночнике; 3) мышечно-тонические проявления; 4) выраженность корешкового синдрома; 5) эмоциональная оценка пациентами своих болевых ощущений.
По шкалам вычисляли ранговый индекс боли (РИБ) как сумму прилагательных, характеризующих болевой синдром: С – сенсорные нарушения; Э – эмоциональные расстройства; И – интенсивность боли; Р – разнообразие болевого синдрома и настоящее ощущение интенсивности боли (НИБ) от 0 до 5 баллов.
Степень выраженности МТС определяли, вычисляя индекс мышечного синдрома (ИМС):
1) выраженность спонтанных болей: 1 балл – в покое болей нет, появляются при нагрузке; 2 балла – боли незначительны в покое, усиливаются при движении; 3 балла – боли в покое, нарушается сон, вынужденная поза;
2) тонус мышц: 1 балл – палец легко погружается в мышцу; 2 балла – для погружения необходимо определенное усилие; 3 балла – мышца каменной плотности;
3) болезненность мышц: 1 балл – при пальпации пациент говорит о наличии боли; 2 балла – ответ на пальпацию мимической реакцией; 3 балла – ответ общей двигательной реакцией;
4) продолжительность болезненности: 1 балл – болезненность прекращается сразу; 2 балла – продолжается до 1 мин; 3 балла – продолжается более 1 мин;
5) степень иррадиации болей при пальпации: 1 балл – болезненность локализуется в месте пальпации; 2 балла – боль распространяется на рядом расположенные ткани; 3 балла – боль распространяется на отдаленные области.
ИМС оценивали по сумме баллов названных признаков: I степень (легкая) – ИМС до 5 баллов; II (средняя, умеренная) – от 5 до 12 баллов; III (тяжелая, выраженная) – более 12 баллов [3].
Неврологический статус оценивался при поступлении, до начала лечения, через 5, 10 дней и при выписке из стационара. Результаты терапии по количественным оценочным шкалам обработаны статистически с вычислением t-критерия Стьюдента. Достоверными считали результаты при р<0,05. Кроме клинической эффективности оценивались безопасность и переносимость препарата.
До начала исследований у всех пациентов в клинической картине преобладал вертеброгенный болевой синдром с различной интенсивностью боли (у 76 – умеренной, у 34 – значительной) в пояснично-крестцовой области, иррадиирующей в нижние конечности, с ограничением активных и пассивных движений в поясничном отделе позвоночника, напряжением околопозвоночных мышц и болезненностью их, остистых отростков, паравертебральных точек при пальпации на уровне L3–S1, положительными симптомами Ласега, Вассермана, Мацкевича. В случаях дискогенной радикулопатии клиническая картина дополнялась снижением или выпадением соответствующих рефлексов (L4 – коленного, S1 – ахиллового), мышечной слабостью и гипестезией в зоне иннервации пораженных нервных корешков.
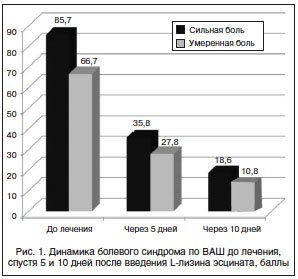
Интенсивность боли все пациенты основной группы оценили как сильную и умеренную, по шкале ВАШ – соответственно 85,7±2 и 66,7±2 балла. Эти данные подтверждало НИБ – 4,4±0,1 и 2,7±0,1, градуированное как сильная/умеренная боль. Эмоциональная и вегетативно-сосудистая окраска боли характеризовалась широким спектром разнообразных ощущений, в количественном отображении РИБ составил 10,8±0,4 балла. ИМС при объективном осмотре определяли как выраженный (12,5±0,2 балла; у 34 пациентов – 31%) и умеренный (7,6±0,2 балла; у 76 пациентов – 69%).
После лечения все 55 пациентов основной группы отметили улучшение своего состояния. Интенсивность боли по ВАШ через 5 дней терапии в 22 (40%) случаях снизилась до 35,8±2 балла (р<0,01) и в 33 (60%) случаях – до 27,8±3 (p<0,01). Выраженность боли по ВАШ через 10 дней терапии уменьшилась до 18,6±2 и 10,8±2 балла соответственно (р<0,01) (рис. 1).
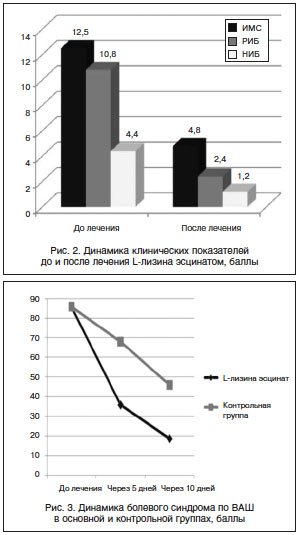
Мышечно-тонические проявления и их динамика соответствовали степени выраженности болевого синдрома. ИМС через 5 дней лечения составлял не более 4,8±0,2 балла (р<0,05); через 10 дней снизился до 2,0±0,2 балла (р<0,05). Положительной динамике болевого синдрома и ИМС сопутствовали значительное уменьшение болезненности паравертебральных точек в проекции сегментов L3–S1, восстановление полного объема движений в позвоночнике у всех пациентов основной группы.
Снижение выраженности боли и ИМС сопровождалось исчезновением субъективных сенсорных ощущений, признаков вегетативной дисфункции, тревожности, депрессии, повышенной эмоциональной возбудимости, что проявлялось уменьшением РИБ и НИБ до 2,4±0,2 и 1,2±0,2 балла соответственно, р<0,05 (рис. 2).
Переносимость L-лизина эсцината у всех пациентов была хорошей.
Оценка результатов лечения в основной группе, по мнению врача и пациентов, совпала во всех случаях. Значительное улучшение отметили 47 (80,5%) больных, умеренное – 8 (19,5%). Таким образом, положительная динамика при применении L-лизина эсцината отмечалась у всех (100%) пациентов основной группы.
Клинические проявления у пациентов контрольной группы совпадали с аналогичными показателями в основной группе. После лечения состояние большинства больных контрольной группы также улучшилось. Интенсивность боли снизилась по ВАШ до 68±2 балла (р<0,05) через 5 дней и до 46±2 (р<0,05) – через 10 дней. Побочные эффекты в виде болей в эпигастральной области и диспепсических проявлений отметили 12 (21,8%) пациентов контрольной группы. При проведении фиброгастродуоденоскопии у всех этих больных выявлена гастропатия, у 3 (5,5%) – эрозивная, что позволяет трактовать эти нарушения как НПВП-гастропатию.
Сопоставление результатов лечения в основной и контрольной группах показало, что под влиянием терапии наблюдается регресс болевого синдрома, МТС, вегетативно-сосудистой дисфункции и эмоционального ощущения боли, но их положительная динамика была более значимой и отчетливой у пациентов основной группы (рис. 3).
Таким образом, L -лизина эсцинат оказывает благоприятное комплексное воздействие на основные патогенетические звенья и клинические проявления спондилогенных дорсалгий, обладает противовоспалительным, обезболивающим, противоотечным, венотонизирующим (значительно улучшился венозный отток по данным реовазографии) эффектами, хорошо переносится больными. Следует отметить, что у пациентов с острой спондилогенной дорсалгией оптимальный курс лечения L-лизина эсцинатом для достижения стойкого желаемого клинического эффекта составляет 10 дней, что существенно сокращает сроки лечения.
Таким образом, высокая клиническая эффективность, благоприятный профиль безопасности, доступная цена позволяют рассматривать L-лизина эсцинат как препарат выбора для оказания медицинской помощи при широком спектре заболеваний, сопровождающихся отечно-воспалительным синдромом, в т. ч. при неврологических проявлениях поясничного остеохондроза.
L-лизина эсцинат оказывает комплексное воздействие на основные патогенетические признаки первичных спондилогенных дорсалгий, позволяет добиться стойкого обезболивающего эффекта, снизить дозы НПВП, исключая тяжелые побочные реакции, способствует скорейшему выздоровлению пациентов, ранней мобилизации.
 «Роль венозных нарушений у пациентов с дорсопатиями и новые подходы к их терапии»
«Роль венозных нарушений у пациентов с дорсопатиями и новые подходы к их терапии»И.А. Щукин, к.м.н., доцент кафедры неврологии и нейрохирургии ГБОУ ВПО
«РНИМУ им. Н.И. Пирогова»
(Москва)
Термин «остеохондроз» был предложен в 1933 г. немецким ортопедом Хильдебрантом для суммарного обозначения инволюционных изменений в тканях опорно-двигательного аппарата. В 1983 г. казанский невролог Я.Ю. Попелянский дал более четкое определение остеохондроза, отметив, что это полифакториальное дегенеративное заболевание позвоночно-двигательного сегмента, поражающее первично межпозвонковые диски и вторично – другие отделы позвоночника и опорно-двигательного аппарата. В 1983 г. Коган указал, что остеохондроз достигает своего апогея у пациентов относительно молодого и среднего возраста и имеет тенденцию к инволюции в пожилом и старческом возрасте.
Позвоночный двигательный сегмент состоит из 2-х позвонков: верхне- и нижележащего, между которыми находится межпозвонковый диск; целого ряда суставов, в частности фасеточных, которые образуют связь между верхне- и нижележащими позвонками и обеспечивают подвижность позвоночного двигательного сегмента. Далеко не все эти структуры имеют большое количество нервных окончаний, в первую очередь болевых рецепторов. Например, передняя продольная связка практически лишена болевых рецепторов, и если возникает грыжа, которая обращена кпереди, то она практически не беспокоит пациента. Точно такая же ситуация с межпозвонковым диском – если его периферия достаточно богато иннервирована, то центральная часть лишена нервных окончаний, хотя есть работы, в которых показано, что по мере прогрессирования дегенеративно-дистрофических изменений нервные окончания начинают прорастать более глубоко в межпозвонковый диск, что, естественно, будет усугублять болевой синдром при остеохондрозе.
Существует несколько разновидностей боли в спине в зависимости от типа, источника и патофизиологического механизма.
Тип боли зависит от тех тканей, которые страдают в первую очередь: хрящевые, костные, миофасциальные, невральные и сосудистые боли. Источник боли – это те структуры, которые образуют позвоночно-двигательный сегмент. Что касается патофизиологических механизмов, то это и дистрофические процессы, которые начинают прогрессировать в достаточно раннем возрасте, и асептическое воспаление, и дистония, и спазм, если имеется в виду мышечный компонент боли. При изменениях корешка вначале происходит демиелинизация, затем отмечаются аксонопатия, ишемия и венозный застой. Все эти процессы дополняют и усугубляют друг друга. При отсутствии своевременного лечения возникают периферическая, центральная сенситизация, хронизация боли.
Повреждение или воспаление приводит к высвобождению большого количества медиаторов, активирующих (серотонин или брадикинин) или сенситизирующих, т. е. повышающих восприятие того или иного возбуждения (простагландины или лейкотриены), что, в свою очередь, приводит к выбросу достаточно большого количества субстанции Р, увеличивающей капиллярную проницаемость, дегрануляцию тучных клеток и высвобождение целого ряда медиаторов воспаления. Большое количество медиатора гистамина, который высвобождается из тучных клеток, воздействует на эндотелиальные клетки, страдает и артериальное, и венозное русло. Основные составляющие межпозвонкового диска – это пульпозное ядро, которое содержит хорошо гидратированные коллагеновые и эластические волокна (с возрастом гидратация пульпозного ядра уменьшается, процессы дегенерации нарастают); фиброзное кольцо, в котором значительно меньше жидкого содержимого и присутствуют коллагеновые, эластические волокна, и замыкательная пластинка, которая отграничивает диск от тела позвонка.
Этапы формирования грыжи:
– расхождение волокон фиброзного кольца – протрузия диска;
– разрыв фиброзного кольца – экструзия диска;
– разрыв задней продольной связки – секвестрация грыжи.
В позвоночно-двигательном сегменте отток из центральных вен, которые собирают кровь, в т. ч. из спинного мозга и оболочечных вен, в первую очередь происходит через корешковые вены. Корешковое отверстие достаточно невелико, и если в данной области возникает какая-либо патология, то это моментально приводит к нарушению венозного оттока и запускает каскад патологических реакций. Корешковые вены соединяются с расположенными в эпидуральном пространстве внутренними венозными сплетениями, которые несут кровь в более крупные вены.
Патофизиологические механизмы венозных расстройств:
– компрессия (в случае компрессии корешка имеет место и компрессия венозного сосуда);
– ишемия как результат компрессии (возникает со стороны не только венозного, но и артериального русла);
– асептическое воспаление;
– возникновение эндоневрального отека.
В этой ситуации очень важную роль играет гематоневральный барьер – те сосуды, которые отвечают за кровоснабжение периферических нервов. В спинномозговых нервах гематоневральный барьер развит значительно меньше, чем в периферических, и это усугубляет эндоневральный отек как результат снижения капиллярного кровотока. Как только капиллярный кровоток снижается, моментально возникает венозный стаз и развивается фиброз нерва. Вследствие этого сразу снижается порог возбуждения, и это усугубляет боль.
Имеется и механическая причина возникновения боли – корешок в пределах корешкового отверстия должен быть мобилен для обеспечения нормальной подвижности позвоночного столба. Ухудшение мобильности корешка еще больше усугубляет болевой синдром и сосудистые нарушения.
Лечение болевого синдрома преследует 2 основные цели: его купирование и восстановление функций.
Консервативное лечение включает применение НПВП, миорелаксантов (в случае преобладания МТС), витаминов группы В, хондропротекторов (на более поздних хронических стадиях). Среди сосудистых препаратов особая роль принадлежит венотоникам.
Следует сказать, что в настоящее время отсутствуют четкие международные рекомендации по хирургическому лечению при болевом синдроме и, соответственно, не определены показания для него. В разных источниках встречаются различные показания: неэффективность консервативного лечения на протяжении не менее чем 6 мес., стеноз позвоночного канала, сдавление корешков конского хвоста с парезом стоп, наличие анестезии аногенитальной области и тазовые нарушения, наличие секвестрированной грыжи по данным нейровизуализации. Однако есть пациенты с секвестрированной грыжей, которых ничего не беспокоит, и не всегда стоить отправлять их к нейрохирургу. Медикаментозная терапия включает:
– местные анестетики (прокаин, лидокаин и др.);
– НПВП;
– опиаты.
С учетом важности роли сосудистых, в первую очередь венозных, нарушений при дорсопатиях целесообразно назначать те или иные венотоники. Одним из таких препаратов является L-лизина эсцинат.
Механизм действия L-лизина эсцината заключается в:
– уменьшении проницаемости сосудистой стенки;
– улучшении тока жидкости в просвете капилляра;
– ингибировании активности лизосомальных гидролаз и устранении венозного стаза.
Нами было проведено исследование L-лизина эсцината для лечения пациентов с острыми болевыми синдромами в нижней части спины, обусловленными остеохондрозом пояснично-крестцового отдела позвоночника. 60 пациентов были разделены на 2 группы: 1-я группа получала базовую терапию + L-лизина эсцинат в течение 7 дней в/в капельно, 2-я группа – только базовую терапию.
Задачей исследования была оценка эффективности L-лизина эсцината в лечении острого болевого синдрома, его влияния на развитие эмоциональных расстройств и динамики показателей качества жизни.
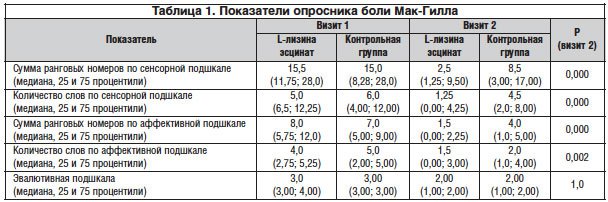
Во время скрининга использовалась ВАШ боли для включения в исследование больных с интенсивной болью (не ниже 5 баллов по оценке пациента). Помимо применения ряда опросников, отражающих различные особенности и характеристики болевого синдрома, оценивалось эмоциональное состояние пациентов, анализировались МТС и корешковый синдром. С этой целью использовались опросник Освестри (анализ влияния боли на различные аспекты жизни); опросник Мак-Гилла (оценка субъективного переживания боли); шкала для оценки эффективности проведенного лечения и качества жизни. На заключительном визите проводились те же обследования.
На визите включения в исследование пациенты основной и контрольной групп по всем характеристикам статистически значимо друг от друга не отличались.
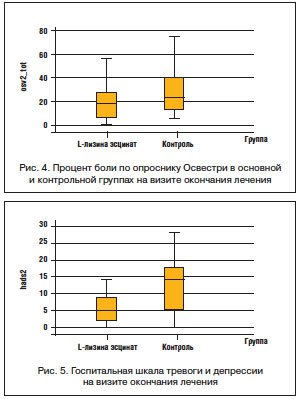
На фоне комплексной терапии, включавшей в основной группе больных L-лизина эсцинат, через 10 дней лечения практически по всем шкалам и опросникам отмечено статистически значимое уменьшение болевого синдрома в обеих группах. Однако при проведении межгруппового анализа на визите окончания лечения в основной группе процент боли по шкале Освестри (рис. 4), балл по сенситивной и аффективной субшкалам опросника Мак-Гилла, были статистически значимо ниже, чем в контроле (табл. 1).
При оценке эмоционального статуса пациентов по госпитальной шкале тревоги и депрессии (рис. 5), на визите окончания лечения также отмечена статистически значимая разница между группами.
Также выявлено, что пациенты, которые получали L–лизина эсцинат, имели более высокий балл по шкале исходов у пациентов с болью в нижней части спины (рис. 6).
Таким образом, использование L-лизина эсцината позволило добиться быстрого и выраженного эффекта у пациентов с болью в нижней части спины. Венотропное действие открывает широкие возможности использования данного препарата при целом ряде нозологий, в генезе которых играет роль венозная недостаточность. Безопасность и быстрота наступления эффекта делают L-лизина эсцинат незаменимым в клинической практике, как неврологов, так и других специалистов.

 «Опыт диагностики и лечения церебральных венозных ангиодистоний»
«Опыт диагностики и лечения церебральных венозных ангиодистоний» Е.Н. Дьяконова, д.м.н., профессор кафедры неврологии и нейрохирургии ИПО ИвГМА (Иваново)
Более 90% работ о сосудистой патологии головного мозга посвящены артериальному кровотоку, хотя в своей клинической практике мы постоянно сталкиваемся с нарушениями деятельности венозной системы. Среди амбулаторных пациентов, которые обратились с жалобами на головную боль, синдром хронической венозной дисциркуляции головного мозга наблюдается в среднем в каждом пятом случае.
Фактором, который осложняет диагностику, является сочетание у одного пациента 2–3 видов головной боли. По нашим данным, у каждого третьего больного с хронической церебральной недостаточностью имеется сочетанная артериально-венозная патология.
Большую роль в мозговом кровообращении играет система микроциркуляции.
Целесообразно вспомнить, что мозг находится в замкнутом пространстве и внутри черепной коробки давление должно быть постоянным. Вещество мозга – это величина неизменная, ликвор вырабатывается с определенной скоростью и имеет относительно постоянную величину (самая непостоянная величина в организме – это кровь). Для того чтобы давление внутри мозговой коробки было нормальным, а перфузия – достаточной, приток крови должен быть сравним с оттоком, в этом случае работа мозга оптимальна.
Существует 3 степени нарушения венозного оттока: легкая, средняя и выраженная.
1-я степень – при исследовании выявляется спазм церебральных артерий, но часто не отмечается наличие затрудненного венозного оттока. Расширяются мозговые вены, сужаются церебральные и магистральные артерии, снижается АД (пациенты-гипотоники). Включается компенсаторный механизм – уменьшается приток крови к мозгу, возникает легкая гипоксия.
2-я степень – расширяются все мозговые сосуды, повышается общее АД, изменяется сердечный ритм – у пациента может появляться тахикардия, изменяется ритм дыхания, ускоряется приток крови к мозгу, усиливается сброс по коллатералям (артериально-венулярные «мостики»), т. е. минуя мозг, из артерии в венулы, при этом количество крови, проходящей через мозг, уменьшено. Компенсация происходит, давление сохраняется, но гипоксия нарастает.
3-я степень – компенсация не происходит, отмечаются нарушения церебральной гемодинамики, расстройство вазомоторной регуляции, гипоксия ствола, ретикулярной формации, нарушаются все виды метаболизма.
На начальном этапе имеются субклинические нарушения, которые диагностируются только с помощью дополнительных методов исследования, при этом пациент астенизирован, предъявляет неспецифические жалобы. Постепенно прогрессируют ишемия, недостаточность кровообращения, развивается оксидантный стресс, и, как следствие, нарастают морфологические нарушения и неврологическая симптоматика.
При классификации церебральных нарушений выделяют церебральные венозные дисгемии, венозные энцефалопатии, кровоизлияния, тромбозы вен головного мозга. Классифицируются по этиологическому фактору: церебральные дистонические дисциркуляторные нарушения при неврозах, первично-сосудистых заболеваниях, травмах, инфекционных, токсических, эндокринных и т. д.
В регуляции венозного оттока ведущую роль играет дыхательная система: при вдохе происходит присасывающее действие грудной клетки, и после выздоровления от бронхита или ОРЗ, сопровождавшегося кашлем, у человека могут возникнуть жалобы на головную боль, т. е. имеют место венозные дисгемические нарушения. Инспирация носом обеспечивает ток крови от решетчатых костей в сагиттальный синус, улучшает мозговое кровообращение. Характерные синдромы: ангиодистонический, астеновегетативный, психопатологический, псевдотуморозный, гипертензионный, мелкоочаговый, инсультообразный. При всех этих состояниях наблюдается цереброастенический синдром.
Венозная дисциркуляция не упоминается в МКБ-10, наиболее подходящей из имеющихся является рубрика G44.1 – сосудистая головная боль. Тупая диффузная головная боль возникает у пациентов после длительного пребывания в горизонтальном положении или при переходе из горизонтального в вертикальное положение, отмечаются также ощущения тяжести, сжимания, распирания, выталкивания глазных яблок. Поскольку венозное и ликворное давление взаимосвязаны, на начальном этапе возникает диффузная головная боль, затем она приобретает характер гипертензивной боли. При кашле, чихании, натуживании, наклонах, чтении головная боль усиливается.
У больных наблюдается цианотичный цвет лица по утрам вследствие затруднения оттока из поверхностных сосудов, отечность лица (может пройти через 2–3 ч или к вечеру, иногда не проходит). В далеко зашедших случаях может отмечаться следующая триада: отечность лица, цианоз кожных покровов, при этом на начальных этапах кожные покровы бледные. Кофе (в частности, натуральный) и чай уменьшают интенсивность головной боли, в то время как алкоголь, особенно пиво, даже в небольших дозах, усиливает головную боль. У молодых людей, злоупотребляющих пивом, имеется нарушенный венозный отток, у них красные и отечные лица из-за расширенных капилляров.
У больных могут быть различные нарушения сна: нарушение засыпания, частые ночные просыпания и, как следствие, некачественный сон. Для больных характерны сонливость днем и повышение работоспособности вечером. Это происходит вследствие того, что в горизонтальном положении затрудняется отток по позвоночно-венозным сплетениям, головная боль усиливается; в вертикальном положении отток лучше. Больные стараются спать на высоких подушках, т. к. при использовании плоских головная боль усиливается. Утром пациентов беспокоят головная боль, заложенность носа из-за дополнительного сброса крови в поверхностные сосуды. При отсутствии насморка отмечаются отечность слизистой в носу, сниженное обоняние и частые носовые кровотечения. Очень часто таких пациентов наблюдают ЛОР-врачи, прижигают им носовые сосуды, а между тем больных с подобными жалобами следует направлять к неврологу.
Встречается антидиуретическая реакция: вследствие нарушения выработки антидиуретического гормона снижается экскреция Na+ и К+ и, как результат, происходит задержка жидкости.
Отмечаются изменения глазного дна (сужение артерии, расширение вен), зрительные нарушения: пелена перед глазами без снижения зрения, мушки, нечеткость контуров; пациенты замечают, что им стало труднее читать. Сразу после начала лечения возникает эффект вынутого стекла – краски воспринимаются ярче. Нарушения слуха как такового нет, но пациенты «недослышат», переспрашивают.
Пациенты лучше переносят холод, плохо чувствуют себя в душных, жарких помещениях, банях. Головная боль появляется или усиливается при контрастном изменении температуры, например, если зайти в жаркое помещение с мороза, через 20 мин это состояние проходит.
Нами было проведено исследование в Доме ребенка, включавшее лежачих детей. Оказалось, что венозная дисгемия влияет на замедление формирования электрогенеза мозга с первых месяцев жизни. К 1 году у этих пациентов выявляются отставание в формировании и доминировании a-ритма, к 2-м годам – задержка психомоторного развития. Поэтому важным фактором, который улучшает прогноз, является вертикализация пациентов.
В исследовании, в котором принимали участие дети от 0 до 12 лет, выявлено, что у пациентов, перенесших перинатальную патологию, имеет место нарушение регуляции, снижена симпатическая реактивность, затруднен венозный отток, нарушена микроциркуляция. Когда ребенок активен, бегает, то у него повышается симпатическая активация, улучшается венозный отток.
Детям при наличии повышенного внутричерепного давления и затруднении венозного оттока рекомендуется применять комбинацию мочегонных препаратов и венотоников.
Определены следующие косвенные УЗИ-признаки венозных нарушений:
– повышение скорости кровотока по прямому синусу;
– ретроградный кровоток по глазным венозным сплетениям;
– кровоток по позвоночным венозным сплетениям.
В медикаментозной терапии церебральных венозных ангиодистоний при наличии признаков повышения ликворного давления проводят дегидратацию (короткий курс), коррекцию венозного оттока, применяют антиоксиданты, антигипоксанты, цитопротекторы, метаболические препараты, нейромедиаторы. Ацетазоламид у данных пациентов следует рекомендовать коротким курсом. Венотоники и ангиопротекторы классифицируют по составу, принадлежности к определенному типу:
Флавоноиды (g-бензопироны): диосмин, гесперидин, гидросмин, троксерутин, экстракт иглицы, кверцетин-глюкуронид и изокверцетин.
Сапонины: эсцин.
Пикногенолы: эндотелон.
Синтетические вещества: трибенозид, кальция добезилат.
Гипоксия приводит к эндотелиальной недостаточности, поражению сосудистой стенки.
Сапонины – это препараты, содержащие экстракт конского каштана; самый известный из них – эсцин. В настоящее время в лечении церебральных венозных ангиодистоний применяется инъекционный препарат растительного происхождения, который оказывает венотоническое действие, – L-лизина эсцинат. Он купирует отек за счет восстановления дренажной функции сосудов из микроциркуляторного русла.
L-лизина эсцинат повышает тонус венозной стенки, закрывает венозные клапаны, улучшает отток крови, нормализует микроциркуляцию. Кроме того, L-лизина эсцинат связывается с липидами, восстанавливает их физико-химические свойства, улучшает и защищает клетку, улучшает отток воды из тканей, что приводит к выраженному противоотечному эффекту. Также препарат выступает в качестве антиоксиданта, противовоспалительного средства, воздействует на перекисное окисление липидов и ингибирует активность фосфолипазы А2, которая начинает действовать при гипоксии.
Имеется опыт применения L-лизина эсцината в нейрохирургии головного мозга, спинальной нейрохирургии.
Мы изучали эффективность L-лизина эсцината как венотоника при церебральных венозных дисгемиях. Исследование проводится в настоящее время, поэтому представить расширенные результаты пока невозможно. В исследование включена группа женщин с выраженными клиническими проявлениями дисциркуляторной венозной дисгемии в сочетании с артериальной гипертензией (скорость кровотока в прямом синусе – до 50 см/с). Пациенткам вводили 5 мл в/в инъекций L-лизина эсцината 100,0 в физрастворе, проводили антигипертензивную терапию. Был получен хороший клинический эффект, отмечена быстрая стабилизация АД.
 «Новые данные о клинике и терапии спондилогенно-венозных радикуломиелоишемий»
«Новые данные о клинике и терапии спондилогенно-венозных радикуломиелоишемий» А.А. Скоромец, академик РАН, д.м.н., профессор, заслуженный деятель науки РФ, заведующий кафедрой нервных болезней ГБОУ ВПО «СПб ГМУ им. И.П. Павлова», главный невролог Санкт-Петербурга
Сосудистые поражения спинного и головного мозга – одна из наиболее актуальных проблем здравоохранения. В 2015 г. будет 115 лет, как наша кафедра занимается изучением сосудистых заболеваний не только головного, но и спинного мозга.
Хороший невролог должен обладать «анатомо-физиологическим зрением», иметь фундаментальные знания. В свое время, готовясь к юбилею наших предшественников, которые заведовали кафедрой, мы перечитали все их труды и поняли, что часть работ, выполненных 150 лет назад, нисколько не устарела. Работы, а также комментарии к ним, подобные труду В.М. Гегелева «Проводящие пути головного и спинного мозга», и через 100 лет будут считаться классикой отечественной неврологии.
Основателем российской невропатологии считается Алексей Яковлевич Кожевников. Его учениками являются С.С. Корсаков, В.К. Рот, Г.И. Россолимо, В.А. Муратов, Т.И. Прибытков, Л.С. Минор, Л.О. Даркшевич, Ф.Г. Рыбаков, С.А. Суханов и др.
После смерти в 1902 г. А.Я. Кожевникова руководителем кафедры стал В.К. Рот (1848–1916). Степень доктора медицины была присвоена ему за монографию о нервно-мышечной патологии. В.К. Рот описал клинику невропатии наружного кожного нерва бедра (болезнь Рота) и симптом «полукуртки» (симптом Рота) при сирингомиелии, изучал апоплексию, двигательные расстройства, хорею, эпилепсию. Его учениками считали себя такие видные неврологи, как М.А. Захарченко, Е.К. Сепп, А.М. Гринштейн, И.Ю. Тарасевич. После ухода В.К. Рота с кафедры ею некоторое время руководил В.А. Муратов, а в 1917 г., после Февральской революции, на заведование кафедрой был избран другой ученик А.Я. Кожевникова – Г.И. Россолимо.
Сегодня для повышения уровня образования молодых специалистов мы проводим ежегодные школы неврологов, очередная школа пройдет 12–15 марта 2015 г.
Говорить изолированно о венозном коллекторе без артериального не совсем верно, это единая система, которая представлена следующим образом: к спинному мозгу кровь поступает от аорты по поперечным крупным артериям, они перпендикулярны, их количество индивидуально у каждого человека. Но чем больше таких артерий («рассыпной тип»), тем незаметнее для спинного мозга проходит выключение из кровотока одной из них. Если 1–2 артерии снабжают спинной мозг, то ишемия очень значительна; и артериальные, и венозные сосуды спинного мозга могут страдать в результате поражения самих подсосудов.
Спинной мозг имеет сильно развитую венозную систему. Вены, дренирующие передние и задние отделы спинного мозга, имеют «водораздел» приблизительно там же, где и артерии. Главные венозные каналы, принимающие кровь вен из вещества спинного мозга, идут в продольном направлении аналогично артериальным стволам. Вверху они соединяются с венами основания черепа, образуя непрерывный венозный тракт. Вены спинного мозга имеют также связь с венозными сплетениями позвоночника, а через них – с венами полостей тела.
Корешковые сосуды проходят через dura mater и несут кровь, как правило, в наружное венозное сплетение, потому что во внутреннем венозном сплетении ундулирующее повышение венозного давления тесно связано с дыхательной системой, и венозная волна на спинной мозг не должна идти в обратную сторону, поэтому природа предусмотрела клапаны, которые находятся в венах корешков.
Венозная система спинного мозга, подобно артериальной, имеет 2 варианта строения: рассыпной и магистральный. Вдоль передней и задней поверхностей спинного мозга располагаются одноименные вены: передняя и задняя. Широко представлена перимедуллярная сосудистая сеть, куда оттекает кровь из интрамедуллярных вен. Далее из перимедуллярной сети кровь оттекает по передним и задним корешковым венам, которые следуют с соответствующими корешками. Число корешковых вен варьирует от 6 до 35. Задние корешковые вены крупнее передних: в 90% случаев имеется большая корешковая вена, которая проходит с первым или вторым поясничным корешком слева, но может входить в канал с одним из корешков от 6-го грудного до 3-го крестцового. Следовательно, вертеброгенные спинальные расстройства венозного кровообращения с компрессией крупной корешковой вены могут развиваться при тех же условиях, что и артериальные радикуломиелопатии и миелопатии.
Чаще всего сдавливается корешковая вена при грыже межпозвонкового поясничного диска. Нередко больные предъявляют лишь жалобы на боль в пояснице проекционного характера, чувство зябкости в ногах. Боли и в пояснице, и в ноге усиливаются в положении лежа, а при легкой разминке имеют тенденцию к уменьшению.
Клиническая картина венозной радикуломиелопатии также отличается рядом особенностей: во-первых, слабость в ногах нарастает постепенно, нередко пациент не может четко указать время развития парезов; во-вторых, при развитии паретических явлений в нижних конечностях у таких больных болевой синдром длительное время не исчезает.
Обязательным для вертеброгенной венозной радикуломиелоишемии является наличие вертебрального синдрома. В пояснично-крестцовом ромбе часто отмечается выраженная венозная сеть – расширенные подкожные вены. Этот симптом в большинстве своем является хорошим подспорьем для диагностики, т. к. свидетельствует о застойных явлениях в эпидуральной венозной сети. Нередко данный признак сочетается с наличием геморроидальных узлов. Походка у этих больных «штампующая» вследствие расстройства глубокой и тактильной чувствительности. Поверхностные же виды чувствительности страдают по сегментарному типу (за счет ишемии задних рогов и роландовой субстанции на протяжении нескольких сегментов). Выявляются пирамидные знаки. Передние рога и функция тазовых органов страдают незначительно.
Практика показывает, что сосудистый фактор имеется почти во всех случаях формирования грыж межпозвонковых дисков, и если его учитывать в лечебных комплексах, то у большинства больных удается добиваться более полного и быстрого регресса неврологического дефицита.
Патогенетическое значение при спондилодискогенных поражениях нервной системы имеют венотонизирующие препараты и средства с противоотечным действием, среди которых наиболее эффективным является L-лизина эсцинат.
L-лизина эсцинат улучшает эластичность вен, повышает тонус венозных сосудов, нормализует реологию крови, стимулирует антитромботическую активность сыворотки, улучшает микроциркуляцию, дозозависимо уменьшает сосудисто-тканевую проницаемость и прохождение плазмолимфатического барьера, уменьшает активность лизосомальных ферментов и препятствует возникновению экссудативной реакции на простагландины, обладает умеренным диуретическим эффектом, благоприятно влияет на трофику тканей.
Кроме того, компоненты препарата снижают воспалительный ответ организма и оказывают выраженный обезболивающий эффект, особенно при болях травматического генеза.
Проведенное нами исследование, в которое были включены 80 пациентов, показало, что под влиянием L–лизина эсцината у пациентов быстро и значительно уменьшаются корешковые боли, парестезии в ногах, нарушенная вибрационная чувствительность, улучшается мышечная сила в ногах, нормализуется походка, быстрее восстанавливаются глубокие рефлексы, функции сфинктеров органов малого таза.
По дизайну это было рандомизированное сопоставимое исследование со следующими критериями включения:
1. Мужчины и женщины в возрасте от 30 до 60 лет.
2. Наличие грыжи одного или нескольких поясничных межпозвонковых дисков, подтвержденное данными МРТ или КТ.
3. Наличие характерных для венозного застоя в поясничном канале позвоночника признаков: расширение корешковых вен конского хвоста, расширение эпидуральных вен (внутреннего позвоночного венозного сплетения) – на поперечных томограммах позвоночника изменения тел позвонков в виде расширения центральной вены тела позвонка, очаги жировой дегенерации и/или склерозирования тела одного или нескольких поясничных позвонков, визуализация крупной корешковой вены на продольных томограммах, расширение подкожных вен в люмбосакральном ромбе (Михаэлиса – у женщин).
4. Наличие характерных симптомов в виде боли в пояснице и тазовом поясе после ночного сна и длительного пребывания в постели, потребность расхаживаться, усиление боли при тепловых процедурах, онемения в ногах, неуверенность при ходьбе, учащенное мочеиспускание.
5. Наличие характерных признаков нарушения функции сегментарного аппарата нижней половины спинного мозга и его корешков: диффузная слабость миотомов, больше в проксимальных отделах нижних конечностей. Снижение глубоких рефлексов (коленных, ахилловых, с длинного разгибателя большого пальца стопы, с двуглавой мышцы бедра). Нарушения болевой, температурной и тактильной чувствительности по корешковому или сегментарному типу (часто пятнистое). Укорочение или отсутствие вибрационной чувствительности на лодыжках голеней. Черты сенситивной атаксии в ногах, иногда инвертированный синдром Броун-Секара (т. е. проводниковые двигательные и псевдопроводниковые спинальные расстройства на одной нижней конечности). Умеренные нарушения функции тазовых органов.
6. Наличие вертебрального синдрома: сглаженность лордоза, ограничение подвижности поясничного отдела позвоночника (по измерению длины подвижности выпрямленных пальцев кисти при их скольжении по бедру при наклонах в стороны). Признаки натяжения спинномозговых корешков – Нери, Ласега, Вассермана.
Все пациенты были разделены на две группы по 40 человек. В первую, контрольную, группу вошли пациенты, которым проводилось общепринятое медикаментозное лечение и физиопроцедуры, в т. ч., массаж мышц спины и нижних конечностей. Во вторую, основную, группу вошли также 40 пациентов, которым наряду с вышеуказанным комплексом лечения вводили препарат L-лизина эсцинат 0,1% р-р 5 мл на 15 мл 0,9% раствора натрия хлорида внутривенно струйно 1 р./сут в течение 10 дней.
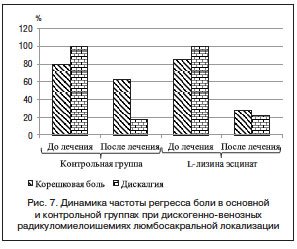
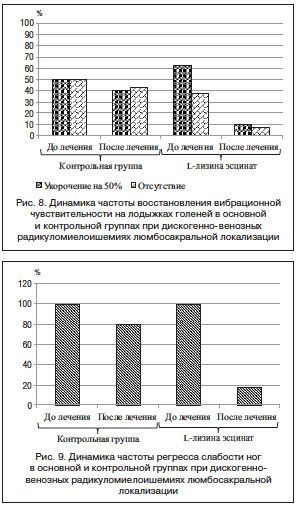
Из рис. 7–9 видно, что под влиянием препарата L–лизина эсцинат (у пациентов основной группы) значительно регрессировали такие неврологические симптомы и признаки как корешковые боли, заднеканатиковые парестезии в ногах, вибрационная чувствительность, улучшилась мышечная сила в ногах, нормализовалась походка.
Исследование показало, что применение L-лизина эсцината позволяет сократить сроки лечения в стационаре и значительно улучшить качество жизни пациентов. Полученные данные позволяют рекомендовать L-лизина эсцинат в моно- или комплексной терапии дискогенно-венозных радикуломиелоишемий пояснично-крестцовой локализации. Применение препарата L-лизина эсцината позволяет уменьшить выраженность болевых ощущений в тазовом поясе, улучшить мышечную силу в ногах, что позволяет расширить двигательную активность, нормализовать функцию тазовых органов, сократить сроки лечения в стационаре и значительно улучшить качество жизни пациента.