Мигрень — это хроническое заболевание нервной системы с периодически повторяющимися пароксизмальными состояниями в виде приступов интенсивной головной боли пульсирующего характера, локализующейся преимущественно в одной половине головы, в основном в глазнично-лобно-височной области, и сопровождающейся тошнотой, рвотой, фото- и фонофобией, а также сонливостью и вялостью после приступа.
Мигрень является первичной головной болью, второй по частоте после головной боли напряжения. Распространенность мигрени в популяции составляет в среднем 10–15%, она поражает преимущественно молодых людей трудоспособного возраста [19]. По данным статистики, только один человек из пяти не перенес ни одного приступа мигрени в своей жизни. Женщины страдают мигренью примерно в 3 раза чаще, чем мужчины, при этом в репродуктивном возрасте (от 30 до 49 лет) распространенность заболевания у них достигает 27%. Около 2/3 пациентов испытывают во время мигренозной атаки сильную и очень сильную боль, что вызывает нарушение трудоспособности и значительно снижает качество жизни в целом [10]. Диагностика и лечение мигрени связаны с огромными финансовыми расходами, и это также определяет значимость правильных подходов и использование современных эффективных средств для ее лечения.
Патогенез мигрени
Мигрень реализуется при генетической предрасположенности и определенных условиях окружающей среды, действующих постоянно либо на протяжении продолжительного периода. Помимо предрасположенности для развития каждой атаки мигрени необходимо воздействие 1 или нескольких запускающих факторов (триггеров). Это могут быть эндогенные (например, гормональные колебания) или экзогенные (определенные продукты питания, алкоголь, метеофакторы и др.) влияния.
Согласно современным представлениям, развитие мигрени связано с активацией ряда структур ствола мозга: голубого пятна в варолиевом мосту, околоводопроводного серого вещества и заднего ядра шва. Активация перечисленных структур приводит к деполяризации корковых нейронов с последующим угнетением их активности. Этот процесс (распространяющаяся депрессия Leo) начинается в затылочной коре и распространяется вперед на соматосенсорную, что вызывает зрительные, чувствительные и двигательные симптомы мигренозной ауры. Возникновение мигренозной боли связано с активацией тригемино-васкулярной системы. Афферентные волокна тройничного нерва иннервируют крупные церебральные сосуды и твердую мозговую оболочку. Афферентная ноцицептивная информация поступает в nucleus caudalis тройничного нерва в стволе мозга. Активация тригемино-васкулярной системы стимулирует выделение воспалительных нейропептидов в окончаниях тройничного нерва на сосудах твердой мозговой оболочки. Следствие этого – расширение сосудов, увеличение проницаемости сосудистой стенки и проникновение алгогенных веществ плазмы крови в околососудистое пространство с формированием нейрогенного воспаления, с чем и связано чувство боли при мигрени.
Мигрень неизлечима в силу своей наследственной природы [13], поэтому основной целью ее лечения является поддержание высокого качества жизни пациента. Крайне важно для эффективного лечения мигрени провести дифференциальную диагностику и установить правильный диагноз.
Диагностика и дифференциальный диагноз
Для мигрени характерны повторяющиеся приступообразные эпизоды головной боли продолжительностью от 4 ч до 3 дней. Частота приступов может колебаться от 1 случая в год до 2 раз в неделю. Обычно приступы носят стереотипный характер (похожи один на другой), сохраняющийся в течение продолжительного времени (несколько месяцев, лет). Как правило, это головная боль от умеренной до выраженной интенсивности (от 5 до 10 баллов по визуально-аналоговой шкале), пульсирующая, чаще односторонняя в области виска, сопровождающаяся тошнотой, иногда рвотой. Спровоцировать или усилить головную боль могут шум, громкая речь, музыка (фонофобия), солнце, яркий электрический свет, свечение экрана телевизора и монитора (фотофобия), а также резкие запахи (осмофобия). Обычная физическая нагрузка, такая как ходьба, подъем по лестнице, могут усиливать проявления мигрени. Во время приступа пациенту трудно сосредоточиться и выполнять умственную работу.
Большинство пациентов с мигренью имеют исключительно приступы мигрени без ауры. У некоторых пациентов мигрень с аурой и мигрень без ауры могут сочетаться, т. е. иногда возникают приступы мигрени с аурой, в других случаях – без ауры. В более редких случаях аура предшествует каждому приступу мигрени. Аура — это комплекс неврологических симптомов: зрительные (вспышки света, светящиеся линии), чувствительные (онемение) или двигательные (слабость в руке) нарушения, возникающие непосредственно перед или в самом начале мигренозной головной боли.
Диагноз мигрени ставится исключительно на основании анамнеза. Неврологические знаки могут быть обнаружены при осмотре пациента с мигренью с аурой только во время приступа. Осмотр проводится для исключения других заболеваний, сопровождающихся головной болью и представляющих опасность для жизни (опухоль, инфекция, сосудистое поражение и др.). Признаки, на которые следует обратить внимание при сборе анамнеза и осмотре пациента (сигналы опасности — «красные флаги») [5]:
• изменение характера головной боли у данного пациента должно настораживать врача в отношении жизнеугрожающего заболевания;
• новая головная боль (т. е. впервые возникшая) у пациента в возрасте старше 50 лет или у ребенка в препубертатном периоде может быть симптомом височного артериита или внутричерепной опухоли;
• новая головная боль (т. е. впервые возникшая) у пациента с указанием в анамнезе на онкологические заболевания, ВИЧ-инфекцию или иммунодефицитное состояние может указывать на вторичный характер головной боли;
• прогрессирующая головная боль — постепенно ухудшающаяся (без ремиссий) в течение нескольких недель или более — может указывать на объемный процесс в мозге;
• головная боль по типу «раската грома» (интенсивная с «взрывным» или внезапным началом) позволяет заподозрить субарахноидальное кровоизлияние;
• головная боль, сопровождающаяся очаговыми неврологическими нарушениями или непонятными физическими симптомами;
• головная боль усугубляется изменением позы или движениями, которые повышают внутричерепное давление, что может свидетельствовать о внутричерепной опухоли;
• лихорадка, не имеющая других причин и сопровождающаяся головной болью;
• головная боль с необычной аурой, например, головная боль с аурой продолжительностью более 1 ч или сопровождающаяся слабостью при движениях;
• аура без головной боли при отсутствии в анамнезе мигрени с аурой;
• аура возникает у пациентки впервые во время использования комбинированных оральных контрацептивов.
При выявлении «красных флагов» необходимо направить пациента на консультацию к неврологу или другому специалисту узкого профиля (в зависимости от характера выявленных сигналов опасности) для дополнительного обследования.
Лечение мигрени
Лечение мигрени комплексное и включает в себя нелекарственные воздействия (рекомендации по изменению образа жизни, применение нелекарственных средств и приспособлений), а также фармакологическое лечение, направленное на предотвращение и купирование приступов мигрени. Необходимым условием эффективности лечения является сотрудничество врача и пациента с активным участием последнего. Пациент при появлении у него интенсивной головной боли с тошнотой и рвотой обычно испытывает серьезное беспокойство по поводу своего здоровья, предполагая, что страдает каким-либо опасным для жизни заболеванием (опухоль, инсульт и др.). Поэтому важнейшей задачей врача при подтверждении диагноза мигрени является объяснение природы и благоприятного прогноза этого заболевания. Такая беседа способствует снятию дистресса, нормализации психического состояния больного и имеет важное значение для успеха будущего лечения. В то же время необходимо рассказать пациенту о генетической предрасположенности и нейрохимических изменениях в головном мозге при мигрени, методах лечения, принципах профилактики и купирования приступов, дать рекомендации по изменению образа жизни, контролю триггеров. Пациент должен понимать суть своего заболевания и знать, как предотвращать и купировать приступ, чтобы поддерживать высокое качество жизни [5].
В течение первых 2–3 мес. (на период обследования и лечения) пациенту рекомендуется вести дневник или календарь головной боли. В нем необходимо регистрировать частоту, интенсивность, длительность головной боли, сопутствующие симптомы, используемые лекарственные средства, день менструального цикла, а также отмечать провоцирующие факторы. Дневник в процессе лечения может наглядно и достоверно демонстрировать его эффективность, и это в значительной степени повысит приверженность пациента терапии, при этом лечащий врач также будет получать объективную информацию [15].
Купирование приступа мигрени
Наиболее эффективным на сегодня способом купирования острых приступов мигрени является медикаментозная терапия. При этом используют препараты как с неспецифическим, так и со специфическим механизмом действия. Препараты с неспецифическим механизмом действия — анальгетики и нестероидные противовоспалительные средства (НПВС), которые способны уменьшать болевой синдром при любой боли, обусловленной травмой или воспалением. Лекарственные средства со специфическим механизмом действия эффективны только при мигренозной головной боли. Они воздействуют на серотониновые 5-НТ1-рецепторы, локализованные как в ядре тройничного нерва, так и в его окончаниях, и препятствуют выделению болевых нейропептидов. Кроме того, данные препараты влияют на 5–НТ1-рецепторы в сосудистой стенке, сужают расширенные во время мигренозного приступа сосуды мозговых оболочек и прерывают приступ. Таким образом, специфические антимигренозные средства способны воздействовать на патогенетические механизмы мигренозной атаки, что и объясняет их высокую эффективность [4].
При выборе препарата для купирования приступа необходимо учитывать интенсивность и длительность самого приступа, сопровождающих симптомов, наличие сопутствующих заболеваний, прошлый опыт применения препаратов, наконец, их стоимость. Большое значение имеет анализ сопутствующих мигрени заболеваний. С одной стороны, коморбидные нарушения наряду с основным заболеванием могут существенным образом влиять на качество жизни пациента. С другой стороны, такие нарушения могут определять показания или предпочтения, а также противопоказания при выборе тех или иных препаратов и путей их введения. Например, наличие во время приступа выраженной тошноты и рвоты определяет внеоральный путь введения лекарственных препаратов — в виде спрея, в свечах или инъекциях. Наличие у пациента кардиоваскулярных нарушений, особенно лабильной артериальной гипертензии, стенокардии или ишемической болезни сердца, является противопоказанием для использования триптанов и препаратов эрготамина [7].
Существуют два методических подхода к выбору препарата: ступенчатый и стратифицированный [1]. При ступенчатом подходе лечение начинают с назначения ацетилсалициловой кислоты (АСК) и других НПВС. Если имеются противопоказания к вышеперечисленным препаратам, применяется парацетамол. Если такое лечение не было эффективным, или препараты перестали быть эффективными через какое-то время, то переходят к лечению комбинированными анальгетиками. При неэффективности этих препаратов назначается специфическое противомигренозное лечение с использованием как селективных агонистов 5-НТ1-рецепторов — триптанов, так и неселективных агонистов 5-НТ1-рецепторов — препаратов эрготамина. Следует отметить, что частое и длительное использование анальгетиков и особенно комбинированных препаратов чревато развитием привыкания и формированием анальгетической зависимости, что приводит к хронификации болевого синдрома и трансформации мигрени в хроническую форму, кроме того, имеется риск развития абузусной головной боли.
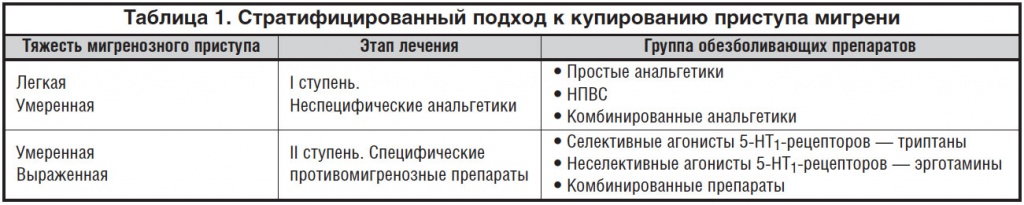
Другой подход к купированию мигренозного приступа — стратифицированный — основан на оценке тяжести приступа с анализом интенсивности боли и степени нарушения трудоспособности (табл. 1). Неспецифическое лечение является эффективным в большинстве случаев мигрени легкой и умеренной степени выраженности (особенно если пациент никогда раньше не принимал никаких лекарственных препаратов для лечения мигрени). Пациентам с тяжелыми приступами лечение сразу следует начинать с препаратов более высокого уровня — например, триптанов. Это позволит во многих случаях избежать вызова скорой помощи, быстро восстановить трудоспособность и повысить уровень самоконтроля у пациента, уменьшить чувство страха и беспомощности перед очередной атакой [16]. Оценку тяжести заболевания можно проводить с помощью специального опросника MIDAS (англ. Migraine Disability Assessment Questionnare). При невозможности использовать MIDAS наиболее простым методом определения тяжести приступов является вопрос: «Что Вы можете делать во время приступа головной боли?». Если пациент отвечает, что головная боль приковывает его к кровати, он вынужден лежать, а любое движение головой вызывает резкое усиление боли, а также нередко тошноту и рвоту, то это свидетельствует о наличии выраженной боли и пациенту необходимо назначать препараты второй ступени. Пациенты с затяжными тяжелыми приступами, мигренозным статусом нуждаются в госпитализации и проведении лечения в условиях неврологического стационара или реанимации.
Несмотря на то, что в настоящее время триптаны считаются «золотым стандартом» купирования приступа, около 30% пациентов с мигренью не отвечают на терапию триптанами [12]. Это может быть связано с низкой и непостоянной абсорбцией, поздним приемом препарата или приемом неполной дозы, а также с индивидуальной нечувствительностью к конкретному триптану. В связи с этим, а также с учетом возможных противопоказаний к назначению триптанов у некоторых пациентов остается актуальным применение во время приступа неспецифических анальгетиков и в первую очередь, конечно, НПВС.
Место НПВС в лечении мигрени
НПВС являются наиболее широко распространенным классом фармакологических препаратов, которые используются пациентами для облегчения мигренозной боли. Они просты в дозировке и применении, их можно приобрести в аптеке без рецепта врача, и они достаточно эффективны, что показывает многолетний опыт их применения. Международные европейские рекомендации называют НПВС средствами выбора для купирования приступов мигрени слабой и средней интенсивности [2, 13].
Антимигренозная активность НПВС обусловлена несколькими механизмами. Прежде всего препараты этой группы блокируют синтез простагландинов из арахидоновой кислоты, которая наряду с другими провоспалительными агентами участвует в развитии вазодилатации и нейрогенного воспаления. Эти два фактора, как известно, играют ключевую роль в сенситизации болевых рецепторов к нормальным механическим и химическим стимулам и в снижении порогов восприятия боли. Наряду с периферическими НПВС имеются и центральные механизмы действия при мигрени, которые связаны с ингибированием синтеза простагландинов в центральной нервной системе, усилением высвобождения норадреналина и активацией нисходящей серотонинергической системы [11]. Кроме того, НПВС ингибируют тромбоцитарную циклооксигеназу с последующим подавлением образования тромбоксана А2, потенциального агента агрегации, что может иметь значение для профилактической терапии мигрени [9, 21].
АСК, которая применяется для лечения боли уже более 100 лет, в настоящее время используется для лечения приступов мигрени слабой и умеренной интенсивности в дозе 1000 мг. Однако для нее характерен весь спектр побочных эффектов, возможных при применении НПВС. Парацетамол по своей болеутоляющей активности не уступает АСК, однако при мигрени его эффективность ниже, чем у АСК. Это связано с отсутствием у парацетамола противовоспалительного действия, а асептическое нейрогенное воспаление твердой мозговой оболочки имеет ключевое значение в формировании болевого синдрома при мигрени. Препарат малотоксичен и практически не обладает ульцерогенной активностью.
Анальгетическая активность многих НПВС в отношении воспаленной ткани не уступает активности наркотических анальгетиков [6]. Одним из самых эффективных НПВС является диклофенак. В проведенном плацебо-контролируемом исследовании было показано, что эффективность калиевой соли диклофенака в виде саше (50 и 100 мг) при купировании мигрени сопоставима с эффективностью суматриптана (100 мг) [20]. Такие препараты, как ибупрофен, напроксен, кетопрофен, кеторолак хорошо всасываются при приеме внутрь. Среди них кеторолак обладает самой выраженной анальгезией, однако при длительном его применении возрастает вероятность нарушений функции печени и/или почек, а также тромбоцитопении и анемии [17].
При назначении пациенту НПВС необходимо не забывать о возможных побочных эффектах. Негативное воздействие НПВС затрагивает преимущественно органы пищеварения, в которых при этом нарушается выработка веществ, защищающих слизистую оболочку от повреждения и способствующих ее регенерации (заживлению). Недостаток этих веществ ведет к развитию воспалительного процесса в слизистой желудка и двенадцатиперстной кишки и ее повреждению с формированием эрозий и язв. Это так называемая НПВС-гастропатия, чреватая внезапным развитием тяжелых, нередко угрожающих жизни больного желудочно-кишечных кровотечений. В связи с этим НПВС противопоказаны при язвенной болезни желудка и двенадцатиперстной кишки, гастроэзофагеальном рефлюксе и других заболеваниях желудочно-кишечного тракта (ЖКТ). НПВС-гастропатия встречается чаще при использовании кеторолака, реже – при применении ибупрофена.
При использовании НПВС риск злоупотребления ими и развития абузусной головной боли значительно меньше, чем при использовании комбинированных анальгетиков. В отличие от опиат-/опиоид-содержащих и барбитурат-содержащих комбинированных анальгетиков НПВС не вызывают учащения и усиления приступов мигрени [8]. НПВС доступны в различных лекарственных формах (быстрорастворимые таблетки и саше, свечи, инъекции), следовательно, могут использоваться даже при нарушении моторики ЖКТ и сильной рвоте. Для усиления всасывания НПВС можно принимать их вместе с противорвотными средствами (метоклопрамид, домперидон) или кофеином [9].
В ходе исследований было выяснено, что эффективность различных лекарственных средств для купирования мигрени зависит от того, в какую фазу приступа был принят препарат. Наибольшая эффективность НПВС отмечена в том случае, если они принимаются в продромальном периоде или во время ауры [17]. В последнее время активно обсуждаются и изучаются возможность и целесообразность комбинированного использования НПВС и триптана для лечения мигрени. Прием НПВС вместе с триптанами потенцирует, усиливает действие обоих препаратов. Результаты проведенного в 2005 г. исследования показали, что фиксированная комбинация суматриптана (50 мг) и напроксена натрия (500 мг) более эффективна при купировании приступа мигрени, чем монотерапия этими препаратами [18]. Преимущество комбинации триптана и НПВС, вероятно, обусловлено комплексным воздействием этих препаратов на различные механизмы патогенеза мигрени, а также различиями в фармакокинетике этих классов препаратов. Целесообразно применение НПВС в фазу ауры, когда триптаны не рекомендованы, или раннее совместное применение у пациентов с тяжелым течением мигрени. Благодаря комбинированному применению НПВС и триптана удается ускорить время наступления анальгезии, а также предупредить рецидив мигрени [3].
В заключение хочется еще раз обратить внимание на то, что хотя правильный подбор лекарственных препаратов очень важен, решающее значение для успеха терапии мигрени имеет умение врача построить диалог с пациентом и правильно сформировать его ожидания. Только комплексное лечение, включающее рекомендации по изменению образа жизни, нелекарственные средства и медикаментозную терапию, позволит добиться максимального эффекта и повысить качество жизни пациентов.












