ОА считается мультифакториальным и полиэтиологическим заболеванием. К основным факторам риска его возникновения относят [2]:
– пожилой возраст;
– женский пол;
– избыточные физические нагрузки;
– избыточный вес;
– перенесенные травмы;
– гормональную заместительную терапию;
– дефицит витамина D;
– курение.
Выделяют первичный (идиопатический) ОА с неясной этиологией и вторичный ОА, возникающий на фоне различных эндокринных, метаболических, воспалительных заболеваний, например, ревматоидного артрита или системной красной волчанки. Разделение это весьма условно.
Наиболее часто ОА поражает коленные, тазобедренные суставы и суставы больших пальцев ног, реже – голеностопные и дистальные межфаланговые суставы пальцев рук, хотя может развиваться в любых костно-суставных структурах. Основные клинические проявления ОА:
– боль при движении;
– напряжение окружающих мышц;
– отечность в области сустава;
– хруст в суставе;
– деформация сустава;
– ограничение подвижности и функциональная недостаточность сустава [3].
Боль обычно возникает при движении и утихает в покое, но по мере развития патологического процесса она усиливается, персистирует в течение всего дня, появляется в ночные часы. Для ОА характерны: грубый хруст при движении в пораженном суставе (трение разрушающихся суставных поверхностей) и утренняя скованность. По мере прогрессирования заболевания суставная щель уменьшается, разрастаются остеофиты, окружающие сустав мышцы из-за боли находятся в постоянном напряжении. Все это приводит к прогрессирующему снижению амплитуды движений в суставе. Из-за деформации костей, сочленяющих сустав, разрастания остеофитов и скопления внутрисуставной жидкости (синовит) форма сустава изменяется. Искривленные места могут принимать странные очертания «лебединой шеи», «пуговичной петли» и др. В результате прогрессирования ОА сустав разрушается, формируется анкилоз – полная неподвижность.
Структурные изменения при ОА принято подразделять на 4 рентгенологических стадии (классификация ОА по Kellgren – Lawrence) [4]:
I стадия (сомнительный ОА) – сомнительное сужение суставной щели, возможны остеофиты.
II стадия (мягкий ОА) – определенные остеофиты и сомнительное сужение суставной щели.
III стадия (умеренный ОА) – умеренные остеофиты, определенное сужение суставного пространства, возможная деформация костей.
IV стадия (тяжелый ОА) – большие остеофиты, сужение суставного пространства, тяжелый остеосклероз, определенная деформация костей.
Несмотря на широкую распространенность заболевания, его патофизиологические механизмы изучены еще далеко не достаточно. Несомненно, что в его развитии принимает участие целый ряд факторов, взаимодействующих между собой на биохимическом и механическом уровнях [5].
Известно, что основным компонентом сустава, подвергающимся дегенерации при ОА, является хрящ, также страдают субхондральные, капсульные, синовиальные и околосуставные структуры [6, 7]. Суставной хрящ состоит из матрикса и погруженных в него хондроцитов. В хондроцитах происходят главные патологические процессы, приводящие к разрушению хряща: чрезмерное местное высвобождение протеолитических ферментов и прогрессивное замедление репарации хряща. Это приводит к дисбалансу между синтезом и деградацией внеклеточного матрикса [1]. Матрикс содержит 2 главные макромолекулы: гликозамины (протеогликаны) и коллаген. При деградации матрикса идет потеря гликозаминов, сопротивление матрикса хряща воздействию физической нагрузки уменьшается, и поверхность хряща становится чувствительной к повреждению. Кроме того, на хондральном уровне синтезируется широкий спектр биоактивных молекул: провоспалительные цитокины, свободные радикалы, фактор роста, простагландин Е2, лейкотриен B4 [8]. Этот воспалительный компонент усиливает дегенеративные механизмы. Воспаление развивается в первую очередь в синовиальной оболочке. Оно приводит к нарушению фильтрации через мембрану гиалуроновой кислоты (строительного материала хряща), ее вымыванию из полости сустава и прогрессированию дегенерации хряща.
Таким образом, к патофизиологическим механизмам развития ОА относят не только механическое поражение сустава и дегенеративный процесс, но и сопутствующее хроническое воспаление, способствующее разрушению гиалинового хряща [8]. В патологический процесс вовлекаются не только хрящевые структуры, но и все компоненты сустава [9], а также структуры ЦНС, связанные с формированием хронического болевого синдрома.
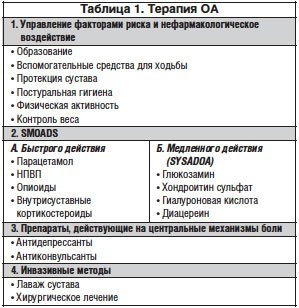
Таким образом, ведущими направлениями патогенетического лечения остеохондроза являются: модуляция воспаления, регуляция метаболизма хондроцитов и стимуляция синтеза хряща [10]. Уменьшение болевого синдрома – еще один не менее важный аспект терапии, поскольку подавляющее число больных ОА страдают от хронических болей. В таблице 1 обобщены методы лечения пациентов с ОА.
Существуют 3 главных принципа терапии ОА:
– уменьшение болей;
– снятие воспаления;
– замедление дальнейшей дегенерации хрящевой ткани [10].
Препараты, применяемые для этих целей, принято называть симптом-модифицирующими (SMOADS) [12]. Существуют 2 основные группы SMOADS:
1. Быстродействующие препараты, включая анальгетики, нестероидные противовоспалительные препараты (НПВП), внутрисуставные глюкокортикоиды и опиоиды.
2. Медленнодействующие препараты или SYSADOA (Symptomatic Slow Acting Drugs for Osteoarthritis).
В 1-й группе препаратами выбора считаются парацетамол и НПВП [12]. Опиоиды и внутрисуставные глюкокортикоиды применяются только в ситуациях, когда препараты первой линии неэффективны.
НПВП широко используются в клинической практике, т. к. оказывают сразу и анальгетический, и противовоспалительный эффекты: снимают боль, отек и гиперемию. Их применение целесообразно в период обострения, поскольку в основе острых болей при ОА лежит воспаление. Недостатком НПВП является ряд побочных эффектов со стороны ЖКТ, а также органов кроветворения и почек. К примеру, применение НПВП в 3–5 раз повышает риск развития таких осложнений, как перфорация пептической язвы, обструкция и кровотечение [11].
Как известно, действие НПВП основано на снижении синтеза простагландинов из арахидоновой кислоты посредством ингибирования фермента циклооксигеназы (ЦОГ). ЦОГ существует в 2 формах: ЦОГ-1, постоянно присутствующая во всех тканях, и ЦОГ-2, синтезирующаяся на фоне воспаления. Большинство НПВП и ненаркотических анальгетиков ингибируют оба вида ЦОГ. Блокирование ЦОГ-1 обусловливает основные побочные эффекты, среди которых на первом месте стоит поражение ЖКТ на всем его протяжении (стоматит, эзофагит, гастрит, язвы желудка и двенадцатиперстной кишки, энтерит, колит, проктит), с возможностью развития кровотечений. Поэтому предпочтение обычно отдается группе НПВП селективного действия (целекоксиб, валдекоксиб, нимесулид, мелоксикам). Считается, что эта группа оказывает менее выраженное действие на ЖКТ [16]. Но не следует забывать, что постоянное применение селективных НПВП имеет свои недостатки. Наиболее неприятным является повышение риска сердечно-сосудистых осложнений (усиление гипертонии и сердечно-сосудистой недостаточности), что особенно касается пожилых пациентов с соответствующей сопутствующей патологией [12].
В 2012 г. были опубликованы результаты метаанализа 28 исследований, проведенных в период 1980–2011 гг. Целью данного анализа была оценка суммарных относительных рисков (ОР) осложнений со стороны верхних отделов ЖКТ при применении различных НПВП, включая селективные ингибиторы ЦОГ-2. Было проанализировано 16 наиболее часто применяемых НПВП. Результаты метаанализа подтвердили вариабельность ОР у разных НПВП. Самый низкий ОР наблюдался у ацеклофенака, целекоксиба и ибупрофена, а наибольший – у пироксикама, кеторолака и азапропазона. Промежуточный ОР, в диапазоне от 2 до 4, наблюдался у остальных НПВП (рофекоксиб, сулиндак, диклофенак, мелоксикам, нимесулид, кетопрофен, теноксикам, напроксен, индометацин и дифлунисал). Отдельно анализировались результаты по кровотечениям из верхних отделов ЖКТ для 8 различных НПВП, оказалось, что наименьший ОР также имеют целекоксиб, ацеклофенак и ибупрофен. Применение НПВП в высокой дозе повышало ОР ЖКТ осложнений примерно в 2–3 раза по сравнению с применением того же препарата в низкой или средней дозе. По результатам проведенного метаанализа ацеклофенак, целекоксиб и ибупрофен (комбинация анальгетический и противовоспалительных доз) попали в группу НПВП с наименьшим ОР [11].
По мере хронизации боли применение НПВП становится все менее эффективным, т. к. в процессе формирования боли начинают преобладать центральные патофизиологические механизмы. Центральная боль плохо поддается воздействию ненаркотических анальгетиков и НПВП, поэтому пациентам с хроническим болевым синдромом рекомендуется дополнительно назначать антидепрессанты (дулоксетин) и антиконвульсанты (габапентин, прегабалин) [13].
Терапия ОА – длительный, практически пожизненный процесс, и особое внимание следует уделять не только эффективности купирования болевого синдрома, но и безопасности применения препаратов [14]. Другим важным моментом является предотвращение дальнейшего развития заболевания, принятие мер, направленных на восстановление структурного и функционального повреждения. Препараты SYSADOA сочетают в себе все нужные качества для длительного восстановительного лечения. Вне обострения рекомендуется монотерапия SYSADOA. При обострении процесса и выраженном болевом синдроме рекомендуется комбинирование SYSADOA с НПВП, т. к. анальгетическое действие последних развивается гораздо быстрее. Совместное применение позволяет снизить дозу НПВП и тем самым предотвратить ряд нежелательных побочных эффектов.
Препараты группы SYSADOA – это биологически активные (хондромодулирующие, хондропротективные) вещества, состоящие из компонентов хрящевой ткани, необходимых для построения и обновления суставного хряща. К ним относятся предшественники хрящевого матрикса (глюкозамин, хондроитин сульфат и гиалуроновая кислота) и модуляторы цитокинов (диацереин и ингибиторы металлопротеаз). Накоплена достаточная доказательная база, свидетельствующая об эффективности SYSADOA и необходимости их применения в плане долгосрочного лечения и профилактики развития ОА. Они способны влиять на метаболизм костной и хрящевой ткани и стимулировать ее регенерацию. Препараты данной группы обладают умеренным обезболивающим и противовоспалительным действием и лишены характерных для НПВП побочных эффектов, поскольку механизм их действия не связан с подавлением синтеза простагландинов и блокированием ЦОГ, а основан на угнетении ядерного фактора kВ, стимулирующего распад хрящевой ткани в организме. Эффективность и безопасность применения препаратов группы SYSADOA доказаны в ряде исследований у пациентов с ОА и другими воспалительно-дегенеративными заболеваниями [14].
На сегодняшний день лидером среди хондропротекторов является комбинированный препарат Терафлекс. Преимущество Терафлекса заключается в сочетании 2-х активных ингредиентов: хондроитина сульфата и глюкозамина в эффективных дозировках.
Хондроитин сульфат и глюкозамин, как уже говорилось, существуют в организме человека и являются естественными хондропротекторами. Хондроитин сульфат вырабатывается хрящевой тканью суставов и входит в состав суставной жидкости. Он способствует отложению кальция в костях и регенерации хряща, укрепляет соединительнотканные структуры хряща, сухожилий, связок, кожи. Сохраняя воду в толще хряща, он повышает прочность соединительной ткани. Именно хондроитин ингибирует специфические ферменты, разрушающие соединительную ткань. Глюкозамин – необходимый компонент хондроитин сульфата, его недостаточность ухудшает качество синовиальной жидкости и может вызвать хруст в суставах [15]. С возрастом, в результате нейродегенеративных процессов, естественный синтез этих веществ снижается, их восполнение возможно при применении Терафлекса.
Терафлекс замедляет процессы естественного (профилактика) и патологического (терапия артроза) разрушения хрящевой ткани. Препарат улучшает внутреннюю структуру хондроцитов и активирует их деятельность. Механизм его действия связан с:
– активацией синтеза протеогликанов;
– угнетением действия ферментов, разрушающих гиалиновый хрящ;
– увеличением выработки синовиальной жидкости;
– уменьшением вымывания кальция из костей и улучшением фосфорно-кальциевого обмена, т. е. укреплением костной ткани.
Клинически действие препарата проявляется уменьшением болей в области сустава и увеличением в нем объема движений. Но главное его свойство – замедление дальнейшего прогрессирования заболевания.
Показанием для назначения Терафлекса является любая патология опорно-двигательного аппарата, связанная с дегенеративными изменениями в хрящевой ткани (ОА и остеохондроз). Назначать препарат нужно как можно раньше, при появлении первых признаков заболевания (скрипа, хруста, болевых ощущений). Терафлекс выпускается в нескольких формах, что обеспечивает удобство применения и максимально удовлетворяет потребности пациента:
– Терафлекс капсулы – для базисной терапии;
– Терафлекс Адванс капсулы – для лечения обострений болевого синдрома.
Лечение рекомендуется начинать с препарата Терафлекс Адванс, который быстро уменьшает боль и одновременно начинает стимулировать обновление хрящевой ткани. Терафлекс Адванс помимо хондроитина сульфата и глюкозамина дополнительно содержит НПВП ибупрофен, который оказывает быстрое обезболивающее и противовоспалительное действие [16], он более безопасен по сравнению с другими НПВП [11]. При совместном приеме глюкозамина и ибупрофена их взаимодействие позволяет добиться снижения дозы последнего в 2 раза, сохранив обезболивающий эффект, что, безусловно, важно для безопасности лечения. Капсулы Терафлекс Адванс удобно применять, они меньше чем таблетки раздражают ЖКТ. Рекомендуется принимать по 2 капсулы 3 р./сут, длительность приема – до 3 нед. Однако курс можно сократить при достижении желаемого результата и перейти на прием базового препарата Терафлекс, не содержащего НПВП (по 2–3 капсулы/сут, 3 мес.), для продления обезболивающего эффекта и защиты хряща.
Наряду с фармакологическими препаратами в терапии ОА обязательно должны применяться нефармакологические методы лечения и профилактики дальнейшего развития ОА. К ним относятся контроль факторов риска и сопутствующих заболеваний, таких как ожирение, диабет и менопауза. Обучение пациентов правильному поведению и соблюдению постуральной гигиены, адекватная физическая активность, защита суставов, физиотерапия, а также снижение веса являются важнейшими инструментами борьбы с травматизацией суставов и болевым синдромом [17, 18].
Многие пациенты считают, что просто принимая НПВП при артрозе и артрите, они избавляют себя от боли и полностью решают проблему. Но это далеко не так – заболевание продолжает развиваться, и важно не только купировать болевой синдром, но и предотвратить дальнейшее прогрессирование дегенеративных изменений. Такую возможность дают препараты из группы хондропротекторов. Регулярный длительный прием хондропротекторов позволяет замедлить прогрессирование дегенеративных изменений хрящевой ткани и снизить дозу принимаемых НПВП, избежав тем самым ряда возможных осложнений.
Литература
1. Туровская Е.Ф., Филатова Е.Г., Алексеева Л.И. Дисфункциональные механизмы хронического болевого синдрома у пациентов с остеоартрозом // Лечение заболеваний нервной системы. 2013. № 1. С. 21–28.
2. Алексеева Л.И. Ревматология. Национальное руководство М., 2010.
3. Пилипович А.А. Боль в спине и суставах // Новая аптека. 2010. № 11 (2). С. 18–19.
4. Kellgren J., Lawrence J. Radiological assessment of osteo-arthrosis // Annals of the rheumatic diseases. 1957. Vol. 4. Р. 494–502.
5. Guilak F. Review. Biomechanical factors in osteoarthritis // Best Pract Res Clin Rheumatol. 2011. Vol. 6. Р. 815–823.
6. Pulsatelli L., Addimanda O., Brusi V., et al. New findings in osteoarthritis pathogenesis: therapeutic implications // Ther Adv Chronic Dis. 2013. Vol. 1. Р. 23–43.
7. Bay-Jensen A.C., Hoegh-Madsen S., Dam E., et al. Review. Which elements are involved in reversible and irreversible cartilage degradation in osteoarthritis? // Rheumatol Int. 2010. Vol. 4. Р. 435-442.
8. Hassanali S.H., Oyoo G.O. Osteoarthritis: a look at pathophysiology and approach to new treatments: a review // East African Orthopaedic Journal. 2011. Vol. 5. Р. 51–57.
9. Glasson S. Identification of targets through histologic evaluation of osteoarthritis in knockout mice // Osteoarthritis Cartilage. 2005. Vol. 13. Р. 3.
10. Stitik T.P., Altschuler E., Foye P.M. Review. Pharmacotherapy of osteoarthritis // Am J Phys Med Rehabil. 2006. Vol. 11. Р. 15–28.
11. Castellsague J., Riera-Guardia N., Calingaert B. et al. Individual NSAIDs and upper gastrointestinal complications: a systematic review and meta-analysis of observational studies (the SOS project) // Drug Saf. 2012. Vol. 12. Р. 1127–1146.
12. Алексеев В.В., Баринов А.Н., Кукушкин М.Л. с соавт. Боль. Руководство для врачей и студентов / под ред. Н.Н. Яхно. М.: Мед Пресс, 2009. 302 с.
13. Данилов А.Б., Данилов Ал.Б. Управление болью. Биопсихосоциальный подход. Руководство для врачей. М.: АММ ПРЕСС, 2012. 582 с.
14. Шарапова Е.П., Алексеева Л.И. Результаты исследования препарата Хондроксид при остеоартрозе коленных суставов // Consilium Medicum. 2012. № 2. С. 72–76.
15. Буйлова Т.В. Открытое рандомизированное исследование эффективности и безопасности препарата Хондроксид в комплексном лечении больных с хронической вертеброгенной люмбоишалгией // РМЖ. 2010. № 18 (27). С. 1678–1685.
16. Терафлекс. Инструкция по применению. http://www.theraflex.ru.
17. Christensen R., Bartels E.M., Astrup A. et al. Review. Effect of weight reduction in obese patients diagnosed with knee osteoarthritis: a systematic review and meta-analysis // Ann Rheum Dis. 2007. Vol. 4. Р. 433–439.
18. Zhang W., Moskowitz R.W., Nuki G. et al. OARSI recommendations for the management of hip and knee osteoarthritis, part II: OARSI evidence-based, expert consensus guidelines // Osteoarthritis and Cartilage. 2008. Vol. 2. Р. 137–162.












