В современных руководствах понятие «неспецифическая боль в спине» вытесняет использующийся в настоящее время диагноз «дорсопатия», заменивший широко распространенный ранее термин «остеохондроз» [6]. Термин «остеохондроз», предложенный A. Hildebrandt еще в 1935 г., обозначает дегенеративно-дистрофическое поражение позвоночника, в основе которого лежит дегенерация диска с последующим вовлечением тел смежных позвонков, межпозвонковых суставов и связочного аппарата. Высокая частота дистрофического поражения позвоночника, выявляемая при рентгенографии у пациентов среднего и пожилого возраста, в 1960-х гг. сформировала устойчивое представление у врачей и пациентов о зависимости боли от остеохондроза. Распространенность подобных взглядов в медицинской литературе привела к тому, что «остеохондроз» стал основной жалобой и одним из самых частых диагнозов у пациентов с болями в спине. Это привело к недопустимому пренебрежению в области клинического обследования пациента – действительно, зачем тратить время и силы на диагностический поиск, если причина боли кроется в дегенеративно-дистрофическом поражении позвоночника? Однако многочисленные исследования показали, что выраженность рентгенологических проявлений остеохондроза позвоночника не соотносится с локализацией, характером, интенсивностью и длительностью болевого синдрома. Из 10 пациентов с дегенеративно-дистрофическими изменениями в позвоночнике только один имеет клинические проявления боли в спине. Кроме того, «теорию остеохондроза» опровергает сохранность патологических изменений анатомических структур позвоночника при наличии рецидивирующего течения болевого синдрома. Поэтому наличие рентгенологических проявлений остеохондроза у пациента не должно определять ни лечебную, ни экспертную тактику [5, 6, 8].
Другой распространенный клинический миф касается грыжи межпозвоночного диска. Так ли она опасна на самом деле и следует ли ее лечить? Бессимптомные грыжи межпозвонковых дисков встречаются во много раз чаще тех грыж, которые вызывают боль в спине, а точнее – в спине и конечности (радикулопатию) [2, 7, 9]. И размер здесь также не имеет значения! Главными определяющими факторами, обусловливающими наличие и характер болевого синдрома, являются направление, в котором пролабирует грыжа, и выраженность аутоиммунной воспалительной реакции организма в ответ на пролабирование пульпозного ядра через дефект фиброзного кольца. Если грыжа направлена в тело позвонка (грыжа Шморля) или в центр позвоночного канала (медиальная грыжа), она будет бессимптомной, т.е. радикулопатия не разовьется. Боли в спине у таких пациентов будут, скорее всего, связаны с уменьшением высоты межпозвоночного диска, ухудшением его амортизирующей функции и перераспределением нагрузки на фасеточные суставы пораженного позвоночного двигательного сегмента, что приводит к прогрессированию остеоартроза из-за функциональной перегрузки и деформации сустава с рефлекторными мышечно-тоническими синдромами [1, 7, 8].
Таким образом, у пациентов, имеющих медиальные грыжи межпозвонковых дисков или грыжи Шморля, чаще всего симптомы болезни отсутствуют либо отмечается неспецифическая боль в спине, обусловленная фасеточным синдромом. Только латеральные грыжи, механически повреждающие корешки нервов или вызывающие вторичные токсические и дизиммунные процессы, по-настоящему опасны в отношении развития радикулопатии [8, 9, 12]. Заподозрить такую грыжу можно, если боль из спины распространяется в руку или ногу и сопровождается слабостью и чувствительными расстройствами в конечности, симптомами натяжения корешка. Но и такая грыжа не является «приговором к операции». Современные медицинские технологии позволяют проводить лечение таких состояний безоперационно (путем блокад) или, в крайнем случае, малоинвазивными методами (лазерная вапоризация, холодно-плазменная аблация) [2, 10, 13]. При консервативной терапии радикулопатий наблюдается типичная ситуация: на фоне лечения (или даже без него) боль в спине исчезает, хотя грыжа остается прежних размеров и на прежнем месте. Проспективные наблюдения за пациентами с компрессионной радикулопатией показывают достоверное уменьшение грыж и секвестраций дисков (в 75–100% случаев) и компрессии неврального содержимого (21–80%) через 14 мес. даже при отсутствии терапии [5, 8, 9].
Современные классификации выделяют неспецифические (доброкачественные саморазрешающиеся в течение 1 мес.) и специфические (см. «красные флажки») боли в спине [2, 5–8], однако вынесение подобных собирательных терминов в клинический диагноз, на наш взгляд, нецелесообразно, т.к. эти понятия не отображают этиопатогенетических особенностей заболевания у каждого конкретного больного и не определяют направления его лечения. Наиболее оптимальна для вынесения в клинический диагноз анатомическая классификация спондилогенных болевых синдромов:
1. Спондилогенная цервикалгия – неспецифическая боль в шейном отделе позвоночника (цервикобрахиалгия – при иррадиации боли в руку, цервикокраниалгия – при иррадиации в голову).
2. Спондилогенная торакалгия – неспецифическая боль в грудном отделе позвоночника.
3. Спондилогенная люмбалгия – неспецифическая боль в нижней части спины (люмбоишиалгия – при иррадиации в ногу).
Вышеобозначенные диагнозы, по сути, столь же неспецифичны, как и устаревший термин «остеохондроз», поэтому требуют уточняющего расширения: с мышечно-тоническим и/или миофасциальным синдромом … мышц, с фасеточным синдромом … позвонков (как вариант – с дисфункцией крестцово-подвздошного сочленения), с компрессионной радикулопатией … корешка. Таким образом, развернутый клинический диагноз пациента с хронической, иррадирующей в правую ногу болью в спине без признаков корешковой компрессии может звучать как «хроническая спондилогенная правосторонняя люмбоишиалгия с мышечно-тоническим синдромом подвздошно-поясничной и средней ягодичной мышц, фасеточного синдрома L5–S1 и дисфункцией правого крестцово-подвздошного сочленения, астено-депрессивный синдром» и кодироваться М54.4 (МКБ-10). Вынесение в диагноз нейроортопедических синдромов позволяет не только уточнить патогенетические особенности заболевания (что важно для оценки динамики состояния больного при следующих визитах), но и обосновать целесообразность применяемых методов лечения: нестероидных противовоспалительных препаратов (НПВП) – для купирования боли, миорелаксантов – для уменьшения мышечно-тонического синдрома, антидепрессантов – для повышения тонуса антиноцицептивной системы, а лечебных блокад (и/или радиочастотной денервации) – для локального воздействия на суставные источники боли.
В качестве основных источников локальной боли в поясничной области в 70–80% случаев обсуждаются миогенные нарушения (спазм, микротравматизация, ишемизация паравертебральных мышц), дисфункция фасеточных суставов (до 40% случаев) и в 5% – дискогенная боль [5, 7, 8]. К сожалению, данные нейроортопедического обследования часто остаются маловоспроизводимыми и неспецифичными: такие болевые синдромы, как фасеточный, миофасциальный и мышечно-тонический, нередко являются во многом гомогенными в отношении жалоб и часто имеют «перекрывающиеся» характеристики при клиническом обследовании.
После клинического неврологического и нейроортопедического обследования для уточнения источников болевой импульсации и механизмов развития боли в ряде случаев необходимо проведение инструментальных методов исследования [2, 5–7]. При болях в шейном и поясничном отделах позвоночника и конечностях особое значение имеют методы визуализации, целесообразность применения которых определяется анамнестическими особенностями и наличием изменений в неврологическом и соматическом статусе пациентов. В подавляющем числе случаев острая и хроническая боль в спине является «доброкачественным» состоянием, и большинство пациентов не нуждаются в проведении дополнительных инструментальных исследований. Однако наличие отчетливых неврологических и соматических расстройств («красных флажков») может потребовать срочного параклинического обследования. Так, слабость в мышцах ног, снижение чувствительности в аногенитальной области по типу «седловидной анестезии», тазовые нарушения указывают на наличие компрессии корешков конского хвоста и требуют незамедлительного проведения магнитно-резонансной томографии (МРТ) или компьютерной томографии (КТ) для решения вопроса о необходимости срочного оперативного вмешательства. Отсутствие связи боли с движением, сохранение ее в ночное время, наличие в анамнезе злокачественного новообразования, ВИЧ-инфекции, применения иммунодепрессантов, беспричинное снижение веса, лихорадка и ночной гипергидроз, возраст больного младше 20 и старше 50 лет требуют проведения дополнительных методов исследования уже при первом обращении пациента с целью исключения, в первую очередь, инфекционного и опухолевого поражения позвоночника. Ниже приведены признаки серьезной патологии при болях в спине («красные флажки») [2, 5, 6]:
• наличие в анамнезе злокачественного новообразования;
• сохранение боли в покое;
• значимая травма в недавнем анамнезе (падение с высоты, автоавария и т.д.);
• беспричинное снижение веса;
• отсутствие улучшения через 1 мес. оптимального лечения;
• лихорадка;
• болезненность при пальпации и перкуссии позвоночника;
• наличие в анамнезе наркотической зависимости, ВИЧ-инфекции, применения иммуносупрессантов;
• длительное применение кортикостероидов;
• дебют боли в возрасте старше 55 лет и младше 20 лет;
• симптомы поражения спинного мозга: чувствительные расстройства на туловище и в конечностях («проводниковые нарушения чувствительности»), слабость в конечностях, тазовые расстройства;
• симптомы поражения корешков конского хвоста (нарушение чувствительности в аногенитальной области, тазовые расстройства, слабость в ногах) или отдельных шейных, поясничных и крестцовых корешков (иррадиация боли в руку или ногу, сочетающаяся со снижением силы и нарушениями чувствительности в зоне иннервации соответствующего корешка).
Во всех перечисленных случаях необходимы рентгенография соответствующих отделов позвоночника в прямой и боковой проекциях, проведение общего анализа крови и мочи, а при подозрении на остеомиелит, эпидуральный абсцесс, поражение спинного мозга и корешков, а также в диагностически сомнительных случаях – проведение МРТ пояснично-крестцового отдела позвоночника. При необходимости уточнения состояния костных структур в ряде случаев после проведения рентгенографии показаны рентгеновская КТ и сцинтиграфия позвоночника. При подозрении на злокачественное новообразование предстательной железы необходимо исследовать уровень специфического антигена простаты. При наличии травмы в недавнем анамнезе (падение с высоты, дорожно-транспортные происшествия и т.д.), а также при длительном применении кортикостероидов и у пациентов старше 55 лет необходимо провести рентгенографию позвоночника, а при недостаточной ее информативности и сохранении боли свыше 10 дней – сцинтиграфию или КТ позвоночника для исключения компрессионного и иного травматического перелома позвонков. Всем пациентам с интенсивным болевым синдромом длительностью свыше 1 мес., а также всем больным с хроническими болями в спине показано однократное проведение рентгенографии позвоночника в прямой и боковой проекциях с целью исключения, в первую очередь, опухолевого или инфекционного поражения позвоночника, а также остеопороза. При болевом синдроме в грудной клетке всем пациентам уже при первом обращении целесообразно проведение электрокардиографии и рентгенографии легких для исключения соматической патологии (ишемической болезни сердца, инфекционного и опухолевого поражения легких и плевры и др.) как основной причины болевого синдрома.
При обследовании пациентов с явными ортопедическими дефектами в виде грубого сколиоза, спондилолистеза, нестабильности поясничного отдела позвоночника, асимметрии длины ног, косого и скрученного таза, с патологией тазобедренных суставов определить этиологию боли не составляет больших трудностей. А вот точное выявление источников болевой импульсации, особенно при хронической неспецифической боли в спине, весьма затруднительно [1, 4, 8]. По мнению отдельных ведущих исследователей в этой области, без применения инвазивных методов диагностики (дискографии, диагностических блокад) оно возможно примерно у 40% пациентов с острыми и подострыми болями в спине и не более чем в 15% случаев хронических скелетно-мышечных болевых синдромов [8, 10–12]. С одной стороны, это отражает сложность строения структур поясничной области и связанную с ней трудность точного определения ноциогенной структуры, с другой – утрату первостепенной роли периферических источников боли при ее хронизации. Соответственно различается и подход к лечению острой и хронической неспецифической боли в спине.
Традиционно считается, что лечение боли должно в первую очередь воздействовать на этиологические факторы, например, компенсацию разницы длины ног, лечение дегенеративных изменений хряща фасеточных суставов, удаление грыжи межпозвоночного диска и т.д., однако этиотропная терапия часто не прекращает ни острую, ни хроническую боль [2, 3, 5]. Это связано с тем, что в основе острых болей чаще всего лежит воспаление, а это значит, что необходимо патогенетическое лечение противовоспалительными препаратами для быстрого купирования болевого синдрома. Основой хронических болей являются изменения в центральной и периферической нервной системе (периферическая и центральная сенситизация, снижение нисходящих ингибирующих влияний антиноцицептивной системы), которые как бы «отрывают» боль от первопричины заболевания, делая ее самостоятельной болезнью. Здесь требуется патогенетическое лечение антидепрессантами или антиконвульсантами [4, 6, 8].
При острой боли в спине необходимо максимально быстро избавить пациента от мучительных болей во избежание хронификации заболевания, вызванной сенситизацией периферической и центральной нервной систем, «бомбардируемых» болевыми импульсами от воспаленных мышц, связок, фасеточных суставов и других структур позвоночника. Это достигается применением препаратов для симптоматического и патогенетического лечения боли (прежде всего – НПВП и миорелаксантов), что попросту недоступно для этиотропной терапии, при которой для этого необходим продолжительный период времени [2, 4, 6]. Для профилактики хронификации острой скелетно-мышечной боли в спине необходимо как можно раньше начать обезболивающую терапию и ограничить нагрузку на пораженный отдел позвоночника путем фиксации специальными ортопедическими пособиями (корсетом, реклинатором, шиной Шанца – в зависимости от пораженного отдела). Микротравмы в процессе реабилитации способны вызвать кинезиофобию (страх движения), а также ускорить процессы хронификации, растормаживая (сенситизируя) потоком афферентной болевой информации соответствующие отделы спинного и головного мозга. В связи с этим современный подход к лечению острой боли в спине подразумевает максимально раннее назначение препаратов, воздействующих в первую очередь на патофизиологические механизмы боли независимо от этиологической природы их развития [1, 2, 4, 6, 7].
Ключевым направлением симптоматического и патогенетического лечения боли в спине является применение НПВП, блокирующих выработку медиаторов воспаления – простагландинов за счет ингибирования фермента циклооксигеназы (ЦОГ). Следует иметь в виду и то, что эта группа препаратов обладает рядом существенных побочных эффектов [15]. Открытие двух изоформ ЦОГ: тканевой, или конституциональной – ЦОГ-1, постоянно присутствующей в большинстве тканей, и индуцибильной – ЦОГ-2, существенно повышающей свой уровень на фоне воспаления, позволило лучше понимать механизмы, лежащие в основе эффективности и токсичности НПВП. Обе изоформы ЦОГ продуцируются и в периферических тканях, и в клетках центральной нервной системы. Под влиянием ЦОГ-1 осуществляется синтез простагландинов, участвующих в реализации физиологических функций. ЦОГ-2 образуется в зоне воспаления и клетках спинного и головного мозга под действием повреждающих стимулов с периферии.
Неселективные НПВП блокируют активность обеих изоформ ЦОГ, что приводит к ряду побочных эффектов, которые связаны с ингибированием ЦОГ-1, прежде всего к поражению желудочно-кишечного тракта (ЖКТ), причем на всем его протяжении (стоматит, эзофагит, гастрит, язва желудка и двенадцатиперстной кишки, энтерит, язвенный колит, проктит). Следует обратить внимание на то, что, являясь хорошими анальгетиками, неселективные НПВП блокируют висцеральные болевые ощущения, и язвенное поражение ЖКТ у таких больных зачастую протекает бессимптомно, заканчиваясь либо кровотечением, либо перфорацией язвы с последующим развитием перитонита. Применение парентеральных форм неселективных НПВП (инъекции и суппозитории) не позволяет избежать вышеуказанных побочных явлений, т.к. при этом создается высокая концентрация препарата в сыворотке крови, что сопровождается системным воздействием на организм [6].
НПВП, обладающие повышенной избирательностью по отношению к индуцибельной ЦОГ, т.е. селективные блокаторы изофермента ЦОГ-2, имеют более высокую степень безопасности в отношении ЖКТ, чем неселективные. Выделяют избирательно селективные ЦОГ-2-ингибиторы (мелоксикам, нимесулид) и высокоселективные (или специфические) ЦОГ-2-ингибиторы (коксибы); при этом чем выше селективность НПВП по отношению к ЦОГ-2, тем выше риск сосудистых осложнений. Именно поэтому ряд высокоселективных ЦОГ-2-ингибиторов, например, вальдекоксиб, был запрещен к применению. С учетом вероятности риска развития эрозивно-язвенных процессов в желудке у больных с высоким риском НПВП-гастропатий на фоне приема селективных ингибиторов ЦОГ-2 также оправданна профилактика осложнений в виде назначения ингибиторов протонной помпы (омепразола), мизопростола [2, 6].
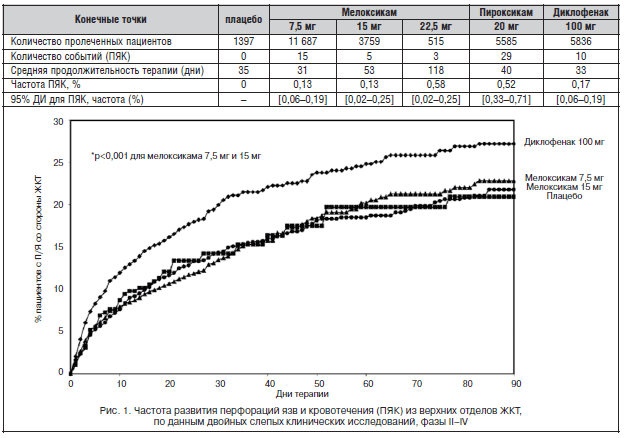
Наилучший профиль безопасности среди НПВП в отношении ЖКТ имеет мелоксикам (Мовалис), являющийся производным энолиновой кислоты [1, 15]. Метаанализ рандомизированных клинических исследований [15] показал, что мелоксикам в дозе 7,5 мг оказался самым безопасным НПВП с точки зрения риска развития осложнений со стороны ЖКТ (диспепсии, появления язв и кровотечений) (рис. 1). При повышении дозы мелоксикама до 15 мг риск возникновения побочных явлений не увеличивался и оставался значительно ниже, чем у других НПВП [15].
При однократном применении Мовалис оказывает кумулятивное действие, максимальная концентрация достигается через 3–5 дней приема. Именно поэтому для более быстрого получения лечебного эффекта целесообразно проводить так называемую «ступенчатую» терапию, которая заключается во внутримышечном введении 15 мг Мовалиса в первые 3 дня лечения, а затем в переводе больного на таблетированную форму мелоксикама по 15 мг в течение 20 дней [1].
Дополнительной возможностью быстрого купирования боли стало появление новой пероральной формы препарата Мовалис – суспензии по 15 мг (2 мерные ложки), которая по сравнению с таблетированной формой имеет улучшенную фармакокинетику – ускоренное всасывание (Tmax 3–7 ч), обеспечивающее начало действия препарата через 30 мин. после приема, с достижением Сmax через 2 ч, что позволяет быстрее купировать острый болевой синдром в тех случаях, когда отсутствует возможность применения инъекций [16]. Таким образом, новая форма мелоксикама дает возможность врачам амбулаторной практики использовать суспензию как альтернативу быстрым таблетированным формам НПВП, таким как нимесулид, коксибы и др.
Среди сердечно-сосудистых осложнений при лечении НПВП и коксибами наиболее актуальными для больных пожилого возраста являются повышение уровня АД, особенно при наличии артериальной гипертензии, а также снижение эффективности некоторых гипотензивных препаратов (ингибиторов ангиотензинпревращающего фермента и β-блокаторов). Наряду с повышением АД на фоне применения НПВП и коксибов могут появляться или усиливаться признаки сердечной недостаточности в связи с задержкой жидкости, менее выраженной при использовании избирательно селективных ингибиторов ЦОГ-2 [2, 5, 6]. При проведении комбинированной терапии Мовалис не взаимодействует с другими медикаментами, включая гипотензивные препараты, диуретики, сердечные гликозиды и β-блокаторы, что важно при лечении больных с сопутствующими заболеваниями, однако следует иметь в виду, что при приеме НПВП необходимо более тщательно контролировать АД у пожилых больных [1, 16].
Следует помнить, что НПВП особенно эффективны на ранних стадиях развития боли в спине. Именно на этом раннем этапе – этапе острой и подострой боли – с помощью традиционных НПВП возможно воздействовать на выработку периферических медиаторов воспаления. В дальнейшем, когда включаются центральные патофизиологические механизмы боли, монотерапия НПВП не будет столь эффективна. В России в качестве базисной терапии суставной патологии (остеоартроз, спондилоартроз) при хронической боли широко используются так называемые «симптом-модифицирующие препараты медленного действия» (SYSADOA), в частности, содержащие глюкозамин и хондроитина сульфат. Они обладают умеренно обезболивающим и противовоспалительным действием, но лишены характерных для НПВП побочных эффектов. И т.к. механизм их противовоспалительного действия не связан с подавлением синтеза простагландинов, а обусловлен блокированием ядерного фактора каппа-Б (NF-kB), инициирующего распад хрящевой ткани, обезболивающий эффект проявляется не сразу, а спустя 4–6 нед. после начала регулярного приема, с умеренным снижением боли, поэтому при обострении заболевания используется их комбинация с НПВП [2, 7, 8]. Обоснованием для применения SYSADOA служат как результаты их многолетнего, безопасного и успешного применения при остеоартрозе (уровень доказательности 1А), так и общность воспалительно-дегенеративных процессов, происходящих в суставах конечностей и межпозвонковых (фасеточных) суставах. Терапия SYSADOA позволяет значительно уменьшить дозировки применяемых НПВП постепенно.
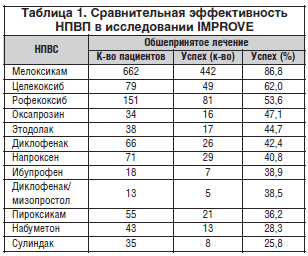
Учитывая хроническое течение суставной патологии, требующее длительной противовоспалительной и обезболивающей фармакотерапии, и распространенную коморбидность, это существенно понижает риск возникновения побочных эффектов НПВП, эффективность и безопасность которых при остеоартрозе была изучена в исследовании IMPROVE (табл. 1). Для оценки терапевтического успеха НПВП были приняты следующие параметры (конечная точка): завершение исследования без перехода на прием другого НПВП или завершение исследования и отсутствие необходимости принимать НПВП. Мелоксикам был назначен 662 больным, другие НПВП – 647. Конечной точки достигли 67% из группы больных, принимавших мелоксикам, и 45% больных из группы сравнения (p<0,0005). Отмена лечения из-за побочных реакций была соответственно у 12 и 20% больных, из-за отсутствия эффекта – у 16 и 28% больных. Приверженность больных к приему Мовалиса свидетельствует о высокой эффективности и безопасности этого препарата [15].
Следует отметить, что при боли в спине НПВП не рекомендуются для монотерапии более 10–14 дней. Если недельный курс приема препарата не купирует болевой синдром, то это должно побудить врача пересмотреть тактику лечения с привлечением невролога, который поможет разобраться в структуре болевого синдрома с целью выявления признаков серьезной патологии и выяснить причины неэффективности НПВП в каждом конкретном случае [2, 5, 6]. А причин такой неэффективности может быть несколько: плохое кровоснабжение в очаге воспаления (тогда противовоспалительный препарат можно ввести адресно, прямо в эпицентр боли и воспаления путем блокады с местными анестетиками под ультразвуковым или рентгеноскопическим контролем) или стойкий спазм паравертебральных мышц с формированием порочного круга «боль – спазм – боль» [3].
При мышечно-тонических болевых синдромах и хронификации боли в спине НПВП становятся недостаточно эффективны в качестве монотерапии. Они просто не способны «успокоить» расторможенные отделы нервной системы. Для воздействия на патогенетические механизмы хронификации боли в спине (прежде всего на мышечный спазм) на втором этапе лечения используют миорелаксанты (баклофен 10–30 мг/сут, тизанидин 6–12 мг/сут, толперизон 150–450 мг/сут). Основным механизмом действия вышеперечисленных препаратов является торможение возбуждения двигательного нейрона в ответ на болевые стимулы и эмоциональный дискомфорт.
Альфа-2-адреномиметик тизанидин нормализует повышенный мышечный тонус, блокируя выделение возбуждающего нейротрансмиттера глутамата в двигательных нейронах переднего рога спинного мозга, а также активирует нисходящие антиноцицептивные влияния голубого пятна ствола мозга. Блокатор натриевых каналов толперизон подавляет ретикулоспинальные растормаживающие воздействия на γ-мотонейроны, регулирующие тонус мышц. Активатор рецепторов γ-аминомасляной кислоты баклофен опосредованно воздействует на кальциевые каналы двигательных и чувствительных нейронов спинного мозга, подавляя медленные постсинаптические потенциалы, суммирующиеся в болевые импульсы и повышение тонуса мышц, а также уменьшая возбудимость нейронов лимбической системы, и, соответственно, тревожность пациентов.
Таким образом, миорелаксанты оказывают обезболивающее действие, помогая расторможенным отделам нервной системы вернуться в состояние покоя, т.е. стирая «болевую память». Это не только уменьшает выраженность боли при хроническом болевом синдроме, но и предотвращает усиление острой боли и переход ее в хроническую форму [2, 3].
При недостаточной эффективности НПВП в сочетании с миорелаксантами возможно кратковременное (7–10 дней) назначение слабых наркотических анальгетиков (трамадол 50–200 мг/сут). Наркотические анальгетики на время дают облегчение, но возникают привыкание к ним (с каждым разом требуются все большие дозы) и лекарственная зависимость (пациент уже не может обходиться без этих препаратов). Поэтому применение опиатов дольше 10 дней не рекомендуется и допустимо лишь при самых интенсивных (>70 мм по визуально-аналоговой шкале) болях в спине при неэффективности НПВП и адъювантных анальгетиков в качестве III ступени обезболивающей терапии, рекомендованной ВОЗ [2, 5, 6].
При отсутствии противопоказаний желательно дополнить лечение немедикаментозной терапией: тепловыми физиопроцедурами, мануальной терапией, вакуумным и ручным массажем. В некоторых случаях релаксации паравертебральных мышц и восстановления микроциркуляции в миофасциальных триггерных зонах удается достичь без дополнительного медикаментозного воздействия при применении вышеуказанных физиотерапевтических методов и/или ударно-волновой терапии [4, 7].
Следует отметить, что на первом и втором этапах лечения пациенты с острыми болями в спине не нуждаются в обязательной консультации невролога или ревматолога и лечатся у врача общей практики, а затем у врача по лечебной физкультуре. При острых скелетно-мышечных болях в спине нет необходимости в соблюдении постельного режима даже в первые дни заболевания, а также в использовании опоры при передвижении (трости или костыля). Необходимо убедить пациента, что небольшая физическая нагрузка не опасна, посоветовать поддерживать повседневную активность, а после купирования острого болевого синдрома – как можно скорее приступить к работе, не забывая при этом о лечебной физкультуре, необходимой для предотвращения последующих эпизодов болей в спине
[2, 4, 5–8].
Дополнительным и наиболее эффективным малоинвазивным методом терапии скелетно-мышечных болей в спине на любом этапе лечения оказывается локальное инъекционное введение лекарственного препарата (блокада), обладающего противоотечным и противовоспалительным действием, в очаг воспаления и устойчивого мышечного спазма [2, 7, 10–13]. Такой способ введения применяется для местных анестетиков, а также НПВП и глюкокортикоидов эпидурально, фораминально, параартикулярно в фасеточные суставы, в миофасциальные триггерные точки и др. Однако проведение блокад требует наличия специальных навыков у врача, осуществляющего эту процедуру, а в ряде случаев – и высокотехнологической аппаратуры, обеспечивающей правильное попадание иглы в пораженную область (рентгенографической установки с электронно-оптическим преобразователем или ультразвукового сканера). Поэтому методика блокад пока не распространена повсеместно, хотя и используется в медицине более 100 лет – с 1906 г., когда Х. Селлхайм впервые применил паравертебральную блокаду межреберного нерва, вводя растворы кокаина и новокаина, синтезированного Эйнхорном двумя годами ранее. В 1912 г. эта блокада была модифицирована Капписом для шейного отдела.
По своему назначению блокады подразделяются на диагностические, прогностические и лечебные. С помощью диагностических блокад осуществляется уточнение диагноза ex juvantibus. Цель прогностической блокады – определить эффективность лечения и дать временно почувствовать пациенту, что он будет испытывать после высокочастотной денервации сустава или деструкции нерва и сможет ли переносить чувствительные и вегетативные нарушения, возникшие в результате данного воздействия [11].
При проведении лечебных блокад используется большой арсенал медикаментозных средств, что, с одной стороны, определяется фармакодинамикой и механизмом их действия, с другой – этиопатогенетическими особенностями развития боли в спине (будет подробно описано ниже). Применяемые препараты делятся на 2 группы: основные (базовые) и дополнительные. В связи с широким спектром действия в качестве базового средства для указанных видов блокад наибольшее применение нашли местные анестетики. В последнее время наиболее эффективным является ропивакаин, преимуществами которого являются малая токсичность и более выраженный анальгетический эффект [2, 10]. В качестве базовых средств для лечения суставного синдрома используются препараты гиалуроновой кислоты. Эти вязко-упругие аллотрансплантаты суставной жидкости не смешиваются с местными анестетиками и вводятся в фасеточные и крестцово-подвздошные суставы под рентгенологическим или ультразвуковым контролем. Лечебные блокады с использованием этой группы препаратов при остеоартрозе, спондилоартрозе отличаются ультрадолгим (до 1 года) действием.
К числу дополнительных препаратов, использующихся для лечения боли в спине лишь при лечебных блокадах, относятся гормональные средства (глюкокортикоиды), применение которых основано на их противовоспалительном, десенсибилизирующем и противоотечном действии как локально в тканях, так и системно в организме [2, 10, 13]. Именно из-за системного действия глюкокортикоиды необходимо с осторожностью применять у пожилых пациентов, больных сахарным диабетом, гипертонической болезнью, лиц с заболеваниями ЖКТ, сердечной недостаточностью, сниженным иммунным статусом и при инфекционных заболеваниях. Альтернативными дополнительными препаратами, лишенными побочных эффектов глюкокортикоидов, являются НПВП. Они применяются преимущественно для инфильтраций (блокад) триггерных зон мышц при миофасциальных синдромах и параартикулярных блокад при фасеточном синдроме. Применение мелоксикама (Мовалиса) для локальной инъекционной терапии (лечебных блокад) при миофасциальных болевых синдромах отличается высоким профилем безопасности, кроме того, Мовалис может использоваться для футлярных блокад, например, при тоннельных синдромах. Для лечебных блокад используется раствор 15 мг (1,5 мл) Мовалиса и от 2 до 5 мл местного анестетика (0,5% новокаина или 0,5–2% лидокаина) в зависимости от размеров инфильтрируемой триггерной зоны и интенсивности болевого синдрома. Помимо Мовалиса при лечебных блокадах используются диклофенак, кеторолак, кетопрофен, лорноксикам и другие НПВП, увеличивающие эффективность и длительность обезболивающего действия местных анестетиков за счет воздействия на механизмы патогенеза миофасциального болевого синдрома [1].
Таким образом, в ряде случаев проведение блокад, помимо лечебных целей, необходимо для диагностики и определения оптимальной стратегии последующего лечения. Так, например, диагностическая блокада фасеточного сустава или крестцово-подвздошного сочленения раствором местного анестетика (2% лидокаина или 0,5% новокаина) не только позволяет определить источник боли в спине, но и предсказать эффективность малоинвазивной нейрохирургической процедуры – высокочастотной денервации сустава [4, 11]. Понятно, что без НПВП и/или глюкокортикоида длительность обезболивающего действия анестетика составит лишь несколько часов, но при исчезновении у пациента после блокады болевого синдрома хотя бы на 1 ч мы можем уверенно говорить о том, что процедура денервации будет эффективна – в этом случае блокаду можно рассматривать как прогностическую.
Таким же образом определяется прогноз эффективности внутридисковой электротермической аннулопластики, лазерной вапоризации или холодно-плазменной аблации межпозвонкового диска при радикулопатии. Если интрафораминальное введение анестетика под контролем КТ устраняет болевой синдром, то проведение вышеуказанных малоинвазивных пункционных нейрохирургических воздействий может быть эффективным [9, 10, 12]. Следует отметить, что в ряде случаев достаточный терапевтический эффект имеет интрафораминальное введение вместе с местным анестетиком раствора глюкокортикоида, обеспечивающего патогенетическое воздействие на аутоиммунные и компрессионно-ишемические механизмы диско-радикулярного конфликта (противовоспалительное, противоотечное и ремиелинизирующее действие). Обычно фораминальной блокады бывает достаточно для того, чтобы уменьшить выраженность болевых ощущений и чувствительных (а иногда и двигательных) расстройств до следующего обострения радикулопатии.
В случае недостаточной по времени эффективности лечебных фораминальных блокад и при наличии несеквестрированной латеральной (фораминальной) грыжи диска (менее 7 мм) проводится малоинвазивная процедура лазерной вапоризации (или ее модификации – фораминопластики), холодно-плазменной аблации или внутридисковой электротермической аннулопластики, которая эффективна у 50–65% пациентов [9]. Если и эта пункционная процедура не приводит к регрессу болевого синдрома, тогда проводится оперативное нейрохирургическое вмешательство открытым доступом. Вопрос о проведении пункционных или открытых нейрохирургических вмешательств при болях в спине ставится в случае неэффективности правильно проводимой консервативной терапии в течение 3 мес. К сожалению, нередко оперативное вмешательство проводится при отсутствии должных показаний (прогрессирующий парез иннервируемых пораженным корешком мышц конечности, тазовые нарушения, перемежающаяся хромота, вызванная стенозом позвоночного канала), что чревато формированием хронического постдискэктомического болевого синдрома, обусловленного множеством факторов (нарушением биомеханики движения в оперированном сегменте позвоночника, спаечным процессом, хроническим эпидуритом и т.д.) [2, 7, 8].
При хроническом течении болевого синдрома на третьем этапе лечения боли в спине применяются психотропные препараты из разряда антидепрессантов. Частое наличие депрессии у пациентов с хронической болью в спине послужило поводом к включению в стандарты терапии антидепрессантов, которые неожиданно оказались весьма эффективны в лечении всех видов хронической боли, независимо от наличия коморбидной депрессии. Более того, оказалось, что анальгетический эффект антидепрессантов развивается значительно раньше тимолептического, что побудило исследователей к поиску механизмов действия этой группы препаратов при болевых синдромах. Полагают, что антидепрессанты увеличивают активность эндогенной подавляющей боль (антиноцицептивной) системы мозга за счет повышения концентрации ключевых нейромедиаторов антиноцицептивной системы – серотонина и норадреналина [2, 8]. Ограничивающим фактором применения трициклических антидепрессантов в лечении хронических болей в спине является наличие выраженных побочных явлений (сонливость, потеря координации движений, повышение артериального давления, задержка мочи и т.д.) и синдрома отмены (возобновление болей, развитие тревожности, психомоторного возбуждения и даже судорожных припадков при резком прекращении приема этих лекарств). В этой связи более безопасно назначение антидепрессантов из группы селективных ингибиторов обратного захвата серотонина, таких как эсциталопрам, не имеющих вышеуказанных побочных эффектов при доказанной эффективности в лечении хронической боли в спине и невропатической боли при радикулопатии [14].
Для активации регенеративных процессов в периферических нервах при радикулопатии используются нейротропные комплексы, содержащие большие дозы витаминов группы В (В1, В6, B12). Применение витамина В12 способствует не только ремиелинизации, но и снижению интенсивности болевого синдрома. Пиридоксин участвует в синтезе сфингозина – структурного элемента мембраны нервного волокна и нейромедиаторов (серотонина, норадреналина). Таким образом, оба нейротропных компонента увеличивают скорость проведения нервного импульса, улучшают его репаративные свойства. Доказано патогенетическое воздействие тиамина на улучшение аксоплазматического тока и восстановление трофической функции нейрона [2, 4, 7]. Получены данные об эффективности антиоксидантов (препаратов тиоктовой кислоты) в патогенетическом лечении чувствительных и двигательных расстройств у больных с радикулопатиями.
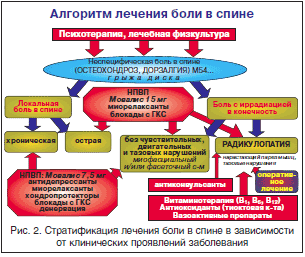
Поведенческая и когнитивно-поведенческая психотерапия помогает скорректировать неправильные, пpепятствующие выздоpовлению пpедставления пациента о пpиpоде своего заболевания, изменить социальное подкрепление болевого поведения, уменьшить зависимость от анальгетической терапии и увеличить степень повседневной активности. Эта концепция легла в основу разработки психотерапевтических программ лечения боли – «школ боли». При реализации этих программ лечение хронической боли оказывается высокорезультативным, т.к. в них используется комплексный подход, сочетающий в себе методы психотерапии, рефлексотерапии, лечебной физкультуры и фармакотерапии (рис. 2) [2, 4–6, 8].
Литература
1. Алексеев В.В. Применение мелоксикама в лечении люмбоишиалгического синдрома // РМЖ. 2003. № 7 (11). С. 416–418.
2. Алексеев В.В., Баринов А.Н., Кукушкин М.Л., Подчуфарова Е.В., Строков И.А., Яхно Н.Н. Боль. Руководство для врачей и студентов / под ред. Н.Н. Яхно. М.: МедПресс, 2009. 302 с.
3. Баринов А.Н. Сегментарные механизмы формирования мышечного спазма, спастичности и хронизации боли // Врач. 2012. № 5. С. 17–23.
4. Баринов А.Н. Современные подходы к лечению болей в спине и радикулопатии // Врач. 2011. № 7. С. 5–9.
5. Европейские рекомендации по лечению неспецифической боли в пояснично-крестцовой области в условиях первичной медицинской помощи: реферат под науч. ред. Яхно Н.Н., Подчуфаровой Е.В. М.: Практическая медицина, 2010. 24 с.
6. Неспецифическая боль в нижней части спины: клинические рекомендации под ред. Ш.Ф. Эрдеса. М.: КомплектСервис, 2008. 70 с.
7. Павленко С.С. Боли в нижней части спины (эпидемиология, клинико-диагностическая классификация, современные направления в диагностике, лечении и стандартизации медицинской помощи): руководство. Новосибирск: Сибмедиздат НГМУ, 2007. 172 с.
8. Яхно Н. Н., Баринов А.Н., Подчуфарова Е.В. Невропатическая и скелетно-мышечная боль. Современные подходы к диагностике и лечению // Клиническая медицина. 2008. Т. 86. № 11. С. 9–15.
9. Andersson G.B., Mekhail N.A., Block J.E. Treatment of intractable discogenic low back pain. A systematic review of spinal fusion and intradiscal electrothermal therapy (IDET) // Pain Physician. 2006. Vol. 9 (3). Р. 237–248.
10. Benyamin R.M., Manchikanti L., Parr A.T. et al. The Effectiveness of Lumbar Interlaminar Epidural Injections in Managing Chronic Low Back and Lower Extremity Pain. Systematic Review // Рain Physician. 2012. Vol. 15. Issue 4. Р. 363–404.
11. Boswell M.V., Colson J.D., Sehgal N. et al. A systematic review of therapeutic facet joint interventions in chronic spinal pain // Pain Physician. 2007. Vol. 10 (1). Р. 229–253.
12. Datta S., Everett C.R., Trescot A.M. et al. An updated systematic review of the diagnostic utility of selective nerve root blocks // Pain Physician. 2007. Vol. 10 (1). Р. 113–128.
13. Manchikanti L., Buenaventura R.M., Manchikanti K.N. et al. Effectiveness of Therapeutic Lumbar Transforaminal Epidural Steroid Injections in Managing Lumbar Spinal Pain, Systematic Review // Рain Physician. 2012. Vol. 15. Issue 3. Р. 199–245.
14. Mazza M., Mazza O., Pazzaglia C. et al. Escitalopram 20 mg versus duloxetine 60 mg for the treatment of chronic low back pain // Expert Opin Pharmacother. 2010 May. Vol. 11 (7). Р. 1049–1052.
15. Frank Degner et al. // Inflammopharmacology. 2001. Vol. 9. No. 1, 2. P. 71–80.
16. Инструкция по применению лекарственного препарата для медицинского применения Мовалис, суспензия для приема внутрь. Рег. свид. ЛС-001185.












