Главной проблемой для врача при ведении пациента с атипичной пневмонией является не столько выбор антимикробной химиотерапии, сколько постановка самого диагноза «атипичная пневмония». Классические проявления трахеита, ларингита, острого бронхита, ОРВИ маскируют клинические проявления атипичной пневмонии, в связи с чем на постановку этого диагноза затрачивается гораздо большее время, в отличие от типичной пневмонии. Диагностические ошибки связаны также с отсутствием классических для пневмонии физикальных и рентгенологических признаков, бактериологический анализ неинформативен (микоплазмы и хламидиии являются внутриклеточными возбудителями), а в случаях ассоциации атипичных возбудителей с другими микроорганизмами может привести к некорректному выбору антибактериальных препаратов [2,3]. Имеются сведения, что до 20% выявленных пневмоний имеют смешанную этиологию с участием возбудителей атипичных пневмоний [7].
В каких же случаях необходимо задуматься об атипичной пневмонии? В случаях, если имеется:
• эпидемиологическая ситуация
• внелегочная симптоматика
• ОРВИ симптомы в дебюте заболевания (характерно для Mycoplasma)
• неинформативный бактериологический анализ, если отсутствует ассоциация микроорганизмов
• специфические серологические данные
• неэффективность b–лактамных антибиотиков
• эффективность макролидов, тетрациклинов, фторхинолонов
Подтверждение диагноза микоплазменной и хламидийной и легионелезной пневмоний основывается в первую очередь на неспецифических для классической типичной пневмонии, особенностях клинико–рентгенологических данных и подтверждается серологически или с помощью полимеразно–цепной реакции (ПЦР).
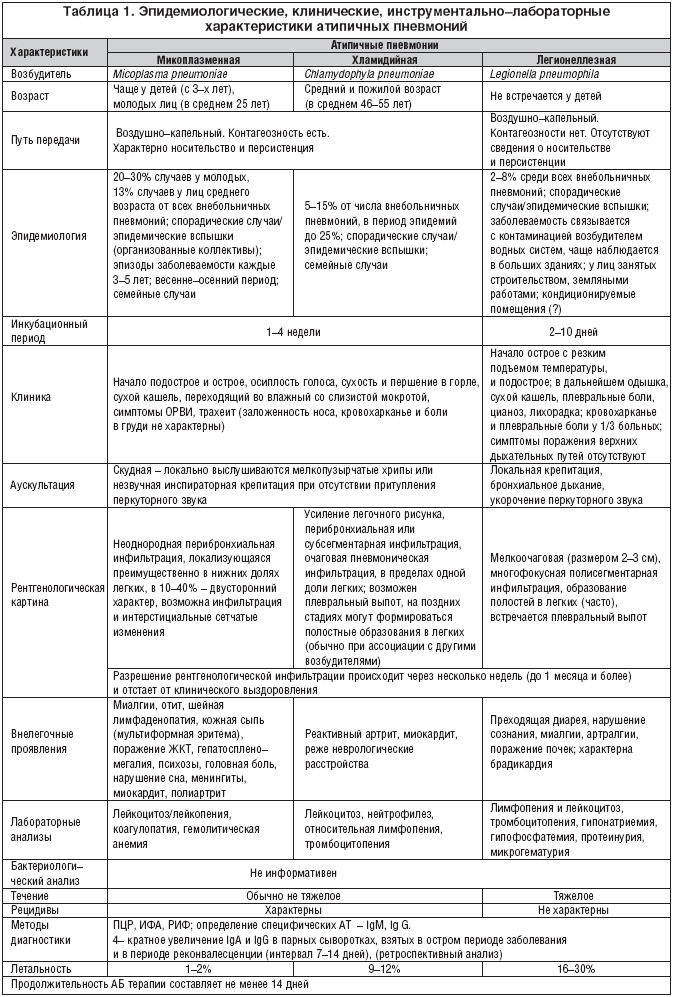
Как правило, микоплазменная и хламидийная пневмонии дебютируют с симптомов ОРВИ и сопровождаются явлениями трахеита, бронхита, фарингита, ларингита; протекают с субфебрилитетом, малопродуктивным кашлем, скудными аускультативными данными. Также очень характерны внелегочные проявления – кожные, суставные, гематологические, гастроэнтерологические, неврологические и другие (табл. 1). Весьма демонстративными являются гематологические показатели, не вписывающиеся в картину типичной пневмонии – отсутствие лейкоцитоза и нейтрофильного сдвига в периферической крови, тромбоцитопении, возможно высокие значения СОЭ. Рентгенологические изменения характеризуются усилением легочного рисунка, перибронхиальной или субсегментарной инфильтрацией (табл. 1) [2,3,5,7].
Несмотря на эффективное и патогенетически–обоснованное использование макролидов, фторхинолонов, доксициклина в лечении атипичных пневмоний, отмечаются случаи неудачи. Имеются сообщения о возникновении повторных инфекций дыхательных путей с тенденцией к обструкции и затяжному течению. Это объясняется снижением антиинфекционной резистентности организма, обусловленного угнетением иммунитета и как внутриклеточной, так и внеклеточной локализацией микроорганизма. Наибольшее значение для лабораторной диагностики хламидийных и микоплазменных пневмоний имеют иммунологические и молекулярно–биологические методы (иммуноферментный анализ, иммунофлюоресценция, полимеразная цепная реакция). Характерные для этих инфекций носительство и персистенция свидетельствуют о необходимости динамического проведения серологических реакций, это не столь актуально для легионелл, для которых не известны случаи носительства и персистенции [7].
Лечение атипичной пневмонии
Микробиологические характеристики возбудителей атипичных пневмоний объясняют отсутствие эффекта от стандартной терапии b–лактамными антибиотиками, действующими на бактериальную стенку, и обусловливают использование антибиотиков, способных проникать и накапливаться в пораженных клетках и блокировать внутриклеточный синтез белка. Из всех антимикробных препаратов такими свойствами обладают макролиды, тетрациклины, фторхинолоны, которые и являются средствами не только антибактериальной, но и эрадикационной терапии. Тем не менее макролиды являются средствами выбора, с учетом особенностей их спектра действия, удачных фармакокинетических и фармакодинамических характеристик, высокого профиля безопасности и хорошей переносимости. Макролиды являются самой безопасной группой антибиотиков. Следует помнить, что тетрациклины противопоказаны при беременности и пациентам с печеночной недостаточностью, к тому же возросла резистентность микроорганизмов к тетрациклинам. Кроме того, по сравнению с тетрациклинами и фторхинолонами макролиды безопасны при лечении новорожденных, детей и беременных. С учетом всего вышеизложенного макролиды (Хемомицин) можно считать препаратами первого ряда для лечения атипичной пневмонии.
Механизм действия макролидов связан с нарушением синтеза белка в клетках микроорганизмов. Макролиды накапливаются в больших количествах в фосфолипидном слое мембран лизосом альвеолярных макрофагов, нейтрофилов, моноцитов и фибробластов, которые составляют самое большое депо препарата [1,9]. Макрофаги, содержащие азитромицин, транспортируют его в очаг инфекционного воспаления, создавая в нем концентрацию выше, чем в здоровых тканях. Для азитромицина характерен постантибиотический эффект, в основе которого лежат необратимые изменения в рибосомах микроорганизма, благодаря чему антибактериальное действие пролонгируется, сохраняясь в течение срока, необходимого для ресинтеза новых функциональных белков микробной клетки. Показано, что процесс диффузии в макрофаги азитромицина (Хемомицина) гораздо дольше (24 ч), чем рокситромицина и кларитромицина (15–20 мин.), но при этом максимальная концентрация азитромицина в клетках сохраняется около 48 ч. Известно, что после приема одного грамма азитромицина его противоинфекционное действие сохраняется до 7 дней. Для макролидов характерно не только антибактериальное, но и противовоспалительное и иммуномодулирующее свойства: ингибирование «окислительного взрыва», в результате чего уменьшается образование окисляющих соединений и, как следствие, снижается способность повреждать собственные ткани и бактериальные клетки (у азитромицина этот эффект в меньшей степени выражен, чем у других макролидов); ингибирование синтеза и секреции провоспалительных цитокинов, таких как интерлейкины–1, –6, –8, фактор некроза опухоли – альфа (ФНО–a), что способствует увеличению секреции противовоспалительных интерлейкинов–2, –4, –10; также макролиды препятствуют адгезии бактерий к поверхности клеток макроорганизма и тормозят экспрессию факторов вирулентности, а по степени влияния на фагоцитоз и киллинг нейтрофилов, (особенно против хламидий) азитромицин занимает первое место по сравнению с другими макролидами [1,6].
Режимы дозирования и способы введения. Несмотря на то, что терапии азитромицином для лечения внебольничных пневмоний составляет 3–5 дней, для терапии атипичных пневмоний курс лечения должен быть не менее чем 2–3 недели (в противном случае повышается риск рецидива инфекции). При нетяжелом течении микоплазменных и хламидийных пневмоний антимикробные препараты назначаются внутрь в среднетерапевтических дозах. При пневмониях тяжелого течения предпочтение следует отдавать внутривенному введению антибиотика. Это особенно важно в лечении легионеллезной пневмонии. Для ее лечения используется комбинация макролида с рифампицином, хотя роль последнего до конца не установлена [5,6]. Для лечения тяжело протекающих атипичных пневмоний используется ступенчатая терапия – после получения адекватного ответа на парентеральное введение антимикробных препаратов возможен переход на пероральные препараты. Таким образом, в лечении атипичных пневмоний вполне рационален переход с внутривенного введения макролидов в высоких дозах на таблетированный прием. Разумеется, пероральные формы антибактериальных препаратов должны обладать высокой биодоступностью, которая характерна для макролидов, в том числе и для азитромицина (Хемомицина). Интерес представляют сообщения о том, что макролиды, преимущественно азитромицин, значительно сокращают сроки госпитализации и снижают вероятность летального исхода. По мнению исследователей, это было связано с противовоспалительными и иммуннокорректирующими свойствами макролидов, причем у азитромицина подобные проявления были более выраженными, чем у кларитромицина [4,8].
Активностью по отношению к атипичным пневмониям также обладают и фторхинолоны – офлоксацин, ципрофлоксацин, в связи с чем эти антимикробные препараты рассматриваются в качестве альтернативы макролидам при данных инфекциях. Высокую активность проявляют новые фторхинолоны – левофлоксацин и моксифлоксацин, которые успешно подавляют практически любую флору, вызывающую пневмонии. Однако их профиль безопасности, уступающий азитромицину, и высокая стоимость вызывают ограничения в применении.
Вывод. Таким образом, азитромицин (Хемомицин) — эффективный, патогенетически обоснованный антибактериальный препарат с высоким профилем безопасности является наряду с другими макролидами препаратом выбора в лечении атипичных пневмоний.
Литература
1. Механизмы воспаления бронхов и легких и противовоспалительная терапия. Под ред. Федосеева Г.Б. С–Петербург: Нормед–издат. 1998.
2. Мусалимова Г.Г., Саперова В.Н., Карзакова Л.М. Микоплазменные и хламидийные пневмонии. Методическая рекомендация. Чебоксары, 2003.
3. Ноников В.Е., Воробьева М.Г. Микоплазменные пневмонии: диагностика и лечение. Consilium Medicum, 2005; N 10, стр. 839–843.
4. Синопальников А.И. Новые горизонты применения макролидов при инфекции дыхательных путей. Российские медицинские вести. 2004; №2, том 9, стр. 16–22.
5. Синопальников А.И. Атипичная пневмония. РМЖ, 2002; том 10, №23, стр. 1080–1085.
6. Страчунский Л.С., Козлов С.Н. Макролиды в современной клинической практике. Смоленск: Русич, 1998.
7. Тартаковский И.С. Современные подходы к диагностике атипичных пневмоний. Клин. Микробиология и антимикробная химиотерапия, 2000; том 2, №1, стр. 60–68.
8. Garcia Vazquez Е, Mensa J., Martinez J.A. et al. Снижение летальности пациентов с внебольничной пневмонией при применении комбинации макролида и бета– лактамного антибиотика по сравнению с монотерапией бета–лактамами. Eur J Clin Microbiol. Infect. Dis., 2005; № 24, 190–195.
9. Rang H.P., Dale M.M., Ritter J.M., Moore P.K. Pharmacology. Fifth edition/ Churchill Livingstone, 2003












