–¶–µ–ї–Є –ї–µ—З–µ–љ–Є—П –°–Я – —А–∞–Ј—А–µ—И–µ–љ–Є–µ –њ–љ–µ–≤–Љ–Њ—В–Њ—А–∞–Ї—Б–∞ (—А–∞—Б–њ—А–∞–≤–ї–µ–љ–Є–µ –ї–µ–≥–Ї–Њ–≥–Њ) –Є –њ—А–µ–і–Њ—В–≤—А–∞—Й–µ–љ–Є–µ –њ–Њ–≤—В–Њ—А–љ—Л—Е –њ–љ–µ–≤–Љ–Њ—В–Њ—А–∞–Ї—Б–Њ–≤ (–њ—А–Њ—Д–Є–ї–∞–Ї—В–Є–Ї–∞ —А–µ—Ж–Є–і–Є–≤–Њ–≤). –Х—Б—В–µ—Б—В–≤–µ–љ–љ–Њ, —В–∞–Ї—В–Є–Ї–∞ –і–Њ—Б—В–Є–ґ–µ–љ–Є—П —Г–Ї–∞–Ј–∞–љ–љ—Л—Е —Ж–µ–ї–µ–є –Ј–∞–≤–Є—Б–Є—В –Њ—В –њ—А–Є—З–Є–љ—Л –њ–љ–µ–≤–Љ–Њ—В–Њ—А–∞–Ї—Б–∞, –µ–≥–Њ –Њ–±—К–µ–Љ–∞ –Є –Њ–±—Й–µ–≥–Њ —Б–Њ—Б—В–Њ—П–љ–Є—П –њ–∞—Ж–Є–µ–љ—В–∞. –Ъ –≤–Њ–Ј–Љ–Њ–ґ–љ—Л–Љ –Љ–µ—В–Њ–і–Є–Ї–∞–Љ –ї–µ—З–µ–љ–Є—П –њ–љ–µ–≤–Љ–Њ—В–Њ—А–∞–Ї—Б–∞ (–Ј–∞ —Б—З–µ—В —Б–Њ–±—Б—В–≤–µ–љ–љ–Њ —Н–≤–∞–Ї—Г–∞—Ж–Є–Є –≤–Њ–Ј–і—Г—Е–∞ –Є–Ј –њ–ї–µ–≤—А–∞–ї—М–љ–Њ–є –њ–Њ–ї–Њ—Б—В–Є) –Њ—В–љ–Њ—Б—П—В—Б—П:
– –њ—Г–љ–Ї—Ж–Є—П –њ–ї–µ–≤—А–∞–ї—М–љ–Њ–є –њ–Њ–ї–Њ—Б—В–Є —Б –∞—Б–њ–Є—А–∞—Ж–Є–µ–є –≤–Њ–Ј–і—Г—Е–∞;
– –і—А–µ–љ–Є—А–Њ–≤–∞–љ–Є–µ –њ–ї–µ–≤—А–∞–ї—М–љ–Њ–є –њ–Њ–ї–Њ—Б—В–Є –њ–Њ –С—О–ї–∞—Г;
– –і—А–µ–љ–Є—А–Њ–≤–∞–љ–Є–µ –њ–ї–µ–≤—А–∞–ї—М–љ–Њ–є –њ–Њ–ї–Њ—Б—В–Є —Б –∞–Ї—В–Є–≤–љ–Њ–є –∞—Б–њ–Є—А–∞—Ж–Є–µ–є.
–Ф–Њ–њ–Њ–ї–љ–Є—В–µ–ї—М–љ–Њ–µ –≤–≤–µ–і–µ–љ–Є–µ –њ—А–µ–њ–∞—А–∞—В–Њ–≤ –і–ї—П –ї–µ–Ї–∞—А—Б—В–≤–µ–љ–љ–Њ–≥–Њ –њ–ї–µ–≤—А–Њ–і–µ–Ј–∞ –љ–∞–њ—А–∞–≤–ї–µ–љ–Њ –љ–∞ –њ—А–Њ—Д–Є–ї–∞–Ї—В–Є–Ї—Г —А–µ—Ж–Є–і–Є–≤–∞.
–Ю—В–Ї—А—Л—В—Л–µ –Њ–њ–µ—А–∞—Ж–Є–Є, –≤–Є–і–µ–Њ–∞—Б—Б–Є—Б—В–Є—А–Њ–≤–∞–љ–љ—Л–µ –≤–Љ–µ—И–∞—В–µ–ї—М—Б—В–≤–∞ –Є—Б–њ–Њ–ї—М–Ј—Г—О—В—Б—П –і–ї—П —Г—И–Є–≤–∞–љ–Є—П –Ї—А—Г–њ–љ—Л—Е –і–µ—Д–µ–Ї—В–Њ–≤ –ї–µ–≥–Њ—З–љ–Њ–є —В–Ї–∞–љ–Є, —А–µ–Ј–µ–Ї—Ж–Є–Є –±—Г–ї–ї–µ–Ј–љ–Њ-–Є–Ј–Љ–µ–љ–µ–љ–љ—Л—Е —Г—З–∞—Б—В–Ї–Њ–≤ –ї–µ–≥–Ї–Њ–≥–Њ, –µ–і–Є–љ–Є—З–љ—Л—Е –Ї—А—Г–њ–љ—Л—Е –±—Г–ї–ї –Є —В. –і. –Я—А–Є —Н—В–Њ–Љ –≤–Њ–Ј–Љ–Њ–ґ–љ–Њ –і–Њ–њ–Њ–ї–љ–Є—В–µ–ї—М–љ–Њ–µ –њ—А–Њ–≤–µ–і–µ–љ–Є–µ –Љ–µ—Е–∞–љ–Є—З–µ—Б–Ї–Њ–≥–Њ, —В–µ—А–Љ–Є—З–µ—Б–Ї–Њ–≥–Њ, —Е–Є–Љ–Є—З–µ—Б–Ї–Њ–≥–Њ –њ–ї–µ–≤—А–Њ–і–µ–Ј–∞. –≠—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В—М –њ–ї–µ–≤—А–Њ–і–µ–Ј–∞, –≤—Л–њ–Њ–ї–љ–µ–љ–љ–Њ–≥–Њ –≤–Њ –≤—А–µ–Љ—П —Е–Є—А—Г—А–≥–Є—З–µ—Б–Ї–Є—Е –≤–Љ–µ—И–∞—В–µ–ї—М—Б—В–≤, –њ—А–µ–≤–Њ—Б—Е–Њ–і–Є—В —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В—М –њ–ї–µ–≤—А–Њ–і–µ–Ј–∞, –њ—А–Њ–≤–µ–і–µ–љ–љ–Њ–≥–Њ –≤–Њ –≤—А–µ–Љ—П –і—А–µ–љ–Є—А–Њ–≤–∞–љ–Є—П –њ–ї–µ–≤—А–∞–ї—М–љ–Њ–є –њ–Њ–ї–Њ—Б—В–Є [3].
–І–∞—Б—В–Њ—В–∞ –Њ—Б–ї–Њ–ґ–љ–µ–љ–Є–є –њ–Њ—Б–ї–µ —В—А–∞–і–Є—Ж–Є–Њ–љ–љ–Њ–є —В–Њ—А–∞–Ї–Њ—В–Њ–Љ–Є–Є –њ–Њ –њ–Њ–≤–Њ–і—Г –°–Я –Љ–Њ–ґ–µ—В –і–Њ—Б—В–Є–≥–∞—В—М 10,4–20%, –∞ –ї–µ—В–∞–ї—М–љ–Њ—Б—В—М – 2,3–4,3%, —З—В–Њ —Б–≤—П–Ј–∞–љ–Њ —Б —А–∞–Ј–≤–Є—В–Є–µ–Љ –Њ—Б–ї–Њ–ґ–љ–µ–љ–Є–є –≤ –њ–Њ—Б–ї–µ–Њ–њ–µ—А–∞—Ж–Є–Њ–љ–љ–Њ–Љ –њ–µ—А–Є–Њ–і–µ, —В–∞–Ї–Є—Е –Ї–∞–Ї —Н–Љ–њ–Є–µ–Љ–∞ –њ–ї–µ–≤—А—Л, –њ–Њ—Б–ї–µ–Њ–њ–µ—А–∞—Ж–Є–Њ–љ–љ–∞—П –њ–љ–µ–≤–Љ–Њ–љ–Є—П, —В—А–Њ–Љ–±–Њ—Н–Љ–±–Њ–ї–Є—П –≤–µ—В–≤–µ–є –ї–µ–≥–Њ—З–љ–Њ–є –∞—А—В–µ—А–Є–Є [4].
–Т –њ–Њ—Б–ї–µ–і–љ–Є–µ –≥–Њ–і—Л –≤ —Б–њ–µ—Ж–Є–∞–ї–Є–Ј–Є—А–Њ–≤–∞–љ–љ—Л—Е —Б—В–∞—Ж–Є–Њ–љ–∞—А–∞—Е –њ–Њ –њ–Њ–≤–Њ–і—Г –°–Я –≤—Л–њ–Њ–ї–љ—П—О—В—Б—П –њ—А–µ–Є–Љ—Г—Й–µ—Б—В–≤–µ–љ–љ–Њ –≤–Є–і–µ–Њ–∞—Б—Б–Є—Б—В–Є—А–Њ–≤–∞–љ–љ—Л–µ –Њ–њ–µ—А–∞—Ж–Є–Є, –∞ —Б—А–µ–і–Є –≤—Б–µ—Е —В–Њ—А–∞–Ї–Њ—Б–Ї–Њ–њ–Є—З–µ—Б–Ї–Є—Е –Њ–њ–µ—А–∞—Ж–Є–є –≤–Є–і–µ–Њ—В–Њ—А–∞–Ї–Њ—Б–Ї–Њ–њ–Є—П (–Т–Ґ–°) –њ–Њ –њ–Њ–≤–Њ–і—Г –°–Я —Б–Њ—Б—В–∞–≤–ї—П–µ—В –Њ–Ї–Њ–ї–Њ 45% [1]. –Т–Њ –Љ–љ–Њ–≥–Є—Е —Ж–µ–љ—В—А–∞—Е –≤–Є–і–µ–Њ–∞—Б—Б–Њ—Ж–Є–Є—А–Њ–≤–∞–љ–љ–∞—П —В–Њ—А–∞–Ї–Њ—Б–Ї–Њ–њ–Є—П —П–≤–ї—П–µ—В—Б—П –Њ—Б–љ–Њ–≤–љ—Л–Љ —Е–Є—А—Г—А–≥–Є—З–µ—Б–Ї–Є–Љ –Љ–µ—В–Њ–і–Њ–Љ –ї–µ—З–µ–љ–Є—П –њ–љ–µ–≤–Љ–Њ—В–Њ—А–∞–Ї—Б–∞. –Ю—З–µ–≤–Є–і–љ—Л –њ—А–µ–Є–Љ—Г—Й–µ—Б—В–≤–∞ –Љ–µ—В–Њ–і–∞ –њ–Њ —Б—А–∞–≤–љ–µ–љ–Є—О —Б –Њ—В–Ї—А—Л—В–Њ–є —В–Њ—А–∞–Ї–Њ—В–Њ–Љ–Є–µ–є: —Б–Њ–Ї—А–∞—Й–µ–љ–Є–µ –≤—А–µ–Љ–µ–љ–Є –Њ–њ–µ—А–∞—Ж–Є–Є –Є –і—А–µ–љ–Є—А–Њ–≤–∞–љ–Є—П, —Г–Љ–µ–љ—М—И–µ–љ–Є–µ —З–Є—Б–ї–∞ –њ–Њ—Б—В–Њ–њ–µ—А–∞—Ж–Є–Њ–љ–љ—Л—Е –Њ—Б–ї–Њ–ґ–љ–µ–љ–Є–є, –Љ–µ–љ–µ–µ –≤—Л—А–∞–ґ–µ–љ–љ—Л–є –±–Њ–ї–µ–≤–Њ–є —Б–Є–љ–і—А–Њ–Љ –≤ –њ–Њ—Б–ї–µ–Њ–њ–µ—А–∞—Ж–Є–Њ–љ–љ–Њ–Љ –њ–µ—А–Є–Њ–і–µ, —Г–Љ–µ–љ—М—И–µ–љ–Є–µ –Њ–±—Й–µ–≥–Њ —З–Є—Б–ї–∞ –Ї–Њ–є–Ї–Њ-–і–љ–µ–є. –Я–Њ –і–∞–љ–љ—Л–Љ –Љ—Г–ї—М—В–Є—Ж–µ–љ—В—А–Њ–≤–Њ–≥–Њ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П, —З–Є—Б–ї–Њ —А–µ—Ж–Є–і–Є–≤–Њ–≤ –њ–љ–µ–≤–Љ–Њ—В–Њ—А–∞–Ї—Б–Њ–≤ –њ–Њ—Б–ї–µ –Т–Р–Ґ —Б–Њ—Б—В–∞–≤–ї—П–µ—В 4% [4]. –Ф—А—Г–≥–Є–µ –∞–≤—В–Њ—А—Л –Њ—В–Љ–µ—З–∞—О—В –µ—Й–µ –±–Њ–ї–µ–µ –љ–Є–Ј–Ї–Є–є —Г—А–Њ–≤–µ–љ—М —А–µ—Ж–Є–і–Є–≤–∞ –°–Я –њ–Њ—Б–ї–µ –Т–Ґ–° –ї–µ—З–µ–љ–Є—П – 1,3% [1], –∞ –Њ—Б–ї–Њ–ґ–љ–µ–љ–Є–є, –њ—А–Є—Б—Г—Й–Є—Е —Б—В–∞–љ–і–∞—А—В–љ–Њ–є —В–Њ—А–∞–Ї–Њ—В–Њ–Љ–Є–Є, –љ–µ –љ–∞–±–ї—О–і–∞–µ—В—Б—П [1]. –І–∞—Б—В–Њ—В–∞ —А–∞–Ј–≤–Є—В–Є—П –ѓ–Я: –њ—А–Є —В—А–∞–љ—Б—В–Њ—А–∞–Ї–∞–ї—М–љ–Њ–є —В–Њ–љ–Ї–Њ–Є–≥–Њ–ї—М–љ–Њ–є –њ—Г–љ–Ї—Ж–Є–Њ–љ–љ–Њ–є –±–Є–Њ–њ—Б–Є–Є – 15–37%, –≤ —Б—А–µ–і–љ–µ–Љ – 10% [5]; –њ—А–Є –Ї–∞—В–µ—В–µ—А–Є–Ј–∞—Ж–Є–Є —Ж–µ–љ—В—А–∞–ї—М–љ—Л—Е –≤–µ–љ – 1–10% [6]; –њ—А–Є —В–Њ—А–∞–Ї–Њ—Ж–µ–љ—В–µ–Ј–µ – 5–20% [7]; –њ—А–Є –±–Є–Њ–њ—Б–Є–Є –њ–ї–µ–≤—А—Л – 10% [8]; –њ—А–Є —В—А–∞–љ—Б–±—А–Њ–љ—Е–Є–∞–ї—М–љ–Њ–є –±–Є–Њ–њ—Б–Є–Є –ї–µ–≥–Ї–Є—Е – 1–2% [9]; –≤–Њ –≤—А–µ–Љ—П –Є—Б–Ї—Г—Б—Б—В–≤–µ–љ–љ–Њ–є –≤–µ–љ—В–Є–ї—П—Ж–Є–Є –ї–µ–≥–Ї–Є—Е – 5–15% [10].
–Ь–∞—В–µ—А–Є–∞–ї—Л –Є –Љ–µ—В–Њ–і—Л
–° 1970 –њ–Њ 2013 –≥. –≤ –Њ—В–і–µ–ї–µ–љ–Є–Є —В–Њ—А–∞–Ї–∞–ї—М–љ–Њ–є —Е–Є—А—Г—А–≥–Є–Є –У–Ъ–С вДЦ 61 –њ–Њ –њ–Њ–≤–Њ–і—Г –њ–љ–µ–≤–Љ–Њ—В–Њ—А–∞–Ї—Б–∞ –љ–∞—Е–Њ–і–Є–ї–Њ—Б—М –љ–∞ –ї–µ—З–µ–љ–Є–Є 882 –±–Њ–ї—М–љ—Л—Е (–≤ 1970–1986 –≥–≥. – 144 —З–µ–ї–Њ–≤–µ–Ї–∞, –≤ 1987–1995 –≥–≥. – 174, –≤ 1996–2013 –≥–≥. – 564). –Ф–Њ 1987 –≥. –µ–і–Є–љ—Б—В–≤–µ–љ–љ—Л–Љ –Љ–µ—В–Њ–і–Њ–Љ –ї–µ—З–µ–љ–Є—П –њ–љ–µ–≤–Љ–Њ—В–Њ—А–∞–Ї—Б–∞, –њ—А–Є–љ—П—В—Л–Љ –≤ –Ї–ї–Є–љ–Є–Ї–µ, –±—Л–ї–Њ –і—А–µ–љ–Є—А–Њ–≤–∞–љ–Є–µ –њ–ї–µ–≤—А–∞–ї—М–љ–Њ–є –њ–Њ–ї–Њ—Б—В–Є —Б –∞–Ї—В–Є–≤–љ–Њ–є –∞—Б–њ–Є—А–∞—Ж–Є–µ–є. –Ф–ї—П –∞–Ї—В–Є–≤–љ–Њ–є –∞—Б–њ–Є—А–∞—Ж–Є–Є –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–ї–Є—Б—М —А–∞–Ј–ї–Є—З–љ—Л–µ –∞–њ–њ–∞—А–∞—В—Л: –Њ—В «–Ю–Я-1» –і–Њ –±–Њ–ї–µ–µ —Б–Њ–≤—А–µ–Љ–µ–љ–љ—Л—Е «–≠–ї–µ–Љ–∞-–Э –Я–†–Ю 1» –Є «Medela».
–° 1987 –≥. –≤ –і–Њ–њ–Њ–ї–љ–µ–љ–Є–µ –Ї –і—А–µ–љ–Є—А–Њ–≤–∞–љ–Є—О –њ–ї–µ–≤—А–∞–ї—М–љ–Њ–є –њ–Њ–ї–Њ—Б—В–Є –љ–∞—З–∞–ї –њ—А–Є–Љ–µ–љ—П—В—М—Б—П –ї–µ–Ї–∞—А—Б—В–≤–µ–љ–љ—Л–є –њ–ї–µ–≤—А–Њ–і–µ–Ј. –Ф–ї—П –µ–≥–Њ –њ—А–Њ–≤–µ–і–µ–љ–Є—П –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–ї–Є —В–µ—В—А–∞—Ж–Є–Ї–ї–Є–љ (20 –Љ–≥ –љ–∞ 1 –Ї–≥ –Љ–∞—Б—Б—Л —В–µ–ї–∞ –±–Њ–ї—М–љ–Њ–≥–Њ), –Љ–Њ—А—Д–Њ—Ж–Є–Ї–ї–Є–љ 0,3 –≥ (—Б—Г—В–Њ—З–љ–∞—П –і–Њ–Ј–∞), –≤ –њ–Њ—Б–ї–µ–і–љ–µ–µ –≤—А–µ–Љ—П – –і–Њ–Ї—Б–Є—Ж–Є–Ї–ї–Є–љ (20 –Љ–≥ –љ–∞ 1 –Ї–≥ –Љ–∞—Б—Б—Л —В–µ–ї–∞ –±–Њ–ї—М–љ–Њ–≥–Њ). –Ы–µ–Ї–∞—А—Б—В–≤–µ–љ–љ—Л–є –њ–ї–µ–≤—А–Њ–і–µ–Ј –њ—А–Њ–≤–Њ–і–Є–ї–Є –Ї–∞–Ї –њ—А–Є –Њ–њ–µ—А–∞—В–Є–≤–љ–Њ–Љ, —В–∞–Ї –Є –њ—А–Є –Ї–Њ–љ—Б–µ—А–≤–∞—В–Є–≤–љ–Њ–Љ –ї–µ—З–µ–љ–Є–Є –њ–љ–µ–≤–Љ–Њ—В–Њ—А–∞–Ї—Б–∞. –Я—А–Є –Њ–њ–µ—А–∞—В–Є–≤–љ–Њ–Љ –ї–µ—З–µ–љ–Є–Є –≤ –њ–ї–µ–≤—А–∞–ї—М–љ—Г—О –њ–Њ–ї–Њ—Б—В—М –≤–≤–Њ–і–Є–ї–Є 0,8 –≥ (–Љ–∞–Ї—Б–Є–Љ–∞–ї—М–љ–∞—П —Б—Г—В–Њ—З–љ–∞—П –і–Њ–Ј–∞) —А–∞—Б—В–≤–Њ—А–∞ –і–Њ–Ї—Б–Є—Ж–Є–Ї–ї–Є–љ–∞ –≤ 50 –Љ–ї 0,9% NaCl. –Т—Б–µ–≥–Њ —Б 1987 –њ–Њ 2013 –≥. –≤—Л–њ–Њ–ї–љ–µ–љ–Њ 250 –ї–µ–Ї–∞—А—Б—В–≤–µ–љ–љ—Л—Е –њ–ї–µ–≤—А–Њ–і–µ–Ј–Њ–≤ –≤ –њ—А–Њ—Ж–µ—Б—Б–µ –Ї–Њ–љ—Б–µ—А–≤–∞—В–Є–≤–љ–Њ–≥–Њ –ї–µ—З–µ–љ–Є—П –њ–љ–µ–≤–Љ–Њ—В–Њ—А–∞–Ї—Б–∞. –Ч–∞ –њ–µ—А–Є–Њ–і —Б 1987 –њ–Њ 1995 –≥. –≤—Л–њ–Њ–ї–љ–µ–љ–Њ –≤—Б–µ–≥–Њ 2 –Њ–њ–µ—А–∞—Ж–Є–Є – –∞—В–Є–њ–Є—З–љ—Л–µ —А–µ–Ј–µ–Ї—Ж–Є–Є –ї–µ–≥–Ї–Њ–≥–Њ —Б –њ—А–Є–Љ–µ–љ–µ–љ–Є–µ–Љ —Б—И–Є–≤–∞—О—Й–Є—Е –∞–њ–њ–∞—А–∞—В–Њ–≤ –£–Ф–Ю, –£–Ю, –£–°. –Ф–Њ—Б—В—Г–њ, –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–≤—И–Є–є—Б—П –њ—А–Є –Њ–њ–µ—А–∞—Ж–Є—П—Е, – –±–Њ–Ї–Њ–≤–∞—П —В–Њ—А–∞–Ї–Њ—В–Њ–Љ–Є—П. –° –≤–љ–µ–і—А–µ–љ–Є–µ–Љ –≤–Є–і–µ–Њ—Н–љ–і–Њ—Б–Ї–Њ–њ–Є—З–µ—Б–Ї–Є—Е —В–µ—Е–љ–Њ–ї–Њ–≥–Є–є (—Б 1996 –≥.) –Њ–њ–µ—А–∞—В–Є–≤–љ–∞—П –∞–Ї—В–Є–≤–љ–Њ—Б—В—М –њ—А–Є –ї–µ—З–µ–љ–Є–Є –њ–љ–µ–≤–Љ–Њ—В–Њ—А–∞–Ї—Б–∞ —Б–Њ—Б—В–∞–≤–Є–ї–∞ 28,5%, –Ј–∞ –њ–Њ—Б–ї–µ–і–љ–Є–µ 3 –≥–Њ–і–∞ —Н—В–∞ —Ж–Є—Д—А–∞ –≤—Л—А–Њ—Б–ї–∞ –і–Њ 61,7% –њ—А–Є —А–∞–Ј–≤–Є—В–Є–Є –њ–љ–µ–≤–Љ–Њ—В–Њ—А–∞–Ї—Б–∞ —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –±—Г–ї–ї–µ–Ј–љ–Њ–є –±–Њ–ї–µ–Ј–љ—М—О –ї–µ–≥–Ї–Є—Е. –° 1996 –њ–Њ 2013 –≥. –≤—Л–њ–Њ–ї–љ–µ–љ–Њ —Б—Г–Љ–Љ–∞—А–љ–Њ 170 –Њ–њ–µ—А–∞—Ж–Є–є –њ–Њ –њ–Њ–≤–Њ–і—Г –њ–љ–µ–≤–Љ–Њ—В–Њ—А–∞–Ї—Б–∞.
–Ф–ї—П –Т–Ґ–° –∞—В–Є–њ–Є—З–љ–Њ–є —А–µ–Ј–µ–Ї—Ж–Є–Є –±—Г–ї–ї–µ–Ј–љ–Њ –Є–Ј–Љ–µ–љ–µ–љ–љ—Л—Е —Г—З–∞—Б—В–Ї–Њ–≤ –ї–µ–≥–Њ—З–љ–Њ–є —В–Ї–∞–љ–Є –њ—А–Є–Љ–µ–љ—П—О—В—Б—П —Н–љ–і–Њ—Б—В–µ–њ–ї–µ—А—Л. –Я—А–Є –≤–Є–і–µ–Њ–∞—Б—Б–Є—Б—В–Є—А–Њ–≤–∞–љ–љ—Л—Е –Њ–њ–µ—А–∞—Ж–Є—П—Е –Є–Ј –Љ–Є–љ–Є-–і–Њ—Б—В—Г–њ–∞ –љ–∞–Є–±–Њ–ї–µ–µ —З–∞—Б—В–Њ –Є—Б–њ–Њ–ї—М–Ј—Г—О—В—Б—П —Б—И–Є–≤–∞—О—Й–Є–µ –∞–њ–њ–∞—А–∞—В—Л –£–Ф–Ю-20 –Є –£–Ф–Ю-30. –Ф–ї—П –Ї–Њ–∞–≥—Г–ї—П—Ж–Є–Є –±—Г–ї–ї–µ–Ј–љ–Њ-—Д–Є–±—А–Њ–Ј–љ–Њ –Є–Ј–Љ–µ–љ–µ–љ–љ—Л—Е —Г—З–∞—Б—В–Ї–Њ–≤ –ї–µ–≥–Ї–Є—Е –Є, –≤ –±–Њ–ї—М—И–µ–є —Б—В–µ–њ–µ–љ–Є, –і–ї—П –Ї–Њ–∞–≥—Г–ї—П—Ж–Є–Є —Б—Г–±–њ–ї–µ–≤—А–∞–ї—М–љ—Л—Е –њ—Г–Ј—Л—А—М–Ї–Њ–≤ –Є —В–µ—А–Љ–Є—З–µ—Б–Ї–Њ–≥–Њ –њ–ї–µ–≤—А–Њ–і–µ–Ј–∞ –њ—А–Є–Љ–µ–љ—П–ї–Є—Б—М —В–µ—А–Љ–Є—З–µ—Б–Ї–Є–µ —Е–Є—А—Г—А–≥–Є—З–µ—Б–Ї–Є–µ –Є–љ—Б—В—А—Г–Љ–µ–љ—В—Л.
–Ю–њ–µ—А–∞—Ж–Є—П –≤—Л–±–Њ—А–∞ – –Т–Ґ–° —Б –∞—В–Є–њ–Є—З–љ–Њ–є —А–µ–Ј–µ–Ї—Ж–Є–µ–є –ї–µ–≥–Ї–Њ–≥–Њ, –Ї–Њ–∞–≥—Г–ї—П—Ж–Є–µ–є –±—Г–ї–ї —В–µ—А–Љ–Є—З–µ—Б–Ї–Є–Љ–Є —Е–Є—А—Г—А–≥–Є—З–µ—Б–Ї–Є–Љ–Є –Є–љ—Б—В—А—Г–Љ–µ–љ—В–∞–Љ–Є, —В–µ—А–Љ–Є—З–µ—Б–Ї–Њ–є –њ–ї–µ–≤—А–Њ–і–µ—Б—В—А—Г–Ї—Ж–Є–µ–є –њ–∞—А–Є–µ—В–∞–ї—М–љ–Њ–є –њ–ї–µ–≤—А—Л —Н—В–Є–Љ–Є –ґ–µ –Є–љ—Б—В—А—Г–Љ–µ–љ—В–∞–Љ–Є –Є –ї–µ–Ї–∞—А—Б—В–≤–µ–љ–љ—Л–Љ –њ–ї–µ–≤—А–Њ–і–µ–Ј–Њ–Љ —А–∞—Б—В–≤–Њ—А–Њ–Љ –і–Њ–Ї—Б–Є—Ж–Є–Ї–ї–Є–љ–∞.
–†–µ–Ј—Г–ї—М—В–∞—В—Л –Є –Њ–±—Б—Г–ґ–і–µ–љ–Є–µ
–Т—Л–њ–Њ–ї–љ–µ–љ–Њ 140 –Т–Ґ–° –Њ–њ–µ—А–∞—Ж–Є–є: 114 –Т–Ґ–° + –∞—В–Є–њ–Є—З–љ–∞—П —А–µ–Ј–µ–Ї—Ж–Є—П –ї–µ–≥–Ї–Њ–≥–Њ (81,4%), 26 –Т–Ґ–° + –Ї–Њ–∞–≥—Г–ї—П—Ж–Є—П –±—Г–ї–ї –Є/–Є–ї–Є –і–µ–њ–ї–µ–≤—А–Є–Ј–Є—А–Њ–≤–∞–љ–љ—Л—Е —Г—З–∞—Б—В–Ї–Њ–≤ –ї–µ–≥–Ї–Њ–≥–Њ (18,5%). –Э–∞–Є–±–Њ–ї–µ–µ —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ–є —Б—В–∞–ї–∞ –Ї–Њ–∞–≥—Г–ї—П—Ж–Є—П –±—Г–ї–ї –Є –±–ї–µ–±—Б–Њ–≤ –њ–ї–∞–Ј–Љ–µ–љ–љ—Л–Љ –њ–Њ—В–Њ–Ї–Њ–Љ. 36 –±–Њ–ї—М–љ—Л–Љ –њ—А–Њ–≤–µ–і–µ–љ–∞ –∞—В–Є–њ–Є—З–љ–∞—П —А–µ–Ј–µ–Ї—Ж–Є—П –ї–µ–≥–Ї–Њ–≥–Њ –Є–Ј –Љ–Є–љ–Є-—В–Њ—А–∞–Ї–Њ—В–Њ–Љ–Є—З–µ—Б–Ї–Њ–≥–Њ –і–Њ—Б—В—Г–њ–∞ —Б –≤–Є–і–µ–Њ–∞—Б—Б–Є—Б—В–µ–љ—Ж–Є–µ–є –Є –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є–µ–Љ —Б—И–Є–≤–∞—О—Й–Є—Е –∞–њ–њ–∞—А–∞—В–Њ–≤ –£–Ф–Ю. 8 —А–∞–Ј –і–ї—П –≤—Л–њ–Њ–ї–љ–µ–љ–Є—П –∞—В–Є–њ–Є—З–љ–Њ–є —А–µ–Ј–µ–Ї—Ж–Є–Є –ї–µ–≥–Ї–Њ–≥–Њ –њ—А–Є–Љ–µ–љ—П–ї–∞—Б—М —В—А–∞–і–Є—Ж–Є–Њ–љ–љ–∞—П —В–Њ—А–∞–Ї–Њ—В–Њ–Љ–Є—П.
–Ч–∞ –њ–Њ—Б–ї–µ–і–љ–Є–µ –≥–Њ–і—Л (2003–2013) –≤ —В–Њ—А–∞–Ї–∞–ї—М–љ–Њ–Љ –Њ—В–і–µ–ї–µ–љ–Є–Є –У–Ъ–С вДЦ 61 –љ–∞–±–ї—О–і–∞–ї–Є—Б—М 165 –±–Њ–ї—М–љ—Л—Е –ѓ–Я, 94 –њ–∞—Ж–Є–µ–љ—В–∞ –±—Л–ї–Є –њ–µ—А–µ–≤–µ–і–µ–љ—Л –Є–Ј —Б—В–∞—Ж–Є–Њ–љ–∞—А–Њ–≤ –≥. –Ь–Њ—Б–Ї–≤—Л –Є 71 – –Є–Ј –і—А—Г–≥–Є—Е –Њ—В–і–µ–ї–µ–љ–Є–є –±–Њ–ї—М–љ–Є—Ж—Л. –У–ї–∞–≤–љ—Л–Љ–Є –њ—А–Є—З–Є–љ–∞–Љ–Є –ѓ–Я –±—Л–ї–Є: –Ї–∞—В–µ—В–µ—А–Є–Ј–∞—Ж–Є—П —Ж–µ–љ—В—А–∞–ї—М–љ–Њ–є (–≤ –Њ—Б–љ–Њ–≤–љ–Њ–Љ –њ–Њ–і–Ї–ї—О—З–Є—З–љ–Њ–є) –≤–µ–љ—Л –Є –њ–ї–µ–≤—А–∞–ї—М–љ–∞—П –њ—Г–љ–Ї—Ж–Є—П –њ–Њ –њ–Њ–≤–Њ–і—Г –≥–Є–і—А–Њ—В–Њ—А–∞–Ї—Б–∞ —А–∞–Ј–ї–Є—З–љ–Њ–≥–Њ –њ—А–Њ–Є—Б—Е–Њ–ґ–і–µ–љ–Є—П, —А–µ–ґ–µ – –±–∞—А–Њ—В—А–∞–≤–Љ–∞ –њ—А–Є –Є—Б–Ї—Г—Б—Б—В–≤–µ–љ–љ–Њ–є –≤–µ–љ—В–Є–ї—П—Ж–Є–Є –ї–µ–≥–Ї–Є—Е, –µ—Й–µ —А–µ–ґ–µ – –њ—А–Є —В—А–∞–љ—Б—В–Њ—А–∞–Ї–∞–ї—М–љ–Њ–є –Є–ї–Є —В—А–∞–љ—Б–±—А–Њ–љ—Е–Є–∞–ї—М–љ–Њ–є –њ—Г–љ–Ї—Ж–Є–Њ–љ–љ–Њ–є –±–Є–Њ–њ—Б–Є–Є –ї–µ–≥–Ї–Њ–≥–Њ. –Ю—Б–љ–Њ–≤–љ—Л–Љ –њ–Њ–≤–Њ–і–Њ–Љ –і–ї—П –њ–µ—А–µ–≤–Њ–і–∞ –≤ –Њ—В–і–µ–ї–µ–љ–Є–µ –Є–Ј –і—А—Г–≥–Є—Е —Б—В–∞—Ж–Є–Њ–љ–∞—А–Њ–≤ –±—Л–ї —А–µ—Ж–Є–і–Є–≤ –њ–љ–µ–≤–Љ–Њ—В–Њ—А–∞–Ї—Б–∞ –њ–Њ—Б–ї–µ –Ї—А–∞—В–Ї–Њ–≤—А–µ–Љ–µ–љ–љ–Њ–≥–Њ –і—А–µ–љ–Є—А–Њ–≤–∞–љ–Є—П –њ–ї–µ–≤—А–∞–ї—М–љ–Њ–є –њ–Њ–ї–Њ—Б—В–Є: –і—А–µ–љ–∞–ґ —Г–і–∞–ї—П–ї—Б—П –≤ –њ–µ—А–≤—Л–µ —Б—Г—В–Ї–Є (–Є–ї–Є —Б—А–∞–Ј—Г) –њ–Њ—Б–ї–µ —А–∞—Б–њ—А–∞–≤–ї–µ–љ–Є—П –ї–µ–≥–Ї–Њ–≥–Њ, —З—В–Њ —В—А–µ–±–Њ–≤–∞–ї–Њ –њ–Њ–≤—В–Њ—А–љ–Њ–≥–Њ (—З–∞—Б—В–Њ –Љ–љ–Њ–≥–Њ–Ї—А–∞—В–љ–Њ–≥–Њ) –і—А–µ–љ–Є—А–Њ–≤–∞–љ–Є—П –њ–ї–µ–≤—А–∞–ї—М–љ–Њ–є –њ–Њ–ї–Њ—Б—В–Є. –†–∞–љ–љ–µ–µ —Г–і–∞–ї–µ–љ–Є–µ –і—А–µ–љ–∞–ґ–∞ –Њ–±—К—П—Б–љ—П–ї–Њ—Б—М –Њ–њ–∞—Б–µ–љ–Є–µ–Љ –Є–љ—Д–Є—Ж–Є—А–Њ–≤–∞–љ–Є—П –њ–ї–µ–≤—А–∞–ї—М–љ–Њ–є –њ–Њ–ї–Њ—Б—В–Є –Є —А–∞–Ј–≤–Є—В–Є–µ–Љ —Б–≤—П–Ј–∞–љ–љ—Л—Е —Б —Н—В–Є–Љ –Њ—Б–ї–Њ–ґ–љ–µ–љ–Є–є – —Н–Љ–њ–Є–µ–Љ—Л –њ–ї–µ–≤—А—Л.
–†–µ—Ж–Є–і–Є–≤—Л –њ—А–Є –ї–µ—З–µ–љ–Є–Є –°–Я –Љ–µ—В–Њ–і–Њ–Љ –і—А–µ–љ–Є—А–Њ–≤–∞–љ–Є—П –Є –њ—Г–љ–Ї—Ж–Є–Є –њ–ї–µ–≤—А–∞–ї—М–љ–Њ–є –њ–Њ–ї–Њ—Б—В–Є –љ–∞–±–ї—О–і–∞–ї–Є—Б—М –≤ 21,5% —Б–ї—Г—З–∞–µ–≤; –њ—А–Є –і—А–µ–љ–Є—А–Њ–≤–∞–љ–Є–Є —Б –њ–Њ—Б–ї–µ–і—Г—О—Й–Є–Љ –ї–µ–Ї–∞—А—Б—В–≤–µ–љ–љ—Л–Љ –њ–ї–µ–≤—А–Њ–і–µ–Ј–Њ–Љ – –≤ 5,5%. –†–∞–љ–љ–Є—Е —А–µ—Ж–Є–і–Є–≤–Њ–≤ –љ–µ –±—Л–ї–Њ (–њ–Њ—Б–ї–µ –і—А–µ–љ–Є—А–Њ–≤–∞–љ–Є—П –±–µ–Ј –њ–ї–µ–≤—А–Њ–і–µ–Ј–∞ –≤ –±–ї–Є–ґ–∞–є—И–Є–µ 10 –і–љ–µ–є –њ–Њ—Б–ї–µ –≤—Л–њ–Є—Б–Ї–Є —А–µ—Ж–Є–і–Є–≤–љ—Л–є –њ–љ–µ–≤–Љ–Њ—В–Њ—А–∞–Ї—Б —А–∞–Ј–≤–Є–≤–∞–ї—Б—П –≤ 4,9% —Б–ї—Г—З–∞–µ–≤). –Х–і–Є–љ—Б—В–≤–µ–љ–љ–Њ–µ –Њ—Б–ї–Њ–ґ–љ–µ–љ–Є–µ –і—А–µ–љ–Є—А–Њ–≤–∞–љ–Є—П –њ–ї–µ–≤—А–∞–ї—М–љ–Њ–є –њ–Њ–ї–Њ—Б—В–Є – –њ–Њ–і–Ї–Њ–ґ–љ–∞—П —Н–Љ—Д–Є–Ј–µ–Љ–∞. –Ю—Б–ї–Њ–ґ–љ–µ–љ–Є–є, —Б–≤—П–Ј–∞–љ–љ—Л—Е —Б –≤—Л–њ–Њ–ї–љ–µ–љ–Є–µ–Љ –ї–µ–Ї–∞—А—Б—В–≤–µ–љ–љ–Њ–≥–Њ –њ–ї–µ–≤—А–Њ–і–µ–Ј–∞, –љ–µ –љ–∞–±–ї—О–і–∞–ї–Њ—Б—М.
–Т —Б–Њ–Њ—В–≤–µ—В—Б—В–≤–Є–Є —Б –љ–∞—Ж–Є–Њ–љ–∞–ї—М–љ—Л–Љ–Є –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є–Љ–Є —А–µ–Ї–Њ–Љ–µ–љ–і–∞—Ж–Є—П–Љ–Є –њ–Њ –і–Є–∞–≥–љ–Њ—Б—В–Є–Ї–µ –Є –ї–µ—З–µ–љ–Є—О –°–Я, –≤—Л–ґ–Є–і–∞—В–µ–ї—М–љ–∞—П —В–∞–Ї—В–Є–Ї–∞ –і–Њ–њ—Г—Б—В–Є–Љ–∞ –њ—А–Є –Њ–±—К–µ–Љ–µ —Б–њ–Њ–љ—В–∞–љ–љ–Њ–≥–Њ –Њ–≥—А–∞–љ–Є—З–µ–љ–љ–Њ–≥–Њ –≤–µ—А—Е—Г—И–µ—З–љ–Њ–≥–Њ –њ–љ–µ–≤–Љ–Њ—В–Њ—А–∞–Ї—Б–∞ –Љ–µ–љ–µ–µ 15% —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –Њ—В—Б—Г—В—Б—В–≤–Є–µ–Љ –і–Є—Б–њ–љ–Њ—Н. –Я—А–Є –љ–∞–ї–Є—З–Є–Є —Г —В–∞–Ї–Є—Е –њ–∞—Ж–Є–µ–љ—В–Њ–≤ –±—Г–ї–ї–µ–Ј–љ–Њ–є –±–Њ–ї–µ–Ј–љ–Є –Є –Њ—В—Б—Г—В—Б—В–≤–Є–Є –њ—А–Њ—В–Є–≤–Њ–њ–Њ–Ї–∞–Ј–∞–љ–Є–є –њ—А–Њ—Д–Є–ї–∞–Ї—В–Є–Ї–Њ–є —А–µ—Ж–Є–і–Є–≤–∞ –±—Г–і–µ—В –њ—А–Њ–≤–µ–і–µ–љ–Є–µ –Њ–њ–µ—А–∞—В–Є–≤–љ–Њ–≥–Њ –ї–µ—З–µ–љ–Є—П –≤ –Њ–±—К–µ–Љ–µ —А–µ–Ј–µ–Ї—Ж–Є–Є –±—Г–ї–ї–µ–Ј–љ–Њ-–Є–Ј–Љ–µ–љ–µ–љ–љ—Л—Е —Г—З–∞—Б—В–Ї–Њ–≤ –ї–µ–≥–Њ—З–љ–Њ–є —В–Ї–∞–љ–Є. –Я—А–Є –Њ–±—К–µ–Љ–µ –њ–љ–µ–≤–Љ–Њ—В–Њ—А–∞–Ї—Б–∞ –і–Њ 30% —Г –±–Њ–ї—М–љ—Л—Е –±–µ–Ј –≤—Л—А–∞–ґ–µ–љ–љ–Њ–≥–Њ –і–Є—Б–њ–љ–Њ—Н –Љ–Њ–ґ–љ–Њ –Њ–і–љ–Њ–Ї—А–∞—В–љ–Њ –Њ—Б—Г—Й–µ—Б—В–≤–Є—В—М –њ–ї–µ–≤—А–∞–ї—М–љ—Г—О –њ—Г–љ–Ї—Ж–Є—О —Б –∞—Б–њ–Є—А–∞—Ж–Є–µ–є –≤–Њ–Ј–і—Г—Е–∞. –Я—А–Њ—Д–Є–ї–∞–Ї—В–Є–Ї–∞ —А–µ—Ж–Є–і–Є–≤–∞ –і–Њ—Б—В–Є–≥–∞–µ—В—Б—П —В–∞–Ї –ґ–µ, –Ї–∞–Ї –Є –≤ –њ—А–µ–і—Л–і—Г—Й–µ–Љ —Б–ї—Г—З–∞–µ.
–Ф—А–µ–љ–Є—А–Њ–≤–∞–љ–Є–µ –њ–ї–µ–≤—А–∞–ї—М–љ–Њ–є –њ–Њ–ї–Њ—Б—В–Є –њ–Њ–Ї–∞–Ј–∞–љ–Њ –њ—А–Є –Њ–±—К–µ–Љ–µ –њ–љ–µ–≤–Љ–Њ—В–Њ—А–∞–Ї—Б–∞ –±–Њ–ї–µ–µ 30%, —А–µ—Ж–Є–і–Є–≤–µ –њ–љ–µ–≤–Љ–Њ—В–Њ—А–∞–Ї—Б–∞, –љ–µ—Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В–Є –њ—Г–љ–Ї—Ж–Є–Є, —Г –±–Њ–ї—М–љ—Л—Е —Б –і–Є—Б–њ–љ–Њ—Н –Є –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б—В–∞—А—И–µ 50 –ї–µ—В. –Ъ–ї—О—З–µ–≤—Л–µ –Љ–Њ–Љ–µ–љ—В—Л –њ—А–∞–≤–Є–ї—М–љ–Њ–є –њ–Њ—Б—В–∞–љ–Њ–≤–Ї–Є –і—А–µ–љ–∞–ґ–∞: –Њ–±—П–Ј–∞—В–µ–ї—М–љ–Њ–µ –њ–Њ–ї–Є–њ–Њ–Ј–Є—Ж–Є–Њ–љ–љ–Њ–µ —А–µ–љ—В–≥–µ–љ–Њ–≤—Б–Ї–Њ–µ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ –і–Њ –і—А–µ–љ–Є—А–Њ–≤–∞–љ–Є—П –Є –Ї–Њ–љ—В—А–Њ–ї—М –њ–Њ–ї–Њ–ґ–µ–љ–Є—П –і—А–µ–љ–∞–ґ–∞ —Б –Ї–Њ—А—А–µ–Ї—Ж–Є–µ–є –µ–≥–Њ –њ–Њ –Љ–µ—А–µ –љ–µ–Њ–±—Е–Њ–і–Є–Љ–Њ—Б—В–Є –њ–Њ—Б–ї–µ –Љ–∞–љ–Є–њ—Г–ї—П—Ж–Є–Є.
–Ю–і–љ–∞–Ї–Њ —А–µ–Ј—Г–ї—М—В–∞—В—Л –ї–µ—З–µ–љ–Є—П –°–Я –Є—Б–Ї–ї—О—З–Є—В–µ–ї—М–љ–Њ –њ—Г–љ–Ї—Ж–Є—П–Љ–Є –Є –і—А–µ–љ–Є—А–Њ–≤–∞–љ–Є–µ–Љ –њ–ї–µ–≤—А–∞–ї—М–љ–Њ–є –њ–Њ–ї–Њ—Б—В–Є —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –±—Г–ї–ї–µ–Ј–љ–Њ–є –±–Њ–ї–µ–Ј–љ—М—О –љ–µ–ї—М–Ј—П —Б—З–Є—В–∞—В—М —Г–і–Њ–≤–ї–µ—В–≤–Њ—А–Є—В–µ–ї—М–љ—Л–Љ–Є: —А–µ—Ж–Є–і–Є–≤ –њ–љ–µ–≤–Љ–Њ—В–Њ—А–∞–Ї—Б–∞ –љ–∞–±–ї—О–і–∞–µ—В—Б—П –≤ 20–45% —Б–ї—Г—З–∞–µ–≤ –њ—А–Є –ї–µ—З–µ–љ–Є–Є –њ–ї–µ–≤—А–∞–ї—М–љ—Л–Љ–Є –њ—Г–љ–Ї—Ж–Є—П–Љ–Є, –≤ 12–18% – –њ–Њ—Б–ї–µ –Ј–∞–Ї—А—Л—В–Њ–≥–Њ –і—А–µ–љ–Є—А–Њ–≤–∞–љ–Є—П –њ–ї–µ–≤—А–∞–ї—М–љ–Њ–є –њ–Њ–ї–Њ—Б—В–Є [2]. –Т —Б–≤—П–Ј–Є —Б —Н—В–Є–Љ –≤ –љ–∞—Б—В–Њ—П—Й–µ–µ –≤—А–µ–Љ—П –њ—А–Є –Њ—В—Б—Г—В—Б—В–≤–Є–Є –њ—А–Њ—В–Є–≤–Њ–њ–Њ–Ї–∞–Ј–∞–љ–Є–є –Т–Ґ–° –Њ–њ–µ—А–∞—Ж–Є–Є —Б –Ї—А–∞–µ–≤–Њ–є —А–µ–Ј–µ–Ї—Ж–Є–µ–є –Є —В–µ—А–Љ–Њ–і–µ—Б—В—А—Г–Ї—Ж–Є–µ–є –±—Г–ї–ї–µ–Ј–љ–Њ-–Є–Ј–Љ–µ–љ–µ–љ–љ—Л—Е —Г—З–∞—Б—В–Ї–Њ–≤ –ї–µ–≥–Ї–Њ–≥–Њ –≤—Л–њ–Њ–ї–љ—П—О—В—Б—П —Г –≤—Б–µ—Е –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –±—Г–ї–ї–µ–Ј–љ–Њ–є –±–Њ–ї–µ–Ј–љ—М—О –ї–µ–≥–Ї–Є—Е.
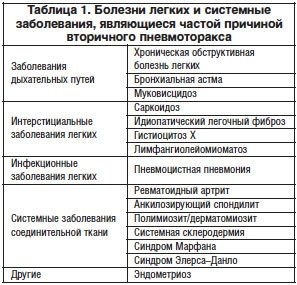
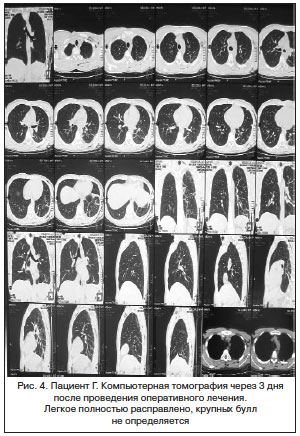
–Ю–њ–µ—А–∞—Ж–Є—О –Ј–∞–Ї–∞–љ—З–Є–≤–∞—О—В –ї–µ–Ї–∞—А—Б—В–≤–µ–љ–љ—Л–Љ –њ–ї–µ–≤—А–Њ–і–µ–Ј–Њ–Љ —Б —А–∞—Б—В–≤–Њ—А–∞–Љ–Є –∞–љ—В–Є–±–Є–Њ—В–Є–Ї–Њ–≤ —В–µ—В—А–∞—Ж–Є–Ї–ї–Є–љ–Њ–≤–Њ–≥–Њ —А—П–і–∞ —Б —Ж–µ–ї—М—О –Њ–±–ї–Є—В–µ—А–∞—Ж–Є–Є –њ–ї–µ–≤—А–∞–ї—М–љ–Њ–є –њ–Њ–ї–Њ—Б—В–Є, —З—В–Њ —Б–ї—Г–ґ–Є—В –њ—А–Њ—Д–Є–ї–∞–Ї—В–Є–Ї–Њ–є –њ–љ–µ–≤–Љ–Њ—В–Њ—А–∞–Ї—Б–∞ –і–∞–ґ–µ –њ—А–Є —А–∞–Ј—А—Л–≤–µ –±—Г–ї–ї—Л (—А–Є—Б. 1–4) [11].
–ѓ–Я –≤ –Њ—В–ї–Є—З–Є–µ –Њ—В –°–Я —А–∞–Ј–≤–Є–≤–∞–µ—В—Б—П –љ–∞ —Д–Њ–љ–µ –Ј–і–Њ—А–Њ–≤–Њ–є –ї–µ–≥–Њ—З–љ–Њ–є —В–Ї–∞–љ–Є –Є–ї–Є –Є–Ј–Љ–µ–љ–µ–љ–Є–є –ї–µ–≥–Њ—З–љ–Њ–є –њ–∞—А–µ–љ—Е–Є–Љ—Л, –љ–µ–і–Њ—Б—В–∞—В–Њ—З–љ—Л—Е –і–ї—П —Б–њ–Њ–љ—В–∞–љ–љ–Њ–≥–Њ —А–∞–Ј—А—Л–≤–∞ –ї–µ–≥–Ї–Њ–≥–Њ, –њ–Њ—Н—В–Њ–Љ—Г –ѓ–Я —П–≤–ї—П–µ—В—Б—П –њ–Њ–Ї–∞–Ј–∞–љ–Є–µ–Љ —В–Њ–ї—М–Ї–Њ –Ї –Ї–Њ–љ—Б–µ—А–≤–∞—В–Є–≤–љ–Њ–Љ—Г –ї–µ—З–µ–љ–Є—О. –Я—А–Є —Н—В–Њ–Љ –≤–∞–ґ–љ–Њ, —З—В–Њ–±—Л –∞–Ї—В–Є–≤–љ–∞—П –∞—Б–њ–Є—А–∞—Ж–Є—П –њ—А–Њ–і–Њ–ї–ґ–∞–ї–∞—Б—М –і–Њ —В–µ—Е –њ–Њ—А, –њ–Њ–Ї–∞ –ї–µ–≥–Ї–Њ–µ –њ–Њ–ї–љ–Њ—Б—В—М—О –љ–µ —А–∞—Б–њ—А–∞–≤–Є—В—Б—П, –Є –љ–µ –Љ–µ–љ–µ–µ 5–7 —Б—Г—В –њ–Њ—Б–ї–µ —А–∞—Б–њ—А–∞–≤–ї–µ–љ–Є—П, –і–Њ —А–∞–Ј–≤–Є—В–Є—П —Б–њ–∞–µ—З–љ–Њ–≥–Њ –њ—А–Њ—Ж–µ—Б—Б–∞ –≤ –њ–ї–µ–≤—А–∞–ї—М–љ–Њ–є –њ–Њ–ї–Њ—Б—В–Є. –Я—А–Є —А–∞—Б–њ—А–∞–≤–ї–µ–љ–љ–Њ–Љ –ї–µ–≥–Ї–Њ–Љ –љ–µ —Б—Г—Й–µ—Б—В–≤—Г–µ—В –Њ–њ–∞—Б–љ–Њ—Б—В–Є –Є–љ—Д–Є—Ж–Є—А–Њ–≤–∞–љ–Є—П –њ–ї–µ–≤—А–∞–ї—М–љ–Њ–є –њ–Њ–ї–Њ—Б—В–Є –Є —А–∞–Ј–≤–Є—В–Є—П —Н–Љ–њ–Є–µ–Љ—Л –њ–ї–µ–≤—А—Л, —В. –Ї. —Б–Њ–±—Б—В–≤–µ–љ–љ–Њ –њ–Њ–ї–Њ—Б—В—М –≤ –њ–ї–µ–≤—А–µ –Њ—В—Б—Г—В—Б—В–≤—Г–µ—В.


–Ы–Є—В–µ—А–∞—В—Г—А–∞
1. –®—Г–ї—Г—В–Ї–Њ –Р.–Ь., –Ю–≤—З–Є–љ–љ–Є–Ї–Њ–≤ –Р.–Р., –ѓ—Б–љ–Њ–≥–Њ—А–Њ–і—Б–Ї–Є–є –Ю.–Ю., –Ь–Њ—В—Г—Б –Ш.–ѓ. –≠–љ–і–Њ—Б–Ї–Њ–њ–Є—З–µ—Б–Ї–∞—П —В–Њ—А–∞–Ї–∞–ї—М–љ–∞—П —Е–Є—А—Г—А–≥–Є—П. –Ь.: –Ь–µ–і–Є—Ж–Є–љ–∞, 2006. 392 —Б.
2. –†–∞–±–µ–і–ґ–∞–љ–Њ–≤ –Ь.–Ь. –†–Њ–ї—М –≤–Є–і–µ–Њ—В–Њ—А–∞–Ї–Њ—Б–Ї–Њ–њ–Є–Є –≤ –і–Є–∞–≥–љ–Њ—Б—В–Є–Ї–µ –Є –≤—Л–±–Њ—А–µ –Љ–µ—В–Њ–і–∞ –ї–µ—З–µ–љ–Є—П —Б–њ–Њ–љ—В–∞–љ–љ–Њ–≥–Њ –њ–љ–µ–≤–Љ–Њ—В–Њ—А–∞–Ї—Б–∞: –Р–≤—В–Њ—А–µ—Д. … –Ї–∞–љ–і. –Љ–µ–і. –љ–∞—Г–Ї. –Ь., 2007. 25 —Б.
3. Noppen M., Schramel F. Pneumothorax // Eur Respir Mon. 2002. Vol. 22. –†. 279–296.
4. Schramel F.M., Postmus P.E., Vanderschueren R.G. Current aspects of spontaneous pneumothorax // Eur Resp J. 1997. Vol. 10. –†. 1372–1379.
5. –Ь–Њ—Б–њ–∞–љ–Њ–≤–∞ –Х.–Т. –Ы–µ–Ї–∞—А—Б—В–≤–µ–љ–љ—Л–є –њ–ї–µ–≤—А–Њ–і–µ–Ј –≤ –ї–µ—З–µ–љ–Є–Є —Б–њ–Њ–љ—В–∞–љ–љ–Њ–≥–Њ –њ–љ–µ–≤–Љ–Њ—В–Њ—А–∞–Ї—Б–∞ –Є –≥–Є–і—А–Њ—В–Њ—А–∞–Ї—Б–∞: –Ф–Є—Б. … –Ї–∞–љ–і. –Љ–µ–і. –љ–∞—Г–Ї. –Ь., 1993. 106 —Б.
6. Mansfield P.F., Hohn D.C., Fornage B.D. et al. Complications and failures of subclavian vein catheterization // N Eng J Med. 1994. Vol. 331. –†. 1735–1738.
7. Grogan D.R., Irwin R.S., Channick R. et al. Complications associated with thoracocentesis. A prospective, randomized study comparing three different methods // Arch Intern Med. 1990. Vol. 150. –†. 873–877.
8. Blasco L.H., Hernandez I.M.S., Garrido V.V. et al. Safety of transbronchial biopsy in outpatients // Chest. 1991. Vol. 99. –†. 562–565.
9. Poe R.H. Sensitivity, specificity, and predictive values of closed pleural biopsy // Arch Intern Med. 1984. Vol. 144. –†. 325–328.
10. Gammon R.B., Shin M.S., Buchalter S.E. Pulmonary barotrauma in mechanical ventilation. Patterns and risk factors // Chest.1992. Vol. 102. –†. 568–572.
11. Light R.W., O’Hara V.S., Moritz T.E. et al. Intrapleural tetracycline for the prevention of recurrent spontaneous pneumothorax: results of a Department of Veterans Affairs Cooperative Study // JAMA. 1990. Vol. 264. –†. 2224–2230.












