Введение
Острый бронхит – широко распространенная болезнь, определяемая как ограниченное воспаление крупных дыхательных путей легких, клинически выражающееся в кашле без пневмонии [1]. Диагностика острого бронхита основана на клинических показателях, так как нет объективных тестов. Он часто характеризуется острым началом кашля, сопровождающимся образованием вязкой мокроты. Среди других возможных симптомов – затрудненное отхождение мокроты, нарушение сна ночью и ухудшение общего состояния пациента [2,3]. Поскольку приступы кашля могут существенно ухудшать качество жизни пациентов, кашель является одним из основных симптомов, по поводу которых пациенты обращаются за медицинской помощью [4]. Основной целью лечения острого бронхита является улучшение эвакуации мокроты и уменьшение кашля. Лечение также должно иметь целью быстрое купирование симптомов, являющихся вторичными по отношению к кашлю, таких как нарушение сна, ухудшение общего состояния, диспноэ и боль в груди, для улучшения общего самочувствия пациентов. Среди других целей – быстрое восстановление работоспособности.
Поскольку основной причиной острого бронхита является вирусная инфекция, в большинстве случаев лечение должно быть симптоматическим [2,3,5–7,9]. Поэтому применение антибиотиков обычно не оправдано – в частности, по причине того, что число антибиотикорезистентных организмов увеличивается, а также из–за побочных эффектов и высокой стоимости антибиотиков [10,11]. Кроме того, во многих клинических исследованиях и мета–анализе было показано, что не отмечается существенного влияния лечения антибиотиками на продолжительность или тяжесть заболевания, а также на возможные осложнения, такие как развитие пневмонии [7–9].
Растительные лекарственные препараты (РЛП) представляют собой эффективные и безопасные терапевтические средства для симптоматического лечения острых неосложненных инфекций дыхательных путей при длительном использовании. Например, эффективность и хорошая переносимость сравнимых РЛП для облегчения симптомов бронхита была показана в недавнем интервенционном и неинтервенционном клиническом исследовании на взрослых и детях, соответственно [12,13].
Целью данного клинического исследования было изучение эффективности и переносимости готовой комбинации сухих экстрактов травы тимьяна и корня первоцвета, называемых комбинацией тимьяна и первоцвета в рекомендованной дозе (1 таблетка три раза в сутки в течение 11 дней) по сравнению с плацебо у взрослых пациентов, страдающих острым бронхитом с продуктивным кашлем, а также расширение существующих данных, указывающих на положительное соотношение польза/риск для данного препарата при этих показаниях.
Комбинация тимьяна и первоцвета была создана для облегчения отхождения мокроты и уменьшения частоты кашля [22]. Трава тимьяна и корень первоцвета имеют разные фармакологические свойства, которые в комбинации работают синергично, обеспечивая отхаркивающий, бронхоспазмолитический, секретолитический и противовоспалительный эффект, обусловливая общую эффективность данного фитопрепарата при остром бронхите с продуктивным кашлем [14–20]. Основными действующими компонентами тимьяна являются эфирные масла, в особенности тимол. Они действуют местно в легких, поскольку выводятся из организма через дыхательные пути, дезинфицируя их, уменьшая бронхоспазм и проявляя муколитическое действие [15,22,23]. Биоактивными соединениями корня первоцвета являются сапонины и фенольные гликозиды (главным образом примеверин) [21]. Сапонины оказывают отхаркивающее действие путем стимуляции верхней части пищеварительного тракта, что рефлекторно индуцирует бронхиальную секрецию [22].
Пациенты, материал и методы
Настоящее клиническое исследование было проспективным, рандомизированным, двойным слепым 11–дневным сравнением в параллельных группах комбинации тимьяна и первоцвета и плацебо при лечении пациентов, страдающих острым бронхитом с продуктивным кашлем. В этом исследовании фазы IV, проведенном в соответствии с Хельсинкской декларацией (версия 1996 г. с изменениями) и гармонизированными трехсторонними указаниями ICH по надлежащей клинической практике (GCP)(CPMP/ICH/135/95), участвовало 23 центра в Германии (22 специалиста по общей и внутренней медицине, 1 врач без специализации). Протокол исследования, информация о пациентах и форма информированного согласия были утверждены комитетом по этике, к которому относился координирующий исследователь («Leiter der klinischen Prüfung« – согласно Германскому законодательству о лекарственных средствах) до набора пациентов. Письменное информированное согласие было получено ото всех пациентов до начала всех связанных с исследованием мероприятий. Клиническая часть исследования была проведена с октября 2006 г. по февраль 2007 г.
Мониторинг, обработка данных и статистическая оценка производились согласно соответствующим указаниям ICH.
Пациенты
Взрослые амбулаторные пациенты мужского и женского пола с клиническим диагнозом острого бронхита с недавно начавшимся (≤ 2 суток) образованием бронхиального секрета при нарушении способности к откашливанию считались подходящими для включения в данное исследование, если они были не моложе 18 лет, имели ≥ 10 приступов кашля в дневное время в последний день перед визитом 1 (согласно оценке пациента) и исходный балл тяжести бронхита (BSS) ≥ 5 баллов (из максимум 20) [13]. Диагноз основывался на анамнезе и физикальном обследовании, которое включало оценку типичных симптомов согласно BSS, т. е. кашель, мокрота, боль в груди при кашле, диспноэ и хрипы при аускультации легких.
Использовали стандартные критерии исключения (включая беременность, отсутствие контрацепции у женщин детородного возраста и лактацию для женщин), основными из них были сопутствующая лихорадка (> 39°С), пневмония, хронические болезни бронхов или легких в анамнезе, такие как хронический бронхит, хроническая обструктивная болезнь легких (включая острый эпизод), бронхоэктатическая болезнь, бронхиальная астма, муковисцидоз, клинически значимые сердечно–сосудистые, почечные, желудочно–кишечные или печеночные заболевания в анамнезе, известная гиперчувствительность к одному или более из компонентов действующего или вспомогательных ингредиентов исследуемого препарата, злокачественные новообразования и любые тяжелые соматические, неврологические и/или психиатрические заболевания.
Применение других препаратов, таких как иммунодепрессанты, системные антибиотики и системные или ингаляционные глюкокортикостероиды (в течение 4 недель до включения в исследования или в ходе исследования), мукоактивные вещества, иные, нежели исследуемый препарат (в течение 2 недель до включения или в ходе исследования), противокашлевые препараты и другие мукоактивные средства, за исключением паровых ингаляций (в ходе исследования) не допускались. Лечение ингибиторами ангиотензинпревращающего фермента (АПФ) не было причиной исключения, если было начато более чем за 4 недели до визита 1. Допускалось применять парацетамол в случае лихорадки, применение других нестероидных противовоспалительных препаратов в ходе исследования не допускалось.
Лечение
Исследуемый препарат (комбинация тимьяна и первоцвета [Бронхипрет® TП, таблетки, покрытые оболочкой] и плацебо) предоставлялся спонсором («Бионорика АГ», Ноймаркт, Германия). Для обеспечения слепого исследования коммерческую комбинацию тимьяна и первоцвета упаковывали таким образом, что активный исследуемый препарат и плацебо были неотличимы друг от друга в отношении размера таблеток и внешнего вида, запаха, упаковки и этикетки. Рандомизацию в группы, получавшие комбинацию тимьяна и первоцвета (серия № 3119201) и плацебо (серия № 3474501), осуществляли согласно параллельно–групповой модели с распределением 1:1 по группам эксперимента. Количество исследуемого препарата, рассчитанное на 11 дней лечения, включая запас, передавали пациенту на визите 1 = день 0 (40 таблеток). Одна таблетка комбинации тимьяна и первоцвета содержала 160,0 мг сухого экстракта травы тимьяна (6,0–10,0 : 1; экстрагент: этанол 70,0 об.%) и 60,0 мг сухого экстракта корня первоцвета (6,0–7,0 : 1; экстрагент: этанол 47,4 об.%). Таблетка плацебо не содержала действующих ингредиентов. Выбранный режим дозировки (1 таблетка три раза в сутки = 33 таблетки за 11 суток) соответствовал рекомендации краткого обзора характеристик продукта (SmPC) для препарата комбинации тимьяна и первоцвета для лечения острого бронхита у взрослых [22]. Исследователь контролировал соблюдение режима пациентами (compliance) путем подсчета числа таблеток.
Процедуры испытания
Индивидуальная продолжительность лечения составила 11 дней, с 3 посещениями исследователя. Пациентов рандомизировали на визите 1 (день 0 = исходное обследование исследователем). Оценка, произведенная исследователем, документировалась в индивидуальной регистрационной карте (ИРК) на каждом визите.
За изменением симптомов острого бронхита наблюдали с использованием дневника симптомов (день 0 – день 10) и путем повторной оценки клинических симптомов, включая аускультацию легких, проводимую после 4 дней (визит 2) и после 10 дней лечения (визит 3).
Целью этого доказательного исследования было подтвердить превосходство препарата тимьяна и первоцвета над плацебо в отношении снижения частоты приступов кашля в дневное время, отмечавшегося с помощью ручного счетчика. Приступы кашля определяли как 3 или более последовательных покашливаний без заметного периода дыхания между ними. Пациента инструктировали нажимать на ручной счетчик при каждом приступе кашля (начиная с подъема утром и до отхода ко сну вечером).
Измерения
Эффективность. Основным критерием было изменение средней частоты приступов кашля в дневное время в дни 7–9–й периода лечения, задокументированное в дневнике пациента, деленное на исходное значение в день 1 (стандартизированное на 1–й день точного подсчета с помощью ручного счетчика). Период времени для анализа (дни 7–9) был основан на фармакологических соображениях и результатах предварительного плацебо–контролируемого исследования с использованием комбинации тимьяна и плюща [13]. В отличие от подавляющих кашель препаратов, начало противокашлевого действия препаратов с секретолитическими свойствами (типа комбинации тимьяна и первоцвета) несколько отсроченное. Поэтому период между 7–м и 9–м днями считался релевантным для оценки основной меры эффективности.
Вторичными критериями для оценки эффективности лечения в отношении приступов кашля (определенных на основе записей в дневнике с использованием точной регистрации при помощи ручного счетчика) были следующие:
• Снижение числа приступов кашля в течение дня на 9–й день лечения исследуемым препаратом, рассчитанное как площадь под кривой (AUC). Этот расчет обобщает эффект лечения на приступы кашля за весь период наблюдений.
• Время до 50%–го снижения числа приступов кашля днем по сравнению с днем 1. Этот параметр показывает пользу для пациента по временной оси.
• Доля пациентов без приступов кашля на день 9–й. Этот параметр сравнивает долю вылеченных пациентов в отношении приступов кашля в последний день периода наблюдений.
• Относительное снижение средней частоты приступов кашля к 9–му дню. Этот параметр определяет изменение по сравнению с исходным уровнем в конце периода наблюдений.
Другие вторичные критерии оценки эффективности приведены ниже.
• Реакция на лечение, оцененная исследователем на визите 2 и 3 по сравнению с визитом 1 с использованием 4–балльной шкалы по устному сообщению (0 = нет симптомов, 1 = улучшение симптомов, 2 = симптомы без изменений, 3 = ухудшение симптомов); пациенты без симптомов или с улучшением были классифицированы как респондеры (ответившие на лечение пациенты), пациенты, у которых симптомы остались без изменений или с ухудшением, были классифицированы как нон–респондеры (не ответившие на лечение пациенты).
• Изменение среднего BSS (оценка баллов по кашлю, мокроте, хрипам, боли в груди при кашле и диспноэ) на визитах 2 и 3 в отношении суммарного балла до лечения, отмеченного в визит 1 (день 0) с использованием 5–балльной шкалы по устному сообщению от 0 (нет) до 4 (очень тяжелый) [13]. Доля ответивших на лечение и BSS характеризуют общий эффект лечения в отношении симптомов, связанных с острым бронхитом.
• Изменение способности откашливать мокроту со дня 0 до дня 9 (рассчитанное как AUC) с использованием 5–балльной шкалы по устному сообщению (0 = нет мокроты, 1 = нет проблем с откашливанием мокроты, 2 = небольшие проблемы с откашливанием мокроты, 3 = откашливание мокроты затруднено, 4 = откашливание мокроты очень затруднено).
• Изменение в отношении нарушений сна, вызванных кашлем, с дня 0 до дня 10 (рассчитанное как AUC) с использованием 4–балльной шкалы по устному сообщению, где 0 указывает, что сон не нарушен, а 3 = сон сильно нарушен.
• Изменение общего самочувствия пациентов со дня 0 по день 9 (рассчитанное как AUC) с использованием 4–балльной шкалы по устному сообщению, отмеченной в дневнике, от 0 (у меня нет симптомов) до 3 (я очень плохо себя чувствую).
Переносимость. Нежелательные явления (НЯ), отмеченные на визитах 2 и 3, были оценены исследователем по тяжести, продолжительности, исходу, предпринятым мерам, частоте и причинной связи с лечением. Среди других критериев безопасности – основные показатели состояния организма (кровяное давление, частота сердечных сокращений, температура тела) отмечались на каждом визите. Кроме того, пациенты ежедневно измеряли температуру, и общее суждение о переносимости выносилось исследователем в конце лечения (визит 3) с использованием 5–балльной шкалы по устному сообщению – от 0 (очень хорошо) до 4 (очень плохо).
Статистика
Расчет размера выборки. На основе результатов предыдущего плацебо–контролируемого исследования комбинации тимьяна и плюща [13], был проведен расчет размера выборки для предположения о снижении первичной конечной точки до 0,54 для плацебо с клинически значимым отличием от комбинации тимьяна и первоцвета 20% (Δ = 0,108). Оцененное стандартное отклонение (s = 0,354) и ограниченная степень ошибки (α1–sided = 0,025; β = 0,2) приводят к определению размера выборки 180 пациентов на группу, если принять во внимание выбывание примерно 5%.
Статистический анализ. Анализы и обработка недостающих данных. Популяция для оценки безопасности (SEP) – для анализа результатов по безопасности – включала всех рандомизированных пациентов с не менее чем 1 задокументированным применением исследуемого препарата и данными по безопасности.
Полный набор для анализа параметров эффективности (FAS) включал всех рандомизированных пациентов с не менее чем 1 задокументированным применением исследуемого препарата и данными по эффективности.
Полностью отсутствующие данные брали на основе принципа «последний результат, перенесенный вперед» (LOCF), за исключением случая преждевременного прекращения исследования, когда данные по визиту 2 отсутствовали. В этом случае отсутствующие данные для визита 2 заменяли значениями для визита 3. Другим исключением из принципа LOCF было, когда число приступов кашля в дневнике не было отмечено, но дополнительные данные (BSS, данные из дневника) демонстрировали отсутствие кашля в этот день. В этом случае число приступов кашля считали равным нулю.
Статистические методы. Эффективность. Исследование, разработанное для проверки статистического превосходства комбинации тимьяна и первоцвета над плацебо, было проведено с использованием двухэтапной адаптивной схемы для проверки расчета размера выборки [24]. Предписанный промежуточный анализ первичной конечной точки включал данные по 265 пациентам.
Основная конечная точка (изменение средней частоты кашля в течение дня с 7–го по 9–й день периода исследования по сравнению с днем 1, задокументированное в дневнике пациента) была исследована на уровень значимости альфа = 0,025 (1–сторонний) с помощью ANOVA с поправкой на эффект центра. Вследствие существенного отклонения от предпосылок ANOVA дополнительно использовали непараметрический критерий Манна–Уитни–Уилкоксона (с группировкой по центру).
Испытание всех гипотез на вторичные конечные точки было проведено описательно на 2–стороннем номинальном уровне вероятности ошибки (альфа) 5%. Для зависимого от настройки анализа использовали методы таблиц дожития Каплана–Мейера и логарифмически–ранговый тест.
Данные по категориям анализировали с помощью критерия хи–квадрат или тренд–критерия Кохрана–Эрмитажа.
Критерий Манна–Уитни–Уилкоксона (с группировкой по центру) также применяли ко всем параметрам, рассчитанным по AUC.
Безопасность. НЯ обобщали описательно по общему числу НЯ для каждой группы исследования и числу и доле пациентов, сообщивших о каком–либо НЯ, в группе, получавшей комбинацию тимьяна и первоцвета, по сравнению с группой плацебо. Критерий Манна–Уитни–Уилкоксона использовали для сравнения различий между средними для групп значениями основных показателей состояния организма (кровяное давление, частота сердечных сокращений, температура тела). Различия между группами исследования в отношении оценки переносимости исследователем и пациентами были проанализированы с использованием критерия Кохрана–Эрмитажа для трендов. Статистический анализ проводили с использованием SAS® версии 8.2 (SAS Institute, Кэри, Северная Каролина, США).
Результаты
Данные по пациентам
В исследование было включено в общей сложности 362 амбулаторных пациента мужского и женского пола (n=184 в группе, получавшей комбинацию тимьяна и первоцвета; n=178 в группе, получавшей плацебо). Шесть пациентов в группе, получавшей комбинацию тимьяна и первоцвета (n=2: недостаточная эффективность; n=2: без последующего наблюдения; n=1: пациент предпочел противокашлевый препарат отхаркивающему; n=1: семейные обстоятельства), и 7 пациентов в группе, получавшей плацебо (n=7: недостаточная эффективность), преждевременно прекратили участие в исследовании. Кроме того, 2 пациента в группе, получавшей комбинацию тимьяна и первоцвета, и 1 пациент в группе плацебо преждевременно прекратили лечение по причине полного выздоровления.
Анализ
По причине отсутствия документирования приема препарата 1 пациент в группе, получавшей комбинацию тимьяна и первоцвета (отсутствие последующего наблюдения), был исключен из SEP. Поэтому SEP включал 361/362 пациента (n=183/184 в группе, получавшей комбинацию тимьяна и первоцвета; n=178/178 в группе, получавшей плацебо). Из них 1 пациент в группе, получавшей комбинацию тимьяна и первоцвета, был исключен из FAS по причине отсутствия данных по эффективности после начала исследования (отсутствие последующего наблюдения). Поэтому FAS включал 360/362 пациента (n=182/184 в группе, получавшей комбинацию тимьяна и первоцвета; n=178/178 в группе, получавшей плацебо). В отношении приступов кашля 6 пациентов в группе, получавшей комбинацию тимьяна и первоцвета, и 1 пациент в группе, получавшей плацебо, были исключены из анализа FAS по причине отсутствия или неприемлемых данных в дневнике.
Заранее запланированный промежуточный анализ был проведен после валидации данных по примерно 70% запланированных пациентов (n=265; n=130 в группе, получавшей комбинацию тимьяна и первоцвета; n=135 в группе, получавшей плацебо).
Продолжительность исследования
и соблюдение схемы лечения
Средняя продолжительность исследования соответствовала протоколу исследования (среднее: 11 дней, максимум: 13 дней в обеих группах лечения; FAS).
Соблюдение схемы лечения, рассчитанное как отношение реального и рекомендованного приема препарата, было очень хорошим, со сходными средними значениями в обеих группах лечения (98,6% в группе, получавшей комбинацию тимьяна и первоцвета, и 99,0% группе, получавшей плацебо).
Демография и исходные характеристики
В таблице 1 представлены демографические данные, а также исходные характеристики 360 пациентов, включая FAS (возрастной диапазон: 18–85 лет в обеих группах). Группы были сопоставимы по демографическим и исходным характеристикам. Большинство пациентов в группе, получавшей комбинацию тимьяна и первоцвета, и в группе, получавшей плацебо, были представители европеоидной расы (96,7% и 98,9 %).
Результаты по эффективности
Кашель. В обеих группах эксперимента (FAS) среднее число приступов кашля постоянно снижалось от исходного уровня до дня 9 (рис. 1). Относительное снижение средней частоты приступов кашля в день 9–й продемонстрировало явное преимущество растительного лекарственного препарата (комбинации тимьяна и первоцвета) по сравнению с плацебо (73,7 и 57,8%; p<0,0001; FAS). Начиная со 2–го дня, снижение числа приступов кашля было более выраженным в случае комбинации тимьяна и первоцвета при превосходстве над плацебо со дня 5 и до конца периода наблюдения, т. е. дня 9 (рис. 1). Рассчитанная средняя площадь под кривой (AUC) для снижения числа приступов кашля подтверждает, что 9–дневное лечение комбинацией тимьяна и первоцвета имеет преимущество над плацебо (4,8±1,9 против 5,5±1,9; p<0,0001; FAS).
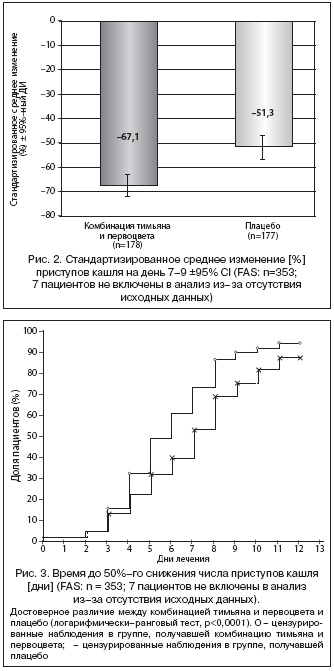
В промежуток времени, выбранный для анализа первичной конечной точки (со дня 7 по день 9), лечение комбинацией тимьяна и первоцвета имело преимущество над плацебо в отношении среднего снижения частоты приступов кашля по сравнению с исходным уровнем (рис. 2). Подтверждающий анализ первичной конечной точки эффективности продемонстрировал превосходство комбинации тимьяна и первоцвета над Анализ эффективности препарата по оси времени показал, что успешное (50%) снижение числа приступов кашля по сравнению с исходным уровнем достигалось на день 5 при лечении комбинацией тимьяна и первоцвета, что было примерно на 2 дня раньше по сравнению с приемом плацебо (рис. 3). Вследствие явного преимущества комбинации тимьяна и первоцвета число пациентов, у которых не было кашля, было более чем в два раза больше в группе активного препарата, чем в группе плацебо, на день 9 (28,6% по сравнению с 10,7%; p<0,0001; FAS).
плацебо в промежуточном анализе (n=265: p<0,0001), что еще раз подтвердилось при анализе FAS (p<0,0001).
Респондеры и балльная оценка тяжести бронхита (BSS). Преимущество комбинации тимьяна и первоцвета над плацебо было также продемонстрировано в отношении доли респондеров и улучшения по BSS. Лечение комбинацией тимьяна и первоцвета приводило к существенно более высокой доле респондеров по сравнению с приемом плацебо уже после 4 дней лечения (визит 2), с дальнейшим усилением эффекта к концу исследования (визит 3) (рис. 4). Среднее BSS снижалось постоянно в обеих группах в период от начала и до конца лечения, но снижение было существенно более выраженным в группе, получавшей комбинацию тимьяна и первоцвета (–6,2 и –4,1 баллов от визита 1 до визита 3; рис. 5).
Другие связанные с симптомами параметры. Превосходство комбинации тимьяна и первоцвета над плацебо было также подтверждено в отношении снижения нарушений сна вследствие кашля и улучшения способности к откашливанию мокроты в течение дня и общего самочувствия пациентов (табл. 2).
Результаты по безопасности
Лечение комбинацией тимьяна и первоцвета до 13 дней и максимальный общий прием до 6,2 г сухого экстракта травы тимьяна и 2,3 г сухого экстракта корня первоцвета хорошо переносилось 183 пациентами. При 3 нежелательных явлениях (НЯ), отмеченных у 3/183 (1,6%) пациентов в группе, получавшей комбинацию тимьяна и первоцвета, встречаемость НЯ была очень низкой и сходной с таковой в группе плацебо, в которой также отмечено 3 НЯ у 3/178 (1,7%) пациентов (SEP).
Два НЯ в группе, получавшей комбинацию тимьяна и первоцвета, классифицировались, как умеренные (нарушения в евстахиевой трубе, боль в спине), а 1 НЯ было классифицировано как слабое (наружный отит). В группе плацебо все 3 НЯ были классифицированы, как слабые (рвота, диспепсия, ринит). Тяжелых или серьезных НЯ не отмечено ни в одной из групп. Никто из пациентов не прекратил лечение преждевременно из–за НЯ.
Оценка пациентами общей переносимости исследуемого препарата в конце исследования (визит 3) согласовалась с соответствующей оценкой исследователя. 97,8% пациентов/исследователей в группе, получавшей комбинацию тимьяна и первоцвета, оценили переносимость как «очень хорошую» или «хорошую», по сравнению с 99,4% пациентов/исследователей в группе, получавшей плацебо (SEP). Лишь 2 (1,1%) пациента и 1 (0,6%) исследователь в группах, получавших комбинацию тимьяна и первоцвета и плацебо соответственно, оценили переносимость исследуемого препарата, как «умеренную», и никто – как «плохую» или «очень плохую». Таким образом, не наблюдается различий между группами в отношении параметров переносимости.
В обеих группах средние значения кровяного давления и частоты сердечных сокращений не демонстрировали клинически существенных изменений по сравнению с исходным уровнем.
В оба визита температура тела не повышалась выше 39°C ни у одного пациента, получавшего комбинацию тимьяна и первоцвета или плацебо (максимум: 38,8°C и 38,6°C в визит 2 и 37,7°C и 38,8°C в визит 3 соответственно). Временное повышение выше 39°C (максимум: 39,2°C) между визитами (день 2) было отмечено в дневнике 1 пациента в группе плацебо. В группе, получавшей комбинацию тимьяна и первоцвета, меньше пациентов (1/19 пациентов) по сравнению с группой плацебо (4/18 пациентов) одновременно принимали парацетамол или антибиотики по предписанию, по причине повышения температуры тела.
Обсуждение
Результаты данного двойного слепого плацебо–контролируемого многоцентрового исследования фазы IV подтвердили, что взрослые пациенты с острым бронхитом и недавним началом продуктивного кашля получали явную пользу от раннего лечения готовой комбинацией сухих экстрактов тимьяна и первоцвета. Цели симптоматического лечения, а именно: уменьшение кашля путем усиления отхаркивания и устранение сопутствующих жалоб пациентов, таких как нарушения сна, диспноэ и боль в груди в результате кашля – были достигнуты. Раннее начало купирования симптомов и наблюдаемое существенное улучшение в отношении тяжести и длительности наиболее выраженных симптомов острого бронхита (BSS) отражаются в существенно большей доле респондеров и явном улучшении общего самочувствия пациентов. Одновременное использование анальгетиков/антипиретиков и/или антибиотиков вследствие повышения температуры тела отмечалось реже при приеме растительного препарата, чем плацебо. Возможных осложнений, таких как развитие пневмонии, не отмечено.
В отличие от благоприятных клинических результатов этого и подобных других исследований с комбинацией травы тимьяна и корня первоцвета [25–27] или экстрактов травы тимьяна и листьев плюща [12,13] польза лечения острого бронхита антибиотиками не доказана. В ряде контролируемых клинических испытаний и в двух мета–анализах не получено убедительных доказательств существенного превосходства лечения антибиотиками над плацебо [10,31–33]. На основе этих результатов лечение острого неосложненного бронхита антибиотиками не рекомендуется во многих национальных руководствах [7,34,35].
Тяжесть болезни до лечения (исходный BSS) в данном исследовании согласовалась с данными, приведенными в других интервенционных исследованиях [13,25–29]. Поэтому пациенты в нашем исследовании представляются репрезентативной группой пациентов, страдающих острым бронхитом с недавним началом симптомов. Можно сделать вывод о внешней валидности нашего исследования.
Ряд исследований [12,13,25–29] показали, что пациенты с острым бронхитом обычно обращаются за медицинской помощью, даже если тяжесть их болезни, выраженная в BSS, намного ниже максимума BSS. В то время как параметры BSS кашель и мокрота могут быть сильно выражены, другие параметры, такие как боль в груди, диспноэ и хрипы, слабо выражены или даже отсутствуют в большинстве случаев острого бронхита. Поэтому относительно низкие значения BSS не обязательно говорят о слабо выраженном заболевании. Более высокие значения BSS могут наблюдаться у пациентов с хронической и обструктивной болезнью бронхов и легких (то есть ХОБЛ и астмой с обострениями). У этих пациентов диспноэ, боль в груди и патологические результаты при аускультации более выражены.
В целом НЯ для комбинации тимьяна и первоцвета были редкими (1,6% пациентов), не тяжелыми и преходящими. Нарушения со стороны желудочно–кишечного тракта (ЖКТ) (тошнота, рвота) или аллергические реакции, которые отмечались при монотерапии корнем первоцвета и травой тимьяна, в этом исследовании не наблюдались [14,18,22]. Для сравнения: частота НЯ, указанная при использовании антибиотиков (в частности, диареи) для лечения острого бронхита, была заметно выше (например, 12% для цефуроксима аксетила, 32% для амоксициллина/клавулановой кислоты) [30]. Кроме того, при оценке переносимости пациентами и исследователями комбинация тимьяна и первоцвета переносилась практически так же, как и плацебо, при преобладающей доле оценок «очень хорошо» и «хорошо». Хорошие параметры переносимости комбинации тимьяна и корневищ первоцвета и отсутствие лекарственных взаимодействий делают ее особенно полезной в лечении пациентов, получающих одновременно препараты для лежащего в основе заболевания.
Заключение
Пероральная фитотерапия готовой комбинацией сухих экстрактов травы тимьяна и корня первоцвета (таблетки, покрытые оболочкой) может считаться хорошим терапевтическим выбором для симптоматического лечения острого бронхита с продуктивным кашлем у взрослых. Раннее лечение в рекомендованной дозе приводило к более быстрому и более полному выздоровлению в отношении симптомов по сравнению с плацебо, что клинически существенно улучшает качество жизни пациентов. Данное лечение безопасно и хорошо переносится. Комбинация тимьяна и первоцвета не создает риска развития устойчивости у патогенов.
Ответственность авторов
и финансирование исследования
Берндт Кеммерих, доктор медицины, специалист по внутренним болезням и пульмонологии, был координирующим исследователем и научным консультантом («Leiter der klinischen Prüfung» согласно §40 Германского закона о лекарственных средствах) данного многоцентрового исследования. Он отвечал за научное руководство при написании рукописи, редактировании статьи и утвердил итоговый вариант рукописи.





Литература
1. Wenzel RP Fowler AA 3rd. Clinical practice. Acute bronchitis. NEngl J Med. 2006;355{20}:2125–2130.
2. Alberta Clinical Practice Guideline Working Group. Guideline for the management of acute bronchitis. December 2000, revised: November 2001. .
3. Kronenberg RS, Griffith DE. Bronchitis and acute febrile tracheobronchitis. In: Respiratory infections. A scientific basis for management. Ed. Niederman, Sarosis. Glassroth. New York: W. B. Saunders Company; 1994. p. 91–102.
4. Irwin RS, Madison JM. The diagnosis and treatment of cough. N Engl J Med. 2000;343(23):1715–1721.
5. Guussen A, Gessner С, Hammerschmidt S, et al Acute bronchitis:– when are antibiotics, and when is symptomatic treatment indicated? MMW Fortschr Med. 2006; 148(1–2):26–28.
6. Kardos P et al.: Leitlinie der Deutschen Gesellschaft fur Pneumologie zur Diagnostik und Therapie von Patienten mit akutem und chronischem Husten. Pneumologie, 2004;58:570–602.
7. Snow V, Mottur–Pilson Ch, Gonzales R. Principles of appropriate antibiotic use For treatment of acute bronchitis in adults. Position paper Clinical practice guideline. Part 1 of the American College of Physicians (ACP). Ann Intern Med. 2001;134(6):518–520.
8. Orr PH, Scherer К, Macdonald А, et al Randomised placebo–controlled trials of antibiotics for acute bronchitis: A critical review of the literature. JFam Pract. 1993;36(5}:507–512.
9. Vogel F, Scholz H, et al Rationaler Einsatz oraler Antibiotika bei Erwachsenen. Med. Monatsschr Pharm. 2002;25 (6): 193–204
10. Smucny J, Fahey X Becker L, et al Antibiotics for acute bronchitis. Cochrane database Syst Rev. 2004;(4):CD000245.
11. Macfarlane J, Holmes W, Gard В et al Reducing antibiotic use for acute bronchitis in primary care: blinded, randomised controlled trial of patient information leaflet. BMJ. 2002;324:91.
12. Marzian O. Behandlung der akuten Bronchitis bei Kindern und Jugendlichen. Anwendungsbeobachtung bestatigt Nutzen und Unbedenklichkeit einer Flussigextrakt–Kombination aus Thymiankraut und Efeublattem (Bronchipret® Saft). MMW–Fortschr Med, Originaiien Nr. 11/2007; 149:69–74.
13. Kemmerich B, Eberhardt R, Stammer H. Efficacy and toi–erabuity of a fluid extract combination of thyme herb and ivy leaves and matched placebo in adults suffering from acute bronchitis with productive cough. A prospective, double–blind, placebo–controlled clinical trial. Arzneim.–ForschJDrug Res. 2006;56(9):652–660,
14. Thymi herba (Thyme). ESCOP Monographs. European Scientific Cooperation on Phytomedicine, Elburg; 2003.
15. Thymi herba (Thymiankraut). Monographie BGA/BfArM (Kommission E). BAnz. 1992;226
16. Primulae radix (Primrose root). ESCOP Monographs. European Scientific Cooperation on Phytomedicine, Elburg; 2003.
17. Primulae radix (Primelwurzel). Monographie BGA/BfArM (Kommission E). BAnz. 1990;50
18. European Medicines Agency (EMEA). Community herbal monograph on Primula Veris I., Primula Elatior (L.) Hill, Radix. Doc. Ref. ЕМЕА/НМРС/143370/2006 (Draft); 2007
19. Hagers Handbuch der pharm. Praxis. 5. Aufl. Berlin–Heidelberg–New York: Springer; 1995.
20. Curie PF, Fraibault V, Prevot A. The evaluation of five Bionorica drugs and bromhexine on tracheo–bronchial phenol red secretion in rats. Batelle Europe, Geneva, Switzerland. Report 1991.
21. Muller A, Ganzera M, Stuppner H. Analysis of phenolic glycosides and saponins in Primula elatior and Primula veris (primula root) by liquid chromatography, evaporative light scattering detection and mass spectrometry. Journal of Chromatography A. 2006; 1112(1–2) :218–223.
22. Bionorica AG. Fachinformation Bronchipret® TP Filmtabletten. Bundesverband der Pharmazeutischen Industrie e.V., Rote Liste Service GmbH; 2006.
23. Kohlert C. Systemische Verfugbarkeit und Pharmakokinetik von Thymol nach oraler Applikation einer thymian–haltigen Zubereitung im Menschen [Dissertation]. Wurzburg: Bayerische Julius–Maximilians–Universitat Wurzburg; 2001
24. Bauer P, Kohne K. Evaluation of experiments with adaptive interim analysis. Biometrics. 1994;50:1029–1041.
25. Gruenwald J, Graubaum HJ, Busch R. Efficacy and tolera–bility of a fixed combination of thyme and primrose root in patients with acute bronchitis. A double–blind, randomized, placebo–controlled clinical trial. Arzneim.–Forsch.l Drug Res. 2005;55(ll):669–676.
26. Gruenwald J, Graubaum HJ, Busch R, et al Thymian und Primelwurzel – ein starkes Doppel gegen akute Bronchitiden. ZPhytother. 2006;27(5):214–220.
27. Gruenwald J, Graubaum HJ, Busch R. Evaluation of the non–inferiority of a fixed combination of thyme fluid– and primrose root extract in comparison to a fixed combination of thyme fluid extract and primrose root tincture in patients with acute bronchitis. A single–blind, randomized, bi–centric clinical trial. Arzneimittel–Forschung (Drug Research). 2006;56(8):574–581.
28. Matthys H, Eisebitt R, Seith B, Heger M. Efficacy and safety of an extract of Pelargonium sidoides (Eps 7630) in adults with acute bronchitis. A randomised, double–blind, placebo–controlled trial. Phytomedicine. 2003;10(IV):7–17.
29. Matthys H, Heger M. Treatment of acute bronchitis with a liquid herbal drug preparation from pelargonium sidoides (EPs 7630): a randomised, double–blind, placebo–controlled, multicentre study. Curr Med Res Opin. 2007; 23(2):323–331.
30. Henry DC, Ruoff GE, Noonan M, et al. Comparison of the efficacy and tolerability of short–course cefuroxime axetil and amoxicillin/clavulanic acid in the treatment of secondary bacterial infections of acute bronchitis. Clin Drug Invest. 1999;18(5):335–344.
31. Evans AT, Husain S, Durairaj L, Sadowski LS, Charles–Damte M, Wang Y. Azithromycin for acute bronchitis: a randomised, double–blind, controlled trial. / Fam Pract 2002;51(9):783.
32. Little P, Rumsby K, Kelly J, et al: Information leaflet and antibiotic prescribing strategies for acute lower respiratory tract infection; a randomized controlled trial. JAMA 2005;293:3029–3035.
33. Bent S, Saint S, Vittinghoff E, Grady D. Antibiotics in acute bronchitis: a meta–analysis. Am J Med. 1999;107(l):62–67.
34. Gonzales R, Bartlett JG, Besser RE, et al Principles of appropriate antibiotic use for treatment of uncomplicated acute bronchitis: background. Ann intern Med. 2001; 134:521–529.
35. Hoffken G, Lorenz L, Kern W| et al S3–Leitlinie zu ambu–lant–erworbener Pneumonie und tiefen Atemwegsinfektionen. Pneumologie. 2005;59:612.












