Наибольшее эпидемическое значение имеют вирусы гриппа А из–за их уникальной способности к антигенной изменчивости, в результате которой появляются высоковирулентные штаммы, в том числе – вызвавшие три пандемии гриппа XX века (1918, 1957 и 1968 гг.) и одну эпидемию, близкую по масштабу к пандемии (1977 г.).
Гриппозная инфекция ассоциируется с высоким уровнем заболеваемости, значительными экономическими затратами и летальностью. По данным ВОЗ, ежегодно в мире болеют гриппом 5–10% взрослых и 20–30% детей, умирают от осложнений 250–500 тыс. человек, а экономические затраты оцениваются в 1–6 млн. долларов США на 100000 населения [1]. В России, по данным Роспотребнадзора Минздравсоцразвития РФ, затраты на одного больного гриппом составляют 3700 руб.
Грипп представляет серьезную опасность для детей первого года жизни, пожилых людей, а также лиц с сопутствующими заболеваниями сердца, легких, сахарным диабетом, другой хронической патологией и является причиной избыточной смертности, составляющей от 104 до 870 на 100000 населения [2].
Высокая социально–экономическая значимость гриппозной инфекции для общества определяет важность проблемы рациональной и безопасной противовирусной терапии. ВОЗ подчеркивает, что противовирусные препараты приобретают особое значение, как единственное специфическое медикаментозное средство снижения заболеваемости и смертности [3], особенно в условиях пандемии, когда применение вакцин будет неэффективно.
К средствам, оказывающим прямое противовирусное действие, в настоящее время относятся два класса химиопрепаратов: соединения адамантанового ряда и ингибиторы нейраминидазы.
В основе механизма действия производных адамантана – амантадина и римантадина лежит подавление процесса формирования ионных каналов вирусным белком М2 на раннем этапе инфекции. Однако узкий спектр действия (препараты являются селективными ингибиторами вируса гриппа А), частые побочные эффекты со стороны ЦНС, желудочно–кишечного тракта и быстрое формирование резистентных штаммов значительно ограничивают возможности лечения этими препаратами. Высокие уровни циркуляции резистентных штаммов зарегистрированы в 2004 г. в Китае (74%); в 2005–2006 гг. в США (91%) [4]. В России доля римантадин–резистентных штаммов вируса гриппа A/H3N2 составила 39% в сезоне 2005–2006 гг. и 35% – в сезоне 2006–2007 гг.; вместе с тем для штаммов вируса гриппа A / H1N1 этот показатель увеличился вдвое, составив 25 и 48% соответственно [5,6].
Результатом разработки новых подходов к лечению гриппа явилось создание противогриппозных препаратов второго поколения – ингибиторов нейраминидазы, представленных в настоящее время занамивиром и осельтамивиром. Механизм их действия основан на подавлении ферментативной активности нейраминидазы [7–9]. Занамивир выпускается в виде порошка для дозированного ингаляционного введения, осельтамивир (Tamiflu™) – в виде капсул и суспензии для детей.
Фармакокинетика осельтамивира всесторонне описана в ряде работ [10,11]. При пероральном приеме осельтамивир под действием печеночных эстераз превращается в активный метаболит. В кровоток поступает 75–80% принятой дозы, и через 1–2 ч препарат распределяется в тканях: слизистой оболочке дыхательных путей и в легких. Следует подчеркнуть, что период полувыведения осельтамивира из бронхоальвеолярной лаважной жидкости был более продолжительным, чем из плазмы, что свидетельствует о стойкой концентрации препарата в респираторном тракте [10]. Активный метаболит не подвергается дальнейшей трансформации и выводится в неизмененном виде преимущественно (80%) почками, поэтому больным с почечной недостаточностью (клиренс креатинина <30 мл/мин) для предотвращения увеличения концентрации препарата рекомендуется снижение суточной дозы.
В клинических исследованиях с двойным слепым плацебо–контролируемым дизайном показана безопасность и терапевтическая эффективность осельтамивира. Назначение препарата в первые 36 ч болезни сокращает продолжительность лихорадки, уменьшает интоксикацию и возможность развития вторичных осложнений [12,13].
В отличие от ингибиторов ионных каналов, образованных белком М2, осельтамивир обладает низкой способностью к селекции устойчивых штаммов вируса гриппа А [14,15].
Продолжающиеся исследования демонстрируют эффективность осельтамивира при лечении заболевания людей, вызванного высоковирулентным вирусом гриппа А птиц субтипа H5N1 [16,17].
В России осельтамивир (Tamiflu™) зарегистрирован в 2001 г. и разрешен для лечения и профилактики гриппа у взрослых и детей старше 1 года. Несмотря на убедительные данные о том, что назначение ингибиторов нейраминидазы является одним из наиболее обоснованных вариантов этиотропной терапии гриппа, применение их в нашей стране ограничено. К сожалению, приходится констатировать, что до настоящего времени эффективность лечения гриппа практикующими врачами остается низкой из–за преимущественного назначения симптоматических средств или химиопрепаратов с низким уровнем активности.
Целью настоящей работы является оценка результатов применения осельтамивира при гриппе у взрослых в период эпидемической вспышки 2007 г.
Материалы и методы
Наблюдали 75 больных (мужчин – 56, женщин – 19) с лабораторно подтвержденным диагнозом гриппа в возрасте от 18 до 61 года (86% до 40 лет) с выраженными клиническими симптомами, температурой тела не ниже 38°С и длительностью заболевания не более 24–36 ч. Диагноз гриппа подтвержден у всех пациентов вирусологическими методами (индикация вирусного антигена в назальных смывах, изоляция вируса на культуре клеток MDCK) и серологически в реакции торможения гемагглютинации (РТГА) (определение титров антител в парных сыворотках крови). Из назальных смывов 27 больных (36%) на культуре клеток MDCK выделены штаммы вирусов гриппа, подобные эталонным: А/Новая Каледония/20/99 (H1N1), А/Калифорния/7/04 (H3N2), А/Висконсин/67/06 (H3N2), В/Малайзия/2506/ 04 и В/Шанхай/361/02.
Рандомизацию пациентов в группе проводили по мере поступления в стационар.
Осельтамивир назначали в капсулах по 75 мг 2 раза в сутки в течение 5 дней (1 группа – 38 больных). Во 2–й группе (37 больных) назначали только симптоматическое лечение: аскорутин, микстуру от кашля, назальные капли. При гипертермии пациенты обеих групп получали парацетамол. Лечение начинали в первые 24–36 ч болезни. У всех больных тяжесть заболевания соответствовала среднетяжелой.
Больные не включались в исследование, если были вакцинированы против гриппа, имели обострение хронического заболевания, получали кортикостероидную терапию или иммунодепрессанты, имели алкогольную или наркотическую зависимость.
Критериями клинической эффективности являлись сроки нормализации температуры, продолжительность основных симптомов болезни, скорость элиминации вируса и частота возникновения вторичных осложнений.
Статистическую обработку проводили с помощью программных пакетов Statistica 6.0, MatLab 7.0.1.
Результаты и обсуждение
Клиническая картина гриппозной инфекции имела все классические признаки и характеризовалась острым началом (100%), быстрым повышением температуры до максимальных значений в первые сутки (39°С и выше – 82,7%), нарастанием токсикоза. У всех больных отмечались озноб (100%), часто ломота (73,3%), головокружение (72,0%), нередко тошнота (25,3%), рвота (9,3%), цианоз губ и слизистой оболочки ротоглотки (45,3%), носовое кровотечение (5,3%). Пульс соответствовал температуре во всех случаях. Артериальное давление чаще было нормальным, гипотония имела место у единичных больных в первые 2–3 дня болезни. С первых суток (в ряде случаях – вторых) появлялись сухой кашель (93,3%), трахеит (62,7%), ринит (96,0%).
По демографическим данным и частоте клинических симптомов сравниваемые группы были сопоставимы (табл. 1).
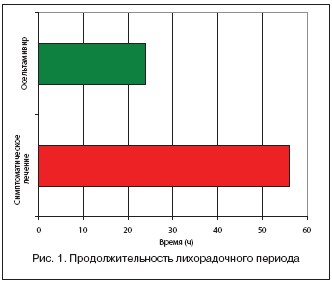
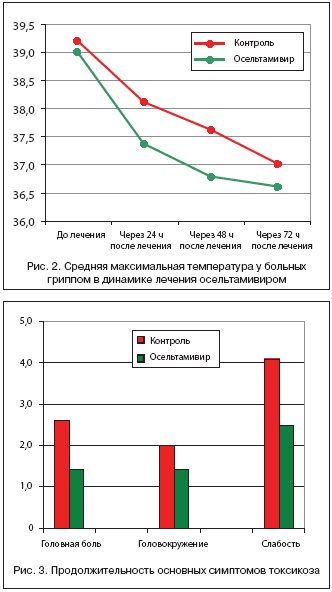
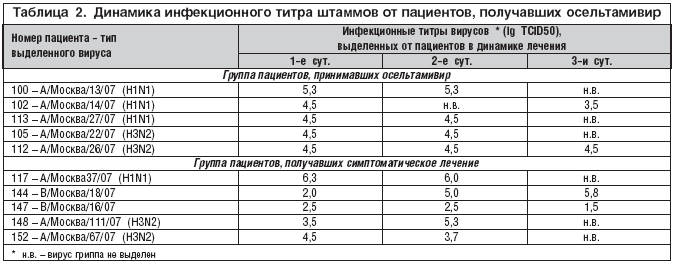
Анализ результатов исследования показал, что при лечении осельтамивиром через 24–36 ч после начала лечения температура нормализовалась у 89,7% больных; в группе получавших только симптоматическую терапию – у 3,3% (р<10–3). Продолжительность лихорадочного периода в группе больных, леченных осельтамивиром, в среднем составила 24±2 ч; в группе сравнения – 56±4 часа (р<10–8) (рис. 1). Значительный лечебный эффект осельтамивира подтвержден достоверной разницей значений средней максимальной температуры на 2–е (р<10–4) и 3–и (р<10–5) сут. лечения (рис. 2). Продолжительность головной боли, головокружения и слабости при лечении осельтамивиром была достоверно короче, чем у больных, получавших симптоматическое лечение (рис. 3). Длительность кашля у пациентов, леченных осельтамивиром, составила 2,6±0,1 сут., а в группе сравнения – 4,4±0,2 (р<10–8); трахеита – 1,7±0,1 и 3,7±0,3 сут. (р<10–8); ринита – 2,5±0,1 и 3,9±0,2 сут. (р<10–6) соответственно (рис. 4).
Следует подчеркнуть, что позитивный эффект препарата пациенты отмечали уже в первые 24 ч терапии. При лечении осельтамивиром не выявлены побочные эффекты и вторичные осложнения, в то время как при симптоматической терапии у 3 пациентов (7,9%) на 3–5 сут. болезни развились отит и пневмония.
Влияние осельтамивира на сроки элиминации вируса анализировали в подгруппе больных (5 пациентов – получали осельтамивир, 5 – симптоматическое лечение), у которых вирус был изолирован до начала терапии и проведено исследование в динамике лечения (табл. 2). Число больных с выделением вируса в обеих группах было одинаковым. В то же время инфекционные титры штаммов от пациентов, получавших симптоматическое лечение, были достоверно выше аналогичных показателей для штаммов от пациентов, леченных осельтамивиром.
Таким образом, результаты проведенного исследования свидетельствуют о высокой эффективности осельтамивира при гриппе. Применение препарата в ранние сроки болезни приводит к снижению температуры тела, уменьшению продолжительности основных симптомов болезни (лихорадки, головной боли, головокружения, кашля, трахеита, ринита) и снижению инфекционного титра вируса.
Полученные данные согласуются с результатами мультицентрового исследования [18] и позволяют рекомендовать осельтамивир в качестве препарата первого выбора для лечения больных гриппом.


Литература
1. Гендон Ю.З. Вакцины и химиопрепараты для профилактики гриппа // Вопросы вирусологии. – 2007. – № 1. – С. 4–10.
2. Семенов Б.Ф. Аргументы в пользу ежегодной вакцинации групп риска против гриппа // Вакцинопрофилактика гриппа. – 2001. – Т. 17. – № 5.
3. Palache A.M. Influenza vaccines. A reappraisal of their use // Drugs. – 1997. – V. 54. – N 6. – P. 841–856.
4. Bright R.A., Medina M.J., Xu X., et al. Incidence of adamantane resistance among influenza A (H3N2) viruses isolated worldwide from 1994 to 2005: a cause for concern // Lancet. – 2005. – V 366. – N 9492. – P. 1175–1181.
5. Бурцева Е.И., Шевченко Е.С., Ленева И.А. и др. Чувствительность к ремантадину и арбидолу вирусов гриппа, вызвавших эпидемические подъемы заболеваемости в России в сезоне 2004–2005 гг. // Вопросы вирусологии. – 2007. – Т. 52. – № 2. – С. 24–29.
6. Шевченко Е.С., Бурцева Е.И., Иванова Т.В. и др. Специфические противогриппозные химиопрепараты, обоснование их применения для профилактики и лечения в России // В сб.: Материалы Конгресса «Актуальные вопросы инфекционной патологии и вакцинопрофилактики у детей» (13–14 декабря 2007 г., Москва, Россия). М., 2007. – С. 191.
7. F. Hoffman–La Roche Ltd. Product Monograph: Tamiflu. – Ontario (Canada), 2004.
8. Hayden FG, Jennings L, Robson R, et al. Oral oseltamivir in human experimental influenza B infection // Antivir. Ther. – 2000. – V. 5. – N 3. – P. 205–213.
9. Oxford J.S., Lambkin R. Targeting influenza virus neuraminidase – a new strategy for antiviral therapy // Drug Discover Today. – 1998. – N 3. – P. 448–456.
10. Eisenberg E.J., Bidgood A., Cundy K.C. Penetration of GS4071, a novel influenza neuraminidase inhibitor, into rat bronchoalveolar lining fluid following oral administration of the prodrug GS4104 // Antimicrob. Agents Chemother. – 1997. – V 41. – N 9. – P. 1949–1452.
11. He G., Massarella J., Ward P. Clinical pharmacokinetics of the prodrug oseltamivir and its active metabolite Ro 64–0802 // Clin. Pharmacokinet. –1999. – V. 37. – N 6. – P. 471–484.
12. Treanor J.J., Hayden F.G., Vrooman P.S., et al. Efficacy and safety of the oral neuraminidase inhibitor oseltamivir in treating acute influenza: a randomized controlled trial. US Oral Neuraminidase Study Group // JAMA. – 2000. – V. 283. – N 8. – P. 1016–1024.
13. Nicholson K.G., Aoki F.Y., Osterhaus A.D., et al. Efficacy and safety of oseltamivir in treatment of acute influenza: a randomised controlled trial. Neuraminidase Inhibitor Flu Treatment Investigator Group // Lancet. – 2000. – V. 355. – N 9218. – P. 1845–1850.
14. Monto A.S., McKimm–Breschkin J.L., Macken C., et al. Detection of influenza viruses resistant to neuraminidase inhibitors in global surveillance during the first 3 years of their use // Antimicrob. Agents Chemother. – 2006. – V 50. – N 7. – P. 2395–2402.
15. Kiso M., Mitamura K., Sakai–Tagawa Y., et al. Resistant influenza A viruses in children treated with oseltamivir: descriptive study // Lancet. – 2004. – V. 364. – N 9436. – P. 759–765.
16. Dybing J.K., Schultz–Cherry S., Swayne D.E. et al. Distinct pathogenesis of Hong Kong–origin H5N1 viruses in mice compared to that of other highly pathogenic H5 avian influenza viruses // J. Virol. – 2000. – V. 74. – N 3. – P. 1443–1450.
17. Kuiken T., Rimmelzwaan G.F., Van Amerongen G., Osterhaus A.D. Pathology of human influenza A (H5N1) virus infection in cynomolgus macaques (Macaca fascicularis) // Vet. Pathol. – 2003. – V. 40. –N 3. – P. 304–310.
18. Малеев В.В. Роль ингибиторов нейраминидазы в профилактике и лечении гриппа // Клиническая фармакология и терапия. – 2007. – № 1. – С. 1–6.












