В настоящее время поллиноз является одним из самых распространенных аллергических заболеваний, по данным разных авторов, его распространенность среди населения достигает 10–30% [2,3]. Как правило, при поллинозе вспышки заболевания носят сезонный характер – отмечаются в период цветения растений. В центральной полосе России выделяют три пика цветения растений: в апреле–мае цветут деревья и кустарники (береза, ольха, орешник, ива, дуб, ясень, клен, вяз, тополь, осина, сосна), в июне–июле – злаки и луговые травы (ежа, костер, тимофеевка, мятлик райграс, лисохвост, овсяница, полевица, пырей, вейник), а в августе–сентябре – сорные травы (полынь, конопля, лебеда, подорожник, марь, амброзия). Первые симптомы заболевания появляются у пациентов при достижении определенной концентрации пыльцы – не менее 10–50 пыльцевых зерен на 1 куб. м воздуха.
Аллергические реакции на пыльцу могут проявляться разнообразно, органами–мишенями становятся и кожа, и бронхи, и желудочно–кишечный тракт. Но чаще всего при аллергических реакциях страдают конъюнктива глаз и слизистая верхних дыхательных путей. Сезонный аллергический ринит (САР) и конъюнктивит, как правило, не требуют госпитализации и не приводят к инвалидности и смерти пациента. Однако на фоне сезонного аллергического риноконъюнктивита (САРК) резко ухудшается качество жизни пациентов, снижается их работоспособность. Как любая хроническая патология поллиноз имеет тенденцию к утяжелению заболевания – симптомы становятся более выраженными, у части больных развивается пыльцевая бронхиальная астма, снижается эффективность традиционной базисной терапии, расширяется спектр аллергенов, что приводит к увеличению продолжительности периода обострения [1,3,4].
Проявлением поллиноза может быть оральный аллергический синдром, который довольно часто связан с перекрестной аллергией растений и пищевых продуктов. Так, у пациентов отмечаются аллергические реакции (генерализованная крапивница, отеки Квинке в области лица, шеи и гортани, анафилактический шок и др.) после употребления в пищу определенных продуктов не только в сезон пыления причинно–значимых растений, но и на протяжении всего года. Наиболее часто встречается перекрестная аллергия между пыльцой березы и яблоками, косточковыми, растущими на деревьях, лесными орехами, морковью, сельдереем, картофелем.
Доказано, что даже легкие и непродолжительные (в течение 2 нед.) проявления поллиноза оказывают нежелательное действие на психологическое состояние и повседневную жизнь больных, вызывая у них нарушение когнитивных функций, снижение памяти, способности к обучению, а также ограничивая их профессиональную деятельность. Адекватное лечение приводит к уменьшению клинических проявлений и улучшению качества жизни пациентов [1,3,4].
В настоящее время основными направлениями терапии поллинозов являются элиминация аллергенов, аллерген–специфическая иммунотерапия (АСИТ), а в период обострения заболевания – фармакотерапия, направленная на устранение симптомов.
АСИТ – единственный на сегодняшний день метод противоаллергического лечения, воздействующий на все патогенетические звенья аллергического процесса и обладающий длительным клиническим и профилактическим эффектом. Терапия аллергенами известна с 1911 г. и широко используется в настоящее время. Однако для проведения АСИТ существуют возрастные ограничения, кроме того, для достижения терапевтической эффективности необходимо длительное введение аллергена под контролем, что существенно осложняет использование данного метода в педиатрической практике.
В период поллинации у больных возникает необходимость в купировании симптомов заболевания. В качестве базисной терапии применяются антигистаминные препараты и топические глюкокортикостероиды, которые действуют на основные патогенетические звенья воспаления.
Согласно современным представлениям, на ранней стадии аллергического воспаления особая роль отводится IgЕ–зависимому иммунному ответу. Особенностью IgЕ является избирательная способность фиксироваться на поверхности клеток–мишеней первого порядка (тучные клетки), способных высвобождать биологически активные вещества, изменяющие функцию других клеток. Под воздействием аллергена у лиц, имеющих генетическую предрасположенность, наблюдается повышенная выработка специфических веществ (антител). Развитие первой стадии аллергического воспаления обусловлено действием медиаторов тучной клетки, которые выделяются в результате взаимодействия аллергена и IgЕ–антител. Антигены и антитела фиксируются на тучной клетке, содержащей гранулы гистамина. Клетка активизируется, и происходит выброс гистамина, который является биологически активным веществом [1,2,5–7].
Гистамин впервые был синтезирован в 1907 г. в лабораторных условиях, а в 1910 г. выделен из спорыньи. В 1920 г. было сформулировано представление о гистамине как о важнейшем медиаторе аллергии. Серия исследований в 1920–х гг. дала возможность установить, что гистамин является причиной таких аллергических проявлений, как анафилактический шок, ринит, бронхиальная астма, крапивница.
При воздействии гистамина на те или иные рецепторы в тканях возникает соответствующая клиническая картина заболевания: расширяются сосуды, повышается их проницаемость с образованием отека и выделением большого количества жидкости во внешнюю среду. Наблюдается также гиперсекреция слизи железами, расположенными в полости носа. Выделение гистамина вызывает раздражение слизистой носа, зуд и чихание. Купировать симптомы заболевания необходимо путем блокирования действия гистамина с помощью антигистаминных препаратов.
Изучение антигистаминов началось в конце 1930–х гг., через 10 лет они стали применяться для лечения различных заболеваний. В 1966 г. была доказана гетерогенность гистаминовых рецепторов, стало понятно, что эффект гистамина зависит от того, с каким рецептором он свяжется. В 1972 г. были выделены два типа гистаминовых рецепторов – Н1 и Н2, в начале 1980–х гг. – Н3–рецепторы, представленные преимущественно в ЦНС. Н1–рецепторы находятся в основном на клетках гладкой мышечной ткани и крупных кровеносных сосудах. Их активация вызывает спазм мышечной ткани трахеи, бронхов, увеличивает сосудистую проницаемость, замедляет атриовентрикулярную проводимость, усиливает зуд.
Н1–блокаторы – это препараты, традиционно применяемые при аллергических заболеваниях. Механизм их действия обусловлен тем, что они, обладая структурой, сходной со структурой гистамина, конкурируют с последним и блокируют Н1–рецепторы. Высвободившийся во время аллергической реакции гистамин лишен возможности связаться с достаточным количеством Н1–рецепторов и, таким образом, его эффект оказывается значительно менее выраженным либо отсутствует.
Н2–блокаторы используются для лечения язвенной болезни, так как они угнетают секрецию соляной кислоты.
В 1942 г. был синтезирован первый антигистаминный препарат Phenbenzamine, а в 1957 г. итальянский фармаколог Д. Бове был удостоен Нобелевской премии за синтез и исследования препаратов, часть из которых впоследствии вошла в состав группы антигистаминных препаратов первого поколения.
В настоящее время к их числу относят дифенгидрамин, дименгидринат, кифенадин, хлоропирамид, клемастин, сетастин, ципрогептадин и др. Эти препараты обладают рядом побочных эффектов, такими как кратковременность терапевтического действия (1,5–3 ч), неполное связывание с Н1–рецепторами, проходимость через гематоэнцефалический барьер, тахифилаксия (привыкание на 7–12 сут.), связывание с М–холинорецепторами и альфа–адренорецепторами (неселективность действия), стимуляция аппетита, потенцирование седативного эффекта под влиянием алкоголя и депрессантов ЦНС.
Наличие у Н1–блокаторов первого поколения нежелательных эффектов ограничивает применение этих препаратов. Тем не менее, по прогнозам ученых, они будут продолжать применяться, во–первых, потому что имеется огромный опыт их использования, во–вторых, из–за того, что в определенных клинических ситуациях побочные эффекты (например, седативный) могут быть значимыми [1,2,5,8].
Вместе с тем наличие нежелательных эффектов у классических антагонистов гистамина стало причиной поиска новых Н1–блокаторов. В 1977 г. был создан антигистаминный препарат, который, обладая выраженной способностью подавлять кожную аллергическую реакцию, практически не оказывал седативного эффекта. В клинической практике стали использоваться препараты второго поколения: терфенадин, лоратадин, астемизол, цетиризин (Зиртек, Зодак), акривастин, эбастин, азеластин, фексофенадин, левокабастин, левоцитиризин.
Эффективность и безопасность Н1–блокаторов второго поколения определили их незаменимость в терапии поллинозов. Препараты данной группы обладают высоким сродством с Н1–рецепторами, не блокируют другие рецепторы, отличаются быстрым началом действия и достаточной его продолжительностью (12–24 ч), что позволяет использовать их 1 раз/сут. Антигистаминные препараты нового поколения имеют низкую проходимость гематоэнцефалического барьера (или она отсутствует), вследствие чего седативный эффект не возникает. Препараты данной группы не вызывают тахифилаксию, их можно применять длительно [1,8].
В большинстве случаев сродством к Н1–гистаминовым рецепторам обладают не сами Н1–блокаторы второго поколения, а их метаболиты, кроме цетиризина, акривастина и фексофенадина, которые метаболизму не подвергаются, а действуют самостоятельно. Этим обстоятельством объясняется вариабельность эффективности препаратов у разных лиц, что может быть связано с индивидуальными особенностями метаболизма препаратов (как врожденными, так и приобретенными) [1,8].
Однако при приеме препаратов нового поколения Н1–блокаторов гистаминовых рецепторов могут развиваться нежелательные побочные эффекты. В случае выраженного нарушения метаболизма некоторых Н1–блокаторов второго поколения в организме пациента может отмечаться высокая концентрация исходного вещества с последующим развитием кардиотоксического эффекта. Так, было установлено, что применение терфенадина и астемизола в тех случаях, когда из–за особенностей метаболизма пациента или из–за взаимодействия с другими лекарственными препаратами их содержание в крови возрастало, приводило к задержке реполяризации сердца, увеличению интервала QТ путем блокады калиевых каналов, нарушению желудочкового сердечного ритма, желудочковой «веретенообразной» тахикардии и внезапной смерти [1,5,8].
Среди антигистаминных препаратов второго поколения одним из наиболее изученных и хорошо зарекомендовавших себя во многих странах мира является препарат цетиризин. Помимо возможности блокировать H1–гистаминовые рецепторы цетиризин обладает выраженной противовоспалительной активностью, связанной со способностью подавлять действие индукторов синтеза гистамина, ингибировать индуцируемый ЛТВ4 хемотаксис моноцитов и прикрепление эозинофилов к эндотелию, тормозить экспрессию адгезивных молекул и продукцию ЛТС4 эозинофилами. Цетиризин ингибирует развитие ранней и поздней фазы аллергического ответа, тормозит процесс аккумуляции эозинофилов в слизистой оболочке бронхов [5,8–11].
Проведено немало исследований, показавших клиническую эффективность цетиризина при аллергических заболеваниях [9–14]. Появление большого числа генерических препаратов цетиризина (более 10 наименований (по данным РЛС, 2009)) привело к снижению стоимости курсового лечения, более широкому их применению в амбулаторной практике. Вместе с тем существует мнение, что у оригинального препарата и его генериков время начала терапевтического эффекта, длительность действия и эффективность различаются, несмотря на одинаковый качественный и количественный состав действующего вещества. Это, в свою очередь, ставит вопрос об их терапевтической эквивалентности и критериях выбора.
С целью оценки безопасности, переносимости и лечебной эффективности цетиризина в каплях (Зодак, Zentiva и Зиртек, UCB) при лечении сезонного аллергического ринита у детей нами проведено открытое рандомизированное сравнительное исследование в параллельных группах в период обострения заболевания. Оценивались терапевтическая эффективность препарата Зодак капли в сравнении с оригинальным препаратом Зиртек капли, а также безопасность и переносимость препарата Зодак в сравнении с препаратом Зиртек.
Работа осуществлялась с апреля по июль 2011 г. под руководством сотрудников кафедры педиатрии ГБОУ ВПО МГМСУ Минздравсоцразвития России (зав. кафедрой профессор О.В. Зайцева) на базе аллергологического отделения детской городской клинической больницы Св. Владимира и отделения аллергологии ГБУЗ «Центральная детская клиническая больница» Федерального медико–биологического агентства России. Исследование проводилось в строгом соответствии с требованиями Хельсинкской декларации (WMA, 1964) и Декларации о политике в области обеспечения прав пациентов в Европе (WHO/EURO, 1994).
Пациенты и методы
В исследовании приняли участие 40 детей с диагностированным сезонным аллергическим ринитом, среди которых преобладали мальчики – 75% (n=30), девочки составили 25% (n=10).
Критериями включения в исследование были возраст детей – от 6 до 17 лет, установленный диагноз – сезонный аллергический ринит легкого интермиттирующего и персистирующего, среднетяжелого персистирующего течения, стаж заболевания – 1 год и более, характерная клиническая картина и сенсибилизация к пыльце деревьев, подтвержденная кожными пробами со стандартизованными аллергенами и/или наличием специфических IgE.
Критериями исключения из исследования стали применение других антигистаминных препаратов (в том числе топических) за 4 нед. до начала исследования, использование интраназальных и ингаляционных глюкокортикостероидов за 4 нед. до начала и во время исследования, тяжелое течение аллергического ринита, круглогодичный аллергический ринит, бронхиальная астма среднетяжелого и тяжелого течения, требующая применения ингаляционных глюкокортикостероидов, тяжелые сопутствующие заболевания (язвенная болезнь желудка и 12–перстной кишки, кровохарканье, легочное кровотечение, сахарный диабет, туберкулез, хронические заболевания печени и почек, онкологические заболевания в любой стадии, ВИЧ), наличие чувствительности, аллергические реакции на цетиризин, несоблюдение пациентом назначений врача или отказ родителей от участия в программе.
Исследование проводилось в течение 8 нед. При первом визите у всех детей на основании клинико–анамнестических и лабораторных данных с учетом аллергологического статуса был диагностирован сезонный аллергический ринит. В ходе аллергологического обследования, проведенного не более чем за 1 год до исследования (специфические иммуноглобулины Е, кожное тестирование), была документально подтверждена сенсибилизация к пыльце деревьев, луговых или сорных трав. Клиническая картина заболевания наблюдалась в один и тот же весенне–летний период в течение последних двух лет и на момент первичного осмотра требовала фармакологического лечения.
В процессе наблюдения в динамике проводилась оценка клинических симптомов заболевания, таких как ринорея, заложенность носа, чихание и зуд в носу, слезотечение, зуд век, гиперемия. Тяжесть симптомов оценивалась по шкале от 0 до 4 и фиксировалась в дневнике (0 – отсутствие симптомов, 1 – легкие симптомы, 2 – симптомы средней тяжести, 3 – тяжелые и 4 – очень тяжелые симптомы).
При первом визите все пациенты методом случайной выборки были разделены на 2 группы. Группу наблюдения составили 20 пациентов, из них 20% (4) – девочки, 80% (16) – мальчики. Дети в данной группе получали препарат Зодак в каплях (капли для приема внутрь 10 мг/1 мл) по 20 капель (10 мг) 1 раз/сут. Группа сравнения также состояла из 20 человек, из них 30% (6) девочек и 70% (14) мальчиков. Пациенты получали Зиртек (капли для приема внутрь 10 мг/1 мл) по 20 капель (10 мг) 1 раз/сут. Продолжительность терапии составила 8 нед.
Последующие визиты проводились на 10, 30 и 60–й дни наблюдения. В ходе исследования осуществлялась сравнительная оценка безопасности, переносимости и лечебной эффективности цетиризина. Клиническая эффективность препарата оценивалась на основании состояния больного и основных симптомов заболевания, выраженных в баллах: ринореи, заложенности носа, чихания, зуда в носу, слезотечения, зуда век, гиперемии век.
Всем пациентам была рекомендована элиминация аллергенов, при необходимости – использование назального деконгестанта и назального топического препарата кромоглиевой кислоты (кромогексал назальный спрей и капли для глаз), при ухудшении состояния – прием топических глюкокортикостероидов, что фиксировалось в дневнике наблюдения.
Результаты исследования
Диагноз сезонного аллергического ринита был установлен у всех 40 детей на основании клинико–анамнестических данных. Анализ аллергологического статуса пациентов помог выявить следующую сенсибилизацию к пыльцевым аллергенам: повышенная чувствительность к пыльце деревьев – у 27,5% (11) детей, к пыльце деревьев и сорных трав – у 22,5% (9), к пыльце деревьев и луговых трав – у 25% (10), одновременно к пыльце деревьев, сорных и луговых трав – у 25% (10) детей. Обострение клинических симптомов на фоне цветения деревьев отмечалось у 70% (28) пациентов. Обострение заболевания, связанное с цветением луговых трав, было выявлено у 20% (8) больных. Обострение аллергического ринита на фоне цветения сорных трав отмечено у 10% (4) пациентов. Именно в период обострения сезонного аллергического ринита проводилось изучение терапевтической эффективности цетиризина.
Исходно тяжесть клинических симптомов у детей в обеих группах была сравнима. У всех пациентов в обеих группах имелись среднетяжелые или тяжелые симптомы аллергического ринита и конъюнктивита. Оценка по шкале выявила сравнимую по тяжести симптомов клиническую картину заболевания в обеих группах: в группе наблюдения – 3,33 балла, в группе сравнения – 2,7 балла (табл. 1, рис. 1).
На фоне терапии препаратами цетиризина было выявлено достоверное улучшение качества жизни пациентов в обеих группах. Уже на 10–е сут. от начала терапии отмечалось уменьшение тяжести симптомов в обеих группах: общий балл тяжести симптомов снизился в группе наблюдения с 3,33 до 2,43, а в группе сравнения – с 3,15 до 1,73 (табл. 1, рис. 1).
В обеих группах отмечалось быстрое купирование симптомов аллергического конъюнктивита на фоне терапии при более длительном сохранении явлений аллергического ринита. В группе сравнения у одного пациента симптомы аллергического конъюнктивита были купированы к десятому дню терапии, в то время как проявления аллергического ринита уменьшились, но еще беспокоили детей. Вместе с тем клиническая эффективность Зиртека в группе сравнения была более выражена. Так, у детей данной группы к десятому дню терапии отмечалось большее снижение тяжести симптомов, чем в группе наблюдения (2,43 и 1,73 балла соответственно). Однако различия в группах, в которых применялись Зодак и Зиртек, на 10–е сут. были недостоверны из–за большого разброса показателей (p>0,05).
К 30–м сут. терапии у 75% больных в обеих группах явления аллергического конъюнктивита были полностью купированы. У 25% в группе наблюдения и 35% в группе сравнения отсутствовали ринорея, зуд в носу, чихание. Однако у 90% (18) детей в группе наблюдения и 85% (17) детей в группе сравнения длительно сохранялась заложенность носа. Данный симптом являлся наиболее частой жалобой пациентов.
Динамика симптомов заболевания на 60–е сут. терапии препаратами цетиризина выявила полное купирование симптомов заболевания у 50% (10) пациентов группы наблюдения и 40% (8) пациентов группы сравнения. Надо отметить, что в группе сравнения на 60–е сут. терапии у трех пациентов вновь появились симптомы риноконъюнктивита, обусловленные началом нового периода поллинации – цветением луговых трав, что потребовало продолжения курса терапии.
Таким образом, на фоне терапии препаратами цетиризина Зиртек и Зодак была выявлена выраженная положительная динамика клинических симптомов сезонного аллергического ринита в обеих группах. Отмечалась несколько большая клиническая эффективность препарата Зиртек на 10–е сут. от начала терапии, но различия в группах были недостоверны из–за большого разброса показателей (p>0,05). Однако в процессе лечения на 30–е и 60–е сут. достоверных различий качества жизни пациентов обеих групп не выявлено.
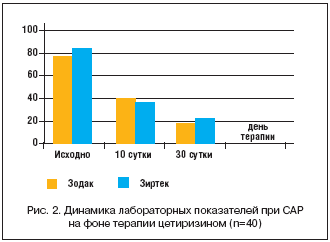
В ходе исследования оценивались лабораторные показатели у пациентов с сезонным аллергическим ринитом на фоне терапии препаратами цетиризина (табл. 2, рис. 2).
Анализ лабораторных показателей объективно подтвердил положительную динамику течения заболевания в обеих группах пациентов. Особенно отчетливо это видно в риноцитограмме с подсчетом процентного содержания эозинофилов. Именно этот показатель характеризует остроту аллергического воспаления на слизистой носа. В процессе наблюдения отмечалось достоверное снижение эозинофилии в риноцитограмме в обеих группах, что коррелировало с динамикой клинической картины заболевания. Различия в группах носили недостоверный характер (p>0,05). В ходе исследования необходимости в назначении топических и системных кортикостероидов не возникло ни в одном случае.
Переносимость препаратов Зодак и Зиртек у детей была удовлетворительной. Серьезных нежелательных явлений, которые потребовали бы отмены препаратов, при проведении терапии в обеих группах выявлено не было. Однако у 25% (5) детей в группе наблюдения и у 20% (4) детей в группе сравнения отмечалась повышенная сонливость, им было рекомендовано перейти на прием препаратов в вечерние часы.
При анализе результатов исследования было выявлено достоверное улучшение субъективных и объективных симптомов заболевания у детей с сезонным аллергическим ринитом на фоне терапии препаратом цетиризина Зодак, сопоставимое с эффективностью препарата Зиртек. При оценке безопасности терапии препаратами Зодак и Зиртек статистически достоверных различий между группами не выявлено, серьезных нежелательных явлений, которые потребовали бы отмены препаратов, зафиксировано не было.
Таким образом, при обострении поллиноза препаратом выбора в составе базисной терапии сезонного аллергического ринита у детей может быть рекомендован препарат цетиризина Зодак, отличающийся высокой клинической эффективностью и безопасностью.



Литература
1. Горячкина Л.А., Передкова Е.В., Храмцова Н.Н. Поллинозы: Учеб. пособие. М.: ООО «Колор Ит Студио», 2004. 24 с.
2. Курбачева О.М., Павлова К.С. Поллиноз: диагностика, клиника, лечение // Медицинская кафедра. 2003. № 2 (6). С. 38–45.
3. Ильина Н.И. Аллергопатология в разных регионах России по результатам клинико–эпидемиологических исследований: Автореф. дисс. докт. мед. наук. М., 1996. 24 с.
4. Данилычева И.В. Некоторые аспекты образа жизни больных поллинозом // Consilium medicum. 2003. Т. 5. № 4. С. 223–225.
5. Гущин И. С. Аллергическое воспаление и его фармакологический контроль. М.: Фармарус Принт, 1998. 25 с.
6. Гущин И. С. Аллергия: аллергены, индукция и регуляция синтеза IgE // Патол. физиол. 1999. № 1. С. 24–32.
7. Клинические рекомендации по диагностике и лечению аллергического ринита. Пособие для врачей / Под ред. А.С. Лопатина. СПб, 2004. 48 с.
8. Смирнова Г.И. Антигистаминные препараты для лечения аллергических болезней у детей. М., 1999. 36 с.
9. Falliers C.J., Brandon M.L., Buchman E., Connell J.T., Dockhorn R., Leese P.T., Miller J., Wasserman S., Zeterberg J. Altman R. Love S. Samuels L.L. Double–blind comparison of cetirizine and placebo in the treatment of seasonal rhinitis // Ann Allergy. 1991. Vol. 66. Р. 257–262.
10. Mansmann Jr. H.C., Altman R.A., Berman B.A., Buchrnan E., Dockhorn R.J., Leese P.T., Love S.J., Middleton Jr. E. Efficacy and safety of cetirizine therapy in perennial allergic rhinitis // Ann Allergy. 1992. Vol. 68. Р. 348–353.
11. Jobst S., Van den Wijngaart W., Schubert A., Van de Venne H. Assessment of the efficacy and safety of three dose levels of cetirizine given once daily in children with perennial allergic rhinitis // Allergy. 1994. Vol. 49. Р. 598–604.
12. Ciprandi G., Tosca M., Ricca Vm Passalacqua G., Riccio A.M., Bagnasco M. et al. Cetirizine treatment of rhinitis in children with pollen allergy: evidence of its antiallergic activity // Clin Exp Allergy. 1997. Vol. 27(10). Р. 1160–1166.
13. Juniper E.F., Howland W.C., Roberts N.B. et al. Measuring quality of life in children with rhinoconjunctivitis // J. Allergy Clin. Immunol. 1998. Vol. 101. P. 163–170.
14. Masi M., Candiani R., Van de Venne H. A placebo–controlled trial of cetirizine in seasonal allergic rhinoconjunctivitis in children aged 6 to 12 years // Pediatr Allergy Immunol. 1993. Vol. 4 (Suppl 4). Р. 47–52.
RU.CTR.12.01.02












