Ведущим клиническим проявлением патологии желчевыводящей системы является боль. Как факторы генеза боли, факторы, определяющие ее характер, обсуждаются спазм гладкой мускулатуры желчного пузыря и сфинктеров, спастическая ишемия, повышение давления в билиарном тракте вследствие нарушения моторики, воспалительный процесс, воздействие кальцинатов. При этом моторно–тоническая дисфункция желчного пузыря (ЖП), желчных протоков и сфинктеров определяет во многом комплекс клинических симптомов как при органической, так и при функциональной билиарной патологии.
Функциональная патология желчевыводящих путей – это заболевания, при которых рутинные методы лабораторно–инструментального исследования не выявляют органического субстрата болезни.
Международной классификацией вместо определения «функциональные заболевания билиарного тракта» (Римский консенсус, 1999) принят термин «дисфункциональные расстройства билиарного тракта». При этом независимо от этиологии их принято подразделять на 2 типа: дисфункция желчного пузыря и дисфункция сфинктера Одди. В Международной классификации болезней (МКБ–10) под рубрикой К 82.8 выделены только «дискинезия желчного пузыря и пузырного протока» и под рубрикой К 83.4 — «спазм сфинктера Одди» [1,2].
В регуляции двигательной активности билиарной системы принимают участие парасимпатический и симпатический отделы вегетативной нервной системы, а также эндокринная система. Такая кооперация обеспечивает синхронизированную последовательность сокращения и расслабления желчного пузыря и сфинктерного аппарата.
Из печеночных протоков и общего желчного протока желчь в ЖП поступает в момент закрытия сфинктера Одди (ему принадлежит решающая роль в создании градиента давления). При этом сфинктер Одди вне пищеварения закрыт непостоянно, но небольшие порции желчи систематически поступают в двенадцатиперстную кишку.
Сфинктер Одди состоит из: собственно сфинктера большого дуоденального сосочка (БДС) – сфинктера Вестфаля, обеспечивающего разобщение протоков и двенадцатиперстной кишки; сфинктера общего желчного протока; сфинктера панкреатического протока. Работа всей билиарной системы строго координирована, что обеспечивается нервной и гуморальной регуляцией. Показано, что умеренное раздражение блуждающего нерва вызывает координированную активность ЖП и сфинктеров, а сильное раздражение — спастическое сокращение с задержкой эвакуации желчи. Раздражение симпатического нерва способствует расслаблению желчного пузыря. Мускулатура сфинктера Одди не зависит от мускулатуры двенадцатиперстной кишки.
Из гастроинтестинальных гормонов максимальный эффект оказывает холецистокинин, который наряду с сокращением желчного пузыря способствует расслаблению сфинктера Одди. Стимулом к выработке ХЦК является поступление жиров в ДПК, а к нервным регулирующим воздействиям — градиент давления и его изменение [10].
Двигательная реакция ЖП и сфинктера Одди находится в прямой зависимости от количества и качества пищи, а также от эмоционального состояния человека. Различают первичные и вторичные дисфункциональные расстройства. Первичные составляют в среднем 10–15%. При этом снижение сократительной функции ЖП может быть связано как с уменьшением мышечной массы (редко), так и со снижением чувствительности рецепторного аппарата к нейрогуморальной стимуляции. Малое количество рецепторов может быть как генетически детерминированным, так и приобретенным при воспалительных, дистрофических и метаболических процессах.
Вторичные дисфункциональные нарушения билиарного тракта могут наблюдаться при гормональных расстройствах, в том числе при предменструальном синдроме, беременности, системных заболеваниях, диабете, гепатите, циррозе печени, еюностомии, а также при воспалении и камнях в ЖП,а также при лечении соматостатином. К нарушениям ритмической деятельности билиарной системы приводят воспалительные процессы в печени, приводящие к снижению синтеза желчи, заметному уменьшению давления в протоковой системе и желчном пузыре и в связи с этим – к постоянному спастическому сокращению сфинктера Одди.
Различные оперативные вмешательства (холецистэктомия, ваготомия, резекция желудка) также являются причиной нарушений моторики желчевыводящих путей.
Для простоты восприятия и более удобного применения на практике в классификации дисфункциональных расстройств билиарного тракта представлены однонаправленные расстройства, хотя в жизни они чаще носят сложный характер, с преобладанием одного из компонентов.
1. По локализации:
• Дисфункция желчного пузыря
• Дисфункция сфинктера Одди
2. По этиологии:
• Первичные
• Вторичные
3. По функциональному состоянию:
• Гиперфункция
• Гипофункция.
При гиперкинетических расстройствах возникают коликообразные боли различной интенсивности без иррадиации или с иррадиацией вправо, в спину, иногда в левую половину живота (при вовлечении протоковой системы поджелудочной железы). При гипокинезии — тупые боли в правом подреберье, чувство давления, распирания, усиливающееся при изменении положения тела и при увеличении внутрибрюшного давления, изменяющего градиент давления для тока желчи [11]. Общими для разных форм дисфункции являются горечь во рту, вздутие живота, неустойчивый стул. Симптомы кишечной диспепсии обусловлены важной ролью желчи в пищеварении и последствиями нарушения поступления желчи в кишечник.
Диагностическими критериями дисфункции ЖП являются эпизоды сильной постоянной боли, локализованной в эпигастрии или в правом верхнем квадранте живота, при этом характерны следующие особенности:
• продолжительность эпизодов в 30 и более минут;
• симптомы встречаются 1 и более раз за предшествующие 12 мес;
• постоянный характер болей, снижение дневной активности пациентов и необходимость консультации у врача;
• отсутствие доказательств органической патологии, обусловливающей симптомы;
• наличие нарушения функции опорожнения желчного пузыря.
В отношении дисфункции сфинктера Одди выделяют 4 клинико–лабораторных типа (3 типа билиарной дисфункции и 1 тип панкреатической дисфункции). В основу диагностических критериев положены: приступ болей билиарного типа и 3 лабораторно–инструментальных признака (подъем АСТ и/или ЩФ в 2 и более раза при двукратном определении; замедление выведения контрастных веществ при ЭРПХГ (> 45 мин); расширение общего желчного протока более 12 мм, исследования проводятся в период обострения).
• Первый тип дисфункции характеризуется болями и 3 признаками.
• Второй тип дисфункции отличается болями и наличием 1 или 2 признаков.
• Третий тип – только приступы болей.
• Четвертый тип – панкреатический, характеризуется «панкреатическими» болями и повышением уровня амилазы или липазы, повышение ферментов может отсутствовать.
Дискинезия желчевыводящих путей представляет собой несогласованное, несвоевременное, недостаточное или чрезмерное сокращение ЖП, протоков и сфинктерного аппарата – сфинктеров Одди (в дистальном отделе общего желчного и главного панкреатического протока), Люткенса–Мартынова (в пузырном протоке), Мирицци (в общем печеночном протоке) [12].
Основными признаками дискинезий являются нарушения кинеза (гипер– и гипокинезия) и тонуса (гипер– и гипотония). На основании чего выделяют две основные формы дискинезии: гипотонически–гипокинетическую (или гипомоторную) и гипертонически–гиперкинетическую (или гипермоторную). Длительные клинические наблюдения показали, что характер дискинезии не является постоянным; описана возможность перехода гиперкинетического типа дискинезии в гипокинетический.
Клинические проявления дискинезии ЖП определяются наличием одного или нескольких синдромов:
• болевого,
• билиарной диспепсии,
• воспалительного (при обострении хронического холецистита),
• вовлечения в процесс других органов и систем,
• астеноневротического.
Наиболее частым проявлением дискинезии желчного пузыря является болевой синдром. Как правило, боли локализуются в правом подреберье, реже – в эпигастральной области. Характер их может различаться при разных формах дискинезии. При гипокинетической – боль постоянная ноющая, усиливается после погрешностей в диете и физических нагрузок. Этим болевым ощущениям нередко сопутствуют диспепсические расстройства – горечь во рту, тошнота, иногда рвота желчью, расстройства стула (чаще запоры), метеоризм. При гиперкинетической дискинезии пациентов обычно беспокоят кратковременные схваткообразные боли в правом подреберье, в большинстве случаев проходящие самостоятельно. Больные отмечают наиболее частую связь приступов с сильными отрицательными эмоциями, значительно реже – с приемом пищи и физическими нагрузками.
Помимо проявлений собственно дискинезии ЖП, у больных могут быть жалобы, связанные с вовлечением в патологический процесс желудка и двенадцатиперстной кишки, поджелудочной железы и печени.
При физикальном обследовании у пациентов с ДЖП обычно выявляются местная болезненность при пальпации в зоне ЖП, а также положительные, хотя и непостоянные, «пузырные» симптомы, обусловленные повышением давления в желчном пузыре, но не воспалением – симптом Мерфи и Кера.
Изменения в общеклиническом и биохимическом анализах крови в первую очередь важны для дифференциации ДЖП и калькулезного или бескаменного холецистита. У больных с «чистой» дискинезией отсутствуют острофазовые показатели; биохимические исследования, характеризующие печеночный цитолитический, холестатический, иммуновоспалительный синдром, как правило, не имеют существенных отклонений от нормы.
В настоящее время широкое распространение получило ультразвуковое исследование ЖП и желчевыводящих путей. При этом чрезвычайно важной является правильная подготовка пациентов к исследованию: двенадцатичасовое ночное голодание, заблаговременное (за 1–2 дня) исключение из рациона продуктов, вызывающих метеоризм (свежие овощи, черный хлеб, молоко), при необходимости – назначение активированного угля, симетикона. Главное достоинство метода – возможность определить конкременты в пузыре, сладж, полипы и признаки воспаления. Ультразвуковыми признаками холецистита являются: утолщение стенки более 3 мм; ультразвуковой симптом Мерфи, хлопьевидная взвесь; уплотнение стенок; неровность контуров .
Размеры желчного пузыря натощак могут значительно варьировать, но в норме его поперечник не превышает 3 см, длинник – 8–10 см.
Для исследования сократимости используются различные методы: рентгенологические (пероральная, в/в и ретроградная холецистография), эхографические (ультразвуковая холецистография), сцинтиграфические (статическая и динамическая гепатобилисцинтиграфия), зондовые (многофракционное дуоденальное зондирование, фракционное хроматическое зондирование). В последнее время для уточнения состояния сфинктера Одди применяется также манометрия – исследование весьма информативное, но дорогостоящее, технически сложное и чреватое возможным развитием осложнений, в частности, острого панкреатита.
Основным в настоящее время, безусловно, стал ультразвуковой метод диагностики дискинезий. Среди преимуществ УЗИ по сравнению с остальными методиками – возможность проведения процедуры без предварительной подготовки больного, неинвазивность метода, отсутствие лучевой нагрузки, высокая информативность, а также наилучшее соотношение затраты/результаты среди всех методов получения изображения.
Для суждения о моторно–эвакуаторной функции ЖП оценивается степень его сократимости после желчегонного завтрака. После измерения исходных размеров (максимальный продольный, поперечный и диагональный размеры акустической тени ЖП) вычисляется объем ЖП натощак и назначается желчегонный завтрак (обычно это два сырых яичных желтка или сорбитол). Повторное определение размеров и степени сократимости желчного пузыря в % проводится в течение 120 минут с интервалом: 15, 30, 45, 60, 90 и 120 минут. Нормальным считается сокращение на 1/2–2/3 исходного объема в течение 30–45 минут и возвращение к первоначальным размерам к концу исследования. При сокращении ЖП менее чем на 1/2 говорят о гипокинетической дискинезии, а сокращение более чем на 2/3 расценивается, как гиперкинетическая дискинезия.
Рентгенологические методы позволяют судить о внешнесекреторной функции печени и концентрационной способности ЖП по срокам появления на снимках тени желчных протоков и ЖП после предварительного их контрастирования. Сократительная функция ЖП оценивается после назначения пищевых раздражителей.
Данные о двигательной функции ЖП, полученные при рентгенохолецистографии и ультразвуковой холецистографии практически идентичны, но поскольку УЗИ не требует использования контрастного вещества, не связано с лучевыми нагрузками, метод является более приемлемым для больного.
Радиоизотопное исследование печени и желчевыводящей системы позволяет детальнее изучить поглотительно–выделительную функцию печени, ее кровообращение и состояние желчевыводящих путей.
Гепатобилисцинтиграфия с радиофармпрепаратами на основе диметилиминодиацетовой кислоты, меченой 99mTc–HIDA, имеет безусловные преимущества в оценке анатомо–топографического и функционального состояния гепатобилиарной системы по сравнению с методом, при котором используется бенгальский розовый, меченый I131. Являясь фармакологическим аналогом билирубина, HIDA, как и билирубин, захватывается гепатоцитами и выделяется в желчные протоки, накапливается в ЖП и при стимуляции его сократительной функции поступает в двенадцатиперстную кишку. Достоинством современной методики является возможность не только визуальной, но и количественной оценки степени тяжести нарушений функций печени и ЖП.
Что касается многофракционного дуоденального зондирования, то в настоящее время преобладает мнение, что это исследование не способно верифицировать ни воспалительные, ни двигательные изменения в желчевыводящих путях. Обнаружение в дуоденальном содержимом лейкоцитов и слизи не имеет большого диагностического значения; на показатели кинетики дуоденального содержимого патология двенадцатиперстной кишки может оказывать более выраженное влияние, чем собственно билиарная патология. Кроме того, даже у здорового человека сама процедура зондирования (введение резиновой трубки и металлической оливы, окаймляющей зонд, в просвет желудка и двенадцатиперстной кишки) является достаточно травматичной и может быть причиной «физиологической» дискинезии сфинктеров как самой двенадцатиперстной кишки, так и билиарной системы с соответствующими нарушениями кинетики дуоденального содержимого. В связи с этим дуоденальное зондирование целесообразно проводить лишь по строгим показаниям, а именно – с целью ранней диагностики обменных нарушений, сопровождающихся появлением в желчи кристаллов биллирубината кальция и холестерина (при условии исследования дуоденального содержимого в первые минуты после его получения), а также для диагностики паразитов, прежде всего описторхоза. В настоящее время этот метод все реже применяется в повседневной клинической практике в связи с трудоемкостью и травматичностью исследования, появлением неинвазивных методов диагностики, а также из–за сложности интерпретации полученных данных.
Повсеместное использование метода ультразвуковой диагностики а гастроэнтерологии позволило не только выявлять «немое камненосительство», но и ввело во врачебный обиход понятие деформации, или дисформии ЖП, т.е. выявляемое прижизненно, безоперационно наличие перегибов и измененной конфигурации. Данные литературы о распространенности дисформии противоречивы. Обсуждается роль дисформии в развитии ДЖП, ХБХ и ЖКБ. Противоречия касаются не только распространенности, характера дисформий, их типов, локализации, механизмов возникновения и прогностического значения. Нарушения формы пузыря при ультразвуковом исследовании выявляют у 1/3 лиц, обратившихся в отделения гастроэнтерологии с различными жалобами. Весьма значимо, что у 88% пациентов с аномальным ЖП определены признаки дискинезии желчевыводящих путей. О роли дисформии в генезе функциональных нарушений свидетельствует наблюдение, что аномалии ЖП не сопровождались холециститом только у 13% лиц старше 25 лет.
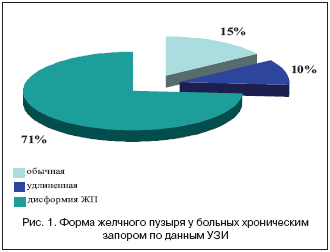
О распространенности дисформии ЖП в гастроэнтерологической практике свидетельствуют результаты нашего исследования с участием 119 больных с запорами (рис. 1). Как видно, у 96% УЗИ выявило преобладание пациентов с отклонениями от нормальной формы желчного пузыря.
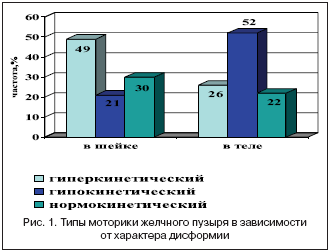
По данным (рис. 2) результатов ультразвуковой холецистографии у 119 больных показано, что при дисформии (перегибе) в шейке пузыря чаще возникает гиперкинетический вариант дискинезии, а изменения формы тела ЖП – гипокинетический вариант.
Различные изменения формы ЖП часто сочетаются с другими проявлениями синдрома дисплазии соединительной ткани желудочно–кишечного тракта – гепатозом, недостаточностью нижнего пищеводного сфинктера, грыжей пищеводного отверстия диафрагмы, долихосигмой, дивертикулезом толстой кишки, а также других органов и систем (пролапсом митрального клапана, гипермобильностью суставов и т.д.). Эти данные позволяют считать заслуживающим внимания мнение о врожденном характере деформаций желчного пузыря.
У здорового человека прием пищи и поступление ее в ДПК приводит к тому, что тонус мускулатуры ЖП повышается, нарастает давление в его полости, и он сокращается. Тонус сфинктера Одди снижается, происходит его расслабление, и желчь поступает в ДПК. В межпищеварительный период ЖП расслабляется и заполняется желчью из печеночных протоков, а тонус сфинктера Одди повышается, предотвращая беспрерывное истечение желчи в ДПК.
Главная роль в регулировании деятельности ЖП и сфинктера Одди принадлежит холецистокинину (ХЦК). Этот гастроинтестинальный гормон стимулирует сокращение желчного пузыря и расслабление сфинктера Одди. Важно, что слизистая оболочка ЖП вырабатывает антагонист ХЦК – гормон антихолецистокинин. Он сокращает действие ХЦК и наступающие в межпищеварительный период расслабление ЖП и повышение тонуса сфинктера Одди. Холецистэктомия приводит к тому, что продукция антихолецистокинина прекращается, в связи с чем ХЦК действует более длительно и в результате возникает дисфункция сфинктера Одди (с преобладанием его спазма).
Гипертонус Сфинктера Одди разделяют на 2 варианта: билиарную и панкреатическую дисфункции.
Несмотря на то, что дисфункциональные расстройства билиарного тракта носят функциональный характер, они имеют достаточно выраженные клинические проявления в виде болевого абдоминального и диспепсического синдромов и могут сопровождаться серьезными нарушениями функционирования организма. Так, моторная дисфункция желчных путей в связи с нарушением эмульгирования жиров и активации кишечных ферментов нередко приводит к расстройству процессов пищеварения. В результате накопления негидролизованных веществ активизируются процессы брожения и гниения с развитием синдрома избыточного бактериального роста. Нарушенный ритм поступления желчи в двенадцатиперстную кишку вследствие снижения санирующего действия желчи и расстройства местных регуляторных механизмов способствует развитию воспалительных и моторных изменений верхних отделов пищеварительного тракта. Нарушается также перистальтическая активность кишечника, вследствие чего возможно развитие и/или усугубление хронических запоров. Нарушение эвакуаторной функции ЖП может также сопровождаться развитием синдрома холестаза с изменением биохимического состава желчи и последующим формированием желчно–каменной болезни, воспалительных заболеваний желчных путей с вовлечением в патологический процесс паренхимы печени [17].
Диетические и лечебные рекомендации принципиально различаются для больных с различными типами дискинезии ЖП.
При гипокинетической дискинезии рекомендуют частое (4–5 раз в сутки) и дробное (небольшими порциями) питание, что способствует улучшению оттока желчи; очень полезны растительные жиры: подсолнечное, оливковое, кукурузное, соевое масло. Входящие в их состав полиненасыщенные жирные кислоты (арахидоновая, линолевая) способствуют нормализации обмена холестерина, участвуют в синтезе простагландинов, которые разжижают желчь и повышают сократительную способность желчного пузыря. Диета также должна содержать достаточное количество растительной клетчатки овощей и фруктов (яблоки, морковь, дыни, арбузы, помидоры и др.); можно рекомендовать пациентам прием мелких белых пшеничных отрубей, которые стимулируют отток желчи, уменьшают содержание в ней холестерина и тем самым снижают вероятность образования камней. Мелкие белые пшеничные отруби целесообразно принимать, начиная с 1 чайной ложки, запивая половиной стакана отвара ромашки (или кипяченой водой), 3 раза в сутки до еды; в дальнейшем постепенно доза может быть увеличена до 1 столовой ложки 2–3 раза в сутки. Среди лекарственных желчегонных средств принято выделять холеретики – препараты, стимулирующие образование печенью желчи, и холекинетики, которые повышают тонус и усиливают сократительную функцию желчного пузыря.
К холеретикам относят препараты, содержащие желчные кислоты, а также средства растительного происхождения, эффект которых обусловлен наличием в них эфирных масел, смол, флавонов и витаминов. Это отвар из цветков бессмертника, кукурузные рыльца, фламин – таблетированный препарат бессмертника, настой мяты перечной, отвар петрушки, шиповника. Препараты этой группы повышают секрецию желчи, увеличивают содержание в ней холатов, оказывают антибактериальное и противовоспалительное действие. Выделяют также гидрохолеретики (минеральные воды), которые увеличивают секрецию желчи за счет ее водного компонента. Эффект минеральных вод зависит от содержания сульфатных анионов, связанных с катионами натрия (желчегонное действие) и магния (холекинетический эффект). Время приема минеральных вод в зависимости от приема пищи обусловлено состоянием секреторной функции желудка: при сниженной секреторной функции – за 30 минут до еды, при повышенной – за 1,5 часа до еды.
Механизм действия холекинетиков связан с раздражением слизистой оболочки двенадцатиперстной кишки и выделением холецистокинина, который способствует сокращению желчного пузыря и расслаблению сфинктера Одди. К препаратам этой группы относят многоатомные спирты ксилит и сорбит, оказывающие, помимо холекинетического, холеретическое и послабляющее действие; магния сульфат, берберина сульфат, растительные масла. Целесообразно также назначение беззондовых тюбажей: например, два раза в неделю утром натощак съедать 2 яйца «в мешочек», приправленных столовой ложкой растительного масла, после чего лежать около получаса с грелкой на правом боку.
Все желчегонные средства назначаются 2–3 раза в сутки за 30 минут до еды. Перед их назначением необходимо исключить наличие у пациента ЖКБ, так как вместе с энергичным оттоком желчи возможно продвижение камней и их ущемление в шейке желчного пузыря или протоках.
Для нормализации моторных нарушений со стороны двенадцатиперстной кишки возможно назначение прокинетиков. При гиперкинетической дискинезии назначается диета с низким содержанием жира, исключением жареных, острых и кислых продуктов; используются спазмолитические препараты. При выраженном болевом синдроме одновременно назначаются ненаркотические анальгетики. Для снятия спазма гладкой мускулатуры традиционно используются нитраты (нитроглицерин для быстрого купирования боли, нитросорбид для курсового лечения), селективные М1–холиноблокаторы, блокаторы медленных кальциевых каналов, миотропные спазмолитики.
В ряду факторов, определяющих клиническую картину патологии билиарной системы, важное место отводится нарушению моторной функции желчного пузыря и сфинктерного аппарата. Стенка желчного пузыря способна к сокращению и растяжению, что обусловлено наличием в средней ее оболочке как гладкомышечных, так и эластических волокон. Возможно сокращение как всего органа, так и отдельных его частей.
Сокращение гладкой мускулатуры ЖКТ, в том числе и желчного пузыря, возникает при стимуляции ацетилхолином мускариновых рецепторов на поверхности мышечной клетки. Это ведет к открытию натриевых каналов и входу Na+ в клетку. Возникшая деполяризация клетки далее способствует открытию кальциевых каналов и входу Са2+ в клетку. Высокий внутриклеточный уровень Са2+ благоприятствует фосфорилированию миозина и, соответственно, сокращению мышцы, длительное сокращение ведет к возникновению мышечного спазма, что и является одним из важнейших факторов боли. В свою очередь, симпатические импульсы содействуют выходу К+ из клетки и Са2+ из кальциевого депо, закрытию кальциевых каналов и расслаблению мышцы. Известно, что в регуляции транспорта ионов Са2+ участвуют такие нейрогенные медиаторы, как ацетилхолин, катехоламины (норадреналин), серотонин, холецистокинин, мотилин и другие [8].
При сохраненной сократительной функции ЖП и сфинктерного аппарата при их координированной деятельности происходит своевременная эвакуация желчи. Нарушение моторики желчного пузыря и/или сфинктерного аппарата (например, спазм сфинктера Одди) приводит к нарушению опорожнения пузыря, повышению давления в желчевыводящих путях [7].
Опорожнение ЖП затрудняется при повышении внутрибрюшного давления, метеоризме, беременности, а также при снижении чувствительности или уменьшении количества рецепторов к холецистокинину, мотилину и другим стимуляторам мышечного сокращения. Снижается чувствительность рецепторного аппарата желчного пузыря желчного пузыря к различным стимуляторам, в том числе к холецистокинину в пожилом и старческом возрасте.
Особую роль в дискинезии ЖП играет нарушение моторики гладкомышечного аппарата сфинктера Одди.
Разнообразны проявления сложной анатомической структуры сфинктерного аппарата, состоящего из сфинктера общего желчного протока, сфинктера панкреатического протока и сфинктера их общей ампулы, которая открывается в 12–перстную кишку. При спазме преимущественно сфинктера холедоха развиваются патофизиологические, патоморфологические последствия и клинические проявления дисфункции сфинктера Одди – по билиарному типу, при спазме панкреатического сфинктера – по панкреатическому, а при спазме сфинктера в целом или только ампулярной его части имеет место смешанный тип дисфункции сфинктера Одди.
Нередко смешанный тип развивается после холецистэктомии, особенно в ранние сроки после удаления пузыря.
Спазм сфинктера Одди может возникнуть и при сохраненном желчном пузыре. При этом нарушается координация сокращения желчного пузыря и сфинктера большого дуоденального сосочка (как в межпищеварительном периоде, так и после приема пищи).
Стойкий спазм сфинктера Одди вызывает нарушение оттока желчи из желчного пузыря, что приводит к его переполнению и перерастяжению, повышению давления в его полости и в протоках, что вызывает появление болей. Частота спастической дисфункции в популяции неизвестна, но по данным манометрии у больных идиопатическим панкреатитом частота нарушений сфинктера Одди колеблется в пределах 39–90%.
При дисфункции любого типа необходимо эффективно устранить спазм, что позволит восстановить отток желчи, снизить протоковое и пузырное давление, уменьшить боль и предотвратить развитие осложнений.
Поскольку тонус и сократительная активность гладких мышц желудочно–кишечного тракта находится под контролем центральной и вегетативной нервной системы, а также нейрогуморальной регуляции, то теоретически нормализация моторики и устранение спазма могут быть достигнуты при воздействии на любом из указанных уровней. Однако подобная коррекция пока труднодостижима, так как средства для ее проведения находятся на разных стадиях клинических испытаний. Практически купирование гладкомышечного спазма возможно только на периферическом уровне при воздействии непосредственно на конечный этап мышечного сокращения.
Таким образом, принимая во внимание тот факт, что в формировании клинической картины дискинезии желчевыводящих путей важную роль играет чрезмерное сокращение гладкой мускулатуры стенки ЖП и сфинктерного аппарата, становится очевидной целесообразность применения антиспастических средств.
Предпочтение отдается миотропным спазмолитикам. М–холиноблокаторы не только расслабляют мышцы пищеварительного тракта, но и оказывают системное холинолитическое действие, вызывая нежелательные реакции. Спазмолитики прямого действия (папаверин, дротаверин) также универсально влияют на все ткани, где присутствуют гладкие мышцы. Поэтому при лечении пациентов с функциональной абдоминальной болью предпочтение отдается миотропным спазмолитикам с селективным действием (мебеверин, пинаверия бромид, отилония бромид). Ранее обращалось внимание на то, что антагонисты кальция, используемые для лечения сердечно–сосудистых заболеваний (нифедипин и верапамил), оказывали релаксирующее влияние на гладкие мышцы ЖКТ. Это послужило поводом для создания группы современных эффективных миотропных спазмолитиков — селективных блокаторов кальциевых каналов гладких мышц ЖКТ.
Классическим представителем этой группы является пинаверия бромид.
В настоящее время благодаря результатам электрофизиологических и фармакологических исследований идентифицировано, по крайней мере, 4 типа кальциевых каналов: L, T, P, N. Каналы L–типа находятся на поверхности цитоплазматической мембраны гладкомышечных клеток и состоят из нескольких субъединиц, из которых наиболее важной является 1 субъединица, которая может открываться за счет разности потенциалов на поверхности клеточной мембраны (нейрональный контроль) или опосредованно в присутствии пищеварительных гормонов и медиаторов. В многочисленных экспериментах in vitro и in vivo было продемонстрировано, что пинаверия бромид снижает сократимость изолированных гладкомышечных клеток путем избирательного ингибирования изоформы 1–субъединицы кальциевого канала L–типа преимущественно. Купирование боли при использовании препарата связано также с уменьшением висцеральной гиперчувствительности. Препарат блокирует не только кальциевые каналы миоцитов, но и кальциевые каналы рецепторов, отвечающих за чувствительность [3–6].
Пинаверия бромид является антагонистом кальция с высокоселективным спазмолитическим действием в отношении гладких мышц кишечника. Это определяет его терапевтическое применение при боли в животе, кишечной дисфункции и кишечном дискомфорте [3].
Высокая антиангинальная эффективность пинаверия бромида, миотропного спазмолитика со свойствами антагониста кальция, объясняется тем, что развитие мышечного спазма зависит напрямую от внутриклеточной концентрации ионов Са. Ионы Са поступают в гладкую мышечную клетку через кальциевые каналы, располагающиеся на клеточной мембране миоцита. Блокировка указанных каналов приводит к снижению внутриклеточной концентрации Са и купированию мышечного спазма. Кроме того, у препарата имеется и второй механизм купирования боли — за счет уменьшения висцеральной гиперчувствительности, приводящей к спазмофилии. Снижение чувствительности слизистой на фоне приема пинаверия бромида связано с тем, что препарат, как и кальциевые каналы миоцитов, блокирует и кальциевые каналы рецепторов, расположенных в слизистой.
В отличие от многих спазмолитических препаратов пинаверия бромид не обладает антихолинергической активностью при использовании в терапевтических дозах, а следовательно, при лечении этим препаратом маловероятно развитие связанных с этим действием побочных эффектов, способных нарушать дневную активность пациента, включая способность к управлению транспортными средствами. Сообщалось, что пинаверия бромид лишен влияния на параметры сердечно–сосудистой системы. Никаких влияний препарата на биохимические и гематологические показатели также отмечено не было [13].
Пинаверия бромид в остром периоде (3–6 дней) назначается по 100 мг 3–4 раза в сутки во время еды. После стихания обострения поддерживающей дозировкой препарата является стандартная доза – 100 мг 2 раза в сутки (или 50 мг 3–4 раза в сутки). Продолжительность курсового лечения – от 2 до 6 недель и более. Пинаверия бромид не имеет побочных антихолинергических эффектов, поэтому его можно без опасений назначать пациентам с глаукомой и гипертрофией предстательной железы.
Литература
1. Drossman D.A. The functional gastrointestinal disorders and the Rome II process. Gut 1999;45(Suppl. ll):1–5.
2. Corazzisri E., Shoffer E.A., Hogan W J et al. №2 «Functional Desorders of the Biliary Tract and the Pancreas». Rome II the functional Gastrointestinal Desorders Diagnosis.Patho physiology and Treatment, Second Edition, 1999, p. 433–481
3. Белоусова Е.А. Спазмолитики в гастроэнтерологии: сравнительная характеристика и показания к применению // фарматека. 2002. № 9. С. 40–6.
4. Gershon M.D. Review article: roles played 5–hydroxytryptamine in the physiology of the bowel. Aliment Pharmacol Ther 1999;13(Suppl. 2):15–30.
5. McCallum R.W., Radke R, SmoutA, etal. Calcium antagonism & Gastrointestinal motility Experta medica 1989:48.
6. Wood I.D., Alpers D.H., Andrews PL.R. Fundamentals of neurogastroenterology. Gut 1999;45(Suppl. 10:6–16.
7. Costa M., Simon J.H. The Enteric Nervous System. AmJGastroenterol 1994:89(8): 129–37.
8. Волынец Г.В. Дисфункции билиарного тракта у детей. Дет. Гастроэнтерология 2005; 267–13.
9. Ивашкин В.Т., Лапина Т.Л. Рациональная фармакотерапия заболеваний органов пищеварения 2003; 183–187.
10. ВГерок В. Блюм Е.Х.. Заболевания печени и желчевыделительной системы. М., «МЕДпресс–информ» 2009. 199 с.
11. Минушкин О.Н. Билиарная дисфункция: определение, классификация, диагностика, лечение. Леч.врач. 2011.
12. Калинин А.В. Функциональные расстройства билиарного тракта и их лечение//Клинические перспективы гастроэнтерологии, гепатологии. — 2002. — № 3. — С. 25–34.
13. Drossman D.A., Corazziari Е. and the Working Team for Functional Disorders of the Biliary Tract (1994)
14. Агафонова Н.А. Спазмолитическая терапия у больных с синдромом раздраженного кишечника. Медицинский вестник № 27, 2010.
15. Ильченко А.А. «Дисфункциональные расстройства билиарного тракта». Consilium medicum, №1, 2002
16. Яковенко Э.П., Григорьев П.Я. «Хронические заболевания внепеченочных желчевыводящих путей. Диагностика и лечение» (методическое пособие для врачей, 2000).
17. Волынец Г.В. Дисфункции билиарного тракта у детей. Дет гастроэнтерол 2005; 2: 7–13.












