–С–Њ–ї—М—И–∞—П —З–∞—Б—В—М –±–Є—Д–Є–і–Њ–±–∞–Ї—В–µ—А–Є–є –ї–Њ–Ї–∞–ї–Є–Ј—Г–µ—В—Б—П –≤ —В–Њ–ї—Б—В–Њ–є –Ї–Є—И–Ї–µ, —Б–Њ—Б—В–∞–≤–ї—П—П –Њ—Б–љ–Њ–≤–љ—Г—О (–њ—А–µ–ґ–і–µ –≤—Б–µ–≥–Њ –њ—А–Є—Б—В–µ–љ–Њ—З–љ—Г—О) –Є –њ—А–Њ—Б–≤–µ—В–љ—Г—О –Љ–Є–Ї—А–Њ—Д–ї–Њ—А—Г. –Т –љ–Њ—А–Љ–µ –Ї–Њ–ї–Є—З–µ—Б—В–≤–Њ –±–Є—Д–Є–і–Њ–±–∞–Ї—В–µ—А–Є–є –≤ –Ј–∞–≤–Є—Б–Є–Љ–Њ—Б—В–Є –Њ—В –≤–Њ–Ј—А–∞—Б—В–∞ –і–µ—В–µ–є –і–Њ—Б—В–Є–≥–∞–µ—В 109–1010 –Ъ–Ю–Х/–≥ —Д–µ–Ї–∞–ї–Є–є. –Т –Њ–±—Й–µ–Љ —Б–Њ–і–µ—А–ґ–∞–љ–Є–Є –±–∞–Ї—В–µ—А–Є–є —Г–і–µ–ї—М–љ—Л–є –≤–µ—Б —Н–љ—В–µ—А–Њ–Ї–Њ–Ї–Ї–Њ–≤ –Љ–µ–љ—М—И–µ, —З–µ–Љ —Н—И–µ—А–Є—Е–Є–є (–Ю–Ъ–Ъ–Я), –Є —Б–Њ—Б—В–∞–≤–ї—П–µ—В –≤ –љ–Њ—А–Љ–µ 105–107 –Ъ–Ю–Х/–≥ —Д–µ–Ї–∞–ї–Є–є. –Я—А–Є —Д–µ—А–Љ–µ–љ—В–∞—Ж–Є–Є —Н–љ—В–µ—А–Њ–Ї–Њ–Ї–Ї–∞–Љ–Є —Г–≥–ї–µ–≤–Њ–і–Њ–≤ –Њ–±—А–∞–Ј—Г–µ—В—Б—П –Љ–Њ–ї–Њ—З–љ–∞—П –Ї–Є—Б–ї–Њ—В–∞, —Б–љ–Є–ґ–∞—О—Й–∞—П —А–Э –і–Њ 4,2–4,6 [1,2].
–Э–∞ —Б–µ–≥–Њ–і–љ—П—И–љ–Є–є –і–µ–љ—М –±–ї–∞–≥–Њ–њ—А–Є—П—В–љ–Њ–µ –≤–Њ–Ј–і–µ–є—Б—В–≤–Є–µ –Є –±–µ–Ј–≤—А–µ–і–љ–Њ—Б—В—М –њ—А–Њ–±–Є–Њ—В–Є—З–µ—Б–Ї–Є—Е —И—В–∞–Љ–Љ–Њ–≤ B. longum, –Є—Б–њ–Њ–ї—М–Ј—Г–µ–Љ—Л—Е –Ї–∞–Ї –і–ї—П –Є–Ј–≥–Њ—В–Њ–≤–ї–µ–љ–Є—П –њ–Є—Й–µ–≤—Л—Е –њ—А–Њ–і—Г–Ї—В–Њ–≤, —В–∞–Ї –Є –њ—А–µ–њ–∞—А–∞—В–Њ–≤––њ—А–Њ–±–Є–Њ—В–Є–Ї–Њ–≤, –њ–Њ–і—В–≤–µ—А–ґ–і–µ–љ–Њ —Г—Б–њ–µ—И–љ—Л–Љ —Н–Ї—Б–њ–µ—А–Є–Љ–µ–љ—В–∞–ї—М–љ—Л–Љ –Њ–±–Њ—Б–љ–Њ–≤–∞–љ–Є–µ–Љ –Є –Љ–љ–Њ–≥–Њ–ї–µ—В–љ–Є–Љ–Є —Н—Д—Д–µ–Ї—В–Є–≤–љ—Л–Љ–Є –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є–Љ–Є –Є—Б–њ—Л—В–∞–љ–Є—П–Љ–Є –Є –љ–µ –≤—Л–Ј—Л–≤–∞–µ—В —Б–Њ–Љ–љ–µ–љ–Є–є. –Ъ –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є—О —Н–љ—В–µ—А–Њ–Ї–Њ–Ї–Ї–Њ–≤ –і–ї—П –Є–Ј–≥–Њ—В–Њ–≤–ї–µ–љ–Є—П –њ—А–Њ–±–Є–Њ—В–Є–Ї–Њ–≤ –±–Њ–ї–µ–µ –Њ—Б—В–Њ—А–Њ–ґ–љ–Њ–µ –Њ—В–љ–Њ—И–µ–љ–Є–µ, —Е–Њ—В—П –Ї –љ–∞—Б—В–Њ—П—Й–µ–Љ—Г –≤—А–µ–Љ–µ–љ–Є –љ–∞–Ї–Њ–њ–ї–µ–љ –њ–Њ–ї–Њ–ґ–Є—В–µ–ї—М–љ—Л–є –Њ–њ—Л—В –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є—П —И—В–∞–Љ–Љ–∞ Enterococcus faecium SF 68 (–њ—А–µ–њ–∞—А–∞—В—Л –С–Є—Д–Є—Д–Њ—А–Љ, –Ы–Є–љ–љ–µ–Ї—Б, –С–Є–Њ—Д–ї–Њ—А–Є–љ). –Т —Б–Њ—Б—В–∞–≤–µ —Г–Ї–∞–Ј–∞–љ–љ—Л—Е –њ—А–Њ–±–Є–Њ—В–Є–Ї–Њ–≤ (–Ј–∞—А–µ–≥–Є—Б—В—А–Є—А–Њ–≤–∞–љ–љ—Л—Е –≤ –†–Њ—Б—Б–Є–Є –Є –Ч–∞–њ–∞–і–љ–Њ–є –Х–≤—А–Њ–њ–µ) –њ—А–Є–Љ–µ–љ—П—О—В —И—В–∞–Љ–Љ, –≤—Л–і–µ–ї–µ–љ–љ—Л–є –Є –Ј–∞–њ–∞—В–µ–љ—В–Њ–≤–∞–љ–љ—Л–є S.A. Giuliani (–њ–∞—В–µ–љ—В вДЦ 1.112.479). –Т –њ–Њ–ї—М–Ј—Г –њ–Њ–ї–Њ–ґ–Є—В–µ–ї—М–љ–Њ–є —А–µ–Ї–Њ–Љ–µ–љ–і–∞—Ж–Є–Є –і–ї—П –њ—А–Є–Љ–µ–љ–µ–љ–Є—П —И—В–∞–Љ–Љ–∞ Enterococcus faecium SF 68 —Б–ї—Г–ґ–∞—В –і–∞–љ–љ—Л–µ –Њ–± –Њ—В—Б—Г—В—Б—В–≤–Є–Є «–Њ—Б—В—А–Њ–≤–Ї–Њ–≤ –њ–∞—В–Њ–≥–µ–љ–љ–Њ—Б—В–Є» – –Љ–∞—А–Ї–µ—А–Њ–≤ –≤–Є—А—Г–ї–µ–љ—В–љ–Њ—Б—В–Є –≤ –≥–µ–љ–Њ–Љ–µ –±–∞–Ї—В–µ—А–Є–є –њ—А–Є –њ–Њ—Б—В–∞–љ–Њ–≤–Ї–µ –Я–¶–† [3,4].
–Ь–Є–Ї—А–Њ–±–Є–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є–µ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П E. faecium (Streptococcus faecium) –њ–Њ–Ї–∞–Ј–∞–ї–Є, —З—В–Њ –Њ–љ –љ–µ –Є–Љ–µ–µ—В –≥–µ–Љ–Њ–ї–Є—В–Є—З–µ—Б–Ї–Є—Е —Б–≤–Њ–є—Б—В–≤ –Є –љ–µ –њ—А–Њ–Є–Ј–≤–Њ–і–Є—В –і–µ–Ї—Б—В—А–∞–љ. –Я—А–Є –Є–љ—В—А–∞–њ–µ—А–Є—В–Њ–љ–µ–∞–ї—М–љ–Њ–Љ –Ј–∞—А–∞–ґ–µ–љ–Є–Є –Љ—Л—И–µ–є —Д–Є–ї—М—В—А–∞—В–Њ–Љ –Ї—Г–ї—М—В—Г—А–∞–ї—М–љ–Њ–є —Б—А–µ–і—Л E. faecium, –∞ —В–∞–Ї–ґ–µ –љ–µ–Њ—З–Є—Й–µ–љ–љ—Л–Љ –ї–Є–Ј–∞—В–Њ–Љ —Б–∞–Љ–Є—Е –±–∞–Ї—В–µ—А–Є–є –ґ–Є–≤–Њ—В–љ—Л–µ –љ–µ –њ–Њ–≥–Є–±–∞–ї–Є. –Ц–Є–Ј–љ–µ—Б–њ–Њ—Б–Њ–±–љ–Њ—Б—В—М –Љ—Л—И–µ–є —Б–Њ—Е—А–∞–љ—П–ї–∞—Б—М –Є –њ—А–Є –њ–µ—А–Њ—А–∞–ї—М–љ–Њ–Љ –Ј–∞—А–∞–ґ–µ–љ–Є–Є –Љ—Л—И–µ–є –Ї—Г–ї—М—В—Г—А–Њ–є E. faecium, –∞ –Љ–Њ—А—Д–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є–µ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П —Б–≤–Є–і–µ—В–µ–ї—М—Б—В–≤–Њ–≤–∞–ї–Є –Њ–± –Њ—В—Б—Г—В—Б—В–≤–Є–Є –њ–∞—В–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є—Е –Є–Ј–Љ–µ–љ–µ–љ–Є–є –≤ –Њ—А–≥–∞–љ–∞—Е. –Р–љ–∞–ї–Њ–≥–Є—З–љ—Л–µ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П –њ–Њ–і—В–≤–µ—А–і–Є–ї–Є –Њ—В—Б—Г—В—Б—В–≤–Є–µ —В–Њ–Ї—Б–Є—З–љ–Њ—Б—В–Є –љ–∞ –њ–Њ—А–Њ—Б—П—В–∞—Е––≥–љ–Њ—В–Њ–±–Є–Њ–љ—В–∞—Е. –Ф–ї–Є—В–µ–ї—М–љ–Њ–µ –њ—А–Є–Љ–µ–љ–µ–љ–Є–µ –љ–µ –≤—Л—П–≤–Є–ї–Њ –љ–µ–ґ–µ–ї–∞—В–µ–ї—М–љ—Л—Е –њ–Њ—Б–ї–µ–і—Б—В–≤–Є–є. –Я—А–Њ–≤–µ–і–µ–љ–љ—Л–є –њ–Њ —Б–Њ–≤—А–µ–Љ–µ–љ–љ—Л–Љ –Ї—А–Є—В–µ—А–Є—П–Љ –Ї–Њ–Љ–њ–ї–µ–Ї—Б –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–є –љ–µ –Њ–±–љ–∞—А—Г–ґ–Є–ї –Ї–∞–љ—Ж–µ—А–Њ–≥–µ–љ–љ–Њ–≥–Њ –Є –Љ—Г—В–∞–≥–µ–љ–љ–Њ–≥–Њ –њ–Њ—В–µ–љ—Ж–Є–∞–ї–∞ –Ї–∞–Ї B. longum, —В–∞–Ї –Є E. faecium.
–Э–∞ –њ–Њ—А–Њ—Б—П—В–∞—Е––≥–љ–Њ—В–Њ–±–Є–Њ–љ—В–∞—Е, –∞ –Ј–∞—В–µ–Љ –Є —Г –Ј–і–Њ—А–Њ–≤—Л—Е –і–Њ–±—А–Њ–≤–Њ–ї—М—Ж–µ–≤ –±—Л–ї–Њ –њ–Њ–Ї–∞–Ј–∞–љ–Њ, —З—В–Њ –≤–≤–µ–і–µ–љ–Є–µ B. longum –Є E. faecium –њ—А–Є–≤–Њ–і–Є—В –Ї —В—А–∞–љ–Ј–Є—В–Њ—А–љ–Њ–є –Ї–Њ–ї–Њ–љ–Є–Ј–∞—Ж–Є–Є –Ї–Є—И–µ—З–љ–Є–Ї–∞ —Н—В–Є–Љ–Є –Љ–Є–Ї—А–Њ–±–∞–Љ–Є (–≤–Њ–Ј—А–∞—Б—В–∞–ї–∞ —З–Є—Б–ї–µ–љ–љ–Њ—Б—В—М). –Я–µ—А—Б–Є—Б—В–µ–љ—Ж–Є—П –Љ–Є–Ї—А–Њ–Њ—А–≥–∞–љ–Є–Ј–Љ–Њ–≤ —Б–Њ—Е—А–∞–љ—П–ї–∞—Б—М –≤ —В–µ—З–µ–љ–Є–µ 7 –і–љ–µ–є [3,4].
–Я—А–µ–і—И–µ—Б—В–≤—Г—О—Й–Є–µ –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є–µ –Є—Б–њ—Л—В–∞–љ–Є—П –њ–Њ –Њ—Ж–µ–љ–Ї–µ —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В–Є –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є—П –њ—А–Њ–±–Є–Њ—В–Є–Ї–Њ–≤, —Б–Њ–і–µ—А–ґ–∞—Й–Є—Е —Г–Ї–∞–Ј–∞–љ–љ—Л–µ –≤–Є–і—Л –±–∞–Ї—В–µ—А–Є–є, —Г –≤–Ј—А–Њ—Б–ї—Л—Е –Є –і–µ—В–µ–є —Б –і–≤—Г—Е–ї–µ—В–љ–µ–≥–Њ –≤–Њ–Ј—А–∞—Б—В–∞ —В–∞–Ї–ґ–µ –±—Л–ї–Є —Г—Б–њ–µ—И–љ—Л–Љ–Є: –Ї–∞–Ї–Є—Е––ї–Є–±–Њ –њ–Њ–±–Њ—З–љ—Л—Е —Н—Д—Д–µ–Ї—В–Њ–≤ –∞–≤—В–Њ—А—Л –љ–µ –љ–∞–±–ї—О–і–∞–ї–Є [5–8].
–Я—А–Є –љ–∞–Ј–љ–∞—З–µ–љ–Є–Є –њ—А–Њ–±–Є–Њ—В–Є–Ї–Њ–≤ —Б–ї–µ–і—Г–µ—В —Г—З–Є—В—Л–≤–∞—В—М, —З—В–Њ —Б—А–Њ–Ї–Є –≤—Л–ґ–Є–≤–∞–љ–Є—П –њ—А–Њ–±–Є–Њ—В–Є—З–µ—Б–Ї–Є—Е –Ї—Г–ї—М—В—Г—А –≤ –ґ–µ–ї—Г–і–Њ—З–љ–Њ––Ї–Є—И–µ—З–љ–Њ–Љ —В—А–∞–Ї—В–µ –Ј–∞–≤–Є—Б—П—В –Њ—В –Њ—Б–Њ–±–µ–љ–љ–Њ—Б—В–µ–є —Б–µ–ї–µ–Ї—Ж–Є–Є —И—В–∞–Љ–Љ–Њ–≤, —Б–Њ—Б—В–∞–≤–ї—П—О—Й–Є—Е –њ—А–µ–њ–∞—А–∞—В, –Є –µ–≥–Њ –ї–µ–Ї–∞—А—Б—В–≤–µ–љ–љ–Њ–є —Д–Њ—А–Љ—Л. –Т–∞–ґ–љ–Њ —Б–Њ—Е—А–∞–љ–µ–љ–Є–µ –ґ–Є–Ј–љ–µ—Б–њ–Њ—Б–Њ–±–љ–Њ—Б—В–Є –±–∞–Ї—В–µ—А–Є–є –њ—А–Є –≤–Њ–Ј–і–µ–є—Б—В–≤–Є–Є –љ–Є–Ј–Ї–Њ–≥–Њ —А–Э –Є –ґ–µ–ї—З–Є. –Ъ–∞–њ—Б—Г–ї—Л, —Г—Б—В–Њ–є—З–Є–≤—Л–µ –Ї –і–µ–є—Б—В–≤–Є—О –Ї–Є—Б–ї–Њ–є —Б—А–µ–і—Л –ґ–µ–ї—Г–і–Њ—З–љ–Њ–≥–Њ –Є –Ї–Є—И–µ—З–љ–Њ–≥–Њ —Б–Њ–Ї–∞, –Њ–±–µ—Б–њ–µ—З–Є–≤–∞—О—В –ї—Г—З—И–µ–µ –≤—Л–ґ–Є–≤–∞–љ–Є–µ –≤–≤–Њ–і–Є–Љ—Л—Е –Ї—Г–ї—М—В—Г—А.
–¶–µ–ї—М –љ–∞—Б—В–Њ—П—Й–µ–≥–Њ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П – –Є–Ј—Г—З–µ–љ–Є–µ –Ї–ї–Є–љ–Є–Ї–Њ––ї–∞–±–Њ—А–∞—В–Њ—А–љ–Њ–є —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В–Є –њ—А–µ–њ–∞—А–∞—В–∞ –С–Є—Д–Є—Д–Њ—А–Љ –≤ –Ї–∞—З–µ—Б—В–≤–µ –µ–і–Є–љ—Б—В–≤–µ–љ–љ–Њ–≥–Њ —Б—А–µ–і—Б—В–≤–∞ —Н—В–Є–Њ–њ–∞—В–Њ–≥–µ–љ–µ—В–Є—З–µ—Б–Ї–Њ–≥–Њ –ї–µ—З–µ–љ–Є—П —Г –і–µ—В–µ–є —Б 2 –і–Њ 7 –ї–µ—В, –±–Њ–ї—М–љ—Л—Е –Њ—Б—В—А—Л–Љ–Є –Ї–Є—И–µ—З–љ—Л–Љ–Є –Є–љ—Д–µ–Ї—Ж–Є—П–Љ–Є (–Ю–Ъ–Ш).
–Я—А–µ–њ–∞—А–∞—В –С–Є—Д–Є—Д–Њ—А–Љ (—Д–∞—А–Љ–∞—Ж–µ–≤—В–Є—З–µ—Б–Ї–∞—П –Ї–Њ–Љ–њ–∞–љ–Є—П «–§–µ—А—А–Њ—Б–∞–љ –Ш–љ—В–µ—А–љ–µ–є—И–µ–љ–ї –Р/–°», –Ф–∞–љ–Є—П) –≤—Л–њ—Г—Б–Ї–∞–µ—В—Б—П –≤ –≤–Є–і–µ –Ї–∞–њ—Б—Г–ї —Б –Ј–∞—Й–Є—В–љ—Л–Љ –Ї–Є—Б–ї–Њ—В–Њ—Г—Б—В–Њ–є—З–Є–≤—Л–Љ –њ–Њ–Ї—А—Л—В–Є–µ–Љ. –Т –Њ–і–љ–Њ–є –Ї–∞–њ—Б—Г–ї–µ —Б–Њ–і–µ—А–ґ–Є—В—Б—П –±–Є–Њ–Љ–∞—Б—Б–∞ Bifidobacterium longum –љ–µ –Љ–µ–љ–µ–µ 107 –Ъ–Ю–Х/–Љ–ї –Є Enterococcus faecium –љ–µ –Љ–µ–љ–µ–µ 107 –Ъ–Ю–Х –≤ 1 –Љ–ї. –Т –Ї–∞—З–µ—Б—В–≤–µ –њ–Є—В–∞—В–µ–ї—М–љ–Њ–є —Б—А–µ–і—Л –Є—Б–њ–Њ–ї—М–Ј—Г–µ—В—Б—П –ї–∞–Ї—В—Г–ї–Њ–Ј–∞, –≥–ї—О–Ї–Њ–Ј–∞, –і—А–Њ–ґ–ґ–µ–≤–Њ–є —Н–Ї—Б—В—А–∞–Ї—В, –Ї–∞–Љ–µ–і—М. –Я—А–µ–њ–∞—А–∞—В –С–Є—Д–Є—Д–Њ—А–Љ –љ–µ —Б–Њ–і–µ—А–ґ–Є—В –ї–∞–Ї—В–Њ–Ј—Л.
–Я–Њ–і –љ–∞–±–ї—О–і–µ–љ–Є–µ–Љ –љ–∞—Е–Њ–і–Є–ї–Є—Б—М –і–≤–µ –≥—А—Г–њ–њ—Л –±–Њ–ї—М–љ—Л—Е –Ю–Ъ–Ш: 1 – –Њ—Б–љ–Њ–≤–љ–∞—П –Є–Ј 20 –і–µ—В–µ–є, –≤ –ї–µ—З–µ–љ–Є–µ –Ї–Њ—В–Њ—А—Л—Е –±—Л–ї –≤–Ї–ї—О—З–µ–љ –њ—А–Њ–±–Є–Њ—В–Є–Ї –С–Є—Д–Є—Д–Њ—А–Љ, –Є 2 – —Б—А–∞–≤–љ–µ–љ–Є—П –Є–Ј 10 –і–µ—В–µ–є, –µ–≥–Њ –љ–µ –њ–Њ–ї—Г—З–∞–≤—И–Є—Е. –Я—А–µ–њ–∞—А–∞—В –С–Є—Д–Є—Д–Њ—А–Љ –љ–∞–Ј–љ–∞—З–∞–ї—Б—П –њ–Њ 1 –Ї–∞–њ—Б—Г–ї–µ —В—А–Є —А–∞–Ј–∞ –≤ –і–µ–љ—М –≤ —В–µ—З–µ–љ–Є–µ 5–7 –і–љ–µ–є. –Т –ї–µ—З–µ–љ–Є–Є –±–Њ–ї—М–љ—Л—Е –Њ—Б–љ–Њ–≤–љ–Њ–є –≥—А—Г–њ–њ—Л –∞–љ—В–Є–±–∞–Ї—В–µ—А–Є–∞–ї—М–љ—Л–µ —Б—А–µ–і—Б—В–≤–∞ –љ–µ –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–ї–Є—Б—М.
–Ю–±–µ –≥—А—Г–њ–њ—Л –±–Њ–ї—М–љ—Л—Е –љ–∞–±–ї—О–і–∞–ї–Є—Б—М –≤ –Њ–і–Є–љ –Є —В–Њ—В –ґ–µ –њ–µ—А–Є–Њ–і –≤—А–µ–Љ–µ–љ–Є (—Д–µ–≤—А–∞–ї—М––Љ–∞–є 2006 –≥.), –њ–Њ–ї—Г—З–∞–ї–Є –Њ–±—Й–µ–њ—А–Є–љ—П—В—Г—О —В–µ—А–∞–њ–Є—О (–і–Є–µ—В–Є—З–µ—Б–Ї–Њ–µ –њ–Є—В–∞–љ–Є–µ, —А–µ–≥–Є–і—А–∞—В–∞—Ж–Є—О –Њ—А–∞–ї—М–љ—Г—О –Є–ї–Є –Є–љ—Д—Г–Ј–Є–Њ–љ–љ—Г—О –њ–Њ –њ–Њ–Ї–∞–Ј–∞–љ–Є—П–Љ, —Б–Є–Љ–њ—В–Њ–Љ–∞—В–Є—З–µ—Б–Ї–Є–µ —Б—А–µ–і—Б—В–≤–∞).
–Т –≥—А—Г–њ–њ–µ –і–µ—В–µ–є, –њ–Њ–ї—Г—З–∞–≤—И–Є—Е –њ—А–µ–њ–∞—А–∞—В –С–Є—Д–Є—Д–Њ—А–Љ, —З–∞—Б—В–Њ—В–∞ –Њ—В—П–≥–Њ—Й–µ–љ–љ–Њ—Б—В–Є –њ—А–µ–Љ–Њ—А–±–Є–і–љ–Њ–≥–Њ —Б–Њ—Б—В–Њ—П–љ–Є—П —Б–Њ—Б—В–∞–≤–Є–ї–∞ 80,0%, –љ–µ—Б–Љ–Њ—В—А—П –љ–∞ —Б–ї—Г—З–∞–є–љ—Л–є —Е–∞—А–∞–Ї—В–µ—А –≤—Л–±–Њ—А–Ї–Є. –Ґ–Њ–ї—М–Ї–Њ —Г 4 –і–µ—В–µ–є –≤ –∞–љ–∞–Љ–љ–µ–Ј–µ –Њ—В—Б—Г—В—Б—В–≤–Њ–≤–∞–ї–Є –Ї–∞–Ї–Є–µ––ї–Є–±–Њ –Њ—В—П–≥–Њ—Й–∞—О—Й–Є–µ —Д–∞–Ї—В–Њ—А—Л. –£ –њ–Њ–ї–Њ–≤–Є–љ—Л –њ–∞—Ж–Є–µ–љ—В–Њ–≤ (50%) —А–µ–≥–Є—Б—В—А–Є—А–Њ–≤–∞–ї–Њ—Б—М 2 –Є –±–Њ–ї–µ–µ –Њ—В—П–≥–Њ—Й–∞—О—Й–Є—Е —Д–∞–Ї—В–Њ—А–Њ–≤. –І–∞—Й–µ –≤—Б–µ–≥–Њ –≤—Б—В—А–µ—З–∞–ї–Є—Б—М –њ–Є—Й–µ–≤–∞—П –Є/–Є–ї–Є –ї–µ–Ї–∞—А—Б—В–≤–µ–љ–љ–∞—П –∞–ї–ї–µ—А–≥–Є—П – 10 (50%), —А–µ–ґ–µ – –Љ–∞–ї—Л–µ –∞–љ–Њ–Љ–∞–ї–Є–Є —А–∞–Ј–≤–Є—В–Є—П —Б–µ—А–і—Ж–∞ – 4 (20%), —Е—А–Њ–љ–Є—З–µ—Б–Ї–∞—П –≥–∞—Б—В—А–Њ—Н–љ—В–µ—А–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–∞—П –њ–∞—В–Њ–ї–Њ–≥–Є—П – 3 (15%), —Е—А–Њ–љ–Є—З–µ—Б–Ї–∞—П –њ–∞—В–Њ–ї–Њ–≥–Є—П –Ы–Ю–†––Њ—А–≥–∞–љ–Њ–≤ –Є —З–∞—Б—В—Л–µ –Ю–†–Т–Ш –≤ –∞–љ–∞–Љ–љ–µ–Ј–µ – –њ–Њ 10%.
–°—А–µ–і–Є —Б–Њ–њ—Г—В—Б—В–≤—Г—О—Й–Є—Е –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є–є –≤ –≥—А—Г–њ–њ–µ –і–Є–∞–≥–љ–Њ—Б—В–Є—А–Њ–≤–∞–љ—Л: –Ю–†–Т–Ш (9–45%), –њ—А–Њ—В–µ–Ї–∞–≤—И–∞—П —Г 2 –і–µ—В–µ–є –≤ –Њ—Б–ї–Њ–ґ–љ–µ–љ–љ–Њ–є —Д–Њ—А–Љ–µ (–Њ—В–Є—В, –≥–∞–є–Љ–Њ—А–Є—В). –£ —В—А–µ—Е (15%) –њ–∞—Ж–Є–µ–љ—В–Њ–≤ –Ї–Є—И–µ—З–љ–∞—П –Є–љ—Д–µ–Ї—Ж–Є—П —Б–Њ–њ—А–Њ–≤–Њ–ґ–і–∞–ї–∞—Б—М —А–∞–Ј–≤–Є—В–Є–µ–Љ –Љ–µ–Ј–Њ–∞–і–µ–љ–Є—В–∞ (—В–∞–±–ї. 1).
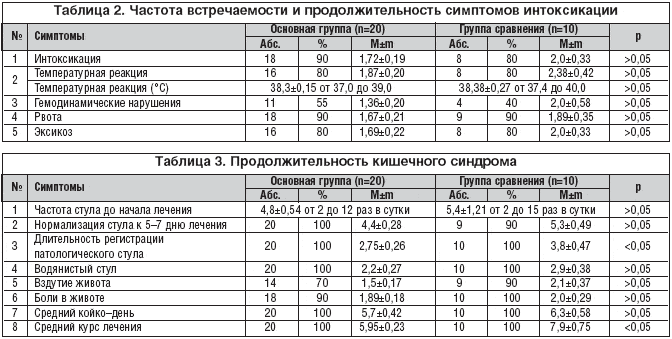
–≠—В–Є–Њ–ї–Њ–≥–Є—П –Ї–Є—И–µ—З–љ–Њ–є –Є–љ—Д–µ–Ї—Ж–Є–Є –±—Л–ї–∞ —А–∞—Б—И–Є—Д—А–Њ–≤–∞–љ–∞ —Г –њ–Њ–ї–Њ–≤–Є–љ—Л –њ–∞—Ж–Є–µ–љ—В–Њ–≤ (–≤ –Њ—Б–љ–Њ–≤–љ–Њ–Љ – —А–Њ—В–∞–≤–Є—А—Г—Б–љ–∞—П –Є–љ—Д–µ–Ї—Ж–Є—П, –≤ –µ–і–Є–љ–Є—З–љ—Л—Е —Б–ї—Г—З–∞—П—Е – —Б–∞–ї—М–Љ–Њ–љ–µ–ї–ї–µ–Ј –Є —И–Є–≥–µ–ї–ї–µ–Ј). –£ –њ–Њ–і–∞–≤–ї—П—О—Й–µ–≥–Њ –±–Њ–ї—М—И–Є–љ—Б—В–≤–∞ –і–µ—В–µ–є –і–Є–∞—А–µ–є–љ—Л–є —Б–Є–љ–і—А–Њ–Љ –њ—А–Њ—В–µ–Ї–∞–ї –њ–Њ —В–Є–њ—Г –≥–∞—Б—В—А–Њ—Н–љ—В–µ—А–Є—В–∞ (18–90%). –£ –≤—Б–µ—Е –љ–∞–±–ї—О–і–∞–≤—И–Є—Е—Б—П –Ј–∞—А–µ–≥–Є—Б—В—А–Є—А–Њ–≤–∞–љ–∞ —Б—А–µ–і–љ–µ—В—П–ґ–µ–ї–∞—П —Д–Њ—А–Љ–∞ –±–Њ–ї–µ–Ј–љ–Є. –І–∞—Б—В–Њ—В–∞ –≤—Б—В—А–µ—З–∞–µ–Љ–Њ—Б—В–Є –Є —Б—А–µ–і–љ—П—П –њ—А–Њ–і–Њ–ї–ґ–Є—В–µ–ї—М–љ–Њ—Б—В—М –Њ—Б–љ–Њ–≤–љ—Л—Е —Б–Є–Љ–њ—В–Њ–Љ–Њ–≤ –±–Њ–ї–µ–Ј–љ–Є —Г –і–µ—В–µ–є –њ—А–µ–і—Б—В–∞–≤–ї–µ–љ–∞ –≤ —В–∞–±–ї–Є—Ж–∞—Е 2 –Є 3.
–Ъ–∞–Ї –≤–Є–і–љ–Њ –Є–Ј —В–∞–±–ї–Є—Ж, –Ї–ї–Є–љ–Є—З–µ—Б–Ї–∞—П –Ї–∞—А—В–Є–љ–∞ –±–Њ–ї–µ–Ј–љ–Є —Г –і–µ—В–µ–є –±—Л–ї–∞ —П—А–Ї–Њ–є. –£ –њ–Њ–і–∞–≤–ї—П—О—Й–µ–≥–Њ –±–Њ–ї—М—И–Є–љ—Б—В–≤–∞ –њ—А–Є—Б—Г—В—Б—В–≤–Њ–≤–∞–ї–∞ –ї–Є—Е–Њ—А–∞–і–Ї–∞ –і–Њ —Д–µ–±—А–Є–ї—М–љ—Л—Е —Ж–Є—Д—А, —А–≤–Њ—В–∞, –≥–µ–Љ–Њ–і–Є–љ–∞–Љ–Є—З–µ—Б–Ї–Є–µ —А–∞—Б—Б—В—А–Њ–є—Б—В–≤–∞. –Т—Л—А–∞–ґ–µ–љ–љ–Њ—Б—В—М –Ї–Є—И–µ—З–љ–Њ–≥–Њ —В–Њ–Ї—Б–Є–Ї–Њ–Ј–∞ —Б —Н–Ї—Б–Є–Ї–Њ–Ј–Њ–Љ 1–2 —Б—В–µ–њ–µ–љ–Є –њ–Њ—В—А–µ–±–Њ–≤–∞–ї–∞ –љ–∞–Ј–љ–∞—З–µ–љ–Є—П –Є–љ—Д—Г–Ј–Є–Њ–љ–љ–Њ–є —В–µ—А–∞–њ–Є–Є 13 (65%) –±–Њ–ї—М–љ—Л–Љ. –Ъ–Є—И–µ—З–љ—Л–є —Б–Є–љ–і—А–Њ–Љ —Е–∞—А–∞–Ї—В–µ—А–Є–Ј–Њ–≤–∞–ї—Б—П –≤–Њ–і—П–љ–Є—Б—В–Њ–є –і–Є–∞—А–µ–µ–є –Є –±–Њ–ї–µ–≤—Л–Љ —Б–Є–љ–і—А–Њ–Љ–Њ–Љ.
–Ф–Є–љ–∞–Љ–Є—З–µ—Б–Ї–Њ–µ –љ–∞–±–ї—О–і–µ–љ–Є–µ –Ј–∞ –њ–∞—Ж–Є–µ–љ—В–∞–Љ–Є —Б–≤–Є–і–µ—В–µ–ї—М—Б—В–≤–Њ–≤–∞–ї–Њ –Њ —Е–Њ—А–Њ—И–µ–є –њ–Њ–ї–Њ–ґ–Є—В–µ–ї—М–љ–Њ–є –і–Є–љ–∞–Љ–Є–Ї–µ –±–Њ–ї–µ–Ј–љ–Є. –£ –і–µ—В–µ–є –±—Л—Б—В—А–Њ –Є—Б—З–µ–Ј–∞–ї–Є –њ—А–Є–Ј–љ–∞–Ї–Є —В–Њ–Ї—Б–Є–Ї–Њ–Ј–∞ –Є —Н–Ї—Б–Є–Ї–Њ–Ј–∞. –Я—А–Њ–і–Њ–ї–ґ–Є—В–µ–ї—М–љ–Њ—Б—В—М –Є–љ—Д—Г–Ј–Є–Њ–љ–љ–Њ–є —В–µ—А–∞–њ–Є–Є —Г 69,2% –і–µ—В–µ–є –љ–µ –њ—А–µ–≤—Л—И–∞–ї–∞ –Њ–і–Є–љ –і–µ–љ—М, —Б–Њ—Б—В–∞–≤–Є–≤ –≤ —Б—А–µ–і–љ–µ–Љ 1,39±0,18 –і–љ–µ–є. –Т –Њ—Б–љ–Њ–≤–љ–Њ–Љ –љ–∞—А—Г—И–µ–љ–Є—П —Е–∞—А–∞–Ї—В–µ—А–∞ —Б—В—Г–ї–∞ –љ–∞–±–ї—О–і–∞–ї–Є –љ–µ –±–Њ–ї–µ–µ 3 –і–љ–µ–є. –Т–Љ–µ—Б—В–µ —Б —В–µ–Љ —Г 50% –і–µ—В–µ–є –Ј–∞ –њ–µ—А–Є–Њ–і–Њ–Љ –њ–∞—В–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Њ–≥–Њ —Б—В—Г–ї–∞ —Б–ї–µ–і–Њ–≤–∞–ї –њ–µ—А–Є–Њ–і –µ–≥–Њ –Њ—В—Б—Г—В—Б—В–≤–Є—П –≤ —В–µ—З–µ–љ–Є–µ 1–2 –і–љ–µ–є (–≤ —Б—А–µ–і–љ–µ–Љ 1,5±0,17 –і–љ–µ–є), –њ–Њ—Б–ї–µ —З–µ–≥–Њ —А–µ–≥–Є—Б—В—А–Є—А–Њ–≤–∞–ї—Б—П —Б—В–Њ–є–Ї–Њ –љ–Њ—А–Љ–∞–ї—М–љ—Л–є —Б—В—Г–ї. –Ф–Њ–њ–Њ–ї–љ–Є—В–µ–ї—М–љ—Л—Е –Љ–µ—А–Њ–њ—А–Є—П—В–Є–є –≤ –≤–Є–і–µ –Њ—З–Є—Б—В–Є—В–µ–ї—М–љ—Л—Е –Ї–ї–Є–Ј–Љ –љ–Є –≤ –Њ–і–љ–Њ–Љ –љ–∞–±–ї—О–і–µ–љ–Є–Є –љ–µ –њ–Њ—В—А–µ–±–Њ–≤–∞–ї–Њ—Б—М.
–Т —Ж–µ–ї–Њ–Љ –љ–Њ—А–Љ–∞–ї–Є–Ј–∞—Ж–Є—П —Б—В—Г–ї–∞ –њ—А–Њ–Є–Ј–Њ—И–ї–∞ —Г –≤—Б–µ—Е (100%) –љ–∞–±–ї—О–і–∞–≤—И–Є—Е—Б—П –њ–∞—Ж–Є–µ–љ—В–Њ–≤ –Ї –Љ–Њ–Љ–µ–љ—В—Г –Њ–Ї–Њ–љ—З–∞–љ–Є—П –ї–µ—З–µ–љ–Є—П. –Э–Є –≤ –Њ–і–љ–Њ–Љ —Б–ї—Г—З–∞–µ –љ–µ –њ–Њ—В—А–µ–±–Њ–≤–∞–ї–Њ—Б—М –Ї–∞–Ї–Є—Е––ї–Є–±–Њ –і–Њ–њ–Њ–ї–љ–Є—В–µ–ї—М–љ—Л—Е —В–µ—А–∞–њ–µ–≤—В–Є—З–µ—Б–Ї–Є—Е –Љ–µ—А–Њ–њ—А–Є—П—В–Є–є, —В–∞–Ї –Ї–∞–Ї –Ї –Љ–Њ–Љ–µ–љ—В—Г –Њ–Ї–Њ–љ—З–∞–љ–Є—П –Ї—Г—А—Б–∞ –ї–µ—З–µ–љ–Є—П –њ—А–µ–њ–∞—А–∞—В–Њ–Љ –С–Є—Д–Є—Д–Њ—А–Љ –≤—Б–µ –њ–∞—Ж–Є–µ–љ—В—Л –≤—Л–Ј–і–Њ—А–Њ–≤–µ–ї–Є.
–Ч–∞ –њ–µ—А–Є–Њ–і –љ–∞–±–ї—О–і–µ–љ–Є—П —Г –±–Њ–ї—М–љ—Л—Е –љ–µ –Ј–∞—Д–Є–Ї—Б–Є—А–Њ–≤–∞–љ–Њ –Њ—В—А–Є—Ж–∞—В–µ–ї—М–љ—Л—Е –њ–Њ–±–Њ—З–љ—Л—Е —А–µ–∞–Ї—Ж–Є–є –њ—А–Є–Љ–µ–љ–µ–љ–Є—П –њ—А–µ–њ–∞—А–∞—В–∞ –С–Є—Д–Є—Д–Њ—А–Љ (–і–∞–ґ–µ —Г –ї–Є—Ж —Б –Њ—В—П–≥–Њ—Й–µ–љ–љ—Л–Љ –∞–ї–ї–µ—А–≥–Є—З–µ—Б–Ї–Є–Љ –∞–љ–∞–Љ–љ–µ–Ј–Њ–Љ). –Ф–Є–љ–∞–Љ–Є—З–µ—Б–Ї–Њ–µ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ –њ–µ—А–Є—Д–µ—А–Є—З–µ—Б–Ї–Њ–є –Ї—А–Њ–≤–Є —Б–≤–Є–і–µ—В–µ–ї—М—Б—В–≤–Њ–≤–∞–ї–Њ –Њ–± –Њ—В—Б—Г—В—Б—В–≤–Є–Є –Њ—В—А–Є—Ж–∞—В–µ–ї—М–љ–Њ–є –і–Є–љ–∞–Љ–Є–Ї–Є –њ–∞—А–∞–Љ–µ—В—А–Њ–≤ –њ–µ—А–Є—Д–µ—А–Є—З–µ—Б–Ї–Њ–є –Ї—А–Њ–≤–Є, –±–Є–Њ—Е–Є–Љ–Є—З–µ—Б–Ї–Њ–≥–Њ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П –Ї—А–Њ–≤–Є –Є –Њ–±—Й–µ–≥–Њ –∞–љ–∞–ї–Є–Ј–∞ –Љ–Њ—З–Є.
–У—А—Г–њ–њ–∞ —Б—А–∞–≤–љ–µ–љ–Є—П —Б–Њ—Б—В–Њ—П–ї–∞ –Є–Ј 10 –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —В–Њ–≥–Њ –ґ–µ –≤–Њ–Ј—А–∞—Б—В–∞ –Є –±—Л–ї–∞ —Б–Њ–њ–Њ—Б—В–∞–≤–Є–Љ–∞ —Б –Њ—Б–љ–Њ–≤–љ–Њ–є –њ–Њ –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є–Љ –њ–∞—А–∞–Љ–µ—В—А–∞–Љ (—В–∞–±–ї. 1–3).
–°—А–∞–≤–љ–Є—В–µ–ї—М–љ—Л–є –∞–љ–∞–ї–Є–Ј –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Њ–є —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В–Є –ї–µ—З–µ–љ–Є—П –≤ –і–≤—Г—Е –≥—А—Г–њ–њ–∞—Е –Њ–±–љ–∞—А—Г–ґ–Є–ї –Њ–њ—А–µ–і–µ–ї–µ–љ–љ—Л–µ –њ—А–µ–Є–Љ—Г—Й–µ—Б—В–≤–∞ –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є—П –њ—А–µ–њ–∞—А–∞—В–∞ –С–Є—Д–Є—Д–Њ—А–Љ. –Т –Њ—Б–љ–Њ–≤–љ–Њ–є –≥—А—Г–њ–њ–µ –љ–∞–Љ–µ—В–Є–ї–Є—Б—М —В–µ–љ–і–µ–љ—Ж–Є–Є –Ї —Б–Њ–Ї—А–∞—Й–µ–љ–Є—О –њ—А–Њ–і–Њ–ї–ґ–Є—В–µ–ї—М–љ–Њ—Б—В–Є —В–µ–Љ–њ–µ—А–∞—В—Г—А–љ–Њ–є —А–µ–∞–Ї—Ж–Є–Є, –≥–µ–Љ–Њ–і–Є–љ–∞–Љ–Є—З–µ—Б–Ї–Є—Е –љ–∞—А—Г—И–µ–љ–Є–є, –≤–Њ–і—П–љ–Є—Б—В–Њ–є –і–Є–∞—А–µ–Є, –≤–Ј–і—Г—В–Є—П –ґ–Є–≤–Њ—В–∞. –Ф–Њ—Б—В–Њ–≤–µ—А–љ–Њ —Б–Њ–Ї—А–∞—В–Є–ї–∞—Б—М –і–ї–Є—В–µ–ї—М–љ–Њ—Б—В—М —А–µ–≥–Є—Б—В—А–∞—Ж–Є–Є –њ–∞—В–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Њ–≥–Њ —Б—В—Г–ї–∞ (—В–∞–±–ї. 3). –Ъ –Љ–Њ–Љ–µ–љ—В—Г –≤—Л–њ–Є—Б–Ї–Є –≤—Б–µ –і–µ—В–Є, –њ–Њ–ї—Г—З–∞–≤—И–Є–µ –њ—А–µ–њ–∞—А–∞—В –С–Є—Д–Є—Д–Њ—А–Љ, –±—Л–ї–Є –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є –Ј–і–Њ—А–Њ–≤—Л. –Т –≥—А—Г–њ–њ–µ —Б—А–∞–≤–љ–µ–љ–Є—П –Њ—В—Б—Г—В—Б—В–≤–Є–µ —Г–і–Њ–≤–ї–µ—В–≤–Њ—А–Є—В–µ–ї—М–љ–Њ–є –њ–Њ–ї–Њ–ґ–Є—В–µ–ї—М–љ–Њ–є –і–Є–љ–∞–Љ–Є–Ї–Є —Б–Њ—Б—В–Њ—П–љ–Є—П –њ–Њ—В—А–µ–±–Њ–≤–∞–ї–Њ –љ–∞–Ј–љ–∞—З–µ–љ–Є—П —Н–љ—В–µ—А–∞–ї—М–љ–Њ–є –∞–љ—В–Є–±–∞–Ї—В–µ—А–Є–∞–ї—М–љ–Њ–є —В–µ—А–∞–њ–Є–Є –≤ –і–≤—Г—Е —Б–ї—Г—З–∞—П—Е –Є –њ—А–Њ–ї–Њ–љ–≥–∞—Ж–Є–Є –ї–µ—З–µ–љ–Є—П –њ–Њ—Б–ї–µ –≤—Л–њ–Є—Б–Ї–Є –Є–Ј —Б—В–∞—Ж–Є–Њ–љ–∞—А–∞ – –≤ –Њ–і–љ–Њ–Љ. –Ґ–∞–Ї–Є–Љ –Њ–±—А–∞–Ј–Њ–Љ, —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В—М —Б—В–∞—А—В–Њ–≤–Њ–≥–Њ –Ї—Г—А—Б–∞ –ї–µ—З–µ–љ–Є—П –≤ –Њ—Б–љ–Њ–≤–љ–Њ–є –≥—А—Г–њ–њ–µ –±—Л–ї–∞ –≤—Л—И–µ –љ–∞ 30%. –Ш—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є–µ –њ—А–µ–њ–∞—А–∞—В–∞ –С–Є—Д–Є—Д–Њ—А–Љ –њ–Њ–Ј–≤–Њ–ї–Є–ї–Њ –і–Њ—Б—В–Њ–≤–µ—А–љ–Њ —Б–Њ–Ї—А–∞—В–Є—В—М –њ—А–Њ–і–Њ–ї–ґ–Є—В–µ–ї—М–љ–Њ—Б—В—М —В–µ—А–∞–њ–µ–≤—В–Є—З–µ—Б–Ї–Њ–≥–Њ –Ї—Г—А—Б–∞.
–Ш—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ –њ–∞—А–∞–Љ–µ—В—А–Њ–≤ –Ї–Њ–њ—А–Њ—Ж–Є—В–Њ–≥—А–∞–Љ–Љ—Л –њ—А–Њ–≤–Њ–і–Є–ї–Њ—Б—М –≤ –Њ—Б—В—А–Њ–Љ –њ–µ—А–Є–Њ–і–µ –±–Њ–ї–µ–Ј–љ–Є –Є —З–µ—А–µ–Ј 5–6 –і–љ–µ–є. –°—А–∞–≤–љ–µ–љ–Є–µ —А–µ–Ј—Г–ї—М—В–∞—В–Њ–≤ –њ—А–Њ–і–µ–Љ–Њ–љ—Б—В—А–Є—А–Њ–≤–∞–ї–Њ —Б–љ–Є–ґ–µ–љ–Є–µ –≤ 4,1 —А–∞–Ј–∞ (p<0,01) –Љ–∞—Б—Б–Є–≤–љ–Њ—Б—В–Є –Њ–±–љ–∞—А—Г–ґ–µ–љ–Є—П –є–Њ–і–Њ—Д–Є–ї—М–љ–Њ–є —Д–ї–Њ—А—Л (–≤ –љ–Њ—А–Љ–µ –Њ—В—Б—Г—В—Б—В–≤—Г–µ—В) –Є —З–∞—Б—В–Њ—В—Л —А–µ–≥–Є—Б—В—А–∞—Ж–Є–Є –≤–Њ—Б–њ–∞–ї–Є—В–µ–ї—М–љ–Њ–≥–Њ –±–µ–ї–Ї–∞ (—В–∞–±–ї. 4).
–°—А–∞–≤–љ–µ–љ–Є–µ —Б –Ї–Њ–љ—В—А–Њ–ї—М–љ–Њ–є –≥—А—Г–њ–њ–Њ–є –≤—Л—П–≤–Є–ї–Њ –±–Њ–ї–µ–µ –±—Л—Б—В—А—Л–µ —Б—А–Њ–Ї–Є –љ–Њ—А–Љ–∞–ї–Є–Ј–∞—Ж–Є–Є –Ї–Є—И–µ—З–љ–Њ–≥–Њ –њ–Є—Й–µ–≤–∞—А–µ–љ–Є—П. –І–∞—Б—В–Њ—В–∞ –Њ–±–љ–∞—А—Г–ґ–µ–љ–Є—П –±–Њ–ї—М—И–Њ–≥–Њ –Ї–Њ–ї–Є—З–µ—Б—В–≤–∞ –ґ–Є—А–љ—Л—Е –Ї–Є—Б–ї–Њ—В —Г –њ–Њ–ї—Г—З–∞–≤—И–Є—Е –њ—А–µ–њ–∞—А–∞—В –С–Є—Д–Є—Д–Њ—А–Љ –±—Л–ї–∞ –љ–Є–ґ–µ –≤ 1,4 —А–∞–Ј–∞, –Љ—Л–ї –≤ 2 —А–∞–Ј–∞ (p<0,1), –є–Њ–і–Њ—Д–Є–ї—М–љ–Њ–є —Д–ї–Њ—А—Л –≤ 6 —А–∞–Ј (p<0,05). –Ш —Е–Њ—В—П —З–∞—Б—В–Њ—В–∞ –Њ–±–љ–∞—А—Г–ґ–µ–љ–Є—П –≤–Њ—Б–њ–∞–ї–Є—В–µ–ї—М–љ–Њ–≥–Њ –±–µ–ї–Ї–∞ –≤ —Д–µ–Ї–∞–ї–Є—П—Е –і–µ—В–µ–є –Є–Ј –Ї–Њ–љ—В—А–Њ–ї—М–љ–Њ–є –≥—А—Г–њ–њ—Л —В–∞–Ї–ґ–µ —Б–Њ–Ї—А–∞—В–Є–ї–∞—Б—М, —В–µ–Љ –љ–µ –Љ–µ–љ–µ–µ, –Њ–љ –Њ–±–љ–∞—А—Г–ґ–Є–≤–∞–ї—Б—П –љ–∞ 27% —З–∞—Й–µ.
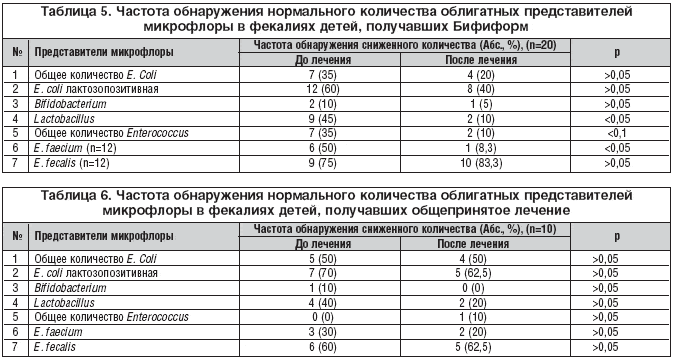
–Т –Њ—Б—В—А–Њ–Љ –њ–µ—А–Є–Њ–і–µ –±–Њ–ї–µ–Ј–љ–Є –і–Є—Б–±–Є–Њ—В–Є—З–µ—Б–Ї–Є–µ –Є–Ј–Љ–µ–љ–µ–љ–Є—П –≤ —В–Њ–ї—Б—В–Њ–є –Ї–Є—И–Ї–µ –Њ–±–љ–∞—А—Г–ґ–Є–≤–∞–ї–Є—Б—М —Г –±–Њ–ї—М—И–Є–љ—Б—В–≤–∞ –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –Ї–Њ–ї–Є—З–µ—Б—В–≤–µ–љ–љ—Л–Љ –љ–∞—А—Г—И–µ–љ–Є–µ–Љ –Њ—В–і–µ–ї—М–љ—Л—Е –њ–∞—А–∞–Љ–µ—В—А–Њ–≤ –≤ 10–60% —Б–ї—Г—З–∞–µ–≤. –Р–љ–∞–ї–Є–Ј, –њ—А–Њ–≤–µ–і–µ–љ–љ—Л–є –і–Њ –Є –њ–Њ—Б–ї–µ –ї–µ—З–µ–љ–Є—П, —Б–≤–Є–і–µ—В–µ–ї—М—Б—В–≤–Њ–≤–∞–ї –Њ –њ–Њ–ї–Њ–ґ–Є—В–µ–ї—М–љ–Њ–є –і–Є–љ–∞–Љ–Є–Ї–µ –≤ –Њ—В–љ–Њ—И–µ–љ–Є–Є –≤—Б–µ—Е –Њ–±–ї–Є–≥–∞—В–љ—Л—Е –њ—А–µ–і—Б—В–∞–≤–Є—В–µ–ї–µ–є –Љ–Є–Ї—А–Њ—Д–ї–Њ—А—Л —В–Њ–ї—Б—В–Њ–є –Ї–Є—И–Ї–Є —Б –і–Њ—Б—В–Њ–≤–µ—А–љ—Л–Љ —Г–≤–µ–ї–Є—З–µ–љ–Є–µ–Љ —З–∞—Б—В–Њ—В—Л –љ–Њ—А–Љ–∞–ї–Є–Ј–∞—Ж–Є–Є —Г—А–Њ–≤–љ—П –ї–∞–Ї—В–Њ–±–∞–Ї—В–µ—А–Є–є –Є —Н–љ—В–µ—А–Њ–Ї–Њ–Ї–Ї–Њ–≤ —Г –і–µ—В–µ–є, –њ–Њ–ї—Г—З–∞–≤—И–Є—Е –С–Є—Д–Є—Д–Њ—А–Љ (—В–∞–±–ї. 5).
–Я—А–Є —Н—В–Њ–Љ —Б—А–µ–і–љ–µ–µ –Ї–Њ–ї–Є—З–µ—Б—В–≤–Њ –ї–∞–Ї—В–Њ–Ј–Њ–њ–Њ–Ј–Є—В–Є–≤–љ–Њ–є –Ї–Є—И–µ—З–љ–Њ–є –њ–∞–ї–Њ—З–Ї–Є (6,96±0,65 –Є 7,71±0,64 lg –Ъ–Ю–Х/–≥, p>0,05), —Н–љ—В–µ—А–Њ–Ї–Њ–Ї–Ї–Њ–≤ (5,69±0,37 –Є 6,21±0,32 lg –Ъ–Ю–Х/–≥, p>0,05) –Є E. faecium (4,67±0,21 –Є 5,27±0,19 lg –Ъ–Ю–Х/–≥, p>0,05) –≤—Л—А–Њ—Б–ї–Њ –љ–∞ –њ–Њ—А—П–і–Њ–Ї. –Ч–∞—А–µ–≥–Є—Б—В—А–Є—А–Њ–≤–∞–љ–∞ —Н–ї–Є–Љ–Є–љ–∞—Ж–Є—П S. aureus –≤ 3 —Б–ї—Г—З–∞—П—Е –Є–Ј —З–µ—В—Л—А–µ—Е.
–Ю–і–љ–Њ–≤—А–µ–Љ–µ–љ–љ–Њ –Њ—В–Љ–µ—З–µ–љ–∞ —В–µ–љ–і–µ–љ—Ж–Є—П –Ї –љ–∞—А–∞—Б—В–∞–љ–Є—О (–±–µ–Ј –і–Њ—Б—В–Њ–≤–µ—А–љ—Л—Е –Њ—В–ї–Є—З–Є–є) —Б—А–µ–і–љ–µ–≥–Њ –Ї–Њ–ї–Є—З–µ—Б—В–≤–∞ –Ї–Є—И–µ—З–љ–Њ–є –њ–∞–ї–Њ—З–Ї–Є —Б –ї–∞–Ї—В–Њ–Ј–Њ–љ–µ–≥–∞—В–Є–≤–љ—Л–Љ–Є –Є –≥–µ–Љ–Њ–ї–Є—В–Є—З–µ—Б–Ї–Є–Љ–Є —Б–≤–Њ–є—Б—В–≤–∞–Љ–Є –Є –і–Њ—Б—В–Њ–≤–µ—А–љ–Њ –Ј–љ–∞—З–Є–Љ–Њ–µ —Г–≤–µ–ї–Є—З–µ–љ–Є–µ —Г–і–µ–ї—М–љ–Њ–≥–Њ –≤–µ—Б–∞ –Ї–ї–Њ—Б—В—А–Є–і–Є–є (–Њ—В 41,7 –і–Њ 91,7%, p<0,001).
–Т –≥—А—Г–њ–њ–µ —Б—А–∞–≤–љ–µ–љ–Є—П —Б—Г—Й–µ—Б—В–≤–µ–љ–љ–Њ–є –і–Є–љ–∞–Љ–Є–Ї–Є –Њ–±–ї–Є–≥–∞—В–љ—Л—Е –њ—А–µ–і—Б—В–∞–≤–Є—В–µ–ї–µ–є –Љ–Є–Ї—А–Њ—Д–ї–Њ—А—Л –љ–µ –Њ–±–љ–∞—А—Г–ґ–µ–љ–Њ (—В–∞–±–ї. 6). –Ъ—А–Њ–Љ–µ —В–Њ–≥–Њ, –Ј–∞—А–µ–≥–Є—Б—В—А–Є—А–Њ–≤–∞–љ–Њ —Г–≥–љ–µ—В–µ–љ–Є–µ —А–Њ—Б—В–∞ –љ–∞ 2 –њ–Њ—А—П–і–Ї–∞ (–Њ—В 7,29±1,03 –і–Њ 5,54±1,51 lg –Ъ–Ю–Х/–≥, p>0,05) –ї–∞–Ї—В–Њ–Ј–Њ–њ–Њ–Ј–Є—В–Є–≤–љ–Њ–є –Ї–Є—И–µ—З–љ–Њ–є –њ–∞–ї–Њ—З–Ї–Є, –њ—А–Є –Њ—В—Б—Г—В—Б—В–≤–Є–Є –≤ —Б—А–µ–і–љ–µ–Љ –њ–Њ –≥—А—Г–њ–њ–µ –Ї–Њ–ї–Є—З–µ—Б—В–≤–µ–љ–љ–Њ–є –і–Є–љ–∞–Љ–Є–Ї–Є —Н–љ—В–µ—А–Њ–Ї–Њ–Ї–Ї–Њ–≤.
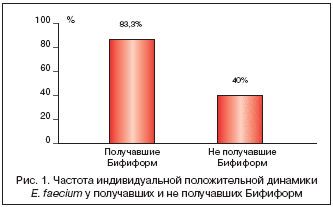
–Ш–љ–і–Є–≤–Є–і—Г–∞–ї—М–љ–∞—П –њ–Њ–ї–Њ–ґ–Є—В–µ–ї—М–љ–∞—П –Ї–Њ–ї–Є—З–µ—Б—В–≤–µ–љ–љ–∞—П –і–Є–љ–∞–Љ–Є–Ї–∞ –Њ–±—Й–µ–≥–Њ –Ї–Њ–ї–Є—З–µ—Б—В–≤–∞ —Н–љ—В–µ—А–Њ–Ї–Њ–Ї–Ї–Њ–≤ —Б—А–µ–і–Є –і–µ—В–µ–є, –њ–Њ–ї—Г—З–∞–≤—И–Є—Е –С–Є—Д–Є—Д–Њ—А–Љ, –≤—Б—В—А–µ—З–∞–ї–∞—Б—М –≤ 65% —Б–ї—Г—З–∞–µ–≤, –≤ –Ї–Њ–љ—В—А–Њ–ї–µ – –≤ 50%, –≤ –Њ—Б–љ–Њ–≤–љ–Њ–Љ –Ј–∞ —Б—З–µ—В E. faecium (83,3% –њ—А–Њ—В–Є–≤ 40%, —А–Є—Б. 1).
–І–∞—Б—В–Њ—В–∞ –Њ–±–љ–∞—А—Г–ґ–µ–љ–Є—П –Ї–ї–Њ—Б—В—А–Є–і–Є–є –≤ –≥—А—Г–њ–њ–µ —Б—А–∞–≤–љ–µ–љ–Є—П –≤ –і–Є–љ–∞–Љ–Є–Ї–µ –ї–µ—З–µ–љ–Є—П —Б–љ–Є–Ј–Є–ї–∞—Б—М (–Њ—В 70 –і–Њ 37,5%, p>0,05).
–Ф–ї—П –њ–Њ–і—В–≤–µ—А–ґ–і–µ–љ–Є—П –Њ–±–љ–∞—А—Г–ґ–µ–љ–љ—Л—Е —В–µ–љ–і–µ–љ—Ж–Є–є —Ж–µ–ї–µ—Б–Њ–Њ–±—А–∞–Ј–љ–Њ –њ—А–Њ–і–Њ–ї–ґ–Є—В—М –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П —Б —Г–≤–µ–ї–Є—З–µ–љ–Є–µ–Љ –Њ–±—К–µ–Љ–∞ –Ї–Њ–љ—В—А–Њ–ї—М–љ–Њ–є –≤—Л–±–Њ—А–Ї–Є.
–Ґ–∞–Ї–Є–Љ –Њ–±—А–∞–Ј–Њ–Љ, –≤—Л—И–µ—Б–Ї–∞–Ј–∞–љ–љ–Њ–µ –њ–Њ–Ј–≤–Њ–ї—П–µ—В —А–µ–Ј—О–Љ–Є—А–Њ–≤–∞—В—М:
– –С–Є—Д–Є—Д–Њ—А–Љ –Љ–Њ–ґ–µ—В –±—Л—В—М —А–µ–Ї–Њ–Љ–µ–љ–і–Њ–≤–∞–љ –≤ –Ї–∞—З–µ—Б—В–≤–µ –µ–і–Є–љ—Б—В–≤–µ–љ–љ–Њ–≥–Њ —Н—В–Є–Њ–њ–∞—В–Њ–≥–µ–љ–µ—В–Є—З–µ—Б–Ї–Њ–≥–Њ —Б—А–µ–і—Б—В–≤–∞ –ї–µ—З–µ–љ–Є—П –≤–Њ–і—П–љ–Є—Б—В—Л—Е –і–Є–∞—А–µ–є —Г –і–µ—В–µ–є —Б—В–∞—А—И–µ –і–≤—Г—Е –ї–µ—В, —В–∞–Ї –Ї–∞–Ї –µ–≥–Њ –љ–∞–Ј–љ–∞—З–µ–љ–Є–µ –≤ —В–µ—З–µ–љ–Є–µ 5–7 –і–љ–µ–є –њ—А–Є–≤–Њ–і–Є–ї–Њ –Ї –≤—Л–Ј–і–Њ—А–Њ–≤–ї–µ–љ–Є—О;
– –њ–Њ–±–Њ—З–љ—Л—Е —А–µ–∞–Ї—Ж–Є–є –њ—А–Є–Љ–µ–љ–µ–љ–Є—П –њ—А–µ–њ–∞—А–∞—В–∞ –С–Є—Д–Є—Д–Њ—А–Љ –љ–µ –Ј–∞—А–µ–≥–Є—Б—В—А–Є—А–Њ–≤–∞–љ–Њ;
– –љ–∞–Ј–љ–∞—З–µ–љ–Є–µ –њ—А–µ–њ–∞—А–∞—В–∞ –С–Є—Д–Є—Д–Њ—А–Љ —Б–њ–Њ—Б–Њ–±—Б—В–≤–Њ–≤–∞–ї–Њ —Б–Њ–Ї—А–∞—Й–µ–љ–Є—О —Б—А–Њ–Ї–Њ–≤ —А–µ–≥–Є—Б—В—А–∞—Ж–Є–Є –њ–∞—В–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Њ–≥–Њ —Б—В—Г–ї–∞ –Є –њ—А–Њ–і–Њ–ї–ґ–Є—В–µ–ї—М–љ–Њ—Б—В–Є –ї–µ—З–µ–љ–Є—П;
– –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є–µ –њ—А–µ–њ–∞—А–∞—В–∞ –С–Є—Д–Є—Д–Њ—А–Љ –њ–Њ–≤—Л—И–∞–µ—В —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В—М —Б—В–∞—А—В–Њ–≤–Њ–≥–Њ –Ї—Г—А—Б–∞ –ї–µ—З–µ–љ–Є—П –њ–Њ —Б—А–∞–≤–љ–µ–љ–Є—О —Б –Њ–±—Й–µ–њ—А–Є–љ—П—В—Л–Љ –ї–µ—З–µ–љ–Є–µ–Љ;
– –≤ —Д–µ–Ї–∞–ї–Є—П—Е –і–µ—В–µ–є, –њ–Њ–ї—Г—З–∞–≤—И–Є—Е –њ—А–µ–њ–∞—А–∞—В –С–Є—Д–Є—Д–Њ—А–Љ, –Њ—В–Љ–µ—З–µ–љ–Њ —Б–љ–Є–ґ–µ–љ–Є–µ —Г—А–Њ–≤–љ—П –є–Њ–і–Њ—Д–Є–ї—М–љ–Њ–є —Д–ї–Њ—А—Л –≤ 4 —А–∞–Ј–∞ –Є –≤–Њ—Б–њ–∞–ї–Є—В–µ–ї—М–љ–Њ–≥–Њ –±–µ–ї–Ї–∞ –≤ 3 —А–∞–Ј–∞, —З—В–Њ —Б–≤–Є–і–µ—В–µ–ї—М—Б—В–≤—Г–µ—В –Њ –±—Л—Б—В—А–Њ–Љ –Є—Б—З–µ–Ј–љ–Њ–≤–µ–љ–Є–Є –≤–Њ—Б–њ–∞–ї–Є—В–µ–ї—М–љ–Њ–≥–Њ –њ—А–Њ—Ж–µ—Б—Б–∞ –≤ –Ї–Є—И–µ—З–љ–Є–Ї–µ (–≤ –≥—А—Г–њ–њ–µ —Б—А–∞–≤–љ–µ–љ–Є—П –њ—А–Њ—Ж–µ—Б—Б—Л –њ–Є—Й–µ–≤–∞—А–µ–љ–Є—П –≤–Њ—Б—Б—В–∞–љ–∞–≤–ї–Є–≤–∞–ї–Є—Б—М –±–Њ–ї–µ–µ –Љ–µ–і–ї–µ–љ–љ—Л–Љ–Є —В–µ–Љ–њ–∞–Љ–Є);
– –≤ –Њ—В–ї–Є—З–Є–µ –Њ—В –Ї–Њ–љ—В—А–Њ–ї—П –Њ—В–Љ–µ—З–µ–љ–Њ —Б—Г—Й–µ—Б—В–≤–µ–љ–љ–Њ–µ –љ–∞—А–∞—Б—В–∞–љ–Є–µ (–љ–∞ 15–45%) —З–∞—Б—В–Њ—В—Л –љ–Њ—А–Љ–∞–ї–Є–Ј–∞—Ж–Є–Є –Њ–±–ї–Є–≥–∞—В–љ—Л—Е –њ—А–µ–і—Б—В–∞–≤–Є—В–µ–ї–µ–є –Љ–Є–Ї—А–Њ—Д–ї–Њ—А—Л —В–Њ–ї—Б—В–Њ–є –Ї–Є—И–Ї–Є (–Њ—Б–Њ–±–µ–љ–љ–Њ –ї–∞–Ї—В–Њ–±–∞–Ї—В–µ—А–Є–є –Є —Н–љ—В–µ—А–Њ–Ї–Њ–Ї–Ї–Њ–≤ –Ј–∞ —Б—З–µ—В E. faecium), –љ–∞–Љ–µ—В–Є–ї–∞—Б—М –±–Њ–ї–µ–µ –≤—Л—А–∞–ґ–µ–љ–љ–∞—П —В–µ–љ–і–µ–љ—Ж–Є—П –Ї –≤–Њ—Б—Б—В–∞–љ–Њ–≤–ї–µ–љ–Є—О —Г—А–Њ–≤–љ—П –ї–∞–Ї—В–Њ–Ј–Њ–њ–Њ–Ј–Є—В–Є–≤–љ–Њ–є –Ї–Є—И–µ—З–љ–Њ–є –њ–∞–ї–Њ—З–Ї–Є.


–Ы–Є—В–µ—А–∞—В—Г—А–∞
1. –°—Г–≤–Њ—А–Њ–≤ –Р.–Э., –Ч–∞—Е–∞—А–µ–љ–Ї–Њ –°.–Ь., –Р–ї–µ—Е–Є–љ–∞ –У.–У. –≠–љ—В–µ—А–Њ–Ї–Њ–Ї–Ї–Є –Ї–∞–Ї –њ—А–Њ–±–Є–Њ—В–Є–Ї–Є –≤—Л–±–Њ—А–∞// –Ъ–ї–Є–љ–Є—З–µ—Б–Ї–Њ–µ –њ–Є—В–∞–љ–Є–µ.–2003.–вДЦ1.––°.26–29.
2. –С–Њ—З–Ї–Њ–≤ –Ш.–Р., –Ѓ—А–Ї–Њ –Ф.–Я. –Ѓ–і–Є—Ж–Ї–∞—П –Э.–Ь. –°–Њ—Б—В–Њ—П–љ–Є–µ –Љ–Є–Ї—А–Њ—Д–ї–Њ—А—Л —В–Њ–ї—Б—В–Њ–є –Ї–Є—И–Ї–Є —Г –і–µ—В–µ–є —А–∞–љ–љ–µ–≥–Њ –≤–Њ–Ј—А–∞—Б—В–∞// –Ш–љ—Д–µ–Ї—Ж–Є–Њ–љ–љ—Л–µ –±–Њ–ї–µ–Ј–љ–Є.–2004.–вДЦ3.––°.83–85
3. Bellomo G.,Mangiagle A., Nicastro L. at al. A controlled doubl–blind study of SF 68 strain as a nowbiological preparation for treatment of diarrhea in pediatrics. Curr/ Ther/ Res, 1980;28:927–936.
4. Wanderlich P.F., Braun L.,Apuzzo V.D. et al. Doubl–blind report on the efficacy of laetic acid producing Enterococcus SF 68 in the prevention of antibiotic–associated diarrhea and in the treatment of acute diarrhea. J. Int. Med. Res. 1989;17:333–338.
5.–Т–∞—Е–Є—В–Њ–≤ –Ґ.–ѓ., –Я–µ—В—А–Њ–≤ –Ы.–Э., –С–Њ–љ–і–∞—А–µ–љ–Ї–Њ –Т.–Ь. –Ъ–Њ–љ—Ж–µ–њ—Ж–Є—П –њ—А–Њ–±–Є–Њ—В–Є—З–µ—Б–Ї–Њ–≥–Њ –њ—А–Њ–і—Г–Ї—В–∞, —Б–Њ–і–µ—А–ґ–∞—Й–µ–≥–Њ –Њ—А–Є–≥–Є–љ–∞–ї—М–љ—Л–µ –Љ–Є–Ї—А–Њ–±–љ—Л–µ –Љ–µ—В–∞–±–Њ–ї–Є—В—Л// –Ц—Г—А–љ. –Љ–Є–Ї—А–Њ–±–Є–Њ–ї.–2005.–вДЦ 5.––°.108–114.
6. –Т–Њ—А–Њ–±—М–µ–≤ –Р.–Р., –С–Њ–љ–і–∞—А–µ–љ–Ї–Њ –Т.–Ь., –Ы—Л–Ї–Њ–≤–∞ –Х.–Т. –Є –і—А. –Ь–∞–Ї—А–Њ—Н–Ї–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є–µ –љ–∞—А—Г—И–µ–љ–Є—П –њ—А–Є –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Њ–є –њ–∞—В–Њ–ї–Њ–≥–Є–Є –Є –Є—Е –Ї–Њ—А—А–µ–Ї—Ж–Є—П –±–Є—Д–Є–і–Њ—Б–Њ–і–µ—А–ґ–∞—Й–Є–Љ–Є –њ—А–µ–њ–∞—А–∞—В–∞–Љ–Є// –Т–µ—Б—В–љ–Є–Ї –†–Р–Ь–Э.–2004.–вДЦ2.––°.13–17.
7. –С–Њ–љ–і–∞—А–µ–љ–Ї–Њ –Т.–Ь., –Т–Њ—А–Њ–±—М–µ–≤ –Р.–Р. –Ф–Є—Б–±–Є–Њ–Ј—Л –Є –њ—А–µ–њ–∞—А–∞—В—Л —Б –њ—А–Њ–±–Є–Њ—В–Є—З–µ—Б–Ї–Њ–є —Д—Г–љ–Ї—Ж–Є–µ–є// –Ц—Г—А–љ. –Љ–Є–Ї—А–Њ–±–Є–Њ–ї.– 2004.–вДЦ1.––°.84–92.
8. –Э–Њ–≤–Њ–Ї—И–Њ–љ–Њ–≤ –Р.–Р., –°–Њ–Ї–Њ–ї–Њ–≤–∞ –Э.–Т., –У–µ–ї–µ–µ–≤–∞ –Х.–Т. –Є –і—А. –Я—А–Њ–±–Є–Њ—В–Є–Ї –С–Є—Д–Є—Д–Њ—А–Љ – –∞–ї—М—В–µ—А–љ–∞—В–Є–≤–∞ —Н—В–Є–Њ—В—А–Њ–њ–љ–Њ–є –∞–љ—В–Є–±–Є–Њ—В–Є–Ї–Њ– –Є —Е–Є–Љ–Є–Њ—В–µ—А–∞–њ–Є–Є –Њ—Б—В—А—Л—Е –Ї–Є—И–µ—З–љ—Л—Е –Є–љ—Д–µ–Ї—Ж–Є–є —Г –і–µ—В–µ–є// –Ф–µ—В—Б–Ї–Є–µ –Є–љ—Д–µ–Ї—Ж–Є–Є.–2003.–вДЦ3.–36–40.








.gif)



