Атерогенные дислипидемии могут развиваться в результате аномалий генов, которые регулируют функции рецепторов, ферментов или транспортных белков, участвующих в липидном обмене. В этих случаях они проявляются, как семейные (наследственные) нарушения липидного метаболизма и относятся к первичным [1]. Нарушения липидного обмена, сопровождающие некоторые заболевания, гормональные нарушения или возникающие при приеме лекарственных препаратов (тиазиды, оксодолин, неселективные β–блокаторы – пропранолол, иммунодепрессанты, половые стероиды, барбитураты и циметидин), классифицируются как вторичные.
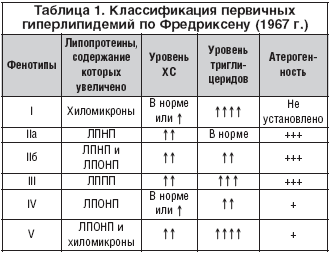
В настоящее время в качестве стандартной номенклатуры гиперлипидемии используется классификация Фредриксона 1965 г., утвержденная ВОЗ в качестве международной в 1970 г. (табл. 1). В повседневной практике врач чаще всего имеет дело с дислипидемией (ДЛП) IIa, IIb и IV типа [4].
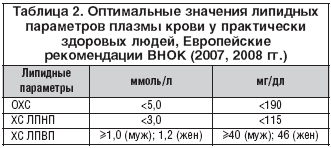
Оптимальные значения липидных параметров, которые были приняты секцией атеросклероза ВНОК в соответствии с Европейскими рекомендациями по профилактике ССЗ, представлены в таблице 2. Эти значения оптимальны для практически здоровых взрослых людей.
У больных с ИБС, облитерирующими заболеваниями артерий нижних конечностей, а также сонных артерий, аневризмой брюшного отдела аорты, сахарным диабетом, оптимальными уровнями ОХС, ХС ЛПНП являются значения: ОХС≤4,5 ммоль/л (175 мг/дл) и ХС ЛПНП 2,5 ммоль/л (100 мг/дл ) [5].
В клинической практике нарушение липидного обмена диагностируется на основании оценки липидного профиля: общего холестерина (ХС), триглицеридов (ТГ), ХС – липопротеидов низкой плотности (ХС ЛПНП) и ХС липопротеидов высокой плотности (ХС ЛПВП) [16].
К липидным факторам риска развития атеросклероза относятся:
• гиперхолестеринемия (общий ХС > 5,0 ммоль/л);
• ХС ЛПНП >3,0 ммоль/л;
• ХС ЛПВП <1,0 ммоль/л у мужчин и <1,2 ммоль/л у женщин;
• гипертриглицеридемия (ТГ >1,7 ммоль/л);
• отношение общего ХС/ХС ЛПВП >5 – индекс атерогенности.
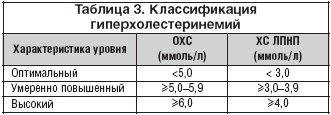
По уровню значения общего ХС гиперхолестеринемии подразделяются на оптимальные, умеренно повышенные, высокие (табл. 3).
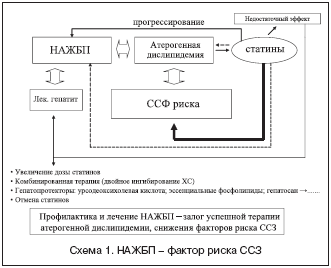
Пациентам с дислипидемиями показано наблюдение и, возможно, специфическая гиполипидемическая терапия. Но проблемным фактором в терапии дислипидемии остается поражение печени.
По современным представлениям нарушения функции печени при дислипидемии проявляются в виде НАЖБП [3,7,11,15,18].
Понятие НАЖБП четко очерчено и представляет собой патогенетически связанную группу поражений печени, включающую:
• жировую дистрофию печени (стеатоз);
• жировую дистрофию с воспалением и повреждением гепатоцитов – неалкогольный стеатогепатит (НАСГ);
• НАСГ с фиброзом (с возможностью прогрессии и исходом в цирроз печени (ЦП)). НАСГ – как вторая стадия развития заболевания, опасна своим переходом в ряде случаев в ЦП и рак печени (в 60–80% наблюдений ЦП неясной этиологии развивается из нераспознанного НАСГ).
Неалкогольный стеатогепатит разделяют на первичный и вторичный.
Основные причины развития первичного НАСГ: висцеральное ожирение, сахарный диабет 2 типа, дислипидемия [3,12,15,17]. Причины развития вторичного НАСГ: лекарственные препараты (глюкокортикоиды, амиодарон, эстрогены, тамоксифен, тетрациклин, ацетилсалициловая кислота, индометацин, бруфен), другие противовоспалительные средства; недостаточное питание, в особенности недостаток белка (при обширных операциях на желудке и тонкой кишке, при резком – более 1,5 кг в неделю снижении веса, при некоторых врожденных аномалиях обмена – болезнь Вильсона–Коновалова, болезнь Вебера–Крисчена).
Патогенез НАСГ до конца не изучен. Существующая модель патогенеза НАСГ – теория «двух толчков» объединяет известные факторы риска стеатогепатита. При нарастании ожирения увеличивается поступление в печень свободных жирных кислот (СЖК) и развивается стеатоз печени – теория «первичного толчка». Во время этого процесса происходят реакции окисления СЖК и образуются продукты перекисного окисления липидов (ПОЛ) и реактивные формы кислорода (РФК) – оксидативный стресс – теория «второго толчка». Теория «второго толчка» несет ответственность за появление стеатогепатита, в связи с чем имеет более важное клиническое и прогностическое значение. Непосредственными факторами, вызывающими воспаление, считаются нарушенные функции внутриклеточных структур (митохондрий), а факторами, вызывающими гибель гепатоцитов и развитие фиброза – ПОЛ, секреция цитокинов [3,15].
Одной из возможных причин, способствующих развитию воспалительного компонента при НАСГ, является эндотоксемия, связанная с дисбиозом кишечника. Считается, что возникновение эндотоксемии при стеатогепатите характеризуется повышенной выработкой провоспалительных цитокинов (TNF–α, IL–6, IL–8) и повышенной экспрессией рецепторов к провоспалительным цитокинам.
Диагностика НАСГ у больных с дислипидемией принципиально важна в связи с тем, что назначение гиполипидемических препаратов при отсутствии объективной информации о клинических, функциональных и морфологических изменениях в печени увеличивает риск развития лекарственных поражений печени [11].
Клиническая картина,
методы диагностики
Как и в случаях многих хронических заболеваний печени другой этиологии, у большинства пациентов НАЖБП протекает бессимптомно. Вследствие этого НАСГ часто диагностируется благодаря выявлению патологических отклонений показателей крови при рутинном обследовании. Привлекают внимание и неспецифические клинические симптомы у этих больных (общая слабость, повышенная утомляемость и неопределенное ощущение дискомфорта в верхнем правом квадранте живота). По данным литературы, в 75% случаев при осмотре пациента с НАСГ выявляется гепатомегалия [3,15,17–19].
При лабораторном исследовании наиболее часто выявляется 2–3–кратное повышение активности АлАТ и АсАТ в сыворотке крови.
Повышение активности щелочной фосфатазы (ЩФ) и γ–глутамилтранспептидазы (ГГТП) до 2–3 норм при НАСГ также наблюдается достаточно часто.
Гипербилирубинемия, увеличение протромбинового времени и гипоальбуминемия имеют место лишь у некоторых больных.
Основные клинические, лабораторные и инструментальные признаки НАСГ приведены в таблице 4.
С целью ранней диагностики поражения печени у больных с атерогенной дислипидемией рекомендуется проведение комплексного клинико–лабораторного и инструментального обследования. При наличии гипертрансаминаземии до 2 норм и/или повышение ГГТП и ЩФ до 2–3 норм показано проведение пункционной биопсии печени.
Несмотря на несомненный риск при биопсии печени, целесообразность ее проведения бесспорна: во–первых, прогноз НАСГ зависит от выраженности гистологических изменений, а развитие цирроза сопровождается высокой опасностью нарастания печеночной недостаточности; во–вторых, при наличии существенных жировых изменений в печени оценка степени выраженности воспаления и фиброза с помощью ультразвукового метода ненадежна, а проведенение гиполипидемической терапии увеличивает риск развития лекарственных поражений.
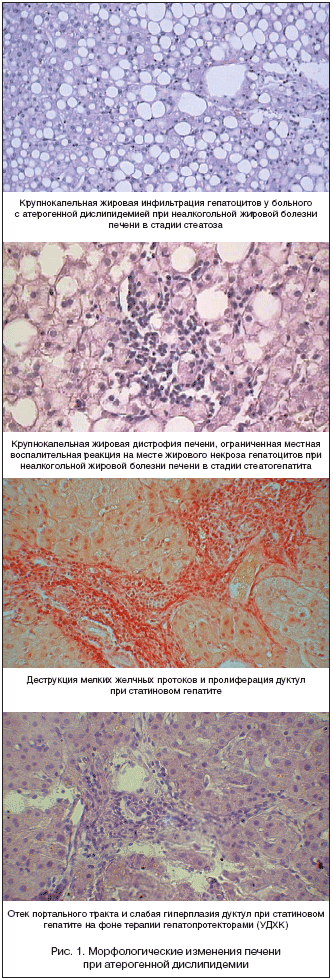
В таблице 5 и на рисунке 1 представлены морфологические характеристики поражения печени у больных с атерогенной дислипидемией.
Коррекция дислипидемии
Терапия дислипидемии включает немедикаментозные мероприятия по профилактике атеросклероза и медикаментозную терапию [1,2,4,5].
Немедикаментозные меры профилактики атеросклероза предусматривают диету (ограничение жиров животного происхождения), коррекцию массы тела, увеличение физической активности, прекращение курения. В проспективных исследованиях было показано, что комплексные меры по изменению образа жизни способствуют снижению смертности от ССЗ на 40%, что сопоставимо с эффективностью медикаментозной коррекции [13].
Медикаментозная терапия нарушений липидного обмена:
• Ингибиторы ГМК–КоА редуктазы (статины)
• Комбинированная терапия: статины + ингибитор абсорбции холестерина (эзетимиб), статины + фибраты
• Производные фиброевой кислоты (фибраты)
• Никотиновая кислота (ниацин)
• Секвестранты желчных кислот (ионно–обменные смолы)
• Омега–3 полиненасыщенные жирные кислоты
• Кишечные антисептики, пре– и пробиотики.
В настоящее время наиболее распространенными препаратами в лечении дислипидемии являются статины [14,16]. В рандомизированных клинических исследованиях была показана высокая эффективность статинов по снижению общего ХС и ХС ЛПНП: 4S, 1994; WOSCOP, 1995; CARE, 1996; Post–CABG, 1997; LIPID, 1998; AFCAPS/TexCAPS, 1998; HPS, 2002 г. В этих же исследованиях наблюдали снижение ССЗ, а в некоторых – общей смертности. В современных исследованиях с использованием аторвастатина и розувастатина была продемонстрирована возможность стабилизации (REVERSAL) и обратного развития (ASTEROID) атеросклеротических бляшек в коронарных артериях [14]. Традиционно статины считают безопасными препаратами, учитывая опыт применения у большого числа пациентов [6,7]. Тем не менее одним из побочных действий этой группы препаратов является повышение уровня трансаминаз (гепатотоксический эффект). В связи с этим статины противопоказаны при болезнях печени. Учитывая распространенность хронических заболеваний печени, можно предположить, что значительное число пациентов не сможет принимать статины, даже при наличии показаний к их применению и очевидном профилактическом эффекте. Кроме того, наличие самой атерогенной дислипидемии также приводит к изменениям функционального состояния печени [6,10,12]. Таким образом, терапия статинами должна применяться не только с учетом индивидуальной переносимости препаратов, но и с учетом стадии НАЖБП.
Больным с дислипидемией и НАЖБП в стадии стеатоза возможно использование препаратов из группы статинов (ловастатин, симвастатин, правастатин, аторвастатин, розувастатин, флувастатин). В настоящее время наиболее распространенными препаратами являются: ловастатин 20–40 мг в сутки, симвастатин 10–40 мг в сутки (максимальная доза до 80 мг), аторвастатин 10–40 мг в сутки (максимальная доза до 80 мг), флувастатин 40–80 мг в сутки. Наибольший гиполипидемический эффект наступает через 2–3 недели от начала лечения, следовательно, повышать дозу любого статина следует с интервалом в 2–3 недели [14]. Плейотропные эффекты статинов и результаты терапии по снижению сердечно–сосудистых осложнений начинают проявляться не ранее 6–9 месяцев от начала терапии. Необходимость длительной терапии диктует тщательный контроль уровня активности печеночных ферментов.
Для предотвращения проявления гепатотоксического эффекта статинов у больных с НАЖБП, целесообразно проводить курсы гепатопротективной терапии эссенциальными фосфолипидами и препаратами урсодезоксихолевой кислоты (УДКХ). Применение эссенциальных фосфолипидов (Эслидин®) курсами, по 2 капсулы 3 раза в сутки в течение 2 месяцев, 2–3 раза в год, способствует нормализации липидного спектра крови, показателей перекисного окисления липидов и системы антиоксидантной защиты. Длительное применение эссенциальных фосфолипидов предотвращает развитие фиброза печени и дальнейшее прогрессирование заболевания. Препаратом выбора среди гепатопротекторов группы эссенциальных фосфолипидов в настоящее время является Эслидин®.
Эссенциальные фосфолипиды (Эслидин®) – это незаменимые факторы для развития и функционирования клеток печени. Основная фракция эссенциальных фосфолипидов в препарате представлена фосфатидилхолином (73%), который является основным компонентом биологических мембран. Попадая в организм, фосфатидилхолин восстанавливает целостность мембран пораженных клеток печени и активирует расположенные в мембране фосфолипидзависимые ферменты, нормализуя тем самым проницаемость и усиливая дезинтоксикационный и экскреторный потенциал клеток печени. Метионин и эссенциальные фосфолипиды усиливают действие друг друга, являясь источником эндогенных и экзогенных фосфолипидов соответственно, улучшают функциональное состояние клеток печени и оказывают гепатопротекторный (защитный) эффект.
Входящий в состав Эслидина® метионин представляет собой незаменимую аминокислоту, которая является источником подвижных метильных групп. Метионин необходим для синтеза холина. Увеличение содержания холина способствует увеличению синтеза эндогенных фосфолипидов и уменьшению отложения нейтрального жира в печени. При атеросклерозе метионин снижает концентрацию холестерина и повышает концентрацию фосфолипидов в крови. Метионин также участвует в обмене серосодержащих аминокислот, в синтезе эпинефрина, креатинина и других биологически активных соединений, преобразует действие гормонов, витаминов (В12, аскорбиновой, фолиевой кислот), ферментов, белков, участвует в реакциях переметилирования, дезаминирования, декарбоксилирования. Таким образом, Эслидин® восстанавливает функцию печени, а также нормализует жировой, углеводный и белковый обмены веществ в организме.
Относительно использования препаратов УДКХ следует сказать, что они могут применяться не только как гепатопротекторы, но и использоваться в качестве альтернативной гиполипидемической терапии у больных с сопутствующей НАЖБП в стадии стеатогепатита (в стандартной дозировке 15 мг/кг). Широкий спектр применения препаратов УДХК основывается на многочисленных механизмах, обусловливающих разносторонность его действия [9,11,20]: УДХК не только изменяет липидный обмен, но и обладает прямым гепатопротективным, желчегонным, холелитолитическим и некоторым иммуномодулирующим действием. Обладая высокими полярными свойствами, УДХК образует нетоксичные смешанные мицеллы с аполярными (токсичными) желчными кислотами, что снижает способность желудочного рефлюктата повреждать клеточные мембраны при билиарном рефлюкс–гастрите и рефлюкс–эзофагите. Кроме того, УДХК образует двойные молекулы, способные включаться в состав клеточных мембран гепатоцитов, холангиоцитов, эпителиоцитов ЖКТ, стабилизировать их и делать невосприимчивыми к действию токсичных мицелл. Уменьшая концентрацию токсичных для гепатоцитов желчных кислот и стимулируя холерез, богатый бикарбонатами, УДХК эффективно способствует разрешению внутрипеченочного холестаза. Уменьшает насыщенность желчи холестерином за счет угнетения его абсорбции в кишечнике, подавления синтеза в печени и понижения секреции в желчь; повышает растворимость холестерина в желчи, образуя с ним жидкие кристаллы; уменьшает литогенный индекс желчи. Результатом является растворение холестериновых желчных камней и предупреждение образования новых конкрементов. Иммуномодулирующее действие обусловлено угнетением экспрессии антигенов HLA–1 на мембранах гепатоцитов и HLA–2 на холангиоцитах, нормализацией естественной киллерной активности лимфоцитов и др. Достоверно задерживает прогрессирование фиброза у больных первичным билиарным циррозом, муковисцидозом и алкогольным стеатогепатитом; уменьшает риск развития варикозного расширения вен пищевода. Также УДХК замедляет процессы преждевременного старения и гибели клеток (гепатоцитов, холангиоцитов). Минимальный курс терапии 3 месяца (2–3 раза в год) или длительно (в течение 6–12 месяцев).
Пациентам с НАЖБП в стадии стеатогепатита (гипертрансаминаземия до 3 норм), которые относятся к высокой категории риска развития атеросклероза и/или имеющим высокие уровни общего ХС и ХС ЛПНП, назначается комбинированная терапия: статин 20 мг + УДХК 15 мг/кг, курсом от 3 до 6 месяцев, до нормализации уровня трансаминаз. В последующем переходят на монотерапию статинами, контролируя уровень активности печеночных ферментов 1 раз в месяц. При необходимости проводят курсы гепатопротективной терапии эссенциальными фосфолипидами (Эссливер®) 2 капсулы 3 раза в сутки в течение 2–х месяцев, 2–3 раза в год, либо препаратами УДКХ в стандартной дозировке в течение 3–6 месяцев.
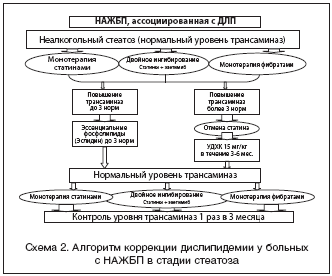
Возможные принципы коррекции дислипидемии у больных с НАЖБП представлены на схемах 2 и 3.
У многих пациентов при монотерапии статинами не удается достичь целевых уровней общего ХС и ХС ЛПНП, и у этих пациентов по–прежнему повышен риск развития ССЗ и их осложнений. Последние исследования характеризуются более агрессивным подходом к гиполипидемической терапии и основываются на принципе «чем ниже – тем лучше». Для решения этой проблемы раньше шли по пути увеличения дозы статина. Однако известно, что большую часть эффекта снижения статинами уровня ХС ЛПНП обеспечивает начальная доза, а повышение дозы любого статина увеличивает снижение уровня ХС ЛПНП примерно на 6% («правило 6»). Также увеличение дозы статина повышает риск развития побочных эффектов, в том числе и гипертрансаминаземию. Интенсификация терапии статинами сопровождается увеличением частоты токсических поражений печени. В частности, в исследовании TNT в группе пациентов, получавших 80 мг аторвастатина, в 6 раз чаще регистрировалось более чем 3–кратное повышение уровня трансаминаз по сравнению с группой больных, принимавших 10 мг препарата. Следует также отметить, что усиление гепатоксического эффекта статинов может быть связано с не диагностируемой НАЖБП.
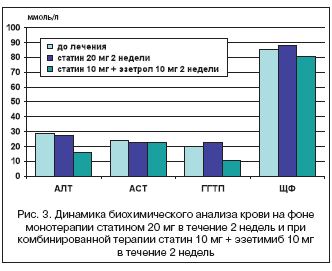
Современные положения лечения атерогенной ДЛП основываются на двойном ингибировании синтеза ХС и его абсорбции, применении селективного ингибитора кишечной абсорбции ХС – эзетимиба. Использование комбинации эзетимиб + статин увеличивает снижение уровня ХС ЛПНП на 40% (рис. 2), не вызывая повышения уровня трансаминаз (рис. 3). Поэтому у больных с высоким риском развития ССЗ для достижения целевых уровней ХС ЛПНП и снижения побочных эффектов наиболее перспективной и обеспечивающей высокую эффективность является комбинация статина (симгал 10 мг) с ингибитором абсорбции ХС (эзетимиб 10 мг). При проведении двойной терапии уже в течение 2–х недель удается достичь целевых значений ХС ЛПНП. Учитывая финансовую сторону вопроса, при достижении целевых уровней ХС ЛПНП возможен переход на поддерживающую терапию эзетимибом 10 мг через день. В настоящее время в продаже появился комбинированный препарат, одна таблетка которого содержит эзетемиб в дозе 10 мг и симвастатин в дозе 10, 20, 40 или 80 мг.
При изолированной гипертриглицеридемии предпочтительно назначение фибратов: фенофибрат 145 мг, при достижении целевых уровней ТГ переход на поддерживающую дозу – 145 мг через день.
С целью коррекции кишечной микрофлоры, учитывая патогенетические аспекты развития НАСГ, необходимо проводить санацию толстой кишки в течение 7–10 дней, с последующим назначением пробиотиков (Бифиформ комплекс по 2 капсулы утром, Пробифор по 25–30 доз 3 раза в сутки, Линекс 2 капсулы 3 раза в сутки, Бактистатин 1 капсула 2 раза в сутки) и пребиотиков (хилак–форте 40–60 капель три раза в сутки, Споробактерин 2–4 мл, Дюфалак в дозе 5–10 мл в сутки), длительность приема 3–4 недели.
Заключение
Неалкогольная жировая болезнь печени является основным фактором риска ССЗ. С целью ранней диагностики поражения печени у больных с атерогенной дислипидемией рекомендуется проведение комплексного клинико–инструментального обследования для уточнения стадии НАЖБП. Гиполипидемическую терапию следует проводить с учетом стадии НАЖБП в комплексе с гепатопротекторами. При НАЖБП в стадии стеатоза целесообразна комбинация гиполипидемической терапии с эссенциальными фосфолипидами (Эссливер®). При НАЖБП в стадии НАСГ необходимо сочетать прием препаратов, снижающих ХС, с препаратами УДХК. У больных с высоким уровнем гиперхолестеринемии для достижения целевых уровней ХС ЛПНП и снижения побочных эффектов лучшей является комбинация статинов с ингибитором абсорбции ХС. При изолированной гипертриглицеридемии препаратами выбора являются фибраты. В комплекс гиполипидемической терапии у больных с НАЖБП необходимо включать препараты, нормализующие кишечную микрофлору (кишечные антиспетики, пре– и пробиотики).




Литература
1. Аронов Д.М. Лечение и профилактика атеросклероза. //М.: Триада. – 2000. – 412 с.
2. Аронов Д.М. Каскад терапевтических эффектов статинов. //Кардиология. –2004. – 10: 85–92.
3. Богомолов П.О., Шульпекова Ю.О. Стеатоз печени и неалкогольный стеатогепатит. //В кн.: Болезни печени и желчевыводящих путей. Изд. 2–е. Под ред. В.Т.Ивашкина. – 2005; 205–16.
4. Диагностика и коррекция нарушений липидного обмена с целью профилактики и лечения атеросклероза. //Российские рекомендации, III пересмотр 2007. Кардиоваск. тер. и профилак. (Прил.).
5. Диагностика и лечение стабильной стенокардии. //Российские рекомендации, II пересмотр 2008. Кардиоваск. тер. и профилак. (Прил. 4).
6. Звенигородская Л.А., Лазебник Л.Б., Черкашова Е.А., Ефремов Л.И. Статиновый гепатит. //Трудный пациент. – 2009. – том 7. – № 4. – С. 44–49.
7. Исаков В.А. Статины и печень: друзья или враги? //Клин. гастроэнтерол. и гепатол. Рус. изд. – 2008. – 1 (5): 372–4.
8. Кардиология. Национальное руководство. //Под ред. Ю.Н. Беленкова, Р.Г.Оганова. М.: Геотар–Медиа, 2007. – 416 с.
9. Лазебник Л.Б., Ильченко Л.Ю., Голованова Е.В. Урсодезоксихолевая кислота. К 100–летию обнаружения. //Consilium medicum. – 2002.– №2.– С.10–14.
10. Лазебник Л.Б., Звенигородская Л.А., Морозов И.А., Шепелева С.Д. Клинико–морфологические изменения печени при атерогенной дислипидемии и при лечении статинами. //Тер. арх. – 2003. – 8: 51–5.
11. Лазебник Л.Б., Звенигородская Л.А. Метаболический синдром и органы пищеварения. //М.: Анахарсис. – 2009. – 184 с.
12. Лазебник Л.Б., Звенигородская Л.А., Мельникова Н.В., Егорова Е.Г., Хомерики С.Г. Атерогенная дислипидемия и инсулинорезистентность, ассоциированные с неалкогольной жировой болезнью печени (сходства и различия), дифференцированный подход к терапии. //Кардиоваскулярная терапия и профилактика. – 2009. – №3. – С. 69–77.
13. Мамедов М.Н. Школа по диагностике и лечению гиперлипидемии. //М.: Медиа Медика. – 2006; 4–7.
14. Оганов Р.Г., Аронов Д.М., Бубнова М.Г. Применение статинов – парадигма профилактики и лечения атеросклеротических заболеваний (фокус на аторвастатин). //Кардиоваск. тер. и профилак. – 2006. – 5 (6). – с. 95–107.
15. Подымова С.Д. Болезни печени. //М.: Медицина, 2005. – 768 с.
16. Руководство по атеросклерозу и ишемической болезни сердца. //Под ред. акад. РАН Е.И.Чазова, чл.–корр. РАМН В.В. Кухарчука, проф. С.А. Бойцова. М.: Медиа Медика, 2007.
17. Burt A.D., Mutton A., Day C.P. Diagnosis and interpretation of steatosis and steatohepatitis. //Semin Diagh Pathol. – 1998. – 4: 246–58.
18. Dixon J.B. et al. Nonalcoholic fatty liver disease: predictors of nonalcoholic steatohepatitis and liver fibrosis in the severely obese. // Gastroenterology. – 2001. – 121: 91–100.
19. Garcia–Monzon C. et al. A wider view of diagnostic criteria of nonalcoholic steatohepatitis. //Gastroenterology. – 2002. – 11: 560–5.
20. Hofmann A.F. Bile acid hepatotoxicity and the rationale of UDCA therapy in chronic cholestatic liver disease: some hypotheses. // Gastroenterology.– 1993.– Vol.75. – P. 22–26.












