Существуют различные классификации в зависимости от макроскопической картины, гистологического варианта, степени злокачественности опухоли и т.д. Наиболее широко распространенные классификации выделяют 2 основные группы опухолей – доброкачественные и злокачественные.
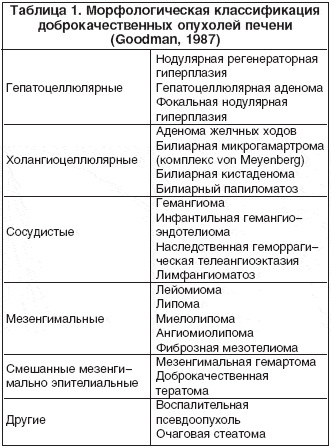
Классификация доброкачественных опухолей базируется на их морфологической дифференцировке (табл. 1).
Гистологическая классификация злокачественных опухолей печени учитывает следующие признаки: первичный или метастатический характер опухоли и ее гистологическое происхождение (табл. 2).
В 1978 г. Всемирная организация здравоохранения приняла классификацию гепацеллюлярных карцином, которая используется и сегодня (табл. 3). На основании оценки опухолевого роста гепатоцеллюлярные карциномы делятся на:
1. Инфильтративный тип (плохо отграниченный от прилежащих тканей).
2. Экспансивный тип (узлы, четко отграниченные от паренхимы):
- мононодулярные;
- мультинодулярные.
3. Смешанный тип.
В зависимости от степени дифференцировки выделяют: высокодифференцированные опухоли, умеренно, низко и недифференцированный рак.
Холангиоцеллюлярная карцинома макроскопически делится на: массивный, нодулярный и диффузный тип.
Морфологическая классификация холангиоцеллюлярных карцином включает следующие виды (табл. 4).
Морфологическая классификация опухолей является четкой, но она не всегда применима в повседневной клинической практике, особенно, когда речь идет о доброкачественных опухолях и о больных, находящихся в терминальном состоянии.
С развитием и усовершенствованием методов визуализации появляется возможность, еще на стадии обследования, отдифференцировать доброкачественную опухоль от злокачественной.
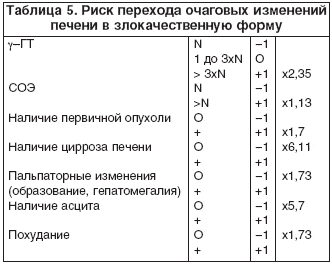
В 1989 г. Menu и соавт. предложили прогностический индекс злокачественной трансформации очаговых изменений печени, с целью сузить диагностический поиск и уменьшить количество дорогостоящих инвазивных методов исследования. Индекс выработан на базе обобщения результатов полученных от 394 больных с очаговыми поражениями печени. После селекции были выбраны 7 прогностически значимых показателей: g-ГТ, СОЭ, наличие первичной опухоли, цирроза печени, данные пальпации, асцит, похудание (табл. 5). Количественная оценка индекса варьирует от -0,05 до 38,85. Если индекс положительный, риск трансформации составляет более 50%.
Индекс Menu является очень доступным для определения риска злокачественной трансформации, так как использует широкодоступные клинические показатели, но имеет только ориентировочное значение, поскольку параметры, на основании которых он вычисляется, являются проявлением далеко зашедшего опухолевого процесса.
Для клиники особую актуальность имеет оценка прогноза злокачественных опухолей (в частности, первичных опухолей печени). Прогноз для больных с гепатоцеллюлярной карциномой зависит от ряда факторов: размера опухоли (< 2 см имеет лучший прогноз); количества очагов и степени злокачественности; возраста больного; наличия цирроза печени и степени тяжести поражения печени по системе Child- Pugh; стадии заболевания.
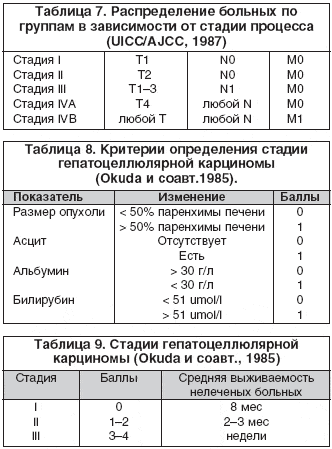
На сегодняшний день, множество критериев оценки стадии гепатоцеллюлярной карциномы объединены в системе ТNM (табл. 6 и 7). TNM-система четко отражает рост и распространение первичной опухоли, но она требует применения всего современного арсенала диагностических средств и ее тяжело использовать в ежедневной клинической практике.
Особенно важным для практического врача является определение стадии первичного рака печени на основе применения клинических показателей. Признаками, указывающими на неблагоприятный прогноз, являются: асцит, потеря массы тела, портальная гипертензия и повышение билирубина более 2 мг/дл. Okuda K. и соавт. в 1985 г. предложили при определении стадии заболевания руководствоваться следующими признаками: размерами опухоли, наличием асцита и изменениями показателей альбумина и билирубина (табл. 8 и 9).
I стадия – рак на начальных этапах развития, опухоль занимает менее 50% паренхимы печени, отсутствует асцит, умеренно снижен альбумин и повышен билирубин.
II стадия – опухоль в процессе развития, имеются 1 или 2 признака прогрессирования заболевания.
III стадия – далеко зашедший процесс, имеются 3 или все 4 из предлагаемых признаков.
Для определения величины опухоли определяют 2 размера при сцинтиграфии, компьютерной томографии, целиакографии. При отсутствии возможности проведения указанных исследований используют данные УЗИ брюшной полости. Объем опухоли представляется как процент объема всей печени.
Система Okuda позволяет достаточно быстро и четко определить клиническую стадию заболевания на базе доступных клинических признаков, отражающих как размер первичной опухоли, так и недостаточность функции печени. Это позволяет широко использовать данную систему в повседневной клинической практике, тем более, что имеются четкие корреляции между стадиями заболевания и выживаемостью больных.
В 1998 г. участники итальянской программы по изучению рака печени (The Cancer of the Liver Italian Program – CLIP) опубликовали оригинальную систему определения прогноза у больных с гепатоцеллюлярной карциномой. Система выработана на основе ретроспективного анализа данных, полученных от 435 больных в 16 больничных центрах Италии. Путем мультифакторного анализа были выбраны признаки, делающие наиболее весомый вклад в определение выживаемости больных: класс цирроза по системе Child-Pugh, морфологическая характеристика опухолей, увеличение a-фетопротеина и тромбоз воротной вены (табл. 10).
Система CLIP дает возможность распределить больных с гепатоцеллюлярной карциномой в 2 основные группы:
1. Больные со значительно более благоприятным прогнозом (0–1–2 балла), средняя выживаемость данной группы составляет от 42,5 до 16,5 мес.
2. Группа больных с гораздо менее благоприятным прогнозом (3–4–5–6 баллов), средняя выживаемость от 4,5 до 1 мес.
Приводим клинический пример: Больная Г., 65 лет, наблюдалась в клинике в течение года с жалобами на увеличение объема живота, боли ноющего характера в правом подреберье, общую слабость.
На основании данных анамнеза, осмотра, лабораторных и инструментальных методов обследования сформулирован клинический диагноз: цирроз печени вирусной этиологии С (HCV-RNA+, Ab+) класс С по Child-Pugh.
На основании наличия резистентного асцита, 4-кратного увеличения a-фетопротеина и данных УЗИ, указывающих на объемное образование, заподозрена гепатоцеллюлярная карцинома.
Оценка стадии заболевания по критериям Okuda:
• Размеры опухоли по данным
УЗИ (5,5х5,5 см) – < 50% паренхимы -
• Асцит +
• Альбумин 2,8 г% +
• Билирубин 4 мг% +
Установлено 3 положительных критерия, что отвечает III стадии заболевания – далеко зашедший процесс.
Определение выживаемости по системе CLIP
• Класс цирроза - С 2 балла
• Мононодулярное поражение < 50% 0 баллов
• a-фетопротеин 1 балл
• Тромбоз портальной вены отсутствует 0 баллов
Больная попадает в группу с плохим прогнозом – средняя выживаемость 4,5 мес.
Таким образом, современные системы классификации рака печени, базирующиеся на комплексной оценке клинических, инструментальных и морфологических показателей, полученных при обследовании больных, дают возможность с большой достоверностью определить стадию заболевания, перспективу выживаемости и оптимальную тактику ведения больного в каждом конкретном случае.






Литература
1. Okuda K. at all. Natural history of hepatocellular carcinoma and prognosis in relation to treatment. Study of 850 patients. Cancer, 56, 1985; 918–28.
2. Hermanec P., L.H. Sobin: UICC:TNM classification of malignant tumors. 4th ed. Berlin, Springer, 1987.
3. Goodman Z.D. Benign tumors of the liver.In.:Neoplasms of the Liver (Eds. K.Okuda, K.D. Ishak), Springer-Verlag , Tokyo, 1987; 105–25.
4. Sugihara S., M.Kojiro,Pathology of cholangiocarcinoma.In. :Neoplasms of the Liver (Eds. K.Okuda, K.D. Ishak), Springer-Verlag, Tokyo, 1987; 143–58.
5. G.Lux et al. Gastro-enterologie,Ed. Vigot Paris, 1995; 295.
6. Lawrence S. Friedman, Emmet B.Keeffe, Liver Disease, Ed. Edinburgh, London,1998; 361–71.
7. З. Кръстев, КАК в Гастроентерологията, Изд. Прудента, София, 1998; 327–37.
8. Yamasaki T. et.al., Clinicopathologic features of early hepatocellular сarcinoma. Hepatogastroenterology 1996; 43: 926–31.
9. Giuseppe Manghisi, Silvana Elba et al.(CLIP) , A New Prognostic System for Hepatocellular Carcinoma: A Retrospective Study of 435 Patients, Am J Hepatology; 1998; 28 (3) Sept.: 751–56.












