• –±–ї–Њ–Ї–∞–і–∞ –≤—Л—Е–Њ–і–∞ –Ї–∞–ї—М—Ж–Є—П –Є–Ј –≤–љ—Г—В—А–Є–Ї–ї–µ—В–Њ—З–љ—Л—Е –і–µ–њ–Њ –≥–ї–∞–і–Ї–Њ–є –Љ—Г—Б–Ї—Г–ї–∞—В—Г—А—Л (–Љ–µ–±–µ–≤–µ—А–Є–љ);
• –±–ї–Њ–Ї–∞–і–∞ –Ь–—Е–Њ–ї–Є–љ–Њ—А–µ—Ж–µ–њ—В–Њ—А–Њ–≤ –≥–ї–∞–і–Ї–Њ–Љ—Л—И–µ—З–љ–Њ–є –Ї–ї–µ—В–Ї–Є (–≥–Є–Њ—Б—Ж–Є–љ–∞ –±—Г—В–Є–ї–±—А–Њ–Љ–Є–і).
–§–Ф–≠ –њ—А–Є–љ–∞–і–ї–µ–ґ–Є—В –≤–∞–ґ–љ–∞—П —А–µ–≥—Г–ї–Є—А—Г—О—Й–∞—П —А–Њ–ї—М –≤ –њ—А–Њ—Ж–µ—Б—Б–µ –Љ—Л—И–µ—З–љ–Њ–≥–Њ —Б–Њ–Ї—А–∞—Й–µ–љ–Є—П. –Я–Њ—Б–Ї–Њ–ї—М–Ї—Г –§–Ф–≠ IV —В–Є–њ–∞ –њ—А–µ–і—Б—В–∞–≤–ї–µ–љ–∞ –≤ –≥–ї–∞–і–Ї–Њ–Љ—Л—И–µ—З–љ—Л—Е –Ї–ї–µ—В–Ї–∞—Е –њ–Њ –≤—Б–µ–є –і–ї–Є–љ–µ –Ї–Є—И–µ—З–љ–Є–Ї–∞, –ґ–µ–ї—З–µ– –Є –Љ–Њ—З–µ–≤—Л–≤–Њ–і—П—Й–Є—Е –њ—Г—В–µ–є, —В–Њ –µ–µ –±–ї–Њ–Ї–∞–і–∞ –і—А–Њ—В–∞–≤–µ—А–Є–љ–Њ–Љ –Њ–Ї–∞–Ј—Л–≤–∞–µ—В —Г–љ–Є–≤–µ—А—Б–∞–ї—М–љ–Њ–µ —Б–њ–∞–Ј–Љ–Њ–ї–Є—В–Є—З–µ—Б–Ї–Њ–µ –і–µ–є—Б—В–≤–Є–µ, –љ–µ–Ј–∞–≤–Є—Б–Є–Љ–Њ –Њ—В —Б—В–µ–њ–µ–љ–Є –Ї–Њ–љ—В—А–∞–Ї—Ж–Є–Є –Є–ї–Є –њ—А–Є—З–Є–љ—Л, –µ–µ –≤—Л–Ј–≤–∞–≤—И–µ–є.
–Ф—А–Њ—В–∞–≤–µ—А–Є–љ –≤ –Њ—В–ї–Є—З–Є–µ –Њ—В –≥–Є–Њ—Б—Ж–Є–љ–∞ –±—Г—В–Є–ї–±—А–Њ–Љ–Є–і–∞ –Є –і—А—Г–≥–Є—Е –Љ–Є–Њ—В—А–Њ–њ–љ—Л—Е —Б–њ–∞–Ј–Љ–Њ–ї–Є—В–Є–Ї–Њ–≤ –Њ–±–ї–∞–і–∞–µ—В –њ—А–Њ—В–Є–≤–Њ–Њ—В–µ—З–љ—Л–Љ –Є –∞–љ—В–Є–≤–Њ—Б–њ–∞–ї–Є—В–µ–ї—М–љ—Л–Љ —Н—Д—Д–µ–Ї—В–∞–Љ–Є. –Я–Њ–Ј–Є—В–Є–≤–љ—Л–µ —Д–∞—А–Љ–∞–Ї–Њ–і–Є–љ–∞–Љ–Є—З–µ—Б–Ї–Є–µ —Б–≤–Њ–є—Б—В–≤–∞ –ї–µ–ґ–∞—В –≤ –Њ—Б–љ–Њ–≤–µ –µ–≥–Њ –њ–∞—В–Њ–≥–µ–љ–µ—В–Є—З–µ—Б–Ї–Њ–≥–Њ –ї–µ—З–µ–±–љ–Њ–≥–Њ —Н—Д—Д–µ–Ї—В–∞ –Є —И–Є—А–Њ–Ї–Њ –Є—Б–њ–Њ–ї—М–Ј—Г—О—В—Б—П –љ–µ —В–Њ–ї—М–Ї–Њ –і–ї—П —Б–љ—П—В–Є—П –Њ—Б—В—А–Њ–≥–Њ —Б–њ–∞—Б—В–Є—З–µ—Б–Ї–Њ–≥–Њ —Б–Є–љ–і—А–Њ–Љ–∞, –љ–Њ –Є –њ—А–Є –Њ–±–µ—Б–њ–µ—З–µ–љ–Є–Є –і–ї–Є—В–µ–ї—М–љ–Њ–є —Д–∞—А–Љ–∞–Ї–Њ—В–µ—А–∞–њ–Є–Є —Е—А–Њ–љ–Є—З–µ—Б–Ї–Є—Е –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є–є –Ї–Є—И–µ—З–љ–Є–Ї–∞ —Б–Њ —Б–њ–∞—Б—В–Є—З–µ—Б–Ї–Є–Љ —Б–Є–љ–і—А–Њ–Љ–Њ–Љ, —Б–Њ–њ—А–Њ–≤–Њ–ґ–і–∞—О—Й–Є–Љ—Б—П –Ї–Њ–ї–Є–Ї–Њ–Њ–±—А–∞–Ј–љ—Л–Љ–Є –Є–ї–Є —А–∞—Б–њ–Є—А–∞—О—Й–Є–Љ–Є –±–Њ–ї—П–Љ–Є. –Ю—В—Б—Г—В—Б—В–≤–Є–µ –∞–љ—В–Є—Е–Њ–ї–Є–љ–µ—А–≥–Є—З–µ—Б–Ї–Њ–є –∞–Ї—В–Є–≤–љ–Њ—Б—В–Є –њ–Њ–ї–Њ–ґ–Є—В–µ–ї—М–љ—Л–Љ –Њ–±—А–∞–Ј–Њ–Љ —Б–Ї–∞–Ј—Л–≤–∞–µ—В—Б—П –љ–∞ –њ–µ—А–µ–љ–Њ—Б–Є–Љ–Њ—Б—В–Є –і—А–Њ—В–∞–≤–µ—А–Є–љ–∞, –≤ —В–Њ–Љ —З–Є—Б–ї–µ –Є –њ—А–Є —Б–Њ–њ—Г—В—Б—В–≤—Г—О—Й–µ–є –њ–∞—В–Њ–ї–Њ–≥–Є–Є –Є —Б–Њ–≤–Љ–µ—Б—В–љ–Њ–Љ –њ—А–Є–µ–Љ–µ —Б –і—А—Г–≥–Є–Љ–Є –њ—А–µ–њ–∞—А–∞—В–∞–Љ–Є [2].
–Я–Є–Ї –Ї–Њ–љ—Ж–µ–љ—В—А–∞—Ж–Є–Є –і—А–Њ—В–∞–≤–µ—А–Є–љ–∞ –≤ –њ–ї–∞–Ј–Љ–µ –њ—А–Є –њ—А–Є–µ–Љ–µ –≤–љ—Г—В—А—М –љ–∞–±–ї—О–і–∞–µ—В—Б—П –≤ —В–µ—З–µ–љ–Є–µ 45 –Љ–Є–љ, —З—В–Њ —Е–∞—А–∞–Ї—В–µ—А–Є–Ј—Г–µ—В –µ–≥–Њ –Ї–∞–Ї –±—Л—Б—В—А–Њ –≤—Б–∞—Б—Л–≤–∞—О—Й–Є–є—Б—П —Д–∞—А–Љ–∞–Ї–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є–є –∞–≥–µ–љ—В. –Я–Њ—Б–ї–µ –Њ–і–љ–Њ–Ї—А–∞—В–љ–Њ–≥–Њ –њ–µ—А–Њ—А–∞–ї—М–љ–Њ–≥–Њ –њ—А–Є–µ–Љ–∞ 80 –Љ–≥ –Љ–∞–Ї—Б–Є–Љ–∞–ї—М–љ–∞—П –Ї–Њ–љ—Ж–µ–љ—В—А–∞—Ж–Є—П –≤ –њ–ї–∞–Ј–Љ–µ –Є—Б—Е–Њ–і–љ–Њ–≥–Њ —Б–Њ–µ–і–Є–љ–µ–љ–Є—П (136–320 –љ–≥/–Љ–ї) –і–Њ—Б—В–Є–≥–∞–µ—В—Б—П —З–µ—А–µ–Ј 2 —З. –С–Є–Њ–і–Њ—Б—В—Г–њ–љ–Њ—Б—В—М –і—А–Њ—В–∞–≤–µ—А–Є–љ–∞ –њ—А–Є –њ—А–Є–µ–Љ–µ –≤–љ—Г—В—А—М —Б–Њ—Б—В–∞–≤–ї—П–µ—В 60%. –Я—А–µ–њ–∞—А–∞—В —Е–Њ—А–Њ—И–Њ –њ—А–Њ–љ–Є–Ї–∞–µ—В –≤ —А–∞–Ј–ї–Є—З–љ—Л–µ —В–Ї–∞–љ–Є: –¶–Э–°, –ґ–Є—А–Њ–≤—Г—О —В–Ї–∞–љ—М, –Љ–Є–Њ–Ї–∞—А–і, –ї–µ–≥–Ї–Є–µ, –њ–Њ—З–Ї–Є, –њ–µ—З–µ–љ—М, —Б—В–µ–љ–Ї—Г –Љ–Њ—З–µ–≤–Њ–≥–Њ –Є –ґ–µ–ї—З–љ–Њ–≥–Њ –њ—Г–Ј—Л—А—П, –Ї–Є—И–Ї–Є, —Б–Њ—Б—Г–і–Є—Б—В—Г—О —Б—В–µ–љ–Ї—Г. –Ь–µ—В–∞–±–Њ–ї–Є–Ј–Є—А—Г–µ—В—Б—П (–Њ–Ї–Є—Б–ї—П–µ—В—Б—П) –њ–Њ—З—В–Є –њ–Њ–ї–љ–Њ—Б—В—М—О –і–Њ –Љ–Њ–љ–Њ—Д–µ–љ–Њ–ї—М–љ—Л—Е —Б–Њ–µ–і–Є–љ–µ–љ–Є–є, –Љ–µ—В–∞–±–Њ–ї–Є—В—Л –±—Л—Б—В—А–Њ –Ї–Њ–љ—К—О–≥–Є—А—Г—О—В—Б—П —Б –≥–ї—О–Ї—Г—А–Њ–љ–Њ–≤–Њ–є –Ї–Є—Б–ї–Њ—В–Њ–є. –Я–µ—А–Є–Њ–і –њ–Њ–ї—Г–≤—Л–≤–µ–і–µ–љ–Є—П —Б–Њ—Б—В–∞–≤–ї—П–µ—В 16 —З. –Ю–Ї–Њ–ї–Њ 60% –і—А–Њ—В–∞–≤–µ—А–Є–љ–∞ –њ—А–Є –њ–µ—А–Њ—А–∞–ї—М–љ–Њ–Љ –њ—А–Є–µ–Љ–µ –≤—Л–і–µ–ї—П–µ—В—Б—П —З–µ—А–µ–Ј –Ї–Є—И–µ—З–љ–Є–Ї –Є –і–Њ 25% – —Б –Љ–Њ—З–Њ–є [3].
–С–ї–Њ–Ї–∞–і–∞ –≤—Л—Е–Њ–і–∞ –Ї–∞–ї—М—Ж–Є—П –Є–Ј –≤–љ—Г—В—А–Є–Ї–ї–µ—В–Њ—З–љ—Л—Е –і–µ–њ–Њ –≥–ї–∞–і–Ї–Њ–є –Љ—Г—Б–Ї—Г–ї–∞—В—Г—А—Л. –Ф–µ–є—Б—В–≤–Є–µ –њ—А–µ–њ–∞—А–∞—В–Њ–≤ —Н—В–Њ–є –≥—А—Г–њ–њ—Л –Њ—Б–љ–Њ–≤—Л–≤–∞–µ—В—Б—П –љ–∞ –љ–∞—А—Г—И–µ–љ–Є–Є –њ–µ—А–≤–Њ–≥–Њ —Н—В–∞–њ–∞ –њ—А–Њ—Ж–µ—Б—Б–∞ —Б–Њ–Ї—А–∞—Й–µ–љ–Є—П – –і–µ–њ–Њ–ї—П—А–Є–Ј–∞—Ж–Є–Є –Љ–µ–Љ–±—А–∞–љ—Л –≥–ї–∞–і–Ї–Њ–Љ—Л—И–µ—З–љ—Л—Е –Ї–ї–µ—В–Њ–Ї. –Э–∞–Є–±–Њ–ї–µ–µ –Є–Ј–≤–µ—Б—В–љ—Л–є –њ—А–µ–њ–∞—А–∞—В —Б —Н—В–Є–Љ –Љ–µ—Е–∞–љ–Є–Ј–Љ–Њ–Љ –і–µ–є—Б—В–≤–Є—П – –Љ–µ–±–µ–≤–µ—А–Є–љ. –Ю–љ —Б–≤—П–Ј—Л–≤–∞–µ—В—Б—П —Б –Љ–Њ–ї–µ–Ї—Г–ї—П—А–љ—Л–Љ–Є —Б—В—А—Г–Ї—В—Г—А–∞–Љ–Є –љ–∞—В—А–Є–µ–≤—Л—Е –Ї–∞–љ–∞–ї–Њ–≤, –љ–µ –Ј–∞—В—А–∞–≥–Є–≤–∞—П —Е–Њ–ї–Є–љ–Њ—А–µ—Ж–µ–њ—В–Њ—А. –Ъ —В–Њ–Љ—Г –ґ–µ –њ—А–µ–њ–∞—А–∞—В —Г–Љ–µ–љ—М—И–∞–µ—В –Њ—В—В–Њ–Ї –Є–Њ–љ–Є–Ј–Є—А–Њ–≤–∞–љ–љ–Њ–≥–Њ –Ї–∞–ї–Є—П –Є–Ј –Ї–ї–µ—В–Ї–Є, –њ–Њ—Н—В–Њ–Љ—Г —Г—Б—В—А–∞–љ—П–µ—В —Б–њ–∞–Ј–Љ, –љ–µ –≤—Л–Ј—Л–≤–∞—П –≥–Є–њ–Њ—В–Њ–љ–Є–Є —В–Њ–ї—Б—В–Њ–є –Ї–Є—И–Ї–Є [4]. –•–Њ—А–Њ—И–Њ –∞–±—Б–Њ—А–±–Є—А—Г—П—Б—М –≤ –Ї–Є—И–µ—З–љ–Є–Ї–µ, –∞–Ї—В–Є–≤–љ–Њ –Љ–µ—В–∞–±–Њ–ї–Є–Ј–Є—А—Г–µ—В—Б—П –њ—А–Є –њ—А–Њ—Е–Њ–ґ–і–µ–љ–Є–Є —З–µ—А–µ–Ј —Б—В–µ–љ–Ї—Г –Ї–Є—И–Ї–Є –Є –њ–µ—З–µ–љ—М. –Ь–µ—В–∞–±–Њ–ї–Є—В—Л –њ—А–µ–њ–∞—А–∞—В–∞ –≤—Л–≤–Њ–і—П—В—Б—П —Б –Љ–Њ—З–Њ–є.
–Ю–і–љ–∞ –Є–Ј —Б—В–∞—А–µ–є—И–Є—Е –≥—А—Г–њ–њ –ї–µ–Ї–∞—А—Б—В–≤–µ–љ–љ—Л—Е —Б—А–µ–і—Б—В–≤ – –±–ї–Њ–Ї–∞—В–Њ—А—Л –Ь–—Е–Њ–ї–Є–љ–Њ—А–µ—Ж–µ–њ—В–Њ—А–Њ–≤ –≤ —А–∞–Ј–ї–Є—З–љ—Л—Е –Њ—В–і–µ–ї–∞—Е –ґ–µ–ї—Г–і–Њ—З–љ–Њ––Ї–Є—И–µ—З–љ–Њ–≥–Њ —В—А–∞–Ї—В–∞ [5]. –С–µ–Ј–Њ–њ–∞—Б–љ–Њ—Б—В—М —В–µ—А–∞–њ–Є–Є –Ь–—Е–Њ–ї–Є–љ–Њ–ї–Є—В–Є–Ї–∞–Љ–Є —Г–≤–µ–ї–Є—З–Є–ї–∞—Б—М —Б —Б–Њ–Ј–і–∞–љ–Є–µ–Љ –≥–Є–Њ—Б—Ж–Є–љ–∞ –±—Г—В–Є–ї–±—А–Њ–Љ–Є–і–∞, –Ї–Њ—В–Њ—А—Л–є –љ–∞–Ї–∞–њ–ї–Є–≤–∞–µ—В—Б—П –≤ –≥–ї–∞–і–Ї–Њ–є –Љ—Г—Б–Ї—Г–ї–∞—В—Г—А–µ –ґ–µ–ї—Г–і–Њ—З–љ–Њ––Ї–Є—И–µ—З–љ–Њ–≥–Њ —В—А–∞–Ї—В–∞, –≤—Л–≤–Њ–і–Є—В—Б—П –Є–Ј –Њ—А–≥–∞–љ–Є–Ј–Љ–∞ –≤ –љ–µ–Є–Ј–Љ–µ–љ–µ–љ–љ–Њ–Љ –≤–Є–і–µ –њ–Њ—З–Ї–∞–Љ–Є. –Я—А–µ–њ–∞—А–∞—В –њ—А–Є–Љ–µ–љ—П–µ—В—Б—П –њ—А–Є –±–Њ–ї—П—Е –≤ –ґ–Є–≤–Њ—В–µ, –Њ–±—Г—Б–ї–Њ–≤–ї–µ–љ–љ—Л—Е —Б–њ–∞–Ј–Љ–Њ–Љ, –Є –Є–Љ–µ–µ—В –і–Њ—Б—В–∞—В–Њ—З–љ–Њ —Б–µ–ї–µ–Ї—В–Є–≤–љ–Њ–µ –і–µ–є—Б—В–≤–Є–µ, –Љ–Њ–ґ–µ—В –≤—Л–Ј—Л–≤–∞—В—М —В–Є–њ–Є—З–љ—Л–µ –і–ї—П –Ь–—Е–Њ–ї–Є–љ–Њ–ї–Є—В–Є–Ї–Њ–≤ –њ–Њ–±–Њ—З–љ—Л–µ —Н—Д—Д–µ–Ї—В—Л (–њ–Њ —Б—А–∞–≤–љ–µ–љ–Є—О —Б –њ–ї–∞—Ж–µ–±–Њ –љ–∞ 4% —З–∞—Й–µ).
–Т—Л–±–Њ—А –Љ–Є–Њ—В—А–Њ–њ–љ–Њ–≥–Њ —Б–њ–∞–Ј–Љ–Њ–ї–Є—В–Є–Ї–∞ –≤ –њ–Њ—Б–ї–µ–і–љ–µ–µ –≤—А–µ–Љ—П –Њ—Б–љ–Њ–≤—Л–≤–∞–µ—В—Б—П –љ–µ —В–Њ–ї—М–Ї–Њ –љ–∞ –µ–≥–Њ —Д–∞—А–Љ–∞–Ї–Њ–і–Є–љ–∞–Љ–Є–Ї–µ, –љ–Њ –Є –љ–∞ —Б—В–Њ–Є–Љ–Њ—Б—В–Є. –Ъ —Б–Њ–ґ–∞–ї–µ–љ–Є—О, –њ–Њ–љ—П—В–Є–µ —Г—В–Є–ї–Є—В–∞—А–љ–Њ–є —Б—В–Њ–Є–Љ–Њ—Б—В–Є –Њ—З–µ–љ—М –њ—А–Њ—З–љ–Њ –≤–Њ—И–ї–Њ –≤–Њ –≤—А–∞—З–µ–±–љ–Њ–µ –Љ–Є—А–Њ–≤–Њ–Ј–Ј—А–µ–љ–Є–µ (—Б—А–∞–≤–љ–µ–љ–Є–µ —Б—В–Њ–Є–Љ–Њ—Б—В–µ–є —Г–њ–∞–Ї–Њ–≤–Њ–Ї —А–∞–Ј–ї–Є—З–љ—Л—Е –њ—А–µ–њ–∞—А–∞—В–Њ–≤) –Є —З–∞—Б—В–Њ —П–≤–ї—П–µ—В—Б—П –µ–і–Є–љ—Б—В–≤–µ–љ–љ—Л–Љ –∞—А–≥—Г–Љ–µ–љ—В–Њ–Љ –і–ї—П –њ—А–Є–љ—П—В–Є—П —А–µ—И–µ–љ–Є—П –Њ –њ—А–Є–Љ–µ–љ–µ–љ–Є–Є –ї–µ–Ї–∞—А—Б—В–≤–µ–љ–љ–Њ–≥–Њ —Б—А–µ–і—Б—В–≤–∞. –≠—В–Њ –і–∞–ї–µ–Ї–Њ –љ–µ –≤—Б–µ–≥–і–∞ –≤–µ—А–љ–Њ, –њ–Њ—Б–Ї–Њ–ї—М–Ї—Г —Д–∞—А–Љ–∞–Ї–Њ—Н–Ї–Њ–љ–Њ–Љ–Є–Ї–∞ –Њ—Ж–µ–љ–Є–≤–∞–µ—В —Б—В–Њ–Є–Љ–Њ—Б—В—М –њ–Њ–ї—Г—З–µ–љ–љ–Њ–≥–Њ —А–µ–Ј—Г–ї—М—В–∞—В–∞, —В–Њ–ї—М–Ї–Њ —В–∞–Ї–Є–Љ –њ—Г—В–µ–Љ –≤–Њ–Ј–Љ–Њ–ґ–љ–Њ –њ–Њ–ї—Г—З–µ–љ–Є–µ —А–µ–∞–ї—М–љ—Л—Е –і–∞–љ–љ—Л—Е –Њ–± —Н–Ї–Њ–љ–Њ–Љ–Є—З–љ–Њ—Б—В–Є —В–Њ–≥–Њ –Є–ї–Є –Є–љ–Њ–≥–Њ –Љ–µ—В–Њ–і–∞ –ї–µ—З–µ–љ–Є—П. –Х—Б–ї–Є –Ј–∞—В—А–∞—В—Л –љ–∞ –і–Њ—Б—В–Є–ґ–µ–љ–Є–µ —А–µ–Ј—Г–ї—М—В–∞—В–∞ –њ—А–Є —Б—А–∞–≤–љ–µ–љ–Є–Є –і–≤—Г—Е —А–∞–Ј–ї–Є—З–љ—Л—Е –њ—А–µ–њ–∞—А–∞—В–Њ–≤ –Љ–µ–љ—М—И–µ —Г –Ї–∞–Ї–Њ–≥–Њ––ї–Є–±–Њ –Є–Ј –љ–Є—Е, —Г—В–Є–ї–Є—В–∞—А–љ—Л–µ —Б—В–Њ–Є–Љ–Њ—Б—В–Є –ї–µ–Ї–∞—А—Б—В–≤ –Љ–Њ–≥—Г—В –љ–µ –Є–Љ–µ—В—М –Ј–љ–∞—З–µ–љ–Є—П –і–ї—П –њ—А–µ–і–њ–Њ—З—В–µ–љ–Є—П —А–µ–ґ–Є–Љ–∞ —Д–∞—А–Љ–∞–Ї–Њ—В–µ—А–∞–њ–Є–Є.
–Ю–њ—В–Є–Љ–∞–ї—М–љ–Њ–є –Љ–Њ–і–µ–ї—М—О –і–ї—П –Њ–њ—А–µ–і–µ–ї–µ–љ–Є—П –Ј–∞—В—А–∞—В –њ–Њ —Г—Б—В—А–∞–љ–µ–љ–Є—О –∞–±–і–Њ–Љ–Є–љ–∞–ї—М–љ—Л—Е –±–Њ–ї–µ–є —Б–њ–∞—Б—В–Є—З–µ—Б–Ї–Њ–≥–Њ –≥–µ–љ–µ–Ј–∞ —П–≤–ї—П–µ—В—Б—П –°–†–Ъ. –Ф–Њ –љ–∞—Б—В–Њ—П—Й–µ–≥–Њ –≤—А–µ–Љ–µ–љ–Є —Н–Ї–Њ–љ–Њ–Љ–Є—З–µ—Б–Ї–Є–µ —А–∞—Б—З–µ—В—Л –њ–Њ —Н—В–Њ–є —В–µ–Љ–∞—В–Є–Ї–µ –љ–µ –њ—А–Њ–Є–Ј–≤–Њ–і–Є–ї–Є—Б—М. –Ґ–µ–Љ –љ–µ –Љ–µ–љ–µ–µ –њ–Њ–і–Њ–±–љ—Л–є –∞–љ–∞–ї–Є–Ј –њ—А–µ–і—Б—В–∞–≤–ї—П–µ—В—Б—П –≤–µ—Б—М–Љ–∞ –∞–Ї—В—Г–∞–ї—М–љ—Л–Љ –Ї–∞–Ї –і–ї—П –њ—А–∞–Ї—В–Є—З–µ—Б–Ї–Њ–≥–Њ –Ј–і—А–∞–≤–Њ–Њ—Е—А–∞–љ–µ–љ–Є—П, —В–∞–Ї –Є —Б–Њ–±—Б—В–≤–µ–љ–љ–Њ –і–ї—П –±–Њ–ї—М–љ–Њ–≥–Њ, –Ї–Њ—В–Њ—А—Л–є –љ–µ–Ї–Њ—В–Њ—А—Л–µ –њ—А–µ–њ–∞—А–∞—В—Л, –љ–∞–њ—А–Є–Љ–µ—А –і—А–Њ—В–∞–≤–µ—А–Є–љ, –Љ–Њ–ґ–µ—В –њ—А–Є–Њ–±—А–µ—В–∞—В—М —Б–∞–Љ–Њ—Б—В–Њ—П—В–µ–ї—М–љ–Њ –±–µ–Ј —А–µ—Ж–µ–њ—В–∞.
–¶–µ–ї—М—О —Н–Ї—Б–њ–µ—А—В–Є–Ј—Л –±—Л–ї–Њ —Б—А–∞–≤–љ–Є—В—М –Ї–ї–Є–љ–Є–Ї–Њ–—Н–Ї–Њ–љ–Њ–Љ–Є—З–µ—Б–Ї–Є–µ —Е–∞—А–∞–Ї—В–µ—А–Є—Б—В–Є–Ї–Є –Њ—Б–љ–Њ–≤–љ—Л—Е –Њ—А–Є–≥–Є–љ–∞–ї—М–љ—Л—Е –Љ–Є–Њ—В—А–Њ–њ–љ—Л—Е —Б–њ–∞–Ј–Љ–Њ–ї–Є—В–Є–Ї–Њ–≤ – –і—А–Њ—В–∞–≤–µ—А–Є–љ–∞, –Љ–µ–±–µ–≤–µ—А–Є–љ–∞ –Є –≥–Є–Њ—Б—Ж–Є–љ–∞ –±—Г—В–Є–ї–±—А–Њ–Љ–Є–і–∞.
–Ь–∞—В–µ—А–Є–∞–ї—Л –Є –Љ–µ—В–Њ–і—Л
–†–µ—В—А–Њ—Б–њ–µ–Ї—В–Є–≤–љ—Л–є –∞–љ–∞–ї–Є–Ј –Є—Б—В–Њ—А–Є–є –±–Њ–ї–µ–Ј–љ–Є 120 –±–Њ–ї—М–љ—Л—Е, –ї–µ—З–Є–≤—И–Є—Е—Б—П –≤ –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Њ–є –±–Њ–ї—М–љ–Є—Ж–µ –≥. –≠–ї–µ–Ї—В—А–Њ—Б—В–∞–ї–Є —Б –і–Є–∞–≥–љ–Њ–Ј–Њ–Љ «–°–Є–љ–і—А–Њ–Љ —А–∞–Ј–і—А–∞–ґ–µ–љ–љ–Њ–є –Ї–Є—И–Ї–Є, —Б–Љ–µ—И–∞–љ–љ–∞—П —Д–Њ—А–Љ–∞ —Б –њ—А–µ–Њ–±–ї–∞–і–∞–љ–Є–µ–Љ –±–Њ–ї–µ–є» –≤ —В–µ—З–µ–љ–Є–µ –Є—О–ї—П 2009 – –Љ–∞—А—В–∞ 2010 –≥., –њ—А–Њ–≤–µ–і–µ–љ —Б–Њ–≥–ї–∞—Б–љ–Њ —Б–ї–µ–і—Г—О—Й–Є–Љ –Ї—А–Є—В–µ—А–Є—П–Љ –≤–Ї–ї—О—З–µ–љ–Є—П:
• –±–Њ–ї—М–љ—Л–µ —Б –°–†–Ъ, —Б–Њ–њ—А–Њ–≤–Њ–ґ–і–∞—О—Й–Є–Љ—Б—П —Б–њ–∞—Б—В–Є—З–µ—Б–Ї–Є–Љ–Є –±–Њ–ї—П–Љ–Є –≤ –ґ–Є–≤–Њ—В–µ;
• –≤–Њ–Ј—А–∞—Б—В – —Б—В–∞—А—И–µ 14 –ї–µ—В;
–Є –Є—Б–Ї–ї—О—З–µ–љ–Є—П:
• –Ј–ї–Њ–Ї–∞—З–µ—Б—В–≤–µ–љ–љ—Л–µ –љ–Њ–≤–Њ–Њ–±—А–∞–Ј–Њ–≤–∞–љ–Є—П –ї—О–±–Њ–є –ї–Њ–Ї–∞–ї–Є–Ј–∞—Ж–Є–Є;
• –±–µ—А–µ–Љ–µ–љ–љ–Њ—Б—В—М –Є –њ–µ—А–Є–Њ–і –ї–∞–Ї—В–∞—Ж–Є–Є;
• —В—П–ґ–µ–ї–Њ–µ —Б–Њ—Б—В–Њ—П–љ–Є–µ –±–Њ–ї—М–љ–Њ–≥–Њ.
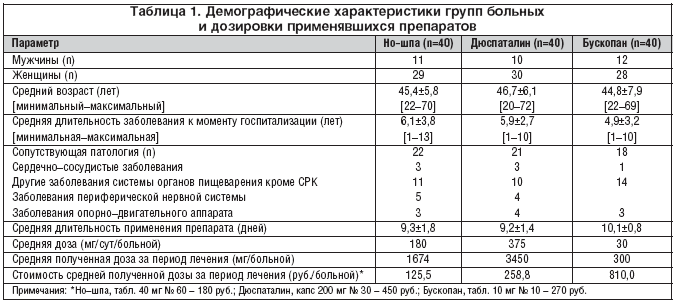
–Ю—В–Њ–±—А–∞–љ–љ—Л–µ –Є—Б—В–Њ—А–Є–Є –±–Њ–ї–µ–Ј–љ–Є –±—Л–ї–Є —А–∞–Ј–і–µ–ї–µ–љ—Л –љ–∞ —В—А–Є –≥—А—Г–њ–њ—Л –≤ –Ј–∞–≤–Є—Б–Є–Љ–Њ—Б—В–Є –Њ—В –Љ–Є–Њ—В—А–Њ–њ–љ–Њ–≥–Њ —Б–њ–∞–Ј–Љ–Њ–ї–Є—В–Є–Ї–∞, –њ—А–Є–Љ–µ–љ—П–≤—И–µ–≥–Њ—Б—П –њ—А–Є –±–Њ–ї–µ–≤–Њ–Љ –∞–±–і–Њ–Љ–Є–љ–∞–ї—М–љ–Њ–Љ —Б–Є–љ–і—А–Њ–Љ–µ, –≤—Л–Ј–≤–∞–љ–љ–Њ–Љ —Б–њ–∞–Ј–Љ–Њ–Љ –Ї–Є—И–Ї–Є. –Я–µ—А–≤—Г—О –≥—А—Г–њ–њ—Г –≤ 40 —З–µ–ї. —Б–Њ—Б—В–∞–≤–Є–ї–Є –±–Њ–ї—М–љ—Л–µ, –њ–Њ–ї—Г—З–∞–≤—И–Є–µ –і—А–Њ—В–∞–≤–µ—А–Є–љ (–Э–Њ–—И–њ–∞, —В–∞–±–ї–µ—В–Ї–Є 40 –Љ–≥, –°–∞–љ–Њ—Д–Є––Р–≤–µ–љ—В–Є—Б), –≤—В–Њ—А—Г—О – 40 —З–µ–ї., –њ–Њ–ї—Г—З–Є–≤—И–Є–µ –Љ–µ–±–µ–≤–µ—А–Є–љ (–Ф—О—Б–њ–∞—В–∞–ї–Є–љ, –Ї–∞–њ—Б—Г–ї—Л 200 –Љ–≥, –°–Њ–ї–≤–µ–є —Д–∞—А–Љ–∞), —В—А–µ—В—М—О – 40 —З–µ–ї., –ї–µ—З–Є–≤—И–Є–µ—Б—П –≥–Є–Њ—Б—Ж–Є–љ–∞ –±—Г—В–Є–ї–±—А–Њ–Љ–Є–і–Њ–Љ (–С—Г—Б–Ї–Њ–њ–∞–љ, —В–∞–±–ї–µ—В–Ї–Є 10 –Љ–≥, –С–µ—А–Є–љ–≥–µ—А –Ш–љ–≥–µ–ї—М—Е–∞–є–Љ). –У—А—Г–њ–њ—Л –љ–µ —А–∞–Ј–ї–Є—З–∞–ї–Є—Б—М –њ–Њ –њ–Њ–ї–Њ–≤–Њ–Ј—А–∞—Б—В–љ–Њ–Љ—Г —Б–Њ—Б—В–∞–≤—Г, –і–ї–Є—В–µ–ї—М–љ–Њ—Б—В–Є –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П –Ї –Љ–Њ–Љ–µ–љ—В—Г –љ–∞—З–∞–ї–∞ —Д–∞—А–Љ–∞–Ї–Њ—В–µ—А–∞–њ–Є–Є (—В–∞–±–ї. 1). –С–Њ–ї—М–љ—Л–µ –њ–Њ–ї—Г—З–∞–ї–Є –≤—Л—И–µ–њ–µ—А–µ—З–Є—Б–ї–µ–љ–љ—Л–µ –Љ–Є–Њ—В—А–Њ–њ–љ—Л–µ —Б–њ–∞–Ј–Љ–Њ–ї–Є—В–Є–Ї–Є –≤ –і–Њ–Ј–∞—Е, –Њ–±–µ—Б–њ–µ—З–Є–≤–∞–≤—И–Є—Е –њ–Њ–ї–Њ–ґ–Є—В–µ–ї—М–љ—Г—О –і–Є–љ–∞–Љ–Є–Ї—Г —Б–њ–∞—Б—В–Є—З–µ—Б–Ї–Њ–≥–Њ –Є –±–Њ–ї–µ–≤–Њ–≥–Њ —Б–Є–љ–і—А–Њ–Љ–∞. –°—А–µ–і–љ–Є–µ —Б—Г—В–Њ—З–љ—Л–µ –і–Њ–Ј—Л –Є –і–Њ–Ј—Л, —Б—Г–Љ–Љ–∞—А–љ–Њ –њ–Њ–ї—Г—З–µ–љ–љ—Л–µ –≤ –њ–µ—А–µ—Б—З–µ—В–µ –љ–∞ –Њ–і–љ–Њ–≥–Њ –±–Њ–ї—М–љ–Њ–≥–Њ –Ї –Њ–Ї–Њ–љ—З–∞–љ–Є—О —Б—А–Њ–Ї–∞ –љ–∞–±–ї—О–і–µ–љ–Є—П, –њ—А–µ–і—Б—В–∞–≤–ї–µ–љ—Л –≤ —В–∞–±–ї–Є—Ж–µ 1.
–Я–Њ –Ј–∞–њ–Є—Б—П–Љ –≤ –Є—Б—В–Њ—А–Є–Є –±–Њ–ї–µ–Ј–љ–Є –Њ—Ж–µ–љ–Є–≤–∞–ї–Є—Б—М —Б–ї–µ–і—Г—О—Й–Є–µ –њ–∞—А–∞–Љ–µ—В—А—Л —Б —Г—З–µ—В–Њ–Љ —Д–Њ—А–Љ–∞–ї–Є–Ј–∞—Ж–Є–Є –Є—Е –≤—Л—А–∞–ґ–µ–љ–љ–Њ—Б—В–Є.
–С–Њ–ї–µ–Ј–љ–µ–љ–љ–Њ—Б—В—М –њ—А–Є –њ–∞–ї—М–њ–∞—Ж–Є–Є –ґ–Є–≤–Њ—В–∞
–Э–µ—В 1
—Б–ї–∞–±–∞—П 2
—Б—А–µ–і–љ–µ–є –Є–љ—В–µ–љ—Б–Є–≤–љ–Њ—Б—В–Є 3
–≤—Л—А–∞–ґ–µ–љ–љ–∞—П 4
–С–Њ–ї–µ–Ј–љ–µ–љ–љ–Њ—Б—В—М –њ—А–Є –њ–∞–ї—М–њ–∞—Ж–Є–Є –ґ–Є–≤–Њ—В–∞
–Э–µ—В 1
–Ы–Њ–Ї–∞–ї—М–љ–∞—П 2
–†–∞–Ј–ї–Є—В–∞—П 3
–°–Є–Љ–њ—В–Њ–Љ—Л –≤–Ј–і—Г—В–Є—П –ґ–Є–≤–Њ—В–∞
–Ю—В—Б—Г—В—Б—В–≤—Г—О—В 1
–Ь–∞–ї–Њ–≤—Л—А–∞–ґ–µ–љ–љ—Л–µ 2
–Т—Л—А–∞–ґ–µ–љ–љ—Л–µ 3
–§–Є–Ј–Є–Ї–∞–ї—М–љ—Л–µ –њ—А–Є–Ј–љ–∞–Ї–Є —Б–њ–∞–Ј–Љ–∞ –Ї–Є—И–µ—З–љ–Є–Ї–∞
–Э–µ—В 1
–°–ї–∞–±–Њ–≤—Л—А–∞–ґ–µ–љ–љ—Л–µ 2
–Т—Л—А–∞–ґ–µ–љ–љ—Л–µ 3
–°–Є–Љ–њ—В–Њ–Љ—Л –љ–∞—А—Г—И–µ–љ–Є—П –Љ–Њ—В–Њ—А–Є–Ї–Є
–Э–µ—В 1
–°–ї–∞–±–Њ–≤—Л—А–∞–ґ–µ–љ–љ—Л–µ 2
–Т—Л—А–∞–ґ–µ–љ–љ—Л–µ 3
–°—Г–Љ–Љ–∞ –±–∞–ї–ї–Њ–≤ –њ—А–Є–Ј–љ–∞–Ї–Њ–≤ –њ—А–µ–і—Б—В–∞–≤–ї–µ–љ–∞ –≤ –≤–Є–і–µ –Њ–±—Й–µ–Ї–ї–Є–љ–Є—З–µ—Б–Ї–Њ–≥–Њ —Б—З–µ—В–∞ (–Ю–Ъ–°), –і–Є–љ–∞–Љ–Є–Ї–∞ –Ї–Њ—В–Њ—А–Њ–≥–Њ –Њ—Ж–µ–љ–Є–≤–∞–ї–∞—Б—М –Њ—В –љ–∞—З–∞–ї–∞ –ї–µ—З–µ–љ–Є—П –і–Њ –њ—А–Є–µ–Љ–∞ —Б–њ–∞–Ј–Љ–Њ–ї–Є—В–Є–Ї–Њ–≤ –Є –≤ —В–Њ—З–Ї–∞—Е «24 —З–∞—Б–∞ —Б –Љ–Њ–Љ–µ–љ—В–∞ –љ–∞—З–∞–ї–∞ —Д–∞—А–Љ–∞–Ї–Њ—В–µ—А–∞–њ–Є–Є», «3 –і–љ—П», «7 –і–љ–µ–є», «–њ—А–Є –≤—Л–њ–Є—Б–Ї–µ –Є–Ј —Б—В–∞—Ж–Є–Њ–љ–∞—А–∞».
–Т—Б–µ –±–Њ–ї—М–љ—Л–µ –њ–Њ–ї—Г—З–∞–ї–Є —Б–Њ–њ—Г—В—Б—В–≤—Г—О—Й—Г—О –і–Є–µ—В–Њ—В–µ—А–∞–њ–Є—О –Є —Д–∞—А–Љ–∞–Ї–Њ—В–µ—А–∞–њ–Є—О, –Є—Б–Ї–ї—О—З–∞–≤—И—Г—О –Є–љ—Л–µ —Б–њ–∞–Ј–Љ–Њ–ї–Є—В–Є–Ї–Є, –Ї—А–Њ–Љ–µ –њ—А–Њ–∞–љ–∞–ї–Є–Ј–Є—А–Њ–≤–∞–љ—Л—Е –≤ –і–∞–љ–љ–Њ–є —Н–Ї—Б–њ–µ—А—В–Є–Ј–µ.
–Т –Ї–∞—З–µ—Б—В–≤–µ —Д–∞—А–Љ–∞–Ї–Њ—Н–Ї–Њ–љ–Њ–Љ–Є—З–µ—Б–Ї–Є—Е –Љ–µ—В–Њ–і–Њ–≤ –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–ї–Є—Б—М –Њ–±—Й–µ–њ—А–Є–љ—П—В—Л–µ: –∞–љ–∞–ї–Є–Ј «—Б—В–Њ–Є–Љ–Њ—Б—В—М–—Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В—М» (–≤ —Б–ї—Г—З–∞–µ —А–∞–≤–љ—Л—Е —А–µ–Ј—Г–ї—М—В–∞—В–Њ–≤ –њ–Њ –Ю–Ъ–°) –Є –∞–љ–∞–ї–Є–Ј «–Љ–Є–љ–Є–Љ–Є–Ј–∞—Ж–Є–Є —Б—В–Њ–Є–Љ–Њ—Б—В–Є» (–≤ —Б–ї—Г—З–∞–µ —А–∞–Ј–ї–Є—З–Є—П —А–µ–Ј—Г–ї—М—В–∞—В–Њ–≤ –њ–Њ –Ю–Ъ–°) [5]. –Ю—Ж–µ–љ–Є–≤–∞–ї–Є—Б—М –њ—А—П–Љ—Л–µ —А–∞—Б—Е–Њ–і—Л –љ–∞ –Э–Њ–—И–њ—Г, –Ф—О—Б–њ–∞—В–∞–ї–Є–љ –Є –С—Г—Б–Ї–Њ–њ–∞–љ, —Б—В–Њ–Є–Љ–Њ—Б—В—М —Г–њ–∞–Ї–Њ–≤–Њ–Ї –Ї–Њ—В–Њ—А—Л—Е –Њ–њ—А–µ–і–µ–ї–µ–љ–∞ –Ї–∞–Ї —Б—А–µ–і–љ–µ–≤–Ј–≤–µ—И–µ–љ–љ–∞—П –∞–њ—В–µ—З–љ—Л—Е —Ж–µ–љ –њ–Њ –≥. –Ь–Њ—Б–Ї–≤–µ –љ–∞ –Ї–Њ–љ–µ—Ж –∞–њ—А–µ–ї—П 2010 –≥. [6].
–†–µ–Ј—Г–ї—М—В–∞—В—Л –Њ–±—А–∞–±–Њ—В–∞–љ—Л —Б—В–∞–љ–і–∞—А—В–љ—Л–Љ–Є —Б—В–∞—В–Є—Б—В–Є—З–µ—Б–Ї–Є–Љ–Є –Љ–µ—В–Њ–і–∞–Љ–Є —Б –њ–Њ–Љ–Њ—Й—М—О –њ–∞–Ї–µ—В–∞ –њ—А–Є–Ї–ї–∞–і–љ—Л—Е –њ—А–Њ–≥—А–∞–Љ–Љ Microsoft Excel.
–†–µ–Ј—Г–ї—М—В–∞—В—Л –Є –Њ–±—Б—Г–ґ–і–µ–љ–Є–µ
–Я–Њ–ї–Њ–≤–Њ–Ј—А–∞—Б—В–љ—Л—Е —А–∞–Ј–ї–Є—З–Є–є –Љ–µ–ґ–і—Г –≥—А—Г–њ–њ–∞–Љ–Є –±–Њ–ї—М–љ—Л—Е –љ–µ –≤—Л—П–≤–ї–µ–љ–Њ (—В–∞–±–ї. 1), –≤–Њ –≤—Б–µ—Е –≥—А—Г–њ–њ–∞—Е –њ—А–µ–Њ–±–ї–∞–і–∞–ї–Є –ґ–µ–љ—Й–Є–љ—Л, —З—В–Њ —Б–Њ–Њ—В–≤–µ—В—Б—В–≤—Г–µ—В –Њ–±—Й–Є–Љ —Б—В–∞—В–Є—Б—В–Є—З–µ—Б–Ї–Є–Љ –і–∞–љ–љ—Л–Љ –њ–Њ —А–∞—Б–њ—А–Њ—Б—В—А–∞–љ–µ–љ–љ–Њ—Б—В–Є –і–∞–љ–љ–Њ–є –њ–∞—В–Њ–ї–Њ–≥–Є–Є [7]. –Т —Ж–µ–ї–Њ–Љ –≤–Њ–Ј—А–∞—Б—В –±–Њ–ї—М–љ—Л—Е –±—Л–ї –љ–Є–ґ–µ 50––ї–µ—В–љ–µ–≥–Њ –≥–Њ—А–Є–Ј–Њ–љ—В–∞, —З—В–Њ –њ–Њ–і—В–≤–µ—А–ґ–і–∞–µ—В –і–∞–љ–љ—Л–µ –Њ –њ–Њ—А–∞–ґ–µ–љ–Є–Є —Н—В–Є–Љ –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є–µ–Љ —В—А—Г–і–Њ—Б–њ–Њ—Б–Њ–±–љ–Њ–є —З–∞—Б—В–Є –љ–∞—Б–µ–ї–µ–љ–Є—П [8], —Е–Њ—В—П –Є –≤—Б—В—А–µ—З–∞–ї–Њ—Б—М –љ–µ–±–Њ–ї—М—И–Њ–µ –Ї–Њ–ї–Є—З–µ—Б—В–≤–Њ –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б—В–∞—А—И–Є—Е –≤–Њ–Ј—А–∞—Б—В–љ—Л—Е –≥—А—Г–њ–њ. –Т —Б—А–µ–і–љ–µ–Љ –і–ї–Є—В–µ–ї—М–љ–Њ—Б—В—М –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П –Ї –Љ–Њ–Љ–µ–љ—В—Г —А–∞—Б—Б–Љ–∞—В—А–Є–≤–∞–µ–Љ–Њ–≥–Њ –Ї—Г—А—Б–∞ —Д–∞—А–Љ–∞–Ї–Њ—В–µ—А–∞–њ–Є–Є —Б–Њ—Б—В–∞–≤–Є–ї–∞ 5–6 –ї–µ—В, –њ—А–Є—З–µ–Љ –≤ –≥—А—Г–њ–њ–µ –±–Њ–ї—М–љ—Л—Е, –њ–Њ–ї—Г—З–∞–≤—И–Є—Е –Э–Њ–—И–њ—Г, —З–∞—Й–µ –≤—Б—В—А–µ—З–∞–ї–Є—Б—М –ї–Є—Ж–∞ —Б –±–Њ–ї–µ–µ –і–ї–Є—В–µ–ї—М–љ—Л–Љ –∞–љ–∞–Љ–љ–µ–Ј–Њ–Љ –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П –Є –±–Њ–ї–µ–µ —В—П–ґ–µ–ї—Л–Љ–Є —Д–Њ—А–Љ–∞–Љ–Є, —З–µ–Љ –≤ –Њ—Б—В–∞–ї—М–љ—Л—Е (–љ–∞ 4 —З–µ–ї–Њ–≤–µ–Ї–∞ –±–Њ–ї—М—И–µ, —З–µ–Љ –≤ –≥—А—Г–њ–њ–µ –Ф—О—Б–њ–∞—В–∞–ї–Є–љ–∞, –Є –љ–∞ 5 –±–Њ–ї—М—И–µ, —З–µ–Љ –≤ –≥—А—Г–њ–њ–µ –С—Г—Б–Ї–Њ–њ–∞–љ–∞). –°–Њ–њ—Г—В—Б—В–≤—Г—О—Й–∞—П –њ–∞—В–Њ–ї–Њ–≥–Є—П –Ј–∞—Д–Є–Ї—Б–Є—А–Њ–≤–∞–љ–∞ —Г –њ–Њ–ї–Њ–≤–Є–љ—Л –±–Њ–ї—М–љ—Л—Е –≤ –Ї–∞–ґ–і–Њ–є –≥—А—Г–њ–њ–µ. –Т –Њ—Б–љ–Њ–≤–љ–Њ–Љ —Н—В–Њ –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П —Б–Є—Б—В–µ–Љ—Л –Њ—А–≥–∞–љ–Њ–≤ –њ–Є—Й–µ–≤–∞—А–µ–љ–Є—П, –Њ—В–ї–Є—З–љ—Л–µ –Њ—В –°–†–Ъ – —Е—А–Њ–љ–Є—З–µ—Б–Ї–Є–є –≥–∞—Б—В—А–Є—В, –≥–∞—Б—В—А–Њ—Н–Ј–Њ—Д–∞–≥–µ–∞–ї—М–љ–Њ–—А–µ—Д–ї—О–Ї—Б–љ–∞—П –±–Њ–ї–µ–Ј–љ—М, —Е—А–Њ–љ–Є—З–µ—Б–Ї–Є–є —Е–Њ–ї–µ—Ж–Є—Б—В–Є—В –Є –і—А. –Т—Б–µ —Н—В–Є –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П –љ–∞—Е–Њ–і–Є–ї–Є—Б—М –≤ —Б—В–∞–і–Є–Є —А–µ–Љ–Є—Б—Б–Є–Є –Ї –Љ–Њ–Љ–µ–љ—В—Г –≥–Њ—Б–њ–Є—В–∞–ї–Є–Ј–∞—Ж–Є–Є –њ–Њ –Њ—Б–љ–Њ–≤–љ–Њ–є –љ–Њ–Ј–Њ–ї–Њ–≥–Є–Є.
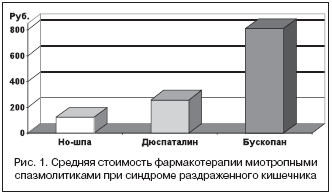
–Ф–ї–Є—В–µ–ї—М–љ–Њ—Б—В—М –њ—А–Є–Љ–µ–љ–µ–љ–Є—П –Э–Њ–—И–њ—Л –Є –Ф—О—Б–њ–∞—В–∞–ї–Є–љ–∞ –і–Њ —Б—В–Є—Е–∞–љ–Є—П –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є—Е –њ—А–Є–Ј–љ–∞–Ї–Њ–≤ –Њ–±–Њ—Б—В—А–µ–љ–Є—П –±—Л–ї–∞ –Њ–і–Є–љ–∞–Ї–Њ–≤–∞ –Є —Б–Њ—Б—В–∞–≤–Є–ї–∞ –≤ —Б—А–µ–і–љ–µ–Љ 9 –і–љ–µ–є, –њ—А–Є –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є–Є –С—Г—Б–Ї–Њ–њ–∞–љ–∞ –Є–Љ–µ–ї–∞—Б—М —В–µ–љ–і–µ–љ—Ж–Є—П –Ї —Г–≤–µ–ї–Є—З–µ–љ–Є—О —Б—А–Њ–Ї–Њ–≤ –њ—А–Є–Љ–µ–љ–µ–љ–Є—П –і–Њ 10 –і–љ–µ–є, —Е–Њ—В—П —А–∞–Ј–ї–Є—З–Є—П –Є –љ–µ –±—Л–ї–Є —Б—В–∞—В–Є—Б—В–Є—З–µ—Б–Ї–Є –і–Њ—Б—В–Њ–≤–µ—А–љ—Л. –°—А–µ–і–љ–µ—Б—Г—В–Њ—З–љ—Л–µ –і–Њ–Ј—Л –њ—А–µ–њ–∞—А–∞—В–Њ–≤ –љ–∞—Е–Њ–і–Є–ї–Є—Б—М –≤ –њ—А–µ–і–µ–ї–∞—Е —Б—А–µ–і–љ–µ—В–µ—А–∞–њ–µ–≤—В–Є—З–µ—Б–Ї–Є—Е. –° —Г—З–µ—В–Њ–Љ —Б—В–Њ–Є–Љ–Њ—Б—В–Є –≤—Б–µ–≥–Њ –њ–µ—А–Є–Њ–і–∞ —Д–∞—А–Љ–∞–Ї–Њ—В–µ—А–∞–њ–Є–Є —Б–њ–∞–Ј–Љ–Њ–ї–Є—В–Є–Ї–∞–Љ–Є –љ–µ—Б–Њ–Љ–љ–µ–љ–љ—Л–µ —Н–Ї–Њ–љ–Њ–Љ–Є—З–µ—Б–Ї–Є–µ –њ—А–µ–Є–Љ—Г—Й–µ—Б—В–≤–∞ –і–∞–ґ–µ –њ–Њ —Г—В–Є–ї–Є—В–∞—А–љ–Њ–є —Б—В–Њ–Є–Љ–Њ—Б—В–Є –Є–Љ–µ–µ—В –Э–Њ–—И–њ–∞, –ї–µ—З–µ–љ–Є–µ –Ї–Њ—В–Њ—А–Њ–є —Б—В–Њ–Є–ї–Њ –љ–∞ 51,5% –Љ–µ–љ—М—И–µ, —З–µ–Љ –Ф—О—Б–њ–∞—В–∞–ї–Є–љ–Њ–Љ, –Є –≤ 6,45 —А–∞–Ј–∞ –љ–Є–ґ–µ, —З–µ–Љ –С—Г—Б–Ї–Њ–њ–∞–љ–Њ–Љ (—А–Є—Б. 1).
–Ґ–∞–Ї–Є–Љ –Њ–±—А–∞–Ј–Њ–Љ, —Г—В–Є–ї–Є—В–∞—А–љ–∞—П —Б—В–Њ–Є–Љ–Њ—Б—В—М (–±–µ–Ј —Г—З–µ—В–∞ –і–Є–љ–∞–Љ–Є–Ї–Є —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В–Є) –і–љ—П –ї–µ—З–µ–љ–Є—П –Э–Њ–—И–њ–Њ–є –Ј–љ–∞—З–Є—В–µ–ї—М–љ–Њ –Љ–µ–љ—М—И–µ, —З–µ–Љ –Ф—О—Б–њ–∞—В–∞–ї–Є–љ–Њ–Љ –Є–ї–Є –С—Г—Б–Ї–Њ–њ–∞–љ–Њ–Љ.
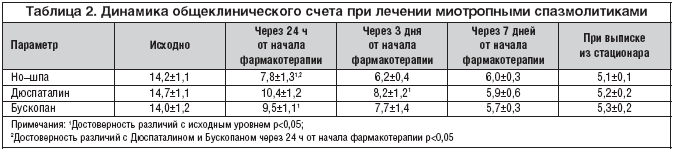
–Ф–ї—П –Њ—Ж–µ–љ–Ї–Є —Н–Ї–Њ–љ–Њ–Љ–Є—З–µ—Б–Ї–Њ–є —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В–Є –њ—А–Њ–Є–Ј–≤–µ–і–µ–љ –њ–Њ–і—Б—З–µ—В —Б—В–Њ–Є–Љ–Њ—Б—В–Є —Б —Г—З–µ—В–Њ–Љ –Ю–Ъ–° (—В–∞–±–ї. 2). –Ш—Б—Е–Њ–і–љ—Л–є –Ю–Ъ–° –њ–Њ –≥—А—Г–њ–њ–∞–Љ –і–Њ—Б—В–Њ–≤–µ—А–љ–Њ –љ–µ —А–∞–Ј–ї–Є—З–∞–ї—Б—П, —З—В–Њ –њ–Њ–Ј–≤–Њ–ї–Є–ї–Њ —Б–і–µ–ї–∞—В—М –≤—Л–≤–Њ–і –Њ–± –Њ–і–љ–Њ—А–Њ–і–љ–Њ—Б—В–Є –≥—А—Г–њ–њ. –Я–Њ –Љ–µ—А–µ –Њ—Б—Г—Й–µ—Б—В–≤–ї–µ–љ–Є—П —Д–∞—А–Љ–∞–Ї–Њ—В–µ—А–∞–њ–Є–Є –Ю–Ъ–° –Ј–∞–Ї–Њ–љ–Њ–Љ–µ—А–љ–Њ —Б–љ–Є–ґ–∞–ї—Б—П, –Є –њ—А–Є –≤—Л–њ–Є—Б–Ї–µ –Є–Ј —Б—В–∞—Ж–Є–Њ–љ–∞—А–∞ –Њ–љ –±—Л–ї –Љ–Є–љ–Є–Љ–∞–ї—М–љ—Л–Љ, —З—В–Њ —Б–Њ–Њ—В–≤–µ—В—Б—В–≤–Њ–≤–∞–ї–Њ –њ–Њ–ї–љ–Њ–Љ—Г —Б—В–Є—Е–∞–љ–Є—О —Б–Є–Љ–њ—В–Њ–Љ–∞—В–Є–Ї–Є. –Ю–і–љ–∞–Ї–Њ –µ—Б–ї–Є –і–Є–љ–∞–Љ–Є–Ї–∞ —Г–Љ–µ–љ—М—И–µ–љ–Є—П –Њ–±—К–µ–Ї—В–Є–≤–љ—Л—Е –њ–∞—В–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є—Е –њ—А–Є–Ј–љ–∞–Ї–Њ–≤ –њ—А–Є –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є–Є –Э–Њ–—И–њ—Л –Є –С—Г—Б–Ї–Њ–њ–∞–љ–∞ –±—Л–ї–∞ —Б—Е–Њ–і–љ–Њ–є –Є –і–Њ—Б—В–Њ–≤–µ—А–љ–Њ –Њ –њ–Њ–ї–Њ–ґ–Є—В–µ–ї—М–љ–Њ–є –і–Є–љ–∞–Љ–Є–Ї–µ –Љ–Њ–ґ–љ–Њ –±—Л–ї–Њ —Б—Г–і–Є—В—М —Г–ґ–µ —З–µ—А–µ–Ј 24 —З, —В–Њ —Б—Г—Й–µ—Б—В–≤–µ–љ–љ–Њ–µ —Г–ї—Г—З—И–µ–љ–Є–µ –њ—А–Є –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є–Є –Ф—О—Б–њ–∞—В–∞–ї–Є–љ–∞ –Ј–∞—Д–Є–Ї—Б–Є—А–Њ–≤–∞–љ–Њ –њ–Њ–Ј–ґ–µ – —З–µ—А–µ–Ј 3 –і–љ—П –Њ—В –љ–∞—З–∞–ї–∞ —В–µ—А–∞–њ–Є–Є. –Т–Љ–µ—Б—В–µ —Б —В–µ–Љ –Ю–Ъ–° –і–ї—П –Э–Њ–—И–њ—Л –њ–Њ —В–Њ—З–Ї–µ «—З–µ—А–µ–Ј 24 —З –Њ—В –љ–∞—З–∞–ї–∞ —Д–∞—А–Љ–∞–Ї–Њ—В–µ—А–∞–њ–Є–Є» –±—Л–ї –і–Њ—Б—В–Њ–≤–µ—А–љ–Њ –Љ–µ–љ—М—И–µ, —З–µ–Љ —Г –Ф—О—Б–њ–∞—В–∞–ї–Є–љ–∞ –Є –С—Г—Б–Ї–Њ–њ–∞–љ–∞. –Ф–ї—П –Ї–∞–ґ–і–Њ–є —В–Њ—З–Ї–Є –љ–∞–±–ї—О–і–µ–љ–Є—П —Н–Ї–Њ–љ–Њ–Љ–Є—З–µ—Б–Ї–Є–є –∞–љ–∞–ї–Є–Ј –≤—Л–њ–Њ–ї–љ–µ–љ —Б–ї–µ–і—Г—О—Й–Є–Љ –Њ–±—А–∞–Ј–Њ–Љ: –°–Х–Р – –і–ї—П —В–Њ—З–Ї–Є «24 —З», –°–Ь–Р – –і–ї—П –≤—Б–µ—Е –Њ—Б—В–∞–ї—М–љ—Л—Е (—В–∞–±–ї. 3).
–Я–Њ–і—Б—З–µ—В –і–ї—П —В–Њ—З–Ї–Є «24 —З» –њ—А–Њ–Є–Ј–≤–µ–і–µ–љ –њ–Њ —Д–Њ—А–Љ—Г–ї–µ:
CER = —Б—В–Њ–Є–Љ–Њ—Б—В—М –і–љ—П –њ—А–Є–Љ–µ–љ–µ–љ–Є—П –Љ–Є–Њ—В—А–Њ–њ–љ–Њ–≥–Њ —Б–њ–∞–Ј–Љ–Њ–ї–Є—В–Є–Ї–∞ / Δ–Ю–Ъ–° –љ–∞ —Н—В–Њ—В –і–µ–љ—М –њ–Њ —Б—А–∞–≤–љ–µ–љ–Є—О —Б –Є—Б—Е–Њ–і–љ—Л–Љ –≤ %,
–≥–і–µ CER – –њ–∞—А–∞–Љ–µ—В—А «—Б—В–Њ–Є–Љ–Њ—Б—В—М–—Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В—М»
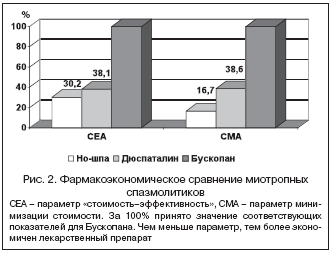
–Я–∞—А–∞–Љ–µ—В—А CER, –Њ—В—А–∞–ґ–∞—О—Й–Є–є —Б—В–Њ–Є–Љ–Њ—Б—В—М 1% –і–Њ—Б—В–Є–≥–љ—Г—В–Њ–є —З–µ—А–µ–Ј 24 —З —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В–Є, –±—Л–ї –љ–∞–Є–Љ–µ–љ—М—И–Є–Љ –њ—А–Є –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є–Є –Э–Њ–—И–њ—Л –Є –љ–∞–Є–±–Њ–ї—М—И–Є–Љ – –њ—А–Є –њ—А–Є–Љ–µ–љ–µ–љ–Є–Є –С—Г—Б–Ї–Њ–њ–∞–љ–∞. –£—З–Є—В—Л–≤–∞—П –і–Њ—Б—В–Є–ґ–µ–љ–Є–µ —А–∞–≤–љ–Њ–є —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В–Є –њ–Њ –Ю–Ъ–° –њ–Њ—Б–ї–µ 3 —Б—Г—В. –ї–µ—З–µ–љ–Є—П, –њ—А–Њ–≤–µ–і–µ–љ –∞–љ–∞–ї–Є–Ј «–Љ–Є–љ–Є–Љ–Є–Ј–∞—Ж–Є–Є —Б—В–Њ–Є–Љ–Њ—Б—В–Є», –њ—А–µ–і—Г—Б–Љ–∞—В—А–Є–≤–∞—О—Й–Є–є –Њ–њ—А–µ–і–µ–ї–µ–љ–Є–µ —Б—В–Њ–Є–Љ–Њ—Б—В–Є –Љ–Є–Њ—В—А–Њ–њ–љ—Л—Е —Б–њ–∞–Ј–Љ–Њ–ї–Є—В–Є–Ї–Њ–≤ –њ–Њ—Б–ї–µ–і–Њ–≤–∞—В–µ–ї—М–љ–Њ –Ј–∞ 3 –і–љ—П, –Ј–∞ 7 –і–љ–µ–є –Є –њ–Њ –Њ–Ї–Њ–љ—З–∞–љ–Є–Є –ї–µ—З–µ–љ–Є—П. –Ю–і–Є–љ–∞–Ї–Њ–≤–∞—П —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В—М –і–Њ—Б—В–Є–≥–∞–µ—В—Б—П –Ј–∞ —Б—З–µ—В —А–∞–Ј–ї–Є—З–љ—Л—Е –Ј–∞—В—А–∞—В –љ–∞ —Д–∞—А–Љ–∞–Ї–Њ—В–µ—А–∞–њ–Є—О, –Ї–Њ—В–Њ—А—Л–µ –±—Л–ї–Є –Љ–µ–љ—М—И–µ –њ—А–Є –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є–Є –Э–Њ–—И–њ—Л –≤ —Б—А–∞–≤–љ–µ–љ–Є–Є —Б –Ф—О—Б–њ–∞—В–∞–ї–Є–љ–Њ–Љ –Є –С—Г—Б–Ї–Њ–њ–∞–љ–Њ–Љ (–љ–∞ 52% –Є 83,3% —Б–Њ–Њ—В–≤–µ—В—Б—В–≤–µ–љ–љ–Њ) (—А–Є—Б. 2).
–Х—Б–ї–Є —Б—А–µ–і—Б—В–≤–∞, –Њ—В–њ—Г—Й–µ–љ–љ—Л–µ –љ–∞ –ї–µ—З–µ–љ–Є–µ 100 –±–Њ–ї—М–љ—Л—Е –С—Г—Б–Ї–Њ–њ–∞–љ–Њ–Љ, –љ–∞–њ—А–∞–≤–Є—В—М –љ–∞ –ї–µ—З–µ–љ–Є–µ –Э–Њ–—И–њ–Њ–є, —В–Њ —Б —В–Њ–є –ґ–µ —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В—М—О –Љ–Њ–ґ–љ–Њ –ї–µ—З–Є—В—М 645 –±–Њ–ї—М–љ—Л—Е. –Х—Б–ї–Є –ґ–µ –Є—Е –љ–∞–њ—А–∞–≤–Є—В—М –љ–∞ –њ—А–Є–Њ–±—А–µ—В–µ–љ–Є–µ –Ф—О—Б–њ–∞—В–∞–ї–Є–љ–∞, —В–Њ —Б—В–∞–љ–µ—В –≤–Њ–Ј–Љ–Њ–ґ–љ—Л–Љ –њ—А–Њ–ї–µ—З–Є—В—М 312 —З–µ–ї–Њ–≤–µ–Ї.
–Ґ–∞–Ї–Є–Љ –Њ–±—А–∞–Ј–Њ–Љ, –њ–Њ —Д–∞—А–Љ–∞–Ї–Њ—Н–Ї–Њ–љ–Њ–Љ–Є—З–µ—Б–Ї–Є–Љ –њ–∞—А–∞–Љ–µ—В—А–∞–Љ, –Њ—Ж–µ–љ–µ–љ–љ—Л–Љ –њ–Њ –і–Є–љ–∞–Љ–Є–Ї–µ —Б—В–Є—Е–∞–љ–Є—П –Њ–±—К–µ–Ї—В–Є–≤–љ—Л—Е –њ—А–Є–Ј–љ–∞–Ї–Њ–≤ –∞–±–і–Њ–Љ–Є–љ–∞–ї—М–љ–Њ–є –±–Њ–ї–Є –њ—А–Є –°–†–Ъ, –љ–∞–Є–±–Њ–ї–µ–µ —Н–Ї–Њ–љ–Њ–Љ–Є—З–љ–∞ –Э–Њ–—И–њ–∞, –љ–∞–Є–Љ–µ–љ–µ–µ – –С—Г—Б–Ї–Њ–њ–∞–љ. –Ф—О—Б–њ–∞—В–∞–ї–Є–љ –Ј–∞–љ–Є–Љ–∞–µ—В –њ—А–Њ–Љ–µ–ґ—Г—В–Њ—З–љ–Њ–µ –њ–Њ–ї–Њ–ґ–µ–љ–Є–µ –њ–Њ —Д–∞—А–Љ–∞–Ї–Њ—Н–Ї–Њ–љ–Њ–Љ–Є—З–µ—Б–Ї–Њ–є —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В–Є.
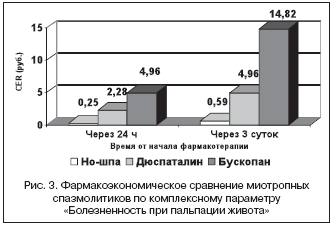
–Р–љ–∞–ї–Є–Ј –і–Є–љ–∞–Љ–Є–Ї–Є –Њ—В–і–µ–ї—М–љ—Л—Е –Њ–±—К–µ–Ї—В–Є–≤–љ—Л—Е –њ—А–Є–Ј–љ–∞–Ї–Њ–≤ –≤—Л—П–≤–Є–ї –љ–µ–Ї–Њ—В–Њ—А—Л–µ –Њ—Б–Њ–±–µ–љ–љ–Њ—Б—В–Є –≤ –і–µ–є—Б—В–≤–Є–Є —А–∞—Б—Б–Љ–∞—В—А–Є–≤–∞–µ–Љ—Л—Е –Љ–Є–Њ—В—А–Њ–њ–љ—Л—Е —Б–њ–∞–Ј–Љ–Њ–ї–Є—В–Є–Ї–Њ–≤. –Ґ–∞–Ї, —Г–ґ–µ —З–µ—А–µ–Ј 24 —З –Њ—В –љ–∞—З–∞–ї–∞ —Д–∞—А–Љ–∞–Ї–Њ—В–µ—А–∞–њ–Є–Є —В–Њ–ї—М–Ї–Њ –Э–Њ–—И–њ–∞ —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ —Г–Љ–µ–љ—М—И–∞–ї–∞ –Њ–±—К–µ–Ї—В–Є–≤–љ—Л–µ –њ—А–Є–Ј–љ–∞–Ї–Є –∞–±–і–Њ–Љ–Є–љ–∞–ї—М–љ–Њ–≥–Њ –±–Њ–ї–µ–≤–Њ–≥–Њ —Б–Є–љ–і—А–Њ–Љ–∞, —Б–≤—П–Ј–∞–љ–љ–Њ–≥–Њ —Б–Њ —Б–њ–∞–Ј–Љ–Њ–Љ (—В–∞–±–ї. 4), –Љ–µ–љ–µ–µ —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ –і–µ–є—Б—В–≤–Њ–≤–∞–ї –Ф—О—Б–њ–∞—В–∞–ї–Є–љ, –і–Є–љ–∞–Љ–Є–Ї–Є –њ—А–Є –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є–Є –С—Г—Б–Ї–Њ–њ–∞–љ–∞ –њ—А–Є –∞–љ–∞–ї–Є–Ј–µ —Н—В–Њ–є –≤—А–µ–Љ–µ–љ–љ–Њ–є —В–Њ—З–Ї–Є –љ–µ –Њ—В–Љ–µ—З–µ–љ–Њ. –Ф–Њ—Б—В–Њ–≤–µ—А–љ—Л–µ —А–∞–Ј–ї–Є—З–Є—П —Б –Є—Б—Е–Њ–і–љ—Л–Љ —Г—А–Њ–≤–љ–µ–Љ –њ—А–Є –њ—А–Є–Љ–µ–љ–µ–љ–Є–Є –Ф—О—Б–њ–∞—В–∞–ї–Є–љ–∞ –Є –С—Г—Б–Ї–Њ–њ–∞–љ–∞ –њ–Њ—П–≤–Є–ї–Є—Б—М —В–Њ–ї—М–Ї–Њ –њ–Њ—Б–ї–µ –љ–µ–і–µ–ї–Є –Є—Е –њ—А–Є–Љ–µ–љ–µ–љ–Є—П, —З—В–Њ —Б–≤–Є–і–µ—В–µ–ї—М—Б—В–≤—Г–µ—В –Њ –±–Њ–ї–µ–µ –±—Л—Б—В—А–Њ–Љ –Є —Б—В–Њ–є–Ї–Њ–Љ –∞–љ—В–Є—Б–њ–∞—Б—В–Є—З–µ—Б–Ї–Њ–Љ –і–µ–є—Б—В–≤–Є–Є –Э–Њ–—И–њ—Л –Є —Б–≤—П–Ј–∞–љ–љ—Л–Љ —Б –љ–Є–Љ –Ї—Г–њ–Є—А–Њ–≤–∞–љ–Є–µ–Љ –±–Њ–ї–µ–≤–Њ–≥–Њ —Б–Є–љ–і—А–Њ–Љ–∞, –≤—Л–Ј–≤–∞–љ–љ–Њ–≥–Њ —Б–њ–∞–Ј–Љ–Њ–Љ –Ї–Є—И–Ї–Є. –Я–∞—А–∞–Љ–µ—В—А —Н–Ї–Њ–љ–Њ–Љ–Є—З–µ—Б–Ї–Њ–є —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В–Є –Э–Њ–—И–њ—Л —З–µ—А–µ–Ј 24 —З –µ–µ –њ—А–Є–Љ–µ–љ–µ–љ–Є—П –Ј–љ–∞—З–Є—В–µ–ї—М–љ–Њ –ї—Г—З—И–µ, —З–µ–Љ —Г –і–≤—Г—Е –і—А—Г–≥–Є—Е –Љ–Є–Њ—В—А–Њ–њ–љ—Л—Е —Б–њ–∞–Ј–Љ–Њ–ї–Є—В–Є–Ї–Њ–≤ (—А–Є—Б. 3). CER –і–ї—П –Э–Њ–—И–њ—Л –њ–Њ —В–Њ—З–Ї–∞–Љ «24 —З» –Є «—З–µ—А–µ–Ј 3 –і–љ—П —Д–∞—А–Љ–∞–Ї–Њ—В–µ—А–∞–њ–Є–Є» –Љ–µ–љ—М—И–µ, —З–µ–Љ –і–ї—П –Ф—О—Б–њ–∞—В–∞–ї–Є–љ–∞ –Є –С—Г—Б–Ї–Њ–њ–∞–љ–∞, –љ–∞ 89%; 95 –Є 88,1%; 96% —Б–Њ–Њ—В–≤–µ—В—Б—В–≤–µ–љ–љ–Њ.
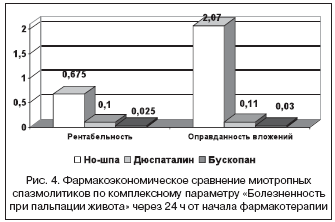
–Т –≥—А—Г–њ–њ–µ –±–Њ–ї—М–љ—Л—Е, –њ–Њ–ї—Г—З–∞–≤—И–Є—Е –Э–Њ–—И–њ—Г, –њ–Њ–ї–љ–∞—П –љ–Њ—А–Љ–∞–ї–Є–Ј–∞—Ж–Є—П –Ї–Њ–Љ–њ–ї–µ–Ї—Б–љ–Њ–≥–Њ –њ–Њ–Ї–∞–Ј–∞—В–µ–ї—П «–С–Њ–ї–µ–Ј–љ–µ–љ–љ–Њ—Б—В—М –њ—А–Є –њ–∞–ї—М–њ–∞—Ж–Є–Є –ґ–Є–≤–Њ—В–∞» —З–µ—А–µ–Ј 24 —З –±—Л–ї–∞ –Ј–∞—Д–Є–Ї—Б–Є—А–Њ–≤–∞–љ–∞ —Г 27 —З–µ–ї., –≤ —В–Њ –≤—А–µ–Љ—П –Ї–∞–Ї –≤ –і–≤—Г—Е –≥—А—Г–њ–њ–∞—Е —В–∞–Ї–Є—Е –њ–∞—Ж–Є–µ–љ—В–Њ–≤ –±—Л–ї–Њ –Љ–µ–љ—М—И–µ: –њ—А–Є –њ—А–Є–µ–Љ–µ –Ф—О—Б–њ–∞—В–∞–ї–Є–љ–∞ – 4, –њ—А–Є –њ—А–Є–µ–Љ–µ –С—Г—Б–Ї–Њ–њ–∞–љ–∞ – 1. –≠—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В—М –≤–ї–Њ–ґ–µ–љ–Є–є –≤ –Ї—Г–њ–Є—А–Њ–≤–∞–љ–Є–µ –±–Њ–ї–µ–≤–Њ–≥–Њ –∞–±–і–Њ–Љ–Є–љ–∞–ї—М–љ–Њ–≥–Њ —Б–Є–љ–і—А–Њ–Љ–∞, –≤—Л–Ј–≤–∞–љ–љ–Њ–≥–Њ —Б–њ–∞–Ј–Љ–Њ–Љ –Ї–Є—И–µ—З–љ–Є–Ї–∞, –њ–Њ —В–Њ—З–Ї–µ «24 —З» –Њ—Ж–µ–љ–µ–љ–∞ –Ї–∞–Ї –Њ—В–љ–Њ—И–µ–љ–Є–µ —Б—В–Њ–Є–Љ–Њ—Б—В–Є –ї–µ—З–µ–љ–Є—П –Љ–Є–Њ—В—А–Њ–њ–љ—Л–Љ–Є —Б–њ–∞–Ј–Љ–Њ–ї–Є—В–Є–Ї–∞–Љ–Є –≤ —В–µ—З–µ–љ–Є–µ —Б—Г—В–Њ–Ї –і–ї—П –±–Њ–ї—М–љ—Л—Е, —Г –Ї–Њ—В–Њ—А—Л—Е –∞–±–і–Њ–Љ–Є–љ–∞–ї—М–љ–∞—П –±–Њ–ї—М, –≤—Л–Ј–≤–∞–љ–љ–∞—П —Б–њ–∞–Ј–Љ–Њ–Љ –Ї–Є—И–Ї–Є, –±—Л–ї–∞ –Ї—Г–њ–Є—А–Њ–≤–∞–љ–∞, –Ї —Б—В–Њ–Є–Љ–Њ—Б—В–Є —Б—Г—В–Њ—З–љ–Њ–≥–Њ –ї–µ—З–µ–љ–Є—П —Г –≤—Б–µ—Е –±–Њ–ї—М–љ—Л—Е –≤ –≥—А—Г–њ–њ–µ. –Ф–ї—П –Э–Њ–—И–њ—Л –њ–Њ —В–Њ—З–Ї–µ «24 —З» –љ–∞ 40 –±–Њ–ї—М–љ—Л—Е –±—Л–ї–Њ –Ј–∞—В—А–∞—З–µ–љ–Њ 540 —А—Г–±., –∞ –і–ї—П —В–µ—Е, —Г –Ї–Њ–≥–Њ —Б–Є–љ–і—А–Њ–Љ –±—Л–ї –Ї—Г–њ–Є—А–Њ–≤–∞–љ (27 —З–µ–ї.) – 364,5 —А—Г–±. –Ш–љ–і–µ–Ї—Б —А–µ–љ—В–∞–±–µ–ї—М–љ–Њ—Б—В–Є – 0,675. –°–Њ–Њ—В–≤–µ—В—Б—В–≤—Г—О—Й–Є–µ –Ј–љ–∞—З–µ–љ–Є—П –і–ї—П –Ф—О—Б–њ–∞—В–∞–ї–Є–љ–∞ – 0,1, –і–ї—П –С—Г—Б–Ї–Њ–њ–∞–љ–∞ – 0,025. –Ґ–∞–Ї–Є–Љ –Њ–±—А–∞–Ј–Њ–Љ, —А–µ–љ—В–∞–±–µ–ї—М–љ–Њ—Б—В—М –Э–Њ–—И–њ—Л –њ–Њ —А–∞—Б—Б–Љ–∞—В—А–Є–≤–∞–µ–Љ–Њ–є —В–Њ—З–Ї–µ –≤ 6,7 —А–∞–Ј –≤—Л—И–µ, —З–µ–Љ –Ф—О—Б–њ–∞—В–∞–ї–Є–љ–∞, –Є –≤ 27 —А–∞–Ј – —З–µ–Љ –С—Г—Б–Ї–Њ–њ–∞–љ–∞.
–Я—А–Є–±—Л–ї—М–љ–Њ—Б—В—М –≤–ї–Њ–ґ–µ–љ–Є–є –Њ–њ—А–µ–і–µ–ї–µ–љ–∞ –Ї–∞–Ї –Њ—В–љ–Њ—И–µ–љ–Є–µ –Ј–∞—В—А–∞—В –љ–∞ –ї–µ—З–µ–љ–Є–µ –Љ–Є–Њ—В—А–Њ–њ–љ—Л–Љ–Є —Б–њ–∞–Ј–Љ–Њ–ї–Є—В–Є–Ї–∞–Љ–Є —Г —В–µ—Е, —Г –Ї–Њ–≥–Њ –±—Л–ї –њ–Њ–ї—Г—З–µ–љ —Н—Д—Д–µ–Ї—В –њ–Њ –Ї–Њ–Љ–њ–ї–µ–Ї—Б–љ–Њ–є —В–Њ—З–Ї–µ «–С–Њ–ї–µ–Ј–љ–µ–љ–љ–Њ—Б—В—М –њ—А–Є –њ–∞–ї—М–њ–∞—Ж–Є–Є –ґ–Є–≤–Њ—В–∞» —З–µ—А–µ–Ј 24 —З –њ–Њ—Б–ї–µ –љ–∞—З–∞–ї–∞ —Д–∞—А–Љ–∞–Ї–Њ—В–µ—А–∞–њ–Є–Є, –Ї —Б—Г–Љ–Љ–µ –Ј–∞—В—А–∞—В —Г —В–µ—Е, —Г –Ї–Њ–≥–Њ —Н—Д—Д–µ–Ї—В –љ–µ –±—Л–ї –і–Њ—Б—В–Є–≥–љ—Г—В. –Ф–ї—П –Э–Њ–—И–њ—Л —Н—В–Њ—В –њ–∞—А–∞–Љ–µ—В—А —Б–Њ—Б—В–∞–≤–Є–ї 2,07, –і–ї—П –Ф—О—Б–њ–∞—В–∞–ї–Є–љ–∞ – 0,11, –і–ї—П –С—Г—Б–Ї–Њ–њ–∞–љ–∞ – 0,03. –Ґ–∞–Ї–Є–Љ –Њ–±—А–∞–Ј–Њ–Љ, –њ—А–Є–±—Л–ї—М–љ–Њ—Б—В—М –≤–ї–Њ–ґ–µ–љ–Є–є –Љ–Њ–ґ–µ—В –±—Л—В—М –Є–љ—В–µ—А–њ—А–µ—В–Є—А–Њ–≤–∞–љ–∞ —Б–ї–µ–і—Г—О—Й–Є–Љ –Њ–±—А–∞–Ј–Њ–Љ: –љ–∞ –Ї–∞–ґ–і—Л–є –≤–ї–Њ–ґ–µ–љ–љ—Л–є –≤ –Э–Њ–—И–њ—Г —А—Г–±–ї—М —З–µ—А–µ–Ј 24 —З –Њ—В –љ–∞—З–∞–ї–∞ –ї–µ—З–µ–љ–Є—П –Љ–Њ–ґ–љ–Њ –њ–Њ–ї—Г—З–Є—В—М 1,07 —А—Г–±. —Н–Ї–Њ–љ–Њ–Љ–Є—З–µ—Б–Ї–Њ–≥–Њ —Н—Д—Д–µ–Ї—В–∞ –њ–Њ —Г—Б—В—А–∞–љ–µ–љ–Є—О –±–Њ–ї–µ–≤–Њ–≥–Њ –∞–±–і–Њ–Љ–Є–љ–∞–ї—М–љ–Њ–≥–Њ —Б–Є–љ–і—А–Њ–Љ–∞, –≤—Л–Ј–≤–∞–љ–љ–Њ–≥–Њ —Б–њ–∞–Ј–Љ–Њ–Љ –Ї–Є—И–µ—З–љ–Є–Ї–∞, –≤ —В–Њ –≤—А–µ–Љ—П –Ї–∞–Ї —Д–∞—А–Љ–∞–Ї–Њ—В–µ—А–∞–њ–Є—П –Ф—О—Б–њ–∞—В–∞–ї–Є–љ–Њ–Љ –Є –С—Г—Б–Ї–Њ–њ–∞–љ–Њ–Љ —Г–±—Л—В–Њ—З–љ–∞ – —Б –Ї–∞–ґ–і–Њ–≥–Њ –≤–ї–Њ–ґ–µ–љ–љ–Њ–≥–Њ —А—Г–±–ї—П –њ–Њ—В–µ—А–Є —Б–Њ—Б—В–∞–≤–ї—П—О—В 89 –Є 97 –Ї–Њ–њ. —Б–Њ–Њ—В–≤–µ—В—Б—В–≤–µ–љ–љ–Њ (—А–Є—Б. 4).
–Ґ–∞–Ї–Є–Љ –Њ–±—А–∞–Ј–Њ–Љ, –≤—Б–µ—Б—В–Њ—А–Њ–љ–љ–Є–є –Ї–Њ–Љ–њ–ї–µ–Ї—Б–љ—Л–є —Д–∞—А–Љ–∞–Ї–Њ—Н–Ї–Њ–љ–Њ–Љ–Є—З–µ—Б–Ї–Є–є –∞–љ–∞–ї–Є–Ј –њ–Њ–і—В–≤–µ—А–ґ–і–∞–µ—В, —З—В–Њ –Э–Њ–—И–њ–∞ –Њ–±–ї–∞–і–∞–µ—В –ї—Г—З—И–µ–є –Ї–ї–Є–љ–Є–Ї–Њ–—Н–Ї–Њ–љ–Њ–Љ–Є—З–µ—Б–Ї–Њ–є —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В—М—О –њ—А–Є –Ї—Г–њ–Є—А–Њ–≤–∞–љ–Є–Є –∞–±–і–Њ–Љ–Є–љ–∞–ї—М–љ–Њ–є –±–Њ–ї–Є, –≤—Л–Ј–≤–∞–љ–љ–Њ–є —Б–њ–∞–Ј–Љ–Њ–Љ –Ї–Є—И–Ї–Є, –≤ —Б—А–∞–≤–љ–µ–љ–Є–Є —Б –Ф—О—Б–њ–∞—В–∞–ї–Є–љ–Њ–Љ –Є –С—Г—Б–Ї–Њ–њ–∞–љ–Њ–Љ.
–Ю—Ж–µ–љ–Ї–∞ –њ–µ—А–µ–љ–Њ—Б–Є–Љ–Њ—Б—В–Є –њ—А–µ–њ–∞—А–∞—В–Њ–≤ –њ—А–Њ–Є–Ј–≤–µ–і–µ–љ–∞ —Б —Г—З–µ—В–Њ–Љ —И–Ї–∞–ї—Л –Э–∞—А–∞–љ–ґ–Њ [9]. –Я–Њ–±–Њ—З–љ—Л–µ —Н—Д—Д–µ–Ї—В—Л –њ—А–Є –њ—А–Є–Љ–µ–љ–µ–љ–Є–Є –Љ–µ–±–µ–≤–µ—А–Є–љ–∞ –Є –≥–Є–Њ—Б—Ж–Є–љ–∞ –±—Г—В–Є–ї–±—А–Њ–Љ–Є–і–∞ –љ–µ –Ј–∞—А–µ–≥–Є—Б—В—А–Є—А–Њ–≤–∞–љ—Л. –Я—А–Є –њ—А–Є–Љ–µ–љ–µ–љ–Є–Є –і—А–Њ—В–∞–≤–µ—А–Є–љ–∞ —Г 3 –±–Њ–ї—М–љ—Л—Е –≤ –і–Њ–Ј–∞—Е 240 –Љ–≥/—Б—Г—В. –љ–∞–±–ї—О–і–∞–ї–∞—Б—М —В—А–∞–љ–Ј–Є—В–Њ—А–љ–∞—П —В–Њ—И–љ–Њ—В–∞, –љ–µ –њ–Њ—В—А–µ–±–Њ–≤–∞–≤—И–∞—П —Д–∞—А–Љ–∞–Ї–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Њ–є –Ї–Њ—А—А–µ–Ї—Ж–Є–Є –Є –Њ—В–Љ–µ–љ—Л –њ—А–µ–њ–∞—А–∞—В–∞. –Я–Њ—Б–ї–µ —Б–љ–Є–ґ–µ–љ–Є—П —Б—Г—В–Њ—З–љ–Њ–є –і–Њ–Ј—Л –і–Њ 200 –Љ–≥ —В–Њ—И–љ–Њ—В–∞ —Г —Н—В–Є—Е –±–Њ–ї—М–љ—Л—Е –љ–µ –≤–Њ–Ј–Њ–±–љ–Њ–≤–ї—П–ї–∞—Б—М. –Ґ–∞–Ї–Є–Љ –Њ–±—А–∞–Ј–Њ–Љ, –≤–Њ–Ј–љ–Є–Ї—И–Є–µ –і–Њ–Ј–Њ–Ј–∞–≤–Є—Б–Є–Љ—Л–µ –њ–Њ–±–Њ—З–љ—Л–µ —Н—Д—Д–µ–Ї—В—Л –і—А–Њ—В–∞–≤–µ—А–Є–љ–∞ –Љ–Њ–≥—Г—В –±—Л—В—М –њ—А–Є–Ј–љ–∞–љ—Л –Љ–∞–ї–Њ—Б—Г—Й–µ—Б—В–≤–µ–љ–љ—Л–Љ–Є –Є –љ–µ –≤–ї–Є—П—О—Й–Є–Љ–Є –љ–∞ —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В—М.
–Т –Ј–∞–Ї–ї—О—З–µ–љ–Є–µ –Љ–Њ–ґ–љ–Њ —Б–і–µ–ї–∞—В—М —Б–ї–µ–і—Г—О—Й–Є–µ –≤—Л–≤–Њ–і—Л.
• –Ь–Є–Њ—В—А–Њ–њ–љ—Л–µ —Б–њ–∞–Ј–Љ–Њ–ї–Є—В–Є–Ї–Є –і—А–Њ—В–∞–≤–µ—А–Є–љ, –Љ–µ–±–µ–≤–µ—А–Є–љ –Є –≥–Є–Њ—Б—Ж–Є–љ–∞ –±—Г—В–Є–ї–±—А–Њ–Љ–Є–і —П–≤–ї—П—О—В—Б—П —Н—Д—Д–µ–Ї—В–Є–≤–љ—Л–Љ–Є —Б—А–µ–і—Б—В–≤–∞–Љ–Є –Ї—Г–њ–Є—А–Њ–≤–∞–љ–Є—П –∞–±–і–Њ–Љ–Є–љ–∞–ї—М–љ–Њ–є –±–Њ–ї–Є, –≤—Л–Ј–≤–∞–љ–љ–Њ–є —Б–њ–∞–Ј–Љ–Њ–Љ –Ї–Є—И–Ї–Є, –Њ—Ж–µ–љ–µ–љ–љ–Њ–≥–Њ –љ–∞ –Љ–Њ–і–µ–ї–Є —Б–Є–љ–і—А–Њ–Љ–∞ —А–∞–Ј–і—А–∞–ґ–µ–љ–љ–Њ–є –Ї–Є—И–Ї–Є.
• –Ф—А–Њ—В–∞–≤–µ—А–Є–љ –Њ–±–ї–∞–і–∞–µ—В –±–Њ–ї–µ–µ –±—Л—Б—В—А–Њ–є –і–Є–љ–∞–Љ–Є–Ї–Њ–є –њ–Њ —Г–Љ–µ–љ—М—И–µ–љ–Є—О –њ—А–Є–Ј–љ–∞–Ї–Њ–≤ —Б–њ–∞–Ј–Љ–∞ –Є —Б–≤—П–Ј–∞–љ–љ–Њ–є —Б –љ–Є–Љ –∞–±–і–Њ–Љ–Є–љ–∞–ї—М–љ–Њ–є –±–Њ–ї–Є –≤ —Б—А–∞–≤–љ–µ–љ–Є–Є —Б –Љ–µ–±–µ–≤–µ—А–Є–љ–Њ–Љ –Є –≥–Є–Њ—Б—Ж–Є–љ–∞ –±—Г—В–Є–ї–±—А–Њ–Љ–Є–і–Њ–Љ, —З—В–Њ –њ–Њ–Ј–≤–Њ–ї—П–µ—В —А–µ–Ї–Њ–Љ–µ–љ–і–Њ–≤–∞—В—М –µ–≥–Њ –≤ –Ї–∞—З–µ—Б—В–≤–µ –њ—А–µ–њ–∞—А–∞—В–∞ –њ–µ—А–≤–Њ–≥–Њ —А—П–і–∞ –і–ї—П –Њ–Ї–∞–Ј–∞–љ–Є—П –±—Л—Б—В—А–Њ–є –њ–Њ–Љ–Њ—Й–Є –њ—А–Є –≤–Њ–Ј–љ–Є–Ї–љ–Њ–≤–µ–љ–Є–Є –±–Њ–ї–Є —Б–њ–∞—Б—В–Є—З–µ—Б–Ї–Њ–≥–Њ –≥–µ–љ–µ–Ј–∞ –≤ –ґ–Є–≤–Њ—В–µ.
• –Э–Њ–—И–њ–∞ –Є–Љ–µ–µ—В –Њ—В—З–µ—В–ї–Є–≤—Л–µ –Ї–ї–Є–љ–Є–Ї–Њ–—Н–Ї–Њ–љ–Њ–Љ–Є—З–µ—Б–Ї–Є–µ –њ—А–µ–Є–Љ—Г—Й–µ—Б—В–≤–∞ –њ–Њ —Б—А–∞–≤–љ–µ–љ–Є—О —Б –Ф—О—Б–њ–∞—В–∞–ї–Є–љ–Њ–Љ –Є –С—Г—Б–Ї–Њ–њ–∞–љ–Њ–Љ –њ—А–Є –ї–µ—З–µ–љ–Є–Є –∞–±–і–Њ–Љ–Є–љ–∞–ї—М–љ–Њ–є –±–Њ–ї–Є, –≤—Л–Ј–≤–∞–љ–љ–Њ–є —Б–њ–∞–Ј–Љ–Њ–Љ –Ї–Є—И–Ї–Є, –Ї–∞–Ї –Ј–∞ —Б—З–µ—В –Љ–µ–љ—М—И–µ–є —Г—В–Є–ї–Є—В–∞—А–љ–Њ–є —Б—В–Њ–Є–Љ–Њ—Б—В–Є, —В–∞–Ї –Є –њ–Њ —Д–∞—А–Љ–∞–Ї–Њ—Н–Ї–Њ–љ–Њ–Љ–Є—З–µ—Б–Ї–Є–Љ –њ–∞—А–∞–Љ–µ—В—А–∞–Љ «—Б—В–Њ–Є–Љ–Њ—Б—В—М–—Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В—М» –Є «–Љ–Є–љ–Є–Љ–Є–Ј–∞—Ж–Є—П —Б—В–Њ–Є–Љ–Њ—Б—В–Є».
• –Ш—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є–µ –Э–Њ–—И–њ—Л –і–ї—П –ї–µ—З–µ–љ–Є—П –∞–±–і–Њ–Љ–Є–љ–∞–ї—М–љ–Њ–є –±–Њ–ї–Є, –≤—Л–Ј–≤–∞–љ–љ–Њ–є —Б–њ–∞–Ј–Љ–Њ–Љ –Ї–Є—И–Ї–Є, —Н–Ї–Њ–љ–Њ–Љ–Є—З–µ—Б–Ї–Є –≤—Л–≥–Њ–і–љ–Њ –Є —Б–њ–Њ—Б–Њ–±—Б—В–≤—Г–µ—В —А–∞—Ж–Є–Њ–љ–∞–ї—М–љ–Њ–Љ—Г —А–∞—Б—Е–Њ–і–Њ–≤–∞–љ–Є—О —Б—А–µ–і—Б—В–≤.
–Ч–∞—П–≤–ї–µ–љ–Є–µ –Њ—В –∞–≤—В–Њ—А–Њ–≤
–Я—А–Њ–≤–µ–і–µ–љ–љ—Л–є –Ї–ї–Є–љ–Є–Ї–Њ–—Н–Ї–Њ–љ–Њ–Љ–Є—З–µ—Б–Ї–Є–є –∞–љ–∞–ї–Є–Ј –Њ—Б—Г—Й–µ—Б—В–≤–ї–µ–љ –њ–Њ –Є—В–Њ–≥–∞–Љ –њ—А–Є–Љ–µ–љ–µ–љ–Є—П –Њ—А–Є–≥–Є–љ–∞–ї—М–љ—Л—Е –Э–Њ–—И–њ—Л, –Ф—О—Б–њ–∞—В–∞–ї–Є–љ–∞ –Є –С—Г—Б–Ї–Њ–њ–∞–љ–∞ –≤ —А–µ–∞–ї—М–љ–Њ–є –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Њ–є –њ—А–∞–Ї—В–Є–Ї–µ –Є –љ–µ –Љ–Њ–ґ–µ—В –±—Л—В—М —Н–Ї—Б—В—А–∞–њ–Њ–ї–Є—А–Њ–≤–∞–љ –љ–∞ –≥–µ–љ–µ—А–Є–Ї–Њ–≤—Л–µ —Д–Њ—А–Љ—Л —Н—В–Є—Е –њ—А–µ–њ–∞—А–∞—В–Њ–≤.
–Ч–∞—П–≤–ї–µ–љ–Є–µ –Њ –Ї–Њ–љ—Д–ї–Є–Ї—В–µ –Є–љ—В–µ—А–µ—Б–Њ–≤
–Э–∞—Б—В–Њ—П—Й–Є–Љ –∞–≤—В–Њ—А—Л –њ–Њ–і—В–≤–µ—А–ґ–і–∞—О—В –Њ—В—Б—Г—В—Б—В–≤–Є–µ —Д–Є–љ–∞–љ—Б–Є—А–Њ–≤–∞–љ–Є—П –њ—А–Њ–≤–µ–і–µ–љ–љ–Њ–є —Н–Ї—Б–њ–µ—А—В–Є–Ј—Л —В—А–µ—В—М–Є–Љ–Є –ї–Є—Ж–∞–Љ–Є –Є–ї–Є –Њ—А–≥–∞–љ–Є–Ј–∞—Ж–Є—П–Љ–Є.


–Ы–Є—В–µ—А–∞—В—Г—А–∞
1. –Ш–≤–∞—И–Ї–Є–љ –Т.–Ґ. –°–Є–љ–і—А–Њ–Љ —А–∞–Ј–і—А–∞–ґ–µ–љ–љ–Њ–є –Ї–Є—И–Ї–Є. –Я—А–∞–Ї—В–Є—З–µ—Б–Ї–Њ–µ —А—Г–Ї–Њ–≤–Њ–і—Б—В–≤–Њ –і–ї—П –≤—А–∞—З–µ–є. –Ь, –†–У–Р, 1999; 28 c.
2. –С–µ–ї–Њ—Г—Б–Њ–≤ –Ѓ. –С., –Ы–µ–Њ–љ–Њ–≤–∞ –Ь. –Т. –Ъ–ї–Є–љ–Є—З–µ—Б–Ї–∞—П —Д–∞—А–Љ–∞–Ї–Њ–ї–Њ–≥–Є—П –љ–Њ–—И–њ—Л. –Ь–µ—В–Њ–і–Є—З–µ—Б–Ї–Њ–µ –њ–Њ—Б–Њ–±–Є–µ –і–ї—П –≤—А–∞—З–µ–є. –Ь., 2002.10 —Б.
3. Blasko G. Pharmacology, mechanism of action and clinical significance of a convenient antispasmodic agent: drotaverine. JAMA India – The physician’s update, 1998, 1;6:63–70.
4. Tyrakowski T, Mlodzik–Danielewicz N, Kurek W et al. Mebeverine influences sodium ion transport in the distal colon // Pharmacol Rep. 2006;58 (5):765–769 –Ь–µ—Е—В–Є–µ–≤ –°.–Э, –У—А–Є–љ–µ–≤–Є—З –Т.–С., –Ъ—А–∞–≤—З—Г–Ї –Ѓ.–Р. –Т—Л–±–Њ—А —Б–њ–∞–Ј–Љ–Њ–ї–Є—В–Є–Ї–Њ–≤ –њ—А–Є –∞–±–і–Њ–Љ–Є–љ–∞–ї—М–љ–Њ–є –±–Њ–ї–Є –≤ –≥–∞—Б—В—А–Њ—Н–љ—В–µ—А–Њ–ї–Њ–≥–Є–Є. –Ь–µ—В–Њ–і–Є—З–µ—Б–Ї–Є–µ —А–µ–Ї–Њ–Љ–µ–љ–і–∞—Ж–Є–Є –і–ї—П –≤—А–∞—З–µ–є. –°–Я–±., 2005. 18 —Б.
5. –§–∞—А–Љ–∞–Ї–Њ—Н–Ї–Њ–љ–Њ–Љ–Є–Ї–∞ –Є —Д–∞—А–Љ–∞–Ї–Њ—Н–њ–Є–і–µ–Љ–Є–Њ–ї–Њ–≥–Є—П – –њ—А–∞–Ї—В–Є–Ї–∞ –њ—А–Є–µ–Љ–ї–µ–Љ—Л—Е —А–µ—И–µ–љ–Є–є / –Я–Њ–ї —А–µ–і. –Т.–С. –У–µ—А–∞—Б–Є–Љ–Њ–≤–∞, –Р.–Ы. –•–Њ—Е–ї–Њ–≤–∞, –Ю.–Ш. –Ъ–∞—А–њ–Њ–≤–∞. – –Ь.: –Ь–µ–і–Є—Ж–Є–љ–∞, 2005. – 352 —Б.
6. http://www.medlux.ru
7. Khoshkrood–Mansoori B., Pourhoseingholi M.A., Safaee A. et al. Irritable bowel syndrome: a population based study // J Gastrointestin Liver Dis. – 2009;18(4):413–418.
8. Coffin B. Diagnosis of irritable bowel syndrome // Gastroenterol Clin Biol. – 2009;33 (Suppl. 1): S9–16.
9. Naranjo C.A., Busto U., Sellers E.M., et al. A method for estimating the probability of adverse drug reactions // Clin. Pharmacol. Ther., 1981; 30: 239–45.












