–£—Б–њ–µ—Е–Є –Є –±–µ–Ј–Њ–њ–∞—Б–љ–Њ—Б—В—М –Њ–њ–Є—Б–∞–љ–љ–Њ–є —В—А–µ—Е–Ї–Њ–Љ–њ–Њ–љ–µ–љ—В–љ–Њ–є —В–µ—А–∞–њ–Є–Є –њ–µ—А–≤–Њ–є –ї–Є–љ–Є–Є –і–Њ–Ї–∞–Ј–∞–љ—Л –≤ –Љ–љ–Њ–≥–Њ—З–Є—Б–ї–µ–љ–љ—Л—Е –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П—Е –Є –Ј–∞ —А—Г–±–µ–ґ–Њ–Љ, –Є –≤ –љ–∞—И–µ–є —Б—В—А–∞–љ–µ. –Ш–Љ–µ—О—В—Б—П –Љ–µ—В–∞––∞–љ–∞–ї–Є–Ј—Л —Н—В–Є—Е –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–є, —Б–Є—Б—В–µ–Љ–∞—В–Є—З–µ—Б–Ї–Є–µ –Њ–±–Ј–Њ—А—Л (–≤ —В–Њ–Љ —З–Є—Б–ї–µ –Ъ–Њ—Е—А–µ–є–љ–Њ–≤—Б–Ї–Є–µ), –Љ–µ–ґ–і—Г–љ–∞—А–Њ–і–љ—Л–µ –Ї–Њ–љ—Б–µ–љ—Б—Г—Б—Л. –Ґ–∞–Ї–Є–Љ –Њ–±—А–∞–Ј–Њ–Љ, –Њ–њ–Є—Б–∞–љ–љ—Л–µ —Б—Е–µ–Љ—Л –њ—А–Њ—В–Є–≤–Њ–≥–µ–ї–Є–Ї–Њ–±–∞–Ї—В–µ—А–љ–Њ–≥–Њ –ї–µ—З–µ–љ–Є—П, –±–µ–Ј—Г—Б–ї–Њ–≤–љ–Њ, –Њ—В–≤–µ—З–∞—О—В —Г—А–Њ–≤–љ—О –і–Њ–Ї–∞–Ј–∞—В–µ–ї—М–љ–Њ—Б—В–Є –Р.
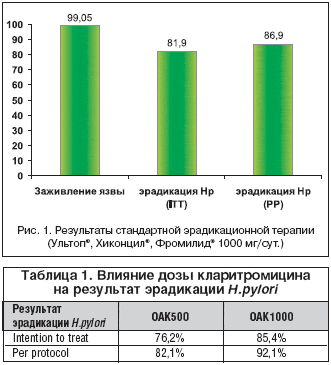
–Т –Ї–∞—З–µ—Б—В–≤–µ –њ—А–Є–Љ–µ—А–∞ –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є—П —В–∞–Ї–Њ–є —Б—Е–µ–Љ—Л –Њ–±—А–∞—В–Є–Љ—Б—П –Ї –Њ—В–µ—З–µ—Б—В–≤–µ–љ–љ—Л–Љ —А–∞–±–Њ—В–∞–Љ. –Т –Њ—В–Ї—А—Л—В–Њ–Љ –љ–µ—Б—А–∞–≤–љ–Є—В–µ–ї—М–љ–Њ–Љ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є, –≤—Л–њ–Њ–ї–љ–µ–љ–љ–Њ–Љ –≤ —В—А–µ—Е —Ж–µ–љ—В—А–∞—Е –≤ –≥–Њ—А–Њ–і–∞—Е –Ъ–∞–Ј–∞–љ–Є, –Ю–Љ—Б–Ї–µ –Є –°–∞–љ–Ї—В––Я–µ—В–µ—А–±—Г—А–≥–µ [–†.–Р. –Р–±–і—Г–ї—Е–∞–Ї–Њ–≤, –Р.–Т. –Ъ–Њ–љ–Њ–љ–Њ–≤, –Т.–Ш. –°–Є–Љ–∞–љ–µ–љ–Ї–Њ–≤ –Є —Б–Њ–∞–≤—В.], —Н—А–∞–і–Є–Ї–∞—Ж–Є–Њ–љ–љ—Г—О —В–µ—А–∞–њ–Є—О –њ—А–Њ–≤–Њ–і–Є–ї–Є 105 –±–Њ–ї—М–љ—Л–Љ —П–Ј–≤–µ–љ–љ–Њ–є –±–Њ–ї–µ–Ј–љ—М—О –і–≤–µ–љ–∞–і—Ж–∞—В–Є–њ–µ—А—Б—В–љ–Њ–є –Ї–Є—И–Ї–Є –≤ —Б—В–∞–і–Є–Є –Њ–±–Њ—Б—В—А–µ–љ–Є—П. –Я—А–Є–Љ–µ–љ—П–ї–Є –ї–µ–Ї–∞—А—Б—В–≤–µ–љ–љ—Л–µ —Б—А–µ–і—Б—В–≤–∞ –£–ї—М—В–Њ–њ® (–Њ–Љ–µ–њ—А–∞–Ј–Њ–ї) 20 –Љ–≥ 2 —А/—Б—Г—В.; –•–Є–Ї–Њ–љ—Ж–Є–ї® (–∞–Љ–Њ–Ї—Б–Є—Ж–Є–ї–ї–Є–љ) 1000 –Љ–≥ 2 —А/—Б—Г—В.; –§—А–Њ–Љ–Є–ї–Є–і® (–Ї–ї–∞—А–Є—В—А–Њ–Љ–Є—Ж–Є–љ) 500 –Љ–≥ 2 —А/—Б—Г—В. –≤ —В–µ—З–µ–љ–Є–µ 7 –і–љ–µ–є. –Ч–∞–ґ–Є–≤–ї–µ–љ–Є–µ —П–Ј–≤—Л 12––њ–µ—А—Б—В–љ–Њ–є –Ї–Є—И–Ї–Є –і–Њ—Б—В–Є–≥–љ—Г—В–Њ —Г 99,05% –±–Њ–ї—М–љ—Л—Е. –Я—А–Њ—Ж–µ–љ—В —Н—А–∞–і–Є–Ї–∞—Ж–Є–Є H.pylori —Б–Њ—Б—В–∞–≤–Є–ї 81,9% —Г –≤—Б–µ—Е –њ–∞—Ж–Є–µ–љ—В–Њ–≤, –≤–Ї–ї—О—З–µ–љ–љ—Л—Е –≤ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ (intention to treat), –Є 86,9% —Г –±–Њ–ї—М–љ—Л—Е, –Ј–∞–≤–µ—А—И–Є–≤—И–Є—Е –њ—А–Њ—В–Њ–Ї–Њ–ї (per protocol) (—А–Є—Б. 1).
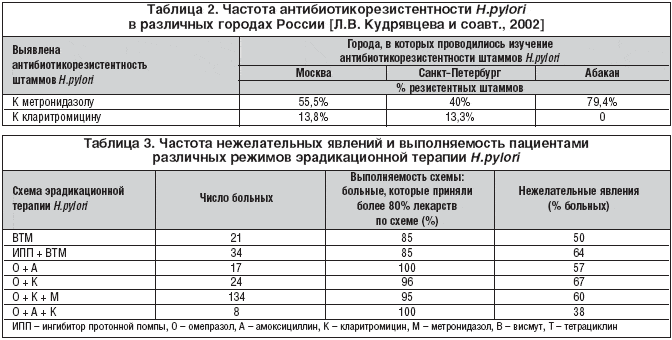
–С–Њ–ї—М—И–Њ–є –Є–љ—В–µ—А–µ—Б –њ—А–µ–і—Б—В–∞–≤–ї—П–µ—В –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ –Т.–Р. –Ш—Б–∞–Ї–Њ–≤–∞, –Ш.–Т. –Ь–∞–µ–≤–∞ –Є —Б–Њ–∞–≤—В. (2002). –°–Њ—Б—В–∞–≤ —В—А–Њ–є–љ–Њ–є —Б—Е–µ–Љ—Л –±—Л–ї —В–Њ—В –ґ–µ: –£–ї—М—В–Њ–њ® (–Њ–Љ–µ–њ—А–∞–Ј–Њ–ї) 20 –Љ–≥ 2 —А/—Б—Г—В.; –•–Є–Ї–Њ–љ—Ж–Є–ї® (–∞–Љ–Њ–Ї—Б–Є—Ж–Є–ї–ї–Є–љ) 1000 –Љ–≥ 2 —А/—Б—Г—В.; –§—А–Њ–Љ–Є–ї–Є–і® (–Ї–ї–∞—А–Є—В—А–Њ–Љ–Є—Ж–Є–љ) (7 –і–љ–µ–є). –Э–Њ –≤ –і–≤–Њ–є–љ–Њ–Љ —Б–ї–µ–њ–Њ–Љ –Ї–Њ–љ—В—А–Њ–ї–Є—А—Г–µ–Љ–Њ–Љ –Є—Б–њ—Л—В–∞–љ–Є–Є —Б—А–∞–≤–љ–Є–≤–∞–ї–Є —Б—Е–µ–Љ—Г —Б —Б—Г—В–Њ—З–љ–Њ–є –і–Њ–Ј–Њ–є –§—А–Њ–Љ–Є–ї–Є–і–∞® 500 –Љ–≥ –Є 1000 –Љ–≥. –Я–Њ —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В–Є –і–∞–љ–љ—Л—Е —Б—Е–µ–Љ —Н—А–∞–і–Є–Ї–∞—Ж–Є–Њ–љ–љ–Њ–є —В–µ—А–∞–њ–Є–Є —Б —В–Њ—З–Ї–Є –Ј—А–µ–љ–Є—П –Ј–∞–ґ–Є–≤–ї–µ–љ–Є—П —П–Ј–≤—Л —Б—В–∞—В–Є—Б—В–Є—З–µ—Б–Ї–Њ–є —А–∞–Ј–љ–Є—Ж—Л –љ–µ –±—Л–ї–Њ: –≤ –≥—А—Г–њ–њ–µ –±–Њ–ї—М–љ—Л—Е, –њ–Њ–ї—Г—З–∞–≤—И–Є—Е –Љ–µ–љ—М—И—Г—О –і–Њ–Ј—Г –Ї–ї–∞—А–Є—В—А–Њ–Љ–Є—Ж–Є–љ–∞ (–Ю–Р–Ъ500), –Њ–љ–Њ —Б–Њ—Б—В–∞–≤–Є–ї–Њ 97,6%, –∞ –≤ –≥—А—Г–њ–њ–µ, –њ–Њ–ї—Г—З–∞–≤—И–µ–є –±–Њ–ї—М—И—Г—О –і–Њ–Ј—Г –Ї–ї–∞—А–Є—В—А–Њ–Љ–Є—Ж–Є–љ–∞ (–Ю–Р–Ъ1000) – 100%. –Ю–і–љ–∞–Ї–Њ —А–∞–Ј–љ–Є—Ж–∞ –±—Л–ї–∞ —Б—Г—Й–µ—Б—В–≤–µ–љ–љ–Њ–є –њ—А–Є —Б—А–∞–≤–љ–µ–љ–Є–Є —Г—Б–њ–µ—И–љ–Њ—Б—В–Є –∞–љ—В–Є—Е–µ–ї–Є–Ї–Њ–±–∞–Ї—В–µ—А–љ–Њ–≥–Њ –ї–µ—З–µ–љ–Є—П (—В–∞–±–ї. 1). –Ґ–∞–Ї, –±—Л–ї–Њ —Г–±–µ–і–Є—В–µ–ї—М–љ–Њ –њ—А–Њ–і–µ–Љ–Њ–љ—Б—В—А–Є—А–Њ–≤–∞–љ–Њ, —З—В–Њ –і–ї—П –љ–∞—И–µ–є —Б—В—А–∞–љ—Л –њ—А–Є–љ—Ж–Є–њ–Є–∞–ї—М–љ–Њ–µ –Ј–љ–∞—З–µ–љ–Є–µ –Є–Љ–µ–µ—В —Б–Њ–±–ї—О–і–µ–љ–Є–µ –њ–Њ–ї–љ–Њ–є –і–Њ–Ј–Є—А–Њ–≤–Ї–Є –Ї–ї–∞—А–Є—В—А–Њ–Љ–Є—Ж–Є–љ–∞ (1000 –Љ–≥/—Б—Г—В.) –≤ –Ї–Њ–Љ–Є–±–Є–љ–Є—А–Њ–≤–∞–љ–љ–Њ–є —В—А–Њ–є–љ–Њ–є —В–µ—А–∞–њ–Є–Є.
–Ъ–∞–Ї–Њ–≤–∞ —А–µ–Ї–Њ–Љ–µ–љ–і—Г–µ–Љ–∞—П –њ—А–Њ–і–Њ–ї–ґ–Є—В–µ–ї—М–љ–Њ—Б—В—М —Н—А–∞–і–Є–Ї–∞—Ж–Є–Њ–љ–љ–Њ–є —В–µ—А–∞–њ–Є–Є? –Ь–Є–љ–Є–Љ–∞–ї—М–љ–∞—П –њ—А–Њ–і–Њ–ї–ґ–Є—В–µ–ї—М–љ–Њ—Б—В—М —В—А–Њ–є–љ–Њ–є —В–µ—А–∞–њ–Є–Є —Б–Њ—Б—В–∞–≤–ї—П–µ—В 7 –і–љ–µ–є. –Ю–і–љ–∞–Ї–Њ, –њ–Њ —Б–Њ–≤—А–µ–Љ–µ–љ–љ—Л–Љ –і–∞–љ–љ—Л–Љ, –Њ–Ї–∞–Ј–∞–ї–Њ—Б—М, —З—В–Њ –і–ї—П —Б—Е–µ–Љ—Л «–Є–љ–≥–Є–±–Є—В–Њ—А –њ—А–Њ—В–Њ–љ–љ–Њ–є –њ–Њ–Љ–њ—Л – –Ї–ї–∞—А–Є—В—А–Њ–Љ–Є—Ж–Є–љ – –∞–Љ–Њ–Ї—Б–Є—Ж–Є–ї–ї–Є–љ –Є–ї–Є –Љ–µ—В—А–Њ–љ–Є–і–∞–Ј–Њ–ї» 14––і–љ–µ–≤–љ—Л–є –Ї—Г—А—Б –ї–µ—З–µ–љ–Є—П –±–Њ–ї–µ–µ —Н—Д—Д–µ–Ї—В–Є–≤–µ–љ, —З–µ–Љ 7––і–љ–µ–≤–љ—Л–є (–љ–∞ 12%; 95% CI 7 – 17%). –Ґ–µ–Љ –љ–µ –Љ–µ–љ–µ–µ, –њ–Њ —А–µ–Ї–Њ–Љ–µ–љ–і–∞—Ж–Є—П–Љ –Ь–∞–∞—Б—В—А–Є—Е—В—Б–Ї–Њ–≥–Њ –Ї–Њ–љ—Б–µ–љ—Б—Г—Б–∞–3 —В—А–Њ–є–љ–∞—П 7––і–љ–µ–≤–љ–∞—П —В–µ—А–∞–њ–Є—П –Љ–Њ–ґ–µ—В –±—Л—В—М –њ—А–Є–љ—П—В–∞, –µ—Б–ї–Є –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П –≤ –Ї–Њ–љ–Ї—А–µ—В–љ–Њ–є —Б—В—А–∞–љ–µ –Є–ї–Є —А–µ–≥–Є–Њ–љ–µ –њ–Њ–Ї–∞–Ј—Л–≤–∞—О—В, —З—В–Њ –Њ–љ–∞ –≤—Л—Б–Њ–Ї–Њ—Н—Д—Д–µ–Ї—В–Є–≤–љ–∞.
–Ю–±—Й–µ–Є–Ј–≤–µ—Б—В–љ–Њ, —З—В–Њ –љ–∞ —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В—М —Н—А–∞–і–Є–Ї–∞—Ж–Є–Њ–љ–љ–Њ–є —В–µ—А–∞–њ–Є–Є –Њ–Ї–∞–Ј—Л–≤–∞–µ—В –≤–ї–Є—П–љ–Є–µ —А–µ–Ј–Є—Б—В–µ–љ—В–љ–Њ—Б—В—М H.pylori –Ї –∞–љ—В–Є–±–∞–Ї—В–µ—А–Є–∞–ї—М–љ—Л–Љ —Б—А–µ–і—Б—В–≤–∞–Љ. –°–≤—П–Ј—М –∞–љ—В–Є–±–Є–Њ—В–Є–Ї–Њ—А–µ–Ј–Є—Б—В–µ–љ—В–љ–Њ—Б—В–Є –Є –њ—А–Є–Љ–µ–љ–Є–Љ–Њ—Б—В–Є —Б—В–∞–љ–і–∞—А—В–љ–Њ–є —В—А–Њ–є–љ–Њ–є —В–µ—А–∞–њ–Є–Є –њ–µ—А–≤–Њ–є –ї–Є–љ–Є–Є —А–∞—Б–Ї—А—Л—В–∞ –≤ —А–µ—И–µ–љ–Є—П—Е –Ґ—А–µ—В—М–µ–є –Ь–∞–∞—Б—В—А–Є—Е—В—Б–Ї–Њ–є –Ї–Њ–љ—Д–µ—А–µ–љ—Ж–Є–Є (2005 –≥.). –Ю–і–љ–Њ –Є–Ј –њ–Њ–ї–Њ–ґ–µ–љ–Є–є –≥–ї–∞—Б–Є—В, —З—В–Њ –Ї–Њ–Љ–±–Є–љ–∞—Ж–Є—П «–Є–љ–≥–Є–±–Є—В–Њ—А –њ—А–Њ—В–Њ–љ–љ–Њ–є –њ–Њ–Љ–њ—Л – –Ї–ї–∞—А–Є—В—А–Њ–Љ–Є—Ж–Є–љ – –∞–Љ–Њ–Ї—Б–Є—Ж–Є–ї–ї–Є–љ –Є–ї–Є –Љ–µ—В—А–Њ–љ–Є–і–∞–Ј–Њ–ї» –Њ—Б—В–∞–µ—В—Б—П —А–µ–Ї–Њ–Љ–µ–љ–і—Г–µ–Љ–Њ–є —В–µ—А–∞–њ–Є–µ–є –њ–µ—А–≤–Њ–є –ї–Є–љ–Є–Є –і–ї—П –њ–Њ–њ—Г–ї—П—Ж–Є–є —Б —З–∞—Б—В–Њ—В–Њ–є —А–µ–Ј–Є—Б—В–µ–љ—В–љ—Л—Е —И—В–∞–Љ–Љ–Њ–≤ –Ї –Ї–ї–∞—А–Є—В—А–Њ–Љ–Є—Ж–Є–љ—Г –Љ–µ–љ–µ–µ 15–20%. –Т –њ–Њ–њ—Г–ї—П—Ж–Є—П—Е —Б —З–∞—Б—В–Њ—В–Њ–є —А–µ–Ј–Є—Б—В–µ–љ—В–љ–Њ—Б—В–Є –Ї –Љ–µ—В—А–Њ–љ–Є–і–∞–Ј–Њ–ї—Г –Љ–µ–љ–µ–µ 40% –њ—А–µ–і–њ–Њ—З—В–Є—В–µ–ї—М–љ–µ–µ —Б—Е–µ–Љ–∞ «–Є–љ–≥–Є–±–Є—В–Њ—А –њ—А–Њ—В–Њ–љ–љ–Њ–є –њ–Њ–Љ–њ—Л – –Ї–ї–∞—А–Є—В—А–Њ–Љ–Є—Ж–Є–љ – –Љ–µ—В—А–Њ–љ–Є–і–∞–Ј–Њ–ї».
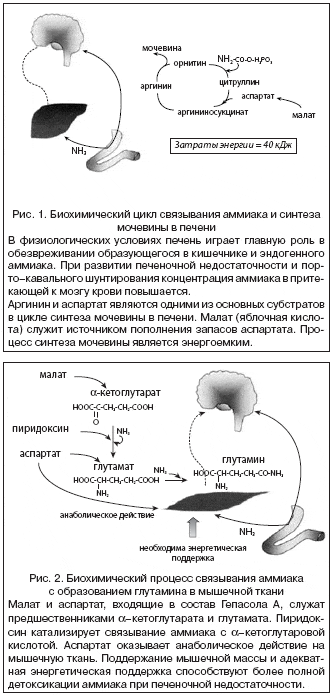
–С–ї–∞–≥–Њ–і–∞—А—П –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П–Љ –Ы.–Т. –Ъ—Г–і—А—П–≤—Ж–µ–≤–Њ–є –Є —Б–Њ–∞–≤—В. –Є–Ј–≤–µ—Б—В–љ—Л –Њ—В–µ—З–µ—Б—В–≤–µ–љ–љ—Л–µ –і–∞–љ–љ—Л–µ –њ–Њ —Г—А–Њ–≤–љ—П–Љ —А–µ–Ј–Є—Б—В–µ–љ—В–љ–Њ—Б—В–Є H.pylori. –Т 2005 –≥–Њ–і—Г –њ—А–Њ—Ж–µ–љ—В —А–µ–Ј–Є—Б—В–µ–љ—В–љ—Л—Е –Ї –Љ–µ—В—А–Њ–љ–Є–і–∞–Ј–Њ–ї—Г —И—В–∞–Љ–Љ–Њ–≤ —Г –≤–Ј—А–Њ—Б–ї—Л—Е –Љ–Њ—Б–Ї–≤–Є—З–µ–є —Б–Њ—Б—В–∞–≤–Є–ї 54,8%, –∞ —А–µ–Ј–Є—Б—В–µ–љ—В–љ—Л—Е –Ї –Ї–ї–∞—А–Є—В—А–Њ–Љ–Є—Ж–Є–љ—Г – 19,3% [–Ы.–Т. –Ъ—Г–і—А—П–≤—Ж–µ–≤–∞, 2006: –њ–µ—А—Б–Њ–љ–∞–ї—М–љ–Њ–µ —Б–Њ–Њ–±—Й–µ–љ–Є–µ]. –Ш—В–∞–Ї, –Є—Б—Е–Њ–і—П –Є–Ј —Б—В–∞–±–Є–ї—М–љ–Њ –≤—Л—Б–Њ–Ї–Њ–≥–Њ —Г—А–Њ–≤–љ—П —А–µ–Ј–Є—Б—В–µ–љ—В–љ–Њ—Б—В–Є H.pylori –Ї –Љ–µ—В—А–Њ–љ–Є–і–∞–Ј–Њ–ї—Г, —Б–Њ—З–µ—В–∞–љ–Є–µ –Ї–ї–∞—А–Є—В—А–Њ–Љ–Є—Ж–Є–љ–∞ —Б –∞–Љ–Њ–Ї—Б–Є—Ж–Є–ї–ї–Є–љ–Њ–Љ —Б–ї—Г–ґ–Є—В –Њ—Б–љ–Њ–≤–Њ–є —В–µ—А–∞–њ–Є–Є –њ–µ—А–≤–Њ–є –ї–Є–љ–Є–Є –≤ –љ–∞—И–µ–є —Б—В—А–∞–љ–µ. –Э–µ—Б–Љ–Њ—В—А—П –љ–∞ –Ї–Њ–ї–µ–±–∞–љ–Є—П —Г—А–Њ–≤–љ—П —А–µ–Ј–Є—Б—В–µ–љ—В–љ–Њ—Б—В–Є H.pylori –Ї –Ї–ї–∞—А–Є—В—А–Њ–Љ–Є—Ж–Є–љ—Г –Њ–Ї–Њ–ї–Њ 15 –Є –і–∞–ґ–µ 20% –≤ –Ь–Њ—Б–Ї–≤–µ –Є –°–∞–љ–Ї—В––Я–µ—В–µ—А–±—Г—А–≥–µ, —Б–ї–µ–і—Г–µ—В —Г–і–µ–ї–Є—В—М –≤–љ–Є–Љ–∞–љ–Є–µ –і–∞–љ–љ—Л–Љ –њ–Њ –Ї–ї–∞—А–Є—В—А–Њ–Љ–Є—Ж–Є–љ–—А–µ–Ј–Є—Б—В–µ–љ—В–љ—Л–Љ —И—В–∞–Љ–Љ–∞–Љ –≤ –≥. –Р–±–∞–Ї–∞–љ – 0% (—В–∞–±–ї. 2). –Э–∞–њ—А–∞—И–Є–≤–∞–µ—В—Б—П –≤—Л–≤–Њ–і –Њ —В–Њ–Љ, —З—В–Њ –≤ —А–∞–Ј–љ—Л—Е —А–µ–≥–Є–Њ–љ–∞—Е –љ–∞—И–µ–є —Б—В—А–∞–љ—Л —А–µ–Ј–Є—Б—В–µ–љ—В–љ–Њ—Б—В—М –Ї –Љ–∞–Ї—А–Њ–ї–Є–і–∞–Љ (–њ–µ—А–µ–Ї—А–µ—Б—В–љ–∞—П –і–ї—П —Н—В–Њ–є –≥—А—Г–њ–њ—Л –∞–љ—В–Є–±–Є–Њ—В–Є–Ї–Њ–≤) –Ї–Њ–ї–µ–±–ї–µ—В—Б—П –Њ—В 0 –і–Њ 19%, —З—В–Њ –≤ —Б–Њ—З–µ—В–∞–љ–Є–Є —Б —Е–Њ—А–Њ—И–Є–Љ–Є —А–µ–Ј—Г–ї—М—В–∞—В–∞–Љ–Є –Њ—В–µ—З–µ—Б—В–≤–µ–љ–љ—Л—Е —А–∞–±–Њ—В –њ–Њ —В–µ—А–∞–њ–Є–Є –њ–µ—А–≤–Њ–є –ї–Є–љ–Є–Є –њ–Њ–Ј–≤–Њ–ї—П–µ—В –Њ–њ–Є—А–∞—В—М—Б—П –љ–∞ –Ї–ї–∞—А–Є—В—А–Њ–Љ–Є—Ж–Є–љ, –Ї–∞–Ї –љ–∞ –±–∞–Ј–Є—Б–љ—Л–є –∞–љ—В–Є–±–Є–Њ—В–Є–Ї.
–Т —Б–ї—Г—З–∞–µ –Њ—В—Б—Г—В—Б—В–≤–Є—П —Г—Б–њ–µ—Е–∞ –ї–µ—З–µ–љ–Є—П —В–µ—А–∞–њ–Є–Є –њ–µ—А–≤–Њ–є –ї–Є–љ–Є–Є –љ–∞–Ј–љ–∞—З–∞–µ—В—Б—П —А–µ–Ј–µ—А–≤–љ–∞—П —Б—Е–µ–Љ–∞ (—В–µ—А–∞–њ–Є—П –≤—В–Њ—А–Њ–є –ї–Є–љ–Є–Є – –Ї–≤–∞–і—А–Њ—В–µ—А–∞–њ–Є—П): –Њ–і–Є–љ –Є–Ј –Є–љ–≥–Є–±–Є—В–Њ—А–Њ–≤ –њ—А–Њ—В–Њ–љ–љ–Њ–є –њ–Њ–Љ–њ—Л (—Б—В–∞–љ–і–∞—А—В–љ–∞—П –і–Њ–Ј–∞ 2 —А/—Б—Г—В.) + –≤–Є—Б–Љ—Г—В–∞ —Б—Г–±—Б–∞–ї–Є—Ж–Є–ї–∞—В/—Б—Г–±—Ж–Є—В—А–∞—В 120 –Љ–≥ 4 —А/—Б—Г—В. + –Љ–µ—В—А–Њ–љ–Є–і–∞–Ј–Њ–ї 500 –Љ–≥ 3 —А/—Б—Г—В. + —В–µ—В—А–∞—Ж–Є–Ї–ї–Є–љ 500 –Љ–≥ 4 —А/—Б—Г—В. –Я—А–µ–і–њ–Њ–ї–∞–≥–∞–µ—В—Б—П, —З—В–Њ —В–∞–Ї–∞—П –Ї–≤–∞–і—А–Њ—В–µ—А–∞–њ–Є—П —Б–њ–Њ—Б–Њ–±–љ–∞ –њ—А–µ–Њ–і–Њ–ї–µ–≤–∞—В—М —А–µ–Ј–Є—Б—В–µ–љ—В–љ–Њ—Б—В—М H.pylori –Ї –Љ–µ—В—А–Њ–љ–Є–і–∞–Ј–Њ–ї—Г. –Ю–і–љ–Є–Љ –Є–Ј –љ–Њ–≤—Л—Е –њ–Њ–ї–Њ–ґ–µ–љ–Є–є –Ґ—А–µ—В—М–µ–≥–Њ –Ь–∞–∞—Б—В—А–Є—Е—В—Б–Ї–Њ–≥–Њ –Ї–Њ–љ—Б–µ–љ—Б—Г—Б–∞ —Б–ї—Г–ґ–Є—В —Г–Ї–∞–Ј–∞–љ–Є–µ –љ–∞ –≤–Њ–Ј–Љ–Њ–ґ–љ–Њ—Б—В—М –њ—А–Є–Љ–µ–љ–µ–љ–Є—П –Ї–≤–∞–і—А–Њ—В–µ—А–∞–њ–Є–Є –≤ –Њ–њ—А–µ–і–µ–ї–µ–љ–љ—Л—Е –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є—Е —Б–Є—В—Г–∞—Ж–Є—П—Е –Ї–∞–Ї —В–µ—А–∞–њ–Є–Є –њ–µ—А–≤–Њ–є –ї–Є–љ–Є–Є (–∞–ї—М—В–µ—А–љ–∞—В–Є–≤–љ–∞—П —В–µ—А–∞–њ–Є—П –њ–µ—А–≤–Њ–є –ї–Є–љ–Є–Є).
–У—А—Г–њ–њ–∞ –Є—Б—Б–ї–µ–і–Њ–≤–∞—В–µ–ї–µ–є –Є–Ј –Ш—Б–њ–∞–љ–Є–Є [D. Marko et al., 2005] –њ—Л—В–∞–ї–∞—Б—М —Г—Б—В–∞–љ–Њ–≤–Є—В—М, –≤ –Ї–∞–Ї–Њ–є –њ–Њ—Б–ї–µ–і–Њ–≤–∞—В–µ–ї—М–љ–Њ—Б—В–Є –±–Њ–ї–µ–µ —Ж–µ–ї–µ—Б–Њ–Њ–±—А–∞–Ј–љ–Њ –њ—А–Њ–≤–Њ–і–Є—В—М —В—А–Њ–є–љ—Г—О –Є –Ї–≤–∞–і—А–Њ—В–µ—А–∞–њ–Є—О. –Т –њ–µ—А–≤–Њ–є —Д–∞–Ј–µ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П 344 –њ–∞—Ж–Є–µ–љ—В–∞ –њ–Њ–ї—Г—З–∞–ї–Є –≤ –Ї–∞—З–µ—Б—В–≤–µ –Є–љ–Є—Ж–Є–∞–ї—М–љ–Њ–є —В–µ—А–∞–њ–Є–Є –Є–ї–Є —Б—В–∞–љ–і–∞—А—В–љ—Г—О —В—А–Њ–є–љ—Г—О —В–µ—А–∞–њ–Є—О, –Є–і–Є —Б—В–∞–љ–і–∞—А—В–љ—Г—О –Ї–≤–∞–і—А–Њ—В–µ—А–∞–њ–Є—О. –£ 47 –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Г—Б–њ–µ—И–љ–∞—П —Н—А–∞–і–Є–Ї–∞—Ж–Є—П H.pylori –љ–µ –±—Л–ї–∞ –і–Њ—Б—В–Є–≥–љ—Г—В–∞, –Є –Є–Љ –љ–∞–Ј–љ–∞—З–Є–ї–Є —В—Г —Б—Е–µ–Љ—Г –ї–µ—З–µ–љ–Є—П, –Ї–Њ—В–Њ—А—Г—О –Њ–љ–Є —А–∞–љ–µ–µ –љ–µ –њ–Њ–ї—Г—З–∞–ї–Є (–њ–Њ—Б–ї–µ —В—А–Њ–є–љ–Њ–є —В–µ—А–∞–њ–Є–Є –Ї–≤–∞–і—А–Њ—В–µ—А–∞–њ–Є—П –Є–ї–Є, –љ–∞–Њ–±–Њ—А–Њ—В – –њ–Њ—Б–ї–µ –Ї–≤–∞–і—А–Њ—В–µ—А–∞–њ–Є–Є —В—А–Њ–є–љ–∞—П —В–µ—А–∞–њ–Є—П). –Я—А–Њ—Ж–µ–љ—В —Н—А–∞–і–Є–Ї–∞—Ж–Є–Є H.pylori (intention to treat) –±—Л–ї 46% (95% CI 24–68%) –і–ї—П —В—А–Њ–є–љ–Њ–є —В–µ—А–∞–њ–Є–Є, –Ї–∞–Ї —В–µ—А–∞–њ–Є–Є –≤—В–Њ—А–Њ–є –ї–Є–љ–Є–Є, –Є 63% (95% CI 42–81%) –і–ї—П –Ї–≤–∞–і—А–Њ—В–µ—А–∞–њ–Є–Є –Ї–∞–Ї —В–µ—А–∞–њ–Є–Є –≤—В–Њ—А–Њ–є –ї–Є–љ–Є–Є. –Я–Њ –і–≤—Г–Љ —Д–∞–Ј–∞–Љ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П –Њ–±—Й–Є–є –њ—А–Њ—Ж–µ–љ—В —Г—Б–њ–µ—И–љ–Њ–є –∞–љ—В–Є—Е–µ–ї–Є–Ї–Њ–±–∞–Ї—В–µ—А–љ–Њ–є —В–µ—А–∞–њ–Є–Є —Б–Њ—Б—В–∞–≤–Є–ї 87% (95% CI 81–92%) –њ—А–Є –њ—А–Њ–≤–µ–і–µ–љ–Є–Є —В—А–Њ–є–љ–Њ–є —В–µ—А–∞–њ–Є–Є –≤ –љ–∞—З–∞–ї–µ –њ—А–Њ—В–Є–≤ 86% (95% CI 80–91%) –њ—А–Є –њ—А–Њ–≤–µ–і–µ–љ–Є–Є –≤ –љ–∞—З–∞–ї–µ –Ї–≤–∞–і—А–Њ—В–µ—А–∞–њ–Є–Є. –Р–≤—В–Њ—А—Л –і–µ–ї–∞—О—В –≤—Л–≤–Њ–і –Њ–± –Њ–і–Є–љ–∞–Ї–Њ–≤–Њ–є —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В–Є —Н—В–Є—Е –і–≤—Г—Е –њ–Њ–і—Е–Њ–і–Њ–≤ –Ї —В–µ—А–∞–њ–Є–Є –Є–љ—Д–µ–Ї—Ж–Є–Є H.pylori, —Е–Њ—В—П, –њ–Њ –Є—Е –њ–Њ–і—Б—З–µ—В–∞–Љ, –і–ї—П –Ш—Б–њ–∞–љ–Є–Є –Љ–µ–љ—М—И—Г—О —Б—В–Њ–Є–Љ–Њ—Б—В—М –Є–Љ–µ–ї–∞ —В–∞–Ї—В–Є–Ї–∞ –њ–µ—А–≤–Є—З–љ–Њ–≥–Њ –њ—А–Њ–≤–µ–і–µ–љ–Є—П –Ї–≤–∞–і—А–Њ—В–µ—А–∞–њ–Є–Є.
–Т —З–µ–Љ –њ—А–µ–Є–Љ—Г—Й–µ—Б—В–≤–Њ —В—А–Њ–є–љ–Њ–є —В–µ—А–∞–њ–Є–Є —Б –Ї–ї–∞—А–Є—В—А–Њ–Љ–Є—Ж–Є–љ–Њ–Љ –њ–µ—А–µ–і –Ї–≤–∞–і—А–Њ—В–µ—А–∞–њ–Є–µ–є? –Т–∞–ґ–љ—Л–Љ –Ї–∞—З–µ—Б—В–≤–Њ–Љ —В—А–Њ–є–љ–Њ–є —В–µ—А–∞–њ–Є–Є —П–≤–ї—П–µ—В—Б—П —Г–і–Њ–≤–ї–µ—В–≤–Њ—А–Є—В–µ–ї—М–љ–∞—П –њ–µ—А–µ–љ–Њ—Б–Є–Љ–Њ—Б—В—М –Є –Њ—В–љ–Њ—Б–Є—В–µ–ї—М–љ–∞—П –њ—А–Њ—Б—В–Њ—В–∞ –њ—А–Є–µ–Љ–∞ –ї–µ–Ї–∞—А—Б—В–≤–µ–љ–љ—Л—Е —Б—А–µ–і—Б—В–≤, —З—В–Њ –Њ–±–µ—Б–њ–µ—З–Є–≤–∞–µ—В –≤—Л–њ–Њ–ї–љ—П–µ–Љ–Њ—Б—В—М —Б—Е–µ–Љ—Л –ї–µ—З–µ–љ–Є—П –њ–∞—Ж–Є–µ–љ—В–Њ–Љ, —В–Њ –µ—Б—В—М –Ї–Њ–Љ–њ–ї–∞–є–љ—Б. –Ф–∞–љ–љ—Л–µ –њ–Њ –њ–µ—А–µ–љ–Њ—Б–Є–Љ–Њ—Б—В–Є –Є –Ї–Њ–Љ–њ–ї–∞–µ–љ—В–љ–Њ—Б—В–Є —А–∞–Ј–ї–Є—З–љ—Л—Е —Б—Е–µ–Љ —Н—А–∞–і–Є–Ї–∞—Ж–Є–Њ–љ–љ–Њ–є —В–µ—А–∞–њ–Є–Є H.pylori –њ—А–µ–і—Б—В–∞–≤–ї–µ–љ—Л –≤ —В–∞–±–ї–Є—Ж–µ 3 [–њ–Њ M.B. Fennerty et al., 1999].
–Ъ–ї–∞—А–Є—В—А–Њ–Љ–Є—Ж–Є–љ –Њ–±–ї–∞–і–∞–µ—В —А—П–і–Њ–Љ —Б–≤–Њ–є—Б—В–≤, –Ї–Њ—В–Њ—А—Л–µ –і–µ–ї–∞—О—В –µ–≥–Њ –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є–µ –њ—А–Є —Н—А–∞–і–Є–Ї–∞—Ж–Є–Њ–љ–љ–Њ–є —В–µ—А–∞–њ–Є–Є H.pylori —Б—В–Њ–ї—М —Г—Б–њ–µ—И–љ—Л–Љ. –Ъ–ї–∞—А–Є—В—А–Њ–Љ–Є—Ж–Є–љ –Њ—В–љ–Њ—Б–Є—В—Б—П –Ї —Б–Њ–≤—А–µ–Љ–µ–љ–љ—Л–Љ –њ—А–µ–і—Б—В–∞–≤–Є—В–µ–ї—П–Љ –Љ–∞–Ї—А–Њ–ї–Є–і–Њ–≤ —Б —И–Є—А–Њ–Ї–Є–Љ –∞–љ—В–Є–Љ–Є–Ї—А–Њ–±–љ—Л–Љ —Б–њ–µ–Ї—В—А–Њ–Љ –і–µ–є—Б—В–≤–Є—П –Є –ї–Є–њ–Њ—Д–Є–ї—М–љ–Њ—Б—В—М—О, —З—В–Њ –Њ–±–µ—Б–њ–µ—З–Є–≤–∞–µ—В –ї–µ–≥–Ї–Њ—Б—В—М –њ—А–Њ–љ–Є–Ї–љ–Њ–≤–µ–љ–Є—П –ї–µ–Ї–∞—А—Б—В–≤–µ–љ–љ–Њ–≥–Њ —Б—А–µ–і—Б—В–≤–∞ —З–µ—А–µ–Ј –≥–Є—Б—В–Њ–≥–µ–Љ–∞—В–Є—З–µ—Б–Ї–Є–µ –±–∞—А—М–µ—А—Л. –Ъ–Њ–љ—Ж–µ–љ—В—А–∞—Ж–Є—П –Ї–ї–∞—А–Є—В—А–Њ–Љ–Є—Ж–Є–љ–∞ –≤ —В–Ї–∞–љ—П—Е –≤ 10–100 —А–∞–Ј –њ—А–µ–≤—Л—И–∞–µ—В –Ї–Њ–љ—Ж–µ–љ—В—А–∞—Ж–Є—О –≤ –њ–ї–∞–Ј–Љ–µ –Ї—А–Њ–≤–Є, —З—В–Њ –≤–µ—Б—М–Љ–∞ –∞–Ї—В—Г–∞–ї—М–љ–Њ –њ–Њ –Њ—В–љ–Њ—И–µ–љ–Є—О –Ї –Ј–∞–і–∞—З–µ —Н—А–∞–і–Є–Ї–∞—Ж–Є–Є H.pylori –≤ —Б–ї–Є–Ј–Є—Б—В–Њ–є –Њ–±–Њ–ї–Њ—З–Ї–µ –ґ–µ–ї—Г–і–Ї–∞. –Т –Њ—В–ї–Є—З–Є–µ –Њ—В –і—А—Г–≥–Є—Е –Љ–∞–Ї—А–Њ–ї–Є–і–Њ–≤, –Ї–Њ—В–Њ—А—Л–µ –≤ –Ї–Є—Б–ї–Њ–є —Б—А–µ–і–µ –њ–Њ–і–≤–µ—А–≥–∞—О—В—Б—П —Г—Б–Є–ї–µ–љ–љ–Њ–Љ—Г –≥–Є–і—А–Њ–ї–Є–Ј—Г, –Ї–ї–∞—А–Є—В—А–Њ–Љ–Є—Ж–Є–љ —Г—Б—В–Њ–є—З–Є–≤ –Ї –Ї–Є—Б–ї–Њ—В–µ –ґ–µ–ї—Г–і–Њ—З–љ–Њ–≥–Њ —Б–Њ–Ї–∞ (–≤ 100 —А–∞–Ј —Г—Б—В–Њ–є—З–Є–≤–µ–µ –њ–Њ —Б—А–∞–≤–љ–µ–љ–Є—О —Б —Н—А–Є—В—А–Њ–Љ–Є—Ж–Є–љ–Њ–Љ), —З—В–Њ –Ї—А–∞–є–љ–µ –≤–∞–ґ–љ–Њ, —Г—З–Є—В—Л–≤–∞—П –Њ—Б–Њ–±—Г—О «—Н–Ї–Њ–ї–Њ–≥–Є—З–µ—Б–Ї—Г—О –љ–Є—И—Г» H.pylori. –Ь–Є–љ–Є–Љ–∞–ї—М–љ–∞—П –њ–Њ–і–∞–≤–ї—П—О—Й–∞—П –Ї–Њ–љ—Ж–µ–љ—В—А–∞—Ж–Є—П –Ї–ї–∞—А–Є—В—А–Њ–Љ–Є—Ж–Є–љ–∞, –њ—А–Є –Ї–Њ—В–Њ—А–Њ–є –њ—А–Њ–Є—Б—Е–Њ–і–Є—В –њ–Њ–і–∞–≤–ї–µ–љ–Є–µ 90% –Є–Ј–Њ–ї—П—В–Њ–≤ H.pylori, —Б–Њ—Б—В–∞–≤–ї—П–µ—В 0,03 –Љ–Ї–≥/–Љ–ї. –Я–Њ –і–∞–љ–љ—Л–Љ W.L. Peterson –Є —Б–Њ–∞–≤—В. (1993), –Љ–Њ–љ–Њ—В–µ—А–∞–њ–Є—П –Ї–ї–∞—А–Є—В—А–Њ–Љ–Є—Ж–Є–љ–Њ–Љ –њ—А–Є–≤–µ–ї–∞ –Ї —Г–љ–Є—З—В–Њ–ґ–µ–љ–Є—О H.pylori –≤ 54% —Б–ї—Г—З–∞–µ–≤; D.Y. Graham –Є M.P. Dore (1998) –љ–∞–Ј—Л–≤–∞—О—В 15% —Н—А–∞–і–Є–Ї–∞—Ж–Є–Є H.pylori, —З—В–Њ –≤—Б–µ —А–∞–≤–љ–Њ –њ—А–µ–і—Б—В–∞–≤–ї—П–µ—В —Б–Њ–±–Њ–є –≤–њ–µ—З–∞—В–ї—П—О—Й–Є–є —А–µ–Ј—Г–ї—М—В–∞—В –і–ї—П –Љ–Њ–љ–Њ—В–µ—А–∞–њ–Є–Є.
–Я—А–Є –Њ–і–љ–Њ–≤—А–µ–Љ–µ–љ–љ–Њ–Љ –љ–∞–Ј–љ–∞—З–µ–љ–Є–Є –Ї–Њ–Љ–њ–Њ–љ–µ–љ—В—Л —Б—В–∞–љ–і–∞—А—В–љ–Њ–є —В—А–Њ–є–љ–Њ–є —В–µ—А–∞–њ–Є–Є —Г—Б–Є–ї–Є–≤–∞—О—В —Н—Д—Д–µ–Ї—В –і—А—Г–≥ –і—А—Г–≥–∞, —В–Њ –µ—Б—В—М –Њ–±–ї–∞–і–∞—О—В —Б–њ–Њ—Б–Њ–±–љ–Њ—Б—В—М—О –Ї —Б–Є–љ–µ—А–≥–Є–Ј–Љ—Г. –Ґ–∞–Ї, –Љ–µ—В–∞–±–Њ–ї–Є–Ј–Љ –Њ–Љ–µ–њ—А–∞–Ј–Њ–ї–∞ –Њ—Б—Г—Й–µ—Б—В–≤–ї—П–µ—В—Б—П CYP3A –Є–Ј–Њ—Д–Њ—А–Љ–Њ–є —Ж–Є—В–Њ—Е—А–Њ–Љ–∞ P450, –∞ –Ї–ї–∞—А–Є—В—А–Њ–Љ–Є—Ж–Є–љ, –Ї–∞–Ї –Є –±–Њ–ї—М—И–Є–љ—Б—В–≤–Њ –Љ–∞–Ї—А–Њ–ї–Є–і–Њ–≤, –Є–љ–≥–Є–±–Є—А—Г–µ—В –∞–Ї—В–Є–≤–љ–Њ—Б—В—М CYP3A, –њ–Њ–і–∞–≤–ї—П—П –Љ–µ—В–∞–±–Њ–ї–Є–Ј–Љ –Њ–Љ–µ–њ—А–∞–Ј–Њ–ї–∞. –≠—Д—Д–µ–Ї—В—Л –≤–Ј–∞–Є–Љ–љ–Њ–≥–Њ —Г—Б–Є–ї–µ–љ–Є—П –Њ–Љ–µ–њ—А–∞–Ј–Њ–ї–∞ –Є –Ї–ї–∞—А–Є—В—А–Њ–Љ–Є—Ж–Є–љ–∞ —Е–Њ—А–Њ—И–Њ –Є–Ј—Г—З–µ–љ—Л, –≤ —В–Њ–Љ —З–Є—Б–ї–µ –≤ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є L. Gustavson –Є —Б–Њ–∞–≤—В. (1995). –°—А–µ–і–љ–Є–µ –Ј–љ–∞—З–µ–љ–Є—П –њ–ї–Њ—Й–∞–і–Є –њ–Њ–і –Ї—А–Є–≤–Њ–є –Ј–∞–≤–Є—Б–Є–Љ–Њ—Б—В–Є –Ї–Њ–љ—Ж–µ–љ—В—А–∞—Ж–Є–Є –Њ–Љ–µ–њ—А–∞–Ј–Њ–ї–∞ –≤ –њ–ї–∞–Ј–Љ–µ –Њ—В –≤—А–µ–Љ–µ–љ–Є (AUC) –±—Л–ї–Є –љ–∞ 89% –±–Њ–ї—М—И–µ, –∞ —Б—А–µ–і–љ–Є–µ –Ј–љ–∞—З–µ–љ–Є—П –Љ–∞–Ї—Б–Є–Љ–∞–ї—М–љ–Њ–є –Ї–Њ–љ—Ж–µ–љ—В—А–∞—Ж–Є–Є –љ–∞ 30% –±–Њ–ї—М—И–µ –њ—А–Є —Б–Њ—З–µ—В–∞–љ–љ–Њ–Љ –љ–∞–Ј–љ–∞—З–µ–љ–Є–Є –Ї–ї–∞—А–Є—В—А–Њ–Љ–Є—Ж–Є–љ–∞ –Є –Њ–Љ–µ–њ—А–∞–Ј–Њ–ї–∞ (–њ–Њ —Б—А–∞–≤–љ–µ–љ–Є—О —Б –њ—А–Є–µ–Љ–Њ–Љ —В–Њ–ї—М–Ї–Њ –Њ–Љ–µ–њ—А–∞–Ј–Њ–ї–∞). –Ф–ї—П –Ї–ї–∞—А–Є—В—А–Њ–Љ–Є—Ж–Є–љ–∞ —Б—А–µ–і–љ–Є–µ –Ј–љ–∞—З–µ–љ–Є—П AUC –±—Л–ї–Є –љ–∞ 15% –±–Њ–ї—М—И–µ –њ—А–Є –Њ–і–љ–Њ–≤—А–µ–Љ–µ–љ–љ–Њ–Љ –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є–Є —Б –Њ–Љ–µ–њ—А–∞–Ј–Њ–ї–Њ–Љ (–њ–Њ —Б—А–∞–≤–љ–µ–љ–Є—О —Б –њ—А–Є–Љ–µ–љ–µ–љ–Є–µ–Љ –Ї–ї–∞—А–Є—В—А–Њ–Љ–Є—Ж–Є–љ–∞ –Є –њ–ї–∞—Ж–µ–±–Њ) (—В–∞–±–ї. 4). –Ґ–Ї–∞–љ–µ–≤—Л–µ –Ї–Њ–љ—Ж–µ–љ—В—А–∞—Ж–Є–Є –Ї–ї–∞—А–Є—В—А–Њ–Љ–Є—Ж–Є–љ–∞ —В–∞–Ї–ґ–µ –±—Л–ї–Є –і–Њ—Б—В–Њ–≤–µ—А–љ–Њ –≤—Л—И–µ –њ—А–Є –Њ–і–љ–Њ–≤—А–µ–Љ–µ–љ–љ–Њ–Љ –љ–∞–Ј–љ–∞—З–µ–љ–Є–Є –Є–љ–≥–Є–±–Є—В–Њ—А–∞ –њ—А–Њ—В–Њ–љ–љ–Њ–є –њ–Њ–Љ–њ—Л –њ–Њ —Б—А–∞–≤–љ–µ–љ–Є—О —Б –њ–ї–∞—Ж–µ–±–Њ. –Т–∞–ґ–љ–Њ –Њ—В–Љ–µ—В–Є—В—М, —З—В–Њ –≤ –±–Є–Њ–њ—Б–Є–є–љ–Њ–Љ –Љ–∞—В–µ—А–Є–∞–ї–µ –Є–Ј —В–µ–ї–∞ –ґ–µ–ї—Г–і–Ї–∞ –∞–љ—В–Є–±–Є–Њ—В–Є–Ї–∞ –±—Л–ї–Њ –і–Њ—Б—В–Њ–≤–µ—А–љ–Њ –±–Њ–ї—М—И–µ, —З–µ–Љ –≤ –±–Є–Њ–њ—В–∞—В–∞—Е –Є–Ј –∞–љ—В—А–∞–ї—М–љ–Њ–≥–Њ –Њ—В–і–µ–ї–∞. –Ґ–∞–Ї–Є–Љ –Њ–±—А–∞–Ј–Њ–Љ, —Б–Њ–Ј–і–∞—О—В—Б—П —Г—Б–ї–Њ–≤–Є—П –і–ї—П –љ–∞–Є–±–Њ–ї–µ–µ —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ–≥–Њ —Г–љ–Є—З—В–Њ–ґ–µ–љ–Є—П H.pylori, –Ї–Њ—В–Њ—А—Л–є –њ–µ—А–µ–Љ–µ—Й–∞–µ—В—Б—П –≤ —В–µ–ї–Њ –ґ–µ–ї—Г–і–Ї–∞ –Є–Ј –µ–≥–Њ –і–Є—Б—В–∞–ї—М–љ—Л—Е –Њ—В–і–µ–ї–Њ–≤ –њ–Њ–і –≤–Њ–Ј–і–µ–є—Б—В–≤–Є–µ–Љ –Є–љ–≥–Є–±–Є—В–Њ—А–∞ –њ—А–Њ—В–Њ–љ–љ–Њ–є –њ–Њ–Љ–њ—Л –Є –∞–Ї—В–Є–≤–љ–Њ–≥–Њ –Є–Ј–Љ–µ–љ–µ–љ–Є—П —А–Э —Б—А–µ–і—Л. –Я—А–Є –∞–љ–∞–ї–Є–Ј–µ –Ї–Њ–љ—Ж–µ–љ—В—А–∞—Ж–Є–Є –Ї–ї–∞—А–Є—В—А–Њ–Љ–Є—Ж–Є–љ–∞ –≤ –ґ–µ–ї—Г–і–Њ—З–љ–Њ–є —Б–ї–Є–Ј–Є –Њ–љ–∞ —В–∞–Ї–ґ–µ –±—Л–ї–∞ –і–Њ—Б—В–Њ–≤–µ—А–љ–Њ –≤—Л—И–µ –њ—А–Є —Б–Њ—З–µ—В–∞–љ–љ–Њ–Љ –љ–∞–Ј–љ–∞—З–µ–љ–Є–Є —Б –Њ–Љ–µ–њ—А–∞–Ј–Њ–ї–Њ–Љ, —З–µ–Љ —Б –њ–ї–∞—Ж–µ–±–Њ.
–†–∞—Б—Б–Љ–Њ—В—А–Є–Љ, –Ї–∞–Ї –Љ–µ–љ—П–µ—В—Б—П —Д–∞—А–Љ–∞–Ї–Њ–Ї–Є–љ–µ—В–Є–Ї–∞ –Ї–Њ–Љ–њ–Њ–љ–µ–љ—В–Њ–≤ —В—А–Њ–є–љ–Њ–є —В–µ—А–∞–њ–Є–Є – –∞–Љ–Њ–Ї—Б–Є—Ж–Є–ї–ї–Є–љ–∞, –Ї–ї–∞—А–Є—В—А–Њ–Љ–Є—Ж–Є–љ–∞ –Є –ї–∞–љ—Б–Њ–њ—А–∞–Ј–Њ–ї–∞ –њ—А–Є –Њ–і–љ–Њ–≤—А–µ–Љ–µ–љ–љ–Њ–Љ –њ—А–Є–Љ–µ–љ–µ–љ–Є–Є. –Ш—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ D. Mainz –Є —Б–Њ–∞–≤—В. (2002) –≤—Л–њ–Њ–ї–љ–µ–љ–Њ —Г –Ј–і–Њ—А–Њ–≤—Л—Е –і–Њ–±—А–Њ–≤–Њ–ї—М—Ж–µ–≤ –Є –Є–Љ–µ–ї–Њ –њ–µ—А–µ–Ї—А–µ—Б—В–љ—Л–є –і–Є–Ј–∞–є–љ (–≤—Б–µ –і–Њ–±—А–Њ–≤–Њ–ї—М—Ж—Л –њ–Њ—Б–ї–µ–і–Њ–≤–∞—В–µ–ї—М–љ–Њ, –≤—Л–і–µ—А–ґ–Є–≤–∞—П –Є–љ—В–µ—А–≤–∞–ї—Л –њ–Њ 9 –і–љ–µ–є –±–µ–Ј –њ—А–Є–µ–Љ–∞ –ї—О–±—Л—Е –ї–µ–Ї–∞—А—Б—В–≤, –њ—А–Є–љ–Є–Љ–∞–ї–Є 1) –ї–∞–љ—Б–Њ–њ—А–∞–Ј–Њ–ї (60 –Љ–≥/—Б—Г—В.) –Є –њ–ї–∞—Ж–µ–±–Њ –≤–Љ–µ—Б—В–Њ –∞–љ—В–Є–±–Є–Њ—В–Є–Ї–Њ–≤; 2) –∞–Љ–Њ–Ї—Б–Є—Ж–Є–ї–ї–Є–љ (2000 –Љ–≥/—Б—Г—В.) –Є –њ–ї–∞—Ж–µ–±–Њ –≤–Љ–µ—Б—В–Њ –ї–∞–љ—Б–Њ–њ—А–∞–Ј–Њ–ї–∞ –Є –Ї–ї–∞—А–Є—В—А–Њ–Љ–Є—Ж–Є–љ–∞; 3) –Ї–ї–∞—А–Є—В—А–Њ–Љ–Є—Ж–Є–љ (1000 –Љ–≥/—Б—Г—В.) –Є –њ–ї–∞—Ж–µ–±–Њ –≤–Љ–µ—Б—В–Њ –ї–∞–љ—Б–Њ–њ—А–∞–Ј–Њ–ї–∞ –Є –∞–Љ–Њ–Ї—Б–Є—Ж–Є–ї–ї–Є–љ–∞ –Є 4) –ї–∞–љ—Б–Њ–њ—А–∞–Ј–Њ–ї (60 –Љ–≥/—Б—Г—В.) —Б –∞–Љ–Њ–Ї—Б–Є—Ж–Є–ї–ї–Є–љ–Њ–Љ (2000 –Љ–≥/—Б—Г—В.) –Є –Ї–ї–∞—А–Є—В—А–Њ–Љ–Є—Ж–Є–љ–Њ–Љ (1000 –Љ–≥/—Б—Г—В.). –Ф–ї—П –ї–∞–љ—Б–Њ–њ—А–∞–Ј–Њ–ї–∞ –≤—А–µ–Љ—П –њ–Њ–ї—Г–ґ–Є–Ј–љ–Є —Б—Г—Й–µ—Б—В–≤–µ–љ–љ–Њ —Г–і–ї–Є–љ–Є–ї–Њ—Б—М (—Б 1,46 —З –і–Њ 1,7 —З –њ—А–Є –Ї–Њ–Љ–±–Є–љ–Є—А–Њ–≤–∞–љ–љ–Њ–Љ –њ—А–Є–µ–Љ–µ), —Г–≤–µ–ї–Є—З–Є–ї–∞—Б—М –Є –њ–ї–Њ—Й–∞–і—М –њ–Њ–і –Ї—А–Є–≤–Њ–є –Ј–∞–≤–Є—Б–Є–Љ–Њ—Б—В–Є –Ї–Њ–љ—Ж–µ–љ—В—А–∞—Ж–Є–Є –Њ—В –≤—А–µ–Љ–µ–љ–Є (AUC: —Б 3,65 –і–Њ 4,59 –Љ–≥—Е—З/–ї –њ—А–Є –Ї–Њ–Љ–±–Є–љ–Є—А–Њ–≤–∞–љ–љ–Њ–Љ –њ—А–Є–µ–Љ–µ). –Ф–ї—П 14––≥–Є–і—А–Њ–Ї—Б–Є–Ї–ї–∞—А–Є—В—А–Њ–Љ–Є—Ж–Є–љ–∞ (–∞–Ї—В–Є–≤–љ—Л–є –Љ–µ—В–∞–±–Њ–ї–Є—В –Ї–ї–∞—А–Є—В—А–Њ–Љ–Є—Ж–Є–љ–∞) –Љ–∞–Ї—Б–Є–Љ–∞–ї—М–љ–∞—П –Ї–Њ–љ—Ж–µ–љ—В—А–∞—Ж–Є—П –≤–Њ–Ј—А–Њ—Б–ї–∞ (—Б 0,95 –і–Њ 1,18 –Љ–≥/–ї –њ—А–Є –Ї–Њ–Љ–±–Є–љ–Є—А–Њ–≤–∞–љ–љ–Њ–Љ –њ—А–Є–µ–Љ–µ), –≤—Л—А–Њ—Б–ї–∞ –Є AUC (—Б 8,3 –і–Њ 10,5 –Љ–≥—Е—З/–ї –њ—А–Є –Ї–Њ–Љ–±–Є–љ–Є—А–Њ–≤–∞–љ–љ–Њ–Љ –њ—А–Є–µ–Љ–µ). –Я—А–Є—З–µ–Љ –∞–≤—В–Њ—А—Л –љ–µ –Њ–±–љ–∞—А—Г–ґ–Є–ї–Є –Є–Ј–Љ–µ–љ–µ–љ–Є—П –Љ–∞–Ї—Б–Є–Љ–∞–ї—М–љ–Њ–є –Ї–Њ–љ—Ж–µ–љ—В—А–∞—Ж–Є–Є –Є AUC –Ї–ї–∞—А–Є—В—А–Њ–Љ–Є—Ж–Є–љ–∞, –њ—А–Є —Н—В–Њ–Љ –≤—Л—А–Њ—Б–ї–Њ –Ј–љ–∞—З–µ–љ–Є–µ –Ґmax –Ї–ї–∞—А–Є—В—А–Њ–Љ–Є—Ж–Є–љ–∞. D. Mainz –Є —Б–Њ–∞–≤—В. —Б—З–Є—В–∞—О—В, —З—В–Њ –Њ–њ–Є—Б–∞–љ–љ—Л–µ –Є–Ј–Љ–µ–љ–µ–љ–Є—П –±–Њ–ї–µ–µ —Е–∞—А–∞–Ї—В–µ—А–љ—Л –і–ї—П —Г–і–ї–Є–љ–µ–љ–Є—П –∞–±—Б–Њ—А–±—Ж–Є–Є –Ї–ї–∞—А–Є—В—А–Њ–Љ–Є—Ж–Є–љ–∞ –њ—А–Є —Г—Б–ї–Њ–≤–Є–Є –Ї–Њ–Љ–±–Є–љ–Є—А–Њ–≤–∞–љ–љ–Њ–≥–Њ –њ—А–Є–µ–Љ–∞ –ї–µ–Ї–∞—А—Б—В–≤–µ–љ–љ—Л—Е —Б—А–µ–і—Б—В–≤. –Ъ–Њ–љ—Ж–µ–љ—В—А–∞—Ж–Є–Є –∞–Љ–Њ–Ї—Б–Є—Ж–Є–ї–ї–Є–љ–∞ –љ–µ—Б–Ї–Њ–ї—М–Ї–Њ –≤–Њ–Ј—А–Њ—Б–ї–Є –њ—А–Є —Б–Њ—З–µ—В–∞–љ–љ–Њ–Љ –њ—А–Є–µ–Љ–µ –ї–µ–Ї–∞—А—Б—В–≤–µ–љ–љ—Л—Е —Б—А–µ–і—Б—В–≤, –љ–Њ —А–∞–Ј–љ–Є—Ж–∞ –љ–µ –±—Л–ї–∞ —Б—В–∞—В–Є—Б—В–Є—З–µ—Б–Ї–Є –і–Њ—Б—В–Њ–≤–µ—А–љ–Њ–є. –Ґ–∞–Ї–Є–Љ –Њ–±—А–∞–Ј–Њ–Љ, –±—Л–ї–Њ –њ–Њ–Ї–∞–Ј–∞–љ–Њ, —З—В–Њ —Д–∞—А–Љ–∞–Ї–Њ–Ї–Є–љ–µ—В–Є–Ї–∞ –∞–Љ–Њ–Ї—Б–Є—Ж–Є–ї–ї–Є–љ–∞ (–≤ –Њ—В–ї–Є—З–Є–µ –Њ—В –Ї–ї–∞—А–Є—В—А–Њ–Љ–Є—Ж–Є–љ–∞) –љ–µ –Є–Ј–Љ–µ–љ—П–µ—В—Б—П –њ—А–Є –љ–∞–Ј–љ–∞—З–µ–љ–Є–Є —Б—В–∞–љ–і–∞—А—В–љ–Њ–є —Н—А–∞–і–Є–Ї–∞—Ж–Є–Њ–љ–љ–Њ–є —В–µ—А–∞–њ–Є–Є. –Э–µ—Б–Љ–Њ—В—А—П –љ–∞ –і—А—Г–≥–Њ–µ –Њ–±—К—П—Б–љ–µ–љ–Є–µ –њ—А–Є—А–Њ–і—Л —В–∞–Ї–Њ–≥–Њ —Д–µ–љ–Њ–Љ–µ–љ–∞, –∞–≤—В–Њ—А—Л –µ—Й–µ —А–∞–Ј –њ—А–Њ–і–µ–Љ–Њ–љ—Б—В—А–Є—А–Њ–≤–∞–ї–Є —Г–≤–µ–ї–Є—З–µ–љ–Є–µ —Б—Л–≤–Њ—А–Њ—В–Њ—З–љ—Л—Е –Ї–Њ–љ—Ж–µ–љ—В—А–∞—Ж–Є–є –Є–љ–≥–Є–±–Є—В–Њ—А–∞ –њ—А–Њ—В–Њ–љ–љ–Њ–є –њ–Њ–Љ–њ—Л –Є –∞–Ї—В–Є–≤–љ–Њ–≥–Њ –Љ–µ—В–∞–±–Њ–ї–Є—В–∞ –Ї–ї–∞—А–Є—В—А–Њ–Љ–Є—Ж–Є–љ–∞ –њ—А–Є –Њ–і–љ–Њ–≤—А–µ–Љ–µ–љ–љ–Њ–Љ –љ–∞–Ј–љ–∞—З–µ–љ–Є–Є.
–Ґ–∞–Ї–Є–Љ –Њ–±—А–∞–Ј–Њ–Љ, —Н–Љ–њ–Є—А–Є—З–µ—Б–Ї–Є —А–∞–Ј—А–∞–±–Њ—В–∞–љ–љ—Л–є —Б–Њ—Б—В–∞–≤ —В—А–Њ–є–љ–Њ–є —В–µ—А–∞–њ–Є–Є –њ–Њ–ї—Г—З–Є–ї —Б–µ—А—М–µ–Ј–љ–Њ–µ —Д–∞—А–Љ–∞–Ї–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Њ–µ –Њ–±–Њ—Б–љ–Њ–≤–∞–љ–Є–µ: –Є–љ–≥–Є–±–Є—В–Њ—А –њ—А–Њ—В–Њ–љ–љ–Њ–є –њ–Њ–Љ–њ—Л, –Ї–ї–∞—А–Є—В—А–Њ–Љ–Є—Ж–Є–љ –Є –∞–Љ–Њ–Ї—Б–Є—Ж–Є–ї–ї–Є–љ –≤ —Б—В–∞–љ–і–∞—А—В–љ–Њ–є —Б—Е–µ–Љ–µ –≤–Ј–∞–Є–Љ–љ–Њ —Г—Б–Є–ї–Є–≤–∞—О—В –∞–љ—В–Є—Е–µ–ї–Є–Ї–Њ–±–∞–Ї—В–µ—А–љ—Л–є —Н—Д—Д–µ–Ї—В –і—А—Г–≥ –і—А—Г–≥–∞.
–≠—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В—М —В—А–Њ–є–љ–Њ–є —Б—Е–µ–Љ—Л, —Б–Њ–і–µ—А–ґ–∞—Й–µ–є –Ї–ї–∞—А–Є—В—А–Њ–Љ–Є—Ж–Є–љ –Є –∞–Љ–Њ–Ї—Б–Є—Ж–Є–ї–ї–Є–љ, –≤ –Ї–∞—З–µ—Б—В–≤–µ –њ–µ—А–≤–Њ–є –ї–Є–љ–Є–Є –Љ–µ–і–Є–Ї–∞–Љ–µ–љ—В–Њ–Ј–љ–Њ–є —В–µ—А–∞–њ–Є–Є –њ—А–Њ—В–Є–≤ H.pylori, –љ–µ –њ–Њ–і–ї–µ–ґ–Є—В —Б–Њ–Љ–љ–µ–љ–Є—О. –£—Б–њ–µ—И–љ–Њ—Б—В—М —В–∞–Ї–Њ–≥–Њ –ї–µ—З–µ–љ–Є—П –Ј–∞–≤–Є—Б–Є—В –Њ—В –њ—А–Њ–≤–µ—А–µ–љ–љ–Њ–є –≤—А–µ–Љ–µ–љ–µ–Љ –Ї–Њ–Љ–±–Є–љ–∞—Ж–Є–Є –∞–љ—В–Є–±–Є–Њ—В–Є–Ї–Њ–≤, —Б—Г—Й–µ—Б—В–≤–µ–љ–љ–Њ–µ –Ј–љ–∞—З–µ–љ–Є–µ –Є–Љ–µ–µ—В —Б–њ–Њ—Б–Њ–±–љ–Њ—Б—В—М –Ї–ї–∞—А–Є—В—А–Њ–Љ–Є—Ж–Є–љ–∞ –Є –Є–љ–≥–Є–±–Є—В–Њ—А–∞ –њ—А–Њ—В–Њ–љ–љ–Њ–є –њ–Њ–Љ–њ—Л —Г—Б–Є–ї–Є–≤–∞—В—М —Г—З–∞—Б—В–Є–µ –і—А—Г–≥ –і—А—Г–≥–∞.
–Т –љ–∞—И–µ–є —Б—В—А–∞–љ–µ –Њ—Б—В—А—Л–Љ –Њ—Б—В–∞–µ—В—Б—П –≤–Њ–њ—А–Њ—Б —Б—В—А–Њ–≥–Њ–≥–Њ —Б–Њ–±–ї—О–і–µ–љ–Є—П —Б—В–∞–љ–і–∞—А—В–Њ–≤ –љ–∞–Ј–љ–∞—З–µ–љ–Є—П —Н—А–∞–і–Є–Ї–∞—Ж–Є–Њ–љ–љ–Њ–є —В–µ—А–∞–њ–Є–Є –Є–љ—Д–µ–Ї—Ж–Є–Є H.pylori –Ї–∞–Ї –њ–Њ —Б–Њ—Б—В–∞–≤—Г —Б—Е–µ–Љ—Л, —В–∞–Ї –Є –њ–Њ –і–Њ–Ј–∞–Љ –Є –і–ї–Є—В–µ–ї—М–љ–Њ—Б—В–Є –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є—П. –Я—А–Є —Н—В–Њ–Љ –≤—А–∞—З—Г –Њ–±—Й–µ–є –њ—А–∞–Ї—В–Є–Ї–Є —Б–ї–µ–і—Г–µ—В –Њ—А–Є–µ–љ—В–Є—А–Њ–≤–∞—В—М—Б—П –љ–∞ –≤—Л—Б–Њ–Ї—Г—О –і–Њ–Ј—Г –Ї–ї–∞—А–Є—В—А–Њ–Љ–Є—Ж–Є–љ–∞ (500 –Љ–≥ 2 —А/—Б—Г—В.) –Є –±–Њ–ї—М—И—Г—О –њ—А–Њ–і–Њ–ї–ґ–Є—В–µ–ї—М–љ–Њ—Б—В—М –Ї—Г—А—Б–∞ —В–µ—А–∞–њ–Є–Є (10–14 –і–љ–µ–є). –Ш–Љ–µ–љ–љ–Њ —В–∞–Ї–∞—П –њ—А–∞–Ї—В–Є–Ї–∞ —Н—А–∞–і–Є–Ї–∞—Ж–Є–Њ–љ–љ–Њ–є —В–µ—А–∞–њ–Є–Є –њ–Њ–Ј–≤–Њ–ї–Є—В –і–Њ–±–Є—В—М—Б—П –Є–Ј–ї–µ—З–µ–љ–Є—П —Е—А–Њ–љ–Є—З–µ—Б–Ї–Њ–≥–Њ –≥–∞—Б—В—А–Є—В–∞, —Б–љ–Є–ґ–µ–љ–Є—П —З–∞—Б—В–Њ—В—Л —А–µ—Ж–Є–і–Є–≤–Њ–≤ —П–Ј–≤–µ–љ–љ–Њ–є –±–Њ–ї–µ–Ј–љ–Є, —Б–љ–Є–ґ–µ–љ–Є—П —З–∞—Б—В–Њ—В—Л –Њ—Б–ї–Њ–ґ–љ–µ–љ–Є–є —П–Ј–≤–µ–љ–љ–Њ–є –±–Њ–ї–µ–Ј–љ–Є –Є, –≤–Њ–Ј–Љ–Њ–ґ–љ–Њ, —Г—Б–њ–µ—И–љ–Њ–є –њ—А–Њ—Д–Є–ї–∞–Ї—В–Є–Ї–Є —А–∞–Ї–∞ –ґ–µ–ї—Г–і–Ї–∞.