Задержка эвакуации желудочного содержимого, обусловленная снижением тонуса желудочной стенки, стойким спазмом привратника или сужением пилородуоденального канала, увеличивает время воздействия агрессивного желудочного сока. Запоздалое срабатывание тормозных нейрогуморальных механизмов, регулируемых поступлением кислого содержимого в луковицу двенадцатиперстной кишки, ведет к избыточной кислотопродукции, что также играет существенную роль в генезе многих заболеваний.
Наличие дуоденогастрального рефлюкса приводит к воздействию на слизистую оболочку антрального отдела желудка кишечного содержимого, содержащего желчные кислоты, к повреждению защитного слоя слизи, покрывающего слизистую оболочку, развитию кишечной метаплазии.
Все эти патологические изменения сократительной активности желудка и двенадцатиперстной кишки приводят к сохранению диспепсических жалоб, поддержанию воспалительного процесса, ослаблению защитных свойств слизистой оболочки, ведут к нарушению функции поджелудочной железы, желчевыводящих путей, способствуют развитию спастических сокращений или парезу тонкой и толстой кишки и, в конечном итоге, являются одной из причин рецидивирующего течения заболеваний желудочно–кишечного тракта. Поэтому поиск эффективных средств, нормализующих моторно–эвакуаторную функцию желудочно–кишечного тракта, изучение особенностей их действия и применения продолжаются и в настоящее время.
Двигательная функция ЖКТ подвержена регулирующим влияниям центральной, периферической и энтеральной нервных систем, большой группы желудочно–кишечных и нейропептидов, биологически активных веществ. Все компоненты нейрогуморальной регуляции поддерживают равновесие между стимулирующими и ингибирующими воздействиями, что определяет нормальный тонус и сократительную активность гладких мышц ЖКТ. На конечном этапе сбалансированная работа гладких мышц зависит от концентрации ионов Са2+ в цитоплазме миоцита и его перемещений через клеточную мембрану. Увеличение содержания Са2+ ведет к сокращению, а снижение – к релаксации миоцита.
Существует два основных пути поступления ионов Са2+ в клетку: из внеклеточного пространства по медленным кальциевым каналам мембран, что приводит к тоническому сокращению и высвобождению Са2+ из внутриклеточных депо, что вызывает фазовое сокращение. Стимуляция ацетилхолином мускариновых рецепторов способствует открытию натриевых каналов и входу Na+ в клетку, что сопровождается деполяризацией мембраны, открытием потенциалзависимых кальциевых каналов и проникновением Са2+ внутрь клетки. Увеличение концентрации Са2+ приводит к образованию комплекса кальций–кальмодулин, фосфорилированию миозина и сокращению миоцита.
Снижение тонуса и сократительной активности миоцита происходит преимущественно при активизации симпатической нервной системы и стимуляции норадреналином a1–адренорецепторов, ассоциированных с депо Са2+ на поверхности клетки, которое постоянно пополняется из внеклеточной среды. При этом происходит мобилизация Са2+ из депо и открытие калиевых каналов. Последующий отток ионов К+ вызывает закрытие кальциевых каналов, гиперполяризацию клеточной мембраны и релаксацию миоцита. Снижению концентрации Са2+ внутри клетки (и соответственно расслаблению) способствует увеличение содержания внутриклеточного цАМФ, стимуляция его выхода цГМФ–зависимой протеинкиназой и активный транспорт Са2+ при помощи кальциевого насоса – кальциевой АТФ–азы на внутренней поверхности мембраны.
В развитии патологии двигательно–эвакуаторной функции желудка и двенадцатиперстной кишки важную роль играют изменение регулирующих влияний ЦНС, парасимпатической и симпатической нервных систем, нарушение баланса нейротрансмиттеров и регуляторных пептидов (серотонина, мотилина, холецистокинина, нейротензина, эндорфинов и энкефалинов, вазоактивного пептида и др.).
Основные виды нарушений перистальтики желудка и ДПК хорошо известны. Однако рассматривая изменения двигательно–эвакуаторной функции, необходимо разграничивать нарушение тонуса желудка, двенадцатиперстной кишки, работы сфинктерного аппарата (гипо– или атония, гипертонус или спазм, дисмоторика при которой расстроена координация сократительной активности) и эвакуации (замедление или ускорение эвакуации, гастро– или дуоденостаз, ретроградная перистальтика, рефлюксы). Данные нарушения могут сочетаться между собой в различных комбинациях. Так, например, спазм привратника может сочетаться с дуоденостазом и замедлением эвакуации при нормальной сократительной активности желудка, а снижение тонуса желудка – с повышенной сократительной активностью двенадцатиперстной кишки, дуоденогастральным рефлюксом и нормальной эвакуацией; дисфункция или спазм сфинктера Одди – с нормальной двигательно–эвакуаторной функцией желудка и ДПК. Многообразие сочетаний подобных нарушений иногда ставит перед врачом трудные и часто прямо противоположные задачи, что существенно затрудняет выбор адекватного лекарственного препарата для коррекции выявленной патологии. Поэтому понятен интерес врачей к препаратам, которые не только бы снимали спазм или стимулировали сократительную активность, но и нормализовали ее.
В настоящее время для нормализации двигательно–эвакуаторной функции желудка наиболее часто применяются прокинетики. К лекарственным средствам этой группы относятся блокаторы дофаминовых рецепторов: центральных – метоклопрамид и периферических – домперидон. Из–за отсутствия центрального действия и значительно меньшего количества побочных эффектов (0,5–1,8% больных по сравнению с 20–30%) домперидон считается препаратом выбора в лечении больных с дискинетическими расстройствами.
Действие домперидона основано на блокаде периферических дофаминовых рецепторов в стенке желудка и двенадцатиперстной кишки, что приводит к усилению перистальтики преимущественно верхних отделов пищеварительного тракта. Домперидон повышает тонус нижнего пищеводного сфинктера, усиливает сократительную активность желудка и ускоряет его опорожнение, улучшает антро–дуоденальную координацию. Многочисленные клинические исследования, посвященные применению домперидона в лечении больных с неязвенной диспепсией, показали его эффективность у 61–85% больных.
Нами также исследовалось действие домперидона у 107 больных с различными вариантами течения язвенной болезни при проведении консолидирующей терапии, обострении хронического панкреатита, при хроническом калькулезном холецистите во время подготовки к плановому оперативному лечению, а также в различные сроки после холецистэктомии при наличии у пациентов диспепсических жалоб. Всем больным выполнялись фиброгастродуоденоскопия, реогастрография (многозональная импедансометрия), УЗИ желудка и двенадцатиперстной кишки, при необходимости – рентгенокимография. Показаниями к назначению препарата были: ослабление сократительной активности желудка, замедление эвакуации, дуодено–гастральный рефлюкс, примесь желчи в желудочном содержимом, наличие сопутствующего рефлюксэзофагита. Все больные принимали препарат в стандартных дозировках в течение 20 суток. Контрольные обследования выполнялись в начале и по окончании лечения. Оценивалась частота пациентов с нормальной, усиленной, ослабленной сократительной активностью и дисмоторными нарушениями до и после курса домперидона.
Для оценки прокинетического эффекта больные были разделены на четыре группы по степени нарушений двигательной функции желудка в начале лечения. В первую группу вошло 34 больных с ослабленной сократительной активностью желудка, во вторую – 24–пациента, у которых при нормальном тонусе желудочной стенки наблюдалось нарушение эвакуаторной функции желудка, в третью – 18 человек с усиленной активностью. Четвертую группу составил 31 больной с дисмоторными нарушениями, т.е. различными типами сократительной активности желудка в теле и в антральном отделах желудка, а также дуоденогастральным рефлюксом.
Оказалось, что действие домперидона при различных типах двигательных нарушений было разнонаправленным. При ослаблении перистальтики в начале лечения происходило повышение тонуса желудочной стенки и нормализация перистальтики у 85,3% больных. При изначально нормальных значениях тонуса желудочной стенки и нарушениях эвакуаторной функции желудка у 29,2% отмечалось появление двигательно–эвакуаторных расстройств. Применение домперидона при усиленной сократительной активности сопровождалось снижением тонуса желудочной стенки и нормализацией показателей у 83,3% больных. У пациентов с дисмоторными нарушениями произошла нормализация моторики в 54,8% случаев. В целом применение домперидона приводило к нормализации двигательно–эвакуаторной функции желудка и двенадцатиперстной кишки у 72,9% больных.
Другой группой лекарственных средств, широко применяемых для нормализации двигательно–эвакуаторной функции желудочно–кишечного тракта, являются спазмолитики, среди которых выделяется мебеверин (Дюспаталин). В отличие от других спазмолитиков дюспаталин обладает двойным механизмом действия. Являясь блокатором натриевых каналов, Дюспаталин препятствует поступлению Na+ внутрь клетки, что опосредованно приводит к закрытию кальциевых каналов и ослаблению мышечных сокращений. Помимо этого, он блокирует восполнение депо кальция на мембране миоцита после стимуляции a1–адренорецепторов, что не дает развиться рефлекторной гипотонии. Двойной механизм действия позволяет говорить о нормализующем действии Дюспаталина на двигательную функцию ЖКТ.
Многочисленные клинические исследования как в нашей стране, так и за рубежом доказали эффективность и безопасность Дюспаталина в лечении многих заболеваний ЖКТ, сопровождающихся спазмом гладкой мускулатуры, и позволили обозначить следующий спектр особенностей его действия:
• выраженное спазмолитическое действие;
• отсутствие рефлекторной гипотонии;
• селективное действие только на гладкомышечные клетки ЖКТ;
• тропность к сфинктеру Одди
• отсутствие холинергических эффектов;
• отсутствие вазадилатирующего и кардиотропного влияния;
• быстрое достижение эффекта при пероральном приеме;
• пролонгированное действие.
Применяя Дюспаталин у больных с желчно–каменной болезнью (как до операции, так и в различные сроки после нее), при обострении хронического панкреатита, с синдромом раздраженной толстой кишки, мы обратили внимание на тот факт, что, помимо улучшения течения основного заболевания, у многих больных происходила и нормализация нарушенной двигательно–эвакуаторной функции желудка и ДПК. Опираясь на данный факт, мы провели целенаправленное изучение действия Дюспаталина на сократительную активность желудка и ДПК у 78 пациентов с указанными заболеваниями. Как и в случае с домперидоном, всем больным выполнялись фиброгастродуоденоскопия, реогастрография (многозональная импедансометрия), УЗИ желудка и двенадцатиперстной кишки, при необходимости – рентгенокимография. Все больные принимали препарат в стандартных дозировках в течение 20 суток. Контрольные обследования выполнялись в начале и по окончании лечения. Оценивалась частота пациентов с нормальной, усиленной, ослабленной сократительной активностью и дисмоторными нарушениями до и после курса Дюспаталина.
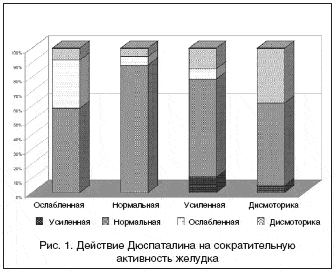
Как и в первом исследовании, все пациенты были разделены на четыре группы: 12 больных с ослабленной сократительной активностью желудка; 17 пациентов, у которых при нормальном тонусе желудочной стенки наблюдалось нарушение эвакуаторной функции желудка; 28 человек с усиленной активностью; 21 больной с дисмоторными нарушениями. При оценке результатов (рис. 1) оказалось, что Дюспаталин также обладает определенным прокинетическим, нормализующим сократительную активность действием на стенку желудка и ДПК, о чем указывают в своих работах и некоторые другие исследователи.
Из 12 больных с ослабленной перистальтикой ее нормализация произошла у 7 человек, у 4 – изменений не произошло и у 1 – появился дуоденогастральный рефлюкс. При изначально нормальной сократительной активности и нарушении эвакуации (ускорение или замедление) эвакуаторная функция восстановилась у 12 из 17 больных, при этом у 1 пациента отмечено ослабление тонуса желудочной стенки и у 1 – развились дисмоторные нарушения. Наиболее выраженное действие Дюспаталин оказывал у больных с усилением перистальтической активности: у 19 из 28 человек она нормализовалась (67,9%), у 3 – изменений не произошло, у 2 – наступило ослабление и у 4 – появились дисмоторные расстройства. Дюспаталин также способствовал устранению дуоденогастрального рефлюкса и нормализации перистальтической активности у 12 из 21 пациента с дисмоторными нарушениями. Таким образом, наличие прокинетического эффекта отмечено у 67,9% пациентов, принимавших Дюспаталин, что сопоставимо с действием домперидона (72,9% больных).
На наличие прокинетического эффекта у Дюспаталина указывают многие исследователи. Наблюдение за эвакуаторной функцией желудка в режиме реального времени при проведении ультразвукового исследования желудка и ДПК позволило нам высказать некоторые предположения.
Исследование проводили натощак. В начале определяли объем тощакового содержимого. Затем наполняли желудок водой в объеме 400 мл. После заполнения его водой достигались оптимальные условия визуализации. Это позволяло расправить стенки желудка и оценить положение, форму, размеры, контуры, структуру и толщину стенок, а также глубину и направление перистальтических сокращений, его моторно–эвакуаторную функцию. Желудок осматривали, перемещая датчик из левого подреберья в эпигастральную область и правое подреберье. При осмотре привратника обращали внимание на его функциональное состояние (нормальное, спазм, зияние), наличие деформаций и нарушения эвакуации (замедление прохождения, маятникообразные движения желудочного содержимого или дуоденогастральный рефлюкс).
За привратником определяли луковицу двенадцатиперстной кишки, которая располагается несколько левее проекции желчного пузыря при сканировании во фронтальной плоскости. При осмотре луковицы оценивали ее форму, размеры, контуры, наличие деформаций, толщину и разделение стенки на слои различной плотности, эхогенность слизистой в соответствии с серой шкалой цветности и присутствие в ее толще постоянных гиперэхогенных линейных рубцовых включений. В ряде случаев луковицу определяли только после начала эвакуации жидкости из желудка и заполнения ее водой. Иногда удавалось визуализировать залуковичный отдел и нисходящую ветвь двенадцатиперстной кишки.
При определении скорости эвакуации изначально нами была использована методика, описанная З.А. Лемешко и С.И. Пимановым (1997), которая заключалась в последовательном определении объема содержимого тела желудка и его антрального отдела. Расчеты велись на основе размеров поперечных и продольных «срезов» соответствующего отдела желудка. Данная методика является точной и достоверной, однако она достаточно трудоемка и продолжительна по времени. В связи с этим в последующем мы измеряли только объем содержимого антрального отдела.
При заполнении желудка водой у подавляющего большинства больных эвакуация небольшой порции желудочного содержимого в двенадцатиперстную кишку происходит на первой минуте. После этого больные разделяются по виду эвакуации желудочного содержимого на несколько групп.
1. В норме происходит смыкание привратника и задержка эвакуации на 3–5 мин, после чего содержимое желудка порционно равномерно эвакуируется в ДПК при нормальной перистальтической активности (глубина перистальтических волн 1/3–2/3 просвета желудка) за 20–30 мин. При этом дуоденогастральный рефлюкс бывает крайне редко и мало выражен.
2. У части больных происходит спазм привратника, задержка эвакуации содержимого в ДПК на 10–15 мин при нормальной или усиленной перистальтической активности (глубина перистальтических волн 2/3 – 3/4 просвета желудка). В дальнейшем эвакуация происходит неравномерно и в целом замедлена (через 40 мин в желудке остается около 100 мл жидкости). В отдельных случаях отмечается выраженный дуоденогастральный рефлюкс.
3. У некоторых больных задержка эвакуации сопровождается спазмом привратника, торможением перистальтики (перистальтика поверхностная, менее 1/4 глубины просвета, редкая – периодичность сокращений более 40 с) на 15–20 мин, а затем стремительной эвакуацией более чем половины объема желудочного содержимого, после чего эвакуация вновь тормозится. Как правило, при этом наблюдаются маятникообразные колебания содержимого в расширенной двенадцатиперстной кишке, дуоденогастральный рефлюкс. В целом эвакуация замедленна.
4. Возможна и полная ускоренная (в течение 3–5 мин) эвакуация содержимого после 15–20 минутной задержки при угнетенной перистальтике.
5. При усилении перистальтической активности (глубина перистальтических волн 3/4 просвета желудка и более, периодичность сокращений – через 10–15 с) возможна ускоренная эвакуация за 15–20 мин. При этом луковица ДПК пустая, но в залуковичном отделе наблюдается маятникообразное движение содержимого или быстрое поступление содержимого в нижележащие отделы. Как правило, данный тип нарушений наблюдается у больных с синдромом раздраженной кишки (СРК).
6. Для дисмоторных нарушений характерно наличие выраженного по частоте и продолжительности дуоденогастрального рефлюкса, который часто наблюдается при хроническом холецистите и желчнокаменной болезни с наличием в желчном пузыре густой застойной желчи, хлопьев, осадка. Эвакуация при этом может быть ускоренной, замедленной или сохраненной.
7. Отмечается также истинное снижение двигательно–эвакуаторной функции желудка, которое сопровождается замедлением и ослаблением перистальтики (перистальтика поверхностная, менее 1/4 глубины просвета, редкая – периодичность сокращений более 1 мин.). Через 40 мин. в желудке остается более 100 мл содержимого.
Как видно из приведенных данных, первоначальной причиной пяти из перечисленных вариантов является либо спазм, либо ускоренный сброс желудочного содержимого, либо усиление сократительной активности, которые могут приводить к рефлекторной гипотонии или замедлению эвакуации. Ликвидация имеющегося спазма при сохранении сократительной активности (что является отличительной особенностью Дюспаталина) может приводить к нормализации двигательно–эвакуаторной функции желудка и, на наш взгляд, объяснять механизм прокинетического действия данного препарата.
Таким образом, способность Дюспаталина нормализовать двигательно–эвакуаторную функцию желудка и двенадцатиперстной кишки позволяет применять его не только в лечении функциональных расстройств ЖКТ, синдрома раздраженной толстой кишки или дисфункции сфинктера Одди, но и в составе комплексного лечения такой «органической» патологии, как язвенная болезнь и ее осложнения, желчно–каменная болезнь (как до операции, так и в различные сроки после нее), при обострении хронического панкреатита. Сочетание же этих заболеваний делает его препаратом выбора для коррекции моторно–эвакуаторных нарушений органов ЖКТ.
Литература
1. Амелин А.В. Клиническая фармакология мебеверина (Дюспаталина) и его роль в лечении заболеваний // Клиническая фармакология и терапия.– 2001.–т.10.– №1.– С.1–4.
2. Белоусова Е.А. Спазмолитики в гастроэнтерологии: сравнительная характеристика и показания к применению //Фарматека.– 2002.– № 9.– С.40–46.
3. Ильченко А.А., Быстровская Е.В. Опыт применения Дюспаталина при функциональных нарушениях сфинктера Одди у больных, перенесших холецистэктомию // Экспериментальная и клиническая гастроэнтерология.– 2002.– № 4.– С.1–3.
4. Ильченко А.А., Селезнева Э.Я. Дюспаталин (мебеверин) в купировании болей при желчнокаменной болезни // Экспериментальная и клиническая гастроэнтерология.– 2002.– № 3.– С.1–3.
5. Климов А.Е. Дюспаталин в терапии функциональных заболеваний кишечника и желчевыводящих путей // Русский медицинский журнал.– 2003.– т.11.– №5.– С.1–2.
6. Кубышкин В.А., Сергеева О.Н. Дюспаталин в практике абдоминальной хирургии// Русский медицинский журнал.– 2003.– т.11.– №8.– С.1–2.
7. Маев И.В., Самсонов А.А., Салова Л.М., Шах Ю.С., Ульянкина Е.В. Диагностика и лечение заболеваний желчевыводящих путей: Учебное пособие.– М.: ГОУ ВУНМЦ МЗ РФ, 2003.– 96 с.












