Морфологические изменения в печени при АДЛ большинство авторов описывают, как жировую дистрофию или жировой гепатоз [4,8,10]. Однако клиницистам нередко приходится сталкиваться с изменениями печени, которые не укладываются в картину жирового гепатоза. Чаще такие изменения встречаются у женщин с повышенной массой тела, дислипидемией, сердечно–сосудистыми заболеваниями, сахарным диабетом. Для обозначения таких изменений был предложен термин «неалкогольный стеатогепатит» (НАСГ) [5,9,11]. НАСГ – самостоятельная нозологическая единица, для которой характерны повышение активности ферментов печени в крови и морфологические изменения в биоптатах печени, подобные изменениям при алкогольном гепатите – жировая дистрофия и воспалительная реакция; однако больные с НАСГ не употребляют алкоголь в количествах, способных вызывать повреждение печени [5,9,10].
Этиология жирового гепатоза и НАСГ многофакторна. Выделяют первичное и вторичное заболевания. К первичным причинам относятся: ожирение, сахарный диабет 2 типа, гиперлипидемия. Вторичный НАСГ индуцируется внешними воздействиями (некоторые лекарственные препараты, синдромом мальабсорбции, быстрое похудание, длительное более 2–х недель парентеральное питание, генерализованная липодистрофия, болезнь Вильяма–Кристчона, болезнь Коновалова–Вильсона и др.) [8–11].
Диагностика НАСГ принципиально важна в связи с тем, что эта форма поражения печени часто сочетается с АДЛ [4,6], а наличие сопутствующих сердечно–сосудистых заболеваний, требует назначения гиполипидемических препаратов. В практике лечения дислипидемии имеется широкий спектр лекарственных препаратов. По данным последних многоцентровых исследований, применение статинов способствует доказанному уменьшению сердечно–сосудистых осложнений, общей и коронарной смертности. Но проблемным фактором в терапии дислипидемий остается поражение печени [6]. Кроме того, для большинства гиполипидемических препаратов, в том числе и для статинов, печень является мишенью их побочных эффектов.
Цель данной работы – оценка морфофункционального состояния печени у больных с атерогенной дислипопротеидемией для определения показаний к гиполипидемической терапии.
Материалы и методы
Обследовано 150 больных с атерогенной дислипидемией в возрасте от 40 до 70 лет: 121 женщина и 29 мужчин. Критериями исключения явились вирусные и алкогольные поражения печени, сахарный диабет 2 типа.
54 больным (38 женщин и 16 мужчин) проводилась гиполипидемическая терапия статинам в течение 8 недель.
30 больных (11 мужчин и 19 женщин) получали урсодезоксихолевую кислоту (УДХ) в течение 3–х месяцев с последующей оценкой гиполипидемического и гепатопротективного эффекта.
В план обследования больных входили сбор анамнеза, объективное обследование больного. Биохимический анализ крови: билирубин, холестерин – ХС, трансаминазы, щелочная фосфатаза– ЩФ, g–глутамилтранспептидаза – ГГТП, общий белок крови, глюкоза крови; изучали показатели липидного спектра крови: общее содержание липидов, ХС липопротеидов низкой плотности (ЛПНП), ХС липопротеидов высокой плотности (ЛПВП), триглицеридов (ТГ). Всем больным проводился анализ на маркеры вирусных гепатитов, ультразвуковое исследование органов брюшной полости. Пункционная биопсия печени с проведением морфологического исследования проведена 68 больным, 36 из них – на фоне приема гиполипидемических препаратов.
Результаты и обсуждение
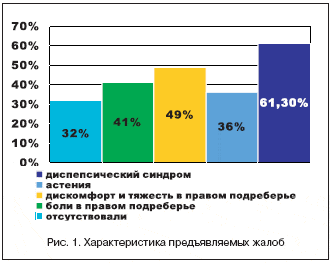
Обращение большинства больных к врачу было вызвано сопутствующей патологией и только при обследовании выявлялась патология гепатобилиарной системы. У 32% обследованных жалобы отсутствовали, 41% в основном предъявляли жалобы на ноющие боли в правом подреберье, 49% отмечали дискомфорт и тяжесть в правом подреберье, у 61% больных превалировали жалобы на явления желудочно–кишечной диспепсии, в 36% случаев основной жалобой являлась слабость (рис. 1).
При осмотре избыточная масса тела была выявлена у 58% больных, умеренная гепатомегалия определялась у 56,7% больных (85 обследованных больных).
При анализе основных изменений в биохимическом анализе выявлено достоверное повышение в плазме крови АЛТ и АСТ (94 и 86 больных; 62,7 и 57,3% соответственно); у 88 пациентов (58,6%) обследованной группы концентрация ГГТП в плазме была повышена в 2 раза (p<0,05), повышение уровня билирубина выявлено у 37 больных (24,7%), и в среднем его значения составили 25,9±5,3 мкмоль/л. При анализе белкового обмена значимых нарушений мы не выявили.
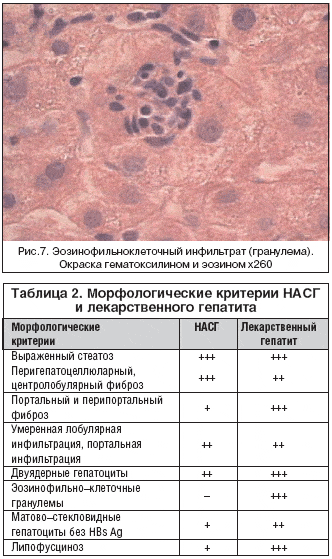
Показатели липидного спектра у обследованных больных представлены в таблице 1, из которой следует, что у всех пациентов было повышено общее содержание липидов, ЛПНП, ТГ, а уровень ЛПВП имел тенденцию к снижению. Данные изменения соответствовали в основном 2а и 2б типу гиперлипидемии.
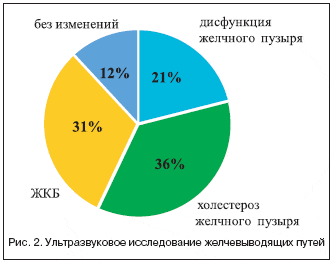
По данным УЗИ у всех больных выявлена жировая дистрофия печени, изменения желчевыводящих путей характеризовались функциональными нарушениями с изменением моторики желчного пузыря и наличием билиарного сладжа 21%, практически у половины обследованных (36%) диагностировался холестероз желчного пузыря; в 31% случаев определялась желчно–каменная болезнь (в том числе холецистэктомия проведена у 19% больных), у 12% больных изменений не выявлено (рис. 2).
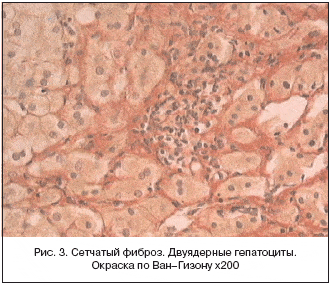
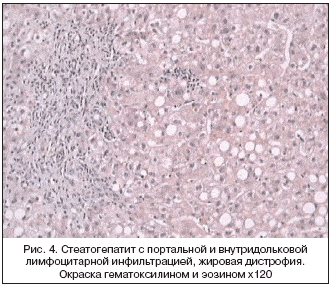
32 больным проведена пункционная биопсия печени. По данным морфологического исследования у 29 больных (92%) диагностирована крупнокапельная жировая инфильтрация гепатоцитов, у 14 больных (45%) гидропическая дистрофия гепатоцитов, также наблюдались двуядерные гепатоциты, что свидетельствует о нарушении пролиферативных процессов, у 26 пациентов (83%) определялся интралобулярный сетчатый фиброз (рис. 3). Воспалительные изменения выявлены у 25 больных (78%): внутрилобулярный и перипортальный гепатиты (рис. 4). Воспалительный инфильтрат содержал лимфоциты и мононуклеарные клетки. Нередко в гепатоцитах выявлялось накопление липофусцина.
Таким образом, результаты исследования свидетельствуют о том, что у больных с АДЛ имеются выраженные изменения печени, которые не противоречат признакам НАСГ.
Наличие АДЛ и сопутствующих сердечно–сосудистых заболеваний требует назначения гиполипидемической терапии. Мы обследовали 54 больных с атерогенной дислипидемией, получавших препараты группы статинов: 38 женщин и 16 мужчин. Все больные получали препараты группы статинов в терапевтической дозе 20–40 мг/сут. в течение 4–8 недель (препарат и его доза определялись кардиологом).
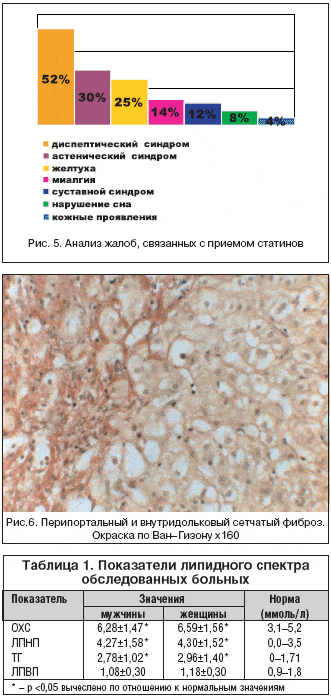
На фоне лечения статинами у 40% больных появились жалобы, связанные с приемом препарата (рис. 5).
Изучение липидного спектра крови проводили до лечения и после его окончания. На фоне приема статинов отмечалось снижение уровня общего холестерина на 24%, ЛПНП на 38%, ТГ на 8% от исходного уровня.
До назначения статинов биохимические пробы печени у всех больных находились в пределах нормальных значений. У 60% больных, получавших статины, выявлялись изменения проб печени: повышение активности трансаминаз АЛТ на 30% от исходного уровня, АСТ на 24% от исходного уровня, повышение уровня билирубина и ЩФ на 15%.
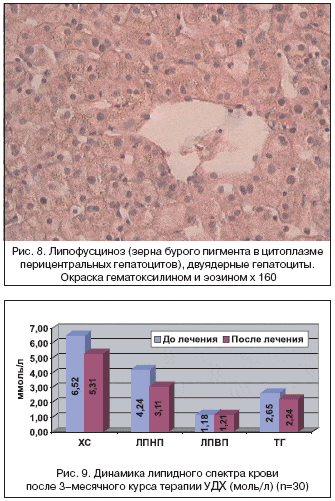
При проведении гистологического исследования биоптатов печени выявлены следующие изменения: липидная инфильтрация с признаками жировой дистрофии гепатоцитов в 90% случаев, в 76% случаев выявлен портальный и внутридольковый фиброз (рис. 6), выявлялись также воспалительные изменения: выраженная диффузная лимфоцитарная инфильтрация, умеренная лобулярная инфильтрация выявлялась в 57% случаев, характерным явилось наличие эозинофильно–клеточных гранулем у 20% больных (рис. 7) и наличие выраженного липофусциноза, который определялся в 65% случаев (рис. 8), также определялись двуядерные гепатоциты.
Результаты гистологического исследования свидетельствовали о развитии лекарственного гепатита у 9 больных (16,6%). В таблице 2 представлена сравнительная характеристика морфологических критериев, выявленных у больных с НАСГ, и больных, получавших статины. Наличие таких изменений, как выраженный липофусциноз, появление эозинофильно–клеточных гранулем и изменение топики фиброза (выявление портального и перипортального фиброза) позволило говорить именно о лекарственном поражении печени.
Наличие НАСГ у больных с АДЛ требует подбора альтернативных методов лечения. Мы обследовали 30 больных (11 мужчин и 19 женщин) с АДЛ и проявлениями НАСГ. Больные получали УДХ в стардартной дозировке (15 мг/кг) однократно на ночь в течение 3–х месяцев. Улучшение самочувствия отметили 63,3% больных (19 из 30): уменьшение дискомфорта и тяжести в правом подреберье, ослабление выраженности диспепсического синдрома. Необходимо подчеркнуть, что в основном значительный эффект связан с положительным влиянием препарата на проявления билиарной патологии, которая, как сказано выше, часто выявляется у больных с атерогенной дислипидемией и нарушениями функции печени.
Изучены показатели липидного состава крови до и после проведенного лечения (рис. 9). При анализе полученных данных отмечено, что терапия УДХ в течение 3 месяцев приводит к снижению уровня общего холестерина крови на 18,6% от исходных значений (в основном за счет уровня ХС ЛПНП: уменьшение на 26,7% и снижение уровня ТГ на 15,5%). Уровень ХС ЛПВП достоверно не изменялся.
Изучено также влияние УДХ на показатели биохимических проб печени. На фоне приема препарата определялось достоверное снижение уровня печеночных ферментов (для АСТ на 33,7%; для АЛТ на 47%; уменьшение уровня ГГТП на 30,5%), показатели общего билирубина и ЩФ оставались в пределах нормальных значений как до, так и после лечения.
Учитывая нормализацию биохимических проб печени, пункционная биопсия печени после курса лечения УДХ не проводилась.
Таким образом, результаты, полученные при исследовании печеночных проб и липидного состава крови в динамике, свидетельствовали о значительной эффективности урсотерапии в нормализации биохимических проб печени и липидного обмена.
Выводы
1. У 63% больных с атерогенной дислипидемией выявляются изменения в печени, характерные для неалкогольной жировой болезни печени (стеатоз; стеатогепатит; фиброз).
2. У больных с высокой вероятностью развития НАСГ перед назначением гиполипидемических препаратов целесообразно учитывать клинико–функциональное состояние печени (в том числе и морфологические изменения).
3. Применение статинов на фоне НАСГ может приводить к возникновению лекарственных поражений печени.
4. Больным с атерогенной дислипидемией и НАСГ целесообразно к лечению добавлять препараты урсодезоксихолевой кислоты.
Литература
1. Аронов Д.М. «Лечение атеросклеротической дислипидемии и атеросклероза». Журнал «Трудный пациент» 2003г. Том1, №4 стр.31–34
2. Петухов В.А. Дислипопротеидемия и ее коррекция при облитерирующем атеросклерозе //Диссертация на соискание ученой степени доктора медицинских наук М.1995г.
3. Савельев В.С. Яблоков Е.Г. Петухов В.А. Липидный дистресс–синдром в хирургии //Бюллетень экспериментальной биологии 1999 т.127 №6 стр. 604–611
4. М. Карнейро де Мура Неалкогольный стеатогепатит. Клинические перспективы гастроэнтерологии, гепатологии. №3 2001г. стр. 12–15.
5. Подымова С.Д. Жировой гепатоз, неалкоголный стеатогепатит. Клинико–морфологические особенности. Прогноз. Лечение. РМЖ2005г. Том 7 №2 Стр. 61–67.
6. Лазебник Л.Б., Звенигородская Л.А., Морозов И.А., Шепелева С.Д. «Клинико–морфологические изменения печени при атерогенной дислипидемии и при лечении статинами.» Терапевтический архив, 2003г. №8 стр. 51–55
7. Angulo P., Keach J.C., Batts K.P., Lindord K.D. Independent predictors of Liver fibrosis in patients with non–alcoholic steatohepatitis // Hepatology.– 1999.– V. 30.– P. 1356–1362.;
8. Brunt EM. Nonalcoholic steatohepatitis: a proposal for grading and staging the histological lesions. Am J Gastroenterol 1999;94:2467–74
9. Ludwig J., Viggiano T.R., McGill D.B., Oh B.J. Nonalcoholic steatohepatitis: Mayo Clinic experiences with a hitherto unnamed disease. Mayo Clin Proc 1980;55:434–8.
10. Powell E.E., Cooksley W.G., Hanson R., Searle J., Halliday J.W., Powell L.W. The natural history of nonalcoholic steatohepatitis: a follow–up study of forty–two patients for up to 21 years. Hepatology 1990;11:74–80.
11. Thaler H. Relation of steatosis to cirrhosis // Clinical gastroenterology Vol. 5№2 рр 273–280, 1975












