При характеристике распространенности неалкогольной жировой болезни печени (НАЖБП) необходимо отметить некоторые особенности. Точность диагностики зависит от метода диагностики внутриклеточного накопления липидов, метода оценки употребления алкоголя и критериев определения границы между «нормальным» употреблением и злоупотреблением алкоголя. Представим имеющиеся в литературе данные по эпидемиологии НАЖБП.
По последним данным, распространенность НАЖБП в Западной Европе составляет 20–30%, 15% – в странах Азии, а в Саудовской Аравии при проведении КТ печени она составляет около 10% [6]. Исследовали данную проблему и иранские ученые: распространенность НАСГ, по их данным, составила 2,9%, причем факторами риска служили мужской пол, городской образ жизни, повышенный ИМТ и ожирение [20].
С января 2002 г. по август 2003 г. в рамках второй фазы исследования Dionysos изучались распространенность и факторы риска НАЖБП. В исследовании участвовало 659 пациентов. Установлена связь НАЖБП с повышенной массой тела, гипертриглицеридемией, сахарным диабетом (СД) 2 типа, возрастом [5].
Опубликованы данные эпидемиологического исследования, проведенного в Бразилии. Среди 1280 пациентов, средний возраст которых составил 49,68±13,59 лет, 53,35% мужчин, у 85% не выявлялись симптомы заболевания. Гиперлипидемия наблюдалась у 66,8%, ожирение – у 44,7%, повышение веса – 44,4%, диабет – 22,7%, метаболический синдром – у 41,3%. Повышение АЛТ, АСТ и ГГТ выявлены в 55,8, 42,2 и 63,1% случаев соответственно. По данным биопсии, проводившейся у 437 пациентов, изолированный стеатоз определялся в 42% случаев, стеатогепатит – в 58%, в 27% из них – фиброз [8]. Цирроз выявлялся у 15,4%, гепатоциллюлярная карцинома – в 0,7% случаев.
В РФ до недавнего времени отсутствовали данные о распространенности НАЖБП. В 2007 году фармацевтической компанией Санофи–Авентис проводилось открытое многоцентровое рандомизированное проспективное исследование – наблюдение DIREG_L_01903, в роли координатора которого выступал академик РАМН, профессор В.Т. Ивашкин. Данное исследование позволило получить исчерпывающую информацию об эпидемиологии заболевания в России [1].
С 25 марта по 26 ноября 2007 года в 208 исследовательских центрах России было обследовано 30787 пациентов, обратившихся к терапевтам поликлиник. За этот период всем пациентам, включенным в исследование, независимо от причины обращения за медицинской помощью, проводились УЗИ печени, клинический и биохимический анализы крови. Собирались и анализировались демографические и антропометрические показатели исследуемых (возраст, пол, социальный статус). При сборе анамнеза важное значение уделялось сопутствующим заболеваниям и состояниям, выявленным до включения в программу исследования (сердечно–сосудистые заболевания (ССЗ), кроме АГ, АГ, дислипидемия, СД, менопауза, заболевания печени). Особого внимания заслуживало употребление алкогольных напитков, поэтому при опросе уточнялись количество и тип алкогольных напитков, количественное содержание в них алкоголя. При осмотре выявлялись признаки поражения печени (телеангиоэктазии – 6,7%, иктеричность склер – 5,7%, пальмарная эритема – 2,2%, порхающий тремор кистей – 1,2%). Далее при перкуссии и пальпации оценивались размеры печени. Гепатомегалия выявлялась у 11,9% обследуемых. При лабораторном исследовании учитывались следующие показатели: активность АЛТ, АСТ, ГГТ, уровень глюкозы, холестерина, триглицеридов, протромбиновое время, количество тромбоцитов, HbS–антитела и HCV–антитела. При УЗИ органов брюшной полости происходила оценка паренхимы и размера печени и поджелудочной железы, диаметра воротной и селезеночных вен.
Таким образом, на основании анамнеза, лабораторных исследований и УЗИ печени был поставлен диагноз НАЖБП. Учитывая большое число пациентов, биопсия печени не проводилась. Получены следующие результаты: НАЖБП была выявлена у 26,1% пациентов, среди них цирроз печени обнаружен у 3% больных, стеатоз – у 79,9%, стеатогепатит – у 17,1%. В возрастной группе до 48 лет НАЖБП отмечался у 2305/15336 (15%) пациентов; в возрастной группе от 48 лет – у 5638/15095 (37,4%) пациентов. По результатам исследования была установлена значимость всех анализируемых факторов риска, причем наиболее распространенными факторами в популяции НАЖБП были: наличие АГ, дислипидемия, отклонение от нормы холестерина и абдоминальное ожирение. По каждому фактору риска доля пациентов в популяции НАЖБП была выше, чем доля пациентов с этим же фактором риска во всей популяции пациентов, включенных в анализ.
Также доказана роль СД 2 типа, который встречается в 22,8% случаев среди пациентов с НАЖБП и также служит фактором риска НАЖБП. Среди пациентов с НАЖБП у 27,8 % имеются заболевания сердечно–сосудистой системы (ССС).
Итак, анализ результатов исследования показал, что НАЖБП характеризуется высокой распространенностью среди населения РФ. С одной стороны, НАЖБП – фактор риска ССЗ, а с другой – у большинства больных протекает бессимптомно или малосимптомно. Выявление заболевания происходит случайно при УЗИ и повышении активности трансаминаз во время обследования пациентов, которые в момент обращения не предъявляют никаких жалоб, связанных с патологией печени.
Не вызывает также сомнения, что НАЖБП – общетерапевтическая проблема, к исследованию и лечению которой должны быть подключены не только гепатологи и гастроэнтерологи, но и кардиологи и терапевты, врачи общей практики [4].
Закономерен вопрос: а необходимо ли введение долгосрочной скрининговой программы по выявлению НАЖБП, наподобие исследования DIREG? Удастся ли, воздействуя на НАЖБП, снизить риск возникновения СД 2 типа и смертность, связанную с сердечно–сосудистыми событиями?
НАЖБП и ССЗ. Новые механизмы
и маркеры НАЖБП
У больных ССЗ неалкогольная жировая болезнь печени – и в качестве единственного проявления нарушений липидного обмена, и как составляющая часть метаболического синдрома (МС) [7], не только служит фактором риска развития заболеваний ССС, но, как утверждается в последних исследованиях, определяет их исход в большей степени, чем исход заболеваний печени. При НАЖБП повышается риск тромбообразования за счет повышения пула провоспалительных цитокинов, проатерогенной дислипидемии, гиперкоагуляции и гипофибринолиза [25]. У больных СД 1 типа НАЖБП встречается довольно часто, что также связано с проявлениями ССЗ [27].
При НАЖБП прогрессирует атеросклероз, что подтверждается зависимостью между толщиной интимы–медии сонной артерии и степенью гистологических изменений в печени [26]. НАЖБП характеризуется эндотелиальной дисфункцией [28].
Существует и другая точка зрения: в работе N. Ghouri, D. Preiss and N. Sattar утверждается, что выявление НАЖБП не обязательно свидетельствует о высоком риске ССЗ. По мнению авторов, НАЖБП свидетельствует прежде всего о высоком риске СД 2 типа [11,23].
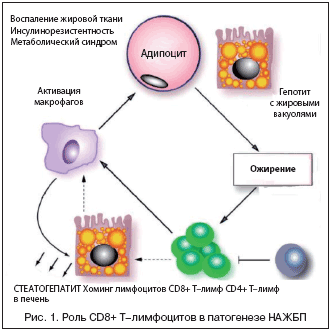
Учитывая рост распространенности НАЖБП, интенсивно изучаются молекулярно–клеточные механизмы ее развития, в первую очередь связанные с генетическими и иммунологическими факторами. Представлены данные о возможной роли CD8+ Т–лимфоцитов (рис. 1), микроРНК–10b (miRNA–10b), PPAR–α, полиморфизма генов ENPP1/PC–1 Lys121GLN, IRS–1 Gly972Arg, PNPLA3, полиморфизма в одном нуклеотиде аллеля rs738409 G гена адипонутрина, GCLC – 129 C/T, MTP –493 G/T гена, а также псевдокиназ семейства Tribble – Tribble 1 (TRB 1), TRB 2 и TRB 3, фетуина–А, влияния генетических вариантов гена APOC3, кодирующего аполипопротеин С3 [3].
Также предложен новый маркер развития НАЖБП – фактор роста фибробластов 21, который повышается при данном заболевании и коррелирует с уровнем триглицеридов [3].
Механизмы НАЖБП продолжают активно изучаться. Сразу несколько работ посвящены роли гиперинсулинемии в развитии НАЖБП. У всех больных НАЖБП наблюдается постпрандиальная гиперинсулинемия [14]. На степень выраженности фиброза у больных НАЖБП без СД 2 типа влияет не уровень глюкозы, а постпрандиальная гиперинсулинемия. Таким больным рекомендуется проводить тест на толерантность к глюкозе для раннего начала лечения [17].
При 5–летнем наблюдении за 4954 участниками исследования без НАЖБП и СД 2 типа у 13% развилась НАЖБП. Распространенность НАЖБП была в 2,5 выше в группе с высокой базовой и тощаковой гиперинсулинемией [19].
Интересные данные обобщены в работе R.E. Franco–Bourland и N. Méndez–Sánchez, в которой высказано предположение о первостепенной роли накопления триглицеридов в гепатоците в генезе метаболического синдрома [10].
При изучении особенностей метаболизма холестерина при НАЖБП установлено, что независимо от веса, его синтез повышен, а всасывание в кишечнике снижено [20].
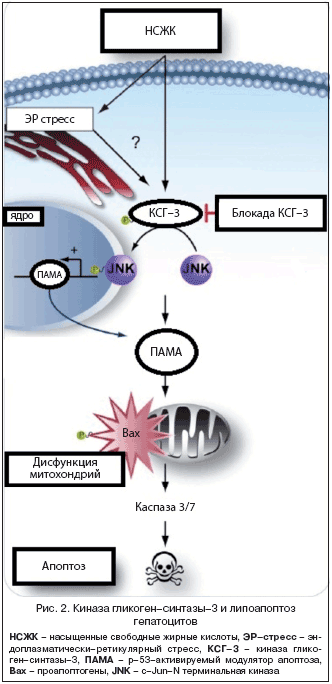
На линиях мышиных гепатоцитов Huh–7 и Hep3B были получены данные о некоторых возможностях блокировать апоптоз, индуцированный накоплением насыщенных свободных жирных кислот (НСЖК). Избыток НСЖК вызывает эндоплазматически–ретикулярный стресс, который характеризуется повреждением и разрушением белков мембраны плазматического ретикулума. Фрагменты разрушенной мембраны инициируют апоптоз, активируя c–Jun–N терминальную киназу, представителей семейства проапоптогенов Bcl–2 и p53–регулируемый модулятор апоптоза (ПАМА). По предположению исследователей данный процесс можно заблокировать, воздействуя на одно из звеньев апоптоза – активную киназу гликоген–синтазы–3 (КСГ–3). КСГ–3 активирует Bax и митохондральный путь апоптоза. Bax увеличивают проницаемость мембраны митохондрий для каспаз, что ведет к завершению апоптоза (рис. 2). Фармакологическое подавление КСГ–3 предотвращало развитие апоптоза в нейронах и фибробластах и рассматривается исследователями в качестве возможного направления в лечении НАЖБП [13].
Остаются невыясненными некоторые особенности патогенеза фиброза при НАЖБП. Определенную роль в прогрессировании НАЖБП играют гепатоциты.
При стеатозе гепатоциты, с одной стороны, более подвержены апоптозу, с другой, – подавлена их репликация. После апоптоза высвобождаются сигнальные молекулы, стимулирующие пролиферацию и дифференцировку овальных клеток в незрелые дуктулоподобные предшественники, а затем в гепатоциты. Тем самым осуществляется регенерация печени. Одновременно с пролиферацией запускается фиброз.
Предположительно процессы регенерации запускаются с участием пути Hedgehog (Hh). Во время эмбриогенеза Hh регулирует пролиферацию и дифференцировку клеток. У взрослого человека он поддерживает на определенном уровне количество стволовых клеток. Лиганд Hh связывается со своим рецептором, который в свободном состоянии подавляет активность трансмембранного белка Smo. Связывание с рецептором блокирует этот белок. Когда Hh связывается со своим рецептором, комплекс рецептор–Smo распадается, Smo активирует транскрипцию белков глиома–ассоциированного онкогена (Gli), фактора роста фибробластов 4, фосфатидилинозитол–3–киназы (ФИ–3–К), сосудистого эндотелиального фактора роста. Недавно было высказано предположение, что ген остеопонтина активируется Gli–1.
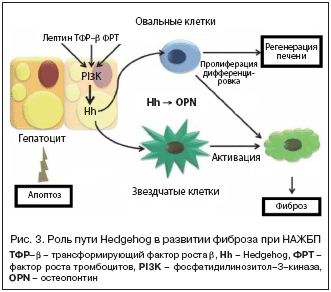
Hh может вызвать эпителиально–мезенхимальную трансформацию дуктулоподобных клеток и звездчатых клеток в миофибробласты при воздействии лептина, фактора роста тромбоцитов, трансформирующего фактора роста–β с вовлечением ФИ–3–К и остеопонтина, гликопротеина – медиатора воспаления и карциногенеза (рис 3). Контентрация остеопонтина повышена при ожирении и коррелирует с инсулинорезистентностью и стеатозом. Изучение патогенеза фиброгенеза также представляет интерес для разработки подходов к лечению и предотвращению прогрессирования фиброза [16,24].
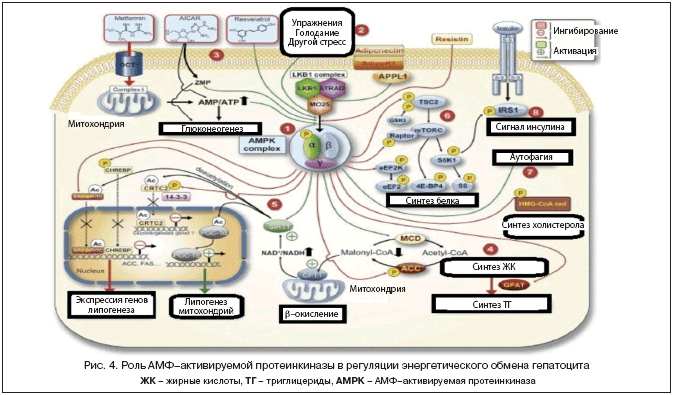
АМФ–активируемой протеинкиназе отводится центральная роль в регуляции энергообмена в гепатоците. На этот фермент воздействуют препараты, применяемые при НАЖБП, например, метформин (рис. 4) [9].
Лечение НАЖБП
Обобщаются результаты исследований с применением основных препаратов, используемых для лечения НАЖБП: метформина, тизазолидиндионов, агонистов глюкагоноподобного пептида–1, производных сульфанилмочевины, витамина Е. Обсуждается возможность применения статинов, урсодезоксихолевой кислоты, L–карнитина, пентоксифиллина, ингибиторов АПФ и блокаторов ангиотензиновых рецепторов. Имеются данные о новых разработках [15]. Те же группы препаратов применяются для лечения НАСГ. Основной целью лечения НАСГ считается снижение фиброза, обсуждаются сроки лечения НАСГ [12].
Среди статинов отмечена способность питавастатина ингибировать стеатоз, фиброз и канцерогенез при НАЖБП у крыс [18]. Также на крысах исследован алкалоид софоры софокарпин, при применении которого отмечалось снижение трансаминаз, провоспалительных цитокинов, стимулировался синтез адипонектина [22].
В России для лечения НАЖБП активно используются гепатопротекторы, например, Эссенциале® форте Н [2]. Продолжается изучение эффективности данной группы препаратов.
RU.PCH.11.04.06
Литература
1. Драпкина О.М, Гацолаева Д.С., Ивашкин В.Т. Неалкогольная жировая болезнь печени как компонент метаболического синдрома. Российские медицинские вести №2 2010, С. 72–78.
2. Драпкина О.М., Корнеева О.Н., Ивашкин В.Т. Терапия неалкогольного стеатогепатита при метаболическом синдроме: фокус на эссенциальные фосфолипиды // Лечащий Врач. 2010, № 2, с. 43–45.
3. Драпкина О.М., Смирин В.И., Ивашкин В.Т. Неалкогольная жировая болезнь печени – современный взгляд на проблему. Лечащий врач. 2010. Т. 5. № 5. С. 57–61.
4. Драпкина О.М., Смирин В.И., Ивашкин В.Т. Сахарный диабет как фактор риска неалкогольной жировой болезни печени. Врач 3: 2010, 30–33.
5. Bedogni G., Miglioli L., Masutti F., Tiribelli C., Marchesini G., Bellentani S. Prevalence of and risk factors for nonalcoholic fatty liver disease: the Dionysos Nutrition and Liver Study. Hepatology 2005; 42:44–52.
6. Bellentani S., Scaglioli F., Marino M., Bedogni G. Epidemiology of non–alcoholic fatty liver disease. Dig Dis 2010; 28: 155–161.
7. CHEN, S. H., HE, F., ZHOU, H. L., WU, H. R., XIA, C. and LI, Y. M. Relationship between nonalcoholic fatty liver disease and metabolic syndrome. Journal of Digestive Diseases, 2011 12: 125–130.
8. Cotrim HP, Parise ER, Oliveira CP, Leite N, Martinelli A, Galizzi J, Silva Rde C, Mattos A, Pereira L, Amorim W, Ivantes C, Souza F, Costa M, Maia L, Pessoa M, Oliveira F. Nonalcoholic fatty liver disease in Brazil. Clinical and histological profile. Ann Hepatol. 2011 Jan 3; 10(1):33–7.
9. Foretz M, Viollet B. Regulation of hepatic metabolism by AMPK. J Hepatol. 2011 Apr; 54(4):827–9.
10. Franco–Bourland R., Mendez–Sanchez N. The liver is the key organ for the development of metabolic syndrome. Annals of Hepatology Vol. 10 No.2, 2011: 216–217.
11. Ghouri N., Preiss D., Sattar N. Liver enzymes, nonalcoholic fatty liver disease, and incident cardiovascular disease: a narrative review and clinical perspective of prospective data. Hepatology 2010; 52:1156–1161.
12. Hojo M, Watanabe S. Pharmacological therapy of nonalcoholic steatohepatitis. Hepatol Res. 2011 Mar; 41(3):209–16.
13. Ibrahim SH, Akazawa Y, Cazanave SC, Bronk SF, Elmi NA, Werneburg NW, Billadeau DD, Gores GJ. Glycogen synthase kinase–3 (GSK–3) inhibition attenuates hepatocyte lipoapoptosis. J Hepatol. 2011 Apr; 54(4):765–72.
14. Kimura, Y., Hyogo, H., Ishitobi, T., Nabeshima, Y., Arihiro, K. and Chayama, K. Postprandial insulin secretion pattern is associated with histological severity in non–alcoholic fatty liver disease patients without prior known diabetes mellitus. Journal of Gastroenterology and Hepatology 2011, 26: 517–522.
15. Lam B., Younossi ZM. Novel treatment strategies for patients with nonalcoholic fatty liver disease. Clinical Investigation, February 2011, Vol. 1, No. 2, 229–239.
16. Machado MV, Cortez–Pinto H. Osteopontin: a missing link between hedgehog signaling and fibrosis in nonalcoholic steatohepatitis. Hepatology. 2011 Feb; 53(2):382–4.
17. Manchanayake, J., Chitturi, S., Nolan, C. and Farrell, G. C. Postprandial hyperinsulinemia is universal in non–diabetic patients with nonalcoholic fatty liver disease. Journal of Gastroenterology and Hepatology 2011, 26: 510–516.
18. Miyaki T, Nojiri S, Shinkai N, Kusakabe A, Matsuura K, Iio E, Takahashi S, Yan G, Ikeda K, Joh T. Pitavastatin inhibits hepatic steatosis and fibrosis in non–alcoholic steatohepatitis model rats. Hepatol Res. 2011 Apr;41(4):375–85.
19. Rhee EJ, Lee WY, Cho YK, Kim BI, Sung KC. Hyperinsulinemia and the development of nonalcoholic Fatty liver disease in nondiabetic adults. Am J Med. 2011 Jan;124(1):69–76.
20. Simonen P, Kotronen A, Hallikainen M, Sevastianova K, Makkonen J, Hakkarainen A, Lundbom N, Miettinen TA, Gylling H, Yki–Jarvinen H. Cholesterol synthesis is increased and absorption decreased in non–alcoholic fatty liver disease independent of obesity. J Hepatol. 2011 Jan; 54(1):153–9.
21. Sohrabpour A.A., Rezvan H., Amini–Kafiabad S., Dayhim M.R., Merat S., Pourshams A. Prevalence of Nonalcoholic Steatohepatitis in Iran: A Population based Study. Middle East Journal of Digestive Diseases/ Vol.2 / No.1, 14–19, January 2010.
22. Song CY, Zeng X, Chen SW, Hu PF, Zheng ZW, Ning BF, Shi J, Xie WF, Chen YX. Sophocarpine alleviates non–alcoholic steatohepatitis in rats. J Gastroenterol Hepatol. 2011 Apr;26(4):765–74.
23. Sung KC, Kim SH. Interrelationship between Fatty Liver and Insulin Resistance in the Development of Type 2 Diabetes. J Clin Endocrinol Metab. 2011 Apr; 96(4):1093–7.
24. Syn WK, Choi SS, Liaskou E, Karaca GF, Agboola KM, Oo YH, Mi Z, Pereira TA, Zdanowicz M, Malladi P, Chen Y, Moylan C, Jung Y, Bhattacharya SD, Teaberry V, Omenetti A, Abdelmalek MF, Guy CD, Adams DH, Kuo PC, Michelotti GA, Whitington PF, Diehl AM. Osteopontin is induced by hedgehog pathway activation and promotes fibrosis progression in nonalcoholic steatohepatitis. Hepatology 2011 Jan; 53(1):106–15.
25. Targer G., Day P.D., Bonora E. Risk of Cardiovascular Disease in Patients with Nonalcoholic Fatty Liver Disease. N Engl J Med 2010; 363:1341–50.
26. Targher G, Bertolini L, Padovani R, et al. Relations between carotid artery wall thickness and liver histology in subjects with nonalcoholic fatty liver disease. Diabetes Care 2006; 29:1325–30.
27. Targher G., Bertolini L., Padovani R et al. Prevalence of non–alcoholic fatty liver disease and its association with cardiovascular disease in patients with type 1 diabetes. Journal of Hepatology 2010 vol. 53:713–718, 2010.
28. Villanova N, Moscatiello S, Ramilli S, et al. Endothelial dysfunction and cardiovascular risk profile in nonalcoholic fatty liver disease. Hepatology 2005; 42:473–80.












