1. –Ю–±—Б—Г–ґ–і–µ–љ—Л –Њ—Б–љ–Њ–≤–љ—Л–µ —Д–∞–Ї—В–Њ—А—Л –∞–≥—А–µ—Б—Б–Є–Є –Є —Н–љ–і–Њ–≥–µ–љ–љ—Л–µ –Љ–µ—Е–∞–љ–Є–Ј–Љ—Л –Ј–∞—Й–Є—В—Л —Б–ї–Є–Ј–Є—Б—В–Њ–є –Њ–±–Њ–ї–Њ—З–Ї–Є –ґ–µ–ї—Г–і–Ї–∞ –Є –і–≤–µ–љ–∞–і—Ж–∞—В–Є–њ–µ—А—Б—В–љ–Њ–є –Ї–Є—И–Ї–Є –Њ—В –њ–Њ–≤—А–µ–ґ–і–µ–љ–Є–є –Є —П–Ј–≤–Њ–Њ–±—А–∞–Ј–Њ–≤–∞–љ–Є—П.
2. –†–∞—Б–Ї—А—Л—В—Л –њ–∞—В–Њ—Д–Є–Ј–Є–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є–µ –Љ–µ—Е–∞–љ–Є–Ј–Љ—Л, –ї–µ–ґ–∞—Й–Є–µ –≤ –Њ—Б–љ–Њ–≤–µ —А–∞–Ј–ї–Є—З–љ—Л—Е –њ–Њ–≤—А–µ–ґ–і–µ–љ–Є–є —Б–ї–Є–Ј–Є—Б—В–Њ–є –Њ–±–Њ–ї–Њ—З–Ї–Є –Є –Њ–±—А–∞–Ј–Њ–≤–∞–љ–Є—П —П–Ј–≤ –њ—А–Є –≥–∞—Б—В—А–Є–љ–Њ–Љ–µ, –њ—А–Є–µ–Љ–µ –∞–ї–Ї–Њ–≥–Њ–ї—П, –љ–µ—Б—В–µ—А–Њ–Є–і–љ—Л—Е –њ—А–Њ—В–Є–≤–Њ–≤–Њ—Б–њ–∞–ї–Є—В–µ–ї—М–љ—Л—Е –њ—А–µ–њ–∞—А–∞—В–Њ–≤ (–Э–Я–Т–Я) –Є –Є–љ—Д–µ–Ї—Ж–Є–Є Helicobacter pylori (H. pylori).
3. –Ю–±—К—П—Б–љ–µ–љ—Л —Д–∞–Ї—В–Њ—А—Л –≤–Є—А—Г–ї–µ–љ—В–љ–Њ—Б—В–Є –Є–љ—Д–µ–Ї—Ж–Є–Є
H. pylori –Є –њ—А–Є—З–∞—Б—В–љ–Њ—Б—В—М —Н—В–Њ–є –Є–љ—Д–µ–Ї—Ж–Є–Є –Ї —А–∞–Ј–≤–Є—В–Є—О —А–∞–Ј–ї–Є—З–љ—Л—Е –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є–є —Б–ї–Є–Ј–Є—Б—В–Њ–є –Њ–±–Њ–ї–Њ—З–Ї–Є –ґ–µ–ї—Г–і–Ї–∞ –Є –і–≤–µ–љ–∞–і—Ж–∞—В–Є–њ–µ—А—Б—В–љ–Њ–є –Ї–Є—И–Ї–Є.
–Ю—Б–љ–Њ–≤–љ—Л–µ —Д–∞–Ї—В–Њ—А—Л –∞–≥—А–µ—Б—Б–Є–Є
–Є –Ј–∞—Й–Є—В–љ—Л–µ –±–∞—А—М–µ—А—Л —Б–ї–Є–Ј–Є—Б—В–Њ–є –Њ–±–Њ–ї–Њ—З–Ї–Є –ґ–µ–ї—Г–і–Ї–∞
–Є –і–≤–µ–љ–∞–і—Ж–∞—В–Є–њ–µ—А—Б—В–љ–Њ–є –Ї–Є—И–Ї–Є
–§–∞–Ї—В–Њ—А—Л –∞–≥—А–µ—Б—Б–Є–Є
–Ю–±—Й–Є–Љ –љ–∞—З–∞–ї–Њ–Љ –≤ –њ—А–Њ—Ж–µ—Б—Б–µ –Њ–±—А–∞–Ј–Њ–≤–∞–љ–Є—П –њ–µ–њ—В–Є—З–µ—Б–Ї–Є—Е –њ–Њ–≤—А–µ–ґ–і–µ–љ–Є–є —Б–ї–Є–Ј–Є—Б—В–Њ–є –Њ–±–Њ–ї–Њ—З–Ї–Є –≤–µ—А—Е–љ–Є—Е –Њ—В–і–µ–ї–Њ–≤ –њ–Є—Й–µ–≤–∞—А–Є—В–µ–ї—М–љ–Њ–≥–Њ —В—А–∞–Ї—В–∞ —Б–ї–µ–і—Г–µ—В —Б—З–Є—В–∞—В—М –љ–∞—А—Г—И–µ–љ–Є–µ —А–∞–≤–љ–Њ–≤–µ—Б–Є—П –Љ–µ–ґ–і—Г —Б–Є–ї–Њ–є –≤–Њ–Ј–і–µ–є—Б—В–≤–Є—П —Д–∞–Ї—В–Њ—А–Њ–≤ –∞–≥—А–µ—Б—Б–Є–Є –Є —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В—М—О –њ—А–Њ—В–Є–≤–Њ—Б—В–Њ—П–љ–Є—П –Є–Љ –Љ–µ—Е–∞–љ–Є–Ј–Љ–Њ–≤ –Ј–∞—Й–Є—В—Л.
–Ъ —Г—Б–ї–Њ–≤–љ–Њ –њ–Њ–≤—А–µ–ґ–і–∞—О—Й–Є–Љ —Д–∞–Ї—В–Њ—А–∞–Љ –∞–≥—А–µ—Б—Б–Є–Є —Б–ї–µ–і—Г–µ—В –Њ—В–љ–µ—Б—В–Є —В–µ —Н–љ–і–Њ–≥–µ–љ–љ—Л–µ —Е–Є–Љ–Є—З–µ—Б–Ї–Є–µ —Б–Њ–µ–і–Є–љ–µ–љ–Є—П, –Ї–Њ—В–Њ—А—Л–µ –Є –≤ –љ–Њ—А–Љ–∞–ї—М–љ—Л—Е —Г—Б–ї–Њ–≤–Є—П—Е –њ–Њ—Б—В–Њ—П–љ–љ–Њ –Ї–Њ–љ—В–∞–Ї—В–Є—А—Г—О—В —Б –њ–Њ–Ї—А–Њ–≤–љ—Л–Љ —Н–њ–Є—В–µ–ї–Є–µ–Љ –њ–Є—Й–µ–≤–Њ–і–∞, –ґ–µ–ї—Г–і–Ї–∞, –і–≤–µ–љ–∞–і—Ж–∞—В–Є–њ–µ—А—Б—В–љ–Њ–є –Ї–Є—И–Ї–Є. –Ъ –љ–Є–Љ –Њ—В–љ–Њ—Б–Є—В—Б—П –ґ–µ–ї—Г–і–Њ—З–љ—Л–є —Б–Њ–Ї, —Б–Њ–і–µ—А–ґ–∞—Й–Є–є 0,16 N —Б–Њ–ї—П–љ—Г—О (—Е–ї–Њ—А–Є—Б—В–Њ–≤–Њ–і–Њ—А–Њ–і–љ—Г—О) –Ї–Є—Б–ї–Њ—В—Г, –њ–µ–њ—Б–Є–љ, –ї–Є–њ–∞–Ј—Г –Є –ґ–µ–ї—З—М, –≤ —Б–Њ—Б—В–∞–≤ –Ї–Њ—В–Њ—А–Њ–є –≤ —Б–≤–Њ—О –Њ—З–µ—А–µ–і—М –≤—Е–Њ–і—П—В –≥–Є–њ–µ—А—В–Њ–љ–Є—З–µ—Б–Ї–Є–µ —А–∞—Б—В–≤–Њ—А—Л —А–∞–Ј–ї–Є—З–љ—Л—Е —Е–Є–Љ–Є—З–µ—Б–Ї–Є—Е —Б–Њ–µ–і–Є–љ–µ–љ–Є–є –Є –Њ–ї–µ–Є–љ–Њ–≤–∞—П –Ї–Є—Б–ї–Њ—В–∞, –Њ–Ї–∞–Ј—Л–≤–∞—О—Й–Є–µ –њ–Њ–≤—А–µ–ґ–і–∞—О—Й–µ–µ –і–µ–є—Б—В–≤–Є–µ –љ–∞ —Б–ї–Є–Ј–Є—Б—В—Г—О –ґ–µ–ї—Г–і–Ї–∞ –њ—А–Є —З–∞—Б—В—Л—Е —А–µ—Д–ї—О–Ї—Б–∞—Е –ґ–µ–ї—З–Є –≤ –∞–љ—В—А–∞–ї—М–љ—Л–є –Њ—В–і–µ–ї –ґ–µ–ї—Г–і–Ї–∞ (—В–∞–±–ї.1).
–≠–Ї–Ј–Њ–≥–µ–љ–љ–Њ –≤ –њ–Є—Й–µ–≤–∞—А–Є—В–µ–ї—М–љ—Л–є —В—А–∞–Ї—В –Љ–Њ–≥—Г—В –њ–Њ—Б—В—Г–њ–∞—В—М —Е–Є–Љ–Є—З–µ—Б–Ї–Є–µ –≤–µ—Й–µ—Б—В–≤–∞, –Њ–±–ї–∞–і–∞—О—Й–Є–µ –њ—А—П–Љ—Л–Љ —Г–ї—М—Ж–µ—А–Њ–≥–µ–љ–љ—Л–Љ –і–µ–є—Б—В–≤–Є–µ–Љ, —Б—А–µ–і–Є –Ї–Њ—В–Њ—А—Л—Е –љ–∞ –њ–µ—А–≤–Њ–µ –Љ–µ—Б—В–Њ –њ–Њ —З–∞—Б—В–Њ—В–µ —П–Ј–≤–Њ–Њ–±—А–∞–Ј–Њ–≤–∞–љ–Є—П –≤—Л—Е–Њ–і—П—В –љ–µ—Б—В–µ—А–Њ–Є–і–љ—Л–µ –њ—А–Њ—В–Є–≤–Њ–≤–Њ—Б–њ–∞–ї–Є—В–µ–ї—М–љ—Л–µ –њ—А–µ–њ–∞—А–∞—В—Л (–Э–Я–Т–Я). –≠—В–∞–љ–Њ–ї —В–∞–Ї–ґ–µ –њ–Њ–≤—А–µ–ґ–і–∞–µ—В —Н–њ–Є—В–µ–ї–Є–∞–ї—М–љ—Л–µ –Ї–ї–µ—В–Ї–Є –љ–µ–њ–Њ—Б—А–µ–і—Б—В–≤–µ–љ–љ–Њ –њ—А–Є –Ї–Њ–љ—В–∞–Ї—В–µ, –Њ—Б–Њ–±–µ–љ–љ–Њ –µ—Б–ї–Є –µ–≥–Њ –Ї–Њ–љ—Ж–µ–љ—В—А–∞—Ж–Є—П —Б–Њ—Б—В–∞–≤–ї—П–µ—В 10% –Є –±–Њ–ї–µ–µ –Њ—В –Њ–±—Й–µ–≥–Њ –Њ–±—К–µ–Љ–∞ —Б–Њ–і–µ—А–ґ–Є–Љ–Њ–≥–Њ –ґ–µ–ї—Г–і–Ї–∞. –Э–Є–Ї–Њ—В–Є–љ –Є –і—А—Г–≥–Є–µ —Б–Њ—Б—В–∞–≤–ї—П—О—Й–Є–µ —В–∞–±–∞—З–љ–Њ–≥–Њ –і—Л–Љ–∞ –њ—А–µ–ґ–і–µ –≤—Б–µ–≥–Њ –њ–Њ–≤—А–µ–ґ–і–∞—О—В –Љ–Є–Ї—А–Њ—Ж–Є—А–Ї—Г–ї—П—В–Њ—А–љ–Њ–µ —А—Г—Б–ї–Њ –≥–∞—Б—В—А–Њ–і—Г–Њ–і–µ–љ–∞–ї—М–љ–Њ–є —Б–ї–Є–Ј–Є—Б—В–Њ–є, –і–µ–ї–∞—П –µ–µ –Љ–µ–љ–µ–µ —Г—Б—В–Њ–є—З–Є–≤–Њ–є –Ї –≤—А–µ–і–љ—Л–Љ –≤–Њ–Ј–і–µ–є—Б—В–≤–Є—П–Љ. –Ф—А—Г–≥–Є–Љ –Љ–µ—Е–∞–љ–Є–Ј–Љ–Њ–Љ –і–µ–є—Б—В–≤–Є—П –љ–Є–Ї–Њ—В–Є–љ–∞, –Њ—Б–ї–∞–±–ї—П—О—Й–Є–Љ –Ј–∞—Й–Є—В—Г —Б–ї–Є–Ј–Є—Б—В–Њ–є –Њ–±–Њ–ї–Њ—З–Ї–Є –ґ–µ–ї—Г–і–Ї–∞ –Є –і–≤–µ–љ–∞–і—Ж–∞—В–Є–њ–µ—А—Б—В–љ–Њ–є –Ї–Є—И–Ї–Є –Њ—В –Њ–±—А–∞–Ј–Њ–≤–∞–љ–Є—П —П–Ј–≤ —Г –Ї—Г—А—П—Й–Є—Е –ї—О–і–µ–є, —П–≤–ї—П–µ—В—Б—П –њ–Њ–і–∞–≤–ї–µ–љ–Є–µ –њ–Њ–і–ґ–µ–ї—Г–і–Њ—З–љ–Њ–є –ґ–µ–ї–µ–Ј–Њ–є —Б–µ–Ї—А–µ—Ж–Є–Є –±–Є–Ї–∞—А–±–Њ–љ–∞—В–Њ–≤. –Т —Б–ї—Г—З–∞–µ —Г–ґ–µ –Є–Љ–µ—О—Й–µ–є—Б—П —П–Ј–≤—Л, –љ–Є–Ї–Њ—В–Є–љ –Ј–∞–Љ–µ–і–ї—П–µ—В –њ—А–Њ—Ж–µ—Б—Б—Л –Ј–∞–ґ–Є–≤–ї–µ–љ–Є—П, —Б–љ–Є–ґ–∞—П –≤—Л—А–∞–ґ–µ–љ–љ–Њ—Б—В—М –Ї–Њ–Љ–њ–µ–љ—Б–∞—В–Њ—А–љ–Њ–є –Ї—А–∞–µ–≤–Њ–є –≥–Є–њ–µ—А–µ–Љ–Є–Є –≤–Њ–Ї—А—Г–≥ —П–Ј–≤—Л.
–Э–µ–Ї–Њ—В–Њ—А—Л–µ –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П —П–≤–ї—П—О—В—Б—П —З–∞—Б—В—Л–Љ–Є –њ—А–µ–і—А–∞—Б–њ–Њ–ї–∞–≥–∞—О—Й–Є–Љ–Є —Д–∞–Ї—В–Њ—А–∞–Љ–Є –Њ–±—А–∞–Ј–Њ–≤–∞–љ–Є—П —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ –≥–∞—Б—В—А–Њ–і—Г–Њ–і–µ–љ–∞–ї—М–љ—Л—Е —П–Ј–≤ – —Е—А–Њ–љ–Є—З–µ—Б–Ї–Є–µ –Њ–±—Б—В—А—Г–Ї—В–Є–≤–љ—Л–µ –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П –ї–µ–≥–Ї–Є—Е, —Н–Љ—Д–Є–Ј–µ–Љ–∞ –ї–µ–≥–Ї–Є—Е, —Ж–Є—А—А–Њ–Ј –њ–µ—З–µ–љ–Є –Є –њ–Њ—З–µ—З–љ–∞—П –љ–µ–і–Њ—Б—В–∞—В–Њ—З–љ–Њ—Б—В—М. –≠–Љ—Д–Є–Ј–µ–Љ–∞ –њ—А–Є–≤–Њ–і–Є—В –Ї —Б–Є—Б—В–µ–Љ–љ–Њ–Љ—Г –∞—Ж–Є–і–Њ–Ј—Г, –≤ —В–Њ–Љ —З–Є—Б–ї–µ –Є —Б—В–µ–љ–Ї–Є –ґ–µ–ї—Г–і–Ї–∞. –Я—А–Є —Ж–Є—А—А–Њ–Ј–µ –њ–µ—З–µ–љ–Є –Є –њ–Њ—З–µ—З–љ–Њ–є –љ–µ–і–Њ—Б—В–∞—В–Њ—З–љ–Њ—Б—В–Є —Б–љ–Є–ґ–∞–µ—В—Б—П –≥—А–∞–і–Є–µ–љ—В pH –Љ–µ–ґ–і—Г –њ—А–Њ—Б–≤–µ—В–Њ–Љ –ґ–µ–ї—Г–і–Ї–∞ –Є –Ї–ї–µ—В–Ї–∞–Љ–Є –њ–Њ–Ї—А–Њ–≤–љ–Њ–≥–Њ —Н–њ–Є—В–µ–ї–Є—П –Ј–∞ —Б—З–µ—В —Г—Б–Є–ї–µ–љ–Є—П –Њ–±—А–∞—В–љ–Њ–є –і–Є—Д—Д—Г–Ј–Є–Є –Є–Њ–љ–Њ–≤ H+ –≤ —Б–ї–Є–Ј–Є—Б—В—Г—О. –Ь–µ–љ–µ–µ —А–∞—Б–њ—А–Њ—Б—В—А–∞–љ–µ–љ–љ—Л–Љ–Є —Д–∞–Ї—В–Њ—А–∞–Љ–Є —П–≤–ї—П—О—В—Б—П —В–∞–Ї–Є–µ –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П, –Ї–∞–Ї –±–Њ–ї–µ–Ј–љ—М –Ъ—А–Њ–љ–∞, –≥–∞—Б—В—А–Є–љ–Њ–Љ–∞, –≥–Є–њ–µ—А–њ–∞—А–∞—В–Є—А–µ–Њ–Є–і–Є–Ј–Љ, –Љ–∞—Б—В–Њ—Ж–Є—В–Њ–Ј, –і–ї—П —В–µ—З–µ–љ–Є—П –Ї–Њ—В–Њ—А—Л—Е —В–∞–Ї–ґ–µ —Е–∞—А–∞–Ї—В–µ—А–љ–Њ —А–∞–Ј–≤–Є—В–Є–µ –њ–µ–њ—В–Є—З–µ—Б–Ї–Є—Е —П–Ј–≤ –ґ–µ–ї—Г–і–Ї–∞ –Є –і–≤–µ–љ–∞–і—Ж–∞—В–Є–њ–µ—А—Б—В–љ–Њ–є –Ї–Є—И–Ї–Є.
–Ю–і–љ–∞–Ї–Њ –≤–µ–і—Г—Й–µ–є –њ—А–Є—З–Є–љ–Њ–є –Њ–±—А–∞–Ј–Њ–≤–∞–љ–Є—П –њ–µ–њ—В–Є—З–µ—Б–Ї–Є—Е —П–Ј–≤ —П–≤–ї—П–µ—В—Б—П –Є–љ—Д–µ–Ї—Ж–Є—П –≥–∞—Б—В—А–Њ–і—Г–Њ–і–µ–љ–∞–ї—М–љ–Њ–є —Б–ї–Є–Ј–Є—Б—В–Њ–є –Њ–±–Њ–ї–Њ—З–Ї–Є, –≤—Л–Ј—Л–≤–∞–µ–Љ–∞—П –±–∞–Ї—В–µ—А–Є–µ–є H. pylori. –У–∞—Б—В—А–Є—В—Л, —П–Ј–≤–µ–љ–љ–∞—П –±–Њ–ї–µ–Ј–љ—М –і–≤–µ–љ–∞–і—Ж–∞—В–Є–њ–µ—А—Б—В–љ–Њ–є –Ї–Є—И–Ї–Є (–ѓ–С–Ф–Ъ) –Є —П–Ј–≤–µ–љ–љ–∞—П –±–Њ–ї–µ–Ј–љ—М –ґ–µ–ї—Г–і–Ї–∞ (–ѓ–С–Ц) –њ–∞—В–Њ–≥–µ–љ–µ—В–Є—З–µ—Б–Ї–Є —Б–≤—П–Ј–∞–љ—Л —Б —Н—В–Њ–є –Є–љ—Д–µ–Ї—Ж–Є–µ–є. –Ю–љ–∞ –≤–њ–µ—А–≤—Л–µ –±—Л–ї–∞ –Њ–±–љ–∞—А—Г–ґ–µ–љ–∞ –≤ —Б–ї–Є–Ј–Є—Б—В–Њ–є –∞–љ—В—А–∞–ї—М–љ–Њ–≥–Њ –Њ—В–і–µ–ї–∞ –ґ–µ–ї—Г–і–Ї–∞ —Г –±–Њ–ї—М–љ—Л—Е —Б —Е—А–Њ–љ–Є—З–µ—Б–Ї–Є–Љ –∞–Ї—В–Є–≤–љ—Л–Љ –≥–∞—Б—В—А–Є—В–Њ–Љ, –Ї–Њ—В–Њ—А—Л–є –≤—Б–µ–≥–і–∞ —Б–Њ–њ—Г—В—Б—В–≤—Г–µ—В –ѓ–С–Ф–Ъ. –Ш–љ—Д–µ–Ї—Ж–Є—П H. pylori –Њ—В–љ–Њ—Б–Є—В—Б—П –Ї —Е—А–Њ–љ–Є—З–µ—Б–Ї–Њ–Љ—Г –≤–Є–і—Г –Є–љ—Д–µ–Ї—Ж–Є–є –Є –њ–µ—А—Б–Є—Б—В–Є—А—Г–µ—В –љ–∞ –њ—А–Њ—В—П–ґ–µ–љ–Є–Є –≤—Б–µ–є –ґ–Є–Ј–љ–Є –і–Њ —В–µ—Е –њ–Њ—А, –њ–Њ–Ї–∞ –љ–µ –±—Г–і–µ—В –њ—А–Њ–≤–µ–і–µ–љ–∞ —Н—А–∞–і–Є–Ї–∞—Ж–Є—П –±–∞–Ї—В–µ—А–Є–є —Б –њ–Њ–Љ–Њ—Й—М—О –∞–і–µ–Ї–≤–∞—В–љ–Њ–є —В–µ—А–∞–њ–Є–Є –∞–љ—В–Є–±–Є–Њ—В–Є–Ї–∞–Љ–Є.
–§–∞–Ї—В–Њ—А—Л –Ј–∞—Й–Є—В—Л
–С–Њ–ї—М—И–Њ–µ —А–∞–Ј–љ–Њ–Њ–±—А–∞–Ј–Є–µ —А–∞–Ј–ї–Є—З–љ—Л—Е –њ–Њ–≤—А–µ–ґ–і–∞—О—Й–Є—Е –≤–µ—Й–µ—Б—В–≤ –Є –∞–≥—А–µ—Б—Б–Є–≤–љ—Л—Е —Д–∞–Ї—В–Њ—А–Њ–≤ –љ–µ–Є–Ј–±–µ–ґ–љ–Њ –≤—Б—В—А–µ—З–∞—О—В –љ–∞ —Б–≤–Њ–µ–Љ –њ—Г—В–Є –Љ–љ–Њ–ґ–µ—Б—В–≤–Њ –Љ–µ—Е–∞–љ–Є–Ј–Љ–Њ–≤ –Ј–∞—Й–Є—В—Л —Б–Њ —Б—В–Њ—А–Њ–љ—Л —Б–ї–Є–Ј–Є—Б—В–Њ–є –Њ–±–Њ–ї–Њ—З–Ї–Є –ґ–µ–ї—Г–і–Ї–∞ –Є –і–≤–µ–љ–∞–і—Ж–∞—В–Є–њ–µ—А—Б—В–љ–Њ–є –Ї–Є—И–Ї–Є.
–Ъ–Њ–љ—Ж–µ–њ—Ж–Є—П —Б–ї–Є–Ј–Є—Б—В–Њ–≥–Њ –±–∞—А—М–µ—А–∞ –Њ–±—К–µ–і–Є–љ—П–µ—В –≤ –µ–і–Є–љ–Њ–µ —Ж–µ–ї–Њ–µ —Б–Є—Б—В–µ–Љ—Г –Ј–∞—Й–Є—В–љ—Л—Е –Љ–µ—Е–∞–љ–Є–Ј–Љ–Њ–≤, –Ї–Њ—В–Њ—А—Л–µ –њ—А–µ–њ—П—В—Б—В–≤—Г—О—В —Б–Ї–Њ–њ–ї–µ–љ–Є—О –Є–Њ–љ–Њ–≤ –≤–Њ–і–Њ—А–Њ–і–∞ –љ–∞ –∞–њ–Є–Ї–∞–ї—М–љ–Њ–є –Љ–µ–Љ–±—А–∞–љ–µ –Є –≤–љ—Г—В—А–Є —Н–њ–Є—В–µ–ї–Є–∞–ї—М–љ—Л—Е –Ї–ї–µ—В–Њ–Ї –ґ–µ–ї—Г–і–Ї–∞ –Є–ї–Є –і–≤–µ–љ–∞–і—Ж–∞—В–Є–њ–µ—А—Б—В–љ–Њ–є –Ї–Є—И–Ї–Є. –°–ї–Є–Ј–Є—Б—В—Л–є –±–∞—А—М–µ—А –≤–Ї–ї—О—З–∞–µ—В –≤ —Б–µ–±—П —В—А–Є –Њ—Б–љ–Њ–≤–љ—Л–µ –ї–Є–љ–Є–Є –Ј–∞—Й–Є—В—Л:
• –Э–µ–∞–Ї—В–Є–≤–љ—Л–є —Б–ї–Њ–є —Б–ї–Є–Ј–Є –Є –±–Є–Ї–∞—А–±–Њ–љ–∞—В–Њ–≤.
• –°–ї–Њ–є —Н–њ–Є—В–µ–ї–Є–∞–ї—М–љ—Л—Е –Ї–ї–µ—В–Њ–Ї –ґ–µ–ї—Г–і–Ї–∞, —Н–љ—В–µ—А–Њ—Ж–Є—В–Њ–≤ –Є –≥–Њ–±–ї–µ—В–Њ–≤—Б–Ї–Є—Е –Ї–ї–µ—В–Њ–Ї –і–≤–µ–љ–∞–і—Ж–∞—В–Є–њ–µ—А—Б—В–љ–Њ–є –Ї–Є—И–Ї–Є, –∞–Ї—В–Є–≤–љ–Њ –њ—А–Њ–і—Г—Ж–Є—А—Г—О—Й–Є—Е —Б–ї–Є–Ј—М –Є –±–Є–Ї–∞—А–±–Њ–љ–∞—В—Л.
• –Ь–Є–Ї—А–Њ—Ж–Є—А–Ї—Г–ї—П—В–Њ—А–љ–Њ–µ —А—Г—Б–ї–Њ –≥–∞—Б—В—А–Њ–і—Г–Њ–і–µ–љ–∞–ї—М–љ–Њ–є —Б–ї–Є–Ј–Є—Б—В–Њ–є.
–°–ї–µ–і—Г–µ—В –њ–Њ–і—З–µ—А–Ї–љ—Г—В—М, —З—В–Њ —Б–ї–Є–Ј–Є—Б—В—Л–є –±–∞—А—М–µ—А – –љ–µ —В–Њ–ї—М–Ї–Њ —Б—В—А—Г–Ї—В—Г—А–љ–∞—П, –љ–Њ, –≤ –њ–µ—А–≤—Г—О –Њ—З–µ—А–µ–і—М, —Д—Г–љ–Ї—Ж–Є–Њ–љ–∞–ї—М–љ–∞—П —Б–Є—Б—В–µ–Љ–∞ —Д–Є–Ј–Є–Ї–Њ-—Е–Є–Љ–Є—З–µ—Б–Ї–Є—Е –Є –±–Є–Њ—Е–Є–Љ–Є—З–µ—Б–Ї–Є—Е –њ—А–Њ—Ж–µ—Б—Б–Њ–≤ –љ–∞ —Г—А–Њ–≤–љ–µ –њ–Њ–≤–µ—А—Е–љ–Њ—Б—В–љ—Л—Е —Н–њ–Є—В–µ–ї–Є–∞–ї—М–љ—Л—Е –Ї–ї–µ—В–Њ–Ї, –Њ–±–µ—Б–њ–µ—З–Є–≤–∞—О—Й–∞—П –≤ —Г—Б–ї–Њ–≤–Є—П—Е –љ–Њ—А–Љ–∞–ї—М–љ–Њ–є –Љ–Є–Ї—А–Њ—Ж–Є—А–Ї—Г–ї—П—Ж–Є–Є –Ї—А–Њ–≤–Є —Н—Д—Д–µ–Ї—В–Є–≤–љ—Г—О –Ј–∞—Й–Є—В—Г —Б–ї–Є–Ј–Є—Б—В–Њ–є –ґ–µ–ї—Г–і–Ї–∞ –Є –і–≤–µ–љ–∞–і—Ж–∞—В–Є–њ–µ—А—Б—В–љ–Њ–є –Ї–Є—И–Ї–Є.
–Э–µ–∞–Ї—В–Є–≤–љ—Л–є —Б–ї–Њ–є
–Я–µ—А–≤–∞—П –ї–Є–љ–Є—П –Ј–∞—Й–Є—В—Л –њ—А–µ–і—Б—В–∞–≤–ї–µ–љ–∞ —В–Њ–љ–Ї–Є–Љ (100-200 –Љ) –≥–Њ–Љ–Њ–≥–µ–љ–љ—Л–Љ —Б–ї–Њ–µ–Љ —Б–ї–Є–Ј–Є –Є —А–∞—Б—В–≤–Њ—А–Є–Љ—Л–Љ–Є –≤ –љ–µ–є –±–Є–Ї–∞—А–±–Њ–љ–∞—В–∞–Љ–Є (–Э–°–Ю3-). –°–ї–Њ–є –≤—Л—Б—В–Є–ї–∞–µ—В 98% –њ–Њ–≤–µ—А—Е–љ–Њ—Б—В–Є –ґ–µ–ї—Г–і–Ї–∞ –Є–Ј–љ—Г—В—А–Є –Є –≤–љ—Г—В—А–µ–љ–љ—О—О –њ–Њ–≤–µ—А—Е–љ–Њ—Б—В—М –і–≤–µ–љ–∞–і—Ж–∞—В–Є–њ–µ—А—Б—В–љ–Њ–є –Ї–Є—И–Ї–Є –љ–∞ –≤—Б–µ–Љ –µ–µ –њ—А–Њ—В—П–ґ–µ–љ–Є–Є. –Х–і–Є–љ—Б—В–≤–µ–љ–љ—Л–Љ–Є –љ–µ–њ–Њ–Ї—А—Л—В—Л–Љ–Є –Њ–±–ї–∞—Б—В—П–Љ–Є —П–≤–ї—П—О—В—Б—П —П–Љ–Ї–Є –ґ–µ–ї—Г–і–Њ—З–љ—Л—Е –ґ–µ–ї–µ–Ј, –Є–Ј –Ї–Њ—В–Њ—А—Л—Е –Ї–Є—Б–ї—Л–є –ґ–µ–ї—Г–і–Њ—З–љ—Л–є —Б–Њ–Ї –Є—Б—В–µ–Ї–∞–µ—В –њ–Њ–і –і–∞–≤–ї–µ–љ–Є–µ–Љ 17 –Љ–Љ —А—В. —Б—В. –≤ –њ—А–Њ—Б–≤–µ—В –ґ–µ–ї—Г–і–Ї–∞. –Т —Н—В–Њ–Љ —Б–ї–Њ–µ –Њ—Б—Г—Й–µ—Б—В–≤–ї—П–µ—В—Б—П —Е–Є–Љ–Є—З–µ—Б–Ї–Є–є –њ—А–Њ—Ж–µ—Б—Б –љ–µ–є—В—А–∞–ї–Є–Ј–∞—Ж–Є–Є –Є–љ–Њ–≤ –≤–Њ–і–Њ—А–Њ–і–∞ (–Э+) –ґ–µ–ї—Г–і–Њ—З–љ–Њ–≥–Њ —Б–Њ–Ї–∞, –њ–Њ—Н—В–Њ–Љ—Г —Б–ї–Њ–є –љ–∞–Ј—Л–≤–∞—О—В –љ–µ–∞–Ї—В–Є–≤–љ—Л–Љ. –°–ї–Є–Ј—М —Б–∞–Љ–∞ –њ–Њ —Б–µ–±–µ –љ–µ –Љ–Њ–ґ–µ—В –љ–µ–є—В—А–∞–ї–Є–Ј–Њ–≤–∞—В—М –Э+ –Є–Њ–љ—Л, –љ–Њ –≤ –љ–µ–µ –њ–Њ—Б—В–Њ—П–љ–љ–Њ —Б–µ–Ї—А–µ—В–Є—А—Г—О—В—Б—П –∞–љ–Є–Њ–љ—Л –Э–°–Ю3- –Є–Ј –Ї–ї–µ—В–Њ–Ї –њ–Њ–≤–µ—А—Е–љ–Њ—Б—В–љ–Њ–≥–Њ —Н–њ–Є—В–µ–ї–Є—П –Є –Њ–±—А–∞–Ј—Г–µ—В—Б—П –Ї–Њ–љ—Ж–µ–љ—В—А–Є—А–Њ–≤–∞–љ–љ—Л–є –±—Г—Д–µ—А–љ—Л–є —А–∞—Б—В–≤–Њ—А –±–Є–Ї–∞—А–±–Њ–љ–∞—В–Њ–≤. –Ю–љ–Є —П–≤–ї—П—О—В—Б—П –≥–ї–∞–≤–љ—Л–Љ–Є –∞–љ–Є–Њ–љ–∞–Љ–Є, —Б–њ–Њ—Б–Њ–±–љ—Л–Љ–Є –љ–µ–є—В—А–∞–ї–Є–Ј–Њ–≤–∞—В—М –Є–Њ–љ—Л –Э+ –љ–µ–њ–Њ—Б—А–µ–і—Б—В–≤–µ–љ–љ–Њ —Г –њ–Њ–≤–µ—А—Е–љ–Њ—Б—В–Є —Н–њ–Є—В–µ–ї–Є–∞–ї—М–љ—Л—Е –Ї–ї–µ—В–Њ–Ї.
–Я–Њ —Б–≤–Њ–µ–Љ—Г –Ї–Њ–ї–ї–Њ–Є–і–љ–Њ–Љ—Г —Б–Њ—Б—В–Њ—П–љ–Є—О —Б–ї–Њ–є –њ—А–µ–і—Б—В–∞–≤–ї—П–µ—В —Б–Њ–±–Њ–є –≤–Њ–і–љ—Л–є –≥–µ–ї—М –Є –њ–Њ—Н—В–Њ–Љ—Г –љ–µ –Љ–Њ–ґ–µ—В —Б–ї—Г–ґ–Є—В—М –і–Њ—Б—В–∞—В–Њ—З–љ–Њ –Љ–Њ—Й–љ–Њ–є —Д–Є–Ј–Є—З–µ—Б–Ї–Њ–є –њ—А–µ–≥—А–∞–і–Њ–є –і–ї—П –Њ–±—А–∞—В–љ–Њ–є –і–Є—Д—Д—Г–Ј–Є–Є –Є–Њ–љ–Њ–≤ –Э+. –≠—В–Њ—В —Б–ї–Њ–є —Б–Њ–Ј–і–∞–µ—В —З–∞—Б—В–Є—З–љ–Њ –њ—А–Њ–љ–Є—Ж–∞–µ–Љ—Л–є –±–∞—А—М–µ—А –і–ї—П –љ–Є–Ј–Ї–Њ–Љ–Њ–ї–µ–Ї—Г–ї—П—А–љ—Л—Е —Б–Њ–µ–і–Є–љ–µ–љ–Є–є, (–љ–∞–њ—А–Є–Љ–µ—А, –Ї–Є—Б–ї–Њ—В) –Є –±–Њ–ї–µ–µ —Н—Д—Д–µ–Ї—В–Є–≤–љ—Г—О –њ—А–µ–≥—А–∞–і—Г –Њ—В –Љ–∞–Ї—А–Њ–Љ–Њ–ї–µ–Ї—Г–ї—П—А–љ—Л—Е –≤–µ—Й–µ—Б—В–≤ –Є –±–∞–Ї—В–µ—А–Є–є.
–Ю—З–µ–љ—М –≤–∞–ґ–љ–Њ–є —Е–∞—А–∞–Ї—В–µ—А–Є—Б—В–Є–Ї–Њ–є –љ–µ–∞–Ї—В–Є–≤–љ–Њ–≥–Њ —Б–ї–Њ—П —П–≤–ї—П–µ—В—Б—П –µ–≥–Њ –≥–Є–і—А–Њ—Д–Њ–±–љ–Њ—Б—В—М, —В–∞–Ї –Ї–∞–Ї –±–Њ–ї—М—И–Є–љ—Б—В–≤–Њ —Д–∞–Ї—В–Њ—А–Њ–≤ –∞–≥—А–µ—Б—Б–Є–Є –Є –њ–Њ–≤—А–µ–ґ–і–∞—О—Й–Є—Е –∞–≥–µ–љ—В–Њ–≤ –ґ–µ–ї—Г–і–Ї–∞ –≤–Њ–і–Њ—А–∞—Б—В–≤–Њ—А–Є–Љ—Л. –У–Є–і—А–Њ—Д–Њ–±–љ–Њ—Б—В—М —Б–ї–Є–Ј–Є –Њ–±–µ—Б–њ–µ—З–Є–≤–∞—О—В –≤—Е–Њ–і—П—Й–Є–µ –≤ –µ–µ —Б–Њ—Б—В–∞–≤ –њ–Њ–≤–µ—А—Е–љ–Њ—Б—В–љ–Њ-–∞–Ї—В–Є–≤–љ—Л–µ —Д–Њ—Б—Д–Њ–ї–Є–њ–Є–і—Л, –Ї–Њ—В–Њ—А—Л–µ –њ–Њ —Б–≤–Њ–µ–Љ—Г —Б–Њ—Б—В–∞–≤—Г —Б—Е–Њ–і–љ—Л —Б —Б—Г—А—Д–∞–Ї—В–∞–љ—В–Њ–Љ –ї–µ–≥–Ї–Є—Е.
–°–ї–Є–Ј—М –њ—А–µ–і—Б—В–∞–≤–ї—П–µ—В —Б–Њ–±–Њ–є —Б–Љ–µ—Б—М –Њ—А–≥–∞–љ–Є—З–µ—Б–Ї–Є—Е –≤–µ—Й–µ—Б—В–≤, —Б–µ–Ї—А–µ—В–Є—А—Г–µ–Љ—Л—Е –≤—Л—Б–Њ–Ї–Є–Љ —Б—В–Њ–ї–±—З–∞—В—Л–Љ —Н–њ–Є—В–µ–ї–Є–µ–Љ –ґ–µ–ї—Г–і–Ї–∞, –і—Г–Њ–і–µ–љ–∞–ї—М–љ—Л–Љ–Є —Н–њ–Є—В–µ–ї–Є–Њ—Ж–Є—В–∞–Љ–Є –Є –≥–Њ–±–ї–µ—В–Њ–≤—Б–Ї–Є–Љ–Є –Ї–ї–µ—В–Ї–∞–Љ–Є. –У–∞—Б—В—А–Њ–і—Г–Њ–і–µ–љ–∞–ї—М–љ–∞—П —Б–ї–Є–Ј—М —Б–Њ—Б—В–Њ–Є—В –Є–Ј —Б—Г–ї—М—Д–∞—В–Є—А–Њ–≤–∞–љ–љ—Л—Е –≥–ї–Є–Ї–Њ–њ—А–Њ—В–µ–Є–љ–Њ–≤ —Б –±–Њ–ї—М—И–Њ–є –Љ–Њ–ї–µ–Ї—Г–ї—П—А–љ–Њ–є –Љ–∞—Б—Б–Њ–є, –Ї–Њ—В–Њ—А—Л–µ —Б–Њ–µ–і–Є–љ–µ–љ—Л –Ї–Є—Б–ї–Њ—А–Њ–і–љ—Л–Љ–Є —Б–≤—П–Ј—П–Љ–Є –Є —Д–Њ—А–Љ–Є—А—Г—О—В –Ї–ї–µ–є–Ї–Є–є –≤—П–Ј–Ї–Њ—Н–ї–∞—Б—В–Є—З–љ—Л–є –≤–Њ–і–љ—Л–є –≥–µ–ї—М, —Б–Љ–∞–Ј—Л–≤–∞—О—Й–Є–є –њ–Њ–≤–µ—А—Е–љ–Њ—Б—В—М —Н–њ–Є—В–µ–ї–Є–∞–ї—М–љ—Л—Е –Ї–ї–µ—В–Њ–Ї. –°–ї–Є–Ј—М —В–∞–Ї–ґ–µ —Б–Њ–і–µ—А–ґ–Є—В –њ–Њ–≤–µ—А—Е–љ–Њ—Б—В–љ–Њ-–∞–Ї—В–Є–≤–љ—Л–µ —Д–Њ—Б—Д–Њ–ї–Є–њ–Є–і—Л, –њ—А–Є–і–∞—О—Й–Є–µ –µ–є –≥–Є–і—А–Њ—Д–Њ–±–љ—Л–µ —Б–≤–Њ–є—Б—В–≤–∞, –Є —В—А–µ—Д–Њ–є–ї–Њ–≤—Л–µ –њ–µ–њ—В–Є–і—Л, –Ї–Њ—В–Њ—А—Л–µ –Ї–Њ–љ—В—А–Њ–ї–Є—А—Г—О—В –µ–і–Є–љ—Б—В–≤–Њ —Б—В—А–Њ–µ–љ–Є—П —Б–ї–Є–Ј–Є—Б—В–Њ–є –Њ–±–Њ–ї–Њ—З–Ї–Є –ґ–µ–ї—Г–і–Ї–∞. –Ъ—А–Њ–Љ–µ —В–Њ–≥–Њ, –±—Л—Б—В—А—Л–є –њ—А–Њ—Ж–µ—Б—Б —Д–Є–Ј–Є–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Њ–є —А–µ–≥–µ–љ–µ—А–∞—Ж–Є–Є —Н–њ–Є—В–µ–ї–Є—П, –њ–Њ—Б—В–Њ—П–љ–љ–Њ –і–Њ–±–∞–≤–ї—П–µ—В –Ї —Б–ї–Є–Ј–Є –і–µ—Б–Ї–≤–∞–Љ–Є—А–Њ–≤–∞–љ–љ—Л–µ —А–∞—Б–њ–∞–і–∞—О—Й–Є–µ—Б—П —Н–њ–Є—В–µ–ї–Є–∞–ї—М–љ—Л–µ –Ї–ї–µ—В–Ї–Є.
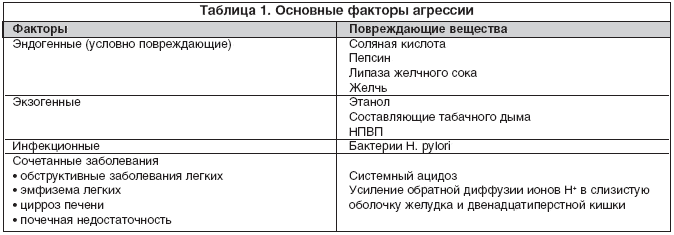
–°–ї–Є–Ј—М —Б–µ–Ї—А–µ—В–Є—А—Г–µ—В—Б—П –њ—Г—В–µ–Љ —Н–Ї–Ј–Њ—Ж–Є—В–Њ–Ј–∞ —Б –њ–Њ–≤–µ—А—Е–љ–Њ—Б—В–Є —Н–њ–Є—В–µ–ї–Є–∞–ї—М–љ—Л—Е –Є –≥–Њ–±–ї–µ—В–Њ–≤—Б–Ї–Є—Е –Ї–ї–µ—В–Њ–Ї. –Э–µ–њ–Њ—Б—А–µ–і—Б—В–≤–µ–љ–љ–∞—П —А–µ–≥—Г–ї—П—Ж–Є—П –≤—Л–±—А–Њ—Б–∞ –Њ—Б—Г—Й–µ—Б—В–≤–ї—П–µ—В—Б—П –≤–љ—Г—В—А–Є–Ї–ї–µ—В–Њ—З–љ—Л–Љ–Є –≤—В–Њ—А–Є—З–љ—Л–Љ–Є –Љ–µ–і–Є–∞—В–Њ—А–∞–Љ–Є, –Ї –Ї–Њ—В–Њ—А—Л–Љ –Њ—В–љ–Њ—Б–Є—В—Б—П —Ж–Є–Ї–ї–Є—З–µ—Б–Ї–∞—П –Р–Ь–§, —Д–Њ—Б—Д–∞—В–Є–і–Є–ї –Є–љ–Њ–Ј–Є—В–Њ–ї –Є Ca2+, –Ї–Њ—В–Њ—А—Л–µ –≤ —Б–≤–Њ—О –Њ—З–µ—А–µ–і—М –∞–Ї—В–Є–≤–Є—А—Г—О—В—Б—П –њ–Њ–і –≤–Њ–Ј–і–µ–є—Б—В–≤–Є–µ–Љ —Н–љ–і–Њ–≥–µ–љ–љ—Л—Е –љ–µ–є—А–Њ—В—А–∞–љ—Б–Љ–Є—В—В–µ—А–Њ–≤ (–љ–µ–є—А–Њ—В–µ–љ–Ј–Є–љ–∞ –Є –∞—Ж–µ—В–Є–ї—Е–Њ–ї–Є–љ–∞) –Є–ї–Є –њ–∞—А–∞–Ї—А–Є–љ–љ—Л—Е –≤–µ—Й–µ—Б—В–≤ (–њ—А–Њ—Б—В–∞–≥–ї–∞–љ–і–Є–љ–∞, –≤–∞–Ј–Њ–∞–Ї—В–Є–≤–љ–Њ–≥–Њ –Є–љ–≥–Є–±–Є—В–Њ—А–∞ –њ–µ–њ—Б–Є–љ–∞ – VIP, —Б–µ–Ї—А–µ—В–Є–љ–∞), —Б–≤—П–Ј—Л–≤–∞—О—Й–Є—Е—Б—П —Б —Б–Њ–Њ—В–≤–µ—В—Б—В–≤—Г—О—Й–Є–Љ–Є —А–µ—Ж–µ–њ—В–Њ—А–∞–Љ–Є –±–∞–Ј–∞–ї—М–љ–Њ–є –Љ–µ–Љ–±—А–∞–љ—Л —Б–µ–Ї—А–µ—В–Є—А—Г—О—Й–Є—Е –Ї–ї–µ—В–Њ–Ї (—А–Є—Б. 1). –°–µ–Ї—А–µ—Ж–Є—П —Б–ї–Є–Ј–Є –њ–Њ–і–∞–≤–ї—П–µ—В—Б—П –∞—В—А–Њ–њ–Є–љ–Њ–Љ —Б—Г–ї—М—Д–∞—В–Њ–Љ –Є –Э–Я–Т–Я. –Ъ–Њ–љ—В–∞–Ї—В —Б–ї–Є–Ј–Є—Б—В–Њ–є —Б –ї–µ–≥–Ї–Є–Љ–Є —А–∞–Ј–і—А–∞–ґ–Є—В–µ–ї—П–Љ–Є (—Б–Њ–ї—П–љ–Њ–є –Ї–Є—Б–ї–Њ—В–Њ–є, –Њ–ї–µ–Є–љ–Њ–≤–Њ–є –Ї–Є—Б–ї–Њ—В–Њ–є –Є–ї–Є —Н—В–∞–љ–Њ–ї–Њ–Љ) –≤–љ–Њ–≤—М —Б—В–Є–Љ—Г–ї–Є—А—Г–µ—В –њ—А–Њ–і—Г–Ї—Ж–Є—О —Б–ї–Є–Ј–Є —Б –њ–Њ–Љ–Њ—Й—М—О –Љ–µ—Б—В–љ—Л—Е –љ–µ–є—А–Њ—В—А–∞–љ—Б–Љ–Є—В—В–µ—А–Њ–≤, –њ–∞—А–∞–Ї—А–Є–љ–љ—Л—Е –≤–µ—Й–µ—Б—В–≤ –Є –≤—В–Њ—А–Є—З–љ—Л—Е –Љ–µ–і–Є–∞—В–Њ—А–Њ–≤. –£ –Ј–і–Њ—А–Њ–≤–Њ–≥–Њ —З–µ–ї–Њ–≤–µ–Ї–∞ —Б—Г—Й–µ—Б—В–≤—Г–µ—В —А–∞–≤–љ–Њ–≤–µ—Б–Є–µ –Љ–µ–ґ–і—Г –њ–Њ—Б—В–Њ—П–љ–љ–Њ–є –њ—А–Њ–і—Г–Ї—Ж–Є–µ–є —Б–ї–Є–Ј–Є –≥–∞—Б—В—А–Њ–і—Г–Њ–і–µ–љ–∞–ї—М–љ—Л–Љ–Є —Б–ї–Є–Ј–Є—Б—В—Л–Љ–Є –Ї–ї–µ—В–Ї–∞–Љ–Є, —Б –Њ–і–љ–Њ–є —Б—В–Њ—А–Њ–љ—Л, –Є –њ—А–Њ—В–µ–Њ–ї–Є—В–Є—З–µ—Б–Ї–Є–Љ –і–µ–є—Б—В–≤–Є–µ–Љ –њ–µ–њ—Б–Є–љ–∞ –Є —В—А–Є–њ—Б–Є–љ–∞, —А–∞–Ј—А—Г—Й–∞—О—Й–Є—Е —Ж–µ–ї–Њ—Б—В–љ–Њ—Б—В—М —Б–ї–Њ—П –≥–ї–Є–Ї–Њ–њ—А–Њ—В–µ–Є–љ–Њ–≤ –Є –њ–µ–њ—В–Є–і–Њ–≤ —Б–ї–Є–Ј–Є –≤ –њ—А–Њ—Б–≤–µ—В–µ –ґ–µ–ї—Г–і–Ї–∞ –Є –і–≤–µ–љ–∞–і—Ж–∞—В–Є–њ–µ—А—Б—В–љ–Њ–є –Ї–Є—И–Ї–Є – —Б –і—А—Г–≥–Њ–є.
–Ґ–∞–Ї–Є–Љ –Њ–±—А–∞–Ј–Њ–Љ, –Ј–∞—Й–Є—В–љ—Л–µ —Д—Г–љ–Ї—Ж–Є–Є —Б–ї–Є–Ј–Є –Њ—Б—Г—Й–µ—Б—В–≤–ї—П—О—В—Б—П —Б–ї–µ–і—Г—О—Й–Є–Љ–Є –њ—Г—В—П–Љ–Є:
1) –Ї–Њ–љ—Ж–µ–љ—В—А–Є—А—Г—П –Є —Г–і–µ—А–ґ–Є–≤–∞—П –∞–љ–Є–Њ–љ—Л –Э–°–Ю3- —Г –њ–Њ–≤–µ—А—Е–љ–Њ—Б—В–Є –њ–∞—А–Є–µ—В–∞–ї—М–љ—Л—Е –Ї–ї–µ—В–Њ–Ї –≤ –љ–µ–∞–Ї—В–Є–≤–љ–Њ–Љ —Б–ї–Њ–µ, –њ—А–µ–њ—П—В—Б—В–≤—Г—П –Є—Е –і–∞–ї—М–љ–µ–є—И–µ–є –і–Є—Д—Д—Г–Ј–Є–Є –≤ –њ—А–Њ—Б–≤–µ—В –ґ–µ–ї—Г–і–Ї–∞;
2) –њ—А–µ–і–Њ—В–≤—А–∞—Й–∞—П –Ї–Њ–љ—В–∞–Ї—В –Ї–ї–µ—В–Њ–Ї –њ–Њ–Ї—А–Њ–≤–љ–Њ–≥–Њ —Н–њ–Є—В–µ–ї–Є—П —Б –њ–µ–њ—Б–Є–љ–Њ–Љ –Є –ґ–µ–ї—Г–і–Њ—З–љ–Њ–є –ї–Є–њ–∞–Ј–Њ–є;
3) –Њ–±–≤–Њ–ї–∞–Ї–Є–≤–∞—П —Б–≤–µ–ґ–Є–µ, —В–Њ–ї—М–Ї–Њ —З—В–Њ –њ—А–Њ–≥–ї–Њ—З–µ–љ–љ—Л–µ —З–∞—Б—В–Є—З–Ї–Є –њ–Є—Й–Є, —Б–Љ–∞–Ј—Л–≤–∞—П –њ–Њ–Ї—А–Њ–≤ –ґ–µ–ї—Г–і–Ї–∞ –Є –њ—А–µ–і–Њ—Е—А–∞–љ—П—П –µ–≥–Њ —В–∞–Ї–Є–Љ –Њ–±—А–∞–Ј–Њ–Љ –Њ—В –њ–Њ–≤—А–µ–ґ–і–µ–љ–Є–є –≥—А—Г–±–Њ–є –њ–Є—Й–µ–є;
4) —З–∞—Б—В–Є—З–љ–Њ –љ–µ–є—В—А–∞–ї–Є–Ј—Г—П –Є–Њ–љ—Л –Э+ —Б –њ–Њ–Љ–Њ—Й—М—О –Њ—В—А–Є—Ж–∞—В–µ–ї—М–љ–Њ –Ј–∞—А—П–ґ–µ–љ–љ—Л—Е –≥–ї–Є–Ї–Њ–њ—А–Њ—В–µ–Є–љ–Њ–≤ –Є –њ–µ–њ—В–Є–і–Њ–≤ —Б–ї–Є–Ј–Є;
5) –Ј–∞—Е–≤–∞—В—Л–≤–∞—П –±–∞–Ї—В–µ—А–Є–Є, –њ–Њ—Б—В—Г–њ–Є–≤—И–Є–µ –≤ –њ—А–Њ—Б–≤–µ—В –ґ–µ–ї—Г–і–Ї–∞ –Є –і–≤–µ–љ–∞–і—Ж–∞—В–Є–њ–µ—А—Б—В–љ–Њ–є –Ї–Є—И–Ї–Є.
–Ч–∞—Й–Є—В–љ—Л–є —Б–ї–Њ–є —Н–њ–Є—В–µ–ї–Є–∞–ї—М–љ—Л—Е –Ї–ї–µ—В–Њ–Ї
–†—П–і –≥–∞—Б—В—А–Њ–і—Г–Њ–і–µ–љ–∞–ї—М–љ—Л—Е —Н–њ–Є—В–µ–ї–Є–∞–ї—М–љ—Л—Е –Ї–ї–µ—В–Њ–Ї, –≤—Л—Б—В–Є–ї–∞—О—Й–Є—Е –њ—А–Њ—Б–≤–µ—В –ґ–µ–ї—Г–і–Ї–∞ –Є –і–≤–µ–љ–∞–і—Ж–∞—В–Є–њ–µ—А—Б—В–љ–Њ–є –Ї–Є—И–Ї–Є, —Б–∞–Љ –њ–Њ —Б–µ–±–µ —Б–Њ–Ј–і–∞–µ—В —Б–≤–Њ–µ–Њ–±—А–∞–Ј–љ—Г—О –љ–µ–њ—А–Њ–љ–Є—Ж–∞–µ–Љ—Г—О –Ј–∞—Й–Є—В–љ—Г—О –Љ–µ–Љ–±—А–∞–љ—Г –Є —П–≤–ї—П–µ—В—Б—П —Б–ї–µ–і—Г—О—Й–µ–є –ї–Є–љ–Є–µ–є –Ј–∞—Й–Є—В—Л —Б–ї–Є–Ј–Є—Б—В–Њ–≥–Њ –±–∞—А—М–µ—А–∞. –Ь–Њ—А—Д–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є–Љ–Є —Б—В—А—Г–Ї—В—Г—А–∞–Љ–Є, —Б–њ–Њ—Б–Њ–±—Б—В–≤—Г—О—Й–Є–Љ–Є –Њ—Б—Г—Й–µ—Б—В–≤–ї–µ–љ–Є—О —Н—В–Њ–є —Д—Г–љ–Ї—Ж–Є–Є, —Б–ї—Г–ґ–∞—В –±–Є—Б–ї–Њ–є–љ—Л–µ —Д–Њ—Б—Д–Њ–ї–Є–њ–Є–і–љ—Л–µ –∞–њ–Є–Ї–∞–ї—М–љ—Л–µ –Љ–µ–Љ–±—А–∞–љ—Л –Ї–ї–µ—В–Њ–Ї, –њ–ї–Њ—В–љ–Њ –њ–Њ–Ї—А—Л–≤–∞—О—Й–Є–µ –Є—Е —Б–Њ —Б—В–Њ—А–Њ–љ—Л –њ—А–Њ—Б–≤–µ—В–∞ –ґ–µ–ї—Г–і–Ї–∞ –Є –љ–µ–њ—А–Њ–љ–Є—Ж–∞–µ–Љ—Л–µ –њ–ї–Њ—В–љ—Л–µ —Б–Њ–µ–і–Є–љ–µ–љ–Є—П –Љ–µ–ґ–і—Г —Б–Њ—Б–µ–і–љ–Є–Љ–Є –Ї–ї–µ—В–Ї–∞–Љ–Є —Н–њ–Є—В–µ–ї–Є—П, –≤ –Њ–±—Л—З–љ—Л—Е —Г—Б–ї–Њ–≤–Є—П—Е –њ—А–µ–і–Њ—В–≤—А–∞—Й–∞—О—Й–Є–µ –Њ–±—А–∞—В–љ–Њ–µ –њ–Њ—Б—В—Г–њ–ї–µ–љ–Є–µ –Ї–Є—Б–ї–Њ–≥–Њ –ґ–µ–ї—Г–і–Њ—З–љ–Њ–≥–Њ —Б–Њ–Ї–∞ –Є–Ј –њ—А–Њ—Б–≤–µ—В–∞ –ґ–µ–ї—Г–і–Ї–∞ –≤ –Ї–ї–µ—В–Ї–Є –Є —З–µ—А–µ–Ј –Њ–Ї–Њ–ї–Њ–Ї–ї–µ—В–Њ—З–љ–Њ–µ –њ—А–Њ—Б—В—А–∞–љ—Б—В–≤–Њ –≤ –Є–љ—В–µ—А—Б—В–Є—Ж–Є–∞–ї—М–љ—Г—О —В–Ї–∞–љ—М. –≠—В–Є –Љ–µ–ґ–Ї–ї–µ—В–Њ—З–љ—Л–µ —Б–Њ–µ–і–Є–љ–µ–љ–Є—П –њ—А–µ–і—Б—В–∞–≤–ї–µ–љ—Л –Љ–љ–Њ–ґ–µ—Б—В–≤–Њ–Љ (–Њ–Ї–Њ–ї–Њ 15) –±–µ–ї–Ї–Њ–≤—Л—Е —В—П–ґ–µ–є, –Ї–Њ—В–Њ—А—Л–µ, –Ї–∞–Ї —А–µ–Љ–љ—П–Љ–Є, —Б—В—П–≥–Є–≤–∞—О—В –Ї–ї–µ—В–Ї–Є –Љ–µ–ґ–і—Г —Б–Њ–±–Њ–є. –Я–Њ–і —Н–ї–µ–Ї—В—А–Њ–љ–љ—Л–Љ –Љ–Є–Ї—А–Њ—Б–Ї–Њ–њ–Њ–Љ –љ–µ –±—Л–ї–Њ –Њ–±–љ–∞—А—Г–ґ–µ–љ–Њ –≤–Є–і–Є–Љ—Л—Е –і–µ—Д–µ–Ї—В–Њ–≤ –≤ –њ–ї–Њ—В–љ—Л—Е –њ—А–Њ—В–µ–Є–љ–Њ–≤—Л—Е —Б—В—П–ґ–Ї–∞—Е –Љ–µ–ґ–і—Г –Ї–ї–µ—В–Ї–∞–Љ–Є –љ–∞ –Ј–∞–Љ–Њ—А–Њ–ґ–µ–љ–љ—Л—Е —Б—А–µ–Ј–∞—Е —Б–ї–Є–Ј–Є—Б—В–Њ–є. –°–Њ–µ–і–Є–љ–µ–љ–Є—П –Ї–ї–µ—В–Њ–Ї –≤ —Д—Г–љ–і–∞–ї—М–љ–Њ–Љ –Њ—В–і–µ–ї–µ –ґ–µ–ї—Г–і–Ї–∞ –±–Њ–ї–µ–µ –њ–ї–Њ—В–љ—Л–µ, —З–µ–Љ –∞–љ–∞–ї–Њ–≥–Є—З–љ—Л–µ —Б–≤—П–Ј–Є –≤ –∞–љ—В—А–∞–ї—М–љ–Њ–Љ –Њ—В–і–µ–ї–µ –Є –і–≤–µ–љ–∞–і—Ж–∞—В–Є–њ–µ—А—Б—В–љ–Њ–є –Ї–Є—И–Ї–µ, –Ї—Г–і–∞ –њ—А–Њ–Є—Б—Е–Њ–і–Є—В –Љ–µ–љ—М—И–Є–є –≤—Л–±—А–Њ—Б –Ї–Є—Б–ї–Њ—В—Л.
–Х—Б–ї–Є —Б–Њ–ї—П–љ–∞—П –Ї–Є—Б–ї–Њ—В–∞ –≤—Б–µ –ґ–µ –њ—А–Њ–љ–Є–Ї–∞–µ—В –≤ —Ж–Є—В–Њ–њ–ї–∞–Ј–Љ—Г, —Н–њ–Є—В–µ–ї–Є–∞–ї—М–љ—Л–µ –Ї–ї–µ—В–Ї–Є —Б–њ–Њ—Б–Њ–±–љ—Л –њ—А–Њ—В–Є–≤–Њ—Б—В–Њ—П—В—М –љ–µ–±–Њ–ї—М—И–Њ–є –Ј–∞–Ї–Є—Б–ї–µ–љ–љ–Њ—Б—В–Є —Б –њ–Њ–Љ–Њ—Й—М—О –Љ–µ—Е–∞–љ–Є–Ј–Љ–∞ –Є–Њ–љ–љ–Њ–≥–Њ Na+/H+ –Њ–±–Љ–µ–љ–∞ –Є –Њ–±—А–∞—В–љ–Њ–≥–Њ –њ–Њ—Б—В—Г–њ–ї–µ–љ–Є—П –Э–°–Ю3- –≤ —Ж–Є—В–Њ–њ–ї–∞–Ј–Љ—Г —З–µ—А–µ–Ј Na+/–Э–°–Ю3- –Ї–∞–љ–∞–ї—Л. –Э–µ–њ—А–Њ–љ–Є—Ж–∞–µ–Љ–Њ—Б—В—М –∞–њ–Є–Ї–∞–ї—М–љ—Л—Е –Љ–µ–Љ–±—А–∞–љ –Є –Њ–Ї–Њ–ї–Њ–Ї–ї–µ—В–Њ—З–љ—Л—Е —Б–Њ–µ–і–Є–љ–µ–љ–Є–є –і–ї—П –Ї–Є—Б–ї–Њ—В—Л –і–µ–ї–∞—О—В —Н—В–Є –Љ–µ—Е–∞–љ–Є–Ј–Љ—Л –і–Њ—Б—В–∞—В–Њ—З–љ—Л–Љ–Є –і–ї—П –њ–Њ–і–і–µ—А–ґ–∞–љ–Є—П –≤–љ—Г—В—А–Є –Ї–ї–µ—В–Њ–Ї –Ј–љ–∞—З–µ–љ–Є–є –њ–Њ–Ї–∞–Ј–∞—В–µ–ї—П pH –љ–∞ –љ–Њ—А–Љ–∞–ї—М–љ–Њ–Љ —Г—А–Њ–≤–љ–µ (pH 7).
–Т —Г—Б–ї–Њ–≤–Є—П—Е —Д–Є–Ј–Є–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Њ–є —А–µ–≥–µ–љ–µ—А–∞—Ж–Є–Є —Н–њ–Є—В–µ–ї–Є–∞–ї—М–љ—Л—Е –≥–∞—Б—В—А–Њ–і—Г–Њ–і–µ–љ–∞–ї—М–љ—Л—Е –Ї–ї–µ—В–Њ–Ї (–≤ –љ–Њ—А–Љ–µ –њ–µ—А–Є–Њ–і –Є—Е –њ–Њ–ї—Г–ґ–Є–Ј–љ–Є —Б–Њ—Б—В–∞–≤–ї—П–µ—В 2 –і–љ—П) –Є–ї–Є –њ—А–Є –Є—Е –≥–Є–±–µ–ї–Є –њ–Њ–і –≤–Њ–Ј–і–µ–є—Б—В–≤–Є–µ–Љ —В–Њ–Ї—Б–Є—З–µ—Б–Ї–Є—Е –≤–µ—Й–µ—Б—В–≤ (–Э–Я–Т–Я, –∞–ї–Ї–Њ–≥–Њ–ї—М –Є –і—А.), –Њ–љ–Є —Б–ї—Г—Й–Є–≤–∞—О—В—Б—П –≤ –љ–µ–∞–Ї—В–Є–≤–љ—Л–є —Б–ї–Њ–є –Є –±—Л—Б—В—А–Њ –Ј–∞–Љ–µ—Й–∞—О—В—Б—П –Љ–Є–≥—А–Є—А—Г—О—Й–Є–Љ–Є —Н–њ–Є—В–µ–ї–Є–∞–ї—М–љ—Л–Љ–Є –Ї–ї–µ—В–Ї–∞–Љ–Є, –њ–Њ–і–љ–Є–Љ–∞—О—Й–Є–Љ–Є—Б—П –Є–Ј –≥–µ–љ–µ—А–∞—В–Є–≤–љ–Њ–є –Ј–Њ–љ—Л –Њ–±–ї–∞—Б—В–Є —И–µ–µ—З–љ—Л—Е –ґ–µ–ї–µ–Ј. –≠—В–Њ—В –њ—А–Њ—Ж–µ—Б—Б –Њ–±–љ–Њ–≤–ї–µ–љ–Є—П —Н–њ–Є—В–µ–ї–Є–∞–ї—М–љ—Л—Е –Ї–ї–µ—В–Њ–Ї, —Б–ї–µ–і—Г—О—Й–Є–є –Ј–∞ –Є—Е –≥–Є–±–µ–ї—М—О, –љ–∞–Ј—Л–≤–∞–µ—В—Б—П “—А–µ—Б—В–Є—В—Г—Ж–Є—П” (–≤–Њ—Б—Б—В–∞–љ–Њ–≤–ї–µ–љ–Є–µ).
–°–µ–Ї—А–µ—Ж–Є—П –±–Є–Ї–∞—А–±–Њ–љ–∞—В–Њ–≤ –≤ –ґ–µ–ї—Г–і–Ї–µ
–°–µ–Ї—А–µ—Ж–Є—П –±–Є–Ї–∞—А–±–Њ–љ–∞—В–Њ–≤ (–∞–љ–Є–Њ–љ–Њ–≤ –Э–°–Ю3-) –Ї–ї–µ—В–Ї–∞–Љ–Є –њ–Њ–≤–µ—А—Е–љ–Њ—Б—В–љ–Њ–≥–Њ —Н–њ–Є—В–µ–ї–Є—П –Њ—Б—Г—Й–µ—Б—В–≤–ї—П–µ—В—Б—П —Б –њ–Њ–Љ–Њ—Й—М—О –њ—А–Њ—Ж–µ—Б—Б–Њ–≤ –≤–љ—Г—В—А–Є–Ї–ї–µ—В–Њ—З–љ–Њ–≥–Њ –Љ–µ—В–∞–±–Њ–ї–Є–Ј–Љ–∞, –∞ –≤—Л–і–µ–ї–µ–љ–Є–µ –Є—Е –≤ –њ—А–Њ—Б–≤–µ—В –ґ–µ–ї—Г–і–Ї–∞ – –∞–Ї—В–Є–≤–љ—Л–Љ —В—А–∞–љ—Б—Ж–µ–ї–ї—О–ї—П—А–љ—Л–Љ –Є–Њ–љ–Њ–Њ–±–Љ–µ–љ–љ—Л–Љ –њ—Г—В–µ–Љ —З–µ—А–µ–Ј –∞–њ–Є–Ї–∞–ї—М–љ—Л–µ –њ–Њ–≤–µ—А—Е–љ–Њ—Б—В–Є –Ї–ї–µ—В–Њ—З–љ—Л—Е –Љ–µ–Љ–±—А–∞–љ.
–Т–љ—Г—В—А–Є–Ї–ї–µ—В–Њ—З–љ–∞—П –Ї–∞—А–±–Њ–∞–љ–≥–Є–і—А–∞–Ј–∞ –њ—А–µ–≤—А–∞—Й–∞–µ—В –°–Ю2 –Є –Э2–Ю –≤ –Э–°–Ю3- –Є H+. Na–Э–°–Ю3 –њ–Њ—Б—В—Г–њ–∞–µ—В –≤ –Ї–ї–µ—В–Ї–Є —Б —В–Њ–Ї–Њ–Љ –Ї—А–Њ–≤–Є –Є–Ј –Є–љ—В–µ—А—Б—В–Є—Ж–Є–∞–ї—М–љ–Њ–є —В–Ї–∞–љ–Є, –і–Њ–±–∞–≤–ї—П—П –±—Г—Д–µ—А–љ—Л–µ –≤–µ—Й–µ—Б—В–≤–∞ –Ї –≤–љ—Г—В—А–Є–Ї–ї–µ—В–Њ—З–љ–Њ–Љ—Г –њ—Г–ї—Г –±–Є–Ї–∞—А–±–Њ–љ–∞—В–Њ–≤. –І–µ—А–µ–Ј –Э–°–Ю3-/Cl--–Є–Њ–љ–Њo–±–Љ–µ–љ–љ–Є–Ї–Є –∞–њ–Є–Ї–∞–ї—М–љ–Њ–є –Љ–µ–Љ–±—А–∞–љ—Л –њ—А–Њ–Є—Б—Е–Њ–і–Є—В –≤—Л–і–µ–ї–µ–љ–Є–µ –Э–°–Ю3- –≤ –љ–µ–∞–Ї—В–Є–≤–љ—Л–є —Б–ї–Њ–є —Б–ї–Є–Ј–Є. –£ –Ј–і–Њ—А–Њ–≤—Л—Е –≤–Ј—А–Њ—Б–ї—Л—Е –ї—О–і–µ–є –∞–±–Њ–ї—О—В–љ–∞—П –њ—А–Њ–і—Г–Ї—Ж–Є—П –Є–Њ–љ–Њ–≤ –Э–°–Ю3- —Б–Њ—Б—В–∞–≤–ї—П–µ—В 1 –Љ–Љ–Њ–ї—М/—З. –Ш–Њ–љ–Њ–Њ–±–Љ–µ–љ–љ–Є–Ї–Є –±–∞–Ј–Њ–ї–∞—В–µ—А–∞–ї—М–љ–Њ–є –Љ–µ–Љ–±—А–∞–љ—Л –≤ —Б–≤–Њ—О –Њ—З–µ—А–µ–і—М –њ–Њ–і–і–µ—А–ґ–Є–≤–∞—О—В –≤–љ—Г—В—А–Є–Ї–ї–µ—В–Њ—З–љ—Г—О –Ї–Њ–љ—Ж–µ–љ—В—А–∞—Ж–Є—О –Є–Њ–љ–Њ–≤ –Э+, Na+ –Є –Ъ+ –љ–∞ –њ–Њ—Б—В–Њ—П–љ–љ–Њ–Љ —Г—А–Њ–≤–љ–µ.
–Ю–±—К–µ–Љ —Б–µ–Ї—А–µ—Ж–Є–Є –±–Є–Ї–∞—А–±–Њ–љ–∞—В–Њ–≤ —Б–ї–Є–Ј–Є—Б—В–Њ–є –ґ–µ–ї—Г–і–Ї–∞ —Б–Њ—Б—В–∞–≤–ї—П–µ—В –љ–µ –±–Њ–ї–µ–µ 10% –≤—Л–±—А–Њ—Б–∞ —Б–Њ–ї—П–љ–Њ–є –Ї–Є—Б–ї–Њ—В—Л. –Я—А–Є–љ–Є–Љ–∞—П –≤–Њ –≤–љ–Є–Љ–∞–љ–Є–µ, —З—В–Њ –ґ–µ–ї—Г–і–Њ–Ї —Б–µ–Ї—А–µ—В–Є—А—Г–µ—В 100 –Љ–Љ–Њ–ї—М HCl, –њ—А–Њ–і—Г–Ї—Ж–Є—П –±–Є–Ї–∞—А–±–Њ–љ–∞—В–Њ–≤ —Б–Њ—Б—В–∞–≤–ї—П–µ—В 10 –Љ–Љ–Њ–ї—М –Э–°–Ю3- –≤ —Б—Г—В–Ї–Є. –°–ї–µ–і–Њ–≤–∞—В–µ–ї—М–љ–Њ, —В–∞–Ї–Њ–є –Њ–±—К–µ–Љ –±–∞–Ј–∞–ї—М–љ–Њ–є –њ—А–Њ–і—Г–Ї—Ж–Є–Є –±–Є–Ї–∞—А–±–Њ–љ–∞—В–Њ–≤ –љ–µ –Љ–Њ–ґ–µ—В –љ–µ–є—В—А–∞–ї–Є–Ј–Њ–≤–∞—В—М —А–∞—Б—В–≤–Њ—А –Ї–Є—Б–ї–Њ—В—Л —Б pH —А–∞–≤–љ–Њ–є 1. –Т —В–Њ –ґ–µ –≤—А–µ–Љ—П, –µ—Б–ї–Є –ґ–µ–ї—Г–і–Њ–Ї —Б–µ–Ї—А–µ—В–Є—А—Г–µ—В 10 –Љ–Љ–Њ–ї—М HCl –≤ —Б—Г—В–Ї–Є, –і–ї—П –љ–µ–є—В—А–∞–ї–Є–Ј–∞—Ж–Є–Є –і–Њ—Б—В–∞—В–Њ—З–љ–Њ —Б–µ–Ї—А–µ—Ж–Є–Є 10 –Љ–Љ–Њ–ї—М –Э–°–Ю3-. –Ґ–∞–Ї–Є–Љ –Њ–±—А–∞–Ј–Њ–Љ, –±–∞–Ј–∞–ї—М–љ–Њ–є —Б–µ–Ї—А–µ—Ж–Є–Є –±–Є–Ї–∞—А–±–Њ–љ–∞—В–Њ–≤ –і–Њ—Б—В–∞—В–Њ—З–љ–Њ –і–ї—П –љ–µ–є—В—А–∞–ї–Є–Ј–∞—Ж–Є–Є —А–∞—Б—В–≤–Њ—А–∞ –Ї–Є—Б–ї–Њ—В—Л —Б pH —А–∞–≤–љ–Њ–є 2.
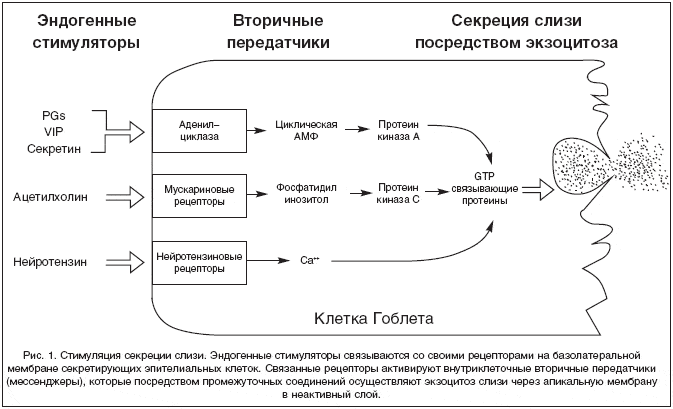
–≠—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В—М —А–∞–±–Њ—В—Л —Б–ї–Є–Ј–Є—Б—В–Њ–≥–Њ –±–∞—А—М–µ—А–∞ –њ–Њ –љ–µ–є—В—А–∞–ї–Є–Ј–∞—Ж–Є–Є –Ї–Є—Б–ї–Њ—В—Л –Њ—В—А–∞–ґ–∞–µ—В –≥—А–∞–і–Є–µ–љ—В pH –Љ–µ–ґ–і—Г –њ—А–Њ—Б–≤–µ—В–Њ–Љ –ґ–µ–ї—Г–і–Ї–∞, –њ–Њ–≤–µ—А—Е–љ–Њ—Б—В—М—О –Ї–ї–µ—В–Њ–Ї —Н–њ–Є—В–µ–ї–Є—П, —Ж–Є—В–Њ–њ–ї–∞–Ј–Љ–Њ–є —Н—В–Є—Е –Ї–ї–µ—В–Њ–Ї –Є –Ї—А–Њ–≤—М—О (—А–Є—Б. 2). –Х—Б–ї–Є —Г –Ј–і–Њ—А–Њ–≤—Л—Е –ї—О–і–µ–є pH –≤ –њ—А–Њ—Б–≤–µ—В–µ –ґ–µ–ї—Г–і–Ї–∞ —Б–Њ—Б—В–∞–≤–ї—П–µ—В 2, –љ–∞ –њ–Њ–≤–µ—А—Е–љ–Њ—Б—В–Є —Б–ї–Є–Ј–Є—Б—В—Л—Е –Ї–ї–µ—В–Њ–Ї pH 6, –≤–љ—Г—В—А–Є —Б–ї–Є–Ј–Є—Б—В–Њ–є pH —А–∞–≤–љ—П–µ—В—Б—П —Г–ґ–µ 7, –∞ –≤ –Ї—А–Њ–≤–Њ—В–Њ–Ї–µ – 7,4. –Ъ–Њ–≥–і–∞ —Б–µ–Ї—А–µ—Ж–Є—П –Э–°–Ю3- –њ–Њ–і–∞–≤–ї—П–µ—В—Б—П –Є–ї–Є —Г—Б–Є–ї–Є–≤–∞—О—В—Б—П –њ—А–Њ—Ж–µ—Б—Б—Л –њ—А–Њ—В–µ–Њ–ї–Є–Ј–∞ —Б–ї–Є–Ј–Є (—З—В–Њ –љ–∞–±–ї—О–і–∞–µ—В—Б—П –њ—А–Є –њ—А–Є–µ–Љ–µ –Э–Я–Т–Я), –≤–љ—Г—В—А–Є–Ї–ї–µ—В–Њ—З–љ—Л–є –∞—Ж–Є–і–Њ–Ј –Љ–Њ–ґ–µ—В –њ—А–Є–≤–µ—Б—В–Є –Ї –љ–µ–Ї—А–Њ–Ј—Г –Ї–ї–µ—В–Њ–Ї —Б–ї–Є–Ј–Є—Б—В–Њ–є.
–°–µ–Ї—А–µ—Ж–Є—П –±–Є–Ї–∞—А–±–Њ–љ–∞—В–Њ–≤ –≤ –і–≤–µ–љ–∞–і—Ж–∞—В–Є–њ–µ—А—Б—В–љ–Њ–є –Ї–Є—И–Ї–µ
–≠–љ—В–µ—А–Њ—Ж–Є—В—Л —В–Њ–љ–Ї–Њ–є –Ї–Є—И–Ї–Є, —В–∞–Ї –ґ–µ –Ї–∞–Ї —Н–њ–Є—В–µ–ї–Є–∞–ї—М–љ—Л–µ –Ї–ї–µ—В–Ї–Є –ґ–µ–ї—Г–і–Ї–∞, —Б–µ–Ї—А–µ—В–Є—А—Г—О—В –Э–°–Ю3- –≤ –љ–µ–∞–Ї—В–Є–≤–љ—Л–є —Б–ї–Њ–є –њ–Њ—Б—А–µ–і—Б—В–≤–Њ–Љ –Њ–њ–Є—Б–∞–љ–љ—Л—Е –∞–Ї—В–Є–≤–љ—Л—Е –Є–Њ–љ–Њ–Њ–±–Љ–µ–љ–љ—Л—Е –Љ–µ—Е–∞–љ–Є–Ј–Љ–Њ–≤. –Ю–і–љ–∞–Ї–Њ –≤ –Њ—В–ї–Є—З–Є–µ –Њ—В —Н–њ–Є—В–µ–ї–Є—П –ґ–µ–ї—Г–і–Ї–∞ —Н–њ–Є—В–µ–ї–Є–∞–ї—М–љ—Л–µ –Ї–ї–µ—В–Ї–Є –і–≤–µ–љ–∞–і—Ж–∞—В–Є–њ–µ—А—Б—В–љ–Њ–є –Ї–Є—И–Ї–Є –Љ–Њ–≥—Г—В –і–Њ–њ–Њ–ї–љ–Є—В–µ–ї—М–љ–Њ —Б–µ–Ї—А–µ—В–Є—А–Њ–≤–∞—В—М –±–Є–Ї–∞—А–±–Њ–љ–∞—В—Л –µ—Й–µ –і–≤—Г–Љ—П –њ–∞—Б—Б–Є–≤–љ—Л–Љ–Є –њ—А–Њ–≤–Њ–і–љ–Є–Ї–Њ–≤—Л–Љ–Є –њ—Г—В—П–Љ–Є: 1) —З–µ—А–µ–Ј –њ—А–Њ–≤–Њ–і–љ–Є–Ї–Є –∞–њ–Є–Ї–∞–ї—М–љ–Њ–є –Љ–µ–Љ–±—А–∞–љ—Л –Є–Ј —Ж–Є—В–Њ–њ–ї–∞–Ј–Љ—Л –≤ –њ—А–Њ—Б–≤–µ—В –Ї–Є—И–Ї–Є –Є 2) –њ–Њ –Љ–µ–ґ–Ї–ї–µ—В–Њ—З–љ—Л–Љ –њ—А–Њ–≤–Њ–і–љ–Є–Ї–∞–Љ –Є–Ј –Є–љ—В–µ—А—Б—В–Є—Ж–Є–∞–ї—М–љ—Л—Е —В–Ї–∞–љ–µ–є –≤ –њ—А–Њ—Б–≤–µ—В –Ї–Є—И–Ї–Є. –Я–Њ—Б–ї–µ–і–љ–Є–є –њ—Г—В—М –≤–Њ–Ј–Љ–Њ–ґ–µ–љ –±–ї–∞–≥–Њ–і–∞—А—П –Љ–µ–љ–µ–µ –њ–ї–Њ—В–љ—Л–Љ –њ–Њ —Б—А–∞–≤–љ–µ–љ–Є—О —Б –ґ–µ–ї—Г–і–Ї–Њ–Љ —Б–Њ–µ–і–Є–љ–µ–љ–Є—П–Љ –Љ–µ–ґ–і—Г —Б–Њ—Б–µ–і–љ–Є–Љ–Є –Ї–ї–µ—В–Ї–∞–Љ–Є —Н–њ–Є—В–µ–ї–Є—П. –Т –і–≤–µ–љ–∞–і—Ж–∞—В–Є–њ–µ—А—Б—В–љ–Њ–є –Ї–Є—И–Ї–µ 40% –Њ–±—К–µ–Љ–∞ –њ—А–Њ–і—Г–Ї—Ж–Є–Є –±–Є–Ї–∞—А–±–Њ–љ–∞—В–Њ–≤ –њ—А–Є—Е–Њ–і–Є—В—Б—П –Є–Љ–µ–љ–љ–Њ –љ–∞ –њ—А–Њ–≤–Њ–і–љ–Є–Ї–Њ–≤—Л–є –њ—Г—В—М —Б–µ–Ї—А–µ—Ж–Є–Є. –≠—В–Є –Љ–љ–Њ–ґ–µ—Б—В–≤–µ–љ–љ—Л–µ –њ—А–Њ—Ж–µ—Б—Б—Л –њ–Њ–Ј–≤–Њ–ї—П—О—В –і—Г–Њ–і–µ–љ–∞–ї—М–љ–Њ–є —Б–ї–Є–Ј–Є—Б—В–Њ–є —Б–µ–Ї—А–µ—В–Є—А–Њ–≤–∞—В—М –љ–∞ –љ–µ—Б–Ї–Њ–ї—М–Ї–Њ –њ–Њ—А—П–і–Ї–Њ–≤ –±–Њ–ї—М—И–µ –∞–љ–Є–Њ–љ–Њ–≤ –Э–°–Ю3- –љ–∞ –≥—А–∞–Љ–Љ —В–Ї–∞–љ–Є, —З–µ–Љ —Б–µ–Ї—А–µ—В–Є—А—Г–µ—В —Б–ї–Є–Ј–Є—Б—В–∞—П –ґ–µ–ї—Г–і–Ї–∞. –Ш, –љ–∞–Ї–Њ–љ–µ—Ж, —Б–Њ—Б–µ–і–љ–Є–µ –Њ—А–≥–∞–љ—Л –њ–Є—Й–µ–≤–∞—А–µ–љ–Є—П –і–Њ–±–∞–≤–ї—П—О—В –Э–°–Ю3- –Є–Њ–љ—Л –≤ –њ—А–Њ—Б–≤–µ—В –Ї–Є—И–Ї–Є –≤ —Б–Њ—Б—В–∞–≤–µ –ґ–µ–ї—З–Є –Є –њ–∞–љ–Ї—А–µ–∞—В–Є—З–µ—Б–Ї–Њ–≥–Њ —Б–Њ–Ї–∞. –Я–Њ–і–ґ–µ–ї—Г–і–Њ—З–љ–∞—П –ґ–µ–ї–µ–Ј–∞ –Є –њ–µ—З–µ–љ—М —Б–µ–Ї—А–µ—В–Є—А—Г—О—В –њ–Њ 60 –Љ–Љ–Њ–ї—М –Э–°–Ю3- –≤ —Б—Г—В–Ї–Є –Ї–∞–ґ–і–∞—П. –Ґ–∞–Ї–Є–Љ –Њ–±—А–∞–Ј–Њ–Љ, –њ—А–Њ—Б–≤–µ—В –і–≤–µ–љ–∞–і—Ж–∞—В–Є–њ–µ—А—Б—В–љ–Њ–є –Ї–Є—И–Ї–Є –њ–Њ–ї—Г—З–∞–µ—В –њ—А–Є–Љ–µ—А–љ–Њ —Б—В–Њ–ї—М–Ї–Њ –ґ–µ –∞–љ–Є–Њ–љ–Њ–≤ –Э–°–Ю3- –≤ –і–µ–љ—М, —Б–Ї–Њ–ї—М–Ї–Њ –≤ –љ–µ–≥–Њ –њ–Њ—Б—В—Г–њ–∞–µ—В –Є–Ј –ґ–µ–ї—Г–і–Ї–∞ –Ї–∞—В–Є–Њ–љ–Њ–≤ –Э+. –°–Њ–Њ—В–≤–µ—В—Б—В–≤–µ–љ–љ–Њ –Ј–љ–∞—З–µ–љ–Є–µ pH –≤ –њ—А–Њ—Б–≤–µ—В–µ –њ–Є–ї–Њ—А–Є—З–µ—Б–Ї–Њ–≥–Њ —Б—Д–Є–љ–Ї—В–µ—А–∞ –Љ–Њ–ґ–µ—В –±—Л—В—М —А–∞–≤–љ—Л–Љ 2, –љ–Њ —Г–ґ–µ —З–µ—А–µ–Ј –љ–µ—Б–Ї–Њ–ї—М–Ї–Њ —Б–∞–љ—В–Є–Љ–µ—В—А–Њ–≤ –≤–љ—Г—В—А–Є –њ—А–Њ—Б–≤–µ—В–∞ –і–≤–µ–љ–∞–і—Ж–∞—В–Є–њ–µ—А—Б—В–љ–Њ–є –Ї–Є—И–Ї–Є pH –њ–Њ–і–љ–Є–Љ–∞–µ—В—Б—П –і–Њ 7–8.
–°–µ–Ї—А–µ—Ж–Є—П –±–Є–Ї–∞—А–±–Њ–љ–∞—В–Њ–≤ –і—Г–Њ–і–µ–љ–∞–ї—М–љ–Њ–є —Б–ї–Є–Ј–Є—Б—В–Њ–є —Г—Б–Є–ї–Є–≤–∞–µ—В—Б—П –≤ 3 —А–∞–Ј–∞ –њ—А–Є –њ—А—П–Љ–Њ–Љ –Ї–Њ–љ—В–∞–Ї—В–µ –Ї–ї–µ—В–Њ–Ї —Б –Є–Њ–љ–∞–Љ–Є –Э+, –Њ–і–љ–∞–Ї–Њ —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –і—Г–Њ–і–µ–љ–∞–ї—М–љ—Л–Љ–Є —П–Ј–≤–∞–Љ–Є —Н—В–∞ —А–µ–∞–Ї—Ж–Є—П –Њ—Б–ї–∞–±–ї–µ–љ–∞.
–Т –Њ—Б–љ–Њ–≤–µ —А–µ–≥—Г–ї—П—Ж–Є–Є —Б–µ–Ї—А–µ—Ж–Є–Є –±–Є–Ї–∞—А–±–Њ–љ–∞—В–Њ–≤ –ї–µ–ґ–Є—В —Ж–µ–љ—В—А–∞–ї—М–љ–∞—П –њ–∞—А–∞—Б–Є–Љ–њ–∞—В–Є—З–µ—Б–Ї–∞—П —Б—В–Є–Љ—Г–ї—П—Ж–Є—П –∞—Ж–µ—В–Є–ї—Е–Њ–ї–Є–љ–Њ–Љ, –≤—Л—Б–≤–Њ–±–Њ–ґ–і–∞—О—Й–Є–Љ—Б—П –њ—А–Є —А–∞–Ј–і—А–∞–ґ–µ–љ–Є–Є –≤–∞–≥—Г—Б–∞. –Ъ—А–Њ–Љ–µ —В–Њ–≥–Њ, –≥–∞—Б—В—А–Њ–і—Г–Њ–і–µ–љ–∞–ї—М–љ–∞—П —Б–µ–Ї—А–µ—Ж–Є—П –Э–°–Ю3- —Б—В–Є–Љ—Г–ї–Є—А—Г–µ—В—Б—П –Љ–µ—Б—В–љ—Л–Љ –≤—Л—Б–≤–Њ–±–Њ–ґ–і–µ–љ–Є–µ–Љ –њ—А–Њ—Б—В–∞–≥–ї–∞–љ–і–Є–љ–Њ–≤, –і–Њ–њ–∞–Љ–Є–љ–Њ–Љ –Є VIP –≤ –Њ—В–≤–µ—В –љ–∞ –њ–µ—А–≤–Є—З–љ–Њ–µ —А–∞–Ј–і—А–∞–ґ–µ–љ–Є–µ —Б–Њ–ї—П–љ–Њ–є –Ї–Є—Б–ї–Њ—В–Њ–є. –Я—А–Є —Н—В–Њ–Љ –љ–∞–Є–±–Њ–ї–µ–µ –Љ–Њ—Й–љ—Л–Љ —Б—В–Є–Љ—Г–ї–Њ–Љ —Б–µ–Ї—А–µ—Ж–Є–Є –±–Є–Ї–∞—А–±–Њ–љ–∞—В–Њ–≤ —П–≤–ї—П–µ—В—Б—П —Б–љ–Є–ґ–µ–љ–Є–µ pH –≤ –њ—А–Њ—Б–≤–µ—В–µ –ґ–µ–ї—Г–і–Ї–∞ –љ–Є–ґ–µ 2. –°–µ–Ї—А–µ—Ж–Є—П –±–Є–Ї–∞—А–±–Њ–љ–∞—В–Њ–≤ –њ–Њ–і–∞–≤–ї—П–µ—В—Б—П —Б–Є–Љ–њ–∞—В–Є—З–µ—Б–Ї–Њ–є –љ–µ—А–≤–љ–Њ–є —Б—В–Є–Љ—Г–ї—П—Ж–Є–µ–є.
–Ь–Є–Ї—А–Њ—Ж–Є—А–Ї—Г–ї—П—Ж–Є—П –Ї—А–Њ–≤–Є –≤ —Б–ї–Є–Ј–Є—Б—В–Њ–є –Њ–±–Њ–ї–Њ—З–Ї–µ
–Ґ—А–µ—В—М—О –ї–Є–љ–Є—О –Ј–∞—Й–Є—В—Л —Н–њ–Є—В–µ–ї–Є—П –ґ–µ–ї—Г–і–Ї–∞ –Є –і–≤–µ–љ–∞–і—Ж–∞—В–Є–њ–µ—А—Б—В–љ–Њ–є –Ї–Є—И–Ї–Є —Б–Њ–Ј–і–∞–µ—В –Љ–Є–Ї—А–Њ—Ж–Є—А–Ї—Г–ї—П—В–Њ—А–љ–Њ–µ —А—Г—Б–ї–Њ –Ї—А–Њ–≤–Є. –°–ї–Є–Ј–Є—Б—В–∞—П –Њ–±–Њ–ї–Њ—З–Ї–∞ –ґ–µ–ї—Г–і–Ї–∞ –Њ–±–Є–ї—М–љ–Њ —Б–љ–∞–±–ґ–µ–љ–∞ –≤–µ—В–≤—П—Й–µ–є—Б—П —Б–µ—В—М—О –Ї—А–Њ–≤–µ–љ–Њ—Б–љ—Л—Е –Ї–∞–њ–Є–ї–ї—П—А–Њ–≤.
–Ь–Є–Ї—А–Њ—Ж–Є—А–Ї—Г–ї—П—В–Њ—А–љ–Њ–µ —А—Г—Б–ї–Њ –≥–∞—Б—В—А–Њ–і—Г–Њ–і–µ–љ–∞–ї—М–љ–Њ–є —Б–ї–Є–Ј–Є—Б—В–Њ–є –Њ–±–µ—Б–њ–µ—З–Є–≤–∞–µ—В —Б–љ–∞–±–ґ–µ–љ–Є–µ —Н–њ–Є—В–µ–ї–Є–∞–ї—М–љ—Л—Е –Ї–ї–µ—В–Њ–Ї –≤–Њ–і–Њ–є, –Ї–Є—Б–ї–Њ—А–Њ–і–Њ–Љ, –њ–Є—В–∞—В–µ–ї—М–љ—Л–Љ–Є –Є –±—Г—Д–µ—А–љ—Л–Љ–Є –≤–µ—Й–µ—Б—В–≤–∞–Љ–Є, –±–µ–Ј –Ї–Њ—В–Њ—А—Л—Е –Ї–ї–µ—В–Ї–Є –љ–µ –Љ–Њ–≥–ї–Є –±—Л —Б–µ–Ї—А–µ—В–Є—А–Њ–≤–∞—В—М –Э–°–Ю3- –Є —Б–ї–Є–Ј—М. –Я—А–Є —Н—В–Њ–Љ —В–Њ–Ї –Ї—А–Њ–≤–Є –љ–∞–њ—А–∞–≤–ї–µ–љ —В–∞–Ї–Є–Љ –Њ–±—А–∞–Ј–Њ–Љ, —З—В–Њ —Н–њ–Є—В–µ–ї–Є–∞–ї—М–љ—Л–µ –Ї–ї–µ—В–Ї–Є –њ–Њ–ї—Г—З–∞—О—В –Ї—А–Њ–≤—М, –Ї–Њ—В–Њ—А–∞—П —Г–ґ–µ –њ—А–Њ—И–ї–∞ –≤ –љ–µ–њ–Њ—Б—А–µ–і—Б—В–≤–µ–љ–љ–Њ–є –±–ї–Є–Ј–Њ—Б—В–Є –Њ—В –њ–∞—А–Є–µ—В–∞–ї—М–љ—Л—Е –Ї–ї–µ—В–Њ–Ї. –°–µ–Ї—А–µ—Ж–Є—П —Б–Њ–ї—П–љ–Њ–є –Ї–Є—Б–ї–Њ—В—Л –њ–∞—А–Є–µ—В–∞–ї—М–љ—Л–Љ–Є –Ї–ї–µ—В–Ї–∞–Љ–Є –≤ –њ—А–Њ—Б–≤–µ—В –ґ–µ–ї—Г–і–Ї–∞ —Г—Б–Є–ї–Є–≤–∞–µ—В –Ї—А–Њ–≤–µ–љ–∞–њ–Њ–ї–љ–µ–љ–Є–µ —Б–ї–Є–Ј–Є—Б—В–Њ–є –Є –≤—Л–Ј—Л–≤–∞–µ—В –Љ–Њ—Й–љ–Њ–є –њ—А–Є—В–Њ–Ї —Б –Ї—А–Њ–≤—М—О —Й–µ–ї–Њ—З–љ—Л—Е —Б–Њ–µ–і–Є–љ–µ–љ–Є–є, —З—В–Њ –Њ–±–µ—Б–њ–µ—З–Є–≤–∞–µ—В –∞–і–µ–Ї–≤–∞—В–љ—Г—О —Б–µ–Ї—А–µ—Ж–Є—О –±–Є–Ї–∞—А–±–Њ–љ–∞—В–Њ–≤ –Ї–ї–µ—В–Ї–∞–Љ–Є –њ–Њ–≤–µ—А—Е–љ–Њ—Б—В–љ–Њ–≥–Њ —Н–њ–Є—В–µ–ї–Є—П. –Ъ–∞–њ–Є–ї–ї—П—А–љ–∞—П —Б–µ—В—М –Њ—Б—Г—Й–µ—Б—В–≤–ї—П–µ—В –Є –і—А–µ–љ–Є—А—Г—О—Й—Г—О —Д—Г–љ–Ї—Ж–Є—О, –Њ—В–≤–Њ–і—П –≤ –Њ–±—Й–Є–є –Ї—А–Њ–≤–Њ—В–Њ–Ї –Є–Њ–љ—Л –Э+, –њ—А–Њ–љ–Є–Ї—И–Є–µ –≤ —Б–ї–Є–Ј–Є—Б—В—Г—О.
–Х—Б–ї–Є —Б—В–Є–Љ—Г–ї—П—Ж–Є—П –ґ–µ–ї—Г–і–Њ—З–љ–Њ–є —Б–µ–Ї—А–µ—Ж–Є–Є –≤—Л–Ј—Л–≤–∞–µ—В –Ј–љ–∞—З–Є—В–µ–ї—М–љ–Њ–µ —Г—Б–Є–ї–µ–љ–Є–µ –Љ–µ—Б—В–љ–Њ–≥–Њ –Ї—А–Њ–≤–Њ—Б–љ–∞–±–ґ–µ–љ–Є—П, —В–Њ —Г–Љ–µ–љ—М—И–µ–љ–Є–µ –Ї–Є—Б–ї–Њ—В–љ–Њ–є –њ—А–Њ–і—Г–Ї—Ж–Є–Є —Б–љ–Є–ґ–∞–µ—В –Љ–µ—Б—В–љ—Л–є –Ї—А–Њ–≤–Њ—В–Њ–Ї –Є, —В–µ–Њ—А–µ—В–Є—З–µ—Б–Ї–Є, –і–µ–ї–∞–µ—В —Б–ї–Є–Ј–Є—Б—В—Г—О –Њ–±–Њ–ї–Њ—З–Ї—Г –±–Њ–ї–µ–µ —Г—П–Ј–≤–Є–Љ–Њ–є –Ї –≤–Њ–Ј–і–µ–є—Б—В–≤–Є—О —Д–∞–Ї—В–Њ—А–Њ–≤ –∞–≥—А–µ—Б—Б–Є–Є, —З—В–Њ —Б–Њ –≤—Б–µ–є –Њ—З–µ–≤–Є–і–љ–Њ—Б—В—М—О –њ–Њ–і—В–≤–µ—А–ґ–і–∞–µ—В—Б—П –≤ –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Њ–є –њ—А–∞–Ї—В–Є–Ї–µ.
b-–Р–і—А–µ–љ–µ—А–≥–Є—З–µ—Б–Ї–∞—П —Б—В–Є–Љ—Г–ї—П—Ж–Є—П, –≥–Є—Б—В–∞–Љ–Є–љ, –≤–∞–Ј–Њ–Ї–Њ–љ—Б—В—А–Є–Ї—В–Њ—А—Л –Є –Њ–Ї–Є—Б—М –∞–Ј–Њ—В–∞ —П–≤–ї—П—О—В—Б—П –Њ—Б–љ–Њ–≤–љ—Л–Љ–Є —Б—В–Є–Љ—Г–ї—П—В–Њ—А–∞–Љ–Є –Ї—А–Њ–≤–µ–љ–∞–њ–Њ–ї–љ–µ–љ–Є—П —Б–ї–Є–Ј–Є—Б—В–Њ–є. –Э–∞–њ—А–Њ—В–Є–≤, a-–∞–і—А–µ–љ–µ—А–≥–Є—З–µ—Б–Ї–∞—П —Б—В–Є–Љ—Г–ї—П—Ж–Є—П, –≤–∞–Ј–Њ–Ї–Њ–љ—Б—В—А–Є–Ї—В–Њ—А–љ—Л–µ –њ—А–Њ—Б—В–∞–≥–ї–∞–љ–і–Є–љ—Л, –Є–љ–і–Њ–Љ–µ—В–∞—Ж–Є–љ, —В—А–Њ–Љ–±–∞–Ї—Б–∞–љ, –ї–µ–є–Ї–Њ—В—А–Є–µ–љ –Т4 –Є —Д–∞–Ї—В–Њ—А, –∞–Ї—В–Є–≤–Є—А—Г—О—Й–Є–є —В—А–Њ–Љ–±–Њ—Ж–Є—В—Л, —Б–љ–Є–ґ–∞—О—В –Ї—А–Њ–≤–Њ—В–Њ–Ї –≤ —Б–ї–Є–Ј–Є—Б—В–Њ–є –Њ–±–Њ–ї–Њ—З–Ї–µ –ґ–µ–ї—Г–і–Ї–∞. –Ы—О–±–Њ–µ —А–µ–Ј–Ї–Њ–µ —Г–Љ–µ–љ—М—И–µ–љ–Є–µ —В–Њ–Ї–∞ –Ї—А–Њ–≤–Є, –љ–∞–њ—А–Є–Љ–µ—А –њ—А–Є –≥–µ–Љ–Њ—А—А–∞–≥–Є—З–µ—Б–Ї–Њ–Љ —И–Њ–Ї–µ, –≤—Л–Ј—Л–≤–∞–µ—В –Њ—Б—В—А—Г—О –Љ–µ—Б—В–љ—Г—О –Є—И–µ–Љ–Є—О —Б–ї–Є–Ј–Є—Б—В–Њ–є, —З—В–Њ —П–≤–ї—П–µ—В—Б—П –Њ—Б–љ–Њ–≤–љ—Л–Љ –Љ–µ—Е–∞–љ–Є–Ј–Љ–Њ–Љ –Њ–±—А–∞–Ј–Њ–≤–∞–љ–Є—П –Њ—Б—В—А—Л—Е —Б—В—А–µ—Б—Б–Њ—А–љ—Л—Е —П–Ј–≤ –ґ–µ–ї—Г–і–Ї–∞ –њ—А–Є –Ї—А–Њ–≤–Њ–њ–Њ—В–µ—А—П—Е. –Ґ—П–ґ–µ–ї–∞—П –Є –і–ї–Є—В–µ–ї—М–љ–∞—П –Є—И–µ–Љ–Є—П, –њ—А–Њ–і–Њ–ї–ґ–∞—О—Й–∞—П—Б—П –Њ–Ї–Њ–ї–Њ 30 –Љ–Є–љ, –Њ–њ—Г—Б—В–Њ—И–∞–µ—В —Б–Њ—Б—Г–і—Л –≥–∞—Б—В—А–Њ–і—Г–Њ–і–µ–љ–∞–ї—М–љ–Њ–є —Б–ї–Є–Ј–Є—Б—В–Њ–є, –≤—Л–Ј—Л–≤–∞–µ—В –љ–µ–Ї—А–Њ–Ј—Л –Є –і–µ—Б–Ї–≤–∞–Љ–∞—Ж–Є—О —Н–њ–Є—В–µ–ї–Є–∞–ї—М–љ—Л—Е –Ї–ї–µ—В–Њ–Ї, –≤—Л—Б—В–Є–ї–∞—О—Й–Є—Е –њ—А–Њ—Б–≤–µ—В –ґ–µ–ї—Г–і–Ї–∞ –Є –і–≤–µ–љ–∞–і—Ж–∞—В–Є–њ–µ—А—Б—В–љ–Њ–є –Ї–Є—И–Ї–Є.
–¶–Є—В–Њ–њ—А–Њ—В–µ–Ї—Ж–Є—П
–Т —Г–Ј–Ї–Њ–Љ —Б–Љ—Л—Б–ї–µ —Н—В–Њ—В —В–µ—А–Љ–Є–љ –±—Л–ї –њ—А–µ–і–ї–Њ–ґ–µ–љ
A. Robert –≤ 1979 –≥. –њ—А–Є –Њ—В–Ї—А—Л—В–Є–Є –Є –Є–Ј—Г—З–µ–љ–Є–Є —Б–њ–Њ—Б–Њ–±–љ–Њ—Б—В–Є –њ—А–Њ—Б—В–∞–≥–ї–∞–љ–і–Є–љ–Њ–≤ –њ—А–µ–і–Њ—В–≤—А–∞—Й–∞—В—М –Є–ї–Є —Б–Љ—П–≥—З–∞—В—М –њ–Њ–≤—А–µ–ґ–і–µ–љ–Є—П —Б–ї–Є–Ј–Є—Б—В–Њ–є –ґ–µ–ї—Г–і–Ї–∞, –≤—Л–Ј–≤–∞–љ–љ—Л–µ –љ–µ–Ї—А–Њ—В–Є–Ј–Є—А—Г—О—Й–Є–Љ–Є —Д–∞–Ї—В–Њ—А–∞–Љ–Є. –Т –њ–Њ—Б–ї–µ–і—Г—О—Й–µ–Љ —Ж–Є—В–Њ–њ—А–Њ—В–µ–Ї—Ж–Є–µ–є —Б—В–∞–ї–∞ –љ–∞–Ј—Л–≤–∞—В—М—Б—П —Б–њ–Њ—Б–Њ–±–љ–Њ—Б—В—М –Є –і—А—Г–≥–Є—Е —Н–љ–і–Њ–≥–µ–љ–љ—Л—Е –≤–µ—Й–µ—Б—В–≤ (–≥–ї—О—В–∞—В–Є–Њ–љ, –Њ–Ї–Є—Б—М –∞–Ј–Њ—В–∞ –Є –і—А.) –Є–ї–Є –ї–µ–Ї–∞—А—Б—В–≤–µ–љ–љ—Л—Е –њ—А–µ–њ–∞—А–∞—В–Њ–≤ (–Љ–Є–Ј–Њ–њ—А–Њ—Б—В–Њ–ї, —Б—Г–Ї—А–∞–ї—Д–∞—В, –∞–љ—В–∞—Ж–Є–і—Л, –њ—А–µ–њ–∞—А–∞—В—Л –≤–Є—Б–Љ—Г—В–∞ –Є –і—А.) –њ—А–µ–і–Њ—В–≤—А–∞—Й–∞—В—М –Є–ї–Є —Б–Љ—П–≥—З–∞—В—М –њ–Њ–≤—А–µ–ґ–і–µ–љ–Є—П –≥–∞—Б—В—А–Њ–Є–љ—В–µ—Б—В–Є–љ–∞–ї—М–љ–Њ–є —Б–ї–Є–Ј–Є—Б—В–Њ–є, –≤—Л–Ј–≤–∞–љ–љ—Л–µ —А–∞–Ј–ї–Є—З–љ—Л–Љ–Є –≤—А–µ–і–љ—Л–Љ–Є –Є–ї–Є —П–і–Њ–≤–Є—В—Л–Љ–Є —Е–Є–Љ–Є—З–µ—Б–Ї–Є–Љ–Є –≤–µ—Й–µ—Б—В–≤–∞–Љ–Є (—Н—В–∞–љ–Њ–ї, –Э–Я–Т–Я, –≥–Є–њ–Њ–Ї—Б–Є—П –Є –і—А.).
–Р—А–∞—Е–Є–і–Њ–љ–Њ–≤–∞—П –Ї–Є—Б–ї–Њ—В–∞, –Ї–Њ—В–Њ—А—Г—О —Б–Є–љ—В–µ–Ј–Є—А—Г—О—В —Н–њ–Є—В–µ–ї–Є–∞–ї—М–љ—Л–µ –Ї–ї–µ—В–Ї–Є –ґ–µ–ї—Г–і–Ї–∞, —П–≤–ї—П–µ—В—Б—П –Є—Б—Е–Њ–і–љ—Л–Љ —Б–Њ–µ–і–Є–љ–µ–љ–Є–µ–Љ –і–ї—П —Б–Є–љ—В–µ–Ј–∞ –њ—А–Њ—Б—В–∞–≥–ї–∞–љ–і–Є–љ–Њ–≤ —Б –њ–Њ–Љ–Њ—Й—М—О —Д–µ—А–Љ–µ–љ—В–∞ —Ж–Є–Ї–ї–Њ–Њ–Ї—Б–Є–і–∞–Ј—Л –Є —Б–Є–љ—В–µ–Ј–∞ –ї–µ–є–Ї–Њ—В—А–Є–µ–љ–∞ —Б –њ–Њ–Љ–Њ—Й—М—О –ї–Є–њ–Њ–Њ–Ї—Б–Є–і–∞–Ј—Л. –¶–Є—В–Њ–њ—А–Њ—В–µ–Ї—Ж–Є—П PGs –Њ–њ—А–µ–і–µ–ї—П–µ—В—Б—П –Є—Е —Б–њ–Њ—Б–Њ–±–љ–Њ—Б—В—М—О —Б—В–Є–Љ—Г–ї–Є—А–Њ–≤–∞—В—М –њ—А–Њ–і—Г–Ї—Ж–Є—О –Э–°–Ю3- –Є —Б–ї–Є–Ј–Є, —Г—Б–Є–ї–Є–≤–∞—В—М –Ї—А–Њ–≤–Њ—В–Њ–Ї –≤ —Б–ї–Є–Ј–Є—Б—В–Њ–є –Њ–±–Њ–ї–Њ—З–Ї–µ, –њ–Њ–і–∞–≤–ї—П—В—М –Њ–±—А–∞—В–љ—Г—О –і–Є—Д—Д—Г–Ј–Є—О –Є–Њ–љ–Њ–≤ –Э+ –Є–Ј –њ—А–Њ—Б–≤–µ—В–∞ –ґ–µ–ї—Г–і–Ї–∞ –≤ –Ї–ї–µ—В–Ї–Є —Н–њ–Є—В–µ–ї–Є—П –Є —Б—В–Є–Љ—Г–ї–Є—А–Њ–≤–∞—В—М —А–µ—Б—В–Є—В—Г—Ж–Є—О –њ–Њ–≤–µ—А—Е–љ–Њ—Б—В–љ–Њ–≥–Њ —Н–њ–Є—В–µ–ї–Є—П, –≤—Л–Ј–≤–∞–љ–љ—Г—О –њ–Њ–≤—А–µ–ґ–і–µ–љ–Є–µ–Љ. –Ъ—А–Њ–Љ–µ —В–Њ–≥–Њ, PGs –і–Њ–Ї–∞–Ј–∞–ї–Є —Б–њ–Њ—Б–Њ–±–љ–Њ—Б—В—М —Г—Б–Є–ї–Є–≤–∞—В—М –њ—А–Є—В–Њ–Ї —Б–µ—А–Њ–Ј–љ–Њ–є –ґ–Є–і–Ї–Њ—Б—В–Є –Ї —В–Ї–∞–љ—П–Љ —Б–ї–Є–Ј–Є—Б—В–Њ–є –Њ–±–Њ–ї–Њ—З–Ї–Є –ґ–µ–ї—Г–і–Ї–∞, –њ—А–Є –Є—Е –њ–Њ–≤—А–µ–ґ–і–µ–љ–Є—П—Е. –≠—В–Њ –њ—А–Є–≤–Њ–і–Є—В –Ї —Б–≤–Њ–µ–Њ–±—А–∞–Ј–љ–Њ–Љ—Г —А–∞—Б—В–≤–Њ—А–µ–љ–Є—О –Є–ї–Є —А–∞–Ј–≤–µ–і–µ–љ–Є—О –Ї–Њ–љ—Ж–µ–љ—В—А–∞—Ж–Є–Є —В–Њ–Ї—Б–Є—З–µ—Б–Ї–Є—Е –≤–µ—Й–µ—Б—В–≤ –≤ —В–Ї–∞–љ—П—Е —Б—В–µ–љ–Ї–Є –ґ–µ–ї—Г–і–Ї–∞ –Є —П–≤–ї—П–µ—В—Б—П –µ—Й–µ –Њ–і–љ–Є–Љ –Љ–µ—Е–∞–љ–Є–Ј–Љ–Њ–Љ –Ј–∞—Й–Є—В—Л —Б–ї–Є–Ј–Є—Б—В–Њ–є —Б –њ–Њ–Љ–Њ—Й—М—О —В–∞–Ї –љ–∞–Ј—Л–≤–∞–µ–Љ–Њ–є “–≥–Є—Б—В–Њ–і–Є–ї—О—Ж–Є–Є”.
–Ч–∞–Ї–ї—О—З–µ–љ–Є–µ
–Т –Ј–∞–Ї–ї—О—З–µ–љ–Є–µ –љ–µ–Њ–±—Е–Њ–і–Є–Љ–Њ –Њ—Б—В–∞–љ–Њ–≤–Є—В—М—Б—П –љ–∞ –≤–Њ–њ—А–Њ—Б–µ —Н—В–Є–Њ–ї–Њ–≥–Є–Є —П–Ј–≤–µ–љ–љ–Њ–є –±–Њ–ї–µ–Ј–љ–Є. –Ч–∞ –≤—А–µ–Љ—П –Є–Ј—Г—З–µ–љ–Є—П —Н—В–Њ–≥–Њ –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П –±—Л–ї–Њ –њ—А–µ–і–ї–Њ–ґ–µ–љ–Њ –Љ–љ–Њ–≥–Њ —А–∞–Ј–ї–Є—З–љ—Л—Е —В–µ–Њ—А–Є–є —П–Ј–≤–Њ–Њ–±—А–∞–Ј–Њ–≤–∞–љ–Є—П, –≤ —В–Њ–Љ —З–Є—Б–ї–µ –љ–∞–Є–±–Њ–ї—М—И—Г—О –њ–Њ–њ—Г–ї—П—А–љ–Њ—Б—В—М –Є–Љ–µ–ї–Є –њ—А–µ–і—Б—В–∞–≤–ї–µ–љ–Є—П –Њ —В–Њ–Љ, —З—В–Њ –Њ—Б–љ–Њ–≤–љ—Г—О —А–Њ–ї—М –≤ –≤–Њ–Ј–љ–Є–Ї–љ–Њ–≤–µ–љ–Є–Є –≥–∞—В—А–Њ–і—Г–Њ–і–µ–љ–∞–ї—М–љ—Л—Е —П–Ј–≤ –Є–≥—А–∞—О—В –њ—Б–Є—Е–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є–µ —Д–∞–Ї—В–Њ—А—Л –Є–ї–Є —А–∞–Ј–ї–Є—З–љ—Л–µ –і–Є–µ—В–Є—З–µ—Б–Ї–Є–µ –њ—А–Є—Б—В—А–∞—Б—В–Є—П, –љ–∞–њ—А–Є–Љ–µ—А —З—А–µ–Ј–Љ–µ—А–љ–Њ–µ —Г–њ–Њ—В—А–µ–±–ї–µ–љ–Є–µ –Њ—Б—В—А–Њ–є –њ–Є—Й–Є. –Ґ–µ–Љ –љ–µ –Љ–µ–љ–µ–µ –љ–Є –Њ–і–љ–∞ –Є–Ј —Н—В–Є—Е —В–µ–Њ—А–Є–є —В–∞–Ї –Є –љ–µ –њ–Њ–ї—Г—З–Є–ї–∞ –і–Њ—Б—В–∞—В–Њ—З–љ–Њ –і–Њ—Б—В–Њ–≤–µ—А–љ—Л—Е –љ–∞—Г—З–љ—Л—Е –і–Њ–Ї–∞–Ј–∞—В–µ–ї—М—Б—В–≤.
–Ъ –љ–∞—Б—В–Њ—П—Й–µ–Љ—Г –≤—А–µ–Љ–µ–љ–Є –і–Њ–Ї–∞–Ј–∞–љ—Л —В—А–Є –Њ—Б–љ–Њ–≤–љ—Л–µ –њ—А–Є—З–Є–љ—Л —П–Ј–≤–µ–љ–љ–Њ–є –±–Њ–ї–µ–Ј–љ–Є, –і–ї—П –Ї–∞–ґ–і–Њ–є –Є–Ј –Ї–Њ—В–Њ—А—Л—Е –Њ–њ—А–µ–і–µ–ї–µ–љ—Л –Є, –≤ —В–Њ–є –Є–ї–Є –Є–љ–Њ–є —Б—В–µ–њ–µ–љ–Є, –Є–Ј—Г—З–µ–љ—Л –њ–∞—В–Њ—Д–Є–Ј–Є–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є–µ –Љ–µ—Е–∞–љ–Є–Ј–Љ—Л –µ–µ —А–∞–Ј–≤–Є—В–Є—П: 1) –Љ–µ—Б—В–љ–∞—П –Є–љ—Д–µ–Ї—Ж–Є—П –±–∞–Ї—В–µ—А–Є—П–Љ–Є H. pylori; 2) –≥–Є–њ–µ—А—Б–µ–Ї—А–µ—В–Њ—А–љ—Л–є —Б–Є–љ–і—А–Њ–Љ, –љ–∞–њ—А–Є–Љ–µ—А, –њ—А–Є –≥–∞—Б—В—А–Є–љ–Њ–Љ–µ; 3) –њ—А–Є–µ–Љ –Э–Я–Т–Я.
–ѓ–Ј–≤–µ–љ–љ–∞—П –±–Њ–ї–µ–Ј–љ—М —А–∞–Ј–≤–Є–≤–∞–µ—В—Б—П –њ—А–Є —Н—В–Њ–Љ –і–∞–ї–µ–Ї–Њ –љ–µ —Г –≤—Б–µ—Е –ї–Є—Ж, –њ–Њ–і–≤–µ—А–≥–∞—О—Й–Є—Е—Б—П –≤–Њ–Ј–і–µ–є—Б—В–≤–Є—О —Н—В–Њ–≥–Њ —Н—В–Є–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Њ–≥–Њ —Д–∞–Ї—В–Њ—А–∞, –∞ —В–Њ–ї—М–Ї–Њ —Г —В–µ—Е –Є–Ј –љ–Є—Е, —Г –Ї–Њ—В–Њ—А—Л—Е –Ј–∞—Й–Є—В–љ—Л–µ –Љ–µ—Е–∞–љ–Є–Ј–Љ—Л, –≤ —Б–Є–ї—Г —В–µ—Е –Є–ї–Є –Є–љ—Л—Е –њ—А–Є—З–Є–љ (—В–∞–Ї –љ–∞–Ј—Л–≤–∞–µ–Љ—Л–µ –њ—А–µ–і—А–∞—Б–њ–Њ–ї–∞–≥–∞—О—Й–Є—Е —Д–∞–Ї—В–Њ—А–Њ–≤), –Њ–Ї–∞–Ј–∞–ї–Є—Б—М –љ–µ–і–Њ—Б—В–∞—В–Њ—З–љ—Л–Љ–Є –Є–ї–Є –њ–Њ–і–∞–≤–ї–µ–љ–љ—Л–Љ–Є. –Э–∞—А—Г—И–µ–љ–Є–µ —А–∞–≤–љ–Њ–≤–µ—Б–Є—П –Љ–µ–ґ–і—Г —Д–∞–Ї—В–Њ—А–∞–Љ–Є –∞–≥—А–µ—Б—Б–Є–Є –Є –Ј–∞—Й–Є—В—Л –≤—Л–Ј—Л–≤–∞–µ—В –Њ—Б—В—А–Њ–µ –њ–Њ–≤—А–µ–ґ–і–µ–љ–Є–µ, –Њ—Б—В—А–Њ–µ –Є–ї–Є —Е—А–Њ–љ–Є—З–µ—Б–Ї–Њ–µ –≤–Њ—Б–њ–∞–ї–µ–љ–Є–µ, —А–∞–Ј–≤–Є—В–Є–µ —Н—А–Њ–Ј–Є–Є (–њ–Њ–≤–µ—А—Е–љ–Њ—Б—В–љ–Њ–≥–Њ –њ–Њ–≤—А–µ–ґ–і–µ–љ–Є—П —Б–ї–Є–Ј–Є—Б—В–Њ–є) –Є/–Є–ї–Є –Њ–±—А–∞–Ј–Њ–≤–∞–љ–Є–µ —П–Ј–≤ (–≥–ї—Г–±–Њ–Ї–Њ–≥–Њ –њ–Њ–≤—А–µ–ґ–і–µ–љ–Є—П, –њ—А–Њ–љ–Є–Ї–∞—О—Й–µ–≥–Њ –і–Њ –Љ—Л—И–µ—З–љ–Њ–≥–Њ —Б–ї–Њ—П —Б–ї–Є–Ј–Є—Б—В–Њ–є).
–°–≤–Њ–µ–≤—А–µ–Љ–µ–љ–љ–∞—П –і–Є–∞–≥–љ–Њ—Б—В–Є–Ї–∞ –≤–µ–і—Г—Й–µ–≥–Њ –њ–∞—В–Њ–≥–µ–љ–µ—В–Є—З–µ—Б–Ї–Њ–≥–Њ —Д–∞–Ї—В–Њ—А–∞ —А–∞–Ј–≤–Є—В–Є—П —П–Ј–≤–µ–љ–љ–Њ–є –±–Њ–ї–µ–Ј–љ–Є –≤ –љ–∞—Б—В–Њ—П—Й–µ–µ –≤—А–µ–Љ—П –њ–Њ–Ј–≤–Њ–ї—П–µ—В –Њ—Б—Г—Й–µ—Б—В–≤–ї—П—В—М —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ–µ –ї–µ—З–µ–љ–Є–µ —Н—В–Њ–≥–Њ –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П. –≠—А–∞–і–Є–Ї–∞—Ж–Є—П (—Г–љ–Є—З—В–Њ–ґ–µ–љ–Є–µ) –Є–љ—Д–µ–Ї—Ж–Є–Є —Г –±–Њ–ї—М–љ—Л—Е H. pylori, –∞—Б—Б–Њ—Ж–Є–Є—А–Њ–≤–∞–љ–љ–Њ–є —П–Ј–≤–µ–љ–љ–Њ–є –±–Њ–ї–µ–Ј–љ—М—О —Б –њ–Њ–Љ–Њ—Й—М—О —Б–Њ–≤—А–µ–Љ–µ–љ–љ—Л—Е –Є–љ–≥–Є–±–Є—В–Њ—А–Њ–≤ –ґ–µ–ї—Г–і–Њ—З–љ–Њ–є —Б–µ–Ї—А–µ—Ж–Є–Є –≤ —Б–Њ—З–µ—В–∞–љ–Є–Є —Б –∞–љ—В–Є–±–Є–Њ—В–Є–Ї–∞–Љ–Є, —П–≤–ї—П–µ—В—Б—П –і–Њ–Ї–∞–Ј–∞–љ–љ—Л–Љ —Н—Д—Д–µ–Ї—В–Є–≤–љ—Л–Љ –њ–Њ–і—Е–Њ–і–Њ–Љ –Ї –ї–µ—З–µ–љ–Є—О –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П, —В–∞–Ї –Ї–∞–Ї –њ–Њ–Ј–≤–Њ–ї—П–µ—В –љ–µ —В–Њ–ї—М–Ї–Њ –і–Њ–±–Є—В—М—Б—П –±—Л—Б—В—А–Њ–≥–Њ –Ї—Г–њ–Є—А–Њ–≤–∞–љ–Є—П –±–Њ–ї–µ–≤–Њ–≥–Њ —Б–Є–љ–і—А–Њ–Љ–∞ –Є –Ј–∞–ґ–Є–≤–ї–µ–љ–Є—П —П–Ј–≤—Л, –љ–Њ –Є, —З—В–Њ –Њ—Б–Њ–±–µ–љ–љ–Њ –≤–∞–ґ–љ–Њ, –Њ—Б—В–∞–љ–∞–≤–ї–Є–≤–∞–µ—В –њ—А–Њ—Ж–µ—Б—Б —А–µ—Ж–Є–і–Є–≤–Є—А–Њ–≤–∞–љ–Є—П, –∞ —Б–ї–µ–і–Њ–≤–∞—В–µ–ї—М–љ–Њ, —Б–љ–Є–ґ–∞–µ—В —А–Є—Б–Ї —А–∞–Ј–≤–Є—В–Є—П –Њ—Б–ї–Њ–ґ–љ–µ–љ–Є–є. –Я—А–Є —Н—В–Њ–Љ –∞–љ—В–Є—Б–µ–Ї—А–µ—В–Њ—А–љ—Л–µ –њ—А–µ–њ–∞—А–∞—В—Л –њ—А–Њ–і–Њ–ї–ґ–∞—О—В –Є–≥—А–∞—В—М –≥–ї–∞–≤–µ–љ—Б—В–≤—Г—О—Й—Г—О —А–Њ–ї—М –≤ –ї–µ—З–µ–љ–Є–Є –±–Њ–ї—М–љ—Л—Е —П–Ј–≤–µ–љ–љ–Њ–є –±–Њ–ї–µ–Ј–љ—М—О –Є –Њ–±—П–Ј–∞—В–µ–ї—М–љ–Њ –і–Њ–ї–ґ–љ—Л –≤–Ї–ї—О—З–∞—В—Б—П –≤ —Б–Њ–≤—А–µ–Љ–µ–љ–љ—Л–µ —Б—Е–µ–Љ—Л —Н—А–∞–і–Є–Ї–∞—Ж–Є–Є, –≥–і–µ –Њ–љ–Є –≤—Л–њ–Њ–ї–љ—П—О—В –Љ–љ–Њ–≥–Њ–Њ–±—А–∞–Ј–љ—Л–µ —Д—Г–љ–Ї—Ж–Є–Є. –С–Њ–ї–µ–µ —В–Њ–≥–Њ, —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В—М –∞–љ—В–Є–≥–µ–ї–Є–Ї–Њ–±–∞–Ї—В–µ—А–љ–Њ–є —В–µ—А–∞–њ–Є–Є –љ–∞–њ—А—П–Љ—Г—О —Б–≤—П–Ј–∞–љ–∞ —Б —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В—М—О –Є –Љ–Њ—Й–љ–Њ—Б—В—М—О –њ—А–Є–Љ–µ–љ—П–µ–Љ–Њ–≥–Њ –≤ —Б—Е–µ–Љ–∞—Е —Н—А–∞–і–Є–Ї–∞—Ж–Є–Є –∞–љ—В–Є—Б–µ–Ї—А–µ—В–Њ—А–љ–Њ–≥–Њ –њ—А–µ–њ–∞—А–∞—В–∞. –Я–Њ—Н—В–Њ–Љ—Г –≤ –љ–∞—Б—В–Њ—П—Й–µ–µ –≤—А–µ–Љ—П —А–µ–Ї–Њ–Љ–µ–љ–і—Г–µ—В—Б—П –≤ –Ї–∞—З–µ—Б—В–≤–µ –њ—А–µ–њ–∞—А–∞—В–Њ–≤ –≤—Л–±–Њ—А–∞ –≤–Ї–ї—О—З–∞—В—М –≤ –∞–љ—В–Є–≥–µ–ї–Є–Ї–Њ–±–∞–Ї—В–µ—А–љ—Г—О —В–µ—А–∞–њ–Є—О –±–ї–Њ–Ї–∞—В–Њ—А—Л –њ—А–Њ—В–Њ–љ–љ–Њ–≥–Њ –љ–∞—Б–Њ—Б–∞.
–Т—Л–і–∞—О—Й–Є–Љ—Б—П –і–Њ—Б—В–Є–ґ–µ–љ–Є–µ–Љ –≤ —Б–Њ–Ј–і–∞–љ–Є–Є –ї–µ–Ї–∞—А—Б—В–≤–µ–љ–љ—Л—Е —Б—А–µ–і—Б—В–≤, –њ–Њ–љ–Є–ґ–∞—О—Й–Є—Е —Б–µ–Ї—А–µ—Ж–Є—О –ґ–µ–ї–µ–Ј –ґ–µ–ї—Г–і–Ї–∞, —Б–ї–µ–і—Г–µ—В –њ—А–Є–Ј–љ–∞—В—М —Б–Є–љ—В–µ–Ј –њ—А–Њ–Є–Ј–≤–Њ–і–љ–Њ–≥–Њ –Ј–∞–Љ–µ—Й–µ–љ–љ–Њ–≥–Њ –±–µ–љ–Ј–Є–Љ–Є–і–∞–Ј–Њ–ї–∞ - –Њ–Љ–µ–њ—А–∞–Ј–Њ–ї–∞ (–Ы–Њ—Б–µ–Ї), —Б –Ї–Њ—В–Њ—А–Њ–≥–Њ –љ–∞—З–∞–ї–Њ—Б—М –Є–Ј—Г—З–µ–љ–Є–µ –Є –њ—А–Є–Љ–µ–љ–µ–љ–Є–µ –њ—А–Є–љ—Ж–Є–њ–Є–∞–ї—М–љ–Њ –љ–Њ–≤–Њ–≥–Њ —В–Є–њ–∞ –њ—А–µ–њ–∞—А–∞—В–Њ–≤, —Г–≥–љ–µ—В–∞—О—Й–Є—Е —Д—Г–љ–Ї—Ж–Є—О –њ—А–Њ—В–Њ–љ–љ–Њ–≥–Њ –љ–∞—Б–Њ—Б–∞, –Ї–Њ—В–Њ—А—Л–Љ —П–≤–ї—П–µ—В—Б—П —Д–µ—А–Љ–µ–љ—В - –Э+ –Ъ+-–Р–Ґ–§–∞–Ј–∞ –Љ–µ–Љ–±—А–∞–љ—Л –њ–∞—А–Є–µ—В–∞–ї—М–љ—Л—Е –Ї–ї–µ—В–Њ–Ї –ґ–µ–ї—Г–і–Ї–∞. –Э–µ—Б–Љ–Њ—В—А—П –љ–∞ —А–∞–Ј—А–∞–±–Њ—В–Ї—Г –Є –њ–Њ—П–≤–ї–µ–љ–Є–µ –љ–Њ–≤—Л—Е –њ—А–µ–њ–∞—А–∞—В–Њ–≤ —Н—В–Њ–є –≥—А—Г–њ–њ—Л (–ї–∞–љ—Б–Њ–њ—А–∞–Ј–Њ–ї–∞, –њ–∞–љ—В–Њ–њ—А–∞–Ј–Њ–ї–∞, —А–∞–±–µ–њ—А–∞–Ј–Њ–ї–∞), –Њ–Љ–µ–њ—А–∞–Ј–Њ–ї –Њ—Б—В–∞–µ—В—Б—П –љ–∞ —Б–µ–≥–Њ–і–љ—П—И–љ–Є–є –і–µ–љ—М «–Ј–Њ–ї–Њ—В—Л–Љ —Б—В–∞–љ–і–∞—А—В–Њ–Љ», —Б –Ї–Њ—В–Њ—А—Л–Љ —Б—А–∞–≤–љ–Є–≤–∞—О—В —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В—М –і—А—Г–≥–Є—Е –∞–љ—В–Є—Б–µ–Ї—А–µ—В–Њ—А–љ—Л—Е —Б—А–µ–і—Б—В–≤. –Т —А–µ–Ј—Г–ї—М—В–∞—В–µ –њ—А–Њ–≤–µ–і–µ–љ–Є—П –Љ–љ–Њ–≥–Њ—З–Є—Б–ї–µ–љ–љ—Л—Е —А–∞–љ–і–Њ–Љ–Є–Ј–Є—А–Њ–≤–∞–љ–љ—Л—Е –Љ—Г–ї—М—В–Є—Ж–µ–љ—В—А–Њ–≤—Л—Е –і–≤–Њ–є–љ—Л—Е —Б–ї–µ–њ—Л—Е –њ–ї–∞—Ж–µ–±–Њ –Ї–Њ–љ—В—А–Њ–ї–Є—А—Г–µ–Љ—Л—Е –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є—Е –Є—Б–њ—Л—В–∞–љ–Є–є –±—Л–ї–Њ –і–Њ–Ї–∞–Ј–∞–љ–Њ, —З—В–Њ –Њ–Љ–µ–њ—А–∞–Ј–Њ–ї –њ—А–µ–≤–Њ—Б—Е–Њ–і–Є—В –±–ї–Њ–Ї–∞—В–Њ—А—Л –Э2-—А–µ—Ж–µ–њ—В–Њ—А–Њ–≤ –≥–Є—Б—В–∞–Љ–Є–љ–∞ –≤ –Њ—В–љ–Њ—И–µ–љ–Є–Є —Б–Ї–Њ—А–Њ—Б—В–Є –Ї—Г–њ–Є—А–Њ–≤–∞–љ–Є—П –±–Њ–ї–µ–≤–Њ–≥–Њ —Б–Є–љ–і—А–Њ–Љ–∞, –Ј–∞–ґ–Є–≤–ї–µ–љ–Є—П —П–Ј–≤ –ґ–µ–ї—Г–і–Ї–∞ –Є –і–≤–µ–љ–∞–і—Ж–∞—В–Є–њ–µ—А—Б—В–љ–Њ–є –Ї–Є—И–Ї–Є, —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В–Є –∞–љ—В–Є–≥–µ–ї–Є–Ї–Њ–±–∞–Ї—В–µ—А–љ–Њ–≥–Њ –ї–µ—З–µ–љ–Є—П –≤ –Ї–Њ–Љ–±–Є–љ–∞—Ж–Є–Є —Б –∞–љ—В–Є–±–Є–Њ—В–Є–Ї–∞–Љ–Є. –Я—А–Є –ї–µ—З–µ–љ–Є–Є –Э. —Аylori - –љ–µ–∞—Б—Б–Њ—Ж–Є–Є—А–Њ–≤–∞–љ–љ–Њ–є —П–Ј–≤–µ–љ–љ–Њ–є –±–Њ–ї–µ–Ј–љ–Є —Б –≤—Л—А–∞–ґ–µ–љ–љ—Л–Љ –≥–Є–њ–µ—А—Б–µ–Ї—А–µ—В–Њ—А–љ—Л–Љ —Б–Є–љ–і—А–Њ–Љ–Њ–Љ –Є –Э–Я–Т–Я-–∞—Б—Б–Њ—Ж–Є–Є—А–Њ–≤–∞–љ–љ—Л—Е –≥–∞—Б—В—А–Њ–і—Г–Њ–і–µ–љ–∞–ї—М–љ—Л—Е —П–Ј–≤ –Њ–Љ–µ–њ—А–∞–Ј–Њ–ї (–Ы–Њ—Б–µ–Ї) –≤ –Ї–∞—З–µ—Б—В–≤–µ –Љ–Њ–љ–Њ—В–µ—А–∞–њ–Є–Є –Њ—Б—В–∞–µ—В—Б—П –≤–µ–і—Г—Й–Є–Љ, –љ–∞–Є–±–Њ–ї–µ–µ —Н—Д—Д–µ–Ї—В–Є–≤–љ—Л–Љ –ї–µ–Ї–∞—А—Б—В–≤–µ–љ–љ—Л–Љ –њ—А–µ–њ–∞—А–∞—В–Њ–Љ.
–Ы–Є—В–µ—А–∞—В—Г—А–∞
1. Allen A., Newton J., Oliver L. et al. Mucus and H. Pylori. Y Physiol & Pharmacol 1997; 48: 297–305.
2. Davenport H., Warner H., Code C. Functional significance of gastric mucosal barrier to sodium. Gastroenterology 1964; 47: 142–52.
3. Denker B., Nigam S. Molecular structure and assembly of the tight function. Am J. Physiol Jan 1998; 274 (1 Pt. 2): F1–9.
4. Flemstrom G. Gastric and dodenal mucosal bicarbonate secretion. In: Phisiology of the gastrointestinal tract. 2nd ed. ., edited by L.R. Johnson and J.H. Walsh. New York, Raven 1987; p. 1011–29.
5. Laboisse C., Jarry A., Branka J. et al. Recent aspects of the regulacion of intestinal mucus secretion. Proc Nutr Soc 1996; 55: 259–64.
6. Modlin I., Hunt, Poulsom R. Trefoil peptides: mitogens, motogens or mirages? J. Clin Gastroenterol 1997; 25 (Suppl. 1): S94–100.
7. Wallace J., Granger D. The cellular and molecular basis of gastric mucosal defense. FASEB J 1996; 10: 731–40.
–Ю–Љ–µ–њ—А–∞–Ј–Њ–ї –
–Ы–Њ—Б–µ–Ї (—В–Њ—А–≥–Њ–≤–Њ–µ –љ–∞–Ј–≤–∞–љ–Є–µ)
(AstraZeneca)












