–§–Є–Ј–Є–Њ–ї–Њ–≥–Є—П –ґ–µ–ї—З–µ–≤—Л–≤–Њ–і—П—Й–Є—Е –њ—Г—В–µ–є
–Ц–µ–ї—З–љ—Л–є –њ—Г–Ј—Л—А—М, –Ї–Њ—В–Њ—А—Л–є —Б–Њ–µ–і–Є–љ—П–µ—В—Б—П —Б –њ–Њ–Љ–Њ—Й—М—О –њ—Г–Ј—Л—А–љ–Њ–≥–Њ –њ—А–Њ—В–Њ–Ї–∞ —Б –Њ–±—Й–Є–Љ –ґ–µ–ї—З–љ—Л–Љ –њ—А–Њ—В–Њ–Ї–Њ–Љ, —А–∞–±–Њ—В–∞–µ—В, –Ї–∞–Ї —Б–Њ–Ї—А–∞—В–Є—В–µ–ї—М–љ—Л–є —А–µ–Ј–µ—А–≤—Г–∞—А, —А–µ–≥—Г–ї–Є—А—Г—О—Й–Є–є –њ—А–Њ—Е–Њ–ґ–і–µ–љ–Є–µ –њ–µ—З–µ–љ–Њ—З–љ–Њ–є –ґ–µ–ї—З–Є —З–µ—А–µ–Ј —Б—Д–Є–љ–Ї—В–µ—А –Ю–і–і–Є –≤ –і–≤–µ–љ–∞–і—Ж–∞—В–Є–њ–µ—А—Б—В–љ—Г—О –Ї–Є—И–Ї—Г. –Ґ–∞–Ї–Є–Љ –Њ–±—А–∞–Ј–Њ–Љ, –њ–Њ–њ–∞–і–∞–љ–Є–µ –ґ–µ–ї—З–Є –≤ –і–≤–µ–љ–∞–і—Ж–∞—В–Є–њ–µ—А—Б—В–љ—Г—О –Ї–Є—И–Ї—Г –Ј–∞–≤–Є—Б–Є—В –Њ—В —А–∞–±–Њ—В—Л –і–≤—Г—Е –≥–ї–∞–і–Ї–Њ–Љ—Л—И–µ—З–љ—Л—Е —Б—В—А—Г–Ї—В—Г—А: –ґ–µ–ї—З–љ–Њ–≥–Њ –њ—Г–Ј—Л—А—П –Є —Б—Д–Є–љ–Ї—В–µ—А–∞ –Ю–і–і–Є. –Ц–µ–ї—З–љ—Л–є –њ—Г–Ј—Л—А—М –≤—Л–њ–Њ–ї–љ—П–µ—В —В—А–Є —А–∞–Ј–ї–Є—З–љ—Л–µ —Д—Г–љ–Ї—Ж–Є–Є: –љ–∞–Ї–Њ–њ–ї–µ–љ–Є–µ –ґ–µ–ї—З–Є –≤ –Љ–µ–ґ–њ–Є—Й–µ–≤–∞—А–Є—В–µ–ї—М–љ—Л–є –њ–µ—А–Є–Њ–і, –∞–±—Б–Њ—А–±—Ж–Є—П –≤–Њ–і—Л –Є —Н–ї–µ–Ї—В—А–Њ–ї–Є—В–Њ–≤, –∞ —В–∞–Ї–ґ–µ —Б–Њ–Ї—А–∞—Й–µ–љ–Є–µ, —Б –њ–Њ–Љ–Њ—Й—М—О –Ї–Њ—В–Њ—А–Њ–≥–Њ –ґ–µ–ї—З—М –њ–Њ—А—Ж–Є—П–Љ–Є –њ–Њ–і–∞–µ—В—Б—П –≤ –і–≤–µ–љ–∞–і—Ж–∞—В–Є–њ–µ—А—Б—В–љ—Г—О –Ї–Є—И–Ї—Г.
–Э–∞–Ї–Њ–њ–Є—В–µ–ї—М–љ–∞—П —Д—Г–љ–Ї—Ж–Є—П –ґ–µ–ї—З–љ–Њ–≥–Њ –њ—Г–Ј—Л—А—П. –Я–µ—З–µ–љ—М —З–µ–ї–Њ–≤–µ–Ї–∞ –≤—Л—А–∞–±–∞—В—Л–≤–∞–µ—В –Њ–Ї–Њ–ї–Њ 1000 –Љ–ї –ґ–µ–ї—З–Є –µ–ґ–µ–і–љ–µ–≤–љ–Њ. –С–Њ–ї–µ–µ –њ–Њ–ї–Њ–≤–Є–љ—Л –µ–µ (–Њ—В 50 –і–Њ 90%) –њ–Њ–њ–∞–і–∞–µ—В –≤ –ґ–µ–ї—З–љ—Л–є –њ—Г–Ј—Л—А—М –≤ –Ї–Њ–љ—Ж–µ–љ—В—А–Є—А–Њ–≤–∞–љ–љ–Њ–Љ –≤–Є–і–µ. –Э–∞–Ї–Њ–њ–Є—В–µ–ї—М–љ–∞—П —Б–њ–Њ—Б–Њ–±–љ–Њ—Б—В—М –ґ–µ–ї—З–љ–Њ–≥–Њ –њ—Г–Ј—Л—А—П –Ј–∞–≤–Є—Б–Є—В –Њ—В —В–Њ–љ—Г—Б–∞ —Б—Д–Є–љ–Ї—В–µ—А–∞ –Ю–і–і–Є –Є —А–∞–Ј–љ–Њ—Б—В–Є –і–∞–≤–ї–µ–љ–Є—П –Љ–µ–ґ–і—Г –ґ–µ–ї—З–љ—Л–Љ –њ—А–Њ—В–Њ–Ї–Њ–Љ –Є –њ—А–Њ—Б–≤–µ—В–Њ–Љ –ґ–µ–ї—З–љ–Њ–≥–Њ –њ—Г–Ј—Л—А—П. –Ю–љ–∞ —Б–Њ—Б—В–∞–≤–ї—П–µ—В –Њ—В 25 –і–Њ 50 –Љ–ї.
–Т—Б–∞—Б—Л–≤–∞–љ–Є–µ –≤ –ґ–µ–ї—З–љ–Њ–Љ –њ—Г–Ј—Л—А–µ. –Ц–µ–ї—З–љ—Л–є –њ—Г–Ј—Л—А—М —Б–њ–Њ—Б–Њ–±–µ–љ –∞–±—Б–Њ—А–±–Є—А–Њ–≤–∞—В—М –Њ—В 10% –і–Њ 30% —Б–≤–Њ–µ–≥–Њ —Б–Њ–і–µ—А–ґ–Є–Љ–Њ–≥–Њ –≤ —А–µ–Ј—Г–ї—М—В–∞—В–µ –∞–Ї—В–Є–≤–љ–Њ–≥–Њ –≤—Б–∞—Б—Л–≤–∞–љ–Є—П NaCl –Є N–∞–Э–°–Ю3 –≤–Љ–µ—Б—В–µ —Б –≤–Њ–і–Њ–є. –≠—В–Њ –њ—А–Є–≤–Њ–і–Є—В –Ї 50––Ї—А–∞—В–љ–Њ–Љ—Г —Г–≤–µ–ї–Є—З–µ–љ–Є—О –Ї–Њ–љ—Ж–µ–љ—В—А–∞—Ж–Є–Є –Њ—Б—В–∞–≤—И–Є—Е—Б—П –Њ—А–≥–∞–љ–Є—З–µ—Б–Ї–Є—Е –Ї–Њ–Љ–њ–Њ–љ–µ–љ—В–Њ–≤ (—Б–Њ–ї–µ–є –ґ–µ–ї—З–љ—Л—Е –Ї–Є—Б–ї–Њ—В, –ї–Є–њ–Њ–њ—А–Њ—В–µ–Є–і–љ–Њ–≥–Њ –Ї–Њ–Љ–њ–ї–µ–Ї—Б–∞, –њ–Є–≥–Љ–µ–љ—В–Њ–≤).
–°–Њ–Ї—А–∞—Й–µ–љ–Є–µ –ґ–µ–ї—З–љ–Њ–≥–Њ –њ—Г–Ј—Л—А—П. –Т–љ–µ –њ—А–Є–µ–Љ–∞ –њ–Є—Й–Є –ґ–µ–ї—З–љ—Л–є –њ—Г–Ј—Л—А—М —Б–њ–Њ–љ—В–∞–љ–љ–Њ –≤—Л–і–µ–ї—П–µ—В –Њ–Ї–Њ–ї–Њ 1/4 —Б–≤–Њ–µ–≥–Њ —Б–Њ–і–µ—А–ґ–Є–Љ–Њ–≥–Њ —Б –Є–љ—В–µ—А–≤–∞–ї–Њ–Љ –њ—А–Є–Љ–µ—А–љ–Њ –≤ 120 –Љ–Є–љ—Г—В, —Б–Є–љ—Е—А–Њ–љ–љ–Њ —Б –њ–Њ–Ј–і–љ–µ–є —З–∞—Б—В—М—О II —Д–∞–Ј—Л –Ї–Є—И–µ—З–љ–Њ–≥–Њ –Љ–Є–≥—А–Є—А—Г—О—Й–µ–≥–Њ –Љ–Њ—В–Њ—А–љ–Њ–≥–Њ –Ї–Њ–Љ–њ–ї–µ–Ї—Б–∞ (–Ь–Ь–Ъ) –Є –њ–Њ–≤—Л—И–µ–љ–Є–µ–Љ —Г—А–Њ–≤–љ—П –Љ–Њ—В–Є–ї–Є–љ–∞ –≤ –њ–ї–∞–Ј–Љ–µ. –≠—В–Њ –њ–µ—А–Є–Њ–і–Є—З–µ—Б–Ї–Њ–µ –њ–Њ—Б—В—Г–њ–ї–µ–љ–Є–µ –ґ–µ–ї—З–Є –≤ –і–≤–µ–љ–∞–і—Ж–∞—В–Є–њ–µ—А—Б—В–љ—Г—О –Ї–Є—И–Ї—Г —Б–Њ–≤–њ–∞–і–∞–µ—В —Б –њ—А–Њ–њ—Г–ї—М—Б–Є–≤–љ—Л–Љ–Є –і–≤–Є–ґ–µ–љ–Є—П–Љ–Є —В–Њ–љ–Ї–Њ–є –Ї–Є—И–Ї–Є. –Ґ–∞–Ї–Є–Љ –Њ–±—А–∞–Ј–Њ–Љ, —Н–љ—В–µ—А–Њ–≥–µ–њ–∞—В–Є—З–µ—Б–Ї–Є–є —Ж–Є–Ї–ї –њ—А–Њ–і–Њ–ї–ґ–∞–µ—В—Б—П –Є –≤–љ–µ –њ–Є—Й–µ–≤–∞—А–Є—В–µ–ї—М–љ–Њ–≥–Њ –њ–µ—А–Є–Њ–і–∞. –Т –љ–µ–Љ —Г—З–∞—Б—В–≤—Г–µ—В –Ї–∞–Ї –њ–µ—З–µ–љ–Њ—З–љ–∞—П –ґ–µ–ї—З—М, –Ї–Њ—В–Њ—А–∞—П, –Љ–Є–љ—Г—П –ґ–µ–ї—З–љ—Л–є –њ—Г–Ј—Л—А—М, –њ–Њ–њ–∞–і–∞–µ—В –≤ –і–≤–µ–љ–∞–і—Ж–∞—В–Є–њ–µ—А—Б—В–љ—Г—О –Ї–Є—И–Ї—Г, —В–∞–Ї –Є –ґ–µ–ї—З—М, –њ–Њ—Б—В—Г–њ–∞—О—Й–∞—П –њ—А–Є –њ–µ—А–Є–Њ–і–Є—З–µ—Б–Ї–Њ–Љ –Њ–њ–Њ—А–Њ–ґ–љ–µ–љ–Є–Є –ґ–µ–ї—З–љ–Њ–≥–Њ –њ—Г–Ј—Л—А—П, —Б–Є–љ—Е—А–Њ–љ–Є–Ј–Є—А–Њ–≤–∞–љ–љ–Њ–≥–Њ —Б –њ—А–Њ—Е–Њ–ґ–і–µ–љ–Є–µ–Љ –Ь–Ь–Ъ –њ–Њ —В–Њ–љ–Ї–Њ–є –Ї–Є—И–Ї–µ. –Я—А–Є–µ–Љ –њ–Є—Й–Є –Є–љ–Є—Ж–Є–Є—А—Г–µ—В —Б–Њ–Ї—А–∞—Й–µ–љ–Є–µ –ґ–µ–ї—З–љ–Њ–≥–Њ –њ—Г–Ј—Л—А—П –њ–Њ—Б—А–µ–і—Б—В–≤–Њ–Љ –љ–µ—А–≤–љ—Л—Е (—Ж–µ–љ—В—А–∞–ї—М–љ—Л—Е «—Ж–µ—Д–∞–ї–Є—З–µ—Б–Ї–Є—Е» –Є –ї–Њ–Ї–∞–ї—М–љ—Л—Е –≥–∞—Б—В—А–Њ–і—Г–Њ–і–µ–љ–∞–ї—М–љ—Л—Е —А–µ—Д–ї–µ–Ї—Б–Њ–≤) –Є –≥—Г–Љ–Њ—А–∞–ї—М–љ—Л—Е –≤–ї–Є—П–љ–Є–є (–≥–ї–∞–≤–љ—Л–Љ –Њ–±—А–∞–Ј–Њ–Љ – —Е–Њ–ї–µ—Ж–Є—Б—В–Њ–Ї–Є–љ–Є–љ), –≤—Л–Ј—Л–≤–∞—П –њ–Њ–њ–∞–і–∞–љ–Є–µ –≤ –і–≤–µ–љ–∞–і—Ж–∞—В–Є–њ–µ—А—Б—В–љ—Г—О –Ї–Є—И–Ї—Г –±–Њ–ї–µ–µ 3/4 —Б–Њ–і–µ—А–ґ–Є–Љ–Њ–≥–Њ –ґ–µ–ї—З–љ–Њ–≥–Њ –њ—Г–Ј—Л—А—П. –Т —Ж–µ—Д–∞–ї–Є—З–µ—Б–Ї—Г—О —Д–∞–Ј—Г –≤—Л—Б–≤–Њ–±–Њ–ґ–і–∞–µ—В—Б—П –Њ–Ї–Њ–ї–Њ 25% –µ–≥–Њ —Б–Њ–і–µ—А–ґ–Є–Љ–Њ–≥–Њ. –Ь–µ–і–Є–∞—В–Њ—А–∞–Љ–Є —Н—В–Њ–≥–Њ –њ—А–Њ—Ж–µ—Б—Б–∞ —Б–ї—Г–ґ–∞—В —Е–Њ–ї–Є–љ–µ—А–≥–Є—З–µ—Б–Ї–Є–µ –≤–Њ–ї–Њ–Ї–љ–∞ –±–ї—Г–ґ–і–∞—О—Й–µ–≥–Њ –љ–µ—А–≤–∞. –°—В–µ–њ–µ–љ—М –Њ–њ–Њ—А–Њ–ґ–љ–µ–љ–Є—П –ґ–µ–ї—З–љ–Њ–≥–Њ –њ—Г–Ј—Л—А—П –≤–Њ –≤—А–µ–Љ—П –µ–і—Л –Њ–њ—А–µ–і–µ–ї—П–µ—В—Б—П –≤ –Њ—Б–љ–Њ–≤–љ–Њ–Љ —Б–Њ—Б—В–∞–≤–Њ–Љ –њ–Є—Й–Є. –•–Њ–ї–µ—Ж–Є—Б—В–Њ–Ї–Є–љ–Є–љ (–•–¶–Ъ) —П–≤–ї—П–µ—В—Б—П –Њ—Б–љ–Њ–≤–љ—Л–Љ –≥–Њ—А–Љ–Њ–љ–Њ–Љ, –Њ—В–≤–µ—В—Б—В–≤–µ–љ–љ—Л–Љ –Ј–∞ –Њ–њ–Њ—А–Њ–ґ–љ–µ–љ–Є–µ –ґ–µ–ї—З–љ–Њ–≥–Њ –њ—Г–Ј—Л—А—П, –њ—А–Њ–Є—Б—Е–Њ–і—П—Й–µ–≥–Њ –њ–Њ—Б–ї–µ –њ—А–Є–µ–Љ–∞ –њ–Є—Й–Є. –Х–≥–Њ –Њ—Б–≤–Њ–±–Њ–ґ–і–µ–љ–Є–µ –Є–Ј —Б–ї–Є–Ј–Є—Б—В–Њ–є –≤–µ—А—Е–љ–µ–≥–Њ –Њ—В–і–µ–ї–∞ —В–Њ–љ–Ї–Њ–є –Ї–Є—И–Ї–Є —Б—В–Є–Љ—Г–ї–Є—А—Г–µ—В –њ–Њ—Б—В—Г–њ–ї–µ–љ–Є–µ —В—Г–і–∞ –∞–Љ–Є–љ–Њ–Ї–Є—Б–ї–Њ—В –Є –ґ–Є—А–љ—Л—Е –Ї–Є—Б–ї–Њ—В. –•–¶–Ъ –≤—Л–Ј—Л–≤–∞–µ—В —Б–Њ–Ї—А–∞—Й–µ–љ–Є–µ –ґ–µ–ї—З–љ–Њ–≥–Њ –њ—Г–Ј—Л—А—П –њ—Г—В–µ–Љ –њ—А—П–Љ–Њ–≥–Њ –≤–Њ–Ј–і–µ–є—Б—В–≤–Є—П –љ–∞ –≥–ї–∞–і–Ї–Є–µ –Љ—Л—И—Ж—Л, –Ї—А–Њ–Љ–µ —В–Њ–≥–Њ, —Б–Њ–Ї—А–∞—Й–µ–љ–Є–µ —З–∞—Б—В–Є—З–љ–Њ –Њ–±—Г—Б–ї–Њ–≤–ї–µ–љ–Њ —Е–Њ–ї–Є–љ–µ—А–≥–Є—З–µ—Б–Ї–Є–Љ–Є –≤–ї–Є—П–љ–Є—П–Љ–Є. –≠—В–Њ –Љ–Њ–ґ–µ—В –±—Л—В—М —Б–≤—П–Ј–∞–љ–Њ —Б –њ–Њ–≤—Л—И–µ–љ–Є–µ–Љ —В–Њ–љ—Г—Б–∞ –±–ї—Г–ґ–і–∞—О—Й–µ–≥–Њ –љ–µ—А–≤–∞ –Є –ї–Њ–Ї–∞–ї—М–љ—Л–Љ–Є —А–µ—Д–ї–µ–Ї—Б–∞–Љ–Є –Є–Ј –ґ–µ–ї—Г–і–Ї–∞ –Є —В–Њ–љ–Ї–Њ–є –Ї–Є—И–Ї–Є, –≤—Л–Ј–≤–∞–љ–љ—Л–Љ–Є –Є—Е —А–∞—Б—В—П–ґ–µ–љ–Є–µ–Љ –Є –≤–Њ–Ј–і–µ–є—Б—В–≤–Є–µ–Љ –Ї–Њ–Љ–њ–Њ–љ–µ–љ—В–Њ–≤ –њ–Є—Й–Є. –Ц–µ–ї—З–љ—Л–є –њ—Г–Ј—Л—А—М –Њ—Б—В–∞–µ—В—Б—П –≤ —Б–Њ–Ї—А–∞—Й–µ–љ–љ–Њ–Љ —Б–Њ—Б—В–Њ—П–љ–Є–Є –і–Њ —В–µ—Е –њ–Њ—А, –њ–Њ–Ї–∞ –њ—А–Њ–і–Њ–ї–ґ–∞–µ—В—Б—П –њ–Њ—Б—В—Г–њ–ї–µ–љ–Є–µ —Е–Є–Љ—Г—Б–∞ –Є–Ј –ґ–µ–ї—Г–і–Ї–∞ –≤ –і–≤–µ–љ–∞–і—Ж–∞—В–Є–њ–µ—А—Б—В–љ—Г—О –Ї–Є—И–Ї—Г. –Ч–∞–њ–Њ–ї–љ–µ–љ–Є–µ –ґ–µ–ї—З–љ–Њ–≥–Њ –њ—Г–Ј—Л—А—П –љ–∞—З–Є–љ–∞–µ—В—Б—П —З–µ—А–µ–Ј 1–2 —З–∞—Б–∞ –њ–Њ—Б–ї–µ –њ–µ—А–µ–≤–∞—А–Є–≤–∞–љ–Є—П –ґ–Є–і–Ї–Њ–є –њ–Є—Й–Є –Є —З–µ—А–µ–Ј 3–4 —З–∞—Б–∞ –њ–Њ—Б–ї–µ —Б–Љ–µ—И–∞–љ–љ–Њ–є –њ–Є—Й–Є.
–≠–љ—В–µ—А–Њ–≥–µ–њ–∞—В–Є—З–µ—Б–Ї–∞—П —Ж–Є—А–Ї—Г–ї—П—Ж–Є—П: —А–Њ–ї—М –ґ–µ–ї—З–љ–Њ–≥–Њ –њ—Г–Ј—Л—А—П. –Ґ—А–∞–љ–Ј–Є—В –ґ–µ–ї—З–љ—Л—Е —Б–Њ–ї–µ–є —З–µ—А–µ–Ј –њ–µ—З–µ–љ—М –Ј–∞–≤–Є—Б–Є—В –Њ—В –Є—Е –њ–Њ—Б—В—Г–њ–ї–µ–љ–Є—П –Є–Ј —В–Њ–љ–Ї–Њ–є –Ї–Є—И–Ї–Є. –≠–љ—В–µ—А–Њ–≥–µ–њ–∞—В–Є—З–µ—Б–Ї–∞—П —Ж–Є—А–Ї—Г–ї—П—Ж–Є—П –Њ—Б—Г—Й–µ—Б—В–≤–ї—П–µ—В—Б—П –Ј–∞ —Б—З–µ—В –і–≤—Г—Е –≤–Є–і–Њ–≤ –∞–Ї—В–Є–≤–љ–Њ–≥–Њ —В—А–∞–љ—Б–њ–Њ—А—В–∞ (–≤ –њ–µ—З–µ–љ–Є –Є –Ї–Њ–љ–µ—З–љ–Њ–Љ –Њ—В–і–µ–ї–µ –њ–Њ–і–≤–Ј–і–Њ—И–љ–Њ–є –Ї–Є—И–Ї–Є) –Є –і–≤—Г–Љ—П –Љ–µ—Е–∞–љ–Є—З–µ—Б–Ї–Є–Љ–Є –љ–∞—Б–Њ—Б–∞–Љ–Є (–ґ–µ–ї—З–љ—Л–є –њ—Г–Ј—Л—А—М –Є —В–Њ–љ–Ї–∞—П –Ї–Є—И–Ї–∞). –Ю–≥—А–∞–љ–Є—З–Є—В–µ–ї—П–Љ–Є —А–∞–±–Њ—В—Л —Н—В–Њ–є —Б–Є—Б—В–µ–Љ—Л —Б–ї—Г–ґ–∞—В: –і–µ–њ–Њ–љ–Є—А–Њ–≤–∞–љ–Є–µ –≤ –ґ–µ–ї—З–љ–Њ–Љ –њ—Г–Ј—Л—А–µ, –≥–і–µ –Њ—Б–∞–ґ–і–∞–µ—В—Б—П –±–Њ–ї—М—И–Є–љ—Б—В–≤–Њ –ґ–µ–ї—З–љ—Л—Е –Ї–Є—Б–ї–Њ—В –≤ –њ—А–Њ–Љ–µ–ґ—Г—В–Ї–Є –Љ–µ–ґ–і—Г –њ—А–Є–µ–Љ–∞–Љ–Є –њ–Є—Й–Є, –Є —В—А–∞–љ–Ј–Є—В –њ–Њ —В–Њ–љ–Ї–Њ–є –Ї–Є—И–Ї–µ.
–Ц–µ–ї—З–љ—Л–є –њ—Г–Ј—Л—А—М, —В–∞–Ї–Є–Љ –Њ–±—А–∞–Ј–Њ–Љ, —П–≤–ї—П–µ—В—Б—П –≤–∞–ґ–љ—Л–Љ —Д–∞–Ї—В–Њ—А–Њ–Љ —Н–љ—В–µ—А–Њ–≥–µ–њ–∞—В–Є—З–µ—Б–Ї–Њ–є —Ж–Є—А–Ї—Г–ї—П—Ж–Є–Є –ґ–µ–ї—З–љ—Л—Е –Ї–Є—Б–ї–Њ—В. –Т–љ–µ –њ—А–Є–µ–Љ–∞ –њ–Є—Й–Є –Ь–Ь–Ъ –Љ–Њ–ґ–µ—В –і–µ–є—Б—В–≤–Њ–≤–∞—В—М –Ї–∞–Ї «–Љ—Г—Б–Њ—А—Й–Є–Ї», —Г–і–∞–ї—П—П –Њ—Б—В–∞—В–Ї–Є –ґ–µ–ї—З–Є –Є–Ј –ґ–µ–ї—З–љ–Њ–≥–Њ –њ—Г–Ј—Л—А—П, —Б—В–Є–Љ—Г–ї–Є—А—Г—П —Н–љ—В–µ—А–Њ–≥–µ–њ–∞—В–Є—З–µ—Б–Ї—Г—О —Ж–Є—А–Ї—Г–ї—П—Ж–Є—О –Є –њ–Њ–і–і–µ—А–ґ–Є–≤–∞—П –ґ–µ–ї—З–µ–Њ–±—А–∞–Ј–Њ–≤–∞–љ–Є–µ –≤ –њ–µ—З–µ–љ–Є. –Т–Њ –≤—А–µ–Љ—П –µ–і—Л —Н–≤–∞–Ї—Г–∞—Ж–Є—П —Б–Њ–і–µ—А–ґ–Є–Љ–Њ–≥–Њ –ґ–µ–ї—З–љ–Њ–≥–Њ –њ—Г–Ј—Л—А—П –Є —Г—Б–Є–ї–µ–љ–љ—Л–µ —Б–Њ–Ї—А–∞—Й–µ–љ–Є—П –Ї–Є—И–Ї–Є —Г–≤–µ–ї–Є—З–Є–≤–∞—О—В —Ж–Є—А–Ї—Г–ї—П—Ж–Є—О –њ—Г–ї–∞ –ґ–µ–ї—З–љ—Л—Е –Ї–Є—Б–ї–Њ—В –Є –њ–Њ–≤—Л—И–∞—О—В –њ–µ—З–µ–љ–Њ—З–љ—Г—О —Б–µ–Ї—А–µ—Ж–Є—О.
–†–∞—Б—Б—В—А–Њ–є—Б—В–≤–∞ —Д—Г–љ–Ї—Ж–Є–Є
–ґ–µ–ї—З–љ–Њ–≥–Њ –њ—Г–Ј—Л—А—П
–Э–∞—А—Г—И–µ–љ–Є–µ –Љ–Њ—В–Њ—А–Є–Ї–Є, —Б–љ–Є–ґ–µ–љ–Є–µ —В–Њ–љ—Г—Б–∞ –Є–ї–Є –Љ–µ—Е–∞–љ–Є—З–µ—Б–Ї–∞—П –Њ–±—Б—В—А—Г–Ї—Ж–Є—П –ґ–µ–ї—З–љ–Њ–≥–Њ –њ—Г–Ј—Л—А—П —П–≤–ї—П—О—В—Б—П –Њ—Б–љ–Њ–≤–Њ–є –і–ї—П —Д–Њ—А–Љ–Є—А–Њ–≤–∞–љ–Є—П —Б–≥—Г—Б—В–Ї–Њ–≤ –ґ–µ–ї—З–Є. –≠—В–Њ –њ—А–Є–≤–Њ–і–Є—В –Ї —Б—Г–±–Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є–Љ –≤–Њ—Б–њ–∞–ї–Є—В–µ–ї—М–љ—Л–Љ –Є–Ј–Љ–µ–љ–µ–љ–Є—П–Љ, –Ї–Њ—В–Њ—А—Л–µ –≤—Л–Ј—Л–≤–∞—О—В –Є–Ј–±—Л—В–Њ—З–љ—Г—О –њ—А–Њ–і—Г–Ї—Ж–Є—О —Б–ї–Є–Ј–Є – –Љ–∞—В—А–Є—Ж—Л, –љ–∞ –Ї–Њ—В–Њ—А–Њ–є –Ї—А–Є—Б—В–∞–ї–ї—Л —Е–Њ–ї–µ—Б—В–µ—А–Є–љ–∞ –Њ–±—А–∞–Ј—Г—О—В —П–і—А–Њ. –Ъ—А–Њ–Љ–µ —В–Њ–≥–Њ, –≤–Њ—Б–њ–∞–ї–Є—В–µ–ї—М–љ—Л–є –њ—А–Њ—Ж–µ—Б—Б –Љ–Њ–ґ–µ—В –њ—А–Є–≤–µ—Б—В–Є –Ї –≤—Л—Б–≤–Њ–±–Њ–ґ–і–µ–љ–Є—О –≥–Є–і—А–Њ–ї–Є—В–Є—З–µ—Б–Ї–Є—Е —Д–µ—А–Љ–µ–љ—В–Њ–≤, –≤—Л–Ј—Л–≤–∞—О—Й–Є—Е –і–µ–Ї–Њ–љ—К—О–≥–∞—Ж–Є—О –±–Є–ї–Є—А—Г–±–Є–љ–∞. –Т —А–µ–Ј—Г–ї—М—В–∞—В–µ —Н—В–Њ–≥–Њ –Њ–±—А–∞–Ј—Г—О—В—Б—П –њ—А–µ—Ж–Є–њ–Є—В–∞—В—Л –±–Є–ї–Є—А—Г–±–Є–љ–∞—В–∞ –Ї–∞–ї—М—Ж–Є—П, —З—В–Њ, –≤ —Б–≤–Њ—О –Њ—З–µ—А–µ–і—М, —В–∞–Ї–ґ–µ –Љ–Њ–ґ–µ—В –њ—А–Є–≤–Њ–і–Є—В—М –Ї —А–∞—Б—Й–µ–њ–ї–µ–љ–Є—О –ґ–Є—А–љ—Л—Е –Ї–Є—Б–ї–Њ—В, –Њ–±—А–∞–Ј—Г—О—Й–Є—Е –Ї–∞–ї—М—Ж–Є–µ–≤—Л–µ —Б–Њ–ї–Є –љ–µ–љ–∞—Б—Л—Й–µ–љ–љ—Л—Е –Ї–Є—Б–ї–Њ—В (–њ–∞–ї—М–Љ–Є—В–∞—В—Л –Є —Б—В–µ–∞—А–∞—В—Л). –°—В–∞–Ј –љ–∞—А—Г—И–∞–µ—В –≤—Л–і–µ–ї–µ–љ–Є–µ –ґ–µ–ї—З–Є –Є–Ј –ґ–µ–ї—З–љ–Њ–≥–Њ –њ—Г–Ј—Л—А—П, —Б–њ–Њ—Б–Њ–±—Б—В–≤—Г–µ—В —Д–Њ—А–Љ–Є—А–Њ–≤–∞–љ–Є—О —Б–ї–∞–і–ґ–∞ –Є –Њ—Б–∞–ґ–і–µ–љ–Є—О —В–≤–µ—А–і—Л—Е –≤–µ—Й–µ—Б—В–≤.
–•–Њ–ї–Є–љ–µ—А–≥–Є—З–µ—Б–Ї–∞—П –Є–љ–љ–µ—А–≤–∞—Ж–Є—П –ґ–µ–ї—З–љ–Њ–≥–Њ –њ—Г–Ј—Л—А—П –Є–≥—А–∞–µ—В —А–µ—И–∞—О—Й—Г—О —А–Њ–ї—М –≤ —Ж–µ—Д–∞–ї–Є—З–µ—Б–Ї—Г—О —Д–∞–Ј—Г –Њ–њ–Њ—А–Њ–ґ–љ–µ–љ–Є—П –Є –Њ–±–µ—Б–њ–µ—З–Є–≤–∞–µ—В –≤–ї–Є—П–љ–Є–µ –•–¶–Ъ –љ–∞ –ґ–µ–ї—З–љ—Л–є –њ—Г–Ј—Л—А—М. –Ш–Ј–≤–µ—Б—В–љ–Њ, —З—В–Њ —Г –±–Њ–ї—М–љ—Л—Е –њ–Њ—Б–ї–µ –≤–∞–≥–Њ—В–Њ–Љ–Є–Є –љ–∞–±–ї—О–і–∞–µ—В—Б—П –њ–Њ–≤—Л—И–µ–љ–Є–µ —З–∞—Б—В–Њ—В—Л —Д–Њ—А–Љ–Є—А–Њ–≤–∞–љ–Є—П –ґ–µ–ї—З–љ—Л—Е –Ї–∞–Љ–љ–µ–є –Є –Ј–∞—Б—В–Њ—П –ґ–µ–ї—З–Є –≤ –ґ–µ–ї—З–љ–Њ–Љ –њ—Г–Ј—Л—А–µ. –Я–Њ—А–∞–ґ–µ–љ–Є–µ –≥–ї–∞–і–Ї–Њ–є –Љ—Г—Б–Ї—Г–ї–∞—В—Г—А—Л –ґ–µ–ї—З–љ–Њ–≥–Њ –њ—Г–Ј—Л—А—П —Е–∞—А–∞–Ї—В–µ—А–љ–Њ –і–ї—П –ґ–µ–ї—З–љ–Њ–Ї–∞–Љ–µ–љ–љ–Њ–є –±–Њ–ї–µ–Ј–љ–Є –Є —А–∞–Ј–≤–Є–≤–∞–µ—В—Б—П —А–∞–љ–Њ, –µ—Й–µ –і–Њ –њ–Њ—П–≤–ї–µ–љ–Є—П –Љ–Є–Ї—А–Њ–Ї—А–Є—Б—В–∞–ї–ї–Њ–≤ –Є –Ї–∞–Љ–љ–µ–є. –£–≤–µ–ї–Є—З–µ–љ–Є–µ —А–∞–Ј–Љ–µ—А–Њ–≤ –ґ–µ–ї—З–љ–Њ–≥–Њ –њ—Г–Ј—Л—А—П —Г —В–∞–Ї–Є—Е –±–Њ–ї—М–љ—Л—Е –Љ–Њ–ґ–љ–Њ —Б—А–∞–≤–љ–Є—В—М —Б —А–∞—Б—И–Є—А–µ–љ–Є–µ–Љ —Б–µ—А–і—Ж–∞ –њ—А–Є —Б–µ—А–і–µ—З–љ–Њ–є –љ–µ–і–Њ—Б—В–∞—В–Њ—З–љ–Њ—Б—В–Є.
–Ч–љ–∞—З–µ–љ–Є–µ —Б—Д–Є–љ–Ї—В–µ—А–∞ –Ю–і–і–Є
–њ—А–Є –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П—Е –ґ–µ–ї—З–љ—Л—Е –њ—Г—В–µ–є
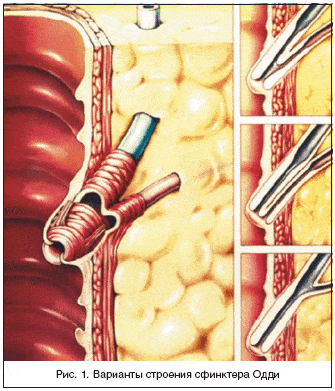
–°—Д–Є–љ–Ї—В–µ—А –Ю–і–і–Є (–°–Ю) – –Љ—Л—И–µ—З–љ–∞—П —Б—В—А—Г–Ї—В—Г—А–∞, —А–µ–≥—Г–ї–Є—А—Г—О—Й–∞—П –і–∞–≤–ї–µ–љ–Є–µ –≤ –і–Є—Б—В–∞–ї—М–љ–Њ–є —З–∞—Б—В–Є –ґ–µ–ї—З–љ–Њ–≥–Њ –Є –њ–∞–љ–Ї—А–µ–∞—В–Є—З–µ—Б–Ї–Њ–≥–Њ –њ—А–Њ—В–Њ–Ї–∞ –≤ –Љ–µ—Б—В–µ –Є—Е –≤—Л—Е–Њ–і–∞ –≤ –љ–Є—Б—Е–Њ–і—П—Й—Г—О —З–∞—Б—В—М –і–≤–µ–љ–∞–і—Ж–∞—В–Є–њ–µ—А—Б—В–љ–Њ–є –Ї–Є—И–Ї–Є. –Т –±–Њ–ї—М—И–Є–љ—Б—В–≤–µ —Б–ї—Г—З–∞–µ–≤ –°–Ю –Є–Љ–µ–µ—В Y––Њ–±—А–∞–Ј–љ—Г—О —Д–Њ—А–Љ—Г: –і–Є—Б—В–∞–ї—М–љ—Л–є –Ї–Њ–љ–µ—Ж –ґ–µ–ї—З–љ–Њ–≥–Њ –њ—А–Њ—В–Њ–Ї–∞ (sphincter choledochus) –Њ–±—А–∞–Ј—Г–µ—В –Њ–і–љ—Г –≤–µ—В–≤—М, –∞ –і–Є—Б—В–∞–ї—М–љ—Л–є —Б–µ–≥–Љ–µ–љ—В –њ–∞–љ–Ї—А–µ–∞—В–Є—З–µ—Б–Ї–Њ–≥–Њ –њ—А–Њ—В–Њ–Ї–∞ (sphincter pancreaticus) – –і—А—Г–≥—Г—О (—А–Є—Б. 1). –Ь–∞–љ–Њ–Љ–µ—В—А–Є—З–µ—Б–Ї–Є–µ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П [18] –њ–Њ–Ї–∞–Ј–∞–ї–Є, —З—В–Њ –°–Ю —Б–њ–Њ—Б–Њ–±–µ–љ –њ–Њ–і–і–µ—А–ґ–Є–≤–∞—В—М –њ–Њ—Б—В–Њ—П–љ–љ–Њ–µ –і–∞–≤–ї–µ–љ–Є–µ, –≤ —В.—З. –љ–µ–Ј–∞–≤–Є—Б–Є–Љ–Њ – –≤ —Б–≤–Њ–µ–Љ –њ–∞–љ–Ї—А–µ–∞—В–Є—З–µ—Б–Ї–Њ–Љ —Б–µ–≥–Љ–µ–љ—В–µ.
–°—Д–Є–љ–Ї—В–µ—А –Ю–і–і–Є –Њ—В–≤–µ—З–∞–µ—В –Ј–∞ –њ–Њ–і–і–µ—А–ґ–∞–љ–Є–µ –≥—А–∞–і–Є–µ–љ—В–∞ –і–∞–≤–ї–µ–љ–Є—П –≤ —Б–Є—Б—В–µ–Љ–∞—Е –ґ–µ–ї—З–љ–Њ–≥–Њ –Є –њ–∞–љ–Ї—А–µ–∞—В–Є—З–µ—Б–Ї–Њ–≥–Њ –њ—А–Њ—В–Њ–Ї–Њ–≤ (–Њ–Ї–Њ–ї–Њ 10 –Є 15 –Љ–Љ —А—В.—Б—В. —Б–Њ–Њ—В–≤–µ—В—Б—В–≤–µ–љ–љ–Њ). –Т –Ј–Њ–љ–µ —Б—Д–Є–љ–Ї—В–µ—А–∞ –љ–∞–±–ї—О–і–∞–µ—В—Б—П –і–≤–∞ —В–Є–њ–∞ –Љ–Њ—В–Њ—А–љ–Њ–є –∞–Ї—В–Є–≤–љ–Њ—Б—В–Є: –±–∞–Ј–∞–ї—М–љ–Њ–µ –і–∞–≤–ї–µ–љ–Є–µ –Є —Д–∞–Ј–љ–∞—П —Б–Њ–Ї—А–∞—В–Є—В–µ–ї—М–љ–∞—П –∞–Ї—В–Є–≤–љ–Њ—Б—В—М [12]. –С–∞–Ј–∞–ї—М–љ–Њ–µ –і–∞–≤–ї–µ–љ–Є–µ –°–Ю – –љ–∞–Є–±–Њ–ї–µ–µ –≤–∞–ґ–љ—Л–є –Ї–Њ–Љ–њ–Њ–љ–µ–љ—В –∞–Ї—В–Є–≤–љ–Њ—Б—В–Є —Б—Д–Є–љ–Ї—В–µ—А–∞. –Т –њ–µ—А–≤—Г—О –Њ—З–µ—А–µ–і—М, –Њ–љ–Њ –Њ—В–≤–µ—З–∞–µ—В –Ј–∞ —А–µ–≥—Г–ї—П—Ж–Є—О –Њ—В—В–Њ–Ї–∞ —Б–µ–Ї—А–µ—В–∞ –Є–Ј –ґ–µ–ї—З–љ—Л—Е –Є –њ–∞–љ–Ї—А–µ–∞—В–Є—З–µ—Б–Ї–Є—Е –њ—А–Њ—В–Њ–Ї–Њ–≤. –Я—А–Є –і–ї–Є—В–µ–ї—М–љ—Л—Е –Љ–∞–љ–Њ–Љ–µ—В—А–Є—З–µ—Б–Ї–Є—Е –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П—Е –±—Л–ї–Њ –Њ–±–љ–∞—А—Г–ґ–µ–љ–Њ, —З—В–Њ –±–∞–Ј–∞–ї—М–љ–Њ–µ –і–∞–≤–ї–µ–љ–Є–µ –њ–Њ–і–≤–µ—А–ґ–µ–љ–Њ –Љ–µ–і–ї–µ–љ–љ—Л–Љ –Ї–Њ–ї–µ–±–∞–љ–Є—П–Љ.
–§–∞–Ј–љ—Л–µ —Б–Њ–Ї—А–∞—Й–µ–љ–Є—П –°–Ю –љ–∞–Ї–ї–∞–і—Л–≤–∞—О—В—Б—П –љ–∞ –±–∞–Ј–∞–ї—М–љ–Њ–µ –і–∞–≤–ї–µ–љ–Є–µ; –Њ–љ–Є –≤–Њ–Ј–љ–Є–Ї–∞—О—В —Б —З–∞—Б—В–Њ—В–Њ–є –Њ–Ї–Њ–ї–Њ 4 –≤ –Љ–Є–љ—Г—В—Г –Є, –Ї–∞–Ї –њ—А–∞–≤–Є–ї–Њ, –њ–µ—А–µ–Љ–µ—Й–∞—О—В—Б—П –Њ—В –њ—А–Њ–Ї—Б–Є–Љ–∞–ї—М–љ—Л—Е –Њ—В–і–µ–ї–Њ–≤ –Ї –і–Є—Б—В–∞–ї—М–љ—Л–Љ (–∞–љ—В–µ–≥—А–∞–і–љ–Њ). –С—Л—Б—В—А—Л–µ —Д–∞–Ј–љ—Л–µ —Б–Њ–Ї—А–∞—Й–µ–љ–Є—П –°–Ю –љ–∞–±–ї—О–і–∞–ї–Є—Б—М –њ—А–Є –њ—А–Њ—Е–Њ–ґ–і–µ–љ–Є–Є —З–µ—А–µ–Ј –і–≤–µ–љ–∞–і—Ж–∞—В–Є–њ–µ—А—Б—В–љ—Г—О –Ї–Є—И–Ї—Г —В—А–µ—В—М–µ–є —Д–∞–Ј—Л –Љ–Є–Њ—Н–ї–µ–Ї—В—А–Є—З–µ—Б–Ї–Њ–≥–Њ –і–≤–Є–≥–∞—В–µ–ї—М–љ–Њ–≥–Њ –Ї–Њ–Љ–њ–ї–µ–Ї—Б–∞ [24]. –§–∞–Ј–љ—Л–µ —Б–Њ–Ї—А–∞—Й–µ–љ–Є—П –°–Ю, –≤–Њ–Ј–Љ–Њ–ґ–љ–Њ, –љ–µ–Њ–±—Е–Њ–і–Є–Љ—Л –і–ї—П —В–Њ–≥–Њ, —З—В–Њ–±—Л –њ–µ—А–Є–Њ–і–Є—З–µ—Б–Ї–Є –≤—Л–±—А–∞—Б—Л–≤–∞—В—М –Є–Ј –Ј–Њ–љ—Л —Б—Д–Є–љ–Ї—В–µ—А–∞ –љ–∞–Ї–∞–њ–ї–Є–≤–∞—О—Й–Є–є—Б—П –≤ –љ–µ–Љ «–Љ—Г—Б–Њ—А». –°—Д–Є–љ–Ї—В–µ—А –Ю–і–і–Є —А–∞–±–Њ—В–∞–µ—В, –Ї–∞–Ї –Љ–µ—Е–∞–љ–Є–Ј–Љ –і–ї—П –њ–Њ–і–і–µ—А–ґ–∞–љ–Є—П –Њ–њ—В–Є–Љ–∞–ї—М–љ–Њ–≥–Њ –і–∞–≤–ї–µ–љ–Є—П –њ–µ—А—Д—Г–Ј–Є–Є –≤ –Њ–±—Й–µ–Љ –ґ–µ–ї—З–љ–Њ–Љ –Є –њ–∞–љ–Ї—А–µ–∞—В–Є—З–µ—Б–Ї–Њ–Љ –њ—А–Њ—В–Њ–Ї–∞—Е. –Ъ–Њ–≥–і–∞ —Б–Ї–Њ—А–Њ—Б—В—М –њ–Њ—В–Њ–Ї–∞ —Г–≤–µ–ї–Є—З–Є–≤–∞–µ—В—Б—П –≤–Њ –≤—А–µ–Љ—П –µ–і—Л, –±–∞–Ј–∞–ї—М–љ–Њ–µ –і–∞–≤–ї–µ–љ–Є–µ –≤ –°–Ю –њ–Њ–љ–Є–ґ–∞–µ—В—Б—П, —Г–≤–µ–ї–Є—З–Є–≤–∞—П –Њ—В—В–Њ–Ї —Б–µ–Ї—А–µ—В–Њ–≤.
–У–Є–њ–µ—А—В–Њ–љ–Є—П —Б—Д–Є–љ–Ї—В–µ—А–∞ –Ю–і–і–Є (–У–°–Ю) –Љ–Њ–ґ–µ—В –Є–Љ–µ—В—М —Б–µ—А—М–µ–Ј–љ—Л–µ –њ–Њ—Б–ї–µ–і—Б—В–≤–Є—П –і–ї—П —Д—Г–љ–Ї—Ж–Є–Њ–љ–Є—А–Њ–≤–∞–љ–Є—П –њ–∞–љ–Ї—А–µ–∞—В–Њ––±–Є–ї–Є–∞—А–љ–Њ–є —Б–Є—Б—В–µ–Љ—Л. –Э–∞–њ—А–Є–Љ–µ—А, 60% –±–Њ–ї—М–љ—Л—Е —Б —З–∞—Б—В–Є—З–љ–Њ–є –±–Є–ї–Є–∞—А–љ–Њ–є –Њ–±—Б—В—А—Г–Ї—Ж–Є–µ–є –Є–Љ–µ—О—В –њ–∞—В–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є –њ–Њ–≤—Л—И–µ–љ–љ–Њ–µ –±–∞–Ј–∞–ї—М–љ–Њ–µ –і–∞–≤–ї–µ–љ–Є–µ –°–Ю –≤ –Њ–±–ї–∞—Б—В–Є –Њ–±—Й–µ–≥–Њ –ґ–µ–ї—З–љ–Њ–≥–Њ –њ—А–Њ—В–Њ–Ї–∞, —В–Њ–≥–і–∞ –Ї–∞–Ї —Г 77% –±–Њ–ї—М–љ—Л—Е —Б –Њ—Б—В—А—Л–Љ —А–µ—Ж–Є–і–Є–≤–Є—А—Г—О—Й–Є–Љ –њ–∞–љ–Ї—А–µ–∞—В–Є—В–Њ–Љ –±–∞–Ј–∞–ї—М–љ–Њ–µ –і–∞–≤–ї–µ–љ–Є–µ –њ–Њ–≤—Л—И–µ–љ–Њ –Є—Б–Ї–ї—О—З–Є—В–µ–ї—М–љ–Њ –≤ —Б–µ–≥–Љ–µ–љ—В–µ –њ–∞–љ–Ї—А–µ–∞—В–Є—З–µ—Б–Ї–Њ–≥–Њ –њ—А–Њ—В–Њ–Ї–∞. –†–µ–Ј—Г–ї—М—В–∞—В—Л –љ–µ–і–∞–≤–љ–Є—Е –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–є –њ–Њ–Ї–∞–Ј–∞–ї–Є, —З—В–Њ –і–ї—П –њ–Њ–і—В–≤–µ—А–ґ–і–µ–љ–Є—П –і–Є–∞–≥–љ–Њ–Ј–∞ –У–°–Ю –Љ–Њ–≥—Г—В –±—Л—В—М –љ–µ–Њ–±—Е–Њ–і–Є–Љ—Л —Б–µ–ї–µ–Ї—В–Є–≤–љ–Њ–µ –Ї–∞–љ—О–ї–Є—А–Њ–≤–∞–љ–Є–µ –Є –Љ–∞–љ–Њ–Љ–µ—В—А–Є—П –ґ–µ–ї—З–љ–Њ–≥–Њ –Є–ї–Є –њ–∞–љ–Ї—А–µ–∞—В–Є—З–µ—Б–Ї–Њ–≥–Њ —Б–µ–≥–Љ–µ–љ—В–∞.
–Ъ–ї–∞—Б—Б–Є—Д–Є–Ї–∞—Ж–Є—П –≥–Є–њ–µ—А—В–Њ–љ–Є—З–µ—Б–Ї–Є—Е
—А–∞—Б—Б—В—А–Њ–є—Б—В–≤ —Б—Д–Є–љ–Ї—В–µ—А–∞ –Ю–і–і–Є
–У–°–Ю –Ї–∞–Ї –њ–∞–љ–Ї—А–µ–∞—В–Є—З–µ—Б–Ї–Њ–є, —В–∞–Ї –Є –±–Є–ї–Є–∞—А–љ–Њ–є —Б–Є—Б—В–µ–Љ —Г—Б–ї–Њ–≤–љ–Њ —А–∞–Ј–і–µ–ї—П–µ—В—Б—П –љ–∞ 3 –≥—А—Г–њ–њ—Л –њ–Њ –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Њ–є –Ї–∞—А—В–Є–љ–µ (–≤ —Б–Њ–Њ—В–≤–µ—В—Б—В–≤–Є–Є —Б –љ–∞–ї–Є—З–Є–µ–Љ «—В–Є–њ–Є—З–љ–Њ–є» –∞–±–і–Њ–Љ–Є–љ–∞–ї—М–љ–Њ–є –±–Њ–ї–Є) –Є –Њ–±—К–µ–Ї—В–Є–≤–љ—Л–Љ –њ—А–Є–Ј–љ–∞–Ї–∞–Љ [14]. –У–Є–њ–µ—А—В–Њ–љ–Є—З–µ—Б–Ї–Є–µ —А–∞—Б—Б—В—А–Њ–є—Б—В–≤–∞ —Б—Д–Є–љ–Ї—В–µ—А–∞ –Ю–і–і–Є –≤ –ґ–µ–ї—З–љ–Њ–Љ —Б–µ–≥–Љ–µ–љ—В–µ –Љ–Њ–ґ–љ–Њ —А–∞–Ј–і–µ–ї–Є—В—М –љ–∞ —В—А–Є —В–Є–њ–∞:
1. –Ґ–Є–њ –±–Є–ї–Є–∞—А–љ–Њ–є –і–Є—Б—Д—Г–љ–Ї—Ж–Є–Є –°–Ю (–Њ–њ—А–µ–і–µ–ї–µ–љ–љ—Л–є). –≠—В–Њ –±–Њ–ї—М–љ—Л–µ —Б —В–Є–њ–Є—З–љ–Њ–є –±–Є–ї–Є–∞—А–љ–Њ–є –±–Њ–ї—М—О, —Г –Ї–Њ—В–Њ—А—Л—Е –Њ–њ—А–µ–і–µ–ї—П–µ—В—Б—П —А–∞—Б—И–Є—А–µ–љ–љ—Л–є –ґ–µ–ї—З–љ—Л–є –њ—А–Њ—В–Њ–Ї (>12 –Љ–Љ) –Є–ї–Є –љ–∞—А—Г—И–µ–љ–Є–µ –Њ—В—В–Њ–Ї–∞ –ґ–µ–ї—З–Є (–≤—А–µ–Љ—П –≤—Л–і–µ–ї–µ–љ–Є—П –Ї–Њ–љ—В—А–∞—Б—В–∞ –њ—А–Є –≠–†–•–Я–У > 45 –Љ–Є–љ.), –∞ —В–∞–Ї–ґ–µ –Њ—В–Ї–ї–Њ–љ–µ–љ–Є—П —Д—Г–љ–Ї—Ж–Є–Њ–љ–∞–ї—М–љ—Л—Е –њ—А–Њ–± –њ–µ—З–µ–љ–Є (–±–Њ–ї–µ–µ —З–µ–Љ –і–≤—Г–Ї—А–∞—В–љ–Њ–µ –њ–Њ–≤—Л—И–µ–љ–Є–µ —Г—А–Њ–≤–љ—П —Й–µ–ї–Њ—З–љ–Њ–є —Д–Њ—Б—Д–∞—В–∞–Ј—Л –Є–ї–Є —В—А–∞–љ—Б–∞–Љ–Є–љ–∞–Ј –њ—А–Є –і–≤—Г—Е –Є–ї–Є –±–Њ–ї–µ–µ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П—Е).
2. –Ґ–Є–њ –±–Є–ї–Є–∞—А–љ–Њ–є –і–Є—Б—Д—Г–љ–Ї—Ж–Є–Є –°–Ю (–њ—А–µ–і–њ–Њ–ї–Њ–ґ–Є—В–µ–ї—М–љ—Л–є). –С–Њ–ї—М–љ—Л–µ –≤ —Н—В–Њ–є –≥—А—Г–њ–њ–µ –Є–Љ–µ—О—В —В–Є–њ–Є—З–љ—Л–µ –±–Њ–ї–Є, –∞ —В–∞–Ї–ґ–µ –Њ–і–Є–љ –Є–ї–Є –і–≤–∞ –Ї—А–Є—В–µ—А–Є—П –Є–Ј —В–Є–њ–∞ 1.
3. –Ґ–Є–њ –±–Є–ї–Є–∞—А–љ–Њ–є –і–Є—Б—Д—Г–љ–Ї—Ж–Є–Є –°–Ю (–≤–Њ–Ј–Љ–Њ–ґ–љ—Л–є). –С–Њ–ї—М–љ—Л–µ –Є–Ј —Н—В–Њ–є –≥—А—Г–њ–њ—Л –Є–Љ–µ—О—В —В–Њ–ї—М–Ї–Њ —В–Є–њ–Є—З–љ—Л–µ –±–Њ–ї–Є, –±–µ–Ј –Ї–∞–Ї–Є—Е––ї–Є–±–Њ –Њ–±—К–µ–Ї—В–Є–≤–љ—Л—Е –љ–∞—А—Г—И–µ–љ–Є–є.
–Я–∞—Ж–Є–µ–љ—В—Л —Б 1 —В–Є–њ–Њ–Љ —А–∞—Б—Б—В—А–Њ–є—Б—В–≤ –°–Ю –Є–Љ–µ—О—В —Б—В—А—Г–Ї—В—Г—А–љ—Л–µ –љ–∞—А—Г—И–µ–љ–Є—П —Б–∞–Љ–Њ–≥–Њ —Б—Д–Є–љ–Ї—В–µ—А–∞ –Є–ї–Є –Ј–Њ–љ—Л —Д–∞—В–µ—А–Њ–≤–∞ —Б–Њ—Б–Ї–∞ (–љ–∞–њ—А–Є–Љ–µ—А, —Б–Ї–ї–µ—А–Њ–Ј); —Г –±–Њ–ї—М–љ—Л—Е —Б–Њ 2 –Є 3 —В–Є–њ–Њ–Љ –≤—Л—А–∞–ґ–µ–љ—Л —В–∞–Ї–ґ–µ –Є —В–∞–Ї –љ–∞–Ј—Л–≤–∞–µ–Љ—Л–µ –і–Є—Б—Д—Г–љ–Ї—Ж–Є–Њ–љ–∞–ї—М–љ—Л–µ –љ–∞—А—Г—И–µ–љ–Є—П –°–Ю [9,11].
–≠—В–Є–Њ–ї–Њ–≥–Є—П –і–Є—Б—Д—Г–љ–Ї—Ж–Є–Њ–љ–∞–ї—М–љ—Л—Е
—А–∞—Б—Б—В—А–Њ–є—Б—В–≤ –ґ–µ–ї—З–µ–≤—Л–≤–Њ–і—П—Й–Є—Е –њ—Г—В–µ–є
–Ф–Є—Б—Д—Г–љ–Ї—Ж–Є–Њ–љ–∞–ї—М–љ—Л–µ —А–∞—Б—Б—В—А–Њ–є—Б—В–≤–∞ –±–Є–ї–Є–∞—А–љ–Њ–≥–Њ —В—А–∞–Ї—В–∞ (–Ф–†–С–Ґ) –Љ–Њ–≥—Г—В –±—Л—В—М —Б–≤—П–Ј–∞–љ—Л —Б –њ–µ—А–≤–Є—З–љ—Л–Љ —Г–Љ–µ–љ—М—И–µ–љ–Є–µ–Љ –Љ—Л—И–µ—З–љ–Њ–є –Љ–∞—Б—Б—Л –ґ–µ–ї—З–љ–Њ–≥–Њ –њ—Г–Ј—Л—А—П –Є —Б—Д–Є–љ–Ї—В–µ—А–∞ –Ю–і–і–Є –Є —Б–Њ —Б–љ–Є–ґ–µ–љ–Є–µ–Љ —З—Г–≤—Б—В–≤–Є—В–µ–ї—М–љ–Њ—Б—В–Є —А–µ—Ж–µ–њ—В–Њ—А–љ–Њ–≥–Њ –∞–њ–њ–∞—А–∞—В–∞ –Ї –љ–µ–є—А–Њ–≥—Г–Љ–Њ—А–∞–ї—М–љ–Њ–є —Б—В–Є–Љ—Г–ї—П—Ж–Є–Є. –Ґ–∞–Ї–Є–µ –љ–∞—А—Г—И–µ–љ–Є—П –≤—Б—В—А–µ—З–∞—О—В—Б—П —А–µ–і–Ї–Њ (10–15%).
–Ч–љ–∞—З–Є—В–µ–ї—М–љ–Њ —З–∞—Й–µ –Ф–†–С–Ґ —А–∞–Ј–≤–Є–≤–∞—О—В—Б—П –љ–∞ —Д–Њ–љ–µ –і—А—Г–≥–Є—Е –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є–є –Њ—А–≥–∞–љ–Њ–≤ –њ–Є—Й–µ–≤–∞—А–µ–љ–Є—П: –≥–µ–њ–∞—В–Є—В–Њ–≤ –Є —Ж–Є—А—А–Њ–Ј–Њ–≤ –њ–µ—З–µ–љ–Є, —Е—А–Њ–љ–Є—З–µ—Б–Ї–Њ–≥–Њ –њ–∞–љ–Ї—А–µ–∞—В–Є—В–∞, —Е—А–Њ–љ–Є—З–µ—Б–Ї–Є—Е –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є–є –ґ–µ–ї—Г–і–Ї–∞ –Є —В–Њ–љ–Ї–Њ–є –Ї–Є—И–Ї–Є. –Ю–љ–Є –Љ–Њ–≥—Г—В –љ–∞–±–ї—О–і–∞—В—М—Б—П –њ—А–Є –≥–Њ—А–Љ–Њ–љ–∞–ї—М–љ—Л—Е –Є–Ј–Љ–µ–љ–µ–љ–Є—П—Е: –њ—А–Є –њ—А–µ–і–Љ–µ–љ—Б—В—А—Г–∞–ї—М–љ–Њ–Љ —Б–Є–љ–і—А–Њ–Љ–µ, –±–µ—А–µ–Љ–µ–љ–љ–Њ—Б—В–Є, —Б–∞—Е–∞—А–љ–Њ–Љ –і–Є–∞–±–µ—В–µ. –Ф–†–С–Ґ —В–∞–Ї–ґ–µ —П–≤–ї—П—О—В—Б—П –Њ–і–љ–Є–Љ –Є–Ј —Д–∞–Ї—В–Њ—А–Њ–≤ —А–∞–Ј–≤–Є—В–Є—П –ґ–µ–ї—З–љ–Њ–Ї–∞–Љ–µ–љ–љ–Њ–є –±–Њ–ї–µ–Ј–љ–Є. –Ч–љ–∞—З–Є—В–µ–ї—М–љ—Г—О —А–Њ–ї—М –≤ —Д–Њ—А–Љ–Є—А–Њ–≤–∞–љ–Є–Є –Ф–†–С–Ґ –Є–≥—А–∞—О—В –њ—Б–Є—Е–Њ—Н–Љ–Њ—Ж–Є–∞–ї—М–љ—Л–µ —Д–∞–Ї—В–Њ—А—Л – —Н–Љ–Њ—Ж–Є–Њ–љ–∞–ї—М–љ—Л–µ –њ–µ—А–µ–≥—А—Г–Ј–Ї–Є, —Б—В—А–µ—Б—Б–Њ–≤—Л–µ —Б–Є—В—Г–∞—Ж–Є–Є.
–Т–ї–Є—П–љ–Є–µ –њ—Б–Є—Е–Њ–≥–µ–љ–љ—Л—Е —Д–∞–Ї—В–Њ—А–Њ–≤ –љ–∞ —Д—Г–љ–Ї—Ж–Є—О –ґ–µ–ї—З–љ–Њ–≥–Њ –њ—Г–Ј—Л—А—П –Є –ґ–µ–ї—З–љ—Л—Е –њ—Г—В–µ–є —А–µ–∞–ї–Є–Ј—Г–µ—В—Б—П —Б —Г—З–∞—Б—В–Є–µ–Љ –Ї–Њ—А–Ї–Њ–≤—Л—Е –Є –њ–Њ–і–Ї–Њ—А–Ї–Њ–≤—Л—Е –Њ–±—А–∞–Ј–Њ–≤–∞–љ–Є–є —Б –љ–µ—А–≤–љ—Л–Љ–Є —Ж–µ–љ—В—А–∞–Љ–Є –њ—А–Њ–і–Њ–ї–≥–Њ–≤–∞—В–Њ–≥–Њ –Љ–Њ–Ј–≥–∞, –≥–Є–њ–Њ—В–∞–ї–∞–Љ—Г—Б–∞, –∞ —В–∞–Ї–ґ–µ —Н–љ–і–Њ–Ї—А–Є–љ–љ–Њ–є —Б–Є—Б—В–µ–Љ—Л. –Э–∞—А—Г—И–µ–љ–Є–µ –њ—А–Њ–і—Г–Ї—Ж–Є–Є –•–¶–Ъ––Я–Ч –Є –і—А—Г–≥–Є—Е –љ–µ–є—А–Њ–њ–µ–њ—В–Є–і–Њ–≤ (—Б–µ–Ї—А–µ—В–Є–љ–∞, –Љ–Њ—В–Є–ї–Є–љ–∞, –≥–∞—Б—В—А–Є–љ–∞), –љ–µ–і–Њ—Б—В–∞—В–Њ—З–љ–Њ–µ –Њ–±—А–∞–Ј–Њ–≤–∞–љ–Є–µ —В–Є—А–µ–Њ–Є–і–Є–љ–∞, –Њ–Ї—Б–Є—В–Њ—Ж–Є–љ–∞, –Ї–Њ—А—В–Є–Ї–Њ—Б—В–µ—А–Њ–Є–і–љ—Л—Е –Є –њ–Њ–ї–Њ–≤—Л—Е –≥–Њ—А–Љ–Њ–љ–Њ–≤ –њ—А–Є–≤–Њ–і–Є—В –Ї –Є–Ј–Љ–µ–љ–µ–љ–Є—О —В–Њ–љ—Г—Б–∞ –ґ–µ–ї—З–љ–Њ–≥–Њ –њ—Г–Ј—Л—А—П –Є —Б—Д–Є–љ–Ї—В–µ—А–Њ–≤ –ґ–µ–ї—З–µ–≤—Л–і–µ–ї–Є—В–µ–ї—М–љ–Њ–є —Б–Є—Б—В–µ–Љ—Л.
–•–Є—А—Г—А–≥–Є—З–µ—Б–Ї–Є–µ –≤–Љ–µ—И–∞—В–µ–ї—М—Б—В–≤–∞ –љ–∞ –Њ—А–≥–∞–љ–∞—Е –≤–µ—А—Е–љ–µ–≥–Њ —Н—В–∞–ґ–∞ –±—А—О—И–љ–Њ–є –њ–Њ–ї–Њ—Б—В–Є (—Е–Њ–ї–µ—Ж–Є—Б—В—Н–Ї—В–Њ–Љ–Є—П, –≤–∞–≥–Њ—В–Њ–Љ–Є—П, —А–µ–Ј–µ–Ї—Ж–Є—П –ґ–µ–ї—Г–і–Ї–∞) –њ—А–Є–≤–Њ–і—П—В –Ї —Б—Г—Й–µ—Б—В–≤–µ–љ–љ—Л–Љ –љ–∞—А—Г—И–µ–љ–Є—П–Љ —Д—Г–љ–Ї—Ж–Є–Є –±–Є–ї–Є–∞—А–љ–Њ–є —Б–Є—Б—В–µ–Љ—Л. –Я–Њ—Б–ї–µ —Е–Њ–ї–µ—Ж–Є—Б—В—Н–Ї—В–Њ–Љ–Є–Є —Г 70–80% –±–Њ–ї—М–љ—Л—Е –љ–∞–±–ї—О–і–∞–µ—В—Б—П –љ–µ–і–Њ—Б—В–∞—В–Њ—З–љ–Њ—Б—В—М —Б—Д–Є–љ–Ї—В–µ—А–∞ –Ю–і–і–Є —Б –љ–µ–њ—А–µ—А—Л–≤–љ—Л–Љ –Є—Б—В–µ—З–µ–љ–Є–µ–Љ –ґ–µ–ї—З–Є –≤ –њ—А–Њ—Б–≤–µ—В –і–≤–µ–љ–∞–і—Ж–∞—В–Є–њ–µ—А—Б—В–љ–Њ–є –Ї–Є—И–Ї–Є. –Я–Њ—Б–ї–µ –≤–∞–≥–Њ—В–Њ–Љ–Є–Є –≤ –њ–µ—А–≤—Л–µ 6 –Љ–µ—Б—П—Ж–µ–≤ –Њ—В–Љ–µ—З–∞–µ—В—Б—П –≤—Л—А–∞–ґ–µ–љ–љ–∞—П –≥–Є–њ–Њ—В–Њ–љ–Є—П –ґ–µ–ї—З–љ–Њ–≥–Њ –њ—Г–Ј—Л—А—П –Є —Б—Д–Є–љ–Ї—В–µ—А–∞ –Ю–і–і–Є. –†–µ–Ј–µ–Ї—Ж–Є—П –ґ–µ–ї—Г–і–Ї–∞ —Б –≤—Л–Ї–ї—О—З–µ–љ–Є–µ–Љ –Є–Ј –∞–Ї—В–∞ –њ–Є—Й–µ–≤–∞—А–µ–љ–Є—П —З–∞—Б—В–Є –ґ–µ–ї—Г–і–Ї–∞ –Є –і–≤–µ–љ–∞–і—Ж–∞—В–Є–њ–µ—А—Б—В–љ–Њ–є –Ї–Є—И–Ї–Є –≤—Л–Ј—Л–≤–∞–µ—В —Б–µ–Ї—А–µ—В–Њ—А–љ—Л–µ –Є –Љ–Њ—В–Њ—А–љ–Њ–—Н–≤–∞–Ї—Г–∞—В–Њ—А–љ—Л–µ –љ–∞—А—Г—И–µ–љ–Є—П –Є–Ј––Ј–∞ —Б–љ–Є–ґ–µ–љ–Є—П –њ—А–Њ–і—Г–Ї—Ж–Є–Є –≥–Њ—А–Љ–Њ–љ–Њ–≤.
–Ъ–ї–Є–љ–Є—З–µ—Б–Ї–Є–µ –њ—А–Њ—П–≤–ї–µ–љ–Є—П
–Я—А–Є –≥–Є–њ–µ—А–Ї–Є–љ–µ—В–Є—З–µ—Б–Ї–Њ–є —Д–Њ—А–Љ–µ –і–Є—Б—Д—Г–љ–Ї—Ж–Є–Є –ґ–µ–ї—З–љ–Њ–≥–Њ –њ—Г–Ј—Л—А—П –Є/–Є–ї–Є –≥–Є–њ–µ—А—В–Њ–љ–Є—З–µ—Б–Ї–Њ–є —Д–Њ—А–Љ–µ –і–Є—Б—Д—Г–љ–Ї—Ж–Є–Є —Б—Д–Є–љ–Ї—В–µ—А–∞ –Ю–і–і–Є –њ–µ—А–Є–Њ–і–Є—З–µ—Б–Ї–Є –≤ –њ—А–∞–≤–Њ–Љ –њ–Њ–і—А–µ–±–µ—А—М–µ –њ–Њ—П–≤–ї—П—О—В—Б—П –Ї–Њ–ї–Є–Ї–Њ–њ–Њ–і–Њ–±–љ—Л–µ –±–Њ–ї–Є —Б –Є—А—А–∞–і–Є–∞—Ж–Є–µ–є –≤ —Б–њ–Є–љ—Г, –њ–Њ–і –њ—А–∞–≤—Г—О –ї–Њ–њ–∞—В–Ї—Г, –њ—А–∞–≤–Њ–µ –њ–ї–µ—З–Њ, —Г—Б–Є–ї–Є–≤–∞—О—Й–Є–µ—Б—П –њ—А–Є –≥–ї—Г–±–Њ–Ї–Њ–Љ –≤–і–Њ—Е–µ. –С–Њ–ї–Є –љ–Њ—Б—П—В –Ї—А–∞—В–Ї–Њ–≤—А–µ–Љ–µ–љ–љ—Л–є —Е–∞—А–∞–Ї—В–µ—А –Є –≤–Њ–Ј–љ–Є–Ї–∞—О—В –Њ–±—Л—З–љ–Њ –њ–Њ—Б–ї–µ –њ–Њ–≥—А–µ—И–љ–Њ—Б—В–Є –≤ –і–Є–µ—В–µ, –њ—А–Є –њ—А–Є–µ–Љ–µ —Е–Њ–ї–Њ–і–љ—Л—Е –љ–∞–њ–Є—В–Ї–Њ–≤, —Д–Є–Ј–Є—З–µ—Б–Ї–Њ–є –љ–∞–≥—А—Г–Ј–Ї–µ, —Б—В—А–µ—Б—Б–Њ–≤—Л—Е —Б–Є—В—Г–∞—Ж–Є—П—Е, —А–µ–і–Ї–Њ – –љ–Њ—З—М—О. –Ш–Ј –Њ–±—Й–Є—Е —Б–Є–Љ–њ—В–Њ–Љ–Њ–≤ –Љ–Њ–ґ–љ–Њ –Њ—В–Љ–µ—В–Є—В—М –њ–Њ—Е—Г–і–∞–љ–Є–µ, —А–∞–Ј–і—А–∞–ґ–Є—В–µ–ї—М–љ–Њ—Б—В—М, –њ–Њ–≤—Л—И–µ–љ–љ—Г—О —Г—В–Њ–Љ–ї—П–µ–Љ–Њ—Б—В—М, –њ–Њ—В–ї–Є–≤–Њ—Б—В—М, –≥–Њ–ї–Њ–≤–љ—Л–µ –±–Њ–ї–Є, —В–∞—Е–Є–Ї–∞—А–і–Є—О.
–Я—А–Є –≥–Є–њ–Њ–Ї–Є–љ–µ—В–Є—З–µ—Б–Ї–Њ–є –Є –≥–Є–њ–Њ—В–Њ–љ–Є—З–µ—Б–Ї–Њ–є –і–Є—Б—Д—Г–љ–Ї—Ж–Є–Є –±–Є–ї–Є–∞—А–љ–Њ–≥–Њ —В—А–∞–Ї—В–∞ –Њ—В–Љ–µ—З–∞—О—В—Б—П —В—Г–њ—Л–µ –±–Њ–ї–Є –≤ –њ—А–∞–≤–Њ–Љ –њ–Њ–і—А–µ–±–µ—А—М–µ, –Њ—Й—Г—Й–µ–љ–Є—П –і–∞–≤–ї–µ–љ–Є—П, —А–∞—Б–њ–Є—А–∞–љ–Є—П, —Г—Б–Є–ї–Є–≤–∞—О—Й–Є–µ—Б—П –њ—А–Є –љ–∞–Ї–ї–Њ–љ–µ —В—Г–ї–Њ–≤–Є—Й–∞. –І–∞—Б—В—Л–Љ–Є —Б–Є–Љ–њ—В–Њ–Љ–∞–Љ–Є —П–≤–ї—П—О—В—Б—П —В–Њ—И–љ–Њ—В–∞, –≥–Њ—А–µ—З—М –≤–Њ —А—В—Г, –≤–Ј–і—Г—В–Є–µ –ґ–Є–≤–Њ—В–∞, –Ј–∞–њ–Њ—А—Л, –Є–Ј–±—Л—В–Њ–Ї –Љ–∞—Б—Б—Л —В–µ–ї–∞.
–Ф–Є–∞–≥–љ–Њ—Б—В–Є–Ї–∞ –і–Є—Б—Д—Г–љ–Ї—Ж–Є–Є —Б—Д–Є–љ–Ї—В–µ—А–∞ –Ю–і–і–Є
–Ю–±—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ –±–Њ–ї—М–љ—Л—Е, —Б—В—А–∞–і–∞—О—Й–Є—Е –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П–Љ–Є –њ–Њ–і–ґ–µ–ї—Г–і–Њ—З–љ–Њ–є –ґ–µ–ї–µ–Ј—Л –Є–ї–Є –ґ–µ–ї—З–µ–≤—Л–≤–Њ–і—П—Й–Є—Е –њ—Г—В–µ–є –њ—А–Є –њ–Њ–і–Њ–Ј—А–µ–љ–Є–Є –љ–∞ –і–Є—Б—Д—Г–љ–Ї—Ж–Є—О –°–Ю, –њ—А–Њ–≤–Њ–і–Є—В—Б—П —Б –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є–µ–Љ –±–Є–Њ—Е–Є–Љ–Є—З–µ—Б–Ї–Є—Е —В–µ—Б—В–Њ–≤, –њ—А–Њ–≤–Њ–Ї–∞—Ж–Є–Њ–љ–љ—Л—Е —В–µ—Б—В–Њ–≤, —Б—Ж–Є–љ—В–Є–≥—А–∞—Д–Є–Є, –£–Ч–Ш, –Љ–∞–љ–Њ–Љ–µ—В—А–Є–Є (–≤ —Б–Њ–Њ—В–≤–µ—В—Б—В–≤–Є–Є —Б –Ї–ї–∞—Б—Б–Є—Д–Є–Ї–∞—Ж–Є–µ–є, –њ—А–Є–≤–µ–і–µ–љ–љ–Њ–є –≤—Л—И–µ).
–У–°–Ю – —Н—В–Њ –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є–є —Б–Є–љ–і—А–Њ–Љ, –≤—Л–Ј–≤–∞–љ–љ—Л–є –≤—А–µ–Љ–µ–љ–љ—Л–Љ —Б–њ–∞–Ј–Љ–Њ–Љ –°–Ю. –°–њ–∞–Ј–Љ –Љ–Њ–ґ–µ—В —В–∞–Ї–ґ–µ –Ј–∞—Е–≤–∞—В—Л–≤–∞—В—М –њ–∞–љ–Ї—А–µ–∞—В–Є—З–µ—Б–Ї–Є–є –њ—А–Њ—В–Њ–Ї, —З—В–Њ –Љ–Њ–ґ–µ—В –±—Л—В—М –њ—А–Є—З–Є–љ–Њ–є –Є–і–Є–Њ–њ–∞—В–Є—З–µ—Б–Ї–Њ–≥–Њ —А–µ—Ж–Є–і–Є–≤–Є—А—Г—О—Й–µ–≥–Њ –њ–∞–љ–Ї—А–µ–∞—В–Є—В–∞. –£ –±–Њ–ї—М–љ—Л—Е, –њ–µ—А–µ–љ–µ—Б—И–Є—Е —Е–Њ–ї–µ—Ж–Є—Б—В—Н–Ї—В–Њ–Љ–Є—О –Є –Є–Љ–µ—О—Й–Є—Е —Е–∞—А–∞–Ї—В–µ—А–љ—Л–µ —Б–Є–Љ–њ—В–Њ–Љ—Л, –Љ–Њ–ґ–µ—В –±—Л—В—М –њ–Њ—Б—В–∞–≤–ї–µ–љ –њ—А–µ–і–њ–Њ–ї–Њ–ґ–Є—В–µ–ї—М–љ—Л–є –і–Є–∞–≥–љ–Њ–Ј –У–°–Ю, –Њ–і–љ–∞–Ї–Њ –і–ї—П –µ–≥–Њ –њ–Њ–і—В–≤–µ—А–ґ–і–µ–љ–Є—П —В—А–µ–±—Г—О—В—Б—П –њ–Њ–ї–Њ–ґ–Є—В–µ–ї—М–љ—Л–µ —А–µ–Ј—Г–ї—М—В–∞—В—Л –њ—А–Њ–≤–Њ–Ї–∞—Ж–Є–Њ–љ–љ—Л—Е —В–µ—Б—В–Њ–≤.
–Ф–ї—П –і–Є–∞–≥–љ–Њ—Б—В–Є–Ї–Є –і–Є—Б–Ї–Є–љ–µ—В–Є—З–µ—Б–Ї–Є—Е —А–∞—Б—Б—В—А–Њ–є—Б—В–≤ –њ–∞–љ–Ї—А–µ–∞—В–Њ––±–Є–ї–Є–∞—А–љ–Њ–є —Б–Є—Б—В–µ–Љ—Л –Ф–µ–±—А—Н–є –Є —Б–Њ–∞–≤—В. [6] –њ—А–µ–і–ї–Њ–ґ–Є–ї–Є –≤–≤–Њ–і–Є—В—М –±–Њ–ї—М–љ–Њ–Љ—Г –Љ–Њ—А—Д–Є–љ –Є —Е–Њ–ї–µ—А–µ—В–Є–Ї, –∞ –Э–∞—А–і–Є –Є —Б–Њ–∞–≤—В. [16] –њ–Њ–Ј–ґ–µ –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–ї–Є –≤–≤–µ–і–µ–љ–Є–µ –Љ–Њ—А—Д–Є–љ–∞ –Є –љ–µ–Њ—Б—В–Є–≥–Љ–Є–љ–∞. –≠—В–Є –Љ–µ—В–Њ–і–Є–Ї–Є –љ–µ –Њ—В–ї–Є—З–∞—О—В—Б—П –≤—Л—Б–Њ–Ї–Њ–є –≤–Њ—Б–њ—А–Њ–Є–Ј–≤–Њ–і–Є–Љ–Њ—Б—В—М—О, –і–Њ—Б—В–∞—В–Њ—З–љ–Њ –≤—Л—Б–Њ–Ї —Г—А–Њ–≤–µ–љ—М –ї–Њ–ґ–љ–Њ–њ–Њ–ї–Њ–ґ–Є—В–µ–ї—М–љ—Л—Е —А–µ–Ј—Г–ї—М—В–∞—В–Њ–≤ –Є, –Ї—А–Њ–Љ–µ —В–Њ–≥–Њ, —Н—В–Є —В–µ—Б—В—Л –Њ—Б–љ–Њ–≤–∞–љ—Л –љ–∞ —Б—Г–±—К–µ–Ї—В–Є–≤–љ—Л—Е –Њ—Й—Г—Й–µ–љ–Є—П—Е –±–Њ–ї—М–љ—Л—Е (–њ–Њ—П–≤–ї–µ–љ–Є–µ —В–Є–њ–Є—З–љ—Л—Е –±–Њ–ї–µ–є –њ–Њ—Б–ї–µ —Б—В–Є–Љ—Г–ї—П—Ж–Є–Є).
–Ф–µ–ї–∞–ї–Њ—Б—М –Љ–љ–Њ–≥–Њ –њ–Њ–њ—Л—В–Њ–Ї —Б–і–µ–ї–∞—В—М –њ—А–Њ–≤–Њ–Ї–∞—Ж–Є–Њ–љ–љ—Л–µ —В–µ—Б—В—Л –±–Њ–ї–µ–µ –Њ–±—К–µ–Ї—В–Є–≤–љ—Л–Љ–Є. –Ь–Њ—А—Д–Є–љ–—Е–Њ–ї–µ—А–µ—В–Є–Ї–Њ–≤—Л–є —В–µ—Б—В –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–ї–Є –≤ —Б–Њ—З–µ—В–∞–љ–Є–Є —Б –Є–Ј–Љ–µ—А–µ–љ–Є–µ–Љ —Г—А–Њ–≤–љ—П —Б—Л–≤–Њ—А–Њ—В–Њ—З–љ—Л—Е —В—А–∞–љ—Б–∞–Љ–Є–љ–∞–Ј. –†–µ–Ј—Г–ї—М—В–∞—В —В–∞–Ї–Њ–≥–Њ —В–µ—Б—В–∞ —Б—З–Є—В–∞–µ—В—Б—П –њ–Њ–ї–Њ–ґ–Є—В–µ–ї—М–љ—Л–Љ, –µ—Б–ї–Є —Б–њ—Г—Б—В—П –љ–µ—Б–Ї–Њ–ї—М–Ї–Њ —З–∞—Б–Њ–≤ –њ–Њ—Б–ї–µ –Є–љ—К–µ–Ї—Ж–Є–Є –њ—А–Њ–Є—Б—Е–Њ–і–Є—В –Ј–љ–∞—З–Є—В–µ–ї—М–љ–Њ–µ –њ–Њ–≤—Л—И–µ–љ–Є–µ —Г—А–Њ–≤–љ—П —В—А–∞–љ—Б–∞–Љ–Є–љ–∞–Ј –Є/–Є–ї–Є –∞–Љ–Є–ї–∞–Ј—Л [25].
–Т–∞—А—А–Њ –Є —Б–Њ–∞–≤—В. [25] –≤–Є–Ј—Г–∞–ї–Є–Ј–Є—А–Њ–≤–∞–ї–Є –ґ–µ–ї—З–љ—Л–µ –њ—А–Њ—В–Њ–Ї–Є —Б –њ–Њ–Љ–Њ—Й—М—О 99mTc–HIDA –Є –њ–Њ–Ї–∞–Ј–∞–ї–Є, —З—В–Њ —Г –±–Њ–ї—М–љ—Л—Е —Б –њ–Њ–ї–Њ–ґ–Є—В–µ–ї—М–љ—Л–Љ —В–µ—Б—В–Њ–Љ –Ф–µ–±—А—Н—П –њ—А–µ–Ї—А–∞—Й–µ–љ–Є–µ –Њ—В—В–Њ–Ї–∞ —Б–µ–Ї—А–µ—В–∞ –љ–∞ —Г—А–Њ–≤–љ–µ –°–Ю –њ—А–Њ–Є—Б—Е–Њ–і–Є—В –Њ–і–љ–Њ–≤—А–µ–Љ–µ–љ–љ–Њ —Б –њ–Њ—П–≤–ї–µ–љ–Є–µ–Љ –±–Њ–ї–Є. –Р–Љ–Є–ї–љ–Є—В—А–Є—В –Є –•–¶–Ъ–8 (—Е–Њ–ї–µ—Ж–Є—Б—В–Њ–Ї–Є–љ–Є–љ) –њ—А–µ–і–Њ—В–≤—А–∞—Й–∞—О—В —Б–Њ–Ї—А–∞—Й–µ–љ–Є–µ –°–Ю –њ–Њ–і –і–µ–є—Б—В–≤–Є–µ–Љ –Љ–Њ—А—Д–Є–љ–∞, –њ—А–Є —Н—В–Њ–Љ –њ—А–Њ–Є—Б—Е–Њ–і–Є—В –Њ–±–ї–µ–≥—З–µ–љ–Є–µ –Є–ї–Є –њ–Њ–ї–љ–Њ–µ –Є—Б—З–µ–Ј–љ–Њ–≤–µ–љ–Є–µ –±–Њ–ї–Є.
–Я—А–Є –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є–Є –Ї–Њ–Љ–њ—М—О—В–µ—А–љ–Њ–є —Б—Ж–Є–љ—В–Є–≥—А–∞—Д–Є–Є –њ–µ—З–µ–љ–Є –Є –ґ–µ–ї—З–µ–≤—Л–≤–Њ–і—П—Й–Є—Е –њ—Г—В–µ–є, —Б–Њ–≤–Љ–µ—Й–µ–љ–љ–Њ–є —Б —В–µ—Б—В–Њ–Љ –Э–∞—А–і–Є, —Б–њ–∞–Ј–Љ —Б—Д–Є–љ–Ї—В–µ—А–∞ –≤—Л–Ј—Л–≤–∞–µ—В—Б—П –≤–≤–µ–і–µ–љ–Є–µ–Љ –љ–µ–Њ—Б—В–Є–≥–Љ–Є–љ–∞ –Є –Љ–Њ—А—Д–Є–љ–∞. –•–∞—А–∞–Ї—В–µ—А–љ–∞—П –і–ї—П –Њ–±—Б—В—А—Г–Ї—Ж–Є–Є —Д–Њ—А–Љ–∞ –Ї—А–Є–≤–Њ–є –≤—А–µ–Љ—П––∞–Ї—В–Є–≤–љ–Њ—Б—В—М –њ—А–Є —А–µ–≥–Є—Б—В—А–∞—Ж–Є–Є –љ–∞–і –Њ–±—Й–Є–Љ –ґ–µ–ї—З–љ—Л–Љ –њ—А–Њ—В–Њ–Ї–Њ–Љ –Є –≤—Л—А–∞–ґ–µ–љ–љ–Њ–µ —Б–љ–Є–ґ–µ–љ–Є–µ —А–∞–і–Є–Њ–Є–Ј–Њ—В–Њ–њ–љ–Њ–є –∞–Ї—В–Є–≤–љ–Њ—Б—В–Є –њ–Њ—Б–ї–µ –≤–≤–µ–і–µ–љ–Є—П –љ–Є—В—А–Њ–≥–ї–Є—Ж–µ—А–Є–љ–∞ –і–Њ–Ї–∞–Ј—Л–≤–∞—О—В –љ–∞–ї–Є—З–Є–µ –У–°–Ю. –Ъ–Њ–Љ–њ—М—О—В–µ—А–љ–∞—П —Б—Ж–Є–љ—В–Є–≥—А–∞—Д–Є—П, —Б–Њ–≤–Љ–µ—Й–µ–љ–љ–∞—П —Б –љ–µ–Њ—Б—В–Є–≥–Љ–Є–љ––Љ–Њ—А—Д–Є–љ–Њ–≤–Њ–є –њ—А–Њ–≤–Њ–Ї–∞—Ж–Є–Њ–љ–љ–Њ–є –њ—А–Њ–±–Њ–є –Є –≤–≤–µ–і–µ–љ–Є–µ–Љ –љ–Є—В—А–Њ–≥–ї–Є—Ж–µ—А–Є–љ–∞, —А–µ–Ї–Њ–Љ–µ–љ–і—Г–µ—В—Б—П, –Ї–∞–Ї –љ–µ–Є–љ–≤–∞–Ј–Є–≤–љ–∞—П –њ—А–Њ—Ж–µ–і—Г—А–∞ –і–ї—П –Њ—Ж–µ–љ–Ї–Є —Б–њ–∞—Б—В–Є—З–µ—Б–Ї–Њ–є –і–Є—Б—Д—Г–љ–Ї—Ж–Є–Є –°–Ю, –Њ—Б–Њ–±–µ–љ–љ–Њ –њ—А–Є –љ–µ–≤–Њ–Ј–Љ–Њ–ґ–љ–Њ—Б—В–Є –≤—Л–њ–Њ–ї–љ–µ–љ–Є—П —Н–љ–і–Њ—Б–Ї–Њ–њ–Є—З–µ—Б–Ї–Њ–є –Љ–∞–љ–Њ–Љ–µ—В—А–Є–Є.
–Я–Њ—Б–ї–µ –њ—А–Є–µ–Љ–∞ –ґ–Є—А–љ–Њ–є –њ–Є—Й–Є –љ–Њ—А–Љ–∞–ї—М–љ–Њ–µ —А–∞—Б—Б–ї–∞–±–ї–µ–љ–Є–µ –°–Ю –і–Њ–ї–ґ–љ–Њ –њ—А–Є–≤–Њ–і–Є—В—М –Ї —Г–≤–µ–ї–Є—З–µ–љ–Є—О –Њ—В—В–Њ–Ї–∞ –ґ–µ–ї—З–Є –≤ –і–≤–µ–љ–∞–і—Ж–∞—В–Є–њ–µ—А—Б—В–љ—Г—О –Ї–Є—И–Ї—Г (–≤—Б–ї–µ–і—Б—В–≤–Є–µ –≤—Л–і–µ–ї–µ–љ–Є—П —Е–Њ–ї–µ—Ж–Є—Б—В–Њ–Ї–Є–љ–Є–љ–∞), –њ—А–Є —Н—В–Њ–Љ –і–Є–∞–Љ–µ—В—А –Њ–±—Й–µ–≥–Њ –ґ–µ–ї—З–љ–Њ–≥–Њ –њ—А–Њ—В–Њ–Ї–∞ –і–Њ–ї–ґ–µ–љ —Г–Љ–µ–љ—М—И–∞—В—М—Б—П. –£–≤–µ–ї–Є—З–µ–љ–Є–µ –і–Є–∞–Љ–µ—В—А–∞ –Њ–±—Й–µ–≥–Њ –ґ–µ–ї—З–љ–Њ–≥–Њ –њ—А–Њ—В–Њ–Ї–∞ –њ–Њ—Б–ї–µ –њ—А–Є–µ–Љ–∞ –ґ–Є—А–љ–Њ–є –њ–Є—Й–Є –њ–Њ –і–∞–љ–љ—Л–Љ —Г–ї—М—В—А–∞–Ј–≤—Г–Ї–Њ–≤–Њ–≥–Њ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П –Њ—В—А–∞–ґ–∞–µ—В –љ–∞—А—Г—И–µ–љ–Є—П –Њ—В—В–Њ–Ї–∞ –ґ–µ–ї—З–Є, —З—В–Њ –Љ–Њ–ґ–µ—В —Б–≤–Є–і–µ—В–µ–ї—М—Б—В–≤–Њ–≤–∞—В—М –Њ –љ–∞–ї–Є—З–Є–Є –У–°–Ю [4]. –£–≤–µ–ї–Є—З–µ–љ–Є–µ –і–Є–∞–Љ–µ—В—А–∞ –њ–∞–љ–Ї—А–µ–∞—В–Є—З–µ—Б–Ї–Њ–≥–Њ –њ—А–Њ—В–Њ–Ї–∞ –њ–Њ—Б–ї–µ —Б—В–Є–Љ—Г–ї—П—Ж–Є–Є —Б–µ–Ї—А–µ—В–Є–љ–Њ–Љ –Є–ї–Є –≤–Њ –≤—А–µ–Љ—П —В–µ—Б—В–∞ –Э–∞—А–і–Є –Љ–Њ–ґ–µ—В –≥–Њ–≤–Њ—А–Є—В—М –Њ –≥–Є–њ–µ—А—В–µ–љ–Ј–Є–Є –њ–∞–љ–Ї—А–µ–∞—В–Є—З–µ—Б–Ї–Њ–≥–Њ —Б–µ–≥–Љ–µ–љ—В–∞ –°–Ю.
–Ь–∞–љ–Њ–Љ–µ—В—А–Є—П –°–Ю –Љ–Њ–ґ–µ—В —Б–ї—Г–ґ–Є—В—М «–Ј–Њ–ї–Њ—В—Л–Љ —Б—В–∞–љ–і–∞—А—В–Њ–Љ» –і–Є–∞–≥–љ–Њ—Б—В–Є–Ї–Є –і–≤–Є–≥–∞—В–µ–ї—М–љ—Л—Е —А–∞—Б—Б—В—А–Њ–є—Б—В–≤ –°–Ю. –†–µ–Ј—Г–ї—М—В–∞—В –Љ–∞–љ–Њ–Љ–µ—В—А–Є—З–µ—Б–Ї–Њ–≥–Њ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П –°–Ю —Б—З–Є—В–∞—О—В –њ–∞—В–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є–Љ –њ—А–Є –±–∞–Ј–∞–ї—М–љ–Њ–Љ –і–∞–≤–ї–µ–љ–Є–Є –°–Ю –≤—Л—И–µ 30–40 –Љ–Љ —А—В.—Б—В. –Ї–∞–Ї –і–ї—П –ґ–µ–ї—З–љ–Њ–≥–Њ, —В–∞–Ї –Є –і–ї—П –њ–∞–љ–Ї—А–µ–∞—В–Є—З–µ—Б–Ї–Њ–≥–Њ —Б–µ–≥–Љ–µ–љ—В–∞ –°–Ю. –°—А–µ–і–Є –±–Њ–ї—М–љ—Л—Е, —Г –Ї–Њ—В–Њ—А—Л—Е –љ–∞ –Њ—Б–љ–Њ–≤–∞–љ–Є–Є –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є—Е –і–∞–љ–љ—Л—Е –±—Л–ї–∞ —Г—Б—В–∞–љ–Њ–≤–ї–µ–љ–∞ –і–Є—Б–Ї–Є–љ–µ–Ј–Є—П –°–Ю, 78% –Є–Љ–µ–ї–Є –њ–Њ –Ї—А–∞–є–љ–µ–є –Љ–µ—А–µ –Њ–і–љ–Њ –Є–Ј —Б–ї–µ–і—Г—О—Й–Є—Е –љ–∞—А—Г—И–µ–љ–Є–є:
1. –Т—Л—Б–Њ–Ї–Њ—З–∞—Б—В–Њ—В–љ—Л–µ —Д–∞–Ј–љ—Л–µ —Б–Њ–Ї—А–∞—Й–µ–љ–Є—П (—В–∞—Е–Є–Њ–і–і–Є—П).
2. –Я—А–µ—Е–Њ–і—П—Й–Є–µ —Н–њ–Є–Ј–Њ–і—Л –њ–Њ–≤—Л—И–µ–љ–Є—П –±–∞–Ј–∞–ї—М–љ–Њ–≥–Њ –і–∞–≤–ї–µ–љ–Є—П –°–Ю.
3. –Ш–Ј–±—Л—В–Њ—З–љ—Л–µ —А–µ—В—А–Њ–≥—А–∞–і–љ—Л–µ —Б–Њ–Ї—А–∞—Й–µ–љ–Є—П.
4. –Я–∞—А–∞–і–Њ–Ї—Б–∞–ї—М–љ—Л–є –Њ—В–≤–µ—В –°–Ю –љ–∞ —Е–Њ–ї–µ—Ж–Є—Б—В–Њ–Ї–Є–љ–Є–љ.
–≠—В–Є –љ–∞—А—Г—И–µ–љ–Є—П –Љ–Њ–ґ–љ–Њ —Б—З–Є—В–∞—В—М —Б–∞–Љ–Њ—Б—В–Њ—П—В–µ–ї—М–љ—Л–Љ–Є —А–∞—Б—Б—В—А–Њ–є—Б—В–≤–∞–Љ–Є –Є–ї–Є —А–∞–Ј–ї–Є—З–љ—Л–Љ–Є –њ—А–Њ—П–≤–ї–µ–љ–Є—П–Љ–Є –Њ–і–љ–Њ–≥–Њ –Є —В–Њ–≥–Њ –ґ–µ —Д—Г–љ–Ї—Ж–Є–Њ–љ–∞–ї—М–љ–Њ–≥–Њ –љ–∞—А—Г—И–µ–љ–Є—П –°–Ю, –Њ–±—Л—З–љ–Њ –љ–∞–Ј—Л–≤–∞–µ–Љ–Њ–≥–Њ –У–°–Ю. –Я–Њ—Б–ї–µ–і–љ—П—П —В–Њ—З–Ї–∞ –Ј—А–µ–љ–Є—П –њ–Њ–і–і–µ—А–ґ–Є–≤–∞–µ—В—Б—П —В–µ–Љ —Д–∞–Ї—В–Њ–Љ, —З—В–Њ –±–Њ–ї—М, –≤–Њ–Ј–љ–Є–Ї–∞—О—Й–∞—П –≤ —А–µ–Ј—Г–ї—М—В–∞—В–µ —Б–њ–∞–Ј–Љ–∞ –Є —А–∞—Б—В—П–ґ–µ–љ–Є—П –њ—А–Њ—В–Њ–Ї–∞ –њ—А–Є –њ–Њ–≤—Л—И–µ–љ–Є–Є –±–∞–Ј–∞–ї—М–љ–Њ–≥–Њ –і–∞–≤–ї–µ–љ–Є—П –≤ –°–Ю, —П–≤–ї—П–µ—В—Б—П –Њ–±—Й–µ–є —Е–∞—А–∞–Ї—В–µ—А–Є—Б—В–Є–Ї–Њ–є –≤—Б–µ—Е —Н—В–Є—Е –љ–∞—А—Г—И–µ–љ–Є–є. –Ъ—А–Є—В–µ—А–Є–Є –і–Є–∞–≥–љ–Њ–Ј–∞ –У–°–Ю –≤–Ї–ї—О—З–∞—О—В –≤ —Б–µ–±—П:
1. –°–≤–Њ–±–Њ–і–љ–Њ–µ –Њ—В–і–µ–ї–µ–љ–Є–µ –ґ–µ–ї—З–Є –≤ –±–µ–Ј–±–Њ–ї–µ–≤—Л–µ –њ–µ—А–Є–Њ–і—Л.
2. –Ґ–Є–њ–Є—З–љ—Л–µ –±–Є–ї–Є–∞—А–љ—Л–µ –±–Њ–ї–Є –Є –њ–Њ–≤—Л—И–µ–љ–Є–µ —Г—А–Њ–≤–љ—П —В—А–∞–љ—Б–∞–Љ–Є–љ–∞–Ј –Є/–Є–ї–Є –∞–Љ–Є–ї–∞–Ј—Л, –≤—Л–Ј–≤–∞–љ–љ—Л–µ –Љ–Њ—А—Д–Є–љ–Њ–Љ, —Д–µ–љ—В–∞–љ–Є–ї–Њ–Љ –Є–ї–Є –Ї–Њ–і–µ–Є–љ–Њ–Љ.
3. –Я–Њ–ї–Њ–ґ–Є—В–µ–ї—М–љ—Л–µ —А–µ–Ј—Г–ї—М—В–∞—В—Л –£–Ч–Ш–—В–µ—Б—В–∞ –њ—А–Є –њ—А–Є–µ–Љ–µ –ґ–Є—А–љ–Њ–є –њ–Є—Й–Є, –≤–≤–µ–і–µ–љ–Є–Є —Е–Њ–ї–µ—Ж–Є—Б—В–Њ–Ї–Є–љ–Є–љ–∞ –Є–ї–Є —Б–µ–Ї—А–µ—В–Є–љ–∞.
4. –§—Г–љ–Ї—Ж–Є–Њ–љ–∞–ї—М–љ—Л–є —Б–њ–∞–Ј–Љ, –≤—Л–Ј–≤–∞–љ–љ—Л–є –Љ–Њ—А—Д–Є–љ–Њ–Љ, –Ї–Њ—В–Њ—А—Л–є –≤—Л—П–≤–ї—П–µ—В—Б—П –њ—А–Є –Ї–Њ–Љ–њ—М—О—В–µ—А–љ–Њ–є —Б—Ж–Є–љ—В–Є–≥—А–∞—Д–Є–Є –њ–µ—З–µ–љ–Є –Є –ґ–µ–ї—З–µ–≤—Л–≤–Њ–і—П—Й–Є—Е –њ—Г—В–µ–є; –њ–Њ–≤—Л—И–µ–љ–љ–Њ–µ –±–∞–Ј–∞–ї—М–љ–Њ–µ –і–∞–≤–ї–µ–љ–Є–µ –≤ –°–Ю –Є —Д–∞–Ј–љ–∞—П –≤–Њ–ї–љ–Њ–≤–∞—П –∞–Ї—В–Є–≤–љ–Њ—Б—В—М –≤–Њ –≤—А–µ–Љ—П –њ—А–Њ–≤–Њ–Ї–∞—Ж–Є–Њ–љ–љ—Л—Е –њ—А–Њ–±, –≤—Л—П–≤–ї—П–µ–Љ–∞—П —Б –њ–Њ–Љ–Њ—Й—М—О —Н–љ–і–Њ—Б–Ї–Њ–њ–Є—З–µ—Б–Ї–Њ–є –Є–ї–Є –Є–љ—В—А–∞–Њ–њ–µ—А–∞—Ж–Є–Њ–љ–љ–Њ–є –Љ–∞–љ–Њ–Љ–µ—В—А–Є–Є;
5. –†–∞—Б—Б—В—А–Њ–є—Б—В–≤–∞, –≤—Л—П–≤–ї—П–µ–Љ—Л–µ –њ—А–Є –Љ–∞–љ–Њ–Љ–µ—В—А–Є–Є –°–Ю.
–Ы–µ—З–µ–љ–Є–µ
–£ –Љ–љ–Њ–≥–Є—Е –±–Њ–ї—М–љ—Л—Е —Б 1 —В–Є–њ–Њ–Љ –і–Є—Б—Д—Г–љ–Ї—Ж–Є–Є –±–Є–ї–Є–∞—А–љ–Њ–≥–Њ —Б–µ–≥–Љ–µ–љ—В–∞ –°–Ю –Ј–љ–∞—З–Є—В–µ–ї—М–љ–Њ–≥–Њ —Г–ї—Г—З—И–µ–љ–Є—П –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Њ–є —Б–Є–Љ–њ—В–Њ–Љ–∞—В–Є–Ї–Є –Є –±–Є–Њ—Е–Є–Љ–Є—З–µ—Б–Ї–Є—Е –њ–Њ–Ї–∞–Ј–∞—В–µ–ї–µ–є —Г–і–∞–µ—В—Б—П –і–Њ—Б—В–Є—З—М –≤ —А–µ–Ј—Г–ї—М—В–∞—В–µ —Н–љ–і–Њ—Б–Ї–Њ–њ–Є—З–µ—Б–Ї–Њ–є —Б—Д–Є–љ–Ї—В–µ—А–Њ—В–Њ–Љ–Є–Є [5]. –Ю–і–љ–∞–Ї–Њ –њ–Њ–ї–Њ–ґ–Є—В–µ–ї—М–љ—Л–є —Н—Д—Д–µ–Ї—В –Њ—В —Н–љ–і–Њ—Б–Ї–Њ–њ–Є—З–µ—Б–Ї–Њ–є —Б—Д–Є–љ–Ї—В–µ—А–Њ—В–Њ–Љ–Є–Є –љ–∞–±–ї—О–і–∞–µ—В—Б—П —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –љ–Њ—А–Љ–∞–ї—М–љ—Л–Љ –і–∞–≤–ї–µ–љ–Є–µ–Љ –°–Ю, –≤ —Б–≤—П–Ј–Є —Б —З–µ–Љ –Љ–Њ–ґ–љ–Њ –њ—А–µ–і–њ–Њ–ї–Њ–ґ–Є—В—М, —З—В–Њ –Љ–∞–љ–Њ–Љ–µ—В—А–Є—П –°–Ю –љ–µ –Є–Љ–µ–µ—В 100%––љ–Њ–є –њ—А–Њ–≥–љ–Њ—Б—В–Є—З–µ—Б–Ї–Њ–є –Ј–љ–∞—З–Є–Љ–Њ—Б—В–Є. –Т –≥—А—Г–њ–њ–µ –±–Њ–ї—М–љ—Л—Е 2 —В–Є–њ–∞ –Љ–∞–љ–Њ–Љ–µ—В—А–Є—П –°–Ю –≤—Л—П–≤–Є–ї–∞ –Њ—В–Ї–ї–Њ–љ–µ–љ–Є—П –≤ 55% —Б–ї—Г—З–∞–µ–≤. –†–µ–Ј—Г–ї—М—В–∞—В—Л —Н–љ–і–Њ—Б–Ї–Њ–њ–Є—З–µ—Б–Ї–Њ–є —Б—Д–Є–љ–Ї—В–µ—А–Њ—В–Њ–Љ–Є–Є –њ–Њ–Ї–∞–Ј–∞–ї–Є, —З—В–Њ –Љ–∞–љ–Њ–Љ–µ—В—А–Є—П –°–Ю –Њ–±–ї–∞–і–∞–µ—В —Б–њ–µ—Ж–Є—Д–Є—З–љ–Њ—Б—В—М—О 76% –Є —З—Г–≤—Б—В–≤–Є—В–µ–ї—М–љ–Њ—Б—В—М—О 91% –њ—А–Є –і–Є–∞–≥–љ–Њ—Б—В–Є–Ї–µ –У–°–Ю –і–ї—П –≤—В–Њ—А–Њ–є –≥—А—Г–њ–њ—Л –њ–∞—Ж–Є–µ–љ—В–Њ–≤ [8]. –Я—А–Є —В—А–µ—В—М–µ–Љ —В–Є–њ–µ –і–Є—Б—Д—Г–љ–Ї—Ж–Є–Є —В–Њ–ї—М–Ї–Њ —Г 15–20% –њ–∞—Ж–Є–µ–љ—В–Њ–≤ –±—Л–ї–Є –≤—Л—П–≤–ї–µ–љ—Л –Њ—В–Ї–ї–Њ–љ–µ–љ–Є—П –њ—А–Є –Љ–∞–љ–Њ–Љ–µ—В—А–Є–Є CO [16,19]. –Т—Л–і–≤–Є–≥–∞–ї–∞—Б—М —В–Њ—З–Ї–∞ –Ј—А–µ–љ–Є—П, —З—В–Њ —А–∞–Ј–љ–Њ–Њ–±—А–∞–Ј–љ—Л–µ –њ–µ—А–≤–Є—З–љ—Л–µ –Љ–Њ—В–Њ—А–љ—Л–µ –љ–∞—А—Г—И–µ–љ–Є—П –Љ–Њ–≥—Г—В –≤–ї–Є—П—В—М –љ–∞ —Д—Г–љ–Ї—Ж–Є—О –°–Ю –Є –≤—Л–Ј—Л–≤–∞—В—М –Ї–ї–Є–љ–Є—З–µ—Б–Ї—Г—О –Ї–∞—А—В–Є–љ—Г –±–Є–ї–Є–∞—А–љ–Њ–є –Ї–Њ–ї–Є–Ї–Є –Є/–Є–ї–Є —З–∞—Б—В–Є—З–љ–Њ–є –љ–µ–њ—А–Њ—Е–Њ–і–Є–Љ–Њ—Б—В–Є –ґ–µ–ї—З–µ–≤—Л–≤–Њ–і—П—Й–Є—Е –њ—Г—В–µ–є.
–Т –±–Њ–ї—М—И–Є–љ—Б—В–≤–µ —Б–ї—Г—З–∞–µ–≤ –±–Њ–ї—М–љ—Л–µ —Б –Ф–†–С–Ґ —В—А–µ–±—Г—О—В –і–ї–Є—В–µ–ї—М–љ–Њ–≥–Њ –∞–Љ–±—Г–ї–∞—В–Њ—А–љ–Њ–≥–Њ –ї–µ—З–µ–љ–Є—П, –љ–∞–њ—А–Є–Љ–µ—А, –њ–∞—Ж–Є–µ–љ—В—Л —Б 3 —В–Є–њ–Њ–Љ –і–Є—Б—Д—Г–љ–Ї—Ж–Є–Є –°–Ю. –Я—А–Є –љ–∞–ї–Є—З–Є–Є –љ–µ–≤—А–Њ—В–Є—З–µ—Б–Ї–Є—Е —А–∞—Б—Б—В—А–Њ–є—Б—В–≤ –њ—А–Є–Љ–µ–љ—П—О—В—Б—П —Б–µ–і–∞—В–Є–≤–љ—Л–µ –Є–ї–Є —В–Њ–љ–Є–Ј–Є—А—Г—О—Й–Є–µ —Б—А–µ–і—Б—В–≤–∞, –њ—А–µ–њ–∞—А–∞—В—Л, –љ–Њ—А–Љ–∞–ї–Є–Ј—Г—О—Й–Є–µ —Б–Њ–љ. –Т–∞–ґ–љ–Њ–µ –Ј–љ–∞—З–µ–љ–Є–µ –Є–Љ–µ–µ—В –і–Є–µ—В–∞: —З–∞—Б—В—Л–є, –і—А–Њ–±–љ—Л–є –њ—А–Є–µ–Љ –њ–Є—Й–Є (5–6 —А–∞–Ј –≤ —Б—Г—В–Ї–Є) —Б–њ–Њ—Б–Њ–±—Б—В–≤—Г–µ—В —А–µ–≥—Г–ї—П—А–љ–Њ–Љ—Г –Њ–њ–Њ—А–Њ–ґ–љ–µ–љ–Є—О –ґ–µ–ї—З–љ–Њ–≥–Њ –њ—Г–Ј—Л—А—П –Є –њ—А–Њ—В–Њ–Ї–Њ–≤–Њ–є —Б–Є—Б—В–µ–Љ—Л. –Ш–Ј —А–∞—Ж–Є–Њ–љ–∞ –Є—Б–Ї–ї—О—З–∞—О—В –∞–ї–Ї–Њ–≥–Њ–ї—М–љ—Л–µ –љ–∞–њ–Є—В–Ї–Є, –≥–∞–Ј–Є—А–Њ–≤–∞–љ–љ—Г—О –≤–Њ–і—Г, –Ї–Њ–њ—З–µ–љ—Л–µ, –ґ–Є—А–љ—Л–µ –Є –ґ–∞—А–µ–љ—Л–µ –±–ї—О–і–∞ –Є –њ—А–Є–њ—А–∞–≤—Л. –Я—А–Є –≥–Є–њ–µ—А–Ї–Є–љ–µ—В–Є—З–µ—Б–Ї–Њ–Љ —В–Є–њ–µ –і–Є—Б—Д—Г–љ–Ї—Ж–Є–Є –Њ–≥—А–∞–љ–Є—З–Є–≤–∞—О—В –њ—А–Њ–і—Г–Ї—В—Л, —Б—В–Є–Љ—Г–ї–Є—А—Г—О—Й–Є–µ —Б–Њ–Ї—А–∞—Й–µ–љ–Є—П –ґ–µ–ї—З–љ–Њ–≥–Њ –њ—Г–Ј—Л—А—П, – –ґ–Є–≤–Њ—В–љ—Л–µ –ґ–Є—А—Л, —А–∞—Б—В–Є—В–µ–ї—М–љ—Л–µ –Љ–∞—Б–ї–∞, –±—Г–ї—М–Њ–љ—Л. –Я—А–Є –≥–Є–њ–Њ—В–Њ–љ–Є–Є –ґ–µ–ї—З–љ–Њ–≥–Њ –њ—Г–Ј—Л—А—П –Љ–Њ–ґ–љ–Њ –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞—В—М —А–∞—Б—В–Є—В–µ–ї—М–љ–Њ–µ –Љ–∞—Б–ї–Њ (–њ–Њ –Њ–і–љ–Њ–є —Б—В–Њ–ї–Њ–≤–Њ–є –ї–Њ–ґ–Ї–µ 2–3 —А–∞–Ј–∞ –≤ –і–µ–љ—М –Ј–∞ 15 –Љ–Є–љ. –і–Њ –µ–і—Л –≤ —В–µ—З–µ–љ–Є–µ 2–3 –љ–µ–і).
–Ъ–∞–Ї –њ–Њ–Ї–∞–Ј—Л–≤–∞—О—В –њ—А–Њ–≤–Њ–Ї–∞—Ж–Є–Њ–љ–љ—Л–µ –њ—А–Њ–±—Л, –Њ—Б–љ–Њ–≤–љ–∞—П –њ—А–Њ–±–ї–µ–Љ–∞ –њ—А–Є –≥–Є–њ–µ—А—В–Њ–љ–Є—З–µ—Б–Ї–Є—Е —А–∞—Б—Б—В—А–Њ–є—Б—В–≤–∞—Е —Б—Д–Є–љ–Ї—В–µ—А–∞ –Ю–і–і–Є –Ј–∞–Ї–ї—О—З–∞–µ—В—Б—П –≤ –њ–Њ–≤—Л—И–µ–љ–љ–Њ–є —З—Г–≤—Б—В–≤–Є—В–µ–ї—М–љ–Њ—Б—В–Є —Б—В–µ–љ–Ї–Є –њ–∞–љ–Ї—А–µ–∞—В–Є—З–µ—Б–Ї–Њ–≥–Њ –Є –ґ–µ–ї—З–љ–Њ–≥–Њ –њ—А–Њ—В–Њ–Ї–Њ–≤ –Ї –Є–Ј–Љ–µ–љ–µ–љ–Є—П–Љ –Њ–±—К–µ–Љ–∞ –Є –і–∞–≤–ї–µ–љ–Є—П, –њ—А–µ–і–њ–Њ–ї–Њ–ґ–Є—В–µ–ї—М–љ–Њ –Є–Ј––Ј–∞ –њ–Њ–љ–Є–ґ–µ–љ–љ–Њ–є —А–∞—Б—В—П–ґ–Є–Љ–Њ—Б—В–Є —Б—В–µ–љ–Ї–Є –ґ–µ–ї—З–љ–Њ–≥–Њ –њ—А–Њ—В–Њ–Ї–∞ –Є–ї–Є –љ–∞—А—Г—И–µ–љ–Є–є —А–µ–≥—Г–ї—П—Ж–Є–Є. –Я–Њ—Б–Ї–Њ–ї—М–Ї—Г —В—А–Є–≥–≥–µ—А–љ–∞—П –Ј–Њ–љ–∞ –≤–Њ–Ј–љ–Є–Ї–љ–Њ–≤–µ–љ–Є—П –±–Њ–ї–Є –љ–∞—Е–Њ–і–Є—В—Б—П –≤ –Њ–±–ї–∞—Б—В–Є –°–Ю –Є –њ—А–Њ—В–Њ–Ї–Њ–≤–Њ–є —Б–Є—Б—В–µ–Љ–µ, –ї–µ—З–µ–±–љ–∞—П —В–∞–Ї—В–Є–Ї–∞ –њ—А–Є –±–Њ–ї–µ–≤—Л—Е –њ—А–Є—Б—В—Г–њ–∞—Е –і–ї–Є—В–µ–ї—М–љ–Њ–µ –≤—А–µ–Љ—П —Б–≤–Њ–і–Є–ї–∞—Б—М –Ї –Љ–µ—А–∞–Љ –њ–Њ –і–µ–Ї–Њ–Љ–њ—А–µ—Б—Б–Є–Є –°–Ю.
–Т—Б–µ –±–Њ–ї–µ–µ —И–Є—А–Њ–Ї–Њ–µ –њ—А–Є–Љ–µ–љ–µ–љ–Є–µ —Г –±–Њ–ї—М–љ—Л—Е —Б –Ф–†–С–Ґ –≤ –њ–Њ—Б–ї–µ–і–љ–Є–µ –≥–Њ–і—Л –љ–∞—Е–Њ–і–Є—В –Ф—О—Б–њ–∞—В–∞–ї–Є–љ (–Љ–µ–±–µ–≤–µ—А–Є–љ–∞ –≥–Є–і—А–Њ—Е–ї–Њ—А–Є–і). –Я–Њ —Е–Є–Љ–Є—З–µ—Б–Ї–Њ–Љ—Г —Б—В—А–Њ–µ–љ–Є—О –Љ–µ–±–µ–≤–µ—А–Є–љ–∞ –≥–Є–і—А–Њ—Е–ї–Њ—А–Є–і —П–≤–ї—П–µ—В—Б—П –њ—А–Њ–Є–Ј–≤–Њ–і–љ—Л–Љ –Љ–µ—В–Њ–Ї—Б–Є–±–µ–љ–Ј–∞–Љ–Є–љ–∞, –њ–Њ –Љ–µ—Е–∞–љ–Є–Ј–Љ—Г –і–µ–є—Б—В–≤–Є—П – –±–ї–Њ–Ї–∞—В–Њ—А–Њ–Љ –љ–∞—В—А–Є–µ–≤—Л—Е –Ї–∞–љ–∞–ї–Њ–≤. –Я—А–µ–њ–∞—А–∞—В –њ—А–µ–і–Њ—В–≤—А–∞—Й–∞–µ—В –њ–Њ—Б–ї–µ–і–Њ–≤–∞—В–µ–ї—М–љ–Њ–µ —В–µ—З–µ–љ–Є–µ –њ—А–Њ—Ж–µ—Б—Б–Њ–≤, –њ—А–Є–≤–Њ–і—П—Й–Є—Е –Ї –Љ—Л—И–µ—З–љ–Њ–Љ—Г —Б–њ–∞–Ј–Љ—Г, –≤–Њ–Ј–і–µ–є—Б—В–≤—Г—П —В–µ–Љ —Б–∞–Љ—Л–Љ –љ–∞ –њ–Њ—Б–ї–µ–і–љ–µ–µ –Ј–≤–µ–љ–Њ –њ–∞—В–Њ–≥–µ–љ–µ–Ј–∞ –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П. –Ф—О—Б–њ–∞—В–∞–ї–Є–љ –±–ї–Њ–Ї–Є—А—Г–µ—В –љ–∞—В—А–Є–µ–≤—Л–µ –Ї–∞–љ–∞–ї—Л –Ї–ї–µ—В–Њ—З–љ–Њ–є –Љ–µ–Љ–±—А–∞–љ—Л, –≤ —Б–≤—П–Ј–Є —Б —З–µ–Љ –њ–Њ—Б—В—Г–њ–ї–µ–љ–Є–µ –≤ –Ї–ї–µ—В–Ї—Г –Є–Њ–љ–Њ–≤ –љ–∞—В—А–Є—П, –∞ —Б–ї–µ–і–Њ–≤–∞—В–µ–ї—М–љ–Њ, –Є –Ї–∞–ї—М—Ж–Є—П —Б—В–∞–љ–Њ–≤–Є—В—Б—П –љ–µ–≤–Њ–Ј–Љ–Њ–ґ–љ—Л–Љ; –≤—Б–ї–µ–і—Б—В–≤–Є–µ —Н—В–Є—Е –њ—А–Њ—Ж–µ—Б—Б–Њ–≤ –Ј–љ–∞—З–Є—В–µ–ї—М–љ–Њ —Г–Љ–µ–љ—М—И–∞–µ—В—Б—П —Б–Є–ї–∞ –Љ—Л—И–µ—З–љ–Њ–≥–Њ —Б–Њ–Ї—А–∞—Й–µ–љ–Є—П. –Ъ—А–Њ–Љ–µ —В–Њ–≥–Њ, –њ—А–µ–њ–∞—А–∞—В –±–ї–Њ–Ї–Є—А—Г–µ—В –≤–Њ—Б–њ–Њ–ї–љ–µ–љ–Є–µ –і–µ–њ–Њ –Ї–∞–ї—М—Ж–Є—П –Є–Ј –≤–љ–µ–Ї–ї–µ—В–Њ—З–љ–Њ–≥–Њ –њ—А–Њ—Б—В—А–∞–љ—Б—В–≤–∞, –Њ–≥—А–∞–љ–Є—З–Є–≤–∞—П —В–µ–Љ —Б–∞–Љ—Л–Љ –≤—Л—Е–Њ–і –Ї–∞–ї–Є—П –Є–Ј –Ї–ї–µ—В–Ї–Є –Є –њ—А–µ–і–Њ—В–≤—А–∞—Й–∞—П —А–∞–Ј–≤–Є—В–Є–µ –≥–Є–њ–Њ—В–Њ–љ–Є–Є.
–Я–Њ—Б–ї–µ –њ—А–Є–µ–Љ–∞ per os –Ф—О—Б–њ–∞—В–∞–ї–Є–љ –Љ–µ—В–∞–±–Њ–ї–Є–Ј–Є—А—Г–µ—В—Б—П –≤ —Б—В–µ–љ–Ї–µ –Ї–Є—И–µ—З–љ–Є–Ї–∞ –Є –њ–µ—З–µ–љ–Є –і–Њ –љ–µ–∞–Ї—В–Є–≤–љ—Л—Е –Љ–µ—В–∞–±–Њ–ї–Є—В–Њ–≤. –Ь–∞–Ї—Б–Є–Љ–∞–ї—М–љ—Л–є —Г—А–Њ–≤–µ–љ—М –µ–≥–Њ –љ–µ–∞–Ї—В–Є–≤–љ–Њ–≥–Њ –Љ–µ—В–∞–±–Њ–ї–Є—В–∞ –≤–µ—А–∞—В–Њ–≤–Њ–є –Ї–Є—Б–ї–Њ—В—Л –Њ–њ—А–µ–і–µ–ї—П–µ—В—Б—П –≤ –њ–ї–∞–Ј–Љ–µ –Ї—А–Њ–≤–Є —З–µ—А–µ–Ј 1,5 —З–∞—Б–∞ –њ–Њ—Б–ї–µ –њ—А–Є–µ–Љ–∞. –Т—Л–≤–Њ–і—П—В—Б—П –Љ–µ—В–∞–±–Њ–ї–Є—В—Л –Ф—О—Б–њ–∞—В–∞–ї–Є–љ–∞ —Б –Љ–Њ—З–Њ–є –≤ —В–µ—З–µ–љ–Є–µ 24 —З–∞—Б–Њ–≤, —В–∞–Ї–Є–Љ –Њ–±—А–∞–Ј–Њ–Љ, –Ї—Г–Љ—Г–ї—П—Ж–Є–Є –њ—А–µ–њ–∞—А–∞—В–∞ –≤ –Њ—А–≥–∞–љ–Є–Ј–Љ–µ –љ–µ –љ–∞–±–ї—О–і–∞–µ—В—Б—П. –Ъ–Њ–љ—В—А–Њ–ї–Є—А—Г–µ–Љ—Л–µ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П, –≤—Л–њ–Њ–ї–љ–µ–љ–љ—Л–µ —Б –њ–Њ–Љ–Њ—Й—М—О –і–≤–Њ–є–љ–Њ–≥–Њ–—Б–ї–µ–њ–Њ–≥–Њ –Љ–µ—В–Њ–і–∞ –њ–Њ–Ї–∞–Ј—Л–≤–∞—О—В, —З—В–Њ —В–µ—А–∞–њ–µ–≤—В–Є—З–µ—Б–Ї–∞—П –і–Њ–Ј–∞ –Ф—О—Б–њ–∞—В–∞–ї–Є–љ–∞ –Њ–±–µ—Б–њ–µ—З–Є–≤–∞–µ—В —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ–µ —Б–њ–∞–Ј–Љ–Њ–ї–Є—В–Є—З–µ—Б–Ї–Њ–µ –і–µ–є—Б—В–≤–Є–µ, –±—Л—Б—В—А–Њ –Ї—Г–њ–Є—А—Г–µ—В —Б–Є–Љ–њ—В–Њ–Љ—Л –≥–Є–њ–µ—А—В–Њ–љ–Є—З–µ—Б–Ї–Є—Е —А–∞—Б—Б—В—А–Њ–є—Б—В–≤ –ґ–µ–ї—З–µ–≤—Л–≤–Њ–і—П—Й–Є—Е –њ—Г—В–µ–є: –±–Њ–ї–Є –≤ –њ—А–∞–≤–Њ–Љ –њ–Њ–і—А–µ–±–µ—А—М–µ, —В–Њ—И–љ–Њ—В—Г, –Љ–µ—В–µ–Њ—А–Є–Ј–Љ.
–Я–Њ –і–∞–љ–љ—Л–Љ –Ю.–Э. –Ь–Є–љ—Г—И–Ї–Є–љ–∞ (2002), –њ–Њ–ї–Њ–ґ–Є—В–µ–ї—М–љ—Л–є –Њ—В–≤–µ—В –љ–∞ —В–µ—А–∞–њ–Є—О –Ф—О—Б–њ–∞—В–∞–ї–Є–љ–Њ–Љ –љ–∞–±–ї—О–і–∞–µ—В—Б—П —Г 90% –±–Њ–ї—М–љ—Л—Е –Ф–†–С–Ґ. –Э–∞ —Д–Њ–љ–µ –њ—А–Є–µ–Љ–∞ –Ф—О—Б–њ–∞—В–∞–ї–Є–љ–∞ —Б—В–Є—Е–∞–љ–Є–µ –±–Њ–ї–µ–є –≤ –њ—А–∞–≤–Њ–Љ –њ–Њ–і—А–µ–±–µ—А—М–µ –љ–∞–±–ї—О–і–∞–µ—В—Б—П —Г–ґ–µ —З–µ—А–µ–Ј 14 –і–љ–µ–є —Г –Ј–љ–∞—З–Є—В–µ–ї—М–љ–Њ–є —З–∞—Б—В–Є –±–Њ–ї—М–љ—Л—Е –ґ–µ–ї—З–љ–Њ–Ї–∞–Љ–µ–љ–љ–Њ–є –±–Њ–ї–µ–Ј–љ—М—О (85%), –њ–Њ—Б—В—Е–Њ–ї–µ—Ж–Є—Б—В—Н–Ї—В–Њ–Љ–љ—Л–Љ —Б–Є–љ–і—А–Њ–Љ–Њ–Љ (40%). –Я–Њ –і–∞–љ–љ—Л–Љ —Г–ї—М—В—А–∞–Ј–≤—Г–Ї–Њ–≤–Њ–≥–Њ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П –Є–Ј 11 –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –Я–•–≠–°, –Є—Б—Е–Њ–і–љ–Њ –Є–Љ–µ–≤—И–Є—Е —А–∞—Б—И–Є—А–µ–љ–љ—Л–є –Њ—В 9 –і–Њ 14 –Љ–Љ –Њ–±—Й–Є–є –ґ–µ–ї—З–љ—Л–є –њ—А–Њ—В–Њ–Ї, —Г 5 –њ–Њ –Є—Б—В–µ—З–µ–љ–Є–Є 14––і–љ–µ–≤–љ–Њ–є —В–µ—А–∞–њ–Є–Є –Ф—О—Б–њ–∞—В–∞–ї–Є–љ–Њ–Љ –љ–∞–±–ї—О–і–∞–ї–∞—Б—М –љ–Њ—А–Љ–∞–ї–Є–Ј–∞—Ж–Є—П –µ–≥–Њ —И–Є—А–Є–љ—Л (–Ш–ї—М—З–µ–љ–Ї–Њ –Р.–Р., 2003).
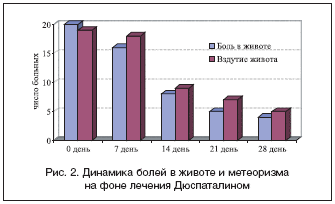
–Т –љ–∞—И–µ–є –Ї–ї–Є–љ–Є–Ї–µ –Љ—Л –њ—А–Є–Љ–µ–љ—П–ї–Є –Љ–µ–±–µ–≤–µ—А–Є–љ –≤ –∞–Љ–±—Г–ї–∞—В–Њ—А–љ—Л—Е –Є —Б—В–∞—Ж–Є–Њ–љ–∞—А–љ—Л—Е —Г—Б–ї–Њ–≤–Є—П—Е —Г –±–Њ–ї—М–љ—Л—Е —Б –≥–Є–њ–µ—А—В–Њ–љ–Є—З–µ—Б–Ї–Є–Љ–Є —А–∞—Б—Б—В—А–Њ–є—Б—В–≤–∞–Љ–Є –ґ–µ–ї—З–µ–≤—Л–≤–Њ–і—П—Й–Є—Е –њ—Г—В–µ–є –њ—А–Є –Њ—В—Б—Г—В—Б—В–≤–Є–Є –ґ–µ–ї—З–љ–Њ–Ї–∞–Љ–µ–љ–љ–Њ–є –±–Њ–ї–µ–Ј–љ–Є. –£ –±–Њ–ї—М—И–Є–љ—Б—В–≤–∞ –њ–∞—Ж–Є–µ–љ—В–Њ–≤ –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є–є —Н—Д—Д–µ–Ї—В –±—Л–ї –і–Њ—Б—В–Є–≥–љ—Г—В –њ—А–Є –љ–∞–Ј–љ–∞—З–µ–љ–Є–Є –њ—А–µ–њ–∞—А–∞—В–∞ –≤ –і–Њ–Ј–µ 200 –Љ–≥ —Е 2 —А–∞–Ј–∞ –≤ —Б—Г—В–Ї–Є –≤ —В–µ—З–µ–љ–Є–µ 4–6 –љ–µ–і–µ–ї—М. –Т —В–Њ –ґ–µ –≤—А–µ–Љ—П –њ—А–Є –љ–∞–ї–Є—З–Є–Є –≥–Є–њ–µ—А—В–Њ–љ–Є—З–µ—Б–Ї–Є—Е —А–∞—Б—Б—В—А–Њ–є—Б—В–≤ –љ–µ —В–Њ–ї—М–Ї–Њ –±–Є–ї–Є–∞—А–љ–Њ–≥–Њ, –љ–Њ –Є –њ–∞–љ–Ї—А–µ–∞—В–Є—З–µ—Б–Ї–Њ–≥–Њ —Б–µ–≥–Љ–µ–љ—В–∞ —Б—Д–Є–љ–Ї—В–µ—А–∞ –њ–Њ–Ї–∞–Ј–∞–љ–Њ –і–≤—Г—Е–Ї—А–∞—В–љ–Њ–µ —Г–≤–µ–ї–Є—З–µ–љ–Є–µ –і–Њ–Ј—Л –≤ —В–µ—З–µ–љ–Є–µ –њ–µ—А–≤—Л—Е 7–10 –і–љ–µ–є —В–µ—А–∞–њ–Є–Є. –°–љ–Є–ґ–µ–љ–Є–µ –Є–љ—В–µ–љ—Б–Є–≤–љ–Њ—Б—В–Є –±–Њ–ї–Є –≤ –њ—А–∞–≤–Њ–Љ –њ–Њ–і—А–µ–±–µ—А—М–µ –Є —В–Њ—И–љ–Њ—В—Л –љ–∞–±–ї—О–і–∞–µ—В—Б—П —Г –±–Њ–ї—М–љ—Л—Е —Б 4–5 –і–љ—П —В–µ—А–∞–њ–Є–Є, –≤ –±–Њ–ї–µ–µ –њ–Њ–Ј–і–љ–Є–µ —Б—А–Њ–Ї–Є –њ—А–Њ–Є—Б—Е–Њ–і–Є—В —Б–љ–Є–ґ–µ–љ–Є–µ –≤—Л—А–∞–ґ–µ–љ–љ–Њ—Б—В–Є –≤–Ј–і—Г—В–Є—П –ґ–Є–≤–Њ—В–∞ (—З—В–Њ –Љ–Њ–ґ–љ–Њ –Њ–±—К—П—Б–љ–Є—В—М –љ–Њ—А–Љ–∞–ї–Є–Ј–∞—Ж–Є–µ–є –Њ—В—В–Њ–Ї–∞ –ґ–µ–ї—З–Є –Є –Љ–Њ—В–Њ—А–Є–Ї–Є –Ї–Є—И–µ—З–љ–Є–Ї–∞). –І–µ—А–µ–Ј 2 –љ–µ–і–µ–ї–Є —В–µ—А–∞–њ–Є–Є –±–Њ–ї—М –Є—Б—З–µ–Ј–∞–µ—В —Г –њ–Њ–ї–Њ–≤–Є–љ—Л –њ–∞—Ж–Є–µ–љ—В–Њ–≤ (—А–Є—Б. 2). –Я—А–Є –њ–Њ–≤—В–Њ—А–љ–Њ–Љ —Г–ї—М—В—А–∞–Ј–≤—Г–Ї–Њ–≤–Њ–Љ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є –Њ—А–≥–∞–љ–Њ–≤ –±—А—О—И–љ–Њ–є –њ–Њ–ї–Њ—Б—В–Є, –Ї–Њ—В–Њ—А–Њ–µ –њ—А–Њ–≤–Њ–і–Є–ї–Њ—Б—М –љ–∞ —Н—В–Њ–Љ —Б—А–Њ–Ї–µ —Г 11 –Є–Ј 18 –±–Њ–ї—М–љ—Л—Е (61%), –љ–∞–±–ї—О–і–∞–ї–Њ—Б—М —Г–Љ–µ–љ—М—И–µ–љ–Є–µ —А–∞–Ј–Љ–µ—А–Њ–≤ –ґ–µ–ї—З–љ–Њ–≥–Њ –њ—Г–Ј—Л—А—П, –њ—А–Є —Н—В–Њ–Љ —Г 9 –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —А–∞–Ј–Љ–µ—А—Л —Б—В–∞–ї–Є –љ–Њ—А–Љ–∞–ї—М–љ—Л–Љ–Є. –Ґ–∞–Ї–Є–Љ –Њ–±—А–∞–Ј–Њ–Љ, –Љ–µ–±–µ–≤–µ—А–Є–љ —Б–њ–Њ—Б–Њ–±—Б—В–≤—Г–µ—В —А–∞–Ј—А–µ—И–µ–љ–Є—О —Б–њ–∞–Ј–Љ–∞, –љ–µ –љ–∞—А—Г—И–∞—П —Б–Њ–Ї—А–∞—В–Є—В–µ–ї—М–љ–Њ–є —Д—Г–љ–Ї—Ж–Є–Є –ґ–µ–ї—З–љ–Њ–≥–Њ –њ—Г–Ј—Л—А—П, —З—В–Њ –Њ—З–µ–љ—М –≤–∞–ґ–љ–Њ —Г —Н—В–Њ–є –≥—А—Г–њ–њ—Л –њ–∞—Ж–Є–µ–љ—В–Њ–≤.
–Ш—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П, –њ–Њ—Б–≤—П—Й–µ–љ–љ—Л–µ –Њ—Ж–µ–љ–Ї–µ –±–µ–Ј–Њ–њ–∞—Б–љ–Њ—Б—В–Є –Є –њ–µ—А–µ–љ–Њ—Б–Є–Љ–Њ—Б—В–Є –Ф—О—Б–њ–∞—В–∞–ї–Є–љ–∞, –њ—А–Њ–≤–Њ–і–Є–ї–Є—Б—М –±–Њ–ї–µ–µ —З–µ–Љ —Г 3500 –±–Њ–ї—М–љ—Л—Е, –Є –≤–Њ –≤—Б–µ—Е –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П—Е –њ—А–µ–њ–∞—А–∞—В —Е–Њ—А–Њ—И–Њ –њ–µ—А–µ–љ–Њ—Б–Є–ї—Б—П –±–Њ–ї—М–љ—Л–Љ–Є. –С–Њ–ї—М—И–Є–љ—Б—В–≤–Њ –∞–≤—В–Њ—А–Њ–≤ –љ–µ –Њ—В–Љ–µ—З–∞–ї–Є —А–∞–Ј–≤–Є—В–Є—П –њ–Њ–±–Њ—З–љ—Л—Е —Н—Д—Д–µ–Ї—В–Њ–≤, –і–∞–ґ–µ –њ—А–Є —Г–≤–µ–ї–Є—З–µ–љ–Є–Є –µ–≥–Њ –і–Њ–Ј—Л. –Ґ–∞–Ї, –±—Л–ї–Њ –Њ—В–Љ–µ—З–µ–љ–Њ, —З—В–Њ –Ф—О—Б–њ–∞—В–∞–ї–Є–љ –љ–µ –∞–Ї—В–Є–≤–µ–љ –≤ –Њ—В–љ–Њ—И–µ–љ–Є–Є –∞–≤—В–Њ–љ–Њ–Љ–љ–Њ–є –љ–µ—А–≤–љ–Њ–є —Б–Є—Б—В–µ–Љ—Л, –љ–µ –≤—Л–Ј—Л–≤–∞–µ—В –≥–µ–Љ–∞—В–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є—Е –Є –±–Є–Њ—Е–Є–Љ–Є—З–µ—Б–Ї–Є—Е –Є–Ј–Љ–µ–љ–µ–љ–Є–є, –љ–µ –Є–Љ–µ–µ—В —В–Є–њ–Є—З–љ—Л—Е –∞–љ—В–Є—Е–Њ–ї–Є–љ–µ—А–≥–Є—З–µ—Б–Ї–Є—Е —Н—Д—Д–µ–Ї—В–Њ–≤, –≤ —Б–≤—П–Ј–Є —Б —З–µ–Љ –±–µ–Ј –Њ–њ–∞—Б–µ–љ–Є—П –Љ–Њ–ґ–µ—В –±—Л—В—М –љ–∞–Ј–љ–∞—З–µ–љ –њ–∞—Ж–Є–µ–љ—В–∞–Љ —Б –≥–Є–њ–µ—А—В—А–Њ—Д–Є–µ–є –њ—А–µ–і—Б—В–∞—В–µ–ї—М–љ–Њ–є –ґ–µ–ї–µ–Ј—Л –Є –≥–ї–∞—Г–Ї–Њ–Љ–Њ–є, –Є –і—А—Г–≥–Є–Љ–Є —Б–Њ–њ—Г—В—Б—В–≤—Г—О—Й–Є–Љ–Є –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П–Љ–Є.
–У–ї–Є—Ж–µ—А–Є–ї–—В—А–Є–љ–Є—В—А–∞—В –Є –∞–Љ–Є–ї–љ–Є—В—А–Є—В –њ–Њ–Ї–∞–Ј–∞–ї–Є —Б–µ–±—П, –Ї–∞–Ї —Н—Д—Д–µ–Ї—В–Є–≤–љ—Л–µ –њ—А–µ–њ–∞—А–∞—В—Л –њ—А–Є —В—П–ґ–µ–ї—Л—Е –њ—А–Є—Б—В—Г–њ–∞—Е –±–Њ–ї–Є, –≤–Њ–Ј–Љ–Њ–ґ–љ–Њ, –Ј–∞ —Б—З–µ—В —Г–≤–µ–ї–Є—З–µ–љ–Є—П –Ї–Њ–љ—Ж–µ–љ—В—А–∞—Ж–Є–Є —Ж–Р–Ь–§ –Є —Ж–У–Ь–§ –≤ –≥–ї–∞–і–Ї–Њ–Љ—Л—И–µ—З–љ—Л—Е –Ї–ї–µ—В–Ї–∞—Е –°–Ю [25,14,1].
–С—Г—В–Є–ї—Б–Ї–Њ–њ–Њ–ї–∞–Љ–Є–љ––±—А–Њ–Љ–Є–і —В–Њ—А–Љ–Њ–Ј–Є—В —Д–∞–Ј–љ—Л–µ —Б–Њ–Ї—А–∞—Й–µ–љ–Є—П –њ—А–Є –≤–љ—Г—В—А–Є–≤–µ–љ–љ–Њ–Љ –≤–≤–µ–і–µ–љ–Є–Є, –љ–µ –≤–ї–Є—П—П –љ–∞ —Г—А–Њ–≤–µ–љ—М –±–∞–Ј–∞–ї—М–љ–Њ–≥–Њ –і–∞–≤–ї–µ–љ–Є—П [20]. –Ф—А–Њ—В–∞–≤–µ—А–Є–љ–∞ —Е–ї–Њ—А–Є–і, –∞–љ–∞–ї–Њ–≥ –њ–∞–њ–∞–≤–µ—А–Є–љ–∞, –њ—А–Є–≤–Њ–і–Є—В –Ї —А–∞—Б—Б–ї–∞–±–ї–µ–љ–Є—О –≥–ї–∞–і–Ї–Њ–Љ—Л—И–µ—З–љ—Л—Е –Ї–ї–µ—В–Њ–Ї, –Є–љ–≥–Є–±–Є—А—Г—П —Ж–Є—В–Њ–њ–ї–∞–Ј–Љ–∞—В–Є—З–µ—Б–Ї–Є–є —Д–µ—А–Љ–µ–љ—В —Д–Њ—Б—Д–Њ–і–Є—Н—Б—В–µ—А–∞–Ј—Г –Є —В–µ–Љ —Б–∞–Љ—Л–Љ —Г–≤–µ–ї–Є—З–Є–≤–∞—П –Ї–Њ–љ—Ж–µ–љ—В—А–∞—Ж–Є—О —Ж–Р–Ь–§. –Я—А–Є –њ—А–Њ–≤–µ–і–µ–љ–Є–Є –њ—А–Њ–≤–Њ–Ї–∞—Ж–Є–Њ–љ–љ—Л—Е —В–µ—Б—В–Њ–≤ –і—А–Њ—В–∞–≤–µ—А–Є–љ (80 –Љ–≥ per os —Б—А–∞–Ј—Г –њ–Њ—Б–ї–µ –Є —З–µ—А–µ–Ј 2 —З–∞—Б–∞ –њ–Њ—Б–ї–µ –Є–љ—К–µ–Ї—Ж–Є–Є –Љ–Њ—А—Д–Є–љ–∞) –њ—А–µ–і–Њ—В–≤—А–∞—Й–∞–µ—В –њ–Њ–≤—Л—И–µ–љ–Є–µ —Г—А–Њ–≤–љ—П —Д–µ—А–Љ–µ–љ—В–Њ–≤ –Є –≤–Њ–Ј–љ–Є–Ї–љ–Њ–≤–µ–љ–Є–µ –±–Њ–ї–µ–≤–Њ–≥–Њ –њ—А–Є—Б—В—Г–њ–∞ —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –і–Є—Б–Ї–Є–љ–µ–Ј–Є–µ–є –°–Ю.
–Ґ–µ—А–±—Г—В–∞–ї–Є–љ, b2––∞–≥–Њ–љ–Є—Б—В, –Ї–Њ—В–Њ—А—Л–є, –Ї–∞–Ї –Є –∞–Љ–Є–љ–Њ—Д–Є–ї–ї–Є–љ, —Г–≤–µ–ї–Є—З–Є–≤–∞–µ—В —Г—А–Њ–≤–µ–љ—М —Ж–Р–Ь–§ –≤ –≥–ї–∞–і–Ї–Њ–Љ—Л—И–µ—З–љ—Л—Е –Ї–ї–µ—В–Ї–∞—Е —Б—Д–Є–љ–Ї—В–µ—А–∞, –≤—Л–Ј—Л–≤–∞–µ—В —А–∞—Б—Б–ї–∞–±–ї–µ–љ–Є–µ –°–Ю [13]. –Р–љ—В–∞–≥–Њ–љ–Є—Б—В—Л –Ї–∞–ї—М—Ж–Є—П —В–∞–Ї–ґ–µ –Є—Б–њ—Л—В—Л–≤–∞–ї–Є—Б—М –≤ —В–µ—А–∞–њ–Є–Є –У–°–Ю. –Т—Л–±–Њ—А –њ—А–∞–≤–Є–ї—М–љ–Њ–є –і–Њ–Ј—Л –Њ–Ї–∞–Ј–∞–ї—Б—П –Њ—З–µ–љ—М –≤–∞–ґ–µ–љ, —В–∞–Ї 10 –Љ–≥ –љ–Є—Д–µ–і–Є–њ–Є–љ–∞ –љ–µ –Њ–Ї–∞–Ј—Л–≤–∞–ї–Є —Н—Д—Д–µ–Ї—В–∞ –≤–Њ–≤—Б–µ, –∞ 20 –Љ–≥ –≤—Л–Ј–≤–∞–ї–Є –Ј–љ–∞—З–Є—В–µ–ї—М–љ–Њ–µ —Г–Љ–µ–љ—М—И–µ–љ–Є–µ –±–∞–Ј–∞–ї—М–љ–Њ–≥–Њ –і–∞–≤–ї–µ–љ–Є—П –≤ –°–Ю —Г –±–Њ–ї—М–љ—Л—Е —Б –±–Є–ї–Є–∞—А–љ–Њ–є –і–Є—Б–Ї–Є–љ–µ–Ј–Є–µ–є. –Я–Є–љ–∞–≤–µ—А–Є–љ–∞ –±—А–Њ–Љ–Є–і, –љ–Њ–≤—Л–є –±–ї–Њ–Ї–∞—В–Њ—А –Ї–∞–ї—М—Ж–Є–µ–≤—Л—Е –Ї–∞–љ–∞–ї–Њ–≤, —В–∞–Ї–ґ–µ –Њ–±–ї–µ–≥—З–∞–µ—В —Б–њ–∞–Ј–Љ—Л –њ—А–Є –і–Є—Б–Ї–Є–љ–µ–Ј–Є–Є –°–Ю.
–Ш–љ—В–µ—А–µ—Б–љ–Њ, —З—В–Њ –њ—Б–Є—Е–Њ—В—А–Њ–њ–љ—Л–µ –њ—А–µ–њ–∞—А–∞—В—Л —В–∞–Ї–ґ–µ –Њ–±–ї–∞–і–∞—О—В —А–µ–ї–∞–Ї—Б–Є—А—Г—О—Й–Є–Љ –і–µ–є—Б—В–≤–Є–µ–Љ –љ–∞ –°–Ю. –Ґ–∞–Ї, –љ–µ–Ї–Њ—В–Њ—А—Л–µ –Є—Б—Б–ї–µ–і–Њ–≤–∞—В–µ–ї–Є —А–µ–Ї–Њ–Љ–µ–љ–і—Г—О—В –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞—В—М –і–ї—П –ї–µ—З–µ–љ–Є—П –У–°–Ю —Е–ї–Њ—А–њ—А–Њ–Љ–∞–Ј–Є–љ, –∞–љ—В–∞–≥–Њ–љ–Є—Б—В –Ї–∞–ї—М–Љ–Њ–і—Г–ї–Є–љ–∞, –Ї–Њ—В–Њ—А—Л–є –Њ–Ї–∞–Ј—Л–≤–∞–µ—В –≤—Л—А–∞–ґ–µ–љ–љ–Њ–µ —Б–њ–∞–Ј–Љ–Њ–ї–Є—В–Є—З–µ—Б–Ї–Њ–µ –і–µ–є—Б—В–≤–Є–µ –љ–∞ –≥–ї–∞–і–Ї–Є–µ –Љ—Л—И—Ж—Л [20]. –Ф–ї—П –Ї—Г–њ–Є—А–Њ–≤–∞–љ–Є—П –±–Њ–ї–Є —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –У–°–Ю –Љ–Њ–ґ–µ—В –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞—В—М—Б—П —Е–Њ–ї–µ—Ж–Є—Б—В–Њ–Ї–Є–љ–Є–љ, –Ї–Њ—В–Њ—А—Л–є –і–∞–ґ–µ –њ–Њ–Ј–≤–Њ–ї—П–µ—В –њ—А–µ–Њ–і–Њ–ї–µ—В—М —Б–њ–∞—Б—В–Є—З–µ—Б–Ї–Є–є —Н—Д—Д–µ–Ї—В –Љ–Њ—А—Д–Є–љ–∞ [26].
–Я—А–µ–њ–∞—А–∞—В—Л, –Њ–њ–Є—Б–∞–љ–љ—Л–µ –≤—Л—И–µ, –Њ–і–љ–Њ–≤—А–µ–Љ–µ–љ–љ–Њ —А–∞—Б—Б–ї–∞–±–ї—П—О—В —Б–Њ–Ї—А–∞—Й–µ–љ–љ—Л–є –°–Ю –Є —В–Њ—А–Љ–Њ–Ј—П—В —Б–Њ–Ї—А–∞—Й–µ–љ–Є–µ –°–Ю –њ—А–Є –µ–≥–Њ –≥–Є–њ–µ—А—З—Г–≤—Б—В–≤–Є—В–µ–ї—М–љ–Њ—Б—В–Є. –Ф–ї–Є—В–µ–ї—М–љ–Њ–µ –љ–∞–Ј–љ–∞—З–µ–љ–Є–µ —Н—В–Є—Е –њ—А–µ–њ–∞—А–∞—В–Њ–≤ (–Ј–∞ 30 –Љ–Є–љ. –њ–µ—А–µ–і –Њ—Б–љ–Њ–≤–љ—Л–Љ–Є –њ—А–Є–µ–Љ–∞–Љ–Є –њ–Є—Й–Є) –Љ–Њ–ґ–µ—В –њ—А–µ–і–Њ—В–≤—А–∞—Й–∞—В—М —А–∞–Ј–≤–Є—В–Є–µ —Б—В–µ–љ–Њ–Ј–∞ –°–Ю. –Я–∞—Ж–Є–µ–љ—В—Л —Б –У–°–Ю –і–Њ–ї–ґ–љ—Л –Є–Ј–±–µ–≥–∞—В—М —Г–њ–Њ—В—А–µ–±–ї–µ–љ–Є—П –ї–µ–Ї–∞—А—Б—В–≤, –≤—Л–Ј—Л–≤–∞—О—Й–Є—Е —Б–Њ–Ї—А–∞—Й–µ–љ–Є–µ –°–Ю (–Ї–Њ–і–µ–Є–љ). –Х—Б–ї–Є –Љ–µ–і–Є–Ї–∞–Љ–µ–љ—В–Њ–Ј–љ–∞—П —В–µ—А–∞–њ–Є—П –љ–µ –њ—А–Є–≤–Њ–і–Є—В –Ї –Њ–±–ї–µ–≥—З–µ–љ–Є—О —Б–Є–Љ–њ—В–Њ–Љ–Њ–≤ –У–°–Ю, —Б–ї–µ–і—Г–µ—В —А–µ—И–∞—В—М –≤–Њ–њ—А–Њ—Б –Њ –њ—А–Њ–≤–µ–і–µ–љ–Є–Є —Н–љ–і–Њ—Б–Ї–Њ–њ–Є—З–µ—Б–Ї–Њ–є –Є–ї–Є —Е–Є—А—Г—А–≥–Є—З–µ—Б–Ї–Њ–є —Б—Д–Є–љ–Ї—В–µ—А–Њ—В–Њ–Љ–Є–Є. –≠—В–Є –њ—А–Њ—Ж–µ–і—Г—А—Л –і–Њ–ї–ґ–љ—Л –њ—А–Є–Љ–µ–љ—П—В—М—Б—П —Б –Њ—Б—В–Њ—А–Њ–ґ–љ–Њ—Б—В—М—О, –њ–Њ—Б–Ї–Њ–ї—М–Ї—Г –Њ–±–ї–µ–≥—З–µ–љ–Є–µ –Њ–љ–Є –њ—А–Є–љ–Њ—Б—П—В —В–Њ–ї—М–Ї–Њ –њ–∞—Ж–Є–µ–љ—В–∞–Љ —Б –њ–Њ–≤—Л—И–µ–љ–љ—Л–Љ –±–∞–Ј–∞–ї—М–љ—Л–Љ –і–∞–≤–ї–µ–љ–Є–µ–Љ –≤ –°–Ю (–Ґ–Є–њ 1–2).
–Я—А–Є –і–Є—Б—Д—Г–љ–Ї—Ж–Є–Є –ґ–µ–ї—З–љ–Њ–≥–Њ –њ—Г–Ј—Л—А—П, –Њ–±—Г—Б–ї–Њ–≤–ї–µ–љ–љ–Њ–є –≥–Є–њ–Њ–Љ–Њ—В–Њ—А–љ–Њ–є –і–Є—Б–Ї–Є–љ–µ–Ј–Є–µ–є, –і–ї—П –њ–Њ–≤—Л—И–µ–љ–Є—П —Б–Њ–Ї—А–∞—В–Є—В–µ–ї—М–љ–Њ–є —Д—Г–љ–Ї—Ж–Є–Є –њ—А–Є–Љ–µ–љ—П—О—В –њ—А–Њ–Ї–Є–љ–µ—В–Є–Ї–Є –≤ —В–µ—З–µ–љ–Є–µ 10–14 –і–љ–µ–є: —Ж–Є–њ—А–∞–Ј–Є–і, –і–Њ–Љ–њ–µ—А–Є–і–Њ–љ –Є–ї–Є –Љ–µ—В–Њ–Ї–ї–Њ–њ—А–∞–Љ–Є–і. –Т –Ї–∞—З–µ—Б—В–≤–µ —Е–Њ–ї–µ—Ж–Є—Б—В–Њ–Ї–Є–љ–µ—В–Є—З–µ—Б–Ї–Є—Е —Б—А–µ–і—Б—В–≤ –Љ–Њ–ґ–љ–Њ –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞—В—М —А–∞—Б—В–≤–Њ—А —Б—Г–ї—М—Д–∞—В–∞ –Љ–∞–≥–љ–Є—П –Є–ї–Є —А–∞—Б—В–≤–Њ—А —Б–Њ—А–±–Є—В–∞.
–Ы–Є—В–µ—А–∞—В—Г—А–∞
1. Bar–Meir, S., Halpern, Z. and Bardan, E.: Nitrate therapy in a patient with papillary dysfunction. Am. J. Gastroenterology 78. 94–95, 1983
2. Berger, Z., Pap, dr. Varro, V: Wirsungodyskinesia an isolated functional disorder of transpapillary pancreatic juice flow (in Hungarian). Magy. Belorv. Arch. 7, (Suppl.) 93, 1980 (Abstr.)
3. Bolondi, L., Gaiani, S., Gullo, L. Labo, G.: Secretin administration induces a dilatation of the main pancreatic duct. Dig. Dis. Sci. 29, 802–808, 1984
4. Darweesh, R.M.A., Dodds, W.J., Hogan, W.J. et al: Efficacy of quantitative hepatobiliary scintigraphy and fatty meal sonography for evaluating patients with suspected partial common bile duct obstruction. Gastroenterology 94, 779–786, 1988
5. Dean R.S., Geenen J.E., Stewart E.T., Dodds W.J., Hogan W.J. Sphincter–of–Oddi (SO) manometry and ultrasound (US) fatty meal test in patients with suspected SO dyskinesia; a comparison of test results. Gastroenterology 1991, vol.100:A314.
6. Debray P.C., Hardouin J.R., Fablet, J.: Le test ,,choleretique–morphine». Son enteret dans les affections des voies biliaries et dans les migraines. Gastroenterologia 97 137–148,1962
7. Geenen J.E., Hogan W.J., Dodds W.J., et al. Intraluminal pressure recording from the human sphincter of Oddi. Gastroenterology 1980, vol.78, p.317–324.
8. Geenen J.E., Hogan W.J., Dodds W.J., et al. The efficacy of endoscopic sphincterotomy after cholecystectomy in patients with sphincter–of–Oddi dysfunction. N EngI J Med 1989, vol.320, p.82–87.
9. Herman S., Troiano F.F.; Hawes R.H., et al. Frequency of abnormal sphincter–of–Oddi manometry compared with clinical suspicion of sphincter–of–Oddi dysfunction. Am J Gastroenterol 1991:86, p.586–590
10. Hogan W.J., Geenen J.E. Biliary dyskinesia. Endoscopy 1988, vol.20, p.179–183.
11. Hogan W.J. Sphincter–of–Oddi; Physiology and pathophysiology. Regulatory Peptide Letter 1991 , vol.111, p.23–28.
12. Holtzer, J.D. Hulst, S.G.T.H.: Confirmation of postcholecystectomy biliary dyskinesia by elevation of serum transaminases (GOT and GPT) after injection of morphine? Acta. Med. Scand. 194, 221–224, 1973
13. Ingmarsson I., Liedberg G., Presson C: Effect of a netaasrenoceptor–stimulating compound (terbutaline) on common bile duct pressure in man. Acta Chir Scand 1972, 138, p. 827–829.
14. Lasson, A.: The postcholecystectomy syndrome: diagnostic and therapeutic strategy. Scand. J. Gastroenterology 22, 897– 902, 1987
15. Lonovics J., Velosy B., Madasy L.: Sphincter of Oddi dyskinesia. In: The papilla of Vater. Zagoni T. (ed) Melania, Budapest, 1995, p. 125–163.
16. Nardi G.L. Acosta, J.M.: Papillitis as a cause of pancreatitis and abdominal pain: role of evocative test, operative pancreatography and histologic evaluation. Ann. Surg. 164,611–621, 1966
17. Pap A., Topa L., Balgha V., Kovats–Megyesi A., Pozsar J., Szikszai E..: Drotaverine antagonizes spasm of Oddi’s sphincter provoked by morphine in man. Gastroenterology 1997 112 Suppl. Vol. 4: A519
18. Raddawi L.I., Geenen J.E., Hogan W.J., Dodds W.J., Venu R.F.; Johnson G.O. Pressure measurements from biliary and pancreatic segments of sphincter of Oddi: comparison between patients with functional abdominal pain, biliary or pancreatic disease. Dig DisSci 1991, vol.36, p.71–74.
19. Rolny R., Geenen J.E., Hogan W.J., Venu R.R. Clinical features, manometric findings and endoscopic therapy results in Group I patients with sphincter–of–Oddi dysfunction. Gastrointestinal Endoscopy 1991, p.37–252.
20. Staritz, M.: Pharmacology of the sphincter of Oddi. Endoscopy 20, (Suppl.) 171 –174, 1988
21. Steinberg, W.M., Salvato, R.F. Toskes, PR: The morphine–prostigmin provocative test – Is it useful for making clinical decisions? Gastroenterology 78; 728–731, 1980
22. Stone J.E., Hogan W.J., Geenen J.E., Wilson S.P., Dodds W.J. Acute recurrent pancreatitis: The role of sphincter–of–Oddi (SO) manometry in predicting long–term benefit of therapy. Gastroenterology 1988 vol.94 :A446.
23. Toouli, J.: Biliary tract motor dysfunction. In: Bailliere’s Clinical Gastroenterology, Dent J (guest ed) Bailliere Tindall, London 1991; 409–430.
24. Torsoli A., Corazziari E., Habib F.L., et al. Frequencies and cyclic pattern of the human sphincter–of–Oddi phasic activity. Gut 1986, vol.27, p.363–369.
25. Varro, V, Dobronte, Z., Hajnal, F. et al.: The diagnosis of hypertonic Oddi’s sphincter dyskinesia. Am. J. Gastroenterol. 28, 736–739, 1983
26. Velosy, B., Jakab, I., Madacsy, L., Hajnal, F, Pap, A. Lonovics, J.: Comparison of the effect of nitroglycerine, aminophylline and papaverine on the prostigmine–morphine–induced sphincter of Oddi spasm. Zeitschr. Gastroent. 30 307, 1992 (Abstr.)
27. Thompson WG. Classification of functional gastrointestinal disorders. Motility 1994;25:10–2.
28. –Ш–ї—М—З–µ–љ–Ї–Њ –Р.–Р. –Ф–Є—Б—Д—Г–љ–Ї—Ж–Є–Њ–љ–∞–ї—М–љ—Л–µ —А–∞—Б—Б—В—А–Њ–є—Б—В–≤–∞ –±–Є–ї–Є–∞—А–љ–Њ–≥–Њ —В—А–∞–Ї—В–∞. Consilium provisorum, —В–Њ–Љ 2, вДЦ 4, 2002.
29. –Ь–Є–љ—Г—И–Ї–Є–љ –Ю.–Э. –Р–±–і–Њ–Љ–Є–љ–∞–ї—М–љ–∞—П –±–Њ–ї—М: –і–Є—Д—Д–µ—А–µ–љ—Ж–Є–∞–ї—М–љ–∞—П –і–Є–∞–≥–љ–Њ—Б—В–Є–Ї–∞, –≤–Њ–Ј–Љ–Њ–ґ–љ—Л–µ –ї–µ—З–µ–±–љ—Л–µ –њ–Њ–і—Е–Њ–і—Л. –†–Ь–Ц, —В–Њ–Љ 10, вДЦ 15, 2002.
30. –£—А—Б–Њ–≤–∞ –Э.–Ш. –Я—А–Њ–±–ї–µ–Љ–∞ —Д—Г–љ–Ї—Ж–Є–Њ–љ–∞–ї—М–љ—Л—Е —А–∞—Б—Б—В—А–Њ–є—Б—В–≤ –±–Є–ї–Є–∞—А–љ–Њ–≥–Њ —В—А–∞–Ї—В–∞ —Г –і–µ—В–µ–є –Є –Є—Е –Ї–Њ—А—А–µ–Ї—Ж–Є—П. –†–Ь–Ц, —В–Њ–Љ 11, вДЦ 3, 2003.
31. –Э.–Ш. –£—А—Б–Њ–≤–∞. –Ф–Є—Б—Д—Г–љ–Ї—Ж–Є–Њ–љ–∞–ї—М–љ—Л–µ —А–∞—Б—Б—В—А–Њ–є—Б—В–≤–∞ –±–Є–ї–Є–∞—А–љ–Њ–≥–Њ —В—А–∞–Ї—В–∞ —Г –і–µ—В–µ–є, –Ї—А–Є—В–µ—А–Є–Є –і–Є–∞–≥–љ–Њ—Б—В–Є–Ї–Є –Є –Ї–Њ—А—А–µ–Ї—Ж–Є–Є. //Consilium Medicum. –°–Є–Љ–њ–Њ–Ј–Є—Г–Љ «–Ь–µ—Е–∞–љ–Є–Ј–Љ—Л —А–µ–≥—Г–ї—П—Ж–Є–Є –ґ–µ–ї—З–µ–Њ–±—А–∞–Ј–Њ–≤–∞–љ–Є—П –Є –Љ–µ—В–Њ–і—Л –µ–≥–Њ –Ї–Њ—А—А–µ–Ї—Ж–Є–Є». – 2002. – –°. 14–15.
32. –Ш–ї—М—З–µ–љ–Ї–Њ –Р.–Р. –≠—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В—М –Љ–µ–±–µ–≤–µ—А–Є–љ–∞ –≥–Є–і—А–Њ—Е–ї–Њ—А–Є–і–∞ –њ—А–Є –±–Є–ї–Є–∞—А–љ–Њ–є –њ–∞—В–Њ–ї–Њ–≥–Є–Є. –†–Ь–Ц, —В–Њ–Љ 11, вДЦ 4, 2003.
33. –Ч–∞–±–Њ–ї–µ–≤–∞–љ–Є—П –≤–љ–µ–њ–µ—З–µ–љ–Њ—З–љ–Њ–є –±–Є–ї–Є–∞—А–љ–Њ–є —Б–Є—Б—В–µ–Љ—Л: –і–Є—Б—Д—Г–љ–Ї—Ж–Є—П –ґ–µ–ї—З–љ–Њ–≥–Њ –њ—Г–Ј—Л—А—П –Є —Б–Њ—Б—В–Њ—П–љ–Є—П –њ–Њ—Б–ї–µ —Е–Њ–ї–µ—Ж–Є—Б—В–Њ–Ї–Њ–Љ–Є–Є. –Ь–µ–ґ–і—Г–љ–∞—А–Њ–і–љ—Л–є –С—О–ї–ї–µ—В–µ–љ—М: –У–∞—Б—В—А–Њ—Н–љ—В–µ—А–Њ–ї–Њ–≥–Є—П. вДЦ6, 2001.












