–Э–Є–ґ–µ –њ—А–Є–≤–µ–і–µ–љ—Л –Ї–ї–Є–љ–Є–Ї–Њ––ї–∞–±–Њ—А–∞—В–Њ—А–љ—Л–µ –Ї—А–Є—В–µ—А–Є–Є, —Е–∞—А–∞–Ї—В–µ—А–љ—Л–µ –і–ї—П –Я–°–†–Ъ.
1. –£–њ–Њ–Љ–Є–љ–∞–љ–Є–µ –≤ –∞–љ–∞–Љ–љ–µ–Ј–µ –Ю–Ъ–Ш, –њ—А–µ–і—И–µ—Б—В–≤–Њ–≤–∞–≤—И–µ–є –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—О.
2. –Ю–±–љ–∞—А—Г–ґ–µ–љ–Є–µ –Љ–∞—А–Ї–µ—А–Њ–≤ –Ю–Ъ–Ш –≤ –±–Є–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є—Е —Б—А–µ–і–∞—Е –±–Њ–ї—М–љ–Њ–≥–Њ.
3. –Я—А–Є–Ј–љ–∞–Ї–Є –і–Є—Б–±–Є–Њ–Ј–∞ –≤ –±–∞–Ї—В–µ—А–Є–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є—Е –њ–Њ—Б–µ–≤–∞—Е –Ї–∞–ї–∞.
4. –Ш–Ј–±—Л—В–Њ—З–љ—Л–є –±–∞–Ї—В–µ—А–Є–∞–ї—М–љ—Л–є —А–Њ—Б—В –≤ —В–Њ–љ–Ї–Њ–є –Ї–Є—И–Ї–µ
5. –°–љ–Є–ґ–µ–љ–Є–µ –љ–∞–њ—А—П–ґ–µ–љ–љ–Њ—Б—В–Є –Є–Љ–Љ—Г–љ–Є—В–µ—В–∞.
6. –Я–Њ–ї–Њ–ґ–Є—В–µ–ї—М–љ—Л–є —Н—Д—Д–µ–Ї—В —В–µ—А–∞–њ–Є–Є –±–Є–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є––∞–Ї—В–Є–≤–љ—Л–Љ–Є –њ—А–µ–њ–∞—А–∞—В–∞–Љ–Є, –њ—А–µ– –Є –њ—А–Њ–±–Є–Њ—В–Є–Ї–∞–Љ–Є.
–¶–µ–ї—М –љ–∞—Б—В–Њ—П—Й–µ–є —А–∞–±–Њ—В—Л – –Є–Ј—Г—З–Є—В—М —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В—М –≤–Є—Б–Љ—Г—В–∞ —В—А–Є–Ї–∞–ї–Є—П –і–Є—Ж–Є—В—А–∞—В (–Ф–µ––Э–Њ–ї–∞) –≤ –ї–µ—З–µ–љ–Є–Є –Я–°–†–Ъ —Б –њ—А–µ–Њ–±–ї–∞–і–∞–љ–Є–µ–Љ –і–Є–∞—А–µ–Є –Є –µ–≥–Њ –≤–ї–Є—П–љ–Є–µ –љ–∞ —Б–Њ—Б—В–∞–≤ –Љ–Є–Ї—А–Њ—Д–ї–Њ—А—Л –Ї–Є—И–µ—З–љ–Є–Ї–∞.
–†–µ—И–µ–љ–Є–µ –Њ–± –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є–Є –Ф–µ––Э–Њ–ї–∞ –і–ї—П –ї–µ—З–µ–љ–Є—П –±–Њ–ї—М–љ—Л—Е –Я–°–†–Ъ –Њ—Б–љ–Њ–≤—Л–≤–∞–ї–Њ—Б—М –љ–∞ —А–µ–Ј—Г–ї—М—В–∞—В–∞—Е –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–є, –і–Њ–Ї–∞–Ј–∞–≤—И–Є—Е, —З—В–Њ –њ—А–µ–њ–∞—А–∞—В —Г—Б–њ–µ—И–љ–Њ –њ—А–Є–Љ–µ–љ—П–µ—В—Б—П –≤ —Н—А–∞–і–Є–Ї–∞—Ж–Є–Њ–љ–љ–Њ–є —В–µ—А–∞–њ–Є–Є Helicobacter pylori, –њ–Њ–і–∞–≤–ї—П—П —А–Њ—Б—В –Љ–Є–Ї—А–Њ–Њ—А–≥–∞–љ–Є–Ј–Љ–∞ –љ–∞ —Б–ї–Є–Ј–Є—Б—В–Њ–є –Њ–±–Њ–ї–Њ—З–Ї–µ –ґ–µ–ї—Г–і–Ї–∞ [5]. –Ґ–µ—А–∞–њ–µ–≤—В–Є—З–µ—Б–Ї–Є–є —Н—Д—Д–µ–Ї—В –Њ—Б–љ–Њ–≤–∞–љ –љ–∞ –±–∞–Ї—В–µ—А–Є—Ж–Є–і–љ—Л—Е —Б–≤–Њ–є—Б—В–≤–∞—Е –њ—А–µ–њ–∞—А–∞—В–∞, –Ї–Њ—В–Њ—А—Л–є –Њ–±—А–∞–Ј—Г–µ—В –Ї–Њ–Љ–њ–ї–µ–Ї—Б—Л –љ–∞ –±–∞–Ї—В–µ—А–Є–∞–ї—М–љ–Њ–є —Б—В–µ–љ–Ї–µ, –Є–љ–≥–Є–±–Є—А—Г–µ—В —Д–µ—А–Љ–µ–љ—В—Л –±–∞–Ї—В–µ—А–Є–є (—Г—А–µ–∞–Ј—Г, –Ї–∞—В–∞–ї–∞–Ј—Г –Є –ї–Є–њ–∞–Ј—Г –Є –і—А.), –њ—А–µ–њ—П—В—Б—В–≤—Г—П –∞–і–≥–µ–Ј–Є–Є –Э. pylori –Ї —Н–њ–Є—В–µ–ї–Є–Њ—Ж–Є—В–∞–Љ –ґ–µ–ї—Г–і–Ї–∞. –Ъ—А–Њ–Љ–µ —В–Њ–≥–Њ, –њ—А–µ–њ–∞—А–∞—В—Л –≤–Є—Б–Љ—Г—В–∞ —В—А–∞–і–Є—Ж–Є–Њ–љ–љ–Њ –њ—А–Є–Љ–µ–љ—П—О—В—Б—П –≤ –Ї–∞—З–µ—Б—В–≤–µ –≤—П–ґ—Г—Й–Є—Е —Б—А–µ–і—Б—В–≤ –њ—А–Є –≤–Њ—Б–њ–∞–ї–Є—В–µ–ї—М–љ—Л—Е –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П—Е –Ц–Ъ–Ґ.
–Ь–∞—В–µ—А–Є–∞–ї –Є –Љ–µ—В–Њ–і—Л
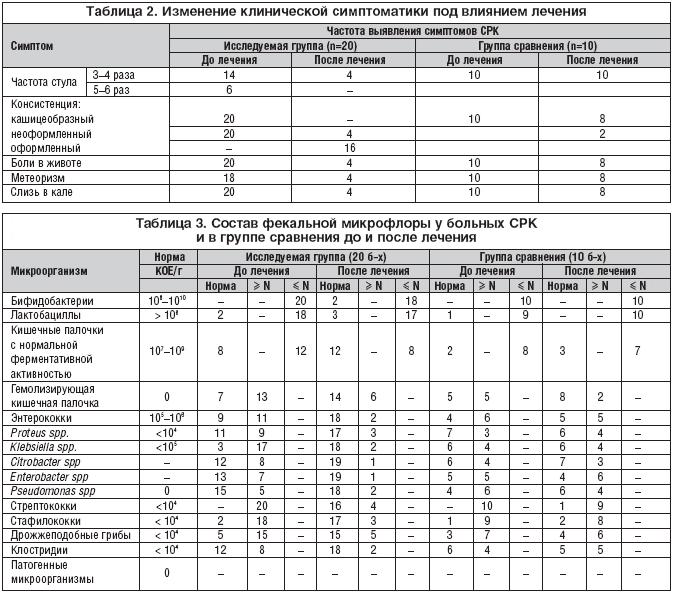
–Я–Њ–і –љ–∞–±–ї—О–і–µ–љ–Є–µ–Љ –љ–∞—Е–Њ–і–Є–ї–Є—Б—М 20 –±–Њ–ї—М–љ—Л—Е –Я–°–†–Ъ —Б –њ—А–µ–Њ–±–ї–∞–і–∞–љ–Є–µ–Љ –і–Є–∞—А–µ–Є. –У—А—Г–њ–њ—Г —Б—А–∞–≤–љ–µ–љ–Є—П —Б–Њ—Б—В–∞–≤–Є–ї–Є 10 –±–Њ–ї—М–љ—Л—Е –°–†–Ъ —Б –њ—А–µ–Њ–±–ї–∞–і–∞–љ–Є–µ–Љ –і–Є–∞—А–µ–Є, —Б–Њ–њ–Њ—Б—В–∞–≤–Є–Љ—Л–µ –њ–Њ –њ–Њ–ї—Г –Є –≤–Њ–Ј—А–∞—Б—В—Г. –•–∞—А–∞–Ї—В–µ—А–Є—Б—В–Є–Ї–∞ –Є—Е –њ–Њ–Ї–∞–Ј–∞–љ–∞ –≤ —В–∞–±–ї–Є—Ж–µ 1.
–Э–∞—З–∞–ї–Њ –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П –±–Њ–ї—М–љ—Л–µ —Б–≤—П–Ј—Л–≤–∞–ї–Є —Б –њ–Є—Й–µ–≤—Л–Љ –Њ—В—А–∞–≤–ї–µ–љ–Є–µ–Љ, –њ–Њ –њ–Њ–≤–Њ–і—Г –Ї–Њ—В–Њ—А–Њ–≥–Њ –Њ–±—Б–ї–µ–і–Њ–≤–∞–ї–Є—Б—М –Є –ї–µ—З–Є–ї–Є—Б—М –∞–Љ–±—Г–ї–∞—В–Њ—А–љ–Њ –њ–Њ –Љ–µ—Б—В—Г –ґ–Є—В–µ–ї—М—Б—В–≤–∞ –Є–ї–Є –≤ –Є–љ—Д–µ–Ї—Ж–Є–Њ–љ–љ–Њ–є –±–Њ–ї—М–љ–Є—Ж–µ. –Т —Б–≤—П–Ј–Є —Б –њ—А–Њ–і–Њ–ї–ґ–∞—О—Й–Є–Љ–Є—Б—П –ґ–∞–ї–Њ–±–∞–Љ–Є –±–Њ–ї—М–љ—Л–Љ, –Ї–∞–Ї –њ—А–∞–≤–Є–ї–Њ, –љ–∞–Ј–љ–∞—З–∞–ї–Є—Б—М –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П –Ї–∞–ї–∞, –≤ –Ї–Њ—В–Њ—А—Л—Е –Њ–њ—А–µ–і–µ–ї—П–ї—Б—П –і–Є—Б–±–∞–Ї—В–µ—А–Є–Њ–Ј –њ—А–Є –Њ—В—Б—Г—В—Б—В–≤–Є–Є —А–Њ—Б—В–∞ –њ–∞—В–Њ–≥–µ–љ–љ–Њ–є –Љ–Є–Ї—А–Њ—Д–ї–Њ—А—Л. –С–Њ–ї—М–љ—Л–Љ –љ–∞–Ј–љ–∞—З–∞–ї–Є—Б—М –∞–і—Б–Њ—А–±–µ–љ—В—Л, –њ—А–Њ–±–Є–Њ—В–Є–Ї–Є, –ї–Њ–њ–µ—А–∞–Љ–Є–і, —Д–µ—А–Љ–µ–љ—В–љ—Л–µ –њ—А–µ–њ–∞—А–∞—В—Л. –Ю–і–љ–∞–Ї–Њ –Љ–µ–і–Є–Ї–∞–Љ–µ–љ—В–Њ–Ј–љ–∞—П —В–µ—А–∞–њ–Є—П –љ–µ –Њ–Ї–∞–Ј—Л–≤–∞–ї–∞ —Б—В–Њ–є–Ї–Њ–≥–Њ –њ–Њ–ї–Њ–ґ–Є—В–µ–ї—М–љ–Њ–≥–Њ —Н—Д—Д–µ–Ї—В–∞, —З—В–Њ –Є —П–≤–ї—П–ї–Њ—Б—М –Њ—Б–љ–Њ–≤–∞–љ–Є–µ–Љ –і–ї—П –љ–∞–њ—А–∞–≤–ї–µ–љ–Є—П –≤ –¶–Э–Ш–Ш–У.
–Я—А–Є –њ–Њ—Б—В—Г–њ–ї–µ–љ–Є–Є –±–Њ–ї—М–љ—Л–µ –ґ–∞–ї–Њ–≤–∞–ї–Є—Б—М –љ–∞ –ґ–Є–і–Ї–Є–є —Б—В—Г–ї –і–Њ 4–6 —А–∞–Ј –≤ —Б—Г—В–Ї–Є (–њ—А–µ–Є–Љ—Г—Й–µ—Б—В–≤–µ–љ–љ–Њ –≤ —Г—В—А–µ–љ–љ–Є–µ —З–∞—Б—Л, –љ–µ–Њ–±–Є–ї—М–љ—Л–є, —Б –њ—А–Є–Љ–µ—Б—М—О —Б–ї–Є–Ј–Є), –Љ–µ—В–µ–Њ—А–Є–Ј–Љ, –≤–Ј–і—Г—В–Є–µ –ґ–Є–≤–Њ—В–∞, –±–Њ–ї—М –Є –і–Є—Б–Ї–Њ–Љ—Д–Њ—А—В –≤ –ґ–Є–≤–Њ—В–µ (—З–∞—Й–µ –≤ –ї–µ–≤—Л—Е –Њ—В–і–µ–ї–∞—Е). –С–Њ–ї—М –љ–Њ—Б–Є–ї–∞ —Б—Е–≤–∞—В–Ї–Њ–Њ–±—А–∞–Ј–љ—Л–є —Е–∞—А–∞–Ї—В–µ—А –Є —Б—В–Є—Е–∞–ї–∞ –Є–ї–Є —Г–Љ–µ–љ—М—И–∞–ї–∞—Б—М –њ–Њ—Б–ї–µ –∞–Ї—В–∞ –і–µ—Д–µ–Ї–∞—Ж–Є–Є. –°–Є–Љ–њ—В–Њ–Љ—Л «—В—А–µ–≤–Њ–≥–Є» –Њ—В—Б—Г—В—Б—В–≤–Њ–≤–∞–ї–Є, —В–∞–Ї–Є–Љ –Њ–±—А–∞–Ј–Њ–Љ, –і–Є–∞–≥–љ–Њ–Ј –°–†–Ъ —Б–Њ–Њ—В–≤–µ—В—Б—В–≤–Њ–≤–∞–ї –†–Є–Љ—Б–Ї–Є–Љ –Ї—А–Є—В–µ—А–Є—П–Љ II.
–Т –Ї–ї–Є–љ–Є–Ї–µ –±–Њ–ї—М–љ—Л–Љ –≤—Л–њ–Њ–ї–љ—П–ї–Є —Б—В–∞–љ–і–∞—А—В–љ–Њ–µ –ї–∞–±–Њ—А–∞—В–Њ—А–љ–Њ––Є–љ—Б—В—А—Г–Љ–µ–љ—В–∞–ї—М–љ–Њ–µ –Њ–±—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ, –≤ —В.—З. –Ї–Њ–ї–Њ–љ–Њ—Б–Ї–Њ–њ–Є—О. –Ф–ї—П —А–µ—И–µ–љ–Є—П –њ–Њ—Б—В–∞–≤–ї–µ–љ–љ—Л—Е –Ј–∞–і–∞—З –±–Њ–ї—М–љ—Л–Љ –Є—Б—Б–ї–µ–і—Г–µ–Љ–Њ–є –≥—А—Г–њ–њ—Л –њ—А–Њ–≤–Њ–і–Є–ї–Є —Н–Ј–Њ—Д–∞–≥–Њ–≥–∞—Б—В—А–Њ–Є–љ—В–µ—Б—В–Є–љ–Њ—Б–Ї–Њ–њ–Є—О —Б –Љ–љ–Њ–ґ–µ—Б—В–≤–µ–љ–љ–Њ–є –±–Є–Њ–њ—Б–Є–µ–є —Б–ї–Є–Ј–Є—Б—В–Њ–є –Њ–±–Њ–ї–Њ—З–Ї–Є —В–Њ–љ–Ї–Њ–є –Ї–Є—И–Ї–Є. –Я–Њ–Љ–Є–Љ–Њ –≥–Є—Б—В–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Њ–≥–Њ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П, –≤ –±–Є–Њ–њ—В–∞—В–∞—Е –Њ–њ—А–µ–і–µ–ї—П–ї–Є —Б–Њ—Б—В–∞–≤ –Љ—Г–Ї–Њ–Ј–љ–Њ–є –Љ–Є–Ї—А–Њ—Д–ї–Њ—А—Л.
–Ь—Г–Ї–Њ–Ј–љ—Г—О —Д–ї–Њ—А—Г –Є—Б—Б–ї–µ–і–Њ–≤–∞–ї–Є –Љ–µ—В–Њ–і–Њ–Љ –≥–∞–Ј–Њ–≤–Њ–є —Е—А–Њ–Љ–∞—В–Њ–≥—А–∞—Д–Є–Є –≤ —Б–Њ—З–µ—В–∞–љ–Є–Є —Б –Љ–∞—Б—Б–—Б–њ–µ–Ї—В—А–Њ–Љ–µ—В—А–Є–µ–є (–У–•––Ь–°). –Я—А–Є–Љ–µ–љ—П–ї–Є —Б–њ–µ—Ж–Є–∞–ї–Є–Ј–Є—А–Њ–≤–∞–љ–љ—Л–є —Е—А–Њ–Љ–∞—В–Њ–≥—А–∞—Д Microbial Identification System, –≤—Л–њ—Г—Б–Ї–∞–µ–Љ–Њ–є —Д–Є—А–Љ–Њ–є MIDI Inc., –Ф–µ–ї–∞–≤–µ—А, –°–®–Р. –Я—А–Є–љ—Ж–Є–њ –Љ–µ—В–Њ–і–∞ – –Љ–Њ–ї–µ–Ї—Г–ї—П—А–љ—Л–є, –Њ—Б–љ–Њ–≤–∞–љ –љ–∞ –њ—А—П–Љ–Њ–Љ –Њ–њ—А–µ–і–µ–ї–µ–љ–Є–Є –≤ –±–Є–Њ–њ—А–Њ–±–µ –ґ–Є—А–љ—Л—Е –Ї–Є—Б–ї–Њ—В (–Ц–Ъ) –Ї–ї–µ—В–Њ—З–љ–Њ–є —Б—В–µ–љ–Ї–Є –Љ–Є–Ї—А–Њ–Њ—А–≥–∞–љ–Є–Ј–Љ–Њ–≤ –Є –њ–Њ–Ј–≤–Њ–ї—П–µ—В –Є–і–µ–љ—В–Є—Д–Є—Ж–Є—А–Њ–≤–∞—В—М –і–Њ –љ–µ—Б–Ї–Њ–ї—М–Ї–Є—Е —В—Л—Б—П—З —И—В–∞–Љ–Љ–Њ–≤ –±–∞–Ї—В–µ—А–Є–є –Є –Љ–Є–Ї—А–Њ—Б–Ї–Њ–њ–Є—З–µ—Б–Ї–Є—Е –≥—А–Є–±–Њ–≤ [6]. –Ю—Б–Њ–±–µ–љ–љ–Њ—Б—В–Є —Б–Њ—Б—В–∞–≤–∞ –ґ–Є—А–љ—Л—Е –Ї–Є—Б–ї–Њ—В –Є—Б–њ–Њ–ї—М–Ј—Г—О—В—Б—П –љ–∞—А—П–і—Г —Б –і—А—Г–≥–Є–Љ–Є –њ–∞—А–∞–Љ–µ—В—А–∞–Љ–Є –≤ –±–∞–Ї—В–µ—А–Є–∞–ї—М–љ–Њ–є —В–∞–Ї—Б–Њ–љ–Њ–Љ–Є–Є –Є –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Њ–є –±–∞–Ї—В–µ—А–Є–∞–ї—М–љ–Њ–є –і–Є–∞–≥–љ–Њ—Б—В–Є–Ї–µ. –Ш—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ –њ—А–Њ–≤–Њ–і–Є–ї–Є –і–≤–∞–ґ–і—Л – –і–Њ –Є –њ–Њ—Б–ї–µ —В–µ—А–∞–њ–Є–Є.
–°–Њ—Б—В–∞–≤ —Д–µ–Ї–∞–ї—М–љ–Њ–є –Љ–Є–Ї—А–Њ—Д–ї–Њ—А—Л –Є—Б—Б–ї–µ–і–Њ–≤–∞–ї–Є –±–∞–Ї—В–µ—А–Є–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є–Љ –Љ–µ—В–Њ–і–Њ–Љ. –Ш—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ –Љ—Г–Ї–Њ–Ј–љ–Њ–є –Є —Д–µ–Ї–∞–ї—М–љ–Њ–є –Љ–Є–Ї—А–Њ—Д–ї–Њ—А—Л –њ—А–Њ–≤–Њ–і–Є–ї–Є –≤ –љ–∞—З–∞–ї–µ –Є –≤ –Ї–Њ–љ—Ж–µ –њ—А–µ–±—Л–≤–∞–љ–Є—П –≤ —Б—В–∞—Ж–Є–Њ–љ–∞—А–µ.
–С–Њ–ї—М–љ—Л–Љ –љ–∞–Ј–љ–∞—З–∞–ї–Є –і–Є–µ—В—Г 4–±, –і—А–Њ—В–∞–≤–µ—А–Є–љ–∞ –≥–Є–і—А–Њ—Е–ї–Њ—А–Є–і –њ—А–Є –±–Њ–ї—П—Е –≤ –ґ–Є–≤–Њ—В–µ (–њ–Њ —В—А–µ–±–Њ–≤–∞–љ–Є—О –њ–Њ 2 —В–∞–±–ї. –і–Њ 3–—Е —А–∞–Ј –≤ —Б—Г—В–Ї–Є) –Є –њ–Њ–ї–Є–≤–Є—В–∞–Љ–Є–љ—Л. –С–Њ–ї—М–љ—Л–Љ –Є—Б—Б–ї–µ–і—Г–µ–Љ–Њ–є –≥—А—Г–њ–њ—Л –љ–∞–Ј–љ–∞—З–∞–ї–Є –Ф–µ––Э–Њ–ї –њ–Њ 120 –Љ–≥ 3 —А–∞–Ј–∞ –≤ —Б—Г—В–Ї–Є, –∞ –±–Њ–ї—М–љ—Л–Љ –≥—А—Г–њ–њ—Л —Б—А–∞–≤–љ–µ–љ–Є—П – –∞–љ—В–∞—Ж–Є–і –њ–Њ 3 –њ–∞–Ї–µ—В–Є–Ї–∞ –≤ —Б—Г—В–Ї–Є. –Ґ–Њ—В –Є –і—А—Г–≥–Њ–є –њ—А–µ–њ–∞—А–∞—В –љ–∞–Ј–љ–∞—З–∞–ї–Є –Ј–∞ 30 –Љ–Є–љ. –і–Њ –µ–і—Л, 3 —А–∞–Ј–∞ –≤ —Б—Г—В–Ї–Є, –≤ —В–µ—З–µ–љ–Є–µ 3 –љ–µ–і–µ–ї—М.
–≠—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В—М –њ—А–Њ–≤–Њ–і–Є–Љ–Њ–є —В–µ—А–∞–њ–Є–Є –Њ—Ж–µ–љ–Є–≤–∞–ї–Є –њ–Њ –і–Є–љ–∞–Љ–Є–Ї–µ –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є—Е —Б–Є–Љ–њ—В–Њ–Љ–Њ–≤, –Є–Ј–Љ–µ–љ–µ–љ–Є—О —Б–Њ—Б—В–∞–≤–∞ —Д–µ–Ї–∞–ї—М–љ–Њ–є –Є –Љ—Г–Ї–Њ–Ј–љ–Њ–є –Љ–Є–Ї—А–Њ—Д–ї–Њ—А—Л —В–Њ–љ–Ї–Њ–є –Ї–Є—И–Ї–Є.
–†–µ–Ј—Г–ї—М—В–∞—В—Л –Є –Њ–±—Б—Г–ґ–і–µ–љ–Є–µ
–Т —В–∞–±–ї–Є—Ж–µ 2 –њ–Њ–Ї–∞–Ј–∞–љ–∞ –і–Є–љ–∞–Љ–Є–Ї–∞ –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Њ–є –Ї–∞—А—В–Є–љ—Л —Г –±–Њ–ї—М–љ—Л—Е –°–†–Ъ —Б –њ—А–µ–Њ–±–ї–∞–і–∞–љ–Є–µ–Љ –і–Є–∞—А–µ–Є –њ–Њ–і –≤–ї–Є—П–љ–Є–µ–Љ –ї–µ—З–µ–љ–Є—П –Ф–µ––Э–Њ–ї–Њ–Љ (–Є—Б—Б–ї–µ–і—Г–µ–Љ–∞—П –≥—А—Г–њ–њ–∞) –Є –∞–љ—В–∞—Ж–Є–і–∞–Љ–Є (–≥—А—Г–њ–њ–∞ —Б—А–∞–≤–љ–µ–љ–Є—П).
–Я–Њ–ї–Њ–ґ–Є—В–µ–ї—М–љ–∞—П –і–Є–љ–∞–Љ–Є–Ї–∞ —Г –±–Њ–ї—М–љ—Л—Е –Є—Б—Б–ї–µ–і—Г–µ–Љ–Њ–є –≥—А—Г–њ–њ—Л –љ–∞—З–Є–љ–∞–ї–∞ –њ–Њ—П–≤–ї—П—В—М—Б—П —Г–ґ–µ —Б–њ—Г—Б—В—П –љ–µ–і–µ–ї—О:
• —Г–Љ–µ–љ—М—И–∞–ї–∞—Б—М —З–∞—Б—В–Њ—В–∞ —Б—В—Г–ї–∞ –і–Њ 2–3 —А–∞–Ј/—Б—Г—В., –Ї–∞–ї —Б—В–∞–љ–Њ–≤–Є–ї—Б—П –±–Њ–ї–µ–µ –Њ—Д–Њ—А–Љ–ї–µ–љ–љ—Л–Љ, —Г–Љ–µ–љ—М—И–∞–ї–∞—Б—М –њ—А–Є–Љ–µ—Б—М –≤ –љ–µ–Љ —Б–ї–Є–Ј–Є;
• —Г–Љ–µ–љ—М—И–∞–ї—Б—П –Љ–µ—В–µ–Њ—А–Є–Ј–Љ –Є —Г—А—З–∞–љ–Є–µ –≤ –ґ–Є–≤–Њ—В–µ;
• —А–µ–ґ–µ –±–µ—Б–њ–Њ–Ї–Њ–Є–ї–Є –±–Њ–ї–Є –≤ –ґ–Є–≤–Њ—В–µ.
–Ъ –љ–∞—З–∞–ї—Г —В—А–µ—В—М–µ–є –љ–µ–і–µ–ї–Є —Г 16 –±–Њ–ї—М–љ—Л—Е –љ–∞—Б—В—Г–њ–Є–ї–∞ —Г—Б—В–Њ–є—З–Є–≤–∞—П –Ї–ї–Є–љ–Є—З–µ—Б–Ї–∞—П —А–µ–Љ–Є—Б—Б–Є—П –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П, –∞ —Г 4 – —Г–Љ–µ–љ—М—И–Є–ї–Є—Б—М –µ–≥–Њ –њ—А–Њ—П–≤–ї–µ–љ–Є—П.
–Т –≥—А—Г–њ–њ–µ —Б—А–∞–≤–љ–µ–љ–Є—П –љ–Є —Г –Њ–і–љ–Њ–≥–Њ –Є–Ј –±–Њ–ї—М–љ—Л—Е —Г–ї—Г—З—И–µ–љ–Є—П –љ–µ –љ–∞—Б—В—Г–њ–Є–ї–Њ, –≤ —Б–≤—П–Ј–Є —Б —З–µ–Љ, –љ–∞—З–Є–љ–∞—П —Б–Њ –≤—В–Њ—А–Њ–є –љ–µ–і–µ–ї–Є, –Є–Љ –±—Л–ї–∞ –љ–∞–Ј–љ–∞—З–µ–љ–∞ —Б—В–∞–љ–і–∞—А—В–љ–∞—П –Ї–Њ–Љ–њ–ї–µ–Ї—Б–љ–∞—П —В–µ—А–∞–њ–Є—П –°–†–Ъ. –Ю–љ–∞ –≤–Ї–ї—О—З–∞–ї–∞: —Б–њ–∞–Ј–Љ–Њ–ї–Є—В–Є–Ї–Є, –Ї–Є—И–µ—З–љ—Л–µ –∞–љ—В–Є—Б–µ–њ—В–Є–Ї–Є —Б –њ–Њ—Б–ї–µ–і—Г—О—Й–Є–Љ –і–ї–Є—В–µ–ї—М–љ—Л–Љ –Ї—Г—А—Б–Њ–Љ –Њ–і–љ–Њ–≥–Њ –Є–Ј –њ—А–Њ–±–Є–Њ—В–Є–Ї–Њ–≤, –њ—А–Є –Љ–µ—В–µ–Њ—А–Є–Ј–Љ–µ – –∞–Ї—В–Є–≤–Є—А–Њ–≤–∞–љ–љ—Л–є —Г–≥–Њ–ї—М.
–Т —В–∞–±–ї–Є—Ж–µ 3 –њ–Њ–Ї–∞–Ј–∞–љ —Б–Њ—Б—В–∞–≤ —Д–µ–Ї–∞–ї—М–љ–Њ–є –Љ–Є–Ї—А–Њ—Д–ї–Њ—А—Л —Г –±–Њ–ї—М–љ—Л—Е –°–†–Ъ –Є –љ–∞–±–ї—О–і–∞–µ–Љ—Л–µ –Є–Ј–Љ–µ–љ–µ–љ–Є—П –њ–Њ—Б–ї–µ –ї–µ—З–µ–љ–Є—П.
–Ш–Ј —В–∞–±–ї–Є—Ж—Л 3 —Б–ї–µ–і—Г–µ—В, —З—В–Њ —Г –≤—Б–µ—Е –±–Њ–ї—М–љ—Л—Е –і–Њ –ї–µ—З–µ–љ–Є—П –Њ—В–Љ–µ—З–∞–ї–Њ—Б—М —Б–љ–Є–ґ–µ–љ–Є–µ —З–Є—Б–ї–µ–љ–љ–Њ—Б—В–Є –љ–Њ—А–Љ–∞–ї—М–љ–Њ–є —Д–ї–Њ—А—Л —В–Њ–ї—Б—В–Њ–є –Ї–Є—И–Ї–Є –±–Є—Д–Є–і–Њ–, –ї–∞–Ї—В–Њ–±–∞–Ї—В–µ—А–Є–є, –±–∞–Ї—В–µ—А–Њ–Є–і–Њ–≤ –Є —Г–≤–µ–ї–Є—З–µ–љ–Є–µ —Г—Б–ї–Њ–≤–љ–Њ––њ–∞—В–Њ–≥–µ–љ–љ—Л—Е –Љ–Є–Ї—А–Њ–Њ—А–≥–∞–љ–Є–Ј–Љ–Њ–≤. –Я–∞—В–Њ–≥–µ–љ–љ—Л—Е –Љ–Є–Ї—А–Њ–Њ—А–≥–∞–љ–Є–Ј–Љ–Њ–≤ –Њ–±–љ–∞—А—Г–ґ–µ–љ–Њ –љ–µ –±—Л–ї–Њ.
–Я–Њ—Б–ї–µ –ї–µ—З–µ–љ–Є—П –Ф–µ––Э–Њ–ї–Њ–Љ –њ–Њ–Ї–∞–Ј–∞—В–µ–ї–Є –Љ–Є–Ї—А–Њ–±–љ–Њ–≥–Њ –њ—А–Њ—Д–Є–ї—П —Д–µ–Ї–∞–ї–Є–є —Г–ї—Г—З—И–Є–ї–Є—Б—М. –Т–Њ––њ–µ—А–≤—Л—Е, —Б–љ–Є–Ј–Є–ї–Њ—Б—М –Ї–Њ–ї–Є—З–µ—Б—В–≤–Њ —Г—Б–ї–Њ–≤–љ–Њ––њ–∞—В–Њ–≥–µ–љ–љ–Њ–є –Љ–Є–Ї—А–Њ—Д–ї–Њ—А—Л: —А–µ–ґ–µ –≤—Л—П–≤–ї—П–ї–Є—Б—М –≥–µ–Љ–Њ–ї–Є–Ј–Є—А—Г—О—Й–∞—П –Ї–Є—И–µ—З–љ–∞—П –њ–∞–ї–Њ—З–Ї–∞, –Ї–Њ–Ї–Ї–Є, –Ї–ї–Њ—Б—В—А–Є–і–Є–Є, –Ї–ї–µ–±—Б–Є–µ–ї–ї—Л, –њ—А–Њ—В–µ–є –Є –Ї–∞–љ–і–Є–і–∞. –Т–Њ––≤—В–Њ—А—Л—Е, –≤—Л—А–Њ—Б–ї–Њ (–≤ —Б—А–µ–і–љ–µ–Љ –љ–∞ –њ–Њ—А—П–і–Њ–Ї) —З–Є—Б–ї–Њ –ї–∞–Ї—В–Њ– –Є –±–Є—Д–Є–і–Њ–±–∞–Ї—В–µ—А–Є–є.
–Э–∞–Є–±–Њ–ї–µ–µ –Є–љ—В–µ—А–µ—Б–љ—Л–µ –Є–Ј–Љ–µ–љ–µ–љ–Є—П, –љ–∞ –љ–∞—И –≤–Ј–≥–ї—П–і, –њ—А–Њ–Є–Ј–Њ—И–ї–Є –≤ —Б–Њ—Б—В–∞–≤–µ –Љ—Г–Ї–Њ–Ј–љ–Њ–є –Љ–Є–Ї—А–Њ—Д–ї–Њ—А—Л, –Є–Ј—Г—З–µ–љ–љ–Њ–є —Б –њ–Њ–Љ–Њ—Й—М—О –Љ–µ—В–Њ–і–∞ –У–•––Ь–°. –° –µ–≥–Њ –њ–Њ–Љ–Њ—Й—М—О —Г–і–∞–ї–Њ—Б—М –Є–Ј–Љ–µ—А–Є—В—М —З–Є—Б–ї–µ–љ–љ–Њ—Б—В—М 57 —В–∞–Ї—Б–Њ–љ–Њ–≤ –Љ–Є–Ї—А–Њ–Њ—А–≥–∞–љ–Є–Ј–Љ–Њ–≤ –Ї–Є—И–µ—З–љ–Є–Ї–∞.
–Р–љ–∞–ї–Є–Ј –Љ–Є–Ї—А–Њ–±–љ–Њ–≥–Њ —Б–Њ—Б—В–∞–≤–∞ –Љ—Г–Ї–Њ–Ј–љ–Њ–є –Љ–Є–Ї—А–Њ—Д–ї–Њ—А—Л —В–Њ—Й–µ–є –Ї–Є—И–Ї–Є —Г –±–Њ–ї—М–љ—Л—Е –°–†–Ъ —Б –і–Є–∞—А–µ–µ–є –њ–Њ–Ї–∞–Ј–∞–ї —А–∞–Ј–ї–Є—З–љ—Л–µ –Њ—В–Ї–ї–Њ–љ–µ–љ–Є—П –њ–Њ —Б—А–∞–≤–љ–µ–љ–Є—О —Б –њ–Њ–Ї–∞–Ј–∞—В–µ–ї—П–Љ–Є –Ј–і–Њ—А–Њ–≤—Л—Е –ї—О–і–µ–є. –£ –≤—Б–µ—Е –±–Њ–ї—М–љ—Л—Е –Њ–±—Й–µ–µ —Б–Њ–і–µ—А–ґ–∞–љ–Є–µ –љ–Њ—А–Љ–Њ—Д–ї–Њ—А—Л –±—Л–ї–Њ —Б–љ–Є–ґ–µ–љ–Њ –≤ 7–8 —А–∞–Ј –њ–Њ —Б—А–∞–≤–љ–µ–љ–Є—О —Б –љ–Њ—А–Љ–Њ–є, –њ—А–Є –Њ–і–љ–Њ–≤—А–µ–Љ–µ–љ–љ–Њ–Љ —А–Њ—Б—В–µ —Г—Б–ї–Њ–≤–љ–Њ––њ–∞—В–Њ–≥–µ–љ–љ–Њ–є –Љ–Є–Ї—А–Њ—Д–ї–Њ—А—Л. –Я–Њ—Б–ї–µ 3––љ–µ–і–µ–ї—М–љ–Њ–≥–Њ –Ї—Г—А—Б–∞ –ї–µ—З–µ–љ–Є—П –Ф–µ––Э–Њ–ї–Њ–Љ —З–Є—Б–ї–µ–љ–љ–Њ—Б—В—М —А—П–і–∞ –Љ–Є–Ї—А–Њ–Њ—А–≥–∞–љ–Є–Ј–Љ–Њ–≤ —Б—В–∞–ї–∞ –њ—А–Є–±–ї–Є–ґ–∞—В—М—Б—П –Ї –љ–Њ—А–Љ–µ, –≤ –Њ—Б–љ–Њ–≤–љ–Њ–Љ –Ј–∞ —Б—З–µ—В —Б–љ–Є–ґ–µ–љ–Є—П –Ї–Њ–љ—Ж–µ–љ—В—А–∞—Ж–Є–Є —Г—Б–ї–Њ–≤–љ–Њ– –њ–∞—В–Њ–≥–µ–љ–љ—Л—Е –Љ–Є–Ї—А–Њ–Њ—А–≥–∞–љ–Є–Ј–Љ–Њ–≤.
–Т—Л—П–≤–ї–µ–љ–Њ —В–∞–Ї–ґ–µ —Б–љ–Є–ґ–µ–љ–Є–µ —З–Є—Б–ї–µ–љ–љ–Њ—Б—В–Є –∞–Ї—В–Є–љ–Њ–±–∞–Ї—В–µ—А–Є–є (Actinomyces, Streptomyces, Nocardia), –≥—А–Є–±–Њ–≤ –Є —Ж–Є—В–Њ–Љ–µ–≥–∞–ї–Њ–≤–Є—А—Г—Б–∞. –Ч–∞–Љ–µ—В–љ–Њ —Г–Љ–µ–љ—М—И–Є–ї–Њ—Б—М –њ–Њ —Б—А–∞–≤–љ–µ–љ–Є—О —Б –љ–Њ—А–Љ–Њ–є –Ї–Њ–ї–Є—З–µ—Б—В–≤–Њ –Ї–Њ–Ї–Ї–Њ–≤ (—Б—В–∞—Д–Є–ї–Њ–Ї–Њ–Ї–Ї–Њ–≤, —Н–љ—В–µ—А–Њ–Ї–Њ–Ї–Ї–Њ–≤, —Н–љ—В–µ—А–Њ–Ї–Њ–Ї–Ї–Њ–≤), –Є–Ј–љ–∞—З–∞–ї—М–љ–Њ –њ—А–µ–≤—Л—И–∞–≤—И–Є—Е –љ–Њ—А–Љ—Г. –І–Є—Б–ї–µ–љ–љ–Њ—Б—В—М Cl. difficile –Є –°l. perfringes –љ–µ –њ—А–µ–≤—Л—И–∞–ї–∞ –љ–Њ—А–Љ—Л, —В–µ–Љ –љ–µ –Љ–µ–љ–µ–µ –Є—Е –Ї–Њ–ї–Є—З–µ—Б—В–≤–Њ –њ–Њ—Б–ї–µ –ї–µ—З–µ–љ–Є—П —Г–Љ–µ–љ—М—И–Є–ї–Њ—Б—М –љ–∞ 20–60%.
–Т –Њ—В–ї–Є—З–Є–µ –Њ—В –∞–љ—В–Є–±–Є–Њ—В–Є–Ї–Њ–≤ –Ф–µ––Э–Њ–ї –љ–µ –њ–Њ–і–∞–≤–ї—П–µ—В –љ–Њ—А–Љ–∞–ї—М–љ—Г—О –Љ–Є–Ї—А–Њ—Д–ї–Њ—А—Г –Ї–Є—И–µ—З–љ–Є–Ї–∞. –Ґ–∞–Ї, –љ–∞ –њ—А–Є–Љ–µ—А–µ –±–Є—Д–Є–і–Њ–±–∞–Ї—В–µ—А–Є–є –Љ–Њ–ґ–љ–Њ –њ–Њ–Ї–∞–Ј–∞—В—М —Б—В–∞–±–Є–ї–Є–Ј–Є—А—Г—О—Й–µ–µ –≤–ї–Є—П–љ–Є–µ –Ф–µ––Э–Њ–ї–∞ –љ–∞ –Љ–Є–Ї—А–Њ–±–љ–Њ–µ —Б–Њ–Њ–±—Й–µ—Б—В–≤–Њ. –Т —А–µ–Ј—Г–ї—М—В–∞—В–µ –ї–µ—З–µ–љ–Є—П –њ—А–Њ–Є—Б—Е–Њ–і–Є–ї–Њ —Г–Љ–µ–љ—М—И–µ–љ–Є–µ –Є–ї–Є —Г–≤–µ–ї–Є—З–µ–љ–Є–µ –і–Њ –љ–Њ—А–Љ—Л —З–Є—Б–ї–∞ –±–Є—Д–Є–і–Њ–±–∞–Ї—В–µ—А–Є–є –Є –Ј–∞–Љ–µ—В–љ–Њ–µ –Њ—В—Б—Г—В—Б—В–≤–Є–µ —Г–≥–љ–µ—В–∞—О—Й–µ–≥–Њ —Н—Д—Д–µ–Ї—В–∞ –њ—А–µ–њ–∞—А–∞—В–∞ –њ—А–Є –Є—Б—Е–Њ–і–љ–Њ –љ–Њ—А–Љ–∞–ї—М–љ–Њ–Љ –Є—Е —Б–Њ–і–µ—А–ґ–∞–љ–Є–Є (—А–Є—Б. 1).
–Т—Л—А–∞–≤–љ–Є–≤–∞–ї–∞—Б—М –Ї–Њ–љ—Ж–µ–љ—В—А–∞—Ж–Є—П –Є –і—А—Г–≥–Є—Е –Њ—Б–љ–Њ–≤–љ—Л—Е –љ–Њ—А–Љ–∞–ї—М–љ—Л—Е –Њ–±–Є—В–∞—В–µ–ї–µ–є —Б–ї–Є–Ј–Є—Б—В–Њ–є –Њ–±–Њ–ї–Њ—З–Ї–Є —В–Њ—Й–µ–є –Ї–Є—И–Ї–Є – —Н—Г–±–∞–Ї—В–µ—А–Є–є (E. moniliforme, E. nodatum, E. sabureum –Є –і—А.), –∞ —В–∞–Ї–ґ–µ –њ—А–Њ–њ–Є–Њ–љ–Њ–≤—Л—Е –±–∞–Ї—В–µ—А–Є–є (—А–Є—Б. 2).
–Ъ–Њ–љ—Ж–µ–љ—В—А–∞—Ж–Є—П Propionibacterium spp. – –љ–Њ—А–Љ–∞–ї—М–љ—Л—Е –Њ–±–Є—В–∞—В–µ–ї–µ–є –Љ—Г–Ї–Њ–Ј–љ–Њ–є –Љ–Є–Ї—А–Њ—Д–ї–Њ—А—Л —В–Њ—Й–µ–є –Ї–Є—И–Ї–Є, –њ—А–Є –Є—Б—Е–Њ–і–љ–Њ–Љ –љ–Є–Ј–Ї–Њ–Љ —Г—А–Њ–≤–љ–µ (–љ–∞ –Њ–і–Є–љ––і–≤–∞ –њ–Њ—А—П–і–Ї–∞ –љ–Є–ґ–µ –љ–Њ—А–Љ—Л) –њ–Њ—Б–ї–µ –Ї—Г—А—Б–∞ –Ф–µ––Э–Њ–ї–Њ–Љ —Г–≤–µ–ї–Є—З–Є–≤–∞–ї–Є—Б—М –≤ —З–Є—Б–ї–µ–љ–љ–Њ—Б—В–Є –Є –њ—А–Є–±–ї–Є–ґ–∞–ї–Є—Б—М –Ї –љ–Њ—А–Љ–µ.
–Ю—В–Љ–µ—З–∞–ї–∞—Б—М —В–µ–љ–і–µ–љ—Ж–Є—П –Ї –Ї–Њ–ї–Є—З–µ—Б—В–≤–µ–љ–љ–Њ–є –љ–Њ—А–Љ–∞–ї–Є–Ј–∞—Ж–Є–Є –Љ–Є–Ї—А–Њ–±–Є–Њ—В—Л —Б–ї–Є–Ј–Є—Б—В–Њ–є –Њ–±–Њ–ї–Њ—З–Ї–Є —В–Њ—Й–µ–є –Ї–Є—И–Ї–Є: —Г–Љ–µ–љ—М—И–µ–љ–Є–µ –Ї–Њ–љ—Ж–µ–љ—В—А–∞—Ж–Є–Є –Љ–Є–Ї—А–Њ–±–Њ–≤, –њ—А–Њ—П–≤–ї—П—О—Й–Є—Е –Є–Ј–±—Л—В–Њ—З–љ—Л–є —А–Њ—Б—В, –Є —Г–≤–µ–ї–Є—З–µ–љ–Є–µ —З–Є—Б–ї–µ–љ–љ–Њ—Б—В–Є –і–µ—Д–Є—Ж–Є—В–љ—Л—Е –Љ–Є–Ї—А–Њ–±–Њ–≤. –Я—А–Є —Н—В–Њ–Љ –њ–Њ–ї–љ–Њ–≥–Њ –≤–Њ—Б—Б—В–∞–љ–Њ–≤–ї–µ–љ–Є—П –љ–µ –љ–∞–±–ї—О–і–∞–ї–Њ—Б—М, —З—В–Њ —П–≤–Є–ї–Њ—Б—М –њ–Њ–≤–Њ–і–Њ–Љ –і–ї—П –њ—А–Њ–і–Њ–ї–ґ–µ–љ–Є—П –ї–µ—З–µ–љ–Є—П —Н—В–Є—Е –±–Њ–ї—М–љ—Л—Е –њ—А–Њ– –Є –њ—А–µ–±–Є–Њ—В–Є–Ї–∞–Љ–Є.
–Ґ–∞–Ї–Є–Љ –Њ–±—А–∞–Ј–Њ–Љ, —Г –≤—Б–µ—Е –±–Њ–ї—М–љ—Л—Е –°–†–Ъ –њ–Њ—Б–ї–µ –Ј–∞–≤–µ—А—И–µ–љ–Є—П –Ї—Г—А—Б–∞ –Ф–µ––Э–Њ–ї–Њ–Љ –њ–Њ–ї—Г—З–µ–љ–∞ –њ–Њ–ї–Њ–ґ–Є—В–µ–ї—М–љ–∞—П –і–Є–љ–∞–Љ–Є–Ї–∞ –≤ —Б–Њ—Б—В–∞–≤–µ —Д–µ–Ї–∞–ї—М–љ–Њ–є –Є –Љ—Г–Ї–Њ–Ј–љ–Њ–є –Љ–Є–Ї—А–Њ—Д–ї–Њ—А—Л —В–Њ—Й–µ–є –Ї–Є—И–Ї–Є, –њ—А–Њ—П–≤–ї—П—О—Й–∞—П—Б—П –њ—А–µ–ґ–і–µ –≤—Б–µ–≥–Њ —Б–љ–Є–ґ–µ–љ–Є–µ–Љ –Ї–Њ–љ—Ж–µ–љ—В—А–∞—Ж–Є–Є —Г—Б–ї–Њ–≤–љ–Њ––њ–∞—В–Њ–≥–µ–љ–љ–Њ–є –Љ–Є–Ї—А–Њ—Д–ї–Њ—А—Л.
–Т –≥—А—Г–њ–њ–µ —Б—А–∞–≤–љ–µ–љ–Є—П —Г –±–Њ–ї—М–љ—Л—Е –°–†–Ъ –љ–∞ —Д–Њ–љ–µ –њ—А–Є–µ–Љ–∞ –∞–љ—В–∞—Ж–Є–і–Њ–≤ –Є –і–Є–µ—В–Њ—В–µ—А–∞–њ–Є–Є –Ј–љ–∞—З–Є–Љ–Њ–≥–Њ —Г–ї—Г—З—И–µ–љ–Є—П —Б–Њ—Б—В–∞–≤–∞ –Ї–Є—И–µ—З–љ–Њ–є –Љ–Є–Ї—А–Њ—Д–ї–Њ—А—Л –і–Њ—Б—В–Є—З—М –љ–µ —Г–і–∞–ї–Њ—Б—М. –Т –њ–Њ–≤—В–Њ—А–љ—Л—Е –њ–Њ—Б–µ–≤–∞—Е –Ї–∞–ї–∞ —Б–Њ—Е—А–∞–љ—П–ї—Б—П –і–µ—Д–Є—Ж–Є—В –±–Є—Д–Є–і–Њ– –Є –ї–∞–Ї—В–Њ–±–∞–Ї—В–µ—А–Є–є, –њ–Њ–Ї–∞–Ј–∞—В–µ–ї–Є —Г—Б–ї–Њ–≤–љ–Њ––њ–∞—В–Њ–≥–µ–љ–љ–Њ–є –Љ–Є–Ї—А–Њ—Д–ї–Њ—А—Л –Њ—Б—В–∞–≤–∞–ї–Є—Б—М –њ–Њ–≤—Л—И–µ–љ–љ—Л–Љ–Є.
–Ґ–∞–Ї–Є–Љ –Њ–±—А–∞–Ј–Њ–Љ, –њ—А–Є—З–Є–љ–Њ–є —А–∞–Ј–≤–Є—В–Є—П –°–†–Ъ —Г –љ–∞—И–Є—Е –±–Њ–ї—М–љ—Л—Е –±—Л–ї–Њ –≤—Л—А–∞–ґ–µ–љ–љ–Њ–µ –Є–Ј–Љ–µ–љ–µ–љ–Є–µ —Н—Г–±–Є–Њ–Ј–∞ —Б–ї–Є–Ј–Є—Б—В–Њ–є –Њ–±–Њ–ї–Њ—З–Ї–Є —В–Њ—Й–µ–є –Ї–Є—И–Ї–Є –Є —Б–Њ—Б—В–∞–≤–∞ —Д–µ–Ї–∞–ї—М–љ–Њ–є –Љ–Є–Ї—А–Њ—Д–ї–Њ—А—Л. –£ –≤—Б–µ—Е –±–Њ–ї—М–љ—Л—Е –≤ –њ–Њ—Б–µ–≤–∞—Е –Ї–∞–ї–∞ –≤—Л—П–≤–ї–µ–љ–Њ —Б–љ–Є–ґ–µ–љ–Є–µ –Ї–Њ–љ—Ж–µ–љ—В—А–∞—Ж–Є–Є –±–Є—Д–Є–і—Г–Љ–±–∞–Ї—В–µ—А–Є–є –Є –ї–∞–Ї—В–Њ–±–∞—Ж–Є–ї–ї. –Ю–і–љ–Њ–≤—А–µ–Љ–µ–љ–љ–Њ –Њ—В–Љ–µ—З–∞–ї—Б—П —А–Њ—Б—В —Г—Б–ї–Њ–≤–љ–Њ––њ–∞—В–Њ–≥–µ–љ–љ–Њ–є –Љ–Є–Ї—А–Њ—Д–ї–Њ—А—Л, —З–∞—Й–µ –≤—Б–µ–≥–Њ –і—А–Њ–ґ–ґ–µ–њ–Њ–і–Њ–±–љ—Л—Е –≥—А–Є–±–Њ–≤, –Ї–Њ–Ї–Ї–Њ–≤ –Љ–Є–Ї—А–Њ—Д–ї–Њ—А—Л, –Ї–ї–Њ—Б—В—А–Є–і–Є–є, –њ—А–Њ—В–µ—П, –Ї–ї–µ–±—Б–Є–µ–ї–ї. –Э–µ–Њ–±—Е–Њ–і–Є–Љ–Њ –Њ—В–Љ–µ—В–Є—В—М, —З—В–Њ —А–Њ—Б—В–∞ –њ–∞—В–Њ–≥–µ–љ–љ—Л—Е —Н–љ—В–µ—А–Њ–±–∞–Ї—В–µ—А–Є–є –љ–µ –љ–∞–±–ї—О–і–∞–ї–Њ—Б—М –љ–Є —Г –Њ–і–љ–Њ–≥–Њ –±–Њ–ї—М–љ–Њ–≥–Њ. –£ –≤—Б–µ—Е –±–Њ–ї—М–љ—Л—Е –°–†–Ъ —Б –і–Є–∞—А–µ–µ–є –Њ—В–Љ–µ—З–∞–ї–Є—Б—М –Ј–љ–∞—З–Є—В–µ–ї—М–љ—Л–µ –љ–∞—А—Г—И–µ–љ–Є—П –Љ—Г–Ї–Њ–Ј–љ–Њ–є –Љ–Є–Ї—А–Њ—Д–ї–Њ—А—Л —В–Њ—Й–µ–є –Ї–Є—И–Ї–Є, —З—В–Њ –њ—А–Њ—П–≤–Є–ї–Њ—Б—М –Є–Ј–Љ–µ–љ–µ–љ–Є—П–Љ–Є –і–Њ 57 –Љ–Є–Ї—А–Њ–±–љ—Л—Е —В–∞–Ї—Б–Њ–љ–Њ–≤, –≤—Л—П–≤–ї–µ–љ–љ—Л—Е —Б –њ–Њ–Љ–Њ—Й—М—О –У–•––Ь–°. –Э–∞–±–ї—О–і–∞–ї–Њ—Б—М –Ј–љ–∞—З–Є—В–µ–ї—М–љ–Њ–µ —Б–љ–Є–ґ–µ–љ–Є–µ –Ї–Њ–љ—Ж–µ–љ—В—А–∞—Ж–Є–Є –љ–Њ—А–Љ–Њ—Д–ї–Њ—А—Л (–і–Њ 15–20 —А–∞–Ј) —Б –Њ–і–љ–Њ–≤—А–µ–Љ–µ–љ–љ—Л–Љ —А–Њ—Б—В–Њ–Љ —Г—Б–ї–Њ–≤–љ–Њ––њ–∞—В–Њ–≥–µ–љ–љ–Њ–є –Љ–Є–Ї—А–Њ—Д–ї–Њ—А—Л.
–Т —А–µ–Ј—Г–ї—М—В–∞—В–µ 3––љ–µ–і–µ–ї—М–љ–Њ–≥–Њ –Ї—Г—А—Б–∞ –Ф–µ––Э–Њ–ї–Њ–Љ –њ–Њ–ї—Г—З–µ–љ–∞ –њ–Њ–ї–Њ–ґ–Є—В–µ–ї—М–љ–∞—П –і–Є–љ–∞–Љ–Є–Ї–∞ —В–µ—З–µ–љ–Є—П –°–†–Ъ —Б –њ—А–µ–Њ–±–ї–∞–і–∞–љ–Є–µ–Љ –і–Є–∞—А–µ–Є, —Е–∞—А–∞–Ї—В–µ—А–Є–Ј—Г—О—Й–∞—П—Б—П —Г–Љ–µ–љ—М—И–µ–љ–Є–µ–Љ —З–∞—Б—В–Њ—В—Л —Б—В—Г–ї–∞, –±–Њ–ї–µ–≤–Њ–≥–Њ —Б–Є–љ–і—А–Њ–Љ–∞ –Є –Љ–µ—В–µ–Њ—А–Є–Ј–Љ–∞. –≠—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В—М –Ф–µ––Э–Њ–ї–∞ –≤ –ї–µ—З–µ–љ–Є–Є –±–Њ–ї—М–љ—Л—Е –°–†–Ъ —Б –њ—А–µ–Њ–±–ї–∞–і–∞–љ–Є–µ–Љ –і–Є–∞—А–µ–Є –Њ–±—К—П—Б–љ—П–µ—В—Б—П —А—П–і–Њ–Љ –њ—А–Є—З–Є–љ.
–Т –≥—А—Г–њ–њ–µ –±–Њ–ї—М–љ—Л—Е –°–†–Ъ, –∞—Б—Б–Њ—Ж–Є–Є—А–Њ–≤–∞–љ–љ–Њ–≥–Њ —Б –і–Є—Б–±–∞–Ї—В–µ—А–Є–Њ–Ј–Њ–Љ –Ї–Є—И–µ—З–љ–Є–Ї–∞, –њ–Њ—Б–ї–µ 3––љ–µ–і–µ–ї—М–љ–Њ–≥–Њ –Ї—Г—А—Б–∞ –Ф–µ––Э–Њ–ї–Њ–Љ –±—Л–ї–∞ –і–Њ—Б—В–Є–≥–љ—Г—В–∞ —А–µ–Љ–Є—Б—Б–Є—П –°–†–Ъ –Є —Г–ї—Г—З—И–Є–ї—Б—П —Б–Њ—Б—В–∞–≤ –Љ—Г–Ї–Њ–Ј–љ–Њ–є –Є —Д–µ–Ї–∞–ї—М–љ–Њ–є –Љ–Є–Ї—А–Њ—Д–ї–Њ—А—Л. –Я—А–Є —Н—В–Њ–Љ –Њ—В–Љ–µ—З–∞–ї–Њ—Б—М —Б–љ–Є–ґ–µ–љ–Є–µ –Ї–Њ–љ—Ж–µ–љ—В—А–∞—Ж–Є–Є —Г—Б–ї–Њ–≤–љ–Њ––њ–∞—В–Њ–≥–µ–љ–љ–Њ–є –Є –≤—В–Њ—А–Є—З–љ—Л–є —А–Њ—Б—В –љ–Њ—А–Љ–∞–ї—М–љ–Њ–є –Љ–Є–Ї—А–Њ—Д–ї–Њ—А—Л. –Ч–∞–Љ–µ—В–љ–Њ —Г–Љ–µ–љ—М—И–Є–ї–∞—Б—М —З–Є—Б–ї–µ–љ–љ–Њ—Б—В—М –Ї–Њ–Ї–Ї–Њ–≤, –∞–Ї—В–Є–љ–Њ–±–∞–Ї—В–µ—А–Є–є (Actinomyces, Streptomyces, Nocardia), –Ї–ї–Њ—Б—В—А–Є–і–Є–є, –≥—А–Є–±–Њ–≤ –Є —Ж–Є—В–Њ–Љ–µ–≥–∞–ї–Њ–≤–Є—А—Г—Б–∞. –Т—Л—П–≤–ї–µ–љ–∞ —В–µ–љ–і–µ–љ—Ж–Є—П –Ї —А–Њ—Б—В—Г –љ–Њ—А–Љ–Њ—Д–ї–Њ—А—Л —Б –Њ–і–љ–Њ–≤—А–µ–Љ–µ–љ–љ—Л–Љ —Г–ї—Г—З—И–µ–љ–Є–µ–Љ —Б–Њ–Њ—В–љ–Њ—И–µ–љ–Є—П —А–∞–Ј–ї–Є—З–љ—Л—Е –≥—А—Г–њ–њ –Љ–Є–Ї—А–Њ–Њ—А–≥–∞–љ–Є–Ј–Љ–Њ–≤ –≤ –Љ–Є–Ї—А–Њ–±–љ–Њ–Љ —Б–Њ–Њ–±—Й–µ—Б—В–≤–µ —Б–ї–Є–Ј–Є—Б—В–Њ–є –Њ–±–Њ–ї–Њ—З–Ї–Є —В–Њ—Й–µ–є –Ї–Є—И–Ї–Є.
–Э–µ–Њ–±—Е–Њ–і–Є–Љ–Њ –њ–Њ–і—З–µ—А–Ї–љ—Г—В—М, —З—В–Њ –≤ –Њ—В–ї–Є—З–Є–µ –Њ—В –∞–љ—В–Є–±–Є–Њ—В–Є–Ї–Њ–≤ –Ф–µ––Э–Њ–ї –љ–µ –њ–Њ–і–∞–≤–ї—П–µ—В —А–Њ—Б—В –љ–Њ—А–Љ–Њ—Д–ї–Њ—А—Л –≤ —А–∞–Ј–ї–Є—З–љ—Л—Е –Њ—В–і–µ–ї–∞—Е –Ї–Є—И–µ—З–љ–Є–Ї–∞. –Я—А–µ–њ–∞—А–∞—В –Њ–±–ї–∞–і–∞–µ—В —И–Є—А–Њ–Ї–Є–Љ –∞–љ—В–Є–±–∞–Ї—В–µ—А–Є–∞–ї—М–љ—Л–Љ —Б–њ–µ–Ї—В—А–Њ–Љ –∞–Ї—В–Є–≤–љ–Њ—Б—В–Є –Є –Љ–Њ–ґ–µ—В –±—Л—В—М –љ–∞–Ј–љ–∞—З–µ–љ –≤ –Ї–∞—З–µ—Б—В–≤–µ –Ї–Є—И–µ—З–љ–Њ–≥–Њ –∞–љ—В–Є—Б–µ–њ—В–Є–Ї–∞. –Ъ—А–Њ–Љ–µ —В–Њ–≥–Њ, –≤–Є—Б–Љ—Г—В, –≤—Е–Њ–і—П—Й–Є–є –≤ —Б–Њ—Б—В–∞–≤ –њ—А–µ–њ–∞—А–∞—В–∞, –Њ–±–ї–∞–і–∞–µ—В –≤—П–ґ—Г—Й–Є–Љ –і–µ–є—Б—В–≤–Є–µ–Љ, —З—В–Њ –њ—А–Є–≤–Њ–і–Є—В –Ї –Ј–∞–Љ–µ–і–ї–µ–љ–Є—О –Љ–Њ—В–Њ—А–Є–Ї–Є –Ї–Є—И–µ—З–љ–Є–Ї–∞ –Є —Б–њ–Њ—Б–Њ–±—Б—В–≤—Г–µ—В –љ–∞—Б—В—Г–њ–ї–µ–љ–Є—О —А–µ–Љ–Є—Б—Б–Є–Є –°–†–Ъ —Б –њ—А–µ–Њ–±–ї–∞–і–∞–љ–Є–µ–Љ –і–Є–∞—А–µ–Є.
–Т –≥—А—Г–њ–њ–µ —Б—А–∞–≤–љ–µ–љ–Є—П –Ј–љ–∞—З–Є—В–µ–ї—М–љ–Њ–≥–Њ —Г–ї—Г—З—И–µ–љ–Є—П –і–Њ—Б—В–Є—З—М –љ–µ —Г–і–∞–ї–Њ—Б—М. –Э–∞—А—П–і—Г —Б –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є–Љ–Є —Б–Є–Љ–њ—В–Њ–Љ–∞–Љ–Є —Б–Њ—Е—А–∞–љ—П–ї–Є—Б—М –љ–∞—А—Г—И–µ–љ–Є—П –Љ–Є–Ї—А–Њ—Д–ї–Њ—А—Л –Ї–Є—И–µ—З–љ–Є–Ї–∞. –Т —Б–≤—П–Ј–Є —Б —З–µ–Љ, –Ї–∞–Ї —Г–ґ–µ –±—Л–ї–Њ —Б–Ї–∞–Ј–∞–љ–Њ, —Н—В–Є–Љ –±–Њ–ї—М–љ—Л–Љ –±—Л–ї–∞ –љ–∞–Ј–љ–∞—З–µ–љ–∞ —Б—В–∞–љ–і–∞—А—В–љ–∞—П —В–µ—А–∞–њ–Є—П –°–†–Ъ.
–Ґ–∞–Ї–Є–Љ –Њ–±—А–∞–Ј–Њ–Љ, –≤ —А–µ–Ј—Г–ї—М—В–∞—В–µ 3––љ–µ–і–µ–ї—М–љ–Њ–≥–Њ –Ї—Г—А—Б–∞ —В–µ—А–∞–њ–Є–Є –Ф–µ––Э–Њ–ї–Њ–Љ –њ–Њ–ї—Г—З–µ–љ–∞ –і–Њ—Б—В–Њ–≤–µ—А–љ–∞—П –њ–Њ–ї–Њ–ґ–Є—В–µ–ї—М–љ–∞—П –і–Є–љ–∞–Љ–Є–Ї–∞ —В–µ—З–µ–љ–Є—П –Я–°–†–Ъ —Б –њ—А–µ–Њ–±–ї–∞–і–∞–љ–Є–µ–Љ –і–Є–∞—А–µ–Є, —Е–∞—А–∞–Ї—В–µ—А–Є–Ј—Г—О—Й–∞—П—Б—П –љ–∞—Б—В—Г–њ–ї–µ–љ–Є–µ–Љ —А–µ–Љ–Є—Б—Б–Є–Є –Є –≤–Њ—Б—Б—В–∞–љ–Њ–≤–ї–µ–љ–Є–µ–Љ —Н—Г–±–Є–Њ–Ј–∞ –Ї–Є—И–µ—З–љ–Є–Ї–∞.
–Т—Л–≤–Њ–і—Л
1. –£ –≤—Б–µ—Е –±–Њ–ї—М–љ—Л—Е –њ–Њ—Б—В–Є–љ—Д–µ–Ї—Ж–Є–Њ–љ–љ—Л–Љ –°–†–Ъ, –∞—Б—Б–Њ—Ж–Є–Є—А–Њ–≤–∞–љ–љ—Л–Љ —Б –і–Є—Б–±–∞–Ї—В–µ—А–Є–Њ–Ј–Њ–Љ –Ї–Є—И–µ—З–љ–Є–Ї–∞, –њ–Њ—Б–ї–µ 3––љ–µ–і–µ–ї—М–љ–Њ–≥–Њ –Ї—Г—А—Б–∞ –Ф–µ––Э–Њ–ї–Њ–Љ –і–Њ—Б—В–Є–≥–љ—Г—В–∞ –Ї–ї–Є–љ–Є—З–µ—Б–Ї–∞—П —А–µ–Љ–Є—Б—Б–Є—П –Є —Г–ї—Г—З—И–µ–љ–Є–µ —Б–Њ—Б—В–∞–≤–∞ –Ї–Є—И–µ—З–љ–Њ–є –Љ–Є–Ї—А–Њ—Д–ї–Њ—А—Л.
2. –Ф–µ––Э–Њ–ї –Љ–Њ–ґ–µ—В –±—Л—В—М –≤–Ї–ї—О—З–µ–љ –≤ –Ї–Њ–Љ–њ–ї–µ–Ї—Б–љ—Г—О —В–µ—А–∞–њ–Є—О –±–Њ–ї—М–љ—Л—Е –°–†–Ъ, –∞—Б—Б–Њ—Ж–Є–Є—А–Њ–≤–∞–љ–љ—Л–Љ —Б –і–Є—Б–±–∞–Ї—В–µ—А–Є–Њ–Ј–Њ–Љ –Ї–Є—И–µ—З–љ–Є–Ї–∞.
3. –Ф–µ––Э–Њ–ї –Љ–Њ–ґ–µ—В —А–∞—Б—Б–Љ–∞—В—А–Є–≤–∞—В—М—Б—П –≤ –Ї–∞—З–µ—Б—В–≤–µ –Ї–Є—И–µ—З–љ–Њ–≥–Њ –∞–љ—В–Є—Б–µ–њ—В–Є–Ї–∞, –Љ–µ—Е–∞–љ–Є–Ј–Љ –і–µ–є—Б—В–≤–Є—П –Ї–Њ—В–Њ—А–Њ–≥–Њ —Б–≤—П–Ј–∞–љ —Б–Њ —Б–њ–Њ—Б–Њ–±–љ–Њ—Б—В—М—О –њ–Њ–і–∞–≤–ї—П—В—М —А–Њ—Б—В —Г—Б–ї–Њ–≤–љ–Њ––њ–∞—В–Њ–≥–µ–љ–љ–Њ–є –Љ–Є–Ї—А–Њ—Д–ї–Њ—А—Л.


–Ы–Є—В–µ—А–∞—В—Г—А–∞
1. –С–Њ–љ–і–∞—А–µ–љ–Ї–Њ –Т.–Ь., –У—А–∞—З–µ–≤–∞ –Э.–Ь., –Ь–∞—Ж—Г–ї–µ–≤–Є—З –Ґ.–Т. –Ф–Є—Б–±–∞–Ї—В–µ—А–Є–Њ–Ј—Л –Ї–Є—И–µ—З–љ–Є–Ї–∞ —Г –≤–Ј—А–Њ—Б–ї—Л—Е. –Ъ–Ь–Ъ Scientific Press, –Ь–Њ—Б–Ї–≤–∞ 2003, 220—Б ]
2. –С—А–Њ–і–Њ–≤ –Ы.–Х. –Я–Є—Й–µ–≤—Л–µ —В–Њ–Ї—Б–Є–Ї–Њ–Є–љ—Д–µ–Ї—Ж–Є–Є –Ї–∞–Ї —Д–∞–Ї—В–Њ—А —А–Є—Б–Ї–∞ —А–∞–Ј–≤–Є—В–Є—П –љ–µ–Ї–Њ—В–Њ—А—Л—Е –Њ—Б—В—А—Л—Е –Є –Њ–±–Њ—Б—В—А–µ–љ–Є—П —Е—А–Њ–љ–Є—З–µ—Б–Ї–Є—Е –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є–є. –Ґ–µ—А. –Р—А—Е..1993;5: 77–80;
3. –Т–Њ—А–Њ–±—М–µ–≤ –У.–Ш., –°–Є–Љ–Ї–Є–љ–∞ –Х.–°. –Я—А–Є–љ—Ж–Є–њ—Л –Њ—А–≥–∞–љ–Є–Ј–∞—Ж–Є–Є –њ—А–Њ—Д–Є–ї–∞–Ї—В–Є–Ї–Є –±–Њ–ї–µ–Ј–љ–µ–є —В–Њ–ї—Б—В–Њ–є –Ї–Є—И–Ї–Є —Б —Г—З–µ—В–Њ–Љ —Н–њ–Є–і–µ–Љ–Є–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Њ–≥–Њ –Њ–њ—Л—В–∞. –Ґ–µ—А. –∞—А—Е.1994;2:53–55]
4. –У—А–Є–≥–Њ—А—М–µ–≤ –Я.–ѓ., –ѓ–Ї–Њ–≤–µ–љ–Ї–Њ –≠.–Я. –°–Є–љ–і—А–Њ–Љ —А–∞–Ј–і—А–∞–ґ–µ–љ–љ–Њ–≥–Њ –Ї–Є—И–µ—З–љ–Є–Ї–∞, –∞—Б—Б–Њ—Ж–Є–Є—А–Њ–≤–∞–љ–љ—Л–є —Б –і–Є—Б–±–∞–Ї—В–µ—А–Є–Њ–Ј–Њ–Љ // Consilium medicum – 2003.– –Ґ. 2, вДЦ7.––°.305–307.
5. –Ы–∞–њ–Є–љ–∞ –Ґ.–Ы. –†–Њ—Б—Б–Є–є—Б–Ї–Є–µ —А–µ–Ї–Њ–Љ–µ–љ–і–∞—Ж–Є–Є –њ–Њ –і–Є–∞–≥–љ–Њ—Б—В–Є–Ї–µ –Є –ї–µ—З–µ–љ–Є—О –Є–љ—Д–µ–Ї—Ж–Є–Є Helicobacter pylori. –Т –Ї–љ.: –Ш–≤–∞—И–Ї–Є–љ –Т.–Ґ. –Є —Б–Њ–∞–≤—В. Helicobacter pylori: —А–µ–≤–Њ–ї—О—Ж–Є—П –≤ –≥–∞—Б—В—А–Њ—Н–љ—В–µ—А–Њ–ї–Њ–≥–Є–Є.– –Ь.,»–Ґ—А–Є–∞–і–∞––•», 1999, 161 – 174
6. –Ю—Б–Є–њ–Њ–≤ –У.–Р. , –Я–∞—А—Д–µ–љ–Њ–≤ –Р.–Ш., –Т–µ—А—Е–Њ–≤—Ж–µ–≤–∞ –Э.–Т. , –†—Г—З–Ї–Є–љ–∞ –Ш.–Э. –Є –і—А. –Ъ–ї–Є–љ–Є—З–µ—Б–Ї–Њ–µ –Ј–љ–∞—З–µ–љ–Є–µ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П –Љ–Є–Ї—А–Њ–Њ—А–≥–∞–љ–Є–Ј–Љ–Њ–≤ —Б–ї–Є–Ј–Є—Б—В–Њ–є –Њ–±–Њ–ї–Њ—З–Ї–Є –Ї–Є—И–µ—З–љ–Є–Ї–∞ –Ї—Г–ї—М—В—Г—А–∞–ї—М–љ–Њ––±–Є–Њ—Е–Є–Љ–Є—З–µ—Б–Ї–Є–Љ –Є —Е—А–Њ–Љ–∞—В–Њ––Љ–∞—Б—Б–—Б–њ–µ–Ї—В—А–Њ–Љ–µ—В—А–Є—З–µ—Б–Ї–Є–Љ –Љ–µ—В–Њ–і–∞–Љ–Є.//–≠–Ї—Б–њ–µ—А–Є–Љ. –Є –Ї–ї–Є–љ–Є—З. –≥–∞—Б—В—А–Њ—Н–љ—В–µ—А–Њ–ї–Њ–≥–Є—П. 2003. – вДЦ4.––°.59–62.
7. –Я–∞—А—Д–µ–љ–Њ–≤ –Р.–Ш., –†—Г—З–Ї–Є–љ–∞ –Ш.–Э., –Я–Њ—В–∞–њ–Њ–≤–∞ –Т.–С., –Ю—Б–Є–њ–Њ–≤ –У.–Р.–Я–Њ—Б—В–Є–љ—Д–µ–Ї—Ж–Є–Њ–љ–љ—Л–є —Б–Є–љ–і—А–Њ–Љ —А–∞–Ј–і—А–∞–ґ–µ–љ–љ–Њ–≥–Њ –Ї–Є—И–µ—З–љ–Є–Ї–∞ –Є–ї–Є —Е—А–Њ–љ–Є—З–µ—Б–Ї–Є–є –Ї–Њ–ї–Є—В? –Ь–∞—В–µ—А–Є–∞–ї—Л V —Б—К–µ–Ј–і–∞ –Њ–±—Й–µ—Б—В–≤–∞ –≥–∞—Б—В—А–Њ—Н–љ—В. –†–Њ—Б—Б–Є–Є –Є XXXII —Б–µ—Б—Б–Є–Є –¶–Э–Ш–Ш–У, –Ь–Њ—Б–Ї–≤–∞ 3–6 —Д–µ–≤—А–∞–ї—П 2005 –≥.––Ь.: –Р–љ–∞—Е–∞—А—Б–Є—Б, 2005.––° 482–483]
8. –†—Г—З–Ї–Є–љ–∞ –Ш.–Э. –†–Њ–ї—М –Њ—Б—В—А—Л—Е –Ї–Є—И–µ—З–љ—Л—Е –Є–љ—Д–µ–Ї—Ж–Є–є –Є –љ–∞—А—Г—И–µ–љ–Є–є –Љ–Є–Ї—А–Њ–±–Є–Њ—Ж–µ–љ–Њ–Ј–∞ –≤ —Н—В–Є–Њ–ї–Њ–≥–Є–Є –Є –њ–∞—В–Њ–≥–µ–љ–µ–Ј–µ —Б–Є–љ–і—А–Њ–Љ–∞ —А–∞–Ј–і—А–∞–ґ–µ–љ–љ–Њ–≥–Њ –Ї–Є—И–µ—З–љ–Є–Ї–∞. –Р–≤—В–Њ—А–µ—Д. –Ф–Є—Б—Б. –і–Њ–Ї—В. –Ь.: 2005: 40 —Б].












