–°–Є–љ–і—А–Њ–Љ –њ–µ—З–µ–љ–Њ—З–љ–Њ–є —Н–љ—Ж–µ—Д–∞–ї–Њ–њ–∞—В–Є–Є (–Я–≠) –Љ–Њ–ґ–µ—В —Б–Њ–њ—Г—В—Б—В–≤–Њ–≤–∞—В—М –Њ—Б—В—А—Л–Љ –Є —Е—А–Њ–љ–Є—З–µ—Б–Ї–Є–Љ –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П–Љ –њ–µ—З–µ–љ–Є.
–Ґ–µ—А–Љ–Є–љ «—Н–љ—Ж–µ—Д–∞–ї–Њ–њ–∞—В–Є—П» –Њ–Ј–љ–∞—З–∞–µ—В, —З—В–Њ –Є–Ј–Љ–µ–љ–µ–љ–Є—П —Б–Њ —Б—В–Њ—А–Њ–љ—Л –љ–µ—А–≤–љ–Њ–є —Б–Є—Б—В–µ–Љ—Л –Є–Љ–µ—О—В –љ–µ–≤–Њ—Б–њ–∞–ї–Є—В–µ–ї—М–љ–Њ–µ –њ—А–Њ–Є—Б—Е–Њ–ґ–і–µ–љ–Є–µ.
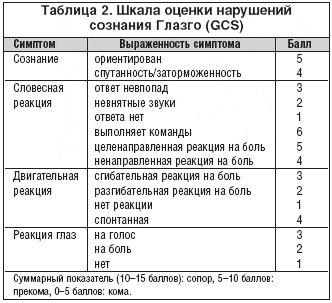
–Ґ—П–ґ–µ—Б—В—М –њ–µ—З–µ–љ–Њ—З–љ–Њ–є –Я–≠ –Њ—Ж–µ–љ–Є–≤–∞—О—В –њ–Њ –Њ–њ–Є—Б–∞—В–µ–ї—М–љ–Њ–є —И–Ї–∞–ї–µ —Б–Є–Љ–њ—В–Њ–Љ–Њ–≤ (—В–∞–±–ї. 1), —И–Ї–∞–ї–µ –њ–Њ–ї—Г–Ї–Њ–ї–Є—З–µ—Б—В–≤–µ–љ–љ–Њ–є –Њ—Ж–µ–љ–Ї–Є West Haven, —И–Ї–∞–ї–µ –Ї–Њ–Љ—Л –У–ї–∞–Ј–≥–Њ (—В–∞–±–ї. 2). –≠—В–Є —И–Ї–∞–ї—Л —Г—З–Є—В—Л–≤–∞—О—В —Б–Њ—Б—В–Њ—П–љ–Є–µ —Б–Њ–Ј–љ–∞–љ–Є—П, —Н–Љ–Њ—Ж–Є–Њ–љ–∞–ї—М–љ—Л–є —Б—В–∞—В—Г—Б, –љ–∞—А—Г—И–µ–љ–Є—П —Б–Њ —Б—В–Њ—А–Њ–љ—Л –і–≤–Є–≥–∞—В–µ–ї—М–љ–Њ–є —Б—Д–µ—А—Л. –®–Ї–∞–ї–∞ West Haven –њ–Њ–і—А–∞–Ј—Г–Љ–µ–≤–∞–µ—В —В–∞–Ї–ґ–µ –Њ—Ж–µ–љ–Ї—Г –і–∞–љ–љ—Л—Е –≠–≠–У –Є –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ –Ї–Њ–љ—Ж–µ–љ—В—А–∞—Ж–Є–Є –∞–Љ–Љ–Є–∞–Ї–∞ –≤ –Ї—А–Њ–≤–Є (—В–∞–±–ї. 3).
–Т—Л–і–µ–ї—П—О—В —З–µ—В—Л—А–µ —Б—В–∞–і–Є–Є –Я–≠. –°–ї–µ–і—Г–µ—В –µ—Й–µ —А–∞–Ј –Ј–∞–Љ–µ—В–Є—В—М, —З—В–Њ, –Ї–∞–Ї –њ—А–∞–≤–Є–ї–Њ, –љ–µ–≤—А–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є–µ –Є–Ј–Љ–µ–љ–µ–љ–Є—П –Њ–±—А–∞—В–Є–Љ—Л –Є —Б—В–∞–і–Є–Є –Я–≠ –і–Њ—Б—В–∞—В–Њ—З–љ–Њ –і–Є–љ–∞–Љ–Є—З–љ–Њ —Б–Љ–µ–љ—П—О—В –Њ–і–љ–∞ –і—А—Г–≥—Г—О.
–†–∞–Ј–ї–Є—З–∞—О—В 5 –Њ—Б–љ–Њ–≤–љ—Л—Е –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є—Е —Д–Њ—А–Љ –Я–≠ [–Э. Conn, 1989]:
1. –°–Є–љ–і—А–Њ–Љ –†–µ–є–µ.
2. –Ф–µ—Д–Є—Ж–Є—В —Д–µ—А–Љ–µ–љ—В–Њ–≤ –Њ—А–љ–Є—В–Є–љ–Њ–≤–Њ–≥–Њ —Ж–Є–Ї–ї–∞ (–≥–Є–њ–µ—А–∞–Љ–Љ–Њ–љ–Є–µ–Љ–Є—П I –Є II —В–Є–њ–Њ–≤).
3. –Я—Б–µ–≤–і–Њ–њ–Њ—А—В–Њ–—Б–Є—Б—В–µ–Љ–љ–∞—П —Н–љ—Ж–µ—Д–∞–ї–Њ–њ–∞—В–Є—П.
4. –§—Г–ї—М–Љ–Є–љ–∞–љ—В–љ–∞—П –њ–µ—З–µ–љ–Њ—З–љ–∞—П –љ–µ–і–Њ—Б—В–∞—В–Њ—З–љ–Њ—Б—В—М.
5. –Я–Њ—А—В–Њ–—Б–Є—Б—В–µ–Љ–љ–∞—П —Н–љ—Ж–µ—Д–∞–ї–Њ–њ–∞—В–Є—П:
– —Б—Г–±–Ї–ї–Є–љ–Є—З–µ—Б–Ї–∞—П (–ї–∞—В–µ–љ—В–љ–∞—П),
– –Њ—Б—В—А–∞—П,
– –Њ—Б—В—А–∞—П —А–µ—Ж–Є–і–Є–≤–Є—А—Г—О—Й–∞—П,
– —Е—А–Њ–љ–Є—З–µ—Б–Ї–∞—П –њ–µ—А—Б–Є—Б—В–Є—А—Г—О—Й–∞—П,
– —Е—А–Њ–љ–Є—З–µ—Б–Ї–∞—П —А–µ—Ж–Є–і–Є–≤–Є—А—Г—О—Й–∞—П.
–°–Є—В—Г–∞—Ж–Є–Є, –≤ –Ї–Њ—В–Њ—А—Л—Е –љ–∞–±–ї—О–і–∞–µ—В—Б—П —А–∞–Ј–≤–Є—В–Є–µ —В–Њ–є –Є–ї–Є –Є–љ–Њ–є –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Њ–є —Д–Њ—А–Љ—Л –Я–≠, —В–∞–Ї–ґ–µ –Ї–∞–Ї –Є –њ–∞—В–Њ—Д–Є–Ј–Є–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є–µ –Љ–µ—Е–∞–љ–Є–Ј–Љ—Л, –ї–µ–ґ–∞—Й–Є–µ –≤ –Є—Е –Њ—Б–љ–Њ–≤–µ, —А–∞–Ј–ї–Є—З–∞—О—В—Б—П.
–Я—А–Є —Б–Є–љ–і—А–Њ–Љ–µ –†–µ–є–µ –љ–∞–±–ї—О–і–∞–µ—В—Б—П —А–∞–Ј–≤–Є—В–Є–µ –Њ—Б—В—А–Њ–є –ґ–Є—А–Њ–≤–Њ–є –і–Є—Б—В—А–Њ—Д–Є–Є –њ–µ—З–µ–љ–Є, –ґ–µ–ї—В—Г—Е–Є, –Њ—В–µ–Ї–∞ –Љ–Њ–Ј–≥–∞ –Є —Н–љ—Ж–µ—Д–∞–ї–Њ–њ–∞—В–Є–Є —Г –і–µ—В–µ–є –љ–∞ —Д–Њ–љ–µ –Њ—Б—В—А–Њ–є –≤–Є—А—Г—Б–љ–Њ–є –Є–љ—Д–µ–Ї—Ж–Є–Є –Є –њ—А–Є–µ–Љ–∞ –∞—Ж–µ—В–Є–ї—Б–∞–ї–Є—Ж–Є–ї–Њ–≤–Њ–є –Ї–Є—Б–ї–Њ—В—Л. –Т –Њ—Б–љ–Њ–≤–µ –ї–µ–ґ–Є—В –љ–∞—А—Г—И–µ–љ–Є–µ —Д—Г–љ–Ї—Ж–Є–Є –Љ–Є—В–Њ—Е–Њ–љ–і—А–Є–є (–Ї–∞–Ї –њ—А–µ–і–њ–Њ–ї–∞–≥–∞–µ—В—Б—П, –≤ —А–µ–Ј—Г–ї—М—В–∞—В–µ –Ї–Њ–Љ–њ–ї–µ–Ї—Б–љ–Њ–≥–Њ –њ–∞—В–Њ–≥–µ–љ–љ–Њ–≥–Њ –≤–Њ–Ј–і–µ–є—Б—В–≤–Є—П –Є–љ—Д–µ–Ї—Ж–Є–Њ–љ–љ–Њ–≥–Њ –Є –ї–µ–Ї–∞—А—Б—В–≤–µ–љ–љ–Њ–≥–Њ —Д–∞–Ї—В–Њ—А–Њ–≤), –љ–∞—А—Г—И–µ–љ–Є–µ –Ї–ї–µ—В–Њ—З–љ–Њ–≥–Њ –і—Л—Е–∞–љ–Є—П –Є –і–µ—В–Њ–Ї—Б–Є–Ї–∞—Ж–Є–Є –љ–µ–є—А–Њ—В–Њ–Ї—Б–Є–љ–Њ–≤.
–Ф–µ—Д–Є—Ж–Є—В —Д–µ—А–Љ–µ–љ—В–Њ–≤ –Њ—А–љ–Є—В–Є–љ–Њ–≤–Њ–≥–Њ —Ж–Є–Ї–ї–∞ – —А–µ–і–Ї–Њ –≤—Б—В—А–µ—З–∞—О—Й–∞—П—Б—П –≤—А–Њ–ґ–і–µ–љ–љ–∞—П –њ–∞—В–Њ–ї–Њ–≥–Є—П, —Б–Њ–њ—А–Њ–≤–Њ–ґ–і–∞—О—Й–∞—П—Б—П –≥–Є–њ–µ—А–∞–Љ–Љ–Њ–љ–Є–µ–Љ–Є–µ–є.
–Я—Б–µ–≤–і–Њ–њ–Њ—А—В–Њ–—Б–Є—Б—В–µ–Љ–љ–∞—П —Н–љ—Ж–µ—Д–∞–ї–Њ–њ–∞—В–Є—П —А–∞–Ј–≤–Є–≤–∞–µ—В—Б—П –њ—А–Є –љ–∞–ї–Є—З–Є–Є —Н–ї–µ–Ї—В—А–Њ–ї–Є—В–љ–Њ–≥–Њ –і–Є—Б–±–∞–ї–∞–љ—Б–∞ (—В–Є–њ–Є—З–љ—Л–є –њ—А–Є–Љ–µ—А – –њ–µ—А–µ–і–Њ–Ј–Є—А–Њ–≤–Ї–∞ –Љ–Њ—З–µ–≥–Њ–љ–љ—Л—Е —Б—А–µ–і—Б—В–≤ –њ—А–Є —Ж–Є—А—А–Њ–Ј–µ –њ–µ—З–µ–љ–Є). –Т —Н—В–Є—Е —Г—Б–ї–Њ–≤–Є—П—Е –љ–∞–±–ї—О–і–∞–µ—В—Б—П «—Н–ї–µ–Ї—В—А–Є—З–µ—Б–Ї–∞—П –і–Є—Б—Д—Г–љ–Ї—Ж–Є—П» –љ–µ—А–≤–љ–Њ–є —В–Ї–∞–љ–Є. –Я—А–Є –і–∞–љ–љ–Њ–Љ —В–Є–њ–µ —Н–љ—Ж–µ—Д–∞–ї–Њ–њ–∞—В–Є–Є –љ–∞–Ї–Њ–њ–ї–µ–љ–Є—О –љ–µ–є—А–Њ—В–Њ–Ї—Б–Є–љ–Њ–≤ –≤ –Њ—А–≥–∞–љ–Є–Ј–Љ–µ –≥–ї–∞–≤–љ–∞—П —А–Њ–ї—М –љ–µ –њ—А–Є–љ–∞–і–ї–µ–ґ–Є—В (–≤ –љ–∞–Ј–≤–∞–љ–Є–Є –љ–∞ —Н—В–Њ —Г–Ї–∞–Ј—Л–≤–∞–µ—В –њ—А–Є—Б—В–∞–≤–Ї–∞ «–њ—Б–µ–≤–і–Њ»).
–§—Г–ї—М–Љ–Є–љ–∞–љ—В–љ–∞—П –њ–µ—З–µ–љ–Њ—З–љ–∞—П –љ–µ–і–Њ—Б—В–∞—В–Њ—З–љ–Њ—Б—В—М – –њ–Њ–љ—П—В–Є–µ, –≤–Ї–ї—О—З–∞—О—Й–µ–µ –≤ —Б–µ–±—П, –њ–Њ–Љ–Є–Љ–Њ —Б–Є–љ–і—А–Њ–Љ–∞ –Я–≠, –љ–∞—А–∞—Б—В–∞—О—Й—Г—О –ґ–µ–ї—В—Г—Е—Г, –≥–Є–њ–Њ–Ї–Њ–∞–≥—Г–ї—П—Ж–Є—О, –≥–Є–њ–Њ–≥–ї–Є–Ї–µ–Љ–Є—О – –Ї–Њ–Љ–њ–ї–µ–Ї—Б –њ—А–Є–Ј–љ–∞–Ї–Њ–≤, —Е–∞—А–∞–Ї—В–µ—А–Є–Ј—Г—О—Й–Є—Е —В—П–ґ–µ–ї—Г—О –њ–µ—З–µ–љ–Њ—З–љ—Г—О –љ–µ–і–Њ—Б—В–∞—В–Њ—З–љ–Њ—Б—В—М –≤ —А–µ–Ј—Г–ї—М—В–∞—В–µ –Љ–∞—Б—Б–Є–≤–љ–Њ–є –њ–Њ—В–µ—А–Є –њ–∞—А–µ–љ—Е–Є–Љ—Л. –Ґ–µ—А–Љ–Є–љ «—Д—Г–ї—М–Љ–Є–љ–∞–љ—В–љ–∞—П» –Њ–Ј–љ–∞—З–∞–µ—В, —З—В–Њ —А–∞–Ј–≤–Є—В–Є–µ —Н—В–Њ–≥–Њ –Ї—А–Є—В–Є—З–µ—Б–Ї–Њ–≥–Њ —Б–Њ—Б—В–Њ—П–љ–Є—П –њ—А–Њ–Є—Б—Е–Њ–і–Є—В –Њ—Б—В—А–Њ –Є–ї–Є –њ–Њ–і–Њ—Б—В—А–Њ —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤, –љ–µ –Є–Љ–µ–≤—И–Є—Е –∞–љ–∞–Љ–љ–µ—Б—В–Є—З–µ—Б–Ї–Є—Е —Г–Ї–∞–Ј–∞–љ–Є–є –љ–∞ –љ–∞–ї–Є—З–Є–µ –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П –њ–µ—З–µ–љ–Є. –Ґ–Є–њ–Є—З–љ—Л–Љ–Є –њ—А–Є–Љ–µ—А–∞–Љ–Є –Љ–Њ–≥—Г—В —Б–ї—Г–ґ–Є—В—М –Љ–Њ–ї–љ–Є–µ–љ–Њ—Б–љ–Њ–µ —В–µ—З–µ–љ–Є–µ –Њ—Б—В—А–Њ–≥–Њ –≤–Є—А—Г—Б–љ–Њ–≥–Њ –≥–µ–њ–∞—В–Є—В–∞ –Р, –Њ—В—А–∞–≤–ї–µ–љ–Є–µ –њ–∞—А–∞—Ж–µ—В–∞–Љ–Њ–ї–Њ–Љ. –Т –њ–∞—В–Њ–≥–µ–љ–µ–Ј–µ –Я–≠ –њ—А–Є —Д—Г–ї—М–Љ–Є–љ–∞–љ—В–љ–Њ–є –њ–µ—З–µ–љ–Њ—З–љ–Њ–є –љ–µ–і–Њ—Б—В–∞—В–Њ—З–љ–Њ—Б—В–Є –≤–∞–ґ–љ—Г—О —А–Њ–ї—М –Є–≥—А–∞–µ—В –љ–∞–Ї–Њ–њ–ї–µ–љ–Є–µ –љ–µ–є—В—А–Њ—В–Њ–Ї—Б–Є–љ–Њ–≤ (—Б–Љ. –љ–Є–ґ–µ).
–Я–Њ—А—В–Њ–—Б–Є—Б—В–µ–Љ–љ–∞—П –Я–≠ – –љ–∞–Є–±–Њ–ї–µ–µ —А–∞—Б–њ—А–Њ—Б—В—А–∞–љ–µ–љ–љ—Л–є –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є–є —В–Є–њ, –њ–Њ—Б–Ї–Њ–ї—М–Ї—Г –Њ–љ–∞ —Б–Њ–њ—Г—В—Б—В–≤—Г–µ—В —Е—А–Њ–љ–Є—З–µ—Б–Ї–Є–Љ –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П–Љ –њ–µ—З–µ–љ–Є. –Т –Њ—Б–љ–Њ–≤–µ —А–∞–Ј–≤–Є—В–Є—П –њ–Њ—А—В–Њ–—Б–Є—Б—В–µ–Љ–љ–Њ–є —Н–љ—Ж–µ—Д–∞–ї–Њ–њ–∞—В–Є–Є –ї–µ–ґ–Є—В –Љ–µ—Е–∞–љ–Є–Ј–Љ –њ–Њ—А—В–Њ––Ї–∞–≤–∞–ї—М–љ–Њ–≥–Њ —И—Г–љ—В–Є—А–Њ–≤–∞–љ–Є—П –Ї—А–Њ–≤–Є, –њ–Њ–≤—Л—И–µ–љ–љ–∞—П –њ—А–Њ–љ–Є—Ж–∞–µ–Љ–Њ—Б—В—М –Ї–Є—И–µ—З–љ–Њ–≥–Њ –±–∞—А—М–µ—А–∞ –Є –љ–∞—А—Г—И–µ–љ–Є–µ –і–µ—В–Њ–Ї—Б–Є–Ї–∞—Ж–Є–Њ–љ–љ–Њ–є —Д—Г–љ–Ї—Ж–Є–Є –≥–µ–њ–∞—В–Њ—Ж–Є—В–Њ–≤.
–Э–∞ –Њ—Б–љ–Њ–≤–∞–љ–Є–Є –∞–љ–∞–ї–Є–Ј–∞ –њ—А–Є–Ј–љ–∞–Ї–Њ–≤ –њ–Њ —И–Ї–∞–ї–µ West Haven –Љ–Њ–ґ–љ–Њ –њ—А–Њ–≤–µ—Б—В–Є –њ–Њ–ї—Г–Ї–Њ–ї–Є—З–µ—Б—В–≤–µ–љ–љ—Г—О –Њ—Ж–µ–љ–Ї—Г –Є–љ–і–µ–Ї—Б–∞ –њ–Њ—А—В–Њ–—Б–Є—Б—В–µ–Љ–љ–Њ–є —Н–љ—Ж–µ—Д–∞–ї–Њ–њ–∞—В–Є–Є (–Є–љ–і–µ–Ї—Б–∞ –Я–°–≠) (—В–∞–±–ї. 4).
–Ы–∞—В–µ–љ—В–љ–∞—П (—Б—Г–±–Ї–ї–Є–љ–Є—З–µ—Б–Ї–∞—П) —Д–Њ—А–Љ–∞ –њ–Њ—А—В–Њ–—Б–Є—Б—В–µ–Љ–љ–Њ–є –Я–≠ —Е–∞—А–∞–Ї—В–µ—А–Є–Ј—Г–µ—В—Б—П –Њ—В—Б—Г—В—Б—В–≤–Є–µ–Љ «–Ј–∞–Љ–µ—В–љ—Л—Е –њ—А–Є –Њ—Б–Љ–Њ—В—А–µ» —Б–Є–Љ–њ—В–Њ–Љ–Њ–≤. –Ю–і–љ–∞–Ї–Њ –њ–∞—Ж–Є–µ–љ—В—Л —Б –ї–∞—В–µ–љ—В–љ–Њ–є –Я–≠ –≤ –ґ–Є–Ј–љ–µ–љ–љ—Л—Е —Б–Є—В—Г–∞—Ж–Є—П—Е, —В—А–µ–±—Г—О—Й–Є—Е –≤–љ–Є–Љ–∞–љ–Є—П –Є —Б–Њ—Б—А–µ–і–Њ—В–Њ—З–µ–љ–љ–Њ—Б—В–Є (–Ї–∞–Ї —В–Њ, –љ–∞–њ—А–Є–Љ–µ—А, –≤–Њ–ґ–і–µ–љ–Є–µ –∞–≤—В–Њ–Љ–Њ–±–Є–ї—П), –Љ–Њ–≥—Г—В –њ—А–Њ—П–≤–ї—П—В—М –љ–µ–і–Њ—Б—В–∞—В–Њ—З–љ—Г—О –±—Л—Б—В—А–Њ—В—Г –Љ—Л—И–ї–µ–љ–Є—П. –Ы–∞—В–µ–љ—В–љ–∞—П –Я–≠ –Љ–Њ–ґ–µ—В –љ–∞–±–ї—О–і–∞—В—М—Б—П –і–∞–ґ–µ –њ—А–Є –і–Њ—Б—В–∞—В–Њ—З–љ–Њ –ї–µ–≥–Ї–Є—Е —Д–Њ—А–Љ–∞—Е –њ–Њ—А–∞–ґ–µ–љ–Є—П –њ–µ—З–µ–љ–Є – –і–Є—Б—В—А–Њ—Д–Є–Є –≥–µ–њ–∞—В–Њ—Ж–Є—В–Њ–≤ –Є –≥–µ–њ–∞—В–Є—В–µ. –†–∞—Б–њ–Њ–Ј–љ–∞–≤–∞–љ–Є–µ —Н—В–Њ–є —Д–Њ—А–Љ—Л –Я–≠ –Њ—Б–љ–Њ–≤—Л–≤–∞–µ—В—Б—П –љ–∞ —А–µ–Ј—Г–ї—М—В–∞—В–∞—Е –њ—А–Њ–≤–µ–і–µ–љ–Є—П —Б–њ–µ—Ж–Є–∞–ї—М–љ—Л—Е —В–µ—Б—В–Њ–≤ (—В–µ—Б—В–∞ —Б–≤—П–Ј–Є —З–Є—Б–µ–ї, —В–µ—Б—В–∞ –ї–Є–љ–Є–Є, —В–µ—Б—В–∞ —Б—З–µ—В–∞ –Є –њ—А.).
–Ю—Б—В—А–∞—П –Є –Њ—Б—В—А–∞—П —А–µ—Ж–Є–і–Є–≤–Є—А—Г—О—Й–∞—П —Д–Њ—А–Љ–∞ –њ–Њ—А—В–Њ–—Б–Є—Б—В–µ–Љ–љ–Њ–є –Я–≠ –њ—А–Є –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П—Е –њ–µ—З–µ–љ–Є —А–∞–Ј–≤–Є–≤–∞–µ—В—Б—П, –Ї–∞–Ї –њ—А–∞–≤–Є–ї–Њ, –њ—А–Є –≤–Њ–Ј–і–µ–є—Б—В–≤–Є–Є –Њ—В—П–≥–Њ—Й–∞—О—Й–Є—Е –Є–ї–Є —В—А–Є–≥–≥–µ—А–љ—Л—Е —Д–∞–Ї—В–Њ—А–Њ–≤: –Ї–Њ–љ–Ї—Г—А–Є—А—Г—О—Й–µ–є –Є–љ—Д–µ–Ї—Ж–Є–Є (–њ–љ–µ–≤–Љ–Њ–љ–Є–Є, –њ–Є–µ–ї–Њ–љ–µ—Д—А–Є—В–∞ –Є –і—А.), –ґ–µ–ї—Г–і–Њ—З–љ–Њ––Ї–Є—И–µ—З–љ–Њ–≥–Њ –Ї—А–Њ–≤–Њ—В–µ—З–µ–љ–Є—П, –Ј–∞–і–µ—А–ґ–Ї–µ —Б—В—Г–ї–∞, –њ–µ—А–µ–≥—А—Г–Ј–Ї–µ –±–µ–ї–Ї–Њ–Љ, –њ–µ—А–µ–і–Њ–Ј–Є—А–Њ–≤–Ї–µ –љ–µ–Ї–Њ—В–Њ—А—Л—Е –ї–µ–Ї–∞—А—Б—В–≤ (–і–Є—Г—А–µ—В–Є–Ї–Є, –±–∞—А–±–Є—В—Г—А–∞—В—Л, —Д–µ–љ–Њ—В–Є–∞–Ј–Є–љ—Л, –±–µ–љ–Ј–Њ–і–Є–∞–Ј–µ–њ–Є–љ—Л –Є –і—А.), –Є—Б–Ї—Г—Б—Б—В–≤–µ–љ–љ–Њ–Љ –њ–Њ—А—В–Њ––Ї–∞–≤–∞–ї—М–љ–Њ–Љ —И—Г–љ—В–Є—А–Њ–≤–∞–љ–Є–Є, –і—А—Г–≥–Є—Е —Е–Є—А—Г—А–≥–Є—З–µ—Б–Ї–Є—Е –≤–Љ–µ—И–∞—В–µ–ї—М—Б—В–≤–∞—Е, –Љ–∞—Б—Б–Є–≤–љ–Њ–Љ –њ–∞—А–∞—Ж–µ–љ—В–µ–Ј–µ –Є –і—А. –Ю—Б—В—А–∞—П —Д–Њ—А–Љ–∞ –Я–≠ –њ—А–Є—Б—Г—Й–∞ –±–Њ–ї–µ–Ј–љ—П–Љ –њ–µ—З–µ–љ–Є –љ–∞ —Б—В–∞–і–Є–Є —Ж–Є—А—А–Њ–Ј–∞ –Є–ї–Є —Е—А–Њ–љ–Є—З–µ—Б–Ї–Њ–Љ—Г –≥–µ–њ–∞—В–Є—В—Г –≤—Л—Б–Њ–Ї–Њ–є –∞–Ї—В–Є–≤–љ–Њ—Б—В–Є.
–•—А–Њ–љ–Є—З–µ—Б–Ї–∞—П —А–µ—Ж–Є–і–Є–≤–Є—А—Г—О—Й–∞—П –Я–≠ —Е–∞—А–∞–Ї—В–µ—А–Є–Ј—Г–µ—В—Б—П –љ–∞–ї–Є—З–Є–µ–Љ –≤–Њ–ї–љ–Њ–Њ–±—А–∞–Ј–љ–Њ–є, —З–∞—Б—В–Њ —А–µ—Ж–Є–і–Є–≤–Є—А—Г—О—Й–µ–є –Я–≠; –≤ —Н–њ–Є–Ј–Њ–і–∞—Е –Љ–µ–ґ–і—Г «—Г–≥–ї—Г–±–ї–µ–љ–Є—П–Љ–Є» –Я–≠ —Б–Њ—Е—А–∞–љ—П—О—В—Б—П —Б—Г–±–Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є–µ –Є–ї–Є –Љ–Є–љ–Є–Љ–∞–ї—М–љ—Л–µ –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є–µ –њ—А–Њ—П–≤–ї–µ–љ–Є—П.
–•—А–Њ–љ–Є—З–µ—Б–Ї–∞—П –њ–µ—А—Б–Є—Б—В–Є—А—Г—О—Й–∞—П –Я–≠ –њ—А–Є—Б—Г—Й–∞ –њ–∞—Ж–Є–µ–љ—В–∞–Љ —Б —В—П–ґ–µ–ї—Л–Љ –њ–Њ—А–∞–ґ–µ–љ–Є–µ–Љ –њ–µ—З–µ–љ–Є –Є–Є–ї–Є –≤—Л—А–∞–ґ–µ–љ–љ—Л–Љ –њ–Њ—А—В–Њ––Ї–∞–≤–∞–ї—М–љ—Л–Љ —И—Г–љ—В–Є—А–Њ–≤–∞–љ–Є–µ–Љ. –Я—А–Є —Н—В–Њ–є —Д–Њ—А–Љ–µ –Я–≠ –≤–Њ–Ј–Љ–Њ–ґ–љ–Њ —Д–Њ—А–Љ–Є—А–Њ–≤–∞–љ–Є–µ —З–∞—Б—В–Є—З–љ–Њ –љ–µ–Њ–±—А–∞—В–Є–Љ—Л—Е –љ–µ–≤—А–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є—Е —А–∞—Б—Б—В—А–Њ–є—Б—В–≤ – —В–∞–Ї –љ–∞–Ј—Л–≤–∞–µ–Љ–Њ–є –≥–µ–њ–∞—В–Њ–—Ж–µ—А–µ–±—А–∞–ї—М–љ–Њ–≥–Њ —Б–Є–љ–і—А–Њ–Љ–∞ – –≤ —А–µ–Ј—Г–ї—М—В–∞—В–µ –∞—В—А–Њ—Д–Є–Є –Љ–Њ–Ј–≥–∞ –љ–∞ —Д–Њ–љ–µ —Е—А–Њ–љ–Є—З–µ—Б–Ї–Њ–є —Ж–Є—А–Ї—Г–ї—П—Ж–Є–Є —В–Њ–Ї—Б–Є–љ–Њ–≤.
–Я–Њ —Б–Њ–≤—А–µ–Љ–µ–љ–љ—Л–Љ –њ—А–µ–і—Б—В–∞–≤–ї–µ–љ–Є—П–Љ, –≤ –±–Њ–ї—М—И–Є–љ—Б—В–≤–µ —Б–ї—Г—З–∞–µ–≤ –≥–ї–∞–≤–љ—Г—О —А–Њ–ї—М –Є–≥—А–∞–µ—В –≤–Њ–Ј–і–µ–є—Б—В–≤–Є–µ –љ–∞ –Љ–Њ–Ј–≥ —Н–љ–і–Њ–≥–µ–љ–љ—Л—Е –љ–µ–є—А–Њ—В–Њ–Ї—Б–Є–љ–Њ–≤, –њ–Њ–ї—Г—З–Є–≤—И–Є—Е –љ–∞–Ј–≤–∞–љ–Є–µ «–Љ–µ–і–Є–∞—В–Њ—А–Њ–≤ –њ–µ—З–µ–љ–Њ—З–љ–Њ–є —Н–љ—Ж–µ—Д–∞–ї–Њ–њ–∞—В–Є–Є». –Ю—Б–љ–Њ–≤–љ—Л–Љ –Є–Ј –љ–Є—Е —П–≤–ї—П–µ—В—Б—П –∞–Љ–Љ–Є–∞–Ї.
–Ш—Б—В–Њ—З–љ–Є–Ї–Њ–Љ –Њ–±—А–∞–Ј–Њ–≤–∞–љ–Є—П –∞–Љ–Љ–Є–∞–Ї–∞ –≤ –Њ—А–≥–∞–љ–Є–Ј–Љ–µ –≥–ї–∞–≤–љ—Л–Љ –Њ–±—А–∞–Ј–Њ–Љ —Б–ї—Г–ґ–Є—В –∞–Ј–Њ—В –њ–Є—Й–µ–≤–Њ–≥–Њ –±–µ–ї–Ї–∞. –Э–∞–Є–±–Њ–ї—М—И–µ–µ –Ї–Њ–ї–Є—З–µ—Б—В–≤–Њ –∞–Љ–Љ–Є–∞–Ї–∞ –Њ–±—А–∞–Ј—Г–µ—В—Б—П –≤ –њ–µ—З–µ–љ–Є –≤ —Е–Њ–і–µ —А–µ–∞–Ї—Ж–Є–є –і–µ–Ј–∞–Љ–Є–љ–Є—А–Њ–≤–∞–љ–Є—П –∞–Љ–Є–љ–Њ–Ї–Є—Б–ї–Њ—В. –Ф–Њ–њ–Њ–ї–љ–Є—В–µ–ї—М–љ—Л–Љ–Є –Є—Б—В–Њ—З–љ–Є–Ї–∞–Љ–Є –µ–≥–Њ –Њ–±—А–∞–Ј–Њ–≤–∞–љ–Є—П —Б–ї—Г–ґ–∞—В —Г—А–µ–∞–Ј–∞ – –њ–Њ–ї–Њ–ґ–Є—В–µ–ї—М–љ–∞—П –Љ–Є–Ї—А–Њ—Д–ї–Њ—А–∞ –ґ–µ–ї—Г–і–Њ—З–љ–Њ––Ї–Є—И–µ—З–љ–Њ–≥–Њ —В—А–∞–Ї—В–∞ (—А–∞–Ј–ї–∞–≥–∞—О—Й–∞—П –Љ–Њ—З–µ–≤–Є–љ—Г –Є –±–µ–ї–Њ–Ї), –Љ—Л—И–µ—З–љ–∞—П —В–Ї–∞–љ—М (–њ—А–Њ–і—Г–Ї—Ж–Є—П –∞–Љ–Љ–Є–∞–Ї–∞ –≤–Њ–Ј—А–∞—Б—В–∞–µ—В –њ—А–Є —Д–Є–Ј–Є—З–µ—Б–Ї–Њ–є –љ–∞–≥—А—Г–Ј–Ї–µ), —В–Њ–љ–Ї–∞—П –Ї–Є—И–Ї–∞ (–≤ —А–µ–Ј—Г–ї—М—В–∞—В–µ —А–∞—Б–њ–∞–і–∞ –≥–ї—Г—В–∞–Љ–Є–љ–∞), –њ–Њ—З–Ї–Є (–∞–±—Б–Њ—А–±—Ж–Є—П –∞–Љ–Љ–Є–∞–Ї–∞ –≤–Њ–Ј—А–∞—Б—В–∞–µ—В –њ—А–Є –≥–Є–њ–Њ–Ї–∞–ї–Є–µ–Љ–Є–Є, –∞–ї–Ї–∞–ї–Њ–Ј–µ).
–Я—А–Є –њ–Њ–≤—Л—И–µ–љ–Є–Є —Б–Њ–і–µ—А–ґ–∞–љ–Є—П –∞–Љ–Љ–Є–∞–Ї–∞ –≤ –Њ—А–≥–∞–љ–Є–Ј–Љ–µ –Њ–љ –њ—А–Њ—П–≤–ї—П–µ—В —В–Њ–Ї—Б–Є—З–µ—Б–Ї–Є–µ —Б–≤–Њ–є—Б—В–≤–∞.
–Ф–µ—В–Њ–Ї—Б–Є–Ї–∞—Ж–Є—П –∞–Љ–Љ–Є–∞–Ї–∞ –≤ –Њ—А–≥–∞–љ–Є–Ј–Љ–µ –Њ—Б—Г—Й–µ—Б—В–≤–ї—П–µ—В—Б—П –≤ –Њ—Б–љ–Њ–≤–љ–Њ–Љ –Ј–∞ —Б—З–µ—В –±–Є–Њ—Е–Є–Љ–Є—З–µ—Б–Ї–Њ–≥–Њ —Б–≤—П–Ј—Л–≤–∞–љ–Є—П –≤ –њ–µ—З–µ–љ–Є –Є –Љ—Л—И–µ—З–љ–Њ–є —В–Ї–∞–љ–Є.
–£ –Ј–і–Њ—А–Њ–≤–Њ–≥–Њ —З–µ–ї–Њ–≤–µ–Ї–∞ –њ–µ—З–µ–љ—М –≤–љ–Њ—Б–Є—В –љ–∞–Є–±–Њ–ї–µ–µ –Ј–љ–∞—З–Є–Љ—Л–є –≤–Ї–ї–∞–і –≤ –Њ–±–µ–Ј–≤—А–µ–ґ–Є–≤–∞–љ–Є–µ –∞–Љ–Љ–Є–∞–Ї–∞. –Т –Љ–Є—В–Њ—Е–Њ–љ–і—А–Є—П—Е –њ–µ—А–Є–њ–Њ—А—В–∞–ї—М–љ—Л—Е –≥–µ–њ–∞—В–Њ—Ж–Є—В–Њ–≤ —Д—Г–љ–Ї—Ж–Є–Њ–љ–Є—А—Г–µ—В –Њ—А–љ–Є—В–Є–љ–Њ–≤—Л–є —Ж–Є–Ї–ї, –≤ –Ї–Њ—В–Њ—А–Њ–Љ –∞–Љ–Љ–Є–∞–Ї —Б–≤—П–Ј—Л–≤–∞–µ—В—Б—П —Б –∞–Љ–Є–љ–Њ–Ї–Є—Б–ї–Њ—В–∞–Љ–Є —Б –Њ–±—А–∞–Ј–Њ–≤–∞–љ–Є–µ–Љ –љ–µ—В–Њ–Ї—Б–Є—З–љ–Њ–є –Љ–Њ—З–µ–≤–Є–љ—Л. –Ю–Ї–Њ–ї–Њ 80% –Љ–Њ—З–µ–≤–Є–љ—Л –≤—Л–і–µ–ї—П–µ—В—Б—П —Б –Љ–Њ—З–Њ–є, –∞ –њ—А–Є–Љ–µ—А–љ–Њ 20% –Љ–Њ—З–µ–≤–Є–љ—Л –њ–Њ—Б—В—Г–њ–∞–µ—В –њ–Њ —Б–Є—Б—В–µ–Љ–љ–Њ–є —Ж–Є—А–Ї—Г–ї—П—Ж–Є–Є –≤ –Ц–Ъ–Ґ, –≥–і–µ –≤–љ–Њ–≤—М —А–∞–Ј–ї–∞–≥–∞–µ—В—Б—П —Г—А–µ–∞–Ј–∞––њ–Њ–ї–Њ–ґ–Є—В–µ–ї—М–љ—Л–Љ–Є –±–∞–Ї—В–µ—А–Є—П–Љ–Є –і–Њ –∞–Љ–Љ–Є–∞–Ї–∞.
–Ф–µ—В–Њ–Ї—Б–Є–Ї–∞—Ж–Є—П –∞–Љ–Љ–Є–∞–Ї–∞ –≤ –Љ—Л—И–µ—З–љ–Њ–є —В–Ї–∞–љ–Є –њ—А–Њ–Є—Б—Е–Њ–і–Є—В –≤ –њ—А–Њ—Ж–µ—Б—Б–µ —Б–Є–љ—В–µ–Ј–∞ –≥–ї—Г—В–∞–Љ–Є–љ–∞ –њ—А–Є —Г—З–∞—Б—В–Є–Є –≥–ї—Г—В–∞–Љ–Є–љ—Б–Є–љ—В–µ—В–∞–Ј—Л. –° –Љ–µ–љ—М—И–µ–є –Є–љ—В–µ–љ—Б–Є–≤–љ–Њ—Б—В—М—О —Н—В–∞ –ґ–µ —А–µ–∞–Ї—Ж–Є—П –њ—А–Њ—В–µ–Ї–∞–µ—В –≤ –∞—Б—В—А–Њ—Ж–Є—В–∞—Е –≥–Њ–ї–Њ–≤–љ–Њ–≥–Њ –Љ–Њ–Ј–≥–∞ –Є –њ–µ—А–Є–≤–µ–љ–Њ–Ј–љ—Л—Е –≥–µ–њ–∞—В–Њ—Ж–Є—В–∞—Е –њ–µ—З–µ–љ–Є. –У–ї—Г—В–∞–Љ–Є–љ –љ–µ—В–Њ–Ї—Б–Є—З–µ–љ –Є –≤—Л–і–µ–ї—П–µ—В—Б—П —Б –Љ–Њ—З–Њ–є.
–Я—А–Є –њ–∞—В–Њ–ї–Њ–≥–Є–Є –њ–µ—З–µ–љ–Є –Љ–Њ–ґ–µ—В –љ–∞–±–ї—О–і–∞—В—М—Б—П —А–∞–Ј–≤–Є—В–Є–µ –≥–Є–њ–µ—А–∞–Љ–Љ–Њ–љ–Є–µ–Љ–Є–Є –Ј–∞ —Б—З–µ—В —Б–љ–Є–ґ–µ–љ–Є—П –∞–Ї—В–Є–≤–љ–Њ—Б—В–Є –Њ—А–љ–Є—В–Є–љ–Њ–≤–Њ–≥–Њ —Ж–Є–Ї–ї–∞ –Є –≥–ї—Г—В–∞–Љ–Є–љ—Б–Є–љ—В–µ—В–∞–Ј–љ–Њ–є —А–µ–∞–Ї—Ж–Є–Є –≤ –њ–µ—З–µ–љ–Є, –∞ —В–∞–Ї–ґ–µ –≤ —А–µ–Ј—Г–ї—М—В–∞—В–µ –њ–Њ—А—В–Њ–—Б–Є—Б—В–µ–Љ–љ–Њ–≥–Њ —И—Г–љ—В–Є—А–Њ–≤–∞–љ–Є—П –Ї—А–Њ–≤–Є.
–Э–∞—А—Г—И–µ–љ–Є–µ –і–µ—В–Њ–Ї—Б–Є–Ї–∞—Ж–Є–Є –∞–Љ–Љ–Є–∞–Ї–∞ –≤ –Њ—А–≥–∞–љ–Є–Ј–Љ–µ –≤—Л–Ј—Л–≤–∞–µ—В –Њ—В–µ–Ї –љ–µ–є—А–Њ–≥–ї–Є–Є –Є –і–Є—Б—Д—Г–љ–Ї—Ж–Є—О –∞—Б—В—А–Њ—Ж–Є—В–Њ–≤. –Р–Љ–Љ–Є–∞–Ї –≤ –њ–Њ–≤—Л—И–µ–љ–љ–Њ–є –Ї–Њ–љ—Ж–µ–љ—В—А–∞—Ж–Є–Є –њ—А–Њ–љ–Є–Ї–∞–µ—В —З–µ—А–µ–Ј –≥–µ–Љ–∞—В–Њ—Н–љ—Ж–µ—Д–∞–ї–Є—З–µ—Б–Ї–Є–є –±–∞—А—М–µ—А, –≥–і–µ –Њ–Ї–∞–Ј—Л–≤–∞–µ—В –љ–µ–є—А–Њ—В–Њ–Ї—Б–Є—З–µ—Б–Ї–Є–є —Н—Д—Д–µ–Ї—В: –љ–∞—А—Г—И–∞–µ—В —Н–Ї—Б–њ—А–µ—Б—Б–Є—О –≥–µ–љ–Њ–≤, –Ї–Њ–і–Є—А—Г—О—Й–Є—Е –Ї–ї—О—З–µ–≤—Л–µ –±–µ–ї–Ї–Є –∞—Б—В—А–Њ—Ж–Є—В–Њ–≤, —Б–љ–Є–ґ–∞–µ—В –∞–Ї—В–Є–≤–љ–Њ—Б—В—М –Ї–∞–љ–∞–ї–Њ–≤ —Е–ї–Њ—А–∞ –љ–∞ –Љ–µ–Љ–±—А–∞–љ–µ –љ–µ–є—А–Њ–љ–Њ–≤. –†–µ–Ј—Г–ї—М—В–∞—В–Њ–Љ —П–≤–ї—П–µ—В—Б—П —А–∞–Ј–≤–Є—В–Є–µ —Н–љ—Ж–µ—Д–∞–ї–Њ–њ–∞—В–Є–Є.
–Х—Й–µ –Њ–і–љ–Є–Љ —Б–ї–µ–і—Б—В–≤–Є–µ–Љ –≥–Є–њ–µ—А–∞–Љ–Љ–Њ–љ–Є–µ–Љ–Є–Є —П–≤–ї—П–µ—В—Б—П –љ–∞—А–∞—Б—В–∞–љ–Є–µ –Њ–±—А–∞–Ј–Њ–≤–∞–љ–Є—П –≥–ї—Г—В–∞–Љ–Є–љ–∞ –≤ –∞—Б—В—А–Њ—Ж–Є—В–∞—Е –Є «—А–∞—Б—Е–Њ–і» –≥–ї—Г—В–∞–Љ–∞—В–∞ –Є –∞—Б–њ–∞—А—В–∞—В–∞ – –≤–Њ–Ј–±—Г–ґ–і–∞—О—Й–Є—Е –љ–µ–є—А–Њ—В—А–∞–љ—Б–Љ–Є—В—В–µ—А–Њ–≤.
–Я–Њ–Љ–Є–Љ–Њ –∞–Љ–Љ–Є–∞–Ї–∞, —В–Њ–Ї—Б–Є—З–µ—Б–Ї–Њ–µ –≤–Њ–Ј–і–µ–є—Б—В–≤–Є–µ –љ–∞ –љ–µ—А–≤–љ—Г—О —Б–Є—Б—В–µ–Љ—Г –Њ–Ї–∞–Ј—Л–≤–∞—О—В –і—А—Г–≥–Є–µ —Н–љ–і–Њ–≥–µ–љ–љ—Л–µ —Б—Г–±—Б—В–∞–љ—Ж–Є–Є – –Љ–µ—А–Ї–∞–њ—В–∞–љ—Л, –њ—А–Њ–Є–Ј–≤–Њ–і–љ—Л–µ –Љ–µ—В–Є–Њ–љ–Є–љ–∞, –Ї–Њ—А–Њ—В–Ї–Њ– –Є —Б—А–µ–і–љ–µ—Ж–µ–њ–Њ—З–µ—З–љ—Л–µ –ґ–Є—А–љ—Л–µ –Ї–Є—Б–ї–Њ—В—Л, —Д–µ–љ–Њ–ї—Л.
–Т –љ–µ–Љ–∞–ї–Њ–є —Б—В–µ–њ–µ–љ–Є —А–∞—Б—Б—В—А–Њ–є—Б—В–≤–∞ —Д—Г–љ–Ї—Ж–Є–є –љ–µ—А–≤–љ–Њ–є —Б–Є—Б—В–µ–Љ—Л —Б–≤—П–Ј–∞–љ—Л —Б –љ–∞—А—Г—И–µ–љ–Є–µ–Љ –∞–Љ–Є–љ–Њ–Ї–Є—Б–ї–Њ—В–љ–Њ–≥–Њ —А–∞–≤–љ–Њ–≤–µ—Б–Є—П, –Ї–Њ—В–Њ—А–Њ–µ –љ–∞–±–ї—О–і–∞–µ—В—Б—П –њ—А–Є —В—П–ґ–µ–ї—Л—Е –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П—Е –њ–µ—З–µ–љ–Є –≤—Б–ї–µ–і—Б—В–≤–Є–µ —А–∞—Б—Б—В—А–Њ–є—Б—В–≤ –±–µ–ї–Ї–Њ–≤–Њ–—Н–љ–µ—А–≥–µ—В–Є—З–µ—Б–Ї–Њ–≥–Њ –Њ–±–Љ–µ–љ–∞. –Ю—В–Љ–µ—З–∞–µ—В—Б—П –њ–Њ–≤—Л—И–µ–љ–љ—Л–є —А–∞—Б—Е–Њ–і –∞–Љ–Є–љ–Њ–Ї–Є—Б–ї–Њ—В —Б —А–∞–Ј–≤–µ—В–≤–ї–µ–љ–љ–Њ–є –±–Њ–Ї–Њ–≤–Њ–є —Ж–µ–њ—М—О (–ї–µ–є—Ж–Є–љ–∞, –Є–Ј–Њ–ї–µ–є—Ж–Є–љ–∞, –≤–∞–ї–Є–љ–∞) –≤ –Ї–∞—В–∞–±–Њ–ї–Є—З–µ—Б–Ї–Є—Е —А–µ–∞–Ї—Ж–Є—П—Е –і–µ–Ј–∞–Љ–Є–љ–Є—А–Њ–≤–∞–љ–Є—П –Є –Њ—В–љ–Њ—Б–Є—В–µ–ї—М–љ–Њ–µ –њ—А–µ–Њ–±–ї–∞–і–∞–љ–Є–µ –∞—А–Њ–Љ–∞—В–Є—З–µ—Б–Ї–Є—Е –∞–Љ–Є–љ–Њ–Ї–Є—Б–ї–Њ—В (—Д–µ–љ–Є–ї–∞–ї–∞–љ–Є–љ–∞, —В–Є—А–Њ–Ј–Є–љ–∞, —В—А–Є–њ—В–Њ—Д–∞–љ–∞, –≥–Є—Б—В–Є–і–Є–љ–∞). –Т —Д–Є–Ј–Є–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є—Е —Г—Б–ї–Њ–≤–Є—П—Е —Д–µ–љ–Є–ї–∞–ї–∞–љ–Є–љ –Є —В–Є—А–Њ–Ј–Є–љ —П–≤–ї—П—О—В—Б—П –Є—Б—В–Њ—З–љ–Є–Ї–∞–Љ–Є —Б–Є–љ—В–µ–Ј–∞ –њ—А–µ–Є–Љ—Г—Й–µ—Б—В–≤–µ–љ–љ–Њ –≤–Њ–Ј–±—Г–ґ–і–∞—О—Й–Є—Е –љ–µ–є—А–Њ–Љ–µ–і–Є–∞—В–Њ—А–Њ–≤ –≤ –¶–Э–° (–і–Є–Њ–Ї—Б–Є—Д–µ–љ–Є–ї–∞–ї–∞–љ–Є–љ–∞, –і–Њ—Д–∞–Љ–Є–љ–∞ –Є –Ї–∞—В–µ—Е–Њ–ї–∞–Љ–Є–љ–Њ–≤). –Т —Г—Б–ї–Њ–≤–Є—П—Е –њ–µ—З–µ–љ–Њ—З–љ–Њ–є –љ–µ–і–Њ—Б—В–∞—В–Њ—З–љ–Њ—Б—В–Є –≤ —А–µ–Ј—Г–ї—М—В–∞—В–µ –Є–Ј–±—Л—В–Ї–∞ –∞—А–Њ–Љ–∞—В–Є—З–µ—Б–Ї–Є—Е –∞–Љ–Є–љ–Њ–Ї–Є—Б–ї–Њ—В –Є –ї–µ–≥–Ї–Њ–≥–Њ –Є—Е –њ—А–Њ–љ–Є–Ї–љ–Њ–≤–µ–љ–Є—П —З–µ—А–µ–Ј –≥–µ–Љ–∞—В–Њ—Н–љ—Ж–µ—Д–∞–ї–Є—З–µ—Б–Ї–Є–є –±–∞—А—М–µ—А (–Є–Ј –≥–Њ–ї–Њ–≤–љ–Њ–≥–Њ –Љ–Њ–Ј–≥–∞ –≥–ї—Г—В–∞–Љ–Є–љ —В—А–∞–љ—Б–њ–Њ—А—В–Є—А—Г–µ—В—Б—П –≤ –Њ–±–Љ–µ–љ –љ–∞ –∞–Љ–Є–љ–Њ–Ї–Є—Б–ї–Њ—В—Л) –Љ–µ—В–∞–±–Њ–ї–Є–Ј–Љ –∞—А–Њ–Љ–∞—В–Є—З–µ—Б–Ї–Є—Е —Б–Њ–µ–і–Є–љ–µ–љ–Є–є –њ—А–Њ—В–µ–Ї–∞–µ—В –∞–ї—М—В–µ—А–љ–∞—В–Є–≤–љ—Л–Љ –њ—Г—В–µ–Љ —Б –љ–∞–Ї–Њ–њ–ї–µ–љ–Є–µ–Љ –≤ –¶–Э–° —В–∞–Ї –љ–∞–Ј—Л–≤–∞–µ–Љ—Л—Е –ї–Њ–ґ–љ—Л—Е –љ–µ–є—А–Њ—В—А–∞–љ—Б–Љ–Є—В—В–µ—А–Њ–≤, –Њ–Ї–∞–Ј—Л–≤–∞—О—Й–Є—Е —В–Њ—А–Љ–Њ–Ј—П—Й–µ–µ –≤–ї–Є—П–љ–Є–µ (–Њ–Ї—В–Њ–њ–∞–Љ–Є–љ–∞, —Д–µ–љ–Є–ї—Н—В–Є–ї–∞–Љ–Є–љ–∞, —В–Є—А–∞–Љ–Є–љ–∞).
–Я–Њ–Љ–Є–Љ–Њ —Н—В–Њ–≥–Њ, —А–∞–Ј–≤–Є—В–Є—О –њ–µ—З–µ–љ–Њ—З–љ–Њ–є —Н–љ—Ж–µ—Д–∞–ї–Њ–њ–∞—В–Є–Є —Б–њ–Њ—Б–Њ–±—Б—В–≤—Г–µ—В –њ–Њ–≤—Л—И–µ–љ–Є–µ –њ—А–Њ–љ–Є—Ж–∞–µ–Љ–Њ—Б—В–Є –≥–µ–Љ–∞—В–Њ—Н–љ—Ж–µ—Д–∞–ї–Є—З–µ—Б–Ї–Њ–≥–Њ –±–∞—А—М–µ—А–∞, –љ–∞—А—Г—И–µ–љ–Є–µ —В—А–∞–љ—Б–њ–Њ—А—В–∞ —Н–љ–µ—А–≥–µ—В–Є—З–µ—Б–Ї–Є—Е —Б—Г–±—Б—В—А–∞—В–Њ–≤, –њ–Њ–≤—Л—И–µ–љ–Є–µ –∞–Ї—В–Є–≤–љ–Њ—Б—В–Є –±–µ–љ–Ј–Њ–і–Є–∞–Ј–µ–њ–Є–љ–Њ–≤—Л—Е —А–µ—Ж–µ–њ—В–Њ—А–Њ–≤.
–Т –ї–µ—З–µ–љ–Є–Є –њ–µ—З–µ–љ–Њ—З–љ–Њ–є —Н–љ—Ж–µ—Д–∞–ї–Њ–њ–∞—В–Є–Є, –њ–Њ–Љ–Є–Љ–Њ –љ–µ–Њ–±—Е–Њ–і–Є–Љ—Л—Е —В—А–∞–і–Є—Ж–Є–Њ–љ–љ—Л—Е –Љ–µ—А–Њ–њ—А–Є—П—В–Є–є, –≤–Ї–ї—О—З–∞—О—Й–Є—Е –≤ —Б–µ–±—П –≤—Л—П–≤–ї–µ–љ–Є–µ –Є —Г—Б—В—А–∞–љ–µ–љ–Є–µ —А–∞–Ј—А–µ—И–∞—О—Й–Є—Е —Д–∞–Ї—В–Њ—А–Њ–≤, –≤—А–µ–Љ–µ–љ–љ–Њ–µ —Б–Њ–±–ї—О–і–µ–љ–Є–µ –і–Є–µ—В—Л —Б –њ–Њ–љ–Є–ґ–µ–љ–љ—Л–Љ —Б–Њ–і–µ—А–ґ–∞–љ–Є–µ–Љ –±–µ–ї–Ї–∞, –љ–∞–Ј–љ–∞—З–µ–љ–Є–µ –Њ—З–Є—Б—В–Є—В–µ–ї—М–љ—Л—Е –Ї–ї–Є–Ј–Љ (–≤–Њ–Ј–Љ–Њ–ґ–љ–Њ –і–Њ–±–∞–≤–ї–µ–љ–Є–µ –≤ –љ–Є—Е –ї–∞–Ї—В—Г–ї–Њ–Ј—Л), —Б–ї–∞–±–Є—В–µ–ї—М–љ—Л—Е (–Љ–∞–љ–љ–Є—В–Њ–ї, —Б—Г–ї—М—Д–∞—В –Љ–∞–≥–љ–Є—П, –ї–∞–Ї—В—Г–ї–Њ–Ј–∞), –∞–љ—В–Є–±–Є–Њ—В–Є–Ї–Њ–≤ (–љ–µ–Њ–Љ–Є—Ж–Є–љ–∞, –Љ–µ—В—А–Њ–љ–Є–і–∞–Ј–Њ–ї–∞, –≤–∞–љ–Ї–Њ–Љ–Є—Ж–Є–љ–∞), –Є—Б–њ–Њ–ї—М–Ј—Г–µ—В—Б—П –љ–∞–Ј–љ–∞—З–µ–љ–Є–µ –њ—А–µ–њ–∞—А–∞—В–Њ–≤, —Б—В–Є–Љ—Г–ї–Є—А—Г—О—Й–Є—Е –њ—А–Њ—Ж–µ—Б—Б—Л –Њ–±–µ–Ј–≤—А–µ–ґ–Є–≤–∞–љ–Є—П «–Љ–µ–і–Є–∞—В–Њ—А–Њ–≤ —Н–љ—Ж–µ—Д–∞–ї–Њ–њ–∞—В–Є–Є». –Я—А–Є –њ–Њ–±–Њ—З–љ–Њ–Љ –і–µ–є—Б—В–≤–Є–Є –±–µ–љ–Ј–Њ–і–Є–∞–Ј–µ–њ–Є–љ–Њ–≤ –њ–Њ–Ї–∞–Ј–∞–љ–Њ –љ–∞–Ј–љ–∞—З–µ–љ–Є–µ –∞–љ—В–∞–≥–Њ–љ–Є—Б—В–∞ –±–µ–љ–Ј–Њ–і–Є–∞–Ј–µ–њ–Є–љ–Њ–≤—Л—Е —А–µ—Ж–µ–њ—В–Њ—А–Њ–≤ – —Д–ї—Г–Љ–∞–Ј–µ–љ–Є–ї–∞.
–Я–Њ–і—Е–Њ–і –Ї –≤–µ–і–µ–љ–Є—О –њ–∞—Ж–Є–µ–љ—В–∞ —Б –Я–≠ –і–Њ–ї–ґ–µ–љ –±—Л—В—М —Б—В—Г–њ–µ–љ—З–∞—В—Л–Љ. –Ъ–Њ–Љ–±–Є–љ–∞—Ж–Є—П –ї–µ—З–µ–±–љ—Л—Е –Љ–µ—А–Њ–њ—А–Є—П—В–Є–є –Њ–њ—А–µ–і–µ–ї—П–µ—В—Б—П –≤—Л—А–∞–ґ–µ–љ–љ–Њ—Б—В—М—О —Б–Є–Љ–њ—В–Њ–Љ–∞—В–Є–Ї–Є (—В–∞–±–ї. 5).
–Т –Њ—В–љ–Њ—И–µ–љ–Є–Є —Б–≤—П–Ј—Л–≤–∞–љ–Є—П –∞–Љ–Љ–Є–∞–Ї–∞ –љ–∞–Є–±–Њ–ї–µ–µ –Љ–Њ—Й–љ—Л–Љ –∞–≥–µ–љ—В–Њ–Љ –њ—А–Є–Ј–љ–∞–љ –Њ—А–љ–Є—В–Є–љ––∞—Б–њ–∞—А—В–∞—В, —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В—М –Ї–Њ—В–Њ—А–Њ–≥–Њ –і–Њ–Ї–∞–Ј–∞–љ–∞ –≤ —А–∞–љ–і–Њ–Љ–Є–Ј–Є—А–Њ–≤–∞–љ–љ—Л—Е –Ї–Њ–љ—В—А–Њ–ї–Є—А—Г–µ–Љ—Л—Е –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П—Е. –≠—В–Њ –љ–µ–Ј–∞–Љ–µ–љ–Є–Љ–Њ–µ —Б—А–µ–і—Б—В–≤–Њ –ї–µ—З–µ–љ–Є—П –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –Я–≠ III –Є IV —Б—В–∞–і–Є–Є.
–Ф–ї—П –Ї–Њ—А—А–µ–Ї—Ж–Є–Є –∞–Љ–Є–љ–Њ–Ї–Є—Б–ї–Њ—В–љ–Њ–≥–Њ —А–∞–≤–љ–Њ–≤–µ—Б–Є—П –њ—А–Є –њ–µ—З–µ–љ–Њ—З–љ–Њ–є –љ–µ–і–Њ—Б—В–∞—В–Њ—З–љ–Њ—Б—В–Є, –њ–µ—З–µ–љ–Њ—З–љ–Њ–є —Н–љ—Ж–µ—Д–∞–ї–Њ–њ–∞—В–Є–Є –њ–Њ–Ї–∞–Ј–∞–љ–Њ —Н–љ—В–µ—А–∞–ї—М–љ–Њ–µ –Є–ї–Є –њ–∞—А–µ–љ—В–µ—А–∞–ї—М–љ–Њ–µ –љ–∞–Ј–љ–∞—З–µ–љ–Є–µ –њ—А–µ–њ–∞—А–∞—В–Њ–≤ –∞–Љ–Є–љ–Њ–Ї–Є—Б–ї–Њ—В —Б —А–∞–Ј–≤–µ—В–≤–ї–µ–љ–љ–Њ–є –±–Њ–Ї–Њ–≤–Њ–є —Ж–µ–њ—М—О.
–Я—А–Є –≤–µ–і–µ–љ–Є–Є –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –њ–µ—З–µ–љ–Њ—З–љ–Њ–є –љ–µ–і–Њ—Б—В–∞—В–Њ—З–љ–Њ—Б—В—М—О –љ–µ–Њ–±—Е–Њ–і–Є–Љ–Њ –њ–Њ–Љ–љ–Є—В—М –Њ —В–Њ–Љ, —З—В–Њ –њ—А–Њ–≤–Њ–і–Є–Љ–Њ–µ –ї–µ—З–µ–љ–Є–µ –љ–µ –±—Г–і–µ—В –і–Њ—Б—В–∞—В–Њ—З–љ–Њ —Н—Д—Д–µ–Ї—В–Є–≤–љ—Л–Љ –±–µ–Ј –∞–і–µ–Ї–≤–∞—В–љ–Њ–≥–Њ –Њ–±–µ—Б–њ–µ—З–µ–љ–Є—П –Њ—А–≥–∞–љ–Є–Ј–Љ–∞ —Н–љ–µ—А–≥–Є–µ–є. –Я—А–Њ—Ж–µ—Б—Б—Л –і–µ—В–Њ–Ї—Б–Є–Ї–∞—Ж–Є–Є –∞–Љ–Љ–Є–∞–Ї–∞, –њ—А–Њ—В–µ–Ї–∞—О—Й–Є–µ –≤ –њ–µ—З–µ–љ–Є –Є –Љ—Л—И–µ—З–љ–Њ–є —В–Ї–∞–љ–Є, —П–≤–ї—П—О—В—Б—П —Н–љ–µ—А–≥–Њ–µ–Љ–Ї–Є–Љ–Є. –Ъ—А–Њ–Љ–µ —В–Њ–≥–Њ, –Њ–±–µ—Б–њ–µ—З–µ–љ–Є–µ —Н–љ–µ—А–≥–Є–µ–є –њ–Њ–Ј–≤–Њ–ї—П–µ—В —Г–Љ–µ–љ—М—И–Є—В—М —А–∞—Б—Е–Њ–і –∞–Љ–Є–љ–Њ–Ї–Є—Б–ї–Њ—В —Б —А–∞–Ј–≤–µ—В–≤–ї–µ–љ–љ–Њ–є –±–Њ–Ї–Њ–≤–Њ–є —Ж–µ–њ—М—О –≤ —А–µ–∞–Ї—Ж–Є—П—Е –і–µ–Ј–∞–Љ–Є–љ–Є—А–Њ–≤–∞–љ–Є—П. –Я–Њ—Б–Ї–Њ–ї—М–Ї—Г –≤—Л—А–∞–ґ–µ–љ–љ–Њ—Б—В—М –њ–µ—З–µ–љ–Њ—З–љ–Њ–є —Н–љ—Ж–µ—Д–∞–ї–Њ–њ–∞—В–Є–Є –Ї–Њ—А—А–µ–ї–Є—А—Г–µ—В —Б –њ–Њ—В–µ—А–µ–є –Љ—Л—И–µ—З–љ–Њ–є –Љ–∞—Б—Б—Л, –Љ–µ—А–Њ–њ—А–Є—П—В–Є—П, –љ–∞–њ—А–∞–≤–ї–µ–љ–љ—Л–µ –љ–∞ —Б–Њ—Е—А–∞–љ–µ–љ–Є–µ –Љ—Л—И–µ—З–љ–Њ–є –Љ–∞—Б—Б—Л (–≤–Ї–ї—О—З–∞—П –љ–∞–Ј–љ–∞—З–µ–љ–Є–µ –∞–Љ–Є–љ–Њ–Ї–Є—Б–ї–Њ—В, –Њ–±–ї–∞–і–∞—О—Й–Є—Е –∞–љ–∞–±–Њ–ї–Є—З–µ—Б–Ї–Є–Љ –і–µ–є—Б—В–≤–Є–µ–Љ) —В–∞–Ї–ґ–µ –Љ–Њ–≥—Г—В —Б–њ–Њ—Б–Њ–±—Б—В–≤–Њ–≤–∞—В—М –њ–Њ–≤—Л—И–µ–љ–Є—О —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В–Є —В–µ—А–∞–њ–Є–Є.
–Я—А–µ–њ–∞—А–∞—В –У–µ–њ–∞—Б–Њ–ї –Р, –≤—Л–њ—Г—Б–Ї–∞–µ–Љ—Л–є —Д–∞—А–Љ–∞—Ж–µ–≤—В–Є—З–µ—Б–Ї–Њ–є –Ї–Њ–Љ–њ–∞–љ–Є–µ–є Hemopharm D.D., –Ї–ї–∞—Б—Б–Є—Д–Є—Ж–Є—А—Г–µ—В—Б—П –Ї–∞–Ї —Б–њ–µ—Ж–Є–∞–ї—М–љ–Њ–µ —Б—А–µ–і—Б—В–≤–Њ –і–ї—П –њ–∞—А–µ–љ—В–µ—А–∞–ї—М–љ–Њ–≥–Њ –њ–Є—В–∞–љ–Є—П –±–Њ–ї—М–љ—Л—Е —Б –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П–Љ–Є –њ–µ—З–µ–љ–Є –Є –≥–Є–њ–µ—А–∞–Љ–Љ–Њ–љ–Є–µ–Љ–Є–µ–є.
–Т —Б–Њ—Б—В–∞–≤ –њ—А–µ–њ–∞—А–∞—В–∞ –≤—Е–Њ–і—П—В L––∞—А–≥–Є–љ–Є–љ, –∞—Б–њ–∞—А–∞–≥–Є–љ–Њ–≤–∞—П –Ї–Є—Б–ї–Њ—В–∞, —Б–Њ—А–±–Є—В, L–—П–±–ї–Њ—З–љ–∞—П –Ї–Є—Б–ї–Њ—В–∞, —А–Є–±–Њ—Д–ї–∞–≤–Є–љ (–≤–Є—В–∞–Љ–Є–љ –Т2), –і–µ–Ї—Б–њ–∞–љ—В–µ–љ–Њ–ї (–≤–Є—В–∞–Љ–Є–љ –Т3), –њ–Є—А–Є–і–Њ–Ї—Б–Є–љ (–≤–Є—В–∞–Љ–Є–љ –Т6), –љ–Є–Ї–Њ—В–Є–љ–∞–Љ–Є–і (–≤–Є—В–∞–Љ–Є–љ –†–†), —В–∞–Ї–ґ–µ –Є–Њ–љ—Л Na+, K+, Cl–. –≠–љ–µ—А–≥–µ—В–Є—З–µ—Б–Ї–∞—П —Ж–µ–љ–љ–Њ—Б—В—М 1 –ї–Є—В—А–∞ —А–∞—Б—В–≤–Њ—А–∞ –У–µ–њ–∞—Б–Њ–ї–∞ –Р —Б–Њ—Б—В–∞–≤–ї—П–µ—В 200 –Ї–Ї–∞–ї. –Ю—Б–Љ–Њ–ї—П—А–љ–Њ—Б—В—М —А–∞—Б—В–≤–Њ—А–∞ – 678 –Љ–Ю—Б–Љ/–ї.
–У–ї–∞–≤–љ—Л–Љ –ї–µ—З–µ–±–љ—Л–Љ –і–µ–є—Б—В–≤–Є–µ–Љ –У–µ–њ–∞—Б–Њ–ї–∞ –Р —Б–ї—Г–ґ–Є—В –µ–≥–Њ —Б–њ–Њ—Б–Њ–±–љ–Њ—Б—В—М —Б–љ–Є–ґ–∞—В—М –≤—Л—А–∞–ґ–µ–љ–љ–Њ—Б—В—М –≥–Є–њ–µ—А–∞–Љ–Љ–Њ–љ–Є–µ–Љ–Є–Є. –Ш –≤ —Н—В–Њ–Љ –Њ—В–љ–Њ—И–µ–љ–Є–Є –Њ–і–љ–Є–Љ–Є –Є–Ј –љ–∞–Є–±–Њ–ї–µ–µ –≤–∞–ґ–љ—Л—Е –і–µ–є—Б—В–≤—Г—О—Й–Є—Е –Ї–Њ–Љ–њ–Њ–љ–µ–љ—В–Њ–≤ –њ—А–µ–њ–∞—А–∞—В–∞ —П–≤–ї—П—О—В—Б—П L––∞—А–≥–Є–љ–Є–љ, –∞—Б–њ–∞—А–∞–≥–Є–љ–Њ–≤–∞—П –Ї–Є—Б–ї–Њ—В–∞, —П–±–ї–Њ—З–љ–∞—П –Ї–Є—Б–ї–Њ—В–∞ (–Љ–∞–ї–∞—В), —А–Є–±–Њ—Д–ї–∞–≤–Є–љ –Є –њ–Є—А–Є–і–Њ–Ї—Б–Є–љ.
–Р—Б–њ–∞—А–∞–≥–Є–љ –Є –∞—А–≥–Є–љ–Є–љ —Б–ї—Г–ґ–∞—В –Њ–і–љ–Є–Љ–Є –Є–Ј –≤–∞–ґ–љ—Л—Е —Б—Г–±—Б—В—А–∞—В–Њ–≤ –Њ—А–љ–Є—В–Є–љ–Њ–≤–Њ–≥–Њ —Ж–Є–Ї–ї–∞ —Б–Є–љ—В–µ–Ј–∞ –Љ–Њ—З–µ–≤–Є–љ—Л, –Ї–Њ—В–Њ—А—Л–є –њ—А–Њ–Є—Б—Е–Њ–і–Є—В –≤ –њ–µ—З–µ–љ–Є. –ѓ–±–ї–Њ—З–љ–∞—П –Ї–Є—Б–ї–Њ—В–∞ —Б–ї—Г–ґ–Є—В –Њ—Б–љ–Њ–≤–Њ–є –і–ї—П –њ–Њ–њ–Њ–ї–љ–µ–љ–Є—П –Ј–∞–њ–∞—Б–Њ–≤ –∞—Б–њ–∞—А–∞–≥–Є–љ–∞ –≤ –Њ—А–≥–∞–љ–Є–Ј–Љ–µ. –Т–∞–ґ–љ–Њ –њ–Њ–Љ–љ–Є—В—М –Њ —В–Њ–Љ, —З—В–Њ –њ—А–Њ—Ж–µ—Б—Б —Б–Є–љ—В–µ–Ј–∞ –Љ–Њ—З–µ–≤–Є–љ—Л –≤ –Њ—А–љ–Є—В–Є–љ–Њ–≤–Њ–Љ —Ж–Є–Ї–ї–µ —Б–Њ–њ—А–Њ–≤–Њ–ґ–і–∞–µ—В—Б—П —Б—Г—Й–µ—Б—В–≤–µ–љ–љ—Л–Љ–Є –Ј–∞—В—А–∞—В–∞–Љ–Є —Н–љ–µ—А–≥–Є–Є.
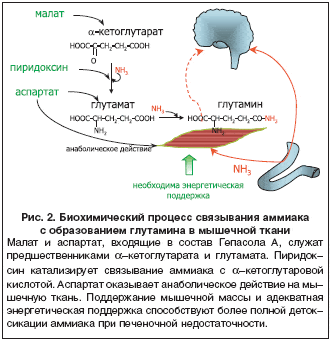
–£—З–∞—Б—В–Є–µ –∞—Б–њ–∞—А–∞–≥–Є–љ–∞, –∞—А–≥–Є–љ–Є–љ–∞ –Є –Љ–∞–ї–∞—В–∞ –≤ –±–Є–Њ—Е–Є–Љ–Є—З–µ—Б–Ї–Є—Е –њ—А–Њ—Ж–µ—Б—Б–∞—Е –Њ–±–µ–Ј–≤—А–µ–ґ–Є–≤–∞–љ–Є—П –∞–Љ–Љ–Є–∞–Ї–∞ –≤ –њ–µ—З–µ–љ–Є —Б—Е–µ–Љ–∞—В–Є—З–љ–Њ –њ—А–µ–і—Б—В–∞–≤–ї–µ–љ–Њ –љ–∞ —А–Є—Б—Г–љ–Ї–µ 1.
–Ъ–∞–Ї –Є–Ј–≤–µ—Б—В–љ–Њ, –њ—А–Є –њ–µ—З–µ–љ–Њ—З–љ–Њ–є –љ–µ–і–Њ—Б—В–∞—В–Њ—З–љ–Њ—Б—В–Є –Ї–Њ–Љ–њ–µ–љ—Б–∞—В–Њ—А–љ–∞—П –љ–∞–≥—А—Г–Ј–Ї–∞ –њ–Њ –Њ–±–µ–Ј–≤—А–µ–ґ–Є–≤–∞–љ–Є—О –∞–Љ–Љ–Є–∞–Ї–∞ –≤ –Њ—А–≥–∞–љ–Є–Ј–Љ–µ –ї–Њ–ґ–Є—В—Б—П –љ–∞ –Љ—Л—И–µ—З–љ—Г—О —Б–Є—Б—В–µ–Љ—Г. –Ч–і–µ—Б—М –њ—А–Њ–Є—Б—Е–Њ–і–Є—В —Б–≤—П–Ј—Л–≤–∞–љ–Є–µ –∞–Љ–Љ–Є–∞–Ї–∞ —Б a––Ї–µ—В–Њ–≥–ї—Г—В–∞—А–∞—В–Њ–Љ –Є –≤ –і–∞–ї—М–љ–µ–є—И–µ–Љ —Б –≥–ї—Г—В–∞–Љ–∞—В–Њ–Љ, —Б –Њ–±—А–∞–Ј–Њ–≤–∞–љ–Є–µ–Љ –≥–ї—Г—В–∞–Љ–Є–љ–∞. –Ф–Њ–њ–Њ–ї–љ–Є—В–µ–ї—М–љ—Л–Љ —Б—Г–±—Б—В—А–∞—В–Њ–Љ –і–ї—П —Б–Є–љ—В–µ–Ј–∞ a––Ї–µ—В–Њ–≥–ї—Г—В–∞—А–Њ–≤–Њ–є –Ї–Є—Б–ї–Њ—В—Л –Љ–Њ–ґ–µ—В –≤—Л—Б—В—Г–њ–∞—В—М –Љ–∞–ї–∞—В, –∞ –і–ї—П —Б–Є–љ—В–µ–Ј–∞ –≥–ї—Г—В–∞–Љ–∞—В–∞ – –∞—Б–њ–∞—А—В–∞—В. –Я–Є—А–Є–і–Њ–Ї—Б–Є–љ –≤—Л—Б—В—Г–њ–∞–µ—В –≤ —А–Њ–ї–Є –Ї–Њ—Д–µ—А–Љ–µ–љ—В–∞ –≤ –њ—А–Њ—Ж–µ—Б—Б–µ –њ–µ—А–µ–љ–Њ—Б–∞ –∞–Љ–Є–љ–Њ–∞—Ж–Є–і–Њ–≥—А—Г–њ–њ—Л –љ–∞ a––Ї–µ—В–Њ–≥–ї—Г—В–∞—А–∞—В. –Ф–∞–љ–љ—Л–µ –њ—А–Њ—Ж–µ—Б—Б—Л —В–∞–Ї–ґ–µ —Б–Њ–њ—А–Њ–≤–Њ–ґ–і–∞—О—В—Б—П –њ–Њ—В—А–µ–±–ї–µ–љ–Є–µ–Љ –Ј–љ–∞—З–Є—В–µ–ї—М–љ–Њ–≥–Њ –Ї–Њ–ї–Є—З–µ—Б—В–≤–∞ —Н–љ–µ—А–≥–Є–Є (—А–Є—Б. 2).
–Ш–Ј–≤–µ—Б—В–љ–Њ, —З—В–Њ –љ–∞—А—Г—И–µ–љ–Є–µ –і–µ—В–Њ–Ї—Б–Є–Ї–∞—Ж–Є–Є –∞–Љ–Љ–Є–∞–Ї–∞ –њ—А–Є –њ–µ—З–µ–љ–Њ—З–љ–Њ–є –љ–µ–і–Њ—Б—В–∞—В–Њ—З–љ–Њ—Б—В–Є –Ї–Њ—А—А–µ–ї–Є—А—Г–µ—В —Б–Њ —Б–љ–Є–ґ–µ–љ–Є–µ–Љ –Љ—Л—И–µ—З–љ–Њ–є –Љ–∞—Б—Б—Л. –Я–Њ—Н—В–Њ–Љ—Г –Њ–і–љ–Њ–є –Є–Ј –≤–∞–ґ–љ—Л—Е –Ј–∞–і–∞—З –ї–µ—З–µ–љ–Є—П –±–Њ–ї—М–љ—Л—Е —Б –њ–µ—З–µ–љ–Њ—З–љ–Њ–є –љ–µ–і–Њ—Б—В–∞—В–Њ—З–љ–Њ—Б—В—М—О —Б–ї—Г–ґ–Є—В –∞–і–µ–Ї–≤–∞—В–љ–∞—П —В—А–Њ—Д–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–∞—П –њ–Њ–і–і–µ—А–ґ–Ї–∞, –Њ–±–µ—Б–њ–µ—З–µ–љ–Є–µ –Њ—А–≥–∞–љ–Є–Ј–Љ–∞ –і–Њ—Б—В–∞—В–Њ—З–љ—Л–Љ –Ї–Њ–ї–Є—З–µ—Б—В–≤–Њ–Љ —Н–љ–µ—А–≥–Є–Є –Є —Б–Њ—Е—А–∞–љ–µ–љ–Є–µ –Љ—Л—И–µ—З–љ–Њ–є –Љ–∞—Б—Б—Л. –Ъ–Њ–Љ–њ–Њ–љ–µ–љ—В –У–µ–њ–∞—Б–Њ–ї–∞ –Р – –∞—Б–њ–∞—А—В–∞—В – –Њ–Ї–∞–Ј—Л–≤–∞–µ—В –∞–љ–∞–±–Њ–ї–Є—З–µ—Б–Ї–Њ–µ –і–µ–є—Б—В–≤–Є–µ –љ–∞ –Љ—Л—И–µ—З–љ—Г—О —В–Ї–∞–љ—М.
–У–µ–њ–∞—Б–Њ–ї –Р –≤ —Б–≤–Њ–µ–Љ —Б–Њ—Б—В–∞–≤–µ —Б–Њ–і–µ—А–ґ–Є—В –љ–µ–Ї–Њ—В–Њ—А—Л–µ —Н–љ–µ—А–≥–µ—В–Є—З–µ—Б–Ї–Є–µ —Б—Г–±—Б—В—А–∞—В—Л, —В–∞–Ї–Є–µ –Ї–∞–Ї —Б–Њ—А–±–Є—В, —П–±–ї–Њ—З–љ–∞—П –Ї–Є—Б–ї–Њ—В–∞ –Є –љ–µ–Ї–Њ—В–Њ—А—Л–µ –≤–Є—В–∞–Љ–Є–љ—Л – —А–Є–±–Њ—Д–ї–∞–≤–Є–љ, –њ–Є—А–Є–і–Њ–Ї—Б–Є–љ, –і–µ–Ї—Б–∞–њ–∞–љ—В–µ–љ–Њ–ї, –љ–Є–Ї–Њ—В–Є–љ–∞–Љ–Є–і (—А–Є—Б. 3).
–ѓ–±–ї–Њ—З–љ–∞—П –Ї–Є—Б–ї–Њ—В–∞ –Є —Б–Њ—А–±–Є—В –≤–Ї–ї—О—З–∞—О—В—Б—П –≤ —Ж–Є–Ї–ї –Ъ—А–µ–±—Б–∞. –†–Є–±–Њ—Д–ї–∞–≤–Є–љ – –≤–Њ–і–Њ—А–∞—Б—В–≤–Њ—А–Є–Љ—Л–є –≤–Є—В–∞–Љ–Є–љ, –љ–µ–Њ–±—Е–Њ–і–Є–Љ—Л–є –і–ї—П –њ—А–Њ—П–≤–ї–µ–љ–Є—П –і–µ–є—Б—В–≤–Є—П –њ–Є—А–Є–і–Њ–Ї—Б–Є–љ–∞ –Є –љ–Є–Ї–Њ—В–Є–љ–Њ–≤–Њ–є –Ї–Є—Б–ї–Њ—В—Л. –Э–Є–Ї–Њ—В–Є–љ–∞–Љ–Є–і —Б–ї—Г–ґ–Є—В –і–ї—П —Б–Є–љ—В–µ–Ј–∞ –Ї–Њ—Д–µ—А–Љ–µ–љ—В–Њ–≤ –Э–Р–Ф –Є –Э–Р–Ф–§, –њ—А–Є–љ–Є–Љ–∞—О—Й–Є—Е —Г—З–∞—Б—В–Є–µ –≤ –њ–µ—А–µ–љ–Њ—Б–µ —Н–ї–µ–Ї—В—А–Њ–љ–Њ–≤ –≤ —А–µ–∞–Ї—Ж–Є—П—Е –Њ–Ї–Є—Б–ї–µ–љ–Є—П –Є –≤–Њ—Б—Б—В–∞–љ–Њ–≤–ї–µ–љ–Є—П. –Я–Є—А–Є–і–Њ–Ї—Б–Є–љ —П–≤–ї—П–µ—В—Б—П –≤–∞–ґ–љ–µ–є—И–Є–Љ –Ї–∞—В–∞–ї–Є–Ј–∞—В–Њ—А–Њ–Љ –њ—А–Њ—Ж–µ—Б—Б–Њ–≤ —Г–≥–ї–µ–≤–Њ–і–љ–Њ–≥–Њ –Є –ґ–Є—А–Њ–≤–Њ–≥–Њ –Њ–±–Љ–µ–љ–∞ (–≤—Л—Б—В—Г–њ–∞–µ—В –≤ —А–Њ–ї–Є –Ї–Њ—Д–µ—А–Љ–µ–љ—В–∞ –≤ —Ж–Є–Ї–ї–µ –Ъ—А–µ–±—Б–∞, –њ—А–Є –њ–µ—А–µ–љ–Њ—Б–µ –Ї–∞—А–±–Њ–Ї—Б–Є–ї—М–љ–Њ–є –≥—А—Г–њ–њ—Л).
–Ф–µ–Ї—Б–њ–∞–љ—В–µ–љ–Њ–ї –≤–Ї–ї—О—З–∞–µ—В—Б—П –≤ –Ї–Њ—Н–љ–Ј–Є–Љ –Р, –љ–µ–Њ–±—Е–Њ–і–Є–Љ—Л–є –і–ї—П —А–∞–Ј–ї–Є—З–љ—Л—Е —Д–µ—А–Љ–µ–љ—В–љ—Л—Е –њ—А–Њ—Ж–µ—Б—Б–Њ–≤ –≤ –Њ—А–≥–∞–љ–Є–Ј–Љ–µ. –Ф–µ–Ї—Б–њ–∞–љ—В–µ–љ–Њ–ї —Г—З–∞—Б—В–≤—Г–µ—В –≤ –Љ–µ—В–∞–±–Њ–ї–Є–Ј–Љ–µ —Г–≥–ї–µ–≤–Њ–і–Њ–≤, –ґ–Є—А–љ—Л—Е –Ї–Є—Б–ї–Њ—В, –≥–ї—О–Ї–Њ–љ–µ–Њ–≥–µ–љ–µ–Ј–µ, –≤ —Б–Є–љ—В–µ–Ј–µ —Б—В–µ—А–Њ–ї–∞, —Б—В–µ—А–Њ–Є–і–љ—Л—Е –≥–Њ—А–Љ–Њ–љ–Њ–≤, –њ–Њ—А—Д–Є—А–Є–љ–∞.
–Р—А–≥–Є–љ–Є–љ –Є —П–±–ї–Њ—З–љ–∞—П –Ї–Є—Б–ї–Њ—В–∞ —Б–љ–Є–ґ–∞—О—В –њ–Њ–≤—Л—И–µ–љ–љ—Л–є —Г—А–Њ–≤–µ–љ—М —Б–≤–Њ–±–Њ–і–љ—Л—Е —Д–µ–љ–Њ–ї–Њ–≤ –≤ –Ї—А–Њ–≤–Є –Ј–∞ —Б—З–µ—В –≤—Л—Б–Њ–Ї–Њ–є —Б–њ–Њ—Б–Њ–±–љ–Њ—Б—В–Є —Б–Њ–µ–і–Є–љ–µ–љ–Є—П —Д–µ–љ–Њ–ї–Њ–≤ —Б –≥–ї—О–Ї—Г—А–Њ–љ–Њ–≤–Њ–є –Ї–Є—Б–ї–Њ—В–Њ–є, —Б—Г–±—Б—В—А–∞—В–Њ–Љ –і–ї—П —Б–Є–љ—В–µ–Ј–∞ –Ї–Њ—В–Њ—А—Л—Е —Б–ї—Г–ґ–∞—В —Н—В–Є –≤–µ—Й–µ—Б—В–≤–∞.
–Я–Њ–Ї–∞–Ј–∞–љ–Є—П–Љ–Є –Ї –љ–∞–Ј–љ–∞—З–µ–љ–Є—О –У–µ–њ–∞—Б–Њ–ї–∞ –Р —П–≤–ї—П—О—В—Б—П:
– –њ–µ—З–µ–љ–Њ—З–љ–∞—П —Н–љ—Ж–µ—Д–∞–ї–Њ–њ–∞—В–Є—П –љ–∞ —Д–Њ–љ–µ –Њ—Б—В—А—Л—Е –Є —Е—А–Њ–љ–Є—З–µ—Б–Ї–Є—Е –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є–є –њ–µ—З–µ–љ–Є;
– —Н–љ—Ж–µ—Д–∞–ї–Њ–њ–∞—В–Є—П –њ–Њ—Б–ї–µ –љ–∞–ї–Њ–ґ–µ–љ–Є—П –њ–Њ—А—В–Њ–—Б–Є—Б—В–µ–Љ–љ—Л—Е –∞–љ–∞—Б—В–Њ–Љ–Њ–Ј–Њ–≤;
– –њ–Њ–≤—Л—И–µ–љ–Є–µ —Г—А–Њ–≤–љ—П –∞–Љ–Љ–Є–∞–Ї–∞ –≤ –Ї—А–Њ–≤–Є –њ–Њ—Б–ї–µ –Љ–∞—Б—Б–Є–≤–љ—Л—Е –њ–Њ–≤—А–µ–ґ–і–µ–љ–Є–є —В–Ї–∞–љ–µ–є (–љ–∞–њ—А–Є–Љ–µ—А, –њ—А–Є –Њ–ґ–Њ–≥–∞—Е).
–Я—А–µ–њ–∞—А–∞—В –≤–≤–Њ–і—П—В –≤/–≤ –Ї–∞–њ–µ–ї—М–љ–Њ –≤ –і–Њ–Ј–µ 500 –Љ–ї —Б–Њ —Б–Ї–Њ—А–Њ—Б—В—М—О 40 –Ї–∞–њ–µ–ї—М/–Љ–Є–љ. –Т–≤–µ–і–µ–љ–Є–µ –њ—А–µ–њ–∞—А–∞—В–∞ –Љ–Њ–ґ–љ–Њ –њ–Њ–≤—В–Њ—А—П—В—М –Ї–∞–ґ–і—Л–µ 12 —З.
–†–µ–ґ–Є–Љ –і–Њ–Ј–Є—А–Њ–≤–∞–љ–Є—П –У–µ–њ–∞—Б–Њ–ї–∞ –Р —Г—Б—В–∞–љ–∞–≤–ї–Є–≤–∞—О—В –Є–љ–і–Є–≤–Є–і—Г–∞–ї—М–љ–Њ (–ґ–µ–ї–∞—В–µ–ї—М–љ–Њ —Б —Г—З–µ—В–Њ–Љ –Є—Б—Е–Њ–і–љ–Њ–є –Ї–Њ–љ—Ж–µ–љ—В—А–∞—Ж–Є–Є –∞–Љ–Љ–Є–∞–Ї–∞ –≤ –Ї—А–Њ–≤–Є) –Є –Ї–Њ—А—А–Є–≥–Є—А—Г—О—В –≤ –Ј–∞–≤–Є—Б–Є–Љ–Њ—Б—В–Є –Њ—В –і–Є–љ–∞–Љ–Є–Ї–Є —Б–Њ—Б—В–Њ—П–љ–Є—П –њ–∞—Ж–Є–µ–љ—В–∞.
–Я—А–Њ—В–Є–≤–Њ–њ–Њ–Ї–∞–Ј–∞–љ–Є—П–Љ–Є –Ї –≤–≤–µ–і–µ–љ–Є—О –њ—А–µ–њ–∞—А–∞—В–∞ —Б–ї—Г–ґ–∞—В:
– –њ–Њ—З–µ—З–љ–∞—П –љ–µ–і–Њ—Б—В–∞—В–Њ—З–љ–Њ—Б—В—М;
– —Е—А–Њ–љ–Є—З–µ—Б–Ї–∞—П —Б–µ—А–і–µ—З–љ–∞—П –љ–µ–і–Њ—Б—В–∞—В–Њ—З–љ–Њ—Б—В—М;
– –≥–µ–Љ–Њ—Д–Є–ї–Є—П;
– —В–µ—А–Љ–Є–љ–∞–ї—М–љ—Л–є –Є–ї–µ–Є—В;
– —П–Ј–≤–µ–љ–љ–∞—П –±–Њ–ї–µ–Ј–љ—М –ґ–µ–ї—Г–і–Ї–∞ –Є –і–≤–µ–љ–∞–і—Ж–∞—В–Є–њ–µ—А—Б—В–љ–Њ–є –Ї–Є—И–Ї–Є –≤ —Д–∞–Ј–µ –Њ–±–Њ—Б—В—А–µ–љ–Є—П;
– –њ–Њ–і–∞–≥—А–∞;
– —Б–∞—Е–∞—А–љ—Л–є –і–Є–∞–±–µ—В;
– —Е–Њ–ї–µ—Ж–Є—Б—В–Є—В;
– –њ–Њ–≤—Л—И–µ–љ–љ–∞—П —З—Г–≤—Б—В–≤–Є—В–µ–ї—М–љ–Њ—Б—В—М –Ї –Ї–Њ–Љ–њ–Њ–љ–µ–љ—В–∞–Љ –њ—А–µ–њ–∞—А–∞—В–∞.
–Ю–њ–Є—Б–∞–љ—Л —Б–ї–µ–і—Г—О—Й–Є–µ –≤–Њ–Ј–Љ–Њ–ґ–љ—Л–µ –њ–Њ–±–Њ—З–љ—Л–µ –і–µ–є—Б—В–≤–Є—П –њ—А–Є –њ—А–Є–Љ–µ–љ–µ–љ–Є–Є –У–µ–њ–∞—Б–Њ–ї–∞ –Р: —В–Њ—И–љ–Њ—В–∞, —А–≤–Њ—В–∞, –∞—А—В–µ—А–Є–∞–ї—М–љ–∞—П –≥–Є–њ–Њ—В–µ–љ–Ј–Є—П, —В–∞—Е–Є–Ї–∞—А–і–Є—П, –≥–Є–њ–µ—А–Ї–∞–ї–Є–µ–Љ–Є—П (–њ—А–Є –≤—Л—А–∞–ґ–µ–љ–љ—Л—Е –љ–∞—А—Г—И–µ–љ–Є—П—Е —Д—Г–љ–Ї—Ж–Є–Є –њ–µ—З–µ–љ–Є –Є –њ–Њ—З–µ–Ї), –≥–Є–њ–Њ—Д–Њ—Б—Д–∞—В–µ–Љ–Є—П (–њ—А–Є —Б–∞—Е–∞—А–љ–Њ–Љ –і–Є–∞–±–µ—В–µ), –њ–Њ–≤—Л—И–µ–љ–љ–∞—П —Г—В–Њ–Љ–ї—П–µ–Љ–Њ—Б—В—М, –њ–Њ—В–ї–Є–≤–Њ—Б—В—М, –≥–Є–њ–µ—А—В–µ—А–Љ–Є—П, —Ж–Є–∞–љ–Њ–Ј.
–Я—А–Є –≤–≤–µ–і–µ–љ–Є–Є –У–µ–њ–∞—Б–Њ–ї–∞ –Р –љ–µ–Њ–±—Е–Њ–і–Є–Љ–Њ –њ–Њ–Љ–љ–Є—В—М –Њ –≤–Њ–Ј–Љ–Њ–ґ–љ–Њ—Б—В–Є –ї–µ–Ї–∞—А—Б—В–≤–µ–љ–љ–Њ–≥–Њ –≤–Ј–∞–Є–Љ–Њ–і–µ–є—Б—В–≤–Є—П –µ–≥–Њ –Ї–Њ–Љ–њ–Њ–љ–µ–љ—В–Њ–≤ —Б –љ–µ–Ї–Њ—В–Њ—А—Л–Љ–Є –і—А—Г–≥–Є–Љ–Є –≤–µ—Й–µ—Б—В–≤–∞–Љ–Є. –Ґ–∞–Ї, —Б–Њ–≤–Љ–µ—Б—В–љ–Њ–µ –њ—А–Є–Љ–µ–љ–µ–љ–Є–µ —В–Є–∞–Ј–Є–і–љ—Л—Е –і–Є—Г—А–µ—В–Є–Ї–Њ–≤, –∞–Љ–Є–љ–Њ—Д–Є–ї–ї–Є–љ–∞ —Б –∞—А–≥–Є–љ–Є–љ–Њ–Љ –Љ–Њ–ґ–µ—В —Б–Њ–њ—А–Њ–≤–Њ–ґ–і–∞—В—М—Б—П –њ–Њ–≤—Л—И–µ–љ–Є–µ–Љ —Б–Њ–і–µ—А–ґ–∞–љ–Є—П –Є–љ—Б—Г–ї–Є–љ–∞ –≤ –Ї—А–Њ–≤–Є; —Б–њ–Є—А–Њ–љ–Њ–ї–∞–Ї—В–Њ–љ–∞ —Б –∞—А–≥–Є–љ–Є–љ–Њ–Љ – –њ–Њ–≤—Л—И–µ–љ–Є–µ–Љ —Г—А–Њ–≤–љ—П –Ї–∞–ї–Є—П –≤ –Ї—А–Њ–≤–Є. –Р—А–≥–Є–љ–Є–љ –љ–µ—Б–Њ–≤–Љ–µ—Б—В–Є–Љ —Б —В–Є–Њ–њ–µ–љ—В–∞–ї–Њ–Љ.
–Ш–Ј–Њ–љ–Є–∞–Ј–Є–і, –њ–µ–љ–Є—Ж–Є–ї–ї–∞–Љ–Є–љ, –њ–µ—А–Њ—А–∞–ї—М–љ—Л–µ –Ї–Њ–љ—В—А–∞—Ж–µ–њ—В–Є–≤—Л —Б–љ–Є–ґ–∞—О—В –Љ–µ—В–∞–±–Њ–ї–Є–Ј–Љ –Є —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В—М –њ–Є—А–Є–і–Њ–Ї—Б–Є–љ–∞.
–Ю–і–љ–Њ–≤—А–µ–Љ–µ–љ–љ–Њ–µ –≤–≤–µ–і–µ–љ–Є–µ —А–Є–±–Њ—Д–ї–∞–≤–Є–љ–∞ –Є —В–µ—В—А–∞—Ж–Є–Ї–ї–Є–љ–Њ–≤, —Н—А–Є—В—А–Њ–Љ–Є—Ж–Є–љ–∞, –ї–Є–љ–Ї–Њ–Љ–Є—Ж–Є–љ–∞ –њ—А–Є–≤–Њ–і–Є—В –Ї —Б—Г—Й–µ—Б—В–≤–µ–љ–љ–Њ–Љ—Г —Б–љ–Є–ґ–µ–љ–Є—О –∞–Ї—В–Є–≤–љ–Њ—Б—В–Є —Н—В–Є—Е –∞–љ—В–Є–±–Є–Њ—В–Є–Ї–Њ–≤. –†–Є–±–Њ—Д–ї–∞–≤–Є–љ –љ–µ—Б–Њ–≤–Љ–µ—Б—В–Є–Љ —Б–Њ —Б—В—А–µ–њ—В–Њ–Љ–Є—Ж–Є–љ–Њ–Љ.
–У–µ–њ–∞—Б–Њ–ї –Р –њ–Њ–Ї–∞–Ј–∞–ї —Б–≤–Њ—О —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В—М –≤ –Ї–Њ–Љ–њ–ї–µ–Ї—Б–љ–Њ–Љ –ї–µ—З–µ–љ–Є–Є –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –ї–∞—В–µ–љ—В–љ–Њ–є –Я–≠ –Є –Я–≠ I –Є II —Б—В–∞–і–Є–Є. –Ч–∞—Б–ї—Г–ґ–Є–≤–∞–µ—В –≤–љ–Є–Љ–∞–љ–Є—П –Є–Ј—Г—З–µ–љ–Є–µ —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В–Є –њ—А–µ–њ–∞—А–∞—В–∞ –њ—А–Є –∞–ї–Ї–Њ–≥–Њ–ї—М–љ–Њ–є –±–Њ–ї–µ–Ј–љ–Є –њ–µ—З–µ–љ–Є, —Г—З–Є—В—Л–≤–∞—П –µ–≥–Њ –∞–љ–∞–±–Њ–ї–Є—З–µ—Б–Ї–Є–є –њ–Њ—В–µ–љ—Ж–Є–∞–ї –Є —Б–Њ–і–µ—А–ґ–∞–љ–Є–µ –≤–Є—В–∞–Љ–Є–љ–Њ–≤ –≥—А—Г–њ–њ—Л –Т.






–Ы–Є—В–µ—А–∞—В—Г—А–∞
1. –С—Г–µ–≤–µ—А–Њ–≤ –Р.–Ю., –Ь–∞–µ–≤—Б–Ї–∞—П –Ь.–Т. –Ґ—А—Г–і–љ—Л–µ –≤–Њ–њ—А–Њ—Б—Л –і–Є–∞–≥–љ–Њ—Б—В–Є–Ї–Є –Є –ї–µ—З–µ–љ–Є—П –њ–µ—З–µ–љ–Њ—З–љ–Њ–є —Н–љ—Ж–µ—Д–∞–ї–Њ–њ–∞—В–Є–Є. // –Ъ–ї–Є–љ–Є—З–µ—Б–Ї–Є–µ –њ–µ—А—Б–њ–µ–Ї—В–Є–≤—Л –≥–∞—Б—В—А–Њ—Н–љ—В–µ—А–Њ–ї–Њ–≥–Є–Є –Є –≥–µ–њ–∞—В–Њ–ї–Њ–≥–Є–Є вДЦ1 – 2005 – —Б—В—А.25–30.
2. –Ш–≤–∞—И–Ї–Є–љ –Т.–Ґ., –Э–∞–і–Є–љ—Б–Ї–∞—П –Ь.–Ѓ., –Ч–Њ–ї–Њ—В–∞—А–µ–≤—Б–Ї–Є–є –Т.–С., —А–µ–і. –С–Њ–ї–µ–Ј–љ–Є –њ–µ—З–µ–љ–Є –Є –ґ–µ–ї—З–µ–≤—Л–≤–Њ–і—П—Й–Є—Е –њ—Г—В–µ–є: –†—Г–Ї–Њ–≤–Њ–і—Б—В–≤–Њ –і–ї—П –≤—А–∞—З–µ–є. –Ь––Т–µ—Б—В–Є, 2002.
3. –Ш–≤–∞—И–Ї–Є–љ –Т.–Ґ., –Э–∞–і–Є–љ—Б–Ї–∞—П –Ь.–Ѓ., –С—Г–µ–≤–µ—А–Њ–≤ –Р.–Ю. –Я–µ—З–µ–љ–Њ—З–љ–∞—П —Н–љ—Ж–µ—Д–∞–ї–Њ–њ–∞—В–Є—П –Є –Љ–µ—В–Њ–і—Л –µ–µ –Љ–µ—В–∞–±–Њ–ї–Є—З–µ—Б–Ї–Њ–є –Ї–Њ—А—А–µ–Ї—Ж–Є–Є. // –С–Њ–ї. –Њ—А–≥. –њ–Є—Й–µ–≤–∞—А. вДЦ 3 – 2001 – —Б—В—А. 25–7.
4. –Ь.–Ѓ.–Э–∞–і–Є–љ—Б–Ї–∞—П. –Я–µ—З–µ–љ–Њ—З–љ–∞—П —Н–љ—Ж–µ—Д–∞–ї–Њ–њ–∞—В–Є—П: –њ–∞—В–Њ–≥–µ–љ–µ—В–Є—З–µ—Б–Ї–Є–µ –њ–Њ–і—Е–Њ–і—Л –Ї –ї–µ—З–µ–љ–Є—О. // Consilium Medicum вДЦ2 – 2004 – —Б—В—А. 12–16.
5. –†–∞–і—З–µ–љ–Ї–Њ –Т.–У., –†–∞–і—З–µ–љ–Ї–Њ –Ю.–Э. –У–µ–њ–∞—Б–Њ–ї –Р –≤ –ї–µ—З–µ–љ–Є–Є —Е—А–Њ–љ–Є—З–µ—Б–Ї–Є—Е –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є–є –њ–µ—З–µ–љ–Є —Б –њ—А–Њ—П–≤–ї–µ–љ–Є—П–Љ–Є —Б–Є—Б—В–µ–Љ–љ–Њ–є —Н–љ—Ж–µ—Д–∞–ї–Њ–њ–∞—В–Є–Є. // –†–Њ—Б—Б–Є–є—Б–Ї–Є–є –ґ—Г—А–љ–∞–ї –≥–∞—Б—В—А–Њ—Н–љ—В–µ—А–Њ–ї–Њ–≥–Є–Є, –≥–µ–њ–∞—В–Њ–ї–Њ–≥–Є–Є, –Ї–Њ–ї–Њ–њ—А–Њ–Ї—В–Њ–ї–Њ–≥–Є–Є вДЦ 2 – 2002 – —Б—В—А. 73–76.
6. –®–µ—А–ї–Њ–Ї –®., –Ф—Г–ї–Є –Ф–ґ. –Ч–∞–±–Њ–ї–µ–≤–∞–љ–Є—П –њ–µ—З–µ–љ–Є –Є –ґ–µ–ї—З–љ—Л—Е –њ—Г—В–µ–є. –Я–µ—А. —Б –∞–љ–≥–ї: –Я–Њ–і —А–µ–і. –Ч.–Ф.–Р–њ—А–Њ—Б–Є–љ–Њ–є, –Э.–Р.–Ь—Г—Е–Є–љ–∞.– –Ь.: –У–µ–Њ—В–∞—А –Ь–µ–і–Є—Ж–Є–љ–∞, 1999.
7. Jeppsson B, Kjallman A, Aslund U et al. Effect of vegan and meat protein diets in mild chronic portal systemic encephalopathy. In: Capocaccia L, Ficher JE, Rossi–Fanelli F. (Eds). Hepatic Encephalopathy in Chronic Liver Failure. Plenum Press, New York. 1984; 359–68.
8. Kuntz E., Kumtz H.–D. Hepatology: pinciples and practice: history, morphology, biochemistry, diagnostics, clinic, therapy. – Springer–Verlag Berlin, Heidelberg, 2002.












