Атопический дерматит (АД) – наследственное, иммуно–нейро–аллергическое, хроническое рецидивирующее воспалительное заболевание кожи, обусловленное атопией, проявляющееся интенсивным зудом, симпатергической реакцией кожи (белым дермографизмом), преимущественно эритематозно–лихеноидными высыпаниями, в сочетании с другими признаками атопии.
В 1923 г. американские аллергологи A.F. Coca и R.A. Cooke, желая описать необычный тип гиперчувствительности к различным веществам окружающей среды, который возникал только у людей и чаще встречался в семьях без явной предшествовавшей сенсибилизации, обратились за помощью к филологу Perry из Колумбийского Университета. Он и предложил ученым использовать термин «атопия», в переводе означающий «не на своем месте» или «странный» [10,16]. Под атопией понимают наследственную предрасположенность к аллергическим реакциям в ответ на определенные антигены. Первым появившимся в литературе «атопиком» был император Октавий Август, у которого был описан крайне выраженный зуд, сезонный ринит и стесненность дыхания. Кроме того, детально описан и семейный анамнез: его внук, император Клавдий, страдал от симптомов риноконъюнктивита, а внучатый племянник, Британик – от аллергии на эпителий лошади [17].
Уже более 80 лет термин «атопия» используется во всем мире, хотя и является порой предметом дискуссий.
Следует отметить, что в отечественной научной медицинской литературе долгое время в качестве синонима АД доминировал термин «диффузный (распространенный) нейродермит». Однако в настоящее время некоторые авторы не признают полной синонимичности этих терминов. Так, Ю.К. Скрипкин (1995) относит АД к группе нейродерматозов, используя термин «нейродермит», что отражает значимую роль неврогенного фактора в патогенезе заболевания [9]. Иногда выявляемый в детском возрасте симптомокомплекс описывается под названием «экссудативный аллергический диатез» или «атопический дерматит раннего детского возраста», а во взрослом возрасте ставится диагноз «диффузный нейродермит».
В зарубежной литературе долгое время не было единого мнения о классификации АД. Об этом говорит богатство исторических синонимов названия данного заболевания (табл. 1). И действительно, европейская школа долгое время придавала главное значение изучению клинических симптомов, тогда как американская школа большое внимание уделяла фундаментальным исследованиям, выявив присутствие реагинов в коже при накожных тестах. Эти две школы объединил дерматолог Marion Baldur Sulzberger, родившийся в Америке и проходивший обучение в Германии вместе с Jadasson и Bloch. По возвращении в США он совместно с Wise предложил термин «атопический дерматит», объединив детскую и взрослую фазы заболевания. Однако и сегодня нет единого названия данного заболевания. Так, немецкие дерматологи объединяют экзему и нейродермит в группу так называемой атопической или эндогенной экземы. Тем не менее в основной массе англоязычных публикаций, при наличии у больного четких признаков атопии и принятых диагностических критериев, используется термин «атопический дерматит» независимо от возраста больного и клинической картины заболевания. Мы придерживаемся такого же мнения.
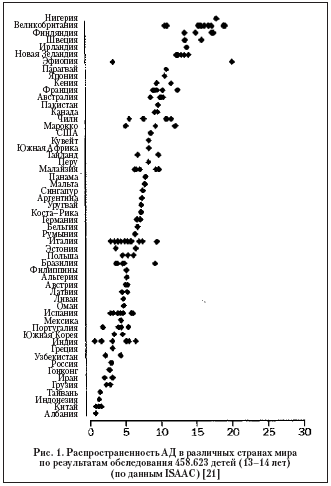
АД является чрезвычайно распространенным и зачастую тяжело протекающим дерматозом. Его частота в структуре кожных заболеваний, по разным данным, составляет от 20 до 40%. Результаты эпидемиологических исследований показывают, что АД чаще встречается у молодых людей, чем у взрослых. Болеют оба пола, несколько чаще женщины. АД возникает у людей всего мира и у всех рас. В течение последних десятилетий распространенность заболевания значительно увеличилась. Например, в Дании общая заболеваемость близнецов в возрасте до 7 лет, рожденных с 1960 по 1964 г. составляла 3%. А у близнецов, рожденных с 1970 по 1974 г., этот показатель уже увеличился до 10%. Эпидемиологические исследования распространенности АД в различных странах мира проиллюстрированы на рисунке 1.
Современные представления о патогенезе АД
Одним из ведущих звеньев в развитии заболевания является генетическая предрасположенность. Существует мнение, что наследуется патологический характер функционирования различных систем организма – нервной, иммунной, пищеварительной и т.д. [3,4,14,15]. Уже с 60–х гг. прошлого столетия было известно, что АД относится к группе так называемых комплексных генетических заболеваний, в основе которых лежит генетическая предрасположенность, но без менделевского типа наследования. То есть, начало заболевания (а также его течение и степень тяжести) обусловлено взаимодействием предрасполагающих генов и триггерных факторов окружающей среды. Таким образом, возникновение и хроническое течение АД обусловливают наследственная предрасположенность, функциональные нарушения нервной системы, влияние неблагоприятных условий окружающей среды, психоэмоциональные расстройства и патология внутренних органов, обменные, нейрогуморальные, нейрососудистые нарушения, аллергическое состояние организма, нерациональное питание, различные интоксикации.
Генетические исследования выявили ряд генов, кодирующих многие патологически или неправильно функционирующие биохимические маркеры, участвующие в патогенезе АД (табл. 2)
Почти 40% пациентов имеют, по крайней мере, одного родственника первой степени, болеющего АД. Принято считать, что 60% и более детей, родители которых болеют АД, также страдают этим заболеванием: АД развивается более чем у 80% детей, если больны оба родителя, и у 50% – когда болен только один родитель. При этом предполагается преимущественное влияние материнской линии. Этот факт можно было бы объяснить воздействием одних и тех же факторов окружающей среды на мать и ребенка, как во время его внутриутробного развития, так и в младенческом возрасте. Но в то же время сами матери могут недооценивать влияние атопических проявлений у отца. Как показано в таблице 3, различий в распространенности АД у детей из семей с АД у отца и у детей из семей с АД у матери обнаружено не было.
Различные факторы окружающей среды, несомненно, являются триггерными факторами АД у предрасположенных людей. Так, контактные раздражители и аллергены (мыла, растворители, одежда из шерсти, механические раздражители, детергенты, консерванты, ароматизаторы) повреждают кожный покров, вызывают раздражение и воспаление, создавая благоприятные условия для дальнейшего воздействия факторов окружающей среды. Среди ингаляционных триггерных факторов чаще всего отмечаются домашняя пыль, пыльца цветущих растений, плесень и перхоть человека и домашних животных. Основным источником аллергенов в домашней пыли является клещ Dermatophagoides pteronyssinus, причем основной аллергенностью обладают фекалии клеща. При контакте с аэроаллергенами развивается эозинофилия в крови, увеличивается уровень IgE, повышается выделение гистамина тучными клетками и увеличивается активность Th2 звена иммунной системы.
Микробные агенты типа Staphylococcus aureus, Pityrosporum ovale, грибов рода Candida могут не только повреждать кожный барьер, но и поддерживать уровень IgE (опосредованные аллергические реакции) посредством выработки так называемых суперантигенов, и таким образом, выступать в качестве триггерных факторов АД.
Пищевая сенсибилизация в патогенезе АД занимает не последнее место. Облегчение тяжести течения АД после исключения из пищевого рациона аллергенных продуктов (чаще всего – яйца, молоко, морепродукты, цитрусовые, грибы, зерновые, арахис, рыба и бобовые) отмечается более чем у 90% детей с тяжелым АД. Известно, что пищевая аллергия протекает в основном с реакциями по I и IV типам, при этом к 1 году жизни значимость этих типов гиперчувствительности обычно уменьшается. Считается, что наличие пищевой аллергии – прогностический показатель тяжелого течения АД. Не менее важная роль в патогенезе АД отводится врожденной, генетически опосредованной ферментопатии пищеварительной системы, которая ведет к формированию выраженной эндогенной интоксикации и утяжеляет течение заболевания [7,14].
Дисфункция иммунной системы имеет большое значение в патогенезе АД. Ведущая роль отводится функциональному иммунодефициту, проявляющемуся снижением супрессорной и киллерной активности Т–системы иммунитета, дисбалансом продукции сывороточных иммуноглобулинов с увеличением уровня IgE, что обусловливает склонность организма к различным аллергическим реакциям и подверженность бактериальной и вирусной инфекциям [6,14].
Обычно действие Th1 и Th2 клеток иммунной системы уравновешено. При АД за счет активации Th2–звена наступает дисбаланс в иммунной системе, приводящий к нарушению регуляции выработки IgE. Этот этап считается ключевым в патогенезе АД. Стоит отметить, однако, что увеличение продукции IgE B–лимфоцитами связано не только со стимулирующим действием цитокинов Th2–системы, но и с отсутствием сдерживающего влияния интерферона–гамма, уровень которого при АД существенно уменьшается.
Психоэмоциональный стресс, несомненно, является фактором, индуцирующим и поддерживающим патологический процесс при АД. Более 50% дерматологов и подавляющее большинство больных убеждены в усугублении АД под действием стресса. При этом влияние стресса на кожный процесс традиционно объясняется на основе психо–эндокрино–иммунологической модели АД. Эта концепция опирается на тесную взаимосвязь центральной нервной системы, эндокринной системы (гипоталамо–гипофизарно–надпочечниковая система – ГГНС), иммунной системы и кожи, которые способны оказывать взаимное регулирующее влияние друг на друга. Так, известно, что в норме стресс вызывает повышение уровня глюкокортикоидов в периферической крови, которые обладают иммуносупрессивным и противовоспалительным действием. Однако у пациентов с АД эта реакция значительно притуплена вследствие снижения реактивности ГГНС [19]. Предполагается, что неспособность секретировать достаточное количество кортикостероидов при стрессе у атопиков повышает риск дисфункции иммунной системы и развития воспалительной реакции в коже.
Другим возможным механизмом трансформации психогенных воздействий в обострение АД является участие невральных путей передачи сигналов между ЦНС и кожей. Это предположение возникло на основе таких клинических симптомов, как симметричность расположения высыпаний, исчезновение высыпаний в зоне денервации кожи [20] и быстрое возникновение эритематозных высыпаний и зуда после стресса, которые могут быть вызваны прямой активацией кожных нервов. И действительно, было показано, что в очагах хронических высыпаний АД плотность нервных волокон повышена, равно как и содержание ряда нейропептидов, обладающих гистамино–подобным действием, например, вазоактивного интестинального пептида. Одновременно в последние годы интерес многих исследователей был сфокусирован на изучении нейротрофинов, например, фактора роста нервов, нейротрофического фактора (НТФ), полученного из мозга (brain–derived neurotrophic factor, BDNF) и нейротрофинов 3, 4 и 5. Оказалось, что будучи синтезирован целым рядом клеток (кератиноциты, тучные клетки, Т–2 лимфоциты, эозинофилы), НТФ способен стимулировать синтез и передачу нейропептидов на периферию, он также является мощным хемоаттрактантом для лейкоцитов. При этом концентрация НТФ в крови сильно коррелирует с активностью заболевания.
Последнее время большое значение в патогенезе АД придается нарушению метаболизма жирных кислот в форменных элементах, плазме крови, жировой ткани. Недостаток определенных жирных кислот приводит к дефициту компонентов простагландинового каскада, обладающих регуляторными функциями (прежде всего в отношении клеточного синтеза IgE).
Таким образом, патогенетические механизмы АД полиморфны и не противоречат, а скорее, дополняют друг друга.
Клинические проявления
Клинические проявления АД разнообразны, однако достаточно типичны и хорошо изучены. Заболевание обычно начинается в раннем детском возрасте, чаще во втором полугодии жизни, может продолжаться долгие годы, характеризуясь ремиссиями, в основном в летний, и рецидивами в весенне–осенний периоды года. Со временем острота заболевания слабеет, и в возрасте 30–40 лет у большинства больных наступает спонтанное излечение. Более позднее существование симптомов атопического дерматита подозрительно на трансформацию заболевания в лимфому кожи.
В течении заболевания четко выделяют три фазы: младенческую (обычно с 7–8–й недели жизни до 3 лет), детскую (с 3 до 7 лет) и взрослую. Клинические проявления их различны. В младенческой и детской фазах чаще наблюдаются очаговые эритематозно–сквамозные высыпания со склонностью к экссудации (везикуляция, мокнутие) на коже лица, ягодицах, конечностях. Во взрослой фазе преобладают зудящие эритематозно–лихеноидные высыпания на сгибательных поверхностях конечностей, на шее с развитием лихенизации (кожа становится утолщенной, грубой на ощупь, кожный рисунок резко выражен). Степень выраженности и распространенности процесса может быть различной – от ограниченных (периоральных) до обширных поражений кожного покрова по типу эритродермий. Непременный признак АД, независимо от фазы течения или клинического варианта – интенсивный зуд, составляющий основу страданий больного, в значительной мере утяжеляющий течение заболевания и снижающий качество жизни [4,8,15].
В соответствии с клинической классификацией К.Н. Суворовой и др., 1989 [10] выделяют 5 форм АД.
Лихеноидная форма характеризуется наличием выраженной лихенификации в области локтевых сгибов и подколенных ямок, лица, шеи, большим количеством полигональных лихеноидных папул, обильными экскориациями, геморрагическими корочками, трещинами, располагающимися на фоне воспалительно–инфильтративных, застойных эритематозных очагов («истинное пруриго Бенье»).
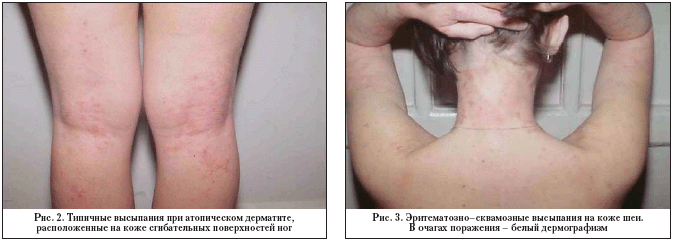
Эритематозно–сквамозная с лихенификацией форма в большинстве наблюдений может характеризоваться как распространенным, так и локализованным процессом; инфильтративные эритематозные очаги, обильно покрытые беловатыми отрубевидными чешуйками, расчесами, располагаются на коже сгибательных поверхностей конечностей (рис. 2), лица, шеи (рис. 3), туловища, больше – верхней его трети. Отмечается обильное высыпание фолликулярных папул, группирующихся или располагающихся рассеянно, многие из которых – с экскориированной или шелушащейся поверхностью. Проявления лихенизации выражены умеренно. В периоды обострения эруптивные элементы быстро принимают отечный характер, а при затихании процесса на месте прежних высыпаний длительно сохраняются поствоспалительные пигментированные пятна.
Пруригинозная форма АД – отмечается чаще при распространенных поражениях кожи, помимо обширных эритематозно–сквамозных очагов, многочисленных рассеянных экскориаций, экскориированных фолликулярных папул и очагов лихенификации в сгибах конечностей, проявляется наличием крупных, стойких, полушаровидных папул, сопровождаемых сильным зудом (преимущественно на коже рук и ног).
При везикуло–крустозной форме АД отмечаются диссеминированные высыпания, с преобладанием экссудативных эритематозно–инфильтративных очагов с трещинами, экскориациями, немногочисленными папуло–везикулами и чешуйко–корками, при удалении которых обнажаются точечные мокнущие эрозии. При этом на коже туловища и конечностей могут располагаться типичные эритематозно–сквамозные, с лихенификацией очаги, отдельные фолликулярные папулы.
На лице у многих больных АД могут отмечаться в той или иной степени выраженная эритема, шелушение. Веки отечны, утолщены, выражены периорбитальная складчатость и гиперпигментация кожи. Губы сухие, растрескивающиеся (атопический хейлит), в углах рта часты заеды. Характерен белый дермографизм, особенно выраженный в периоды обострения болезни. У отдельных больных отмечаются другие проявления атопии (бронхиальная астма, поллиноз, крапивница и др.). Субъективно высыпания всегда сопровождаются зудом, который может предшествовать высыпным элементам. У части больных зуд принимает мучительный характер, приводя к многочисленным, иногда «биопсирующим» расчесам, и к появлению симптома «полированных ногтей».
Диагноз
Диагноз АД основывается на комплексе диагностических признаков АД, который получил название критериев Hanifin а. Rajka, 1980 [13] (табл. 4). Они базируются прежде всего на частоте встречаемости, наличии или отсутствии того или иного клинического симптома. Диагноз АД требует наличия, по крайней мере, трех из четырех главных критериев и трех малых критериев.
Объективная оценка
Объективная оценка степени тяжести и распространенности кожного процесса и выраженности зуда при АД имеет чрезвычайно важное научно–практическое значение. С этой целью группой исследователей Европейского центра по изучению атопического дерматита была разработана унифицированная шкала симптомов (SCORAD), представляющая собой многопараметровую балльную оценку степени тяжести АД, которая может быть использована в качестве наиболее объективного («золотого») стандарта при научных исследованиях и в клинической практике [12].
Лабораторное подтверждение
Лабораторное подтверждение диагноза АД весьма неспецифично, но может включать прежде всего определение уровня IgE сыворотки и исследование количества эозинофилов в крови. Необходимо отметить, что повышенное содержание IgE у больных АД сохраняется и в периоды ремиссий.
Заболевания, редко возникающие при атопическом дерматите
Интересно, что инсулин–зависимый диабет, псориаз, ревматоидный артрит и меланоцитарные невусы редко возникают у пациентов с АД. Однако работы, посвященные изучению причин такой негативной ассоциации данных заболеваний, пока немногочисленны.
Дифференциальный диагноз
Дифференциальный диагноз АД сводится к разграничению с такими зудящими заболеваниями кожи, как чесотка, экзема, себорейный дерматит, контактный дерматит, лимфомы кожи и др.
Осложнения
Осложнения АД в основном представлены вторичными кожными инфекциями. Наиболее часто отмечается импетигинизация очагов; в случае стафилококковой природы отмечаются распространенные фолликулиты. Особой формой вторичной инфекции при АД является герпетиформная экзема Капоши, обусловленная вирусом простого герпеса.
Лечение АД
Для лечения АД в современной дерматологии используется целый ряд разнообразных терапевтических методов. Прежде всего рекомендуется гипоаллергенная диета (с исключением острых, излишне соленых, жареных и копченых блюд, экзотических фруктов, сладостей, шипучих напитков и др.), соблюдение рационального режима. Также проводится коррекция нарушений функций пищеварительного тракта (ферментотерапия, устранение дисбактериоза и др.), санация очагов хронической инфекции. Назначают антигистаминные препараты, психотропные – в зависимости от тяжести и сложности сопутствующих психосоматических расстройств) и седативные средства: препараты валерианы, пустырника [1,4,7,15].
В тяжелых случаях, при развитии эритродермии возможно применение системных кортикостероидов (наиболее удобен бетаметазон – 1–2 мл не чаще 1 раза в неделю, кратковременными курсами); хороший эффект наблюдается при сорбционно–дезинтоксикационной терапии (инфузия раствора гемодеза, обменный плазмаферез и др.). В последнее время для лечения тяжелых, торпидных форм атопического дерматита применяют циклоспорин А, в дозе 3–5 мг/кг в сутки [5,15]. При осложнении пиодермией назначают антибиотики (эритромицин до 1,5 г в сутки).
Наружно назначают смягчающие и охлаждающие кремы (крем Унны, висмутовый крем и др.), кератопластические мази (с ихтиолом, нафталаном, дегтем и пр.). Первостепенное значение имеют топические кортикостероидные средства («Локоид», «Адвантан», «Афлодерм», «Элоком», «Целестодерм В», «Целестодерм В с гарамицином», «Тридерм» и др.), с рациональным подбором той или иной лекарственной формы (мази, крема, лосьона, эмульсии и др.) [2]. В последнее время получены обнадеживающие результаты при применении принципиально новых наружных иммуносупресивных нестероидных средств – такролимуса и пимекролимуса [11].
Из физиотерапевтических методов применяют УФ – А и В облучение, рефлексотерапию, гипербарическую оксигенацию, магнитотерапию и другие процедуры. При лечении АД, особенно тяжелых форм, очень эффективна курорто– и климатотерапия в условиях сухого морского климата.
Профилактика
Профилактика включает диетические рекомендации при вскармливании детей, лечение сопутствующих заболеваний, рациональный режим труда и отдыха, динамическое клиническое наблюдение и рациональную профессиональную ориентацию больных.
Прогноз
Прогноз при АД в каждом случае индивидуален, однако в целом благоприятный. Обычно заболевание угасает или в ранние сроки (3–5 лет), или существует на протяжении 3–4 десятилетий жизни пациента, а затем постепенно прекращает свое развитие, вплоть до полного регресса симптоматики.



Литература
1. Иванов О.Л., Мареева Е.Б., Кривда А.Ю. Современный антигистаминный препарат зиртек в терапии аллергодерматозов // Росс. журн. кожн. вен. бол., 1999, № 5, с. 23–26.
2. Иванов О.Л., Самгин М.А. Адвантан – препарат выбора для наружной терапии аллергодерматозов у детей // Росс. журн. кожн. вен. бол., 2000, № 3, с. 28–30.
3. Короткий Н.Г., Шарова Н.М., Тихомиров А.А. Новые возможности терапии атопического дерматита у детей в зависимости от его клинико–патогенетических вариантов // Росс. журн. кожн. вен. бол., 2000, № 6, стр. 35–38.
4. Кочергин Н.Г. Атопический дерматит // Росс. журн. кожн. вен. бол., 1998, № 5, с. 59–64.
5. Кочергин Н.Г. Опыт применения неорала при атопическом дерматите у детей // Росс. журн. кожн. вен. бол., 1998, № 2, с. 35–37
6. Кунгуров Н.В. Иммунологические аспекты атопического дерматита // Вестн. дерматол. венерол., 1999, № 3, с. 14–17.
7. Сергеев Ю.В. (ред.) Атопический дерматит (руководство для врачей). – М.: Медицина для всех, 2002. – 183 с.
8. Сергеев Ю.В., Константинова Н.А., Грабовская О.В., Кортукова В.М. Атопический дерматит // Вестн. дерматол. венерол., 1990, № 1, с. 8–11.
9. Скрипкин Ю.К. (ред.) Кожные и венерические болезни (руководство для врачей). – М.: Медицина, 1995. – Т. II, стр. 52–68.
10. Суворова К.Н., Антоньев А.А., Довжанский С.И., Писаренко М.Ф. Атопический дерматит. – Изд–во Сарат. Ун–та, 1989. – 168 с.
11. Bieber T. Topical tacrolimus (FK 506): a new milestone in the management of atopic dermatitis. J Allergy Clin Immunol 1998;102:555–7.
12. European Task Force on Atopic Dermatitis. Severity scoring of atopic dermatitis: the SCORAD index. Dermatology 1993;186:23–31.
13. Hanifin JM, Rajka G. Diagnostic features of atopic dermatitis. Acta Derm Venereol Suppl (Stockh) 1980; 92:44–7.
14. Leung DYM, Rhodes AR, Geha RS, Schneider L, Ring J. Atopic dermatitis. In: Fitzpatrick TB, Eisen AZ, Wolff K, Freeberg IM, Austen KF, editors. Dermatology in general medicine. New York: McGraw–Hill; 1993:1543–64.
15. Rothe MJ, Grant–Kels JM Atopic dermatitis: An update. – Journal of the American Academy of Dermatology, Volume 35, Number 1, July 1996, p. 1–16.
16. Coca A.F., Cooke R.A. On classification of the phenomena of hypersensitiveness. J immunol 1923, 10:445.
17. Ring J., Erstbeschreibung einer “atopischen Familienanamnese” im Julisch–Claudischen Keiserhaus: Augustus, Claudius, Britannicus. Hautarzt 36:47–478.
18. Wallach D., Taieb A., Tilles G. Historie de la dermatite atopique. 2004, Masson, Paris.
19. Buske–Kirschbaum A., Jobst S., Wustmans A. Attenuated free cortisol response to psychological stress in children with atopic dermatitis. Psychosom Med 1997:59:419–426.
20. Amon U., Wolff H.H. Healing of chronic atopic dermatitis lesions in skin areas of paraplegia after trauma. J Dermatol 21(12):982–983.
21. ISAAC S.C. (1998) Worldwide wariation in prevalence of symptoms of asthma, allergic rhinoconjunctivitis, and atopic eczema: ISAAC (The international Study of Asthma and Allergies in Childhood). Lancet 351:1225–1232.
22. Ring J., Przybilla B., Ruzicka T. Handbook of Atopic eczema. Berlin, Springer 2006.












