–Т —Б—В–∞—В—М–µ –Њ–њ–Є—Б–∞–љ–∞ –Њ–≥—А–∞–љ–Є—З–µ–љ–љ–∞—П —Б–Ї–ї–µ—А–Њ–і–µ—А–Љ–Є—П —Г –і–µ—В–µ–є: —Н—В–Є–Њ–ї–Њ–≥–Є—П, –њ–∞—В–Њ–≥–µ–љ–µ–Ј, –Ї–ї–∞—Б—Б–Є—Д–Є–Ї–∞—Ж–Є—П –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П, –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є–µ —Д–Њ—А–Љ—Л –Є –њ—А–Њ—П–≤–ї–µ–љ–Є—П. –Ф–∞–љ—Л –њ—А–∞–Ї—В–Є—З–µ—Б–Ї–Є–µ —А–µ–Ї–Њ–Љ–µ–љ–і–∞—Ж–Є–Є –њ–Њ –і–Є–∞–≥–љ–Њ—Б—В–Є—З–µ—Б–Ї–Є–Љ –Є –Љ–µ–і–Є–Ї–∞–Љ–µ–љ—В–Њ–Ј–љ—Л–Љ –њ–Њ–і—Е–Њ–і–∞–Љ.
Key words: Scleroderma - etiology - pathogenesis - autoimmune disorders - classification - clinical forms - lichen sclerosus et atrophicus - penicillin - lidase - biostimulants - pyrogenic agents - vasoprotectors.
The paper outlines localized scleroderma in children, its etiology, pathogenesis, classification, clinical forms, and manifestations. Practical guidelines for diagnostic and medical approaches are given.
–Т. –Э. –У—А–µ–±–µ–љ—О–Ї, –њ—А–Њ—Д., –і–Њ–Ї—В–Њ—А –Љ–µ–і. –љ–∞—Г–Ї, –Ј–∞–≤.–Њ—В–і–µ–ї–Њ–Љ –і–µ—В—Б–Ї–Њ–є –і–µ—А–Љ–∞—В–Њ–ї–Њ–≥–Є–Є –¶–Э–Ш–Ъ–Т–Ш –Ь–Є–љ–Ј–і—А–∞–≤–∞ –†–§
Prof. V.N.Grebenyuk, MD, Head, Department of Pediatric Dermatology, Central Research Dermatovenereologic Institute, Ministry of Health of the Russian Federation
–Т–≤–µ–і–µ–љ–Є–µ
–Ю–≥—А–∞–љ–Є—З–µ–љ–љ–∞—П —Б–Ї–ї–µ—А–Њ–і–µ—А–Љ–Є—П (–Ю–°) —Г –і–µ—В–µ–є – —Б–µ—А—М–µ–Ј–љ–∞—П —Б–Њ–≤—А–µ–Љ–µ–љ–љ–∞—П –Љ–µ–і–Є—Ж–Є–љ—Б–Ї–∞—П –Є —Б–Њ—Ж–Є–∞–ї—М–љ–∞—П –њ—А–Њ–±–ї–µ–Љ–∞. –Т –Њ—В–ї–Є—З–Є–µ –Њ—В —Б–Є—Б—В–µ–Љ–љ–Њ–є —Б–Ї–ї–µ—А–Њ–і–µ—А–Љ–Є–Є (–°–°–Ф), –њ—А–Є –Ї–Њ—В–Њ—А–Њ–є –≤ –њ–∞—В–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є–є –њ—А–Њ—Ж–µ—Б—Б –≤–Њ–≤–ї–µ–Ї–∞—О—В—Б—П —А–∞–Ј–ї–Є—З–љ—Л–µ –Њ—А–≥–∞–љ—Л, –Ю–° "–Њ–≥—А–∞–љ–Є—З–Є–≤–∞–µ—В—Б—П" –њ–Њ—А–∞–ґ–µ–љ–Є–µ–Љ —В–Њ–ї—М–Ї–Њ –Ї–Њ–ґ–Є. –Т —В–Њ –ґ–µ –≤—А–µ–Љ—П –љ–µ—А–µ–і–Ї–Њ –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є–µ –њ—А–Є–Њ–±—А–µ—В–∞–µ—В —Б–Є—Б—В–µ–Љ–љ—Л–є —Е–∞—А–∞–Ї—В–µ—А, —В.–µ. —Б—В–∞–љ–Њ–≤–Є—В—Б—П –°–°–Ф. –Ю–і–љ–∞–Ї–Њ –Љ–љ–µ–љ–Є–µ, —З—В–Њ —Н—В–Є –і–≤–∞ –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П –њ–Њ —Б—Г—В–Є –њ—А–µ–і—Б—В–∞–≤–ї—П—О—В –µ–і–Є–љ—Л–є –њ–∞—В–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є–є –њ—А–Њ—Ж–µ—Б—Б, —А–∞–Ј–і–µ–ї—П—О—В –љ–µ –≤—Б–µ –Є—Б—Б–ї–µ–і–Њ–≤–∞—В–µ–ї–Є. –Э–µ–Ї–Њ—В–Њ—А—Л–µ –∞–≤—В–Њ—А—Л –њ–Њ–ї–∞–≥–∞—О—В, —З—В–Њ –Ю–° –Є –°–°–Ф –љ–µ —В–Њ–ґ–і–µ—Б—В–≤–µ–љ–љ—Л, –Є —А–∞–Ј–≥—А–∞–љ–Є—З–Є–≤–∞—О—В –Є—Е –њ–Њ –њ–∞—В–Њ–≥–µ–љ–µ–Ј—Г, –Ї–ї–Є–љ–Є–Ї–µ –Є —В–µ—З–µ–љ–Є—О. –Ш –≤ —В–∞–Ї–Њ–Љ —Б–ї—Г—З–∞–µ –°–°–Ф –Њ—В–љ–Њ—Б—П—В –Ї –і–Є—Д—Д—Г–Ј–љ—Л–Љ –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П–Љ —Б–Њ–µ–і–Є–љ–Є—В–µ–ї—М–љ–Њ–є —В–Ї–∞–љ–Є (–Ф–Ч–°–Ґ), –∞ –Ю–° —В–∞–Ї–Њ–≤—Л–Љ –љ–µ —П–≤–ї—П–µ—В—Б—П.
–Ъ–∞–Ї –Є–Ј–≤–µ—Б—В–љ–Њ, –Ф–Ч–°–Ґ –≤–Ї–ї—О—З–∞—О—В –°–°–Ф, —Б–Є—Б—В–µ–Љ–љ—Г—О –Ї—А–∞—Б–љ—Г—О –≤–Њ–ї—З–∞–љ–Ї—Г (–°–Ъ–Т), –і–µ—А–Љ–∞—В–Њ–Љ–Є–Њ–Ј–Є—В, —Г–Ј–µ–ї–Ї–Њ–≤—Л–є –њ–µ—А–Є–∞—А—В–µ—А–Є–Є—В –Є —А–µ–≤–Љ–∞—В–Њ–Є–і–љ—Л–є –∞—А—В—А–Є—В – –≥—А–Њ–Ј–љ—Л–µ –±–Њ–ї–µ–Ј–љ–Є, —В—А–µ–±—Г—О—Й–Є–µ –Њ–њ—А–µ–і–µ–ї–µ–љ–љ–Њ–є —Б—В—А–∞—В–µ–≥–Є–Є –Є —В–∞–Ї—В–Є–Ї–Є –≤–µ–і–µ–љ–Є—П –±–Њ–ї—М–љ—Л—Е, –њ—А–Њ–≤–µ–і–µ–љ–Є—П –Є–љ—В–µ–љ—Б–Є–≤–љ–Њ–≥–Њ –ї–µ—З–µ–±–љ–Њ-–њ—А–Њ—Д–Є–ї–∞–Ї—В–Є—З–µ—Б–Ї–Њ–≥–Њ –Ї–Њ–Љ–њ–ї–µ–Ї—Б–∞. –°–°–Ф – –≤—В–Њ—А–Њ–µ –њ–Њ —З–∞—Б—В–Њ—В–µ –≤—Б—В—А–µ—З–∞–µ–Љ–Њ—Б—В–Є –њ–Њ—Б–ї–µ –°–Ъ–Т –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є–µ –Є–Ј –≥—А—Г–њ–њ—Л –Ф–Ч–°–Ґ (–Њ—В 32 –і–Њ 45 —Б–ї—Г—З–∞–µ–≤ –љ–∞ 100 —В—Л—Б. –љ–∞—Б–µ–ї–µ–љ–Є—П) [1]. –°–ї–µ–і—Г–µ—В –µ—Й–µ —А–∞–Ј –њ–Њ–і—З–µ—А–Ї–љ—Г—В—М, —З—В–Њ –љ–µ–ї—М–Ј—П –Є–≥–љ–Њ—А–Є—А–Њ–≤–∞—В—М –≤–Њ–Ј–Љ–Њ–ґ–љ–Њ—Б—В—М –њ–µ—А–µ—Е–Њ–і–∞ –Ю–° –≤ –°–°–Ф.
–Т –і–µ—В—Б–Ї–Њ–Љ –≤–Њ–Ј—А–∞—Б—В–µ –і–Њ–Љ–Є–љ–Є—А—Г–µ—В –Ю–°. –Ю–љ–∞ –≤—Б—В—А–µ—З–∞–µ—В—Б—П —Г –і–µ—В–µ–є –±–Њ–ї–µ–µ —З–µ–Љ –≤ 10 —А–∞–Ј —З–∞—Й–µ –°–Ъ–Т. –Ф–µ–≤–Њ—З–Ї–Є –±–Њ–ї–µ—О—В —З–∞—Й–µ –Љ–∞–ї—М—З–Є–Ї–Њ–≤ –±–Њ–ї–µ–µ —З–µ–Љ –≤ 3 —А–∞–Ј–∞.
–Ч–∞–±–Њ–ї–µ–≤–∞–љ–Є–µ –Љ–Њ–ґ–µ—В –≤–Њ–Ј–љ–Є–Ї–∞—В—М –≤ –ї—О–±–Њ–Љ –≤–Њ–Ј—А–∞—Б—В–µ, –і–∞–ґ–µ —Г –љ–Њ–≤–Њ—А–Њ–ґ–і–µ–љ–љ—Л—Е, –љ–∞—З–Є–љ–∞—П—Б—М –Њ–±—Л—З–љ–Њ –Є—Б–њ–Њ–і–≤–Њ–ї—М, –±–µ–Ј –Ї–∞–Ї–Є—Е-–ї–Є–±–Њ —Б—Г–±—К–µ–Ї—В–Є–≤–љ—Л—Е –Њ—Й—Г—Й–µ–љ–Є–є –Є –љ–∞—А—Г—И–µ–љ–Є—П –Њ–±—Й–µ–≥–Њ —Б–Њ—Б—В–Њ—П–љ–Є—П. –Т —Б–≤—П–Ј–Є —Б —В–µ–љ–і–µ–љ—Ж–Є–µ–є —А–∞—Б—В—Г—Й–µ–≥–Њ –Њ—А–≥–∞–љ–Є–Ј–Љ–∞ –Ї —А–∞—Б–њ—А–Њ—Б—В—А–∞–љ–µ–љ–љ–Њ–є –њ–∞—В–Њ–ї–Њ–≥–Є–Є, –Ї –≤—Л—А–∞–ґ–µ–љ–љ—Л–Љ —Н–Ї—Б—Б—Г–і–∞—В–Є–≤–љ—Л–Љ –Є —Б–Њ—Б—Г–і–Є—Б—В—Л–Љ —А–µ–∞–Ї—Ж–Є—П–Љ —Г –і–µ—В–µ–є —Н—В–Њ –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є–µ —З–∞—Б—В–Њ –Њ–±–љ–∞—А—Г–ґ–Є–≤–∞–µ—В —Б–Ї–ї–Њ–љ–љ–Њ—Б—В—М –Ї –њ—А–Њ–≥—А–µ—Б—Б–Є—А—Г—О—Й–µ–Љ—Г —В–µ—З–µ–љ–Є—О, –Њ–±—И–Є—А–љ–Њ–Љ—Г –њ–Њ—А–∞–ґ–µ–љ–Є—О, —Е–Њ—В—П –≤ —А–∞–љ–љ–Є–µ —Б—А–Њ–Ї–Є –Љ–Њ–ґ–µ—В –њ—А–Њ—П–≤–ї—П—В—М—Б—П –µ–і–Є–љ–Є—З–љ—Л–Љ–Є –Њ—З–∞–≥–∞–Љ–Є. –Т –њ–Њ—Б–ї–µ–і–љ–µ–µ –і–µ—Б—П—В–Є–ї–µ—В–Є–µ –≤—Б—В—А–µ—З–∞–µ–Љ–Њ—Б—В—М —Н—В–Њ–є –њ–∞—В–Њ–ї–Њ–≥–Є–Є —Г –і–µ—В–µ–є –≤–Њ–Ј—А–Њ—Б–ї–∞. –Ю–° —Е–∞—А–∞–Ї—В–µ—А–Є–Ј—Г–µ—В—Б—П –њ—А–µ–Є–Љ—Г—Й–µ—Б—В–≤–µ–љ–љ–Њ –ї–Њ–Ї–∞–ї–Є–Ј–Њ–≤–∞–љ–љ—Л–Љ–Є –Њ—З–∞–≥–∞–Љ–Є —Е—А–Њ–љ–Є—З–µ—Б–Ї–Њ–≥–Њ –≤–Њ—Б–њ–∞–ї–µ–љ–Є—П –Є —Д–Є–±—А–Њ–Ј–љ–Њ-–∞—В—А–Њ—Д–Є—З–µ—Б–Ї–Њ–≥–Њ –њ–Њ—А–∞–ґ–µ–љ–Є—П –Ї–Њ–ґ–Є –Є —Б–ї–Є–Ј–Є—Б—В—Л—Е –Њ–±–Њ–ї–Њ—З–µ–Ї.
–Я–µ—А–≤–Њ–µ –Њ–њ–Є—Б–∞–љ–Є–µ –њ–Њ—Е–Њ–ґ–µ–≥–Њ –љ–∞ —Б–Ї–ї–µ—А–Њ–і–µ—А–Љ–Є—О –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П, –Є–Ј–≤–µ—Б—В–љ–Њ–≥–Њ –µ—Й–µ –і—А–µ–≤–љ–µ–≥—А–µ—З–µ—Б–Ї–Є–Љ –Є –і—А–µ–≤–љ–µ—А–Є–Љ—Б–Ї–Є–Љ –≤—А–∞—З–∞–Љ, –њ—А–Є–љ–∞–і–ї–µ–ґ–Є—В Zacucutus Zusitanus (1634). Alibert (1817) –Ј–љ–∞—З–Є—В–µ–ї—М–љ–Њ –і–Њ–њ–Њ–ї–љ–Є–ї —Е–∞—А–∞–Ї—В–µ—А–Є—Б—В–Є–Ї—Г —Н—В–Њ–є –±–Њ–ї–µ–Ј–љ–Є, –і–ї—П –Њ–±–Њ–Ј–љ–∞—З–µ–љ–Є—П –Ї–Њ—В–Њ—А–Њ–є –Х. Gintrac [2] –њ—А–µ–і–ї–Њ–ґ–Є–ї —В–µ—А–Љ–Є–љ "—Б–Ї–ї–µ—А–Њ–і–µ—А–Љ–Є—П".
–≠—В–Є–Њ–ї–Њ–≥–Є—П –Є –њ–∞—В–Њ–≥–µ–љ–µ–Ј
–≠—В–Є–Њ–ї–Њ–≥–Є—П —Б–Ї–ї–µ—А–Њ–і–µ—А–Љ–Є–Є –Њ–Ї–Њ–љ—З–∞—В–µ–ї—М–љ–Њ –µ—Й–µ –љ–µ —Г—Б—В–∞–љ–Њ–≤–ї–µ–љ–∞. –У–Є–њ–Њ—В–µ–Ј–∞ –Є–љ—Д–µ–Ї—Ж–Є–Њ–љ–љ–Њ–≥–Њ –≥–µ–љ–µ–Ј–∞ –Є–љ—В–µ—А–µ—Б–љ–∞ –≤ –Є—Б—В–Њ—А–Є—З–µ—Б–Ї–Њ–Љ –∞—Б–њ–µ–Ї—В–µ, –Њ–і–љ–∞–Ї–Њ —А–Њ–ї—М –њ–∞–ї–Њ—З–Ї–Є –Ъ–Њ—Е–∞, –±–ї–µ–і–љ–Њ–є —Б–њ–Є—А–Њ—Е–µ—В—Л, –њ–Є–Њ–Ї–Њ–Ї–Ї–Њ–≤ –Ї–∞–Ї –≤–Њ–Ј–Љ–Њ–ґ–љ–Њ–є –њ–µ—А–≤–Њ–њ—А–Є—З–Є–љ—Л —Б–Ї–ї–µ—А–Њ–і–µ—А–Љ–Є–Є –љ–µ –њ–Њ–і—В–≤–µ—А–і–Є–ї–∞—Б—М. –Э–µ —Г–±–µ–і–Є—В–µ–ї—М–љ–Њ —В–∞–Ї–ґ–µ –Ј–љ–∞—З–µ–љ–Є–µ –Є Borrelia burgdorferi –≤ —А–∞–Ј–≤–Є—В–Є–Є —Н—В–Њ–≥–Њ –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П [3]. –•–Њ—В—П –≤ –Ї–ї–µ—В–Ї–∞—Е —А–∞–Ј–ї–Є—З–љ—Л—Е —В–Ї–∞–љ–µ–є —Г –±–Њ–ї—М–љ—Л—Е —Б–Ї–ї–µ—А–Њ–і–µ—А–Љ–Є–µ–є –Њ–±–љ–∞—А—Г–ґ–Є–≤–∞–ї–Є —Б—В—А—Г–Ї—В—Г—А—Л, —П–≤–ї—П—О—Й–Є–µ—Б—П —А–µ–Ј—Г–ї—М—В–∞—В–Њ–Љ –Њ–њ–Њ—Б—А–µ–і–Њ–≤–∞–љ–љ–Њ–≥–Њ –≤–ї–Є—П–љ–Є—П –≤–Є—А—Г—Б–љ–Њ–є –Є–љ—Д–µ–Ї—Ж–Є–Є, –≤–Є—А—Г—Б –љ–µ –±—Л–ї –≤—Л–і–µ–ї–µ–љ.
–Э–µ –Є—Б–Ї–ї—О—З–∞–µ—В—Б—П —А–Њ–ї—М –≥–µ–љ–µ—В–Є—З–µ—Б–Ї–Є—Е —Д–∞–Ї—В–Њ—А–Њ–≤.
–Я—А–µ–і–њ–Њ–ї–∞–≥–∞–µ—В—Б—П –Љ—Г–ї—М—В–Є—Д–∞–Ї—В–Њ—А–Є–∞–ї—М–љ–Њ–µ –љ–∞—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ [4].
–Я–∞—В–Њ–≥–µ–љ–µ–Ј —Б–Ї–ї–µ—А–Њ–і–µ—А–Љ–Є–Є —Б–≤—П–Ј—Л–≤–∞—О—В –≥–ї–∞–≤–љ—Л–Љ –Њ–±—А–∞–Ј–Њ–Љ —Б –≥–Є–њ–Њ—В–µ–Ј–∞–Љ–Є –Њ–±–Љ–µ–љ–љ—Л—Е, —Б–Њ—Б—Г–і–Є—Б—В—Л—Е –Є –Є–Љ–Љ—Г–љ–љ—Л—Е –љ–∞—А—Г—И–µ–љ–Є–є.
–Э–∞ –≤–Њ–Ј–љ–Є–Ї–љ–Њ–≤–µ–љ–Є–µ —Б–Ї–ї–µ—А–Њ–і–µ—А–Љ–Є–Є –≤–ї–Є—П—О—В —В–∞–Ї–ґ–µ –љ–∞—А—Г—И–µ–љ–Є—П –≤–µ–≥–µ—В–∞—В–Є–≤–љ–Њ–є –љ–µ—А–≤–љ–Њ–є —Б–Є—Б—В–µ–Љ—Л –Є –љ–µ–є—А–Њ—Н–љ–і–Њ–Ї—А–Є–љ–љ—Л–µ —А–∞—Б—Б—В—А–Њ–є—Б—В–≤–∞ [5, 6].
–Э–∞—А—Г—И–µ–љ–Є—П –Љ–µ—В–∞–±–Њ–ї–Є–Ј–Љ–∞ —Б–Њ–µ–і–Є–љ–Є—В–µ–ї—М–љ–Њ–є —В–Ї–∞–љ–Є –њ—А–Њ—П–≤–ї—П—О—В—Б—П –≥–Є–њ–µ—А–њ—А–Њ–і—Г–Ї—Ж–Є–µ–є –Ї–Њ–ї–ї–∞–≥–µ–љ–∞ —Д–Є–±—А–Њ–±–ї–∞—Б—В–∞–Љ–Є, –њ–Њ–≤—Л—И–µ–љ–љ—Л–Љ —Б–Њ–і–µ—А–ґ–∞–љ–Є–µ–Љ –Њ–Ї—Б–Є–њ—А–Њ–ї–Є–љ–∞ –≤ –њ–ї–∞–Ј–Љ–µ –Ї—А–Њ–≤–Є –Є –Љ–Њ—З–µ, –љ–∞—А—Г—И–µ–љ–Є–µ–Љ —Б–Њ–Њ—В–љ–Њ—И–µ–љ–Є—П —А–∞—Б—В–≤–Њ—А–Є–Љ–Њ–є –Є –љ–µ—А–∞—Б—В–≤–Њ—А–Є–Љ–Њ–є —Д—А–∞–Ї—Ж–Є–є –Ї–Њ–ї–ї–∞–≥–µ–љ–∞ –Є –љ–∞–Ї–Њ–њ–ї–µ–љ–Є–µ–Љ –≤ –Ї–Њ–ґ–µ –Љ–µ–і–Є [3,4].
–Ю—Б–Њ–±–Њ–µ –њ–∞—В–Њ–≥–µ–љ–µ—В–Є—З–µ—Б–Ї–Њ–µ –Ј–љ–∞—З–µ–љ–Є–µ –њ—А–Є —Б–Ї–ї–µ—А–Њ–і–µ—А–Љ–Є–Є –њ—А–Є–і–∞—О—В –Є–Ј–Љ–µ–љ–µ–љ–Є—П–Љ –Љ–Є–Ї—А–Њ—Ж–Є—А–Ї—Г–ї—П—Ж–Є–Є. –Т –Є—Е –Њ—Б–љ–Њ–≤–µ –ї–µ–ґ–∞—В –њ–Њ—А–∞–ґ–µ–љ–Є—П –њ—А–µ–Є–Љ—Г—Й–µ—Б—В–≤–µ–љ–љ–Њ —Б—В–µ–љ–Ї–Є –Љ–µ–ї–Ї–Є—Е –∞—А—В–µ—А–Є–є, –∞—А—В–µ—А–Є–Њ–ї –Є –Ї–∞–њ–Є–ї–ї—П—А–Њ–≤, –њ—А–Њ–ї–Є—Д–µ—А–∞—Ж–Є—П –Є –і–µ—Б—В—А—Г–Ї—Ж–Є—П —Н–љ–і–Њ—В–µ–ї–Є—П, –≥–Є–њ–µ—А–њ–ї–∞–Ј–Є—П –Є–љ—В–Є–Љ—Л, —Б–Ї–ї–µ—А–Њ–Ј [4].
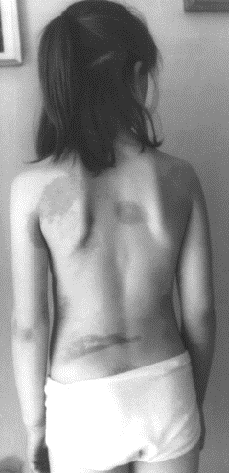
–Р—В—А–Њ—Д–Њ–і–µ—А–Љ–Є—П –Я–∞–Ј–Є–љ–Є – –Я—М–µ—А–Є–љ–Є —Б–Њ—З–µ—В–∞–µ—В—Б—П —Б –њ–Њ–ї–Њ—Б–Њ–≤–Є–і–љ–Њ–є —Д–Њ—А–Љ–Њ–є (–≤ –Њ–±–ї–∞—Б—В–Є –њ–Њ—П—Б–љ–Є—Ж—Л).
–Ф–∞–љ–љ—Л–µ –Ї–ї–Є–љ–Є–Ї–Њ-–ї–∞–±–Њ—А–∞—В–Њ—А–љ—Л—Е –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–є –Є–Љ–Љ—Г–љ–љ—Л—Е –љ–∞—А—Г—И–µ–љ–Є–є (—Б –Є–Ј–Љ–µ–љ–µ–љ–Є—П–Љ–Є –Ї–∞–Ї –≤ –≥—Г–Љ–Њ—А–∞–ї—М–љ–Њ–Љ, —В–∞–Ї –Є –≤ –Ї–ї–µ—В–Њ—З–љ–Њ–Љ –Ј–≤–µ–љ–µ –Є–Љ–Љ—Г–љ–Є—В–µ—В–∞) —Г–Ї–∞–Ј—Л–≤–∞—О—В –љ–∞ –Є—Е –≤–∞–ґ–љ–Њ—Б—В—М –≤ –њ–∞—В–Њ–≥–µ–љ–µ–Ј–µ —Б–Ї–ї–µ—А–Њ–і–µ—А–Љ–Є–Є [7, 8].
–С–Њ–ї–µ–µ —З–µ–Љ —Г 70% –±–Њ–ї—М–љ—Л—Е —Б–Ї–ї–µ—А–Њ–і–µ—А–Љ–Є–µ–є –Њ–±–љ–∞—А—Г–ґ–Є–≤–∞—О—В —Ж–Є—А–Ї—Г–ї–Є—А—Г—О—Й–Є–µ –≤ –Ї—А–Њ–≤–Є –∞—Г—В–Њ–∞–љ—В–Є—В–µ–ї–∞ [9]. –Т –Ї—А–Њ–≤–Є –Є —В–Ї–∞–љ—П—Е –≤—Л—П–≤–ї—П—О—В –њ–Њ–≤—Л—И–µ–љ–љ–Њ–µ —Б–Њ–і–µ—А–ґ–∞–љ–Є–µ –°–Ф4+-–ї–Є–Љ—Д–Њ—Ж–Є—В–Њ–≤ –Є –≤—Л—Б–Њ–Ї–Є–µ —Г—А–Њ–≤–љ–Є –Є–љ—В–µ—А–ї–µ–є–Ї–Є–љ–∞-2 (IL - 2) –Є IL-2-—А–µ—Ж–µ–њ—В–Њ—А–Њ–≤. –£—Б—В–∞–љ–Њ–≤–ї–µ–љ–∞ –Ї–Њ—А—А–µ–ї—П—Ж–Є—П –Љ–µ–ґ–і—Г –∞–Ї—В–Є–≤–љ–Њ—Б—В—М—О –Ґ-—Е–µ–ї–њ–µ—А–Њ–≤ –Є –∞–Ї—В–Є–≤–љ–Њ—Б—В—М—О —Б–Ї–ї–µ—А–Њ–і–µ—А–Љ–Є—З–µ—Б–Ї–Њ–≥–Њ –њ—А–Њ—Ж–µ—Б—Б–∞ [10].
–†.–Т. –Я–µ—В—А–Њ–≤ [11] —А–∞—Б—Б–Љ–∞—В—А–Є–≤–∞–µ—В —Б–Ї–ї–µ—А–Њ–і–µ—А–Љ–Є—О –Ї–∞–Ї –∞—Г—В–Њ–Є–Љ–Љ—Г–љ–Њ–µ –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є–µ, –њ—А–Є –Ї–Њ—В–Њ—А–Њ–Љ –≤ –Њ—Б–љ–Њ–≤–µ –љ–∞—А—Г—И–µ–љ–Є–є –ї–µ–ґ–Є—В –≤–Ј–∞–Є–Љ–Њ–і–µ–є—Б—В–≤–Є–µ –∞—Г—В–Њ–∞–љ—В–Є–≥–µ–љ–Њ–≤ —Б –ї–Є–Љ—Д–Њ–Є–і–љ—Л–Љ–Є –Ї–ї–µ—В–Ї–∞–Љ–Є. –Я—А–Є —Н—В–Њ–Љ –Ґ-—Е–µ–ї–њ–µ—А—Л, –∞–Ї—В–Є–≤–Є—А–Њ–≤–∞–љ–љ—Л–µ —Н–Ї–Ј–Њ- –Є–ї–Є —Н–љ–і–Њ–≥–µ–љ–љ—Л–Љ–Є —Д–∞–Ї—В–Њ—А–∞–Љ–Є, –≤—Л—А–∞–±–∞—В—Л–≤–∞—О—В –ї–Є–Љ—Д–Њ–Ї–Є–љ—Л, —Б—В–Є–Љ—Г–ї–Є—А—Г—О—Й–Є–µ —Д–Є–±—А–Њ–±–ї–∞—Б—В—Л. –Т.–Р. –Т–ї–∞–і–Є–Љ–Є—А—Ж–µ–≤ –Є —Б–Њ–∞–≤—В. [12] —Б—З–Є—В–∞—О—В, —З—В–Њ –њ–Њ–≤—Л—И–µ–љ–љ—Л–є —Г—А–Њ–≤–µ–љ—М –Ї–Њ–ї–ї–∞–≥–µ–љ–Њ–≤—Л—Е –±–µ–ї–Ї–Њ–≤, —П–≤–ї—П—П—Б—М –Є—Б—В–Њ—З–љ–Є–Ї–Њ–Љ –∞–Ї—В–Є–≤–љ–Њ–є –∞–љ—В–Є–≥–µ–љ–љ–Њ–є —Б—В–Є–Љ—Г–ї—П—Ж–Є–Є, —Б–Њ–Ј–і–∞–µ—В —Д–Њ–љ, –љ–∞ –Ї–Њ—В–Њ—А–Њ–Љ –њ—А–Є –≥–µ–љ–µ—В–Є—З–µ—Б–Ї–Њ–є –њ—А–µ–і—А–∞—Б–њ–Њ–ї–Њ–ґ–µ–љ–љ–Њ—Б—В–Є —А–µ–∞–ї–Є–Ј—Г—О—В—Б—П –∞—Г—В–Њ–Є–Љ–Љ—Г–љ–љ—Л–µ —А–µ–∞–Ї—Ж–Є–Є. –Т–Њ–Ј–љ–Є–Ї–∞—О—Й–Є–є –њ–Њ—А–Њ—З–љ—Л–є –Ї—А—Г–≥ –≤–Ј–∞–Є–Љ–Њ–≤–ї–Є—П–љ–Є—П –ї–Є–Љ—Д–Њ–Є–і–љ—Л—Е –Є –Ї–Њ–ї–ї–∞–≥–µ–љ—Б–Є–љ—В–µ–Ј–Є—А—Г—О—Й–Є—Е –Ї–ї–µ—В–Њ–Ї –≤–µ–і–µ—В –Ї –њ—А–Њ–≥—А–µ—Б—Б–Є—А–Њ–≤–∞–љ–Є—О —Д–Є–±—А–Њ–Ј–љ–Њ–≥–Њ –њ—А–Њ—Ж–µ—Б—Б–∞.
–Я—А–Є —Б–Ї–ї–µ—А–Њ–і–µ—А–Љ–Є–Є –љ–∞–±–ї—О–і–∞—О—В—Б—П —А–∞–Ј–љ–Њ–Њ–±—А–∞–Ј–љ—Л–µ –і—А—Г–≥–Є–µ –∞—Г—В–Њ–Є–Љ–Љ—Г–љ–љ—Л–µ –љ–∞—А—Г—И–µ–љ–Є—П: —А–∞–Ј–ї–Є—З–љ—Л–µ –∞—Г—В–Њ–∞–љ—В–Є—В–µ–ї–∞, —Б–љ–Є–ґ–µ–љ–Є–µ —Г—А–Њ–≤–љ—П –Ґ-–ї–Є–Љ—Д–Њ—Ж–Є—В–Њ–≤ –њ—А–Є –љ–µ–Є–Ј–Љ–µ–љ–µ–љ–љ–Њ–Љ –Є–ї–Є –њ–Њ–≤—Л—И–µ–љ–љ–Њ–Љ —Б–Њ–і–µ—А–ґ–∞–љ–Є–Є –Т-–ї–Є–Љ—Д–Њ—Ж–Є—В–Њ–≤, —Б–љ–Є–ґ–µ–љ–Є–µ —Д—Г–љ–Ї—Ж–Є–Є –Ґ-—Б—Г–њ—А–µ—Б—Б–Њ—А–Њ–≤ –њ—А–Є –љ–µ–Є–Ј–Љ–µ–љ–µ–љ–љ–Њ–є –Є–ї–Є –њ–Њ–≤—Л—И–µ–љ–љ–Њ–є —Д—Г–љ–Ї—Ж–Є–Є –Ґ-—Е–µ–ї–њ–µ—А–Њ–≤, —Б–љ–Є–ґ–µ–љ–Є–µ —Д—Г–љ–Ї—Ж–Є–Њ–љ–∞–ї—М–љ–Њ–є –∞–Ї—В–Є–≤–љ–Њ—Б—В–Є –µ—Б—В–µ—Б—В–≤–µ–љ–љ—Л—Е –Ї–Є–ї–ї–µ—А–Њ–≤ [13 – 15].
–Т 20 – 40% —Б–ї—Г—З–∞–µ–≤ –њ—А–Є –±–ї—П—И–µ—З–љ–Њ–є —Б–Ї–ї–µ—А–Њ–і–µ—А–Љ–Є–Є –Њ–±–љ–∞—А—Г–ґ–Є–≤–∞—О—В –∞–љ—В–Є–љ—Г–Ї–ї–µ–∞—А–љ—Л–µ –∞–љ—В–Є—В–µ–ї–∞ [16], —Г 30 – 74% –±–Њ–ї—М–љ—Л—Е —Б–Ї–ї–µ—А–Њ–і–µ—А–Љ–Є–µ–є –≤—Л—П–≤–ї—П—О—В —Ж–Є—А–Ї—Г–ї–Є—А—Г—О—Й–Є–µ –Є–Љ–Љ—Г–љ–љ—Л–µ –Ї–Њ–Љ–њ–ї–µ–Ї—Б—Л [18 – 19].
–Ъ–ї–∞—Б—Б–Є—Д–Є–Ї–∞—Ж–Є—П
–Ь–љ–Њ–≥–Њ–Њ–±—А–∞–Ј–Є–µ –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є—Е —Д–Њ—А–Љ –Є –≤–∞—А–Є–∞–љ—В–Њ–≤ –Ю–°, –∞ —В–∞–Ї–ґ–µ –љ–∞–ї–Є—З–Є–µ —Б—В–µ—А—В—Л—Е (–∞–±–Њ—А—В–Є–≤–љ—Л—Е) –њ—А–Њ—П–≤–ї–µ–љ–Є–є –±–Њ–ї–µ–Ј–љ–Є, —А–∞–Ј–љ–∞—П —Б—В–µ–њ–µ–љ—М –≤–Њ–≤–ї–µ—З–µ–љ–Є—П –≤ –њ–∞—В–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є–є –њ—А–Њ—Ж–µ—Б—Б –Ї–Њ–ґ–Є –Є –њ–Њ–і–ї–µ–ґ–∞—Й–Є—Е —В–Ї–∞–љ–µ–є –Ј–∞—В—А—Г–і–љ—П—О—В –µ–µ –і–Є–∞–≥–љ–Њ—Б—В–Є–Ї—Г.
–Я—А–∞–Ї—В–Є—З–µ—Б–Ї–Є –њ—А–Є–µ–Љ–ї–µ–Љ–∞ –Ї–ї–∞—Б—Б–Є—Д–Є–Ї–∞—Ж–Є—П –Ю–°, –Њ—Б–љ–Њ–≤–∞–љ–љ–∞—П –љ–∞ –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Њ–Љ –њ—А–Є–љ—Ж–Є–њ–µ [17, 19, 20].
I. –С–ї—П—И–µ—З–љ–∞—П —Д–Њ—А–Љ–∞ —Б –µ–µ –≤–∞—А–Є–∞–љ—В–∞–Љ–Є (—А–∞–Ј–љ–Њ–≤–Є–і–љ–Њ—Б—В—П–Љ–Є):
1) –Є–љ–і—Г—А–∞—В–Є–≤–љ–Њ-–∞—В—А–Њ—Д–Є—З–µ—Б–Ї–∞—П (–Т–Є–ї—М—Б–Њ–љ–∞);
2) –њ–Њ–≤–µ—А—Е–љ–Њ—Б—В–љ–∞—П "—Б–Є—А–µ–љ–µ–≤–∞—П" (–У—Г–ґ–µ—А–Њ);
3) –Ї–µ–ї–Њ–Є–і–Њ–њ–Њ–і–Њ–±–љ–∞—П;
4) —Г–Ј–ї–Њ–≤–∞—В–∞—П, –≥–ї—Г–±–Њ–Ї–∞—П;
5) –±—Г–ї–ї–µ–Ј–љ–∞—П;
6) –≥–µ–љ–µ—А–∞–ї–Є–Ј–Њ–≤–∞–љ–љ–∞—П.
II. –Ы–Є–љ–µ–є–љ–∞—П —Д–Њ—А–Љ–∞ (–њ–Њ–ї–Њ—Б–Њ–≤–Є–і–љ–∞—П):
1) —Б–∞–±–ї–µ–≤–Є–і–љ–∞—П;
2) –ї–µ–љ—В–Њ–≤–Є–і–љ–∞—П;
3) –Ј–Њ—Б—В–µ—А–Є—Д–Њ—А–Љ–љ–∞—П.
III. –°–Ї–ї–µ—А–Њ–∞—В—А–Њ—Д–Є—З–µ—Б–Ї–Є–є –ї–Є—Е–µ–љ (–±–Њ–ї–µ–Ј–љ—М –±–µ–ї—Л—Е –њ—П—В–µ–љ).
IV. –Ш–і–Є–Њ–њ–∞—В–Є—З–µ—Б–Ї–∞—П –∞—В—А–Њ—Д–Њ–і–µ—А–Љ–Є—П –Я–∞–Ј–Є–љ–Є – –Я—М–µ—А–Є–љ–Є.
–Ъ–ї–Є–љ–Є–Ї–∞
–Т –і–Є–љ–∞–Љ–Є–Ї–µ —А–∞–Ј–≤–Є—В–Є—П –Њ—З–∞–≥–Є —Б–Ї–ї–µ—А–Њ–і–µ—А–Љ–Є–Є –Њ–±—Л—З–љ–Њ –њ—А–Њ—Е–Њ–і—П—В —В—А–Є —Б—В–∞–і–Є–Є: —Н—А–Є—В–µ–Љ–∞, —Г–њ–ї–Њ—В–љ–µ–љ–Є–µ –Ї–Њ–ґ–Є –Є –∞—В—А–Њ—Д–Є—П. –Я—А–Є –Њ—В–і–µ–ї—М–љ—Л—Е –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є—Е —Д–Њ—А–Љ–∞—Е –Є–љ–і—Г—А–∞—Ж–Є—П –љ–µ –≤—Б–µ–≥–і–∞ –≤—Л—А–∞–ґ–µ–љ–∞ –Є–ї–Є –і–∞–ґ–µ –Њ—В—Б—Г—В—Б—В–≤—Г–µ—В.
–Ю—Б–Њ–±–µ–љ–љ–Њ—Б—В—М—О –Ю–° —П–≤–ї—П–µ—В—Б—П –µ–µ –Ї–ї–Є–љ–Є—З–µ—Б–Ї–∞—П –Љ–љ–Њ–≥–Њ–ї–Є–Ї–Њ—Б—В—М. –С–ї—П—И–µ—З–љ–∞—П —Д–Њ—А–Љ–∞ —Е–∞—А–∞–Ї—В–µ—А–Є–Ј—Г–µ—В—Б—П –≤–Њ–Ј–љ–Є–Ї–љ–Њ–≤–µ–љ–Є–µ–Љ –љ–∞ —А–∞–Ј–ї–Є—З–љ—Л—Е —Г—З–∞—Б—В–Ї–∞—Е –Ї–Њ–ґ–љ–Њ–≥–Њ –њ–Њ–Ї—А–Њ–≤–∞ (–≤ –Њ—В–і–µ–ї—М–љ—Л—Е —Б–ї—Г—З–∞—П—Е –Є –љ–∞ —Б–ї–Є–Ј–Є—Б—В—Л—Е –Њ–±–Њ–ї–Њ—З–Ї–∞—Е). –С–ї—П—И–Ї–Є –Њ–Ї—А—Г–≥–ї–Њ-–Њ–≤–∞–ї—М–љ–Њ–є —Д–Њ—А–Љ—Л, —А–µ–ґ–µ – —Б –љ–µ–њ—А–∞–≤–Є–ї—М–љ—Л–Љ–Є –Њ—З–µ—А—В–∞–љ–Є—П–Љ–Є. –Ш—Е —А–∞–Ј–Љ–µ—А – –Њ—В –Њ–і–љ–Њ–≥–Њ –і–Њ –љ–µ—Б–Ї–Њ–ї—М–Ї–Є—Е —Б–∞–љ—В–Є–Љ–µ—В—А–Њ–≤ –≤ –і–Є–∞–Љ–µ—В—А–µ. –Ю–Ї—А–∞—Б–Ї–∞ –Ї–Њ–ґ–Є –≤ –Њ—З–∞–≥–∞—Е –њ–Њ—А–∞–ґ–µ–љ–Є—П —А–Њ–Ј–Њ–≤–∞—В–Њ-—Б–Є—А–µ–љ–µ–≤–∞—П, –ї–Є–≤–Є–і–љ–∞—П. –Т —Ж–µ–љ—В—А–µ –±–ї—П—И–Ї–Є –Њ–±—Л—З–љ–Њ —Д–Њ—А–Љ–Є—А—Г–µ—В—Б—П –і–µ—А–Љ–∞—В–Њ—Б–Ї–ї–µ—А–Њ–Ј –≤ –≤–Є–і–µ –і–Є—Б–Ї–∞ —Г–њ–ї–Њ—В–љ–µ–љ–љ–Њ–є –Є–ї–Є –њ–ї–Њ—В–љ–Њ–є –Ї–Њ–ґ–Є, –≤–Њ—Б–Ї–Њ–≤–Є–і–љ–Њ-—Б–µ—А–Њ–≤–∞—В–Њ–є –Њ–Ї—А–∞—Б–Ї–Є –Є–ї–Є —Ж–≤–µ—В–∞ —Б–ї–Њ–љ–Њ–≤–Њ–є –Ї–Њ—Б—В–Є, —Б –≥–ї–∞–і–Ї–Њ–є –±–ї–µ—Б—В—П—Й–µ–є –њ–Њ–≤–µ—А—Е–љ–Њ—Б—В—М—О. –Я–Њ –њ–µ—А–Є—Д–µ—А–Є–Є –Њ—З–∞–≥–∞ —З–∞—Б—В–Њ –Є–Љ–µ–µ—В—Б—П –Ї–∞–є–Љ–∞ –ї–Є–≤–Є–і–љ–Њ–≥–Њ, —А–Њ–Ј–Њ–≤–∞—В–Њ-—Б–Є–љ—О—И–љ–Њ–≥–Њ —Ж–≤–µ—В–∞ —Б —Д–Є–Њ–ї–µ—В–Њ–≤—Л–Љ –Њ—В—В–µ–љ–Ї–Њ–Љ, —З—В–Њ —П–≤–ї—П–µ—В—Б—П –њ–Њ–Ї–∞–Ј–∞—В–µ–ї–µ–Љ –∞–Ї—В–Є–≤–љ–Њ—Б—В–Є –њ—А–Њ—Ж–µ—Б—Б–∞.
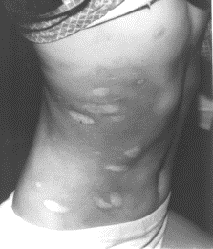
–Ь–љ–Њ–≥–Њ–Њ—З–∞–≥–Њ–≤–∞—П –±–ї—П—И–µ—З–љ–∞—П —Б–Ї–ї–µ—А–Њ–і–µ—А–Љ–Є—П (–љ–∞ —Д–Њ–љ–µ –Ј–∞—Б—В–Њ–є–љ–Њ–є –≥–Є–њ–µ—А–µ–Љ–Є–Є –Є –њ–Є–≥–Љ–µ–љ—В–∞—Ж–Є–Є –Њ—З–∞–≥–Є –і–µ—А–Љ–∞—В–Њ—Б–Ї–ї–µ—А–Њ–Ј–∞).
–Я–µ—А–Є—Д–µ—А–Є—З–µ—Б–Ї–Є–є —А–Њ—Б—В –±–ї—П—И–Ї–Є –Є –њ–Њ—П–≤–ї–µ–љ–Є–µ –љ–Њ–≤—Л—Е –Њ—З–∞–≥–Њ–≤ –Њ–±—Л—З–љ–Њ –њ—А–Њ–Є—Б—Е–Њ–і—П—В –Љ–µ–і–ї–µ–љ–љ–Њ –Є –љ–µ —Б–Њ–њ—А–Њ–≤–Њ–ґ–і–∞—О—В—Б—П —Б—Г–±—К–µ–Ї—В–Є–≤–љ—Л–Љ–Є –Њ—Й—Г—Й–µ–љ–Є—П–Љ–Є. –Т –Њ—З–∞–≥–∞—Е –Є –њ—А–Є–ї–µ–ґ–∞—Й–Є—Е —Г—З–∞—Б—В–Ї–∞—Е –Ї–Њ–ґ–Є –Љ–Њ–≥—Г—В –≤–Њ–Ј–љ–Є–Ї–∞—В—М –њ–Є–≥–Љ–µ–љ—В–∞—Ж–Є—П –Є —В–µ–ї–µ–∞–љ–≥–Є—Н–Ї—В–∞–Ј–Є–Є.
–Э–∞ –њ–Њ—А–∞–ґ–µ–љ–љ–Њ–є –Ї–Њ–ґ–µ –њ–Њ—В–Њ–Њ—В–і–µ–ї–µ–љ–Є–µ –њ–Њ–љ–Є–ґ–µ–љ–Њ –Є–ї–Є –Њ—В—Б—Г—В—Б—В–≤—Г–µ—В, –љ–∞—А—Г—И–∞—О—В—Б—П —Д—Г–љ–Ї—Ж–Є—П —Б–∞–ї—М–љ—Л—Е –ґ–µ–ї–µ–Ј –Є —А–Њ—Б—В –≤–Њ–ї–Њ—Б.
–Ъ—А–∞–є–љ–µ —А–µ–і–Ї–Њ–є —А–∞–Ј–љ–Њ–≤–Є–і–љ–Њ—Б—В—М—О –Ю–° —П–≤–ї—П–µ—В—Б—П –±—Г–ї–ї–µ–Ј–љ–∞—П, —Н—А–Њ–Ј–Є–≤–љ–Њ-—П–Ј–≤–µ–љ–љ–∞—П —Д–Њ—А–Љ–∞, –Њ–±—Л—З–љ–Њ –≤–Њ–Ј–љ–Є–Ї–∞—О—Й–∞—П –љ–∞ —Д–Њ–љ–µ —Б–Ї–ї–µ—А–Њ–Ј–Є—А–Њ–≤–∞–љ–Є—П –Ї–Њ–ґ–Є –≤ –њ–µ—А–Є–∞—А—В–Є–Ї—Г–ї—П—А–љ—Л—Е —Г—З–∞—Б—В–Ї–∞—Е. –Ю–љ–∞ –Љ–Њ–ґ–µ—В –њ—А–Њ—П–≤–Є—В—М—Б—П –љ–∞ –ї—О–±–Њ–Љ –Њ—З–∞–≥–µ —Б–Ї–ї–µ—А–Њ–і–µ—А–Љ–Є–Є. –Я–Њ—Б–ї–µ–і–Њ–≤–∞—В–µ–ї—М–љ–Њ–µ —Д–Њ—А–Љ–Є—А–Њ–≤–∞–љ–Є–µ –≤–µ–Ј–Є–Ї—Г–ї–µ–Ј–љ–Њ-–±—Г–ї–ї–µ–Ј–љ—Л—Е –Є —Н—А–Њ–Ј–Є–≤–љ–Њ-—П–Ј–≤–µ–љ–љ—Л—Е –њ–Њ—А–∞–ґ–µ–љ–Є–є —Б–≤—П–Ј—Л–≤–∞—О—В —Б –і–Є—Б—В—А–Њ—Д–Є—З–µ—Б–Ї–Є–Љ–Є –Є–Ј–Љ–µ–љ–µ–љ–Є—П–Љ–Є –≤ —Б–Ї–ї–µ—А–Њ–Ј–Є—А–Њ–≤–∞–љ–љ–Њ–є –Ї–Њ–ґ–µ. –Ь–Њ–≥—Г—В –Є–≥—А–∞—В—М –њ—А–Є—З–Є–љ–љ—Г—О —А–Њ–ї—М —В—А–∞–≤–Љ–∞ –Є –≤—В–Њ—А–Є—З–љ–Њ–µ –Є–љ—Д–Є—Ж–Є—А–Њ–≤–∞–љ–Є–µ.
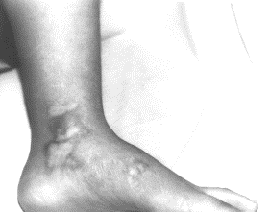
–Э–µ—Б–Ї–Њ–ї—М–Ї–Њ –Њ—З–∞–≥–Њ–≤ –±–ї—П—И–µ—З–љ–Њ–є —Б–Ї–ї–µ—А–Њ–і–µ—А–Љ–Є–Є —Б –≤—Л—А–∞–ґ–µ–љ–љ—Л–Љ –і–µ—А–Љ–∞—В–Њ—Б–Ї–ї–µ—А–Њ–Ј–Њ–Љ; –њ–Њ –Ї—А–∞—О –љ–µ–Ї–Њ—В–Њ—А—Л—Е –Є–Ј –љ–Є—Е –Ї–∞–є–Љ–∞ —А–Њ–Ј–Њ–≤–Њ-–Ї–Њ—А–Є—З–љ–µ–≤–∞—В–Њ–є –Њ–Ї—А–∞—Б–Ї–Є.
–Я—А–Є –њ–Њ–≤–µ—А—Е–љ–Њ—Б—В–љ–Њ–є —Б–Є—А–µ–љ–µ–≤–Њ–є –±–ї—П—И–µ—З–љ–Њ–є –Ю–° (–У—Г–ґ–µ—А–Њ) –љ–∞–±–ї—О–і–∞—О—В –µ–і–≤–∞ –Ј–∞–Љ–µ—В–љ–Њ–µ –њ–Њ–≤–µ—А—Е–љ–Њ—Б—В–љ–Њ–µ —Г–њ–ї–Њ—В–љ–µ–љ–Є–µ, –Ї–Њ–ґ–∞ –≤ –Њ—З–∞–≥–µ —А–Њ–Ј–Њ–≤–∞—В–Њ-—Б–Є—А–µ–љ–µ–≤–∞—П —Б –±–Њ–ї–µ–µ –Є–љ—В–µ–љ—Б–Є–≤–љ–Њ–є –Њ–Ї—А–∞—Б–Ї–Њ–є –љ–∞ –≥—А–∞–љ–Є—Ж–µ –Њ—З–∞–≥–∞.
–Я—А–Є –њ–Њ–ї–Њ—Б–Њ–≤–Є–і–љ–Њ–є —Д–Њ—А–Љ–µ –Ю–° –Њ—З–∞–≥–Є –ї–Є–љ–µ–є–љ—Л–µ, –≤ –≤–Є–і–µ –њ–Њ–ї–Њ—Б, —З–∞—Й–µ –ї–Њ–Ї–∞–ї–Є–Ј—Г—О—Й–Є–µ—Б—П –≤–і–Њ–ї—М –Њ–і–љ–Њ–є –Ї–Њ–љ–µ—З–љ–Њ—Б—В–Є, –љ–µ—А–µ–і–Ї–Њ – –њ–Њ —Е–Њ–і—Г –љ–µ—А–≤–љ–Њ-—Б–Њ—Б—Г–і–Є—Б—В–Њ–≥–Њ –њ—Г—З–Ї–∞. –Ю–љ–Є –Љ–Њ–≥—Г—В —А–∞—Б–њ–Њ–ї–∞–≥–∞—В—М—Б—П —В–∞–Ї–ґ–µ —Ж–Є—А–Ї—Г–ї—П—А–љ–Њ –љ–∞ —В—Г–ї–Њ–≤–Є—Й–µ –Є–ї–Є –Ї–Њ–љ–µ—З–љ–Њ—Б—В—П—Е. –Э–∞ –ї–Є—Ж–µ, –≤–Њ–ї–Њ—Б–Є—Б—В–Њ–є —З–∞—Б—В–Є –≥–Њ–ї–Њ–≤—Л –Њ—В–Љ–µ—З–∞—О—В –љ–µ—А–µ–і–Ї—Г—О –њ—А–Є —Н—В–Њ–є —Д–Њ—А–Љ–µ –ї–Њ–Ї–∞–ї–Є–Ј–∞—Ж–Є—О –њ–Њ—А–∞–ґ–µ–љ–Є–є, —З–∞—Б—В–Њ —А—Г–±—Ж–µ–≤–Є–і–љ–Њ-—Б–∞–±–ї–µ–≤–Є–і–љ—Л—Е (–љ–∞–њ–Њ–Љ–Є–љ–∞—О—Й–Є—Е —А—Г–±–µ—Ж –њ–Њ—Б–ї–µ —Г–і–∞—А–∞ —Б–∞–±–ї–µ–є). –Я–ї–Њ—В–љ—Л–є —В—П–ґ —Б–Ї–ї–µ—А–Њ–Ј–Є—А–Њ–≤–∞–љ–љ–Њ–є –Ї–Њ–ґ–Є –Љ–Њ–ґ–µ—В –Є–Љ–µ—В—М —А–∞–Ј–ї–Є—З–љ—Г—О –і–ї–Є–љ—Г –Є —И–Є—А–Є–љ—Г, –±—Г—А–Њ–≤–∞—В—Г—О –Њ–Ї—А–∞—Б–Ї—Г, –±–ї–µ—Б—В—П—Й—Г—О –њ–Њ–≤–µ—А—Е–љ–Њ—Б—В—М.
–Т –Љ–µ—Б—В–µ –µ–≥–Њ –ї–Њ–Ї–∞–ї–Є–Ј–∞—Ж–Є–Є –љ–∞ –Ї–Њ–ґ–µ –≥–Њ–ї–Њ–≤—Л –Њ—В—Б—Г—В—Б—В–≤—Г–µ—В —А–Њ—Б—В –≤–Њ–ї–Њ—Б. –Т–µ—А—В–Є–Ї–∞–ї—М–љ–Њ –Њ—З–∞–≥ –Љ–Њ–ґ–µ—В –њ—А–Њ—Е–Њ–і–Є—В—М –Њ—В –≤–Њ–ї–Њ—Б–Є—Б—В–Њ–є —З–∞—Б—В–Є –≥–Њ–ї–Њ–≤—Л, –њ–µ—А–µ—Б–µ–Ї–∞—П –ї–Њ–±, —Б–њ–Є–љ–Ї—Г –љ–Њ—Б–∞, –≥—Г–±—Л, –њ–Њ–і–±–Њ—А–Њ–і–Њ–Ї. –Э–µ—А–µ–і–Ї–Њ –≤ –њ—А–Њ—Ж–µ—Б—Б –≤–Њ–≤–ї–µ–Ї–∞–µ—В—Б—П —Б–ї–Є–Ј–Є—Б—В–∞—П –Њ–±–Њ–ї–Њ—З–Ї–∞ —А–Њ—В–Њ–≤–Њ–є –њ–Њ–ї–Њ—Б—В–Є.
–Я—А–Є —А–∞–Ј—А–µ—И–µ–љ–Є–Є –њ—А–Њ—Ж–µ—Б—Б–∞ –њ–Њ–≤–µ—А—Е–љ–Њ—Б—В—М –Њ—З–∞–≥–∞ —Б–≥–ї–∞–ґ–Є–≤–∞–µ—В—Б—П, –Њ–±—А–∞–Ј—Г–µ—В—Б—П –Ј–∞–њ–∞–і–µ–љ–Є–µ, –Њ–±—Г—Б–ї–Њ–≤–ї–µ–љ–љ–Њ–µ –∞—В—А–Њ—Д–Є–µ–є –Ї–Њ–ґ–Є, –Љ—Л—И—Ж –Є –Ї–Њ—Б—В–љ–Њ–є —В–Ї–∞–љ–Є.
–°–Ї–ї–µ—А–Њ–∞—В—А–Њ—Д–Є—З–µ—Б–Ї–Є–є –ї–Є—Е–µ–љ (–°–Р–Ы) –¶—Г–Љ–±—Г—И–∞ (—Б–Є–љ–Њ–љ–Є–Љ—Л: –±–Њ–ї–µ–Ј–љ—М –±–µ–ї—Л—Е –њ—П—В–µ–љ, –Ї–∞–њ–ї–µ–≤–Є–і–љ–∞—П —Б–Ї–ї–µ—А–Њ–і–µ—А–Љ–Є—П) —А–∞—Б—Б–Љ–∞—В—А–Є–≤–∞—О—В –Ї–∞–Ї –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є–µ, –±–ї–Є–Ј–Ї–Њ–µ –њ–Њ –Ї–ї–Є–љ–Є–Ї–µ –Ї –Њ–≥—А–∞–љ–Є—З–µ–љ–љ–Њ–є –њ–Њ–≤–µ—А—Е–љ–Њ—Б—В–љ–Њ–є —Б–Ї–ї–µ—А–Њ–і–µ—А–Љ–Є–Є, –љ–Њ –љ–µ –њ–Њ–ї–љ–Њ—Б—В—М—О –µ–є —В–Њ–ґ–і–µ—Б—В–≤–µ–љ–љ–Њ–µ.
–Ъ–ї–Є–љ–Є—З–µ—Б–Ї–Є–µ –њ—А–Њ—П–≤–ї–µ–љ–Є—П: –±–µ–ї–Њ–≤–∞—В—Л–µ, –њ–Њ—З—В–Є –Љ–Њ–ї–Њ—З–љ–Њ–≥–Њ —Ж–≤–µ—В–∞ –њ–∞–њ—Г–ї—Л –і–Є–∞–Љ–µ—В—А–Њ–Љ 1 – 3 –Љ–Љ, –Њ–±—Л—З–љ–Њ –Њ–Ї—А—Г–≥–ї—Л—Е –Њ—З–µ—А—В–∞–љ–Є–є, —А–∞—Б–њ–Њ–ї–Њ–ґ–µ–љ–љ—Л–µ –љ–∞ –љ–µ–Є–Ј–Љ–µ–љ–µ–љ–љ–Њ–є –Ї–Њ–ґ–µ. –Т –љ–∞—З–∞–ї–µ —Б–≤–Њ–µ–≥–Њ –њ–Њ—П–≤–ї–µ–љ–Є—П –Њ–љ–Є –Є–Љ–µ—О—В –Ї—А–∞—Б–љ–Њ–≤–∞—В—Г—О –Њ–Ї—А–∞—Б–Ї—Г, –Є–љ–Њ–≥–і–∞ –Њ–Ї—А—Г–ґ–µ–љ—Л –µ–і–≤–∞ –Ј–∞–Љ–µ—В–љ–Њ–є –ї–Є–ї–Њ–≤–∞—В–Њ–є –Ї–∞–µ–Љ–Ї–Њ–є. –Т —Ж–µ–љ—В—А–µ —Н–ї–µ–Љ–µ–љ—В–Њ–≤ –Љ–Њ–ґ–µ—В –±—Л—В—М –Ј–∞–њ–∞–і–µ–љ–Є–µ. –Я—А–Є —Б–ї–Є—П–љ–Є–Є —Б–≥—А—Г–њ–њ–Є—А–Њ–≤–∞–љ–љ—Л—Е –њ–∞–њ—Г–ї –Њ–±—А–∞–Ј—Г—О—В—Б—П –Њ—З–∞–≥–Є —Б —Д–µ—Б—В–Њ–љ—З–∞—В—Л–Љ–Є –Њ—З–µ—А—В–∞–љ–Є—П–Љ–Є. –Ы–Њ–Ї–∞–ї–Є–Ј—Г—О—В—Б—П —Н—В–Є –њ–Њ—А–∞–ґ–µ–љ–Є—П —З–∞—Й–µ –љ–∞ —И–µ–µ, —В—Г–ї–Њ–≤–Є—Й–µ, –њ–Њ–ї–Њ–≤—Л—Е –Њ—А–≥–∞–љ–∞—Е, –∞ —В–∞–Ї–ґ–µ –љ–∞ –і—А—Г–≥–Є—Е —Г—З–∞—Б—В–Ї–∞—Е –Ї–Њ–ґ–љ–Њ–≥–Њ –њ–Њ–Ї—А–Њ–≤–∞ –Є —Б–ї–Є–Ј–Є—Б—В—Л—Е –Њ–±–Њ–ї–Њ—З–Ї–∞—Е. –Т—Л—Б—Л–њ–∞–љ–Є—П –Є–Љ–µ—О—В —Б–Ї–ї–Њ–љ–љ–Њ—Б—В—М –Ї —Б–њ–Њ–љ—В–∞–љ–љ–Њ–Љ—Г —А–∞–Ј—А–µ—И–µ–љ–Є—О, –Њ—Б—В–∞–≤–ї—П—П –∞—В—А–Њ—Д–Є—З–µ—Б–Ї–Є–µ –≥–Є–њ–Њ–њ–Є–≥–Љ–µ–љ—В–љ—Л–µ –Є–ї–Є –∞–Љ–µ–ї–∞–љ–Њ—В–Є—З–µ—Б–Ї–Є–µ –њ—П—В–љ–∞. –Я–Њ–≤–µ—А—Е–љ–Њ—Б—В—М –Є—Е –±–ї–µ—Б—В—П—Й–∞—П, –Љ–Њ—А—Й–Є–љ–Є—Б—В–∞—П. –Ю–±—Л—З–љ–Њ —Б—Л–њ—М –љ–µ —Б–Њ–њ—А–Њ–≤–Њ–ґ–і–∞–µ—В—Б—П —Б—Г–±—К–µ–Ї—В–Є–≤–љ—Л–Љ–Є –Њ—Й—Г—Й–µ–љ–Є—П–Љ–Є.
–Ъ–ї–Є–љ–Є—З–µ—Б–Ї–Њ–є —А–∞–Ј–љ–Њ–≤–Є–і–љ–Њ—Б—В—М—О –°–Р–Ы —П–≤–ї—П–µ—В—Б—П –±–ї—П—И–µ—З–љ–∞—П —Д–Њ—А–Љ–∞ —Б –Њ—З–∞–≥–∞–Љ–Є, –і–Њ—Б—В–Є–≥–∞—О—Й–Є–Љ–Є –њ–Њ —А–∞–Ј–Љ–µ—А—Г –љ–µ—Б–Ї–Њ–ї—М–Ї–Њ —Б–∞–љ—В–Є–Љ–µ—В—А–Њ–≤, —Б –Њ–Ї—А—Г–≥–ї—Л–Љ–Є –Є–ї–Є –љ–µ–њ—А–∞–≤–Є–ї—М–љ—Л–Љ–Є –Њ—З–µ—А—В–∞–љ–Є—П–Љ–Є. –Ъ–Њ–ґ–∞ –≤ —В–∞–Ї–Є—Е –Њ—З–∞–≥–∞—Е –Є—Б—В–Њ–љ—З–µ–љ–∞, –ї–µ–≥–Ї–Њ —Б–Њ–±–Є—А–∞–µ—В—Б—П –≤ —Б–Ї–ї–∞–і–Ї–Є –њ–Њ —В–Є–њ—Г —Б–Љ—П—В–Њ–є –њ–∞–њ–Є—А–Њ—Б–љ–Њ–є –±—Г–Љ–∞–≥–Є. –Я—А–Є –њ–µ–Љ—Д–Є–≥–Њ–і–љ–Њ–є —Д–Њ—А–Љ–µ –Њ–±—А–∞–Ј—Г—О—В—Б—П –њ—Г–Ј—Л—А–Є –≤–µ–ї–Є—З–Є–љ–Њ–є —Б –≥–Њ—А–Њ—И–Є–љ—Г, —З–µ—А–µ–Ј –Є—Е —В–Њ–љ–Ї—Г—О –њ–Њ–Ї—А—Л—И–Ї—Г –њ—А–Њ—Б–≤–µ—З–Є–≤–∞–µ—В –њ—А–Њ–Ј—А–∞—З–љ–Њ–µ —Б–Њ–і–µ—А–ґ–Є–Љ–Њ–µ. –Я—А–Є —А–∞–Ј—А—Л–≤–µ –њ—Г–Ј—Л—А–µ–є –Њ–±—А–∞–Ј—Г—О—В—Б—П —Н—А–Њ–Ј–Є–Є.
–Ф–Є–∞–≥–љ–Њ—Б—В–Є–Ї–∞ –Ю–° –њ—А–µ–і—Б—В–∞–≤–ї—П–µ—В –Њ–њ—А–µ–і–µ–ї–µ–љ–љ—Л–µ —В—А—Г–і–љ–Њ—Б—В–Є –≤ —А–∞–љ–љ–Є–µ —Б—А–Њ–Ї–Є –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П. –Ю–± —Н—В–Њ–Љ —Б–≤–Є–і–µ—В–µ–ї—М—Б—В–≤—Г—О—В –љ–µ—А–µ–і–Ї–Є–µ —Б–ї—Г—З–∞–Є –і–Є–∞–≥–љ–Њ—Б—В–Є—З–µ—Б–Ї–Є—Е –Њ—И–Є–±–Њ–Ї. –Ч–∞–њ–Њ–Ј–і–∞–ї–Њ–µ –љ–∞ –Љ–µ—Б—П—Ж—Л, –∞ –Є–љ–Њ–≥–і–∞ –Є –љ–∞ –≥–Њ–і—Л —А–∞—Б–њ–Њ–Ј–љ–∞–≤–∞–љ–Є–µ –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П —В–∞–Є—В –≤ —Б–µ–±–µ —А–Є—Б–Ї —А–∞–Ј–≤–Є—В–Є—П —В—П–ґ–µ–ї—Л—Е —Д–Њ—А–Љ, –Ї–Њ—В–Њ—А—Л–µ –Љ–Њ–≥—Г—В –њ—А–Є–≤–Њ–і–Є—В—М –Ї –Є–љ–≤–∞–ї–Є–і–љ–Њ—Б—В–Є. –°–ї–µ–і—Б—В–≤–Є–µ–Љ –і–ї–Є—В–µ–ї—М–љ–Њ–≥–Њ –њ—А–Њ–≥—А–µ—Б—Б–Є—А—Г—О—Й–µ–≥–Њ —В–µ—З–µ–љ–Є—П —В–∞–Ї–ґ–µ –Љ–Њ–ґ–µ—В –±—Л—В—М —Д—Г–љ–Ї—Ж–Є–Њ–љ–∞–ї—М–љ–∞—П –љ–µ–і–Њ—Б—В–∞—В–Њ—З–љ–Њ—Б—В—М –Ї–Њ–ґ–Є –Є –Њ–њ–Њ—А–љ–Њ-–і–≤–Є–≥–∞—В–µ–ї—М–љ–Њ–≥–Њ –∞–њ–њ–∞—А–∞—В–∞.
–Я–Њ–і –≤–ї–Є—П–љ–Є–µ–Љ –ї–µ—З–µ–љ–Є—П, —А–µ–і–Ї–Њ —Б–њ–Њ–љ—В–∞–љ–љ–Њ, –Њ—З–∞–≥–Є –њ–Њ—А–∞–ґ–µ–љ–Є—П —А–∞–Ј—А–µ—И–∞—О—В—Б—П (–Є—Б—З–µ–Ј–∞—О—В —Г–њ–ї–Њ—В–љ–µ–љ–Є–µ, –Ї—А–∞—Б–љ–Њ—В–∞, –±–ї–µ—Б–Ї) —Б –Є—Б—Е–Њ–і–Њ–Љ –≤ –∞—В—А–Њ—Д–Є—О –Ї–Њ–ґ–Є, –љ–µ—А–µ–і–Ї–Њ –Њ—Б—В–∞–≤–ї—П—П –≤–Є—В–Є–ї–Є–≥–Є–љ–Њ–Ј–љ—Л–µ –Є–ї–Є –њ–Є–≥–Љ–µ–љ—В–љ—Л–µ –њ—П—В–љ–∞.
–Т–љ–µ—И–љ–µ –њ—А–Є —Н—В–Њ–Љ –Ї–Њ–ґ–∞ –љ–∞–њ–Њ–Љ–Є–љ–∞–µ—В –њ–µ—А–≥–∞–Љ–µ–љ—В. –Я—Г—И–Ї–Њ–≤—Л–µ –≤–Њ–ї–Њ—Б—Л –≤ —А–µ–Ј–Є–і—Г–∞–ї—М–љ—Л—Е –Њ—З–∞–≥–∞—Е –Њ—В—Б—Г—В—Б—В–≤—Г—О—В. –Ю—В–Љ–µ—З–∞–µ—В—Б—П –Є—Б—В–Њ–љ—З–µ–љ–Є–µ –љ–µ —В–Њ–ї—М–Ї–Њ –Ї–Њ–ґ–Є, –љ–Њ –Є –њ–Њ–і–ї–µ–ґ–∞—Й–Є—Е —В–Ї–∞–љ–µ–є. –Я–Њ—Б–ї–µ —А–∞–Ј—А–µ—И–µ–љ–Є—П —Б–Ї–ї–µ—А–Њ–і–µ—А–Љ–Є—З–µ—Б–Ї–Њ–≥–Њ –њ—А–Њ—Ж–µ—Б—Б–∞ –≤ –њ–Њ–≤–µ—А—Е–љ–Њ—Б—В–љ—Л—Е –±–ї—П—И–µ—З–љ—Л—Е –Њ—З–∞–≥–∞—Е –Є–Ј–Љ–µ–љ–µ–љ–Є—П –Ї–Њ–ґ–Є –Ј–љ–∞—З–Є—В–µ–ї—М–љ–Њ –Љ–µ–љ–µ–µ –≤—Л—А–∞–ґ–µ–љ—Л.
–Ю–±—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ
–Т—Б–µ –і–µ—В–Є, –±–Њ–ї–µ—О—Й–Є–µ –Ю–°, –љ–µ–Ј–∞–≤–Є—Б–Є–Љ–Њ –Њ—В –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Њ–є —Д–Њ—А–Љ—Л –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П –Є –Є–љ—В–µ–љ—Б–Є–≤–љ–Њ—Б—В–Є –њ–Њ—А–∞–ґ–µ–љ–Є—П –њ–Њ–і–ї–µ–ґ–∞—В –Є–љ—Б—В—А—Г–Љ–µ–љ—В–∞–ї—М–љ–Њ–Љ—Г –Њ–±—Б–ї–µ–і–Њ–≤–∞–љ–Є—О –≤ —Ж–µ–ї—П—Е —А–∞–љ–љ–µ–є –і–Є–∞–≥–љ–Њ—Б—В–Є–Ї–Є –≤–Є—Б—Ж–µ—А–∞–ї—М–љ–Њ–є –њ–∞—В–Њ–ї–Њ–≥–Є–Є, –≤—Л—П–≤–ї–µ–љ–Є—П –њ—А–Є–Ј–љ–∞–Ї–Њ–≤ —Б–Є—Б—В–µ–Љ–љ–Њ—Б—В–Є –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П. –Р —Г—З–Є—В—Л–≤–∞—П –≤–Њ–Ј–Љ–Њ–ґ–љ–Њ—Б—В—М –ї–∞—В–µ–љ—В–љ–Њ–≥–Њ —В–µ—З–µ–љ–Є—П –°–°–Ф, –Њ—Б–Њ–±–µ–љ–љ–Њ –≤ —А–∞–љ–љ–Є–µ —Б—А–Њ–Ї–Є –µ–µ –≤–Њ–Ј–љ–Є–Ї–љ–Њ–≤–µ–љ–Є—П, –Њ—Ж–µ–љ–Ї—Г —Б–Њ—Б—В–Њ—П–љ–Є—П –≤–љ—Г—В—А–µ–љ–љ–Є—Е –Њ—А–≥–∞–љ–Њ–≤ —Б –њ–Њ–Љ–Њ—Й—М—О –Є–љ—Б—В—А—Г–Љ–µ–љ—В–∞–ї—М–љ—Л—Е –Љ–µ—В–Њ–і–Њ–≤ —Г –і–µ—В–µ–є —Б –Ю–° —Б–ї–µ–і—Г–µ—В –њ—А–Њ–≤–Њ–і–Є—В—М –љ–µ —А–µ–ґ–µ 1 —А–∞–Ј–∞ –≤ 3 –≥–Њ–і–∞.
–Ч–љ–∞—П –Њ –љ–µ—А–µ–і–Ї–Њ–Љ —Б—Г–±–Ї–ї–Є–љ–Є—З–µ—Б–Ї–Њ–Љ —В–µ—З–µ–љ–Є–Є –°–°–Ф —Г –і–µ—В–µ–є –Є–ї–Є –і–∞–ґ–µ –Њ–± –Њ—В—Б—Г—В—Б—В–≤–Є–Є –µ–µ –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є—Е –њ—А–Є–Ј–љ–∞–Ї–Њ–≤, –Ї–Њ—В–Њ—А—Л–µ –Њ–±—Л—З–љ–Њ –Є–Љ–µ—О—В –љ–µ—Б–њ–µ—Ж–Є—Д–Є—З–µ—Б–Ї–Є–є —Е–∞—А–∞–Ї—В–µ—А, –≤—А–∞—З –і–Њ–ї–ґ–µ–љ –њ—А–Њ—П–≤–ї—П—В—М –љ–∞—Б—В–Њ—А–Њ–ґ–µ–љ–љ–Њ—Б—В—М –≤ –Њ—В–љ–Њ—И–µ–љ–Є–Є –≤–Њ–Ј–Љ–Њ–ґ–љ–Њ–≥–Њ —А–∞–Ј–≤–Є—В–Є—П —Б–Є—Б—В–µ–Љ–љ–Њ–≥–Њ –њ—А–Њ—Ж–µ—Б—Б–∞ –љ–µ —В–Њ–ї—М–Ї–Њ –њ—А–Є –Љ–љ–Њ–≥–Њ–Њ—З–∞–≥–Њ–≤—Л—Е –Є —А–∞—Б–њ—А–Њ—Б—В—А–∞–љ–µ–љ–љ—Л—Е –њ—А–Њ—П–≤–ї–µ–љ–Є—П—Е, –љ–Њ –Є –њ—А–Є –µ–і–Є–љ–Є—З–љ—Л—Е –Њ–≥—А–∞–љ–Є—З–µ–љ–љ—Л—Е –±–ї—П—И–Ї–∞—Е.
–Ч–∞ –Љ–љ–Њ–≥–Њ–ї–µ—В–љ–µ–µ –љ–∞–±–ї—О–і–µ–љ–Є–µ –Э.–Э. –£–≤–∞—А–Њ–≤–Њ–є [21] 173 –і–µ—В–µ–є —Б –°–°–Ф, –Ї–ї–Є–љ–Є–Ї–Њ-–Є–љ—Б—В—А—Г–Љ–µ–љ—В–∞–ї—М–љ–Њ –Њ–±—Б–ї–µ–і–Њ–≤–∞–љ–љ—Л—Е, –≤ 63% —Б–ї—Г—З–∞–µ–≤ –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є–µ –љ–∞—З–Є–љ–∞–ї–Њ—Б—М —Б –њ–Њ—А–∞–ґ–µ–љ–Є—П –Ї–Њ–ґ–Є (–Ї–Њ–ґ–љ—Л–є —Б–Є–љ–і—А–Њ–Љ). –Я—А–Є —Н—В–Њ–Љ –Ї–Њ–ґ–љ—Л–µ –Є–Ј–Љ–µ–љ–µ–љ–Є—П –≤ —А–∞–Ј–≥–∞—А–µ —Б–Є—Б—В–µ–Љ–љ–Њ–≥–Њ –њ—А–Њ—Ж–µ—Б—Б–∞ –±—Л–ї–Є –Њ—В–Љ–µ—З–µ–љ—Л —Г –≤—Б–µ—Е –±–Њ–ї—М–љ—Л—Е. –Ґ.–Ь. –Т–ї–∞—Б–Њ–≤–∞ [22] –њ—А–Є –Ї–ї–Є–љ–Є–Ї–Њ-–Є–љ—Б—В—А—Г–Љ–µ–љ—В–∞–ї—М–љ–Њ–Љ –Њ–±—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є —Г 51 (25,1%) –Є–Ј 203 –і–µ—В–µ–є, –±–Њ–ї—М–љ—Л—Е –Ю–°, –≤—Л—П–≤–Є–ї–∞ –≤–Є—Б—Ж–µ—А–∞–ї—М–љ—Л–µ –Є–Ј–Љ–µ–љ–µ–љ–Є—П, —В.–µ. –њ—А–Є–Ј–љ–∞–Ї–Є —Б–Є—Б—В–µ–Љ–љ–Њ–≥–Њ –њ—А–Њ—Ж–µ—Б—Б–∞. –°—А–µ–і–Є –љ–Є—Е – –њ–Њ—А–∞–ґ–µ–љ–Є—П —Б–µ—А–і—Ж–∞ (—Б–Ї–ї–µ—А–Њ–і–µ—А–Љ–Є—З–µ—Б–Ї–Њ–µ —Б–µ—А–і—Ж–µ – –љ–∞—А—Г—И–µ–љ–Є–µ –∞—В—А–Є–Њ–≤–µ–љ—В—А–Є–Ї—Г–ї—П—А–љ–Њ–є –Є –≤–љ—Г—В—А–Є–ґ–µ–ї—Г–і–Њ—З–Ї–Њ–≤–Њ–є –њ—А–Њ–≤–Њ–і–Є–Љ–Њ—Б—В–Є, —Б–Є–љ—Г—Б–Њ–≤–∞—П —В–∞—Е–Є–Ї–∞—А–і–Є—П, –∞—А–Є—В–Љ–Є—П, —Б–Љ–µ—Й–µ–љ–Є–µ –Є–љ—В–µ—А–≤–∞–ї–∞ S – T), –ї–µ–≥–Ї–Є—Е (—Г—Б–Є–ї–µ–љ–Є–µ –±—А–Њ–љ—Е–Њ–ї–µ–≥–Њ—З–љ–Њ–≥–Њ —А–Є—Б—Г–љ–Ї–∞, –і–Є—Д—Д—Г–Ј–љ—Л–є –Є–ї–Є –Њ—З–∞–≥–Њ–≤—Л–є –њ–љ–µ–≤–Љ–Њ—Б–Ї–ї–µ—А–Њ–Ј, –Ї–Є—Б—В—Л –≤ –ї–µ–≥–Ї–Є—Е – "—П—З–µ–Є—Б—В–Њ–µ" –ї–µ–≥–Ї–Њ–µ, —Г—В–Њ–ї—Й–µ–љ–Є–µ –Љ–µ–ґ–і–Њ–ї–µ–≤–Њ–є –њ–ї–µ–≤—А—Л), –ґ–µ–ї—Г–і–Њ—З–љ–Њ-–Ї–Є—И–µ—З–љ–Њ–≥–Њ —В—А–∞–Ї—В–∞ (–≥–∞—Б—В—А–Є—В, –Ї–Њ–ї–Є—В, –∞—В–Њ–љ–Є—П –њ–Є—Й–µ–≤–Њ–і–∞ –Є –ґ–µ–ї—Г–і–Ї–∞, –љ–∞—А—Г—И–µ–љ–Є—П —А–Є—В–Љ–∞, —Н–≤–∞–Ї—Г–∞—Ж–Є–Є), –њ–Њ—З–µ–Ї (—Б–љ–Є–ґ–µ–љ–Є–µ —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ–≥–Њ –њ–Њ—З–µ—З–љ–Њ–≥–Њ –њ–ї–∞–Ј–Љ–Њ—В–Њ–Ї–∞, –њ—А–Њ—В–µ–Є–љ—Г—А–Є—П).
–Ь.–Э. –Э–Є–Ї–Є—В–Є–љ–Њ–є [23] –њ—А–Є –Њ–±—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є 259 –і–µ—В–µ–є, –±–Њ–ї—М–љ—Л—Е –Ю–°, –±—Л–ї–Є –Њ–±–љ–∞—А—Г–ґ–µ–љ—Л —Б—Е–Њ–і–љ—Л–µ –≤–Є—Б—Ж–µ—А–∞–ї—М–љ—Л–µ –љ–∞—А—Г—И–µ–љ–Є—П. –Ъ–ї–Є–љ–Є—З–µ—Б–Ї–Є –њ—А–Њ–≤–µ—Б—В–Є –≥—А–∞–љ—М –Љ–µ–ґ–і—Г –Ю–° –Є –Ї–Њ–ґ–љ—Л–Љ —Б–Є–љ–і—А–Њ–Љ–Њ–Љ –њ—А–Є –°–°–Ф –љ–µ–≤–Њ–Ј–Љ–Њ–ґ–љ–Њ.
–Ф–µ—В–Є, –±–Њ–ї–µ—О—Й–Є–µ –Ю–°, –≤ –њ—А–Њ—Ж–µ—Б—Б–µ –Љ–љ–Њ–≥–Њ–Ї—Г—А—Б–Њ–≤–Њ–≥–Њ –ї–µ—З–µ–љ–Є—П –Є –љ–∞–±–ї—О–і–µ–љ–Є—П –і–Њ–ї–ґ–љ—Л –љ–∞—Е–Њ–і–Є—В—М—Б—П –њ–Њ–і –њ–Њ—Б—В–Њ—П–љ–љ—Л–Љ –Ї–Њ–љ—В—А–Њ–ї–µ–Љ –њ–µ–і–Є–∞—В—А–∞, –і–µ—А–Љ–∞—В–Њ–ї–Њ–≥–∞ –Є –Ї–Њ–љ—Б—Г–ї—М—В–Є—А–Њ–≤–∞—В—М—Б—П –њ–Њ –њ–Њ–Ї–∞–Ј–∞–љ–Є—П–Љ –і—А—Г–≥–Є–Љ–Є —Б–њ–µ—Ж–Є–∞–ї–Є—Б—В–∞–Љ–Є.
–Ы–µ—З–µ–љ–Є–µ
–Ы–µ—З–µ–љ–Є–µ –±–Њ–ї—М–љ—Л—Е –Ю–° –і–µ—В–µ–є –Њ—Б—В–∞–µ—В—Б—П —В—А—Г–і–љ–Њ–є –Ј–∞–і–∞—З–µ–є. –Ю–љ–Њ –і–Њ–ї–ґ–љ–Њ –±—Л—В—М –Ї–Њ–Љ–њ–ї–µ–Ї—Б–љ—Л–Љ –Є —Н—В–∞–њ–љ–Њ-–Ї—Г—А—Б–Њ–≤—Л–Љ. –Я—А–Є —Н—В–Њ–Љ –≤–∞–ґ–µ–љ –і–Є—Д—Д–µ—А–µ–љ—Ж–Є—А–Њ–≤–∞–љ–љ—Л–є –њ–Њ–і—Е–Њ–і, –њ—А–Є –Ї–Њ—В–Њ—А–Њ–Љ —Г—З–Є—В—Л–≤–∞—О—В—Б—П –∞–љ–∞–Љ–љ–µ–Ј –Є —А–µ–Ј—Г–ї—М—В–∞—В—Л –Ї–ї–Є–љ–Є–Ї–Њ-–ї–∞–±–Њ—А–∞—В–Њ—А–љ–Њ–≥–Њ –Њ–±—Б–ї–µ–і–Њ–≤–∞–љ–Є—П, —З—В–Њ –њ–Њ–Ј–≤–Њ–ї—П–µ—В –љ–∞–Ј–љ–∞—З–Є—В—М –∞–і–µ–Ї–≤–∞—В–љ—Л–µ –ї–µ—З–µ–±–љ—Л–µ –Љ–µ—А–Њ–њ—А–Є—П—В–Є—П. –Ю–љ–Є, –≤ —З–∞—Б—В–љ–Њ—Б—В–Є, –≤–Ї–ї—О—З–∞—О—В —Б–∞–љ–∞—Ж–Є—О –Њ—А–≥–∞–љ–Є–Ј–Љ–∞, –Ї–Њ—А—А–µ–Ї—Ж–Є—О —Д—Г–љ–Ї—Ж–Є–Њ–љ–∞–ї—М–љ—Л—Е –љ–∞—А—Г—И–µ–љ–Є–є –љ–µ—А–≤–љ–Њ–є, —Н–љ–і–Њ–Ї—А–Є–љ–љ–Њ–є, –Є–Љ–Љ—Г–љ–љ–Њ–є —Б–Є—Б—В–µ–Љ, –∞ —В–∞–Ї–ґ–µ –њ—А–µ–њ–∞—А–∞—В—Л –њ–∞—В–Њ–≥–µ–љ–µ—В–Є—З–µ—Б–Ї–Њ–є –љ–∞–њ—А–∞–≤–ї–µ–љ–љ–Њ—Б—В–Є.
–Т –њ—А–Њ–≥—А–µ—Б—Б–Є—А—Г—О—Й–µ–є —Б—В–∞–і–Є–Є –њ—А–µ–і–њ–Њ—З—В–Є—В–µ–ї—М–љ–Њ —Б—В–∞—Ж–Є–Њ–љ–∞—А–љ–Њ–µ –ї–µ—З–µ–љ–Є–µ —Б –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є–µ–Љ –њ–µ–љ–Є—Ж–Є–ї–ї–Є–љ–∞, –ї–Є–і–∞–Ј—Л –њ—А–Є –і–µ—А–Љ–∞—В–Њ—Б–Ї–ї–µ—А–Њ–Ј–µ, –і–Є–Љ–µ–Ї—Б–Є–і–∞ (–Ф–Ь–°–Ю), –≤–Є—В–∞–Љ–Є–љ–Њ–≤. –Я—А–Є —Б—В–∞–±–Є–ї–Є–Ј–∞—Ж–Є–Є –њ–∞—В–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Њ–≥–Њ –њ—А–Њ—Ж–µ—Б—Б–∞ —Б —В–µ–љ–і–µ–љ—Ж–Є–µ–є –Ї —А–∞–Ј—А–µ—И–µ–љ–Є—О –Є–љ–і—Г—А–∞—Ж–Є–Є –Є —Б–Ї–ї–µ—А–Њ–Ј–∞ –њ–Њ–Ї–∞–Ј–∞–љ—Л —Д–µ—А–Љ–µ–љ—В–љ—Л–µ –њ—А–µ–њ–∞—А–∞—В—Л, –Є–Љ–Љ—Г–љ–Њ–Љ–Њ–і—Г–ї—П—В–Њ—А—Л, —Б–њ–∞–Ј–Љ–Њ–ї–Є—В–Є–Ї–Є, –±–Є–Њ—Б—В–Є–Љ—Г–ї—П—В–Њ—А—Л, –њ–Є—А–Њ–≥–µ–љ–љ—Л–µ –њ—А–µ–њ–∞—А–∞—В—Л. –Ч–∞–Ї—А–µ–њ–ї—П—О—В –Є —Г—Б–Є–ї–Є–≤–∞—О—В –ї–µ—З–µ–±–љ—Л–є —Н—Д—Д–µ–Ї—В, –∞ —В–∞–Ї–ґ–µ –Њ–Ї–∞–Ј—Л–≤–∞—О—В —А–µ–∞–±–Є–ї–Є—В–∞—Ж–Є–Њ–љ–љ–Њ–µ –≤–Њ–Ј–і–µ–є—Б—В–≤–Є–µ —Д–Є–Ј–Є–Њ—В–µ—А–∞–њ–Є—П –Є —Б–∞–љ–∞—В–Њ—А–љ–Њ-–Ї—Г—А–Њ—А—В–љ–Њ–µ –ї–µ—З–µ–љ–Є–µ.
–Я–µ–љ–Є—Ж–Є–ї–ї–Є–љ —А–µ–Ї–Њ–Љ–µ–љ–і—Г–µ—В—Б—П –≤–≤–Њ–і–Є—В—М –≤ –њ—А–Њ–≥—А–µ—Б—Б–Є—А—Г—О—Й–µ–є —Б—В–∞–і–Є–Є –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П –њ–Њ 1 –Љ–ї–љ –Х–Ф/—Б—Г—В –≤ 2 – 3 –Є–љ—К–µ–Ї—Ж–Є—П—Е, –љ–∞ –Ї—Г—А—Б –і–Њ 15 –Љ–ї–љ –Х–Ф 2 – 3 –Ї—Г—А—Б–∞–Љ–Є —Б –Є–љ—В–µ—А–≤–∞–ї–Њ–Љ –Љ–µ–ґ–і—Г –љ–Є–Љ–Є 1,5 – 2 –Љ–µ—Б. –†–µ–ґ–µ –њ—А–Є–Љ–µ–љ—П—О—В –њ–Њ–ї—Г—Б–Є–љ—В–µ—В–Є—З–µ—Б–Ї–Є–µ –њ–µ–љ–Є—Ж–Є–ї–ї–Є–љ—Л (–∞–Љ–њ–Є—Ж–Є–ї–ї–Є–љ, –Њ–Ї—Б–∞—Ж–Є–ї–ї–Є–љ).
–Я—А–µ–і–њ–Њ–ї–∞–≥–∞–µ—В—Б—П, —З—В–Њ –ї–µ—З–µ–±–љ—Л–є —Н—Д—Д–µ–Ї—В –њ–µ–љ–Є—Ж–Є–ї–ї–Є–љ–∞ –Њ–±—Г—Б–ї–Њ–≤–ї–µ–љ –µ–≥–Њ —Б—В—А—Г–Ї—В—Г—А–љ—Л–Љ –Ї–Њ–Љ–њ–Њ–љ–µ–љ—В–Њ–Љ – –њ–µ–љ–Є—Ж–Є–ї–ї–∞–Љ–Є–љ–Њ–Љ, –Ї–Њ—В–Њ—А—Л–є –Є–љ–≥–Є–±–Є—А—Г–µ—В –Њ–±—А–∞–Ј–Њ–≤–∞–љ–Є–µ –љ–µ—А–∞—Б—В–≤–Њ—А–Є–Љ–Њ–≥–Њ –Ї–Њ–ї–ї–∞–≥–µ–љ–∞. –Ф–Њ–њ—Г—Б–Ї–∞–µ—В—Б—П —В–∞–Ї–ґ–µ —Б–∞–љ–Є—А—Г—О—Й–Є–є —Н—Д—Д–µ–Ї—В –њ–µ–љ–Є—Ж–Є–ї–ї–Є–љ–∞ –њ—А–Є –љ–∞–ї–Є—З–Є–Є —Д–Њ–Ї–∞–ї—М–љ–Њ–є –Є–љ—Д–µ–Ї—Ж–Є–Є.
–Ш–Ј —Д–µ—А–Љ–µ–љ—В–љ—Л—Е –њ—А–µ–њ–∞—А–∞—В–Њ–≤ —И–Є—А–Њ–Ї–Њ –њ—А–Є–Љ–µ–љ—П—О—В –ї–Є–і–∞–Ј—Г –Є —А–Њ–љ–Є–і–∞–Ј—Г, —Б–Њ–і–µ—А–ґ–∞—Й–Є–µ –≥–Є–∞–ї—Г—А–Њ–љ–Є–і–∞–Ј—Г. –Ы–µ—З–µ–±–љ—Л–є —Н—Д—Д–µ–Ї—В —Б–≤—П–Ј–∞–љ —Б–Њ —Б–≤–Њ–є—Б—В–≤–∞–Љ–Є –њ—А–µ–њ–∞—А–∞—В–Њ–≤ —Г–ї—Г—З—И–∞—В—М –Љ–Є–Ї—А–Њ—Ж–Є—А–Ї—Г–ї—П—Ж–Є—О –≤ —В–Ї–∞–љ—П—Е –Є —Б–њ–Њ—Б–Њ–±—Б—В–≤–Њ–≤–∞—В—М —А–∞–Ј—А–µ—И–µ–љ–Є—О —Б–Ї–ї–µ—А–Њ–Ј–∞ –≤ –Њ—З–∞–≥–∞—Е. –Э–∞ –Ї—Г—А—Б 15 – 20 –Є–љ—К–µ–Ї—Ж–Є–є. –Ы–Є–і–∞–Ј—Г –≤–≤–Њ–і—П—В –≤–љ—Г—В—А–Є–Љ—Л—И–µ—З–љ–Њ –њ–Њ 1 –Љ–ї —Б 32 – 64 –£–Х –≤ 1 –Љ–ї 0,5% —А–∞—Б—В–≤–Њ—А–∞ –љ–Њ–≤–Њ–Ї–∞–Є–љ–∞. –Ы–µ—З–µ–±–љ—Л–є —Н—Д—Д–µ–Ї—В –њ–Њ–≤—Л—И–∞–µ—В—Б—П –њ—А–Є —Б–Њ—З–µ—В–∞–љ–Є–Є –њ–∞—А–µ–љ—В–µ—А–∞–ї—М–љ–Њ–≥–Њ –≤–≤–µ–і–µ–љ–Є—П –њ—А–µ–њ–∞—А–∞—В–∞ —Б —Н–ї–µ–Ї—В—А–Њ—Д–Њ—А–µ—В–Є—З–µ—Б–Ї–Є–Љ. –Ъ—Г—А—Б—Л –њ–Њ–≤—В–Њ—А—П—О—В —З–µ—А–µ–Ј 1,5 – 2 –Љ–µ—Б –њ—А–Є –љ–∞–ї–Є—З–Є–Є –і–µ—А–Љ–∞—В–Њ—Б–Ї–ї–µ—А–Њ–Ј–∞.
–†–Њ–љ–Є–і–∞–Ј—Г –њ—А–Є–Љ–µ–љ—П—О—В –љ–∞—А—Г–ґ–љ–Њ, –љ–∞–љ–Њ—Б—П –µ–µ –њ–Њ—А–Њ—И–Њ–Ї (0,5 – 1,0 –≥) –љ–∞ —Б–Љ–Њ—З–µ–љ–љ—Г—О —Д–Є–Ј–Є–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є–Љ —А–∞—Б—В–≤–Њ—А–Њ–Љ —Б–∞–ї—Д–µ—В–Ї—Г. –Э–∞–Ї–ї–∞–і—Л–≤–∞—О—В —Б–∞–ї—Д–µ—В–Ї—Г –љ–∞ –Њ—З–∞–≥ –њ–Њ—А–∞–ґ–µ–љ–Є—П, —Д–Є–Ї—Б–Є—А—Г—П –±–Є–љ—В–Њ–Љ –≤ —В–µ—З–µ–љ–Є–µ –њ–Њ–ї—Г—Б—Г—В–Њ–Ї. –Ъ—Г—А—Б –∞–њ–њ–ї–Є–Ї–∞—Ж–Є–є –њ—А–Њ–і–Њ–ї–ґ–∞—О—В 2 – 3 –љ–µ–і.
–С–ї–∞–≥–Њ–њ—А–Є—П—В–љ–Њ–µ –≤–ї–Є—П–љ–Є–µ –љ–∞ —А–∞–Ј—А–µ—И–µ–љ–Є–µ —Б–Ї–ї–µ—А–Њ–і–µ—А–Љ–Є—З–µ—Б–Ї–Є—Е –Њ—З–∞–≥–Њ–≤ –Њ–Ї–∞–Ј—Л–≤–∞–µ—В —Н–ї–µ–Ї—В—А–Њ—Д–Њ—А–µ–Ј —Б 0,5% —А–∞—Б—В–≤–Њ—А–Њ–Љ —Б—Г–ї—М—Д–∞—В–∞ —Ж–Є–љ–Ї–∞. –Я—А–Њ—Ж–µ–і—Г—А—Л –њ—А–Њ–≤–Њ–і—П—В —З–µ—А–µ–Ј –і–µ–љ—М –њ–Њ 7 – 20 –Љ–Є–љ, –љ–∞ –Ї—Г—А—Б 10 – 12 —Б–µ–∞–љ—Б–Њ–≤.
–С–Є–Њ—Б—В–Є–Љ—Г–ї—П—В–Њ—А—Л (—Б–њ–ї–µ–љ–Є–љ, —Б—В–µ–Ї–ї–Њ–≤–Є–і–љ–Њ–µ —В–µ–ї–Њ, –∞–ї–Њ—Н), –∞–Ї—В–Є–≤–Є—А—Г—П –њ—А–Њ—Ж–µ—Б—Б—Л –Љ–µ—В–∞–±–Њ–ї–Є–Ј–Љ–∞ –≤ —Б–Њ–µ–і–Є–љ–Є—В–µ–ї—М–љ–Њ–є —В–Ї–∞–љ–Є, —Б–њ–Њ—Б–Њ–±—Б—В–≤—Г—О—В —А–µ–≥–µ–љ–µ—А–∞—Ж–Є–Є —В–Ї–∞–љ–µ–є –Є –њ–Њ–≤—Л—И–µ–љ–Є—О —А–µ–∞–Ї—В–Є–≤–љ–Њ—Б—В–Є –Њ—А–≥–∞–љ–Є–Ј–Љ–∞. –°–њ–ї–µ–љ–Є–љ –≤–≤–Њ–і—П—В –њ–Њ 1 – 2 –Љ–ї –≤–љ—Г—В—А–Є–Љ—Л—И–µ—З–љ–Њ, —Б—В–µ–Ї–ї–Њ–≤–Є–і–љ–Њ–µ —В–µ–ї–Њ – –њ–Њ 1 – 2 –Љ–ї –њ–Њ–і–Ї–Њ–ґ–љ–Њ, –∞–ї–Њ—Н – –њ–Њ 1 – 2 –Љ–ї –њ–Њ–і–Ї–Њ–ґ–љ–Њ, –љ–∞ –Ї—Г—А—Б 15 – 20 –Є–љ—К–µ–Ї—Ж–Є–є.
–Я–Є—А–Њ–≥–µ–љ–љ—Л–µ –њ—А–µ–њ–∞—А–∞—В—Л –њ–Њ–≤—Л—И–∞—О—В —А–µ–Ј–Є—Б—В–µ–љ—В–љ–Њ—Б—В—М –Њ—А–≥–∞–љ–Є–Ј–Љ–∞, —Б—В–Є–Љ—Г–ї–Є—А—Г—О—В –Ґ-–Ї–ї–µ—В–Њ—З–љ–Њ–µ –Ј–≤–µ–љ–Њ –Є–Љ–Љ—Г–љ–Є—В–µ—В–∞. –Ш–Ј —Н—В–Є—Е –њ—А–µ–њ–∞—А–∞—В–Њ–≤ —З–∞—Й–µ –Є—Б–њ–Њ–ї—М–Ј—Г—О—В –њ–Є—А–Њ–≥–µ–љ–∞–ї. –Я—А–Є–Љ–µ–љ—П—О—В –µ–≥–Њ –Њ–±—Л—З–љ–Њ —З–µ—А–µ–Ј 2 –і–љ—П –љ–∞ —В—А–µ—В–Є–є –≤–љ—Г—В—А–Є–Љ—Л—И–µ—З–љ–Њ, –љ–∞—З–Є–љ–∞—П —Б 10 – 15 –Ь–Я–Ф. –Ф–Њ–Ј—Г –≤ –Ј–∞–≤–Є—Б–Є–Љ–Њ—Б—В–Є –Њ—В —В–µ–Љ–њ–µ—А–∞—В—Г—А–љ–Њ–є —А–µ–∞–Ї—Ж–Є–Є –њ–Њ–≤—Л—И–∞—О—В –љ–∞ 5 – 10 –Ь–Я–Ф. –Ъ—Г—А—Б —Б–Њ—Б—В–Њ–Є—В –Є–Ј 10 – 15 –Є–љ—К–µ–Ї—Ж–Є–є.
–Ш–Љ–Љ—Г–љ–Њ–Ї–Њ—А—А–Є–≥–Є—А—Г—О—Й–Є–є —Н—Д—Д–µ–Ї—В –Њ–Ї–∞–Ј—Л–≤–∞—О—В –Є–Љ–Љ—Г–љ–Њ–Љ–Њ–і—Г–ї—П—В–Њ—А—Л, –≤ —З–∞—Б—В–љ–Њ—Б—В–Є —В–∞–Ї—В–Є–≤–Є–љ –Є —В–Є–Љ–Њ–њ—В–Є–љ. –Я–Њ–і –Є—Е –≤–ї–Є—П–љ–Є–µ–Љ –љ–∞—Б—В—Г–њ–∞–µ—В –љ–Њ—А–Љ–∞–ї–Є–Ј–∞—Ж–Є—П —А—П–і–∞ –Є–Љ–Љ—Г–љ–љ—Л—Е –њ–Њ–Ї–∞–Ј–∞—В–µ–ї–µ–є –Є –Ї–Њ–ї–ї–∞–≥–µ–љ–Њ–Њ–±—А–∞–Ј–Њ–≤–∞–љ–Є—П. –Ґ–∞–Ї—В–Є–≤–Є–љ –≤–≤–Њ–і—П—В –µ–ґ–µ–і–љ–µ–≤–љ–Њ –њ–Њ–і –Ї–Њ–ґ—Г –њ–Њ 1 –Љ–ї 0,01% —А–∞—Б—В–≤–Њ—А–∞ –≤ —В–µ—З–µ–љ–Є–µ 1 – 2 –љ–µ–і, 2 – 3 —А–∞–Ј–∞ –≤ –≥–Њ–і. –Ґ–Є–Љ–Њ–њ—В–Є–љ –љ–∞–Ј–љ–∞—З–∞–µ—В—Б—П –њ–Њ–і–Ї–Њ–ґ–љ–Њ –Ї–∞–ґ–і—Л–є 4-–є –і–µ–љ—М –≤ —В–µ—З–µ–љ–Є–µ 3 –љ–µ–і (–Є–Ј —А–∞—Б—З–µ—В–∞ 2 –Љ–Ї–≥ –љ–∞ 1 –Ї–≥ –Љ–∞—Б—Б—Л —В–µ–ї–∞).
–Р–љ–≥–Є–Њ–њ—А–Њ—В–µ–Ї—В–Њ—А—Л, —Г–ї—Г—З—И–∞—П –њ–µ—А–Є—Д–µ—А–Є—З–µ—Б–Ї–Њ–µ –Ї—А–Њ–≤–Њ–Њ–±—А–∞—Й–µ–љ–Є–µ –Є —В—А–Њ—Д–Є—З–µ—Б–Ї–Є–µ –њ—А–Њ—Ж–µ—Б—Б—Л –≤ –Њ—З–∞–≥–∞—Е –њ–Њ—А–∞–ґ–µ–љ–Є—П, —Б–њ–Њ—Б–Њ–±—Б—В–≤—Г—О—В —А–∞–Ј—А–µ—И–µ–љ–Є—О —Б–Ї–ї–µ—А–Њ—В–Є—З–µ—Б–Ї–Є—Е –Є–Ј–Љ–µ–љ–µ–љ–Є–є –Ї–Њ–ґ–Є. –Ш–Ј —Н—В–Њ–є –≥—А—Г–њ–њ—Л –Є—Б–њ–Њ–ї—М–Ј—Г—О—В: –њ–µ–љ—В–Њ–Ї—Б–Є—Д–Є–ї–ї–Є–љ (–њ–Њ 0,05 – 0,1 –≥ 2 – 3 —А–∞–Ј–∞ –≤ –і–µ–љ—М), –Ї—Б–∞–љ—В–Є–љ–Њ–ї–∞ –љ–Є–Ї–Њ—В–Є–љ–∞—В (–њ–Њ 1/2 – 1 —В–∞–±–ї–µ—В–Ї–µ 2 —А–∞–Ј–∞ –≤ –і–µ–љ—М), –љ–Є–Ї–Њ—И–њ–∞–љ (–њ–Њ 1/2 – 1 —В–∞–±–ї–µ—В–Ї–µ 2 – 3 —А–∞–Ј–∞ –≤ –і–µ–љ—М), –∞–њ—А–µ—Б—Б–Є–љ (–њ–Њ 0,005 – 0,015 –≥ 2 – 3 —А–∞–Ј–∞ –≤ –і–µ–љ—М). –Ю–і–Є–љ –Є–Ј —Н—В–Є—Е –њ—А–µ–њ–∞—А–∞—В–Њ–≤ –њ—А–Є–љ–Є–Љ–∞—О—В –Ї—Г—А—Б–Њ–Љ –њ—А–Њ–і–Њ–ї–ґ–Є—В–µ–ї—М–љ–Њ—Б—В—М—О 3 – 4 –љ–µ–і.
–Ф–Ь–°–Ю –љ–∞–Ј–љ–∞—З–∞—О—В –љ–∞—А—Г–ґ–љ–Њ –≤ –≤–Є–і–µ 33 – 50% —А–∞—Б—В–≤–Њ—А–∞ 1 – 2 —А–∞–Ј–∞ –≤ –і–µ–љ—М –њ–Њ–≤—В–Њ—А–љ—Л–Љ–Є –Љ–µ—Б—П—З–љ—Л–Љ–Є –Ї—Г—А—Б–∞–Љ–Є —Б –Є–љ—В–µ—А–≤–∞–ї–∞–Љ–Є –Љ–µ–ґ–і—Г –љ–Є–Љ–Є 1 – 1,5 –Љ–µ—Б. –Ъ–Њ–Љ–њ—А–µ—Б—Б–љ—Л–µ –њ–Њ–≤—П–Ј–Ї–Є –Є–ї–Є –∞–њ–њ–ї–Є–Ї–∞—Ж–Є–Є –њ—А–Є–Љ–µ–љ—П—О—В –љ–∞ –і–µ—А–Љ–∞—В–Њ—Б–Ї–ї–µ—А–Њ—В–Є—З–µ—Б–Ї–Є–µ –±–ї—П—И–Ї–Є –і–Њ –Є—Е –Ј–∞–Љ–µ—В–љ–Њ–≥–Њ —А–∞–Ј—А–µ—И–µ–љ–Є—П. –Я—А–µ–њ–∞—А–∞—В, –њ—А–Њ–љ–Є–Ї–∞—П –≥–ї—Г–±–Њ–Ї–Њ –≤ —В–Ї–∞–љ–Є, –Њ–Ї–∞–Ј—Л–≤–∞–µ—В –≤—Л—А–∞–ґ–µ–љ–љ–Њ–µ –њ—А–Њ—В–Є–≤–Њ–≤–Њ—Б–њ–∞–ї–Є—В–µ–ї—М–љ–Њ–µ –і–µ–є—Б—В–≤–Є–µ, —Б–і–µ—А–ґ–Є–≤–∞–µ—В –≥–Є–њ–µ—А–њ—А–Њ–і—Г–Ї—Ж–Є—О –Ї–Њ–ї–ї–∞–≥–µ–љ–∞.
–°–Њ–ї–Ї–Њ—Б–µ—А–Є–ї (—Н–Ї—Б—В—А–∞–Ї—В –Ї—А–Њ–≤–Є –Ї—А—Г–њ–љ–Њ–≥–Њ —А–Њ–≥–∞—В–Њ–≥–Њ —Б–Ї–Њ—В–∞, –Њ—Б–≤–Њ–±–Њ–ґ–і–µ–љ–љ—Л–є –Њ—В –±–µ–ї–Ї–∞), –≤–≤–µ–і–µ–љ–љ—Л–є –≤–љ—Г—В—А–Є–Љ—Л—И–µ—З–љ–Њ –њ–Њ 2 –Љ–ї –≤ –і–µ–љ—М (20 – 25 –Є–љ—К–µ–Ї—Ж–Є–є –љ–∞ –Ї—Г—А—Б), —Г–ї—Г—З—И–∞–µ—В –Љ–Є–Ї—А–Њ—Ж–Є—А–Ї—Г–ї—П—Ж–Є—О –Є –∞–Ї—В–Є–≤–Є—А—Г–µ—В —В—А–Њ—Д–Є—З–µ—Б–Ї–Є–µ –њ—А–Њ—Ж–µ—Б—Б—Л –≤ –Њ—З–∞–≥–µ.
–Э–∞—А—Г–ґ–љ–Њ, –Ї—А–Њ–Љ–µ –Ф–Ь–°–Ю –Є —А–Њ–љ–Є–і–∞–Ј—Л, –њ—А–Є–Љ–µ–љ—П—О—В –њ—А–µ–њ–∞—А–∞—В—Л, —Г–ї—Г—З—И–∞—О—Й–Є–µ –Њ–±–Љ–µ–љ–љ—Л–µ –њ—А–Њ—Ж–µ—Б—Б—Л –≤ –Ї–Њ–ґ–µ –Є —Б—В–Є–Љ—Г–ї–Є—А—Г—О—Й–Є–µ —А–µ–≥–µ–љ–µ—А–∞—Ж–Є—О: —Б–Њ–ї–Ї–Њ—Б–µ—А–Є–ї (–ґ–µ–ї–µ –Є –Љ–∞–Ј—М), 2% –≥–µ–ї—М —В—А–Њ–Ї—Б–µ–≤–∞–Ј–Є–љ–∞, –Љ–∞–Ј—М –≤—Г–ї–љ—Г–Ј–∞–љ, –∞–Ї—В–Њ–≤–µ–≥–Є–љ (5% –Љ–∞–Ј—М, –ґ–µ–ї–µ), 5% –њ–∞—А–Љ–Є–і–Є–љ–Њ–≤—Г—О –Љ–∞–Ј—М. –Я—А–Є–Љ–µ–љ—П—О—В –Њ–і–љ–Њ –Є–Ј —Н—В–Є—Е —Б—А–µ–і—Б—В–≤ 2 —А–∞–Ј–∞ –≤ –і–µ–љ—М, –≤—В–Є—А–∞—П –≤ –Њ—З–∞–≥–Є –њ–Њ—А–∞–ґ–µ–љ–Є—П. –Ь–Њ–ґ–љ–Њ —З–µ—А–µ–Ј –Ї–∞–ґ–і—Г—О –љ–µ–і–µ–ї—О —З–µ—А–µ–і–Њ–≤–∞—В—М —Н—В–Є –њ—А–µ–њ–∞—А–∞—В—Л, –њ—А–Њ–і–Њ–ї–ґ–Є—В–µ–ї—М–љ–Њ—Б—В—М –ї–Њ–Ї–∞–ї—М–љ—Л—Е –∞–њ–њ–ї–Є–Ї–∞—Ж–Є–є —Б–Њ—Б—В–∞–≤–ї—П–µ—В 1 – 1,5 –Љ–µ—Б. –≠—Д—Д–µ–Ї—В–Є–≤–µ–љ –њ—А–Є –ї–µ—З–µ–љ–Є–Є –і–µ—В–µ–є, –±–Њ–ї—М–љ—Л—Е —Б–Ї–ї–µ—А–Њ–і–µ—А–Љ–Є–µ–є, —В–∞–Ї–ґ–µ –Љ–∞–і–µ–Ї–∞—Б—Б–Њ–ї. –≠—В–Њ—В –њ—А–µ–њ–∞—А–∞—В —А–∞—Б—В–Є—В–µ–ї—М–љ–Њ–≥–Њ –њ—А–Њ–Є—Б—Е–Њ–ґ–і–µ–љ–Є—П —А–µ–≥—Г–ї–Є—А—Г–µ—В –Ї–Њ–ї–Є—З–µ—Б—В–≤–µ–љ–љ–Њ–µ –Є –Ї–∞—З–µ—Б—В–≤–µ–љ–љ–Њ–µ –Њ–±—А–∞–Ј–Њ–≤–∞–љ–Є–µ —Б–Њ–µ–і–Є–љ–Є—В–µ–ї—М–љ–Њ–є —В–Ї–∞–љ–Є, —В–Њ—А–Љ–Њ–Ј–Є—В —З—А–µ–Ј–Љ–µ—А–љ–Њ–µ –Њ–±—А–∞–Ј–Њ–≤–∞–љ–Є–µ –Ї–Њ–ї–ї–∞–≥–µ–љ–∞.
–Р–і–µ–Ї–≤–∞—В–љ–Њ–µ –љ–∞—А—Г–ґ–љ–Њ–µ –ї–µ—З–µ–љ–Є–µ –≤ –Ї–Њ–Љ–±–Є–љ–∞—Ж–Є–Є —Б —Б–Њ—Б—Г–і–Њ—А–∞—Б—И–Є—А—П—О—Й–Є–Љ–Є –њ—А–µ–њ–∞—А–∞—В–∞–Љ–Є –Є–Љ–µ–µ—В –±–Њ–ї—М—И–Њ–µ –Ј–љ–∞—З–µ–љ–Є–µ –њ—А–Є –ї–µ—З–µ–љ–Є–Є –°–Р–Ы –≤—Г–ї—М–≤—Л –Є –њ–Њ–Ј–≤–Њ–ї—П–µ—В –Њ—В–Ї–∞–Ј–∞—В—М—Б—П –Њ—В –Љ–љ–Њ–≥–Њ–Ї—Г—А—Б–Њ–≤–Њ–≥–Њ –ї–µ—З–µ–љ–Є—П –њ–µ–љ–Є—Ж–Є–ї–ї–Є–љ–Њ–Љ –Є –ї–Є–і–∞–Ј–Њ–є.
–£ –±–Њ–ї—М—И–Є–љ—Б—В–≤–∞ –і–µ–≤–Њ—З–µ–Ї –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є–µ –Є–Љ–µ–µ—В –±–ї–∞–≥–Њ–њ—А–Є—П—В–љ—Л–є –Є—Б—Е–Њ–і. –Я—А–Њ—Ж–µ—Б—Б —А–∞–Ј—А–µ—И–∞–µ—В—Б—П –Є–ї–Є —Б–љ–Є–ґ–∞–µ—В—Б—П –і–Њ —Б—Г–±–Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є—Е –њ—А–Є–Ј–љ–∞–Ї–Њ–≤ –Њ–±—Л—З–љ–Њ –Ї –њ–µ—А–Є–Њ–і—Г –љ–∞—Б—В—Г–њ–ї–µ–љ–Є—П –Љ–µ–љ–∞—А—Е–µ. –Ґ–µ—З–µ–љ–Є–µ –і—А—Г–≥–Є—Е —Д–Њ—А–Љ –Ю–° –Љ–µ–љ–µ–µ –њ—А–µ–і—Б–Ї–∞–Ј—Г–µ–Љ–Њ. –°–љ–Є–ґ–µ–љ–Є–µ –∞–Ї—В–Є–≤–љ–Њ—Б—В–Є –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П, —Б—В–∞–±–Є–ї–Є–Ј–∞—Ж–Є—П —Б–Ї–ї–µ—А–Њ–і–µ—А–Љ–Є—З–µ—Б–Ї–Њ–≥–Њ –њ—А–Њ—Ж–µ—Б—Б–∞ –Є –µ–≥–Њ —А–µ–≥—А–µ—Б—Б–Є—А–Њ–≤–∞–љ–Є–µ –Њ–±—Л—З–љ–Њ –Њ—В–Љ–µ—З–∞—О—В –њ—А–Є —Г—Б–ї–Њ–≤–Є–Є —А–∞–љ–љ–µ–є –і–Є–∞–≥–љ–Њ—Б—В–Є–Ї–Є —Б–Ї–ї–µ—А–Њ–і–µ—А–Љ–Є–Є –Є —Б–≤–Њ–µ–≤—А–µ–Љ–µ–љ–љ–Њ–≥–Њ –њ—А–Њ–≤–µ–і–µ–љ–Є—П –љ–µ–Њ–±—Е–Њ–і–Є–Љ–Њ–≥–Њ –Ї–Њ–Љ–њ–ї–µ–Ї—Б–љ–Њ–≥–Њ –Ї—Г—А—Б–Њ–≤–Њ–≥–Њ –ї–µ—З–µ–љ–Є—П.
–Ы–Є—В–µ—А–∞—В—Г—А–∞:
1. –Ф–Њ–≤–ґ–∞–љ—Б–Ї–Є–є –°.–Ш. // –°–Ї–ї–µ—А–Њ–і–µ—А–Љ–Є—П. – –Ш–Ј–і.-–≤–Њ –°–∞—А–∞—В–Њ–≤—Б–Ї–Њ–≥–Њ —Г–љ–Є–≤–µ—А—Б–Є—В–µ—В–∞. – 1979. – –°. 195.
2. Gintrac M. Note sur la sclerodermie. Rev med Chir 1847;2:263–7.
3. Wienenecke R, Schliipen EM, Zochling N, et al. No evidence for Borrilia burgdorferi – specific DNA in lesions of localized scleroderma. J In vest Derm 1995;104:23–6.
4. –У—Г—Б–µ–≤–∞ –Э.–У. // –°–Ї–ї–µ—А–Њ–і–µ—А–Љ–Є—З–µ—Б–Ї–∞—П –≥—А—Г–њ–њ–∞ –±–Њ–ї–µ–Ј–љ–µ–є. – –Ґ–µ—А. –∞—А—Е. – 1988. – вДЦ8. – –°. 20–26.
5. –®–ї—П–њ–∞–Ї –Х.–Р., –Ъ—Г–Ј–љ–µ—Ж–Њ–≤ –С.–У. // –У–Њ—А–Љ–Њ–љ–∞–ї—М–љ—Л–µ —Б–і–≤–Є–≥–Є —Г –±–Њ–ї—М–љ—Л—Е —Б–Ї–ї–µ—А–Њ–і–µ—А–Љ–Є–µ–є –і–µ—В–µ–є –≤ –њ—А–Њ—Ж–µ—Б—Б–µ –Ї—Г—А–Њ—А—В–љ–Њ–≥–Њ –ї–µ—З–µ–љ–Є—П // –Т–Њ–њ—А–Њ—Б—Л –Ї—Г—А–Њ—А—В–Њ–ї., —Д–Є–Ј–Є–Њ—В–µ—А. –Є –ї–µ—З. —Д–Є–Ј–Ї—Г–ї—М—В—Г—А—Л. – 1985. – 6. – –°. 40–42.
6. Jablonska S, Bubnow B, Lukusiak. Auswertung von Chronaxie messungen bei Scherodermie. Derm Wschir 1957; 136(31): 831–37.
7. Medsger TA. Systemic sclerosis (scleroderma); eosinophilic fuseiitis and calanosis. In: McCarty D.J., editor. Arthritis and Allied Conditions, 11 th edition. Philadelphia: Lea & Febiger 1989;1118–65.
8. Korn J.H. // Immunologic aspects of scleroderma. – Curr. Opur Rheumatol, 1991; 3: 947–52.
9. Ferri C, Bernini L, Cecchetti R, et al. Cutaneous and serological subsets of systemic sclerosis. Their relevance in diagnosis, severity and prognosis of the disease. J Rheumatol 1991;18:1826–32.
10. Steen V. Treatment of Systemic sclerosis. Curr Opin Rheum 1991;3:979–85.
11. –Я–µ—В—А–Њ–≤ –†.–Т. // –Ш–Љ–Љ—Г–љ–Њ–ї–Њ–≥–Є—П –Є –Є–Љ–Љ—Г–љ–Њ–≥–µ–љ–µ—В–Є–Ї–∞. – –Ь. – 1976.
12. –Т–ї–∞–і–Є–Љ–Є—А—Ж–µ–≤ –Т.–Р., –Р–≤–і–µ–µ–≤–∞ –Ц.–Ш., –У—Г—Б–µ–≤–∞ –Э.–У. –Є –і—А. // –Ш–Ј—Г—З–µ–љ–Є–µ –Ї–ї–µ—В–Њ—З–љ–Њ–≥–Њ –Є–Љ–Љ—Г–љ–љ–Њ–≥–Њ –Њ—В–≤–µ—В–∞ –љ–∞ –Ї–Њ–ї–ї–∞–≥–µ–љ I —В–Є–њ–∞ —Г –±–Њ–ї—М–љ—Л—Е —Б–Є—Б—В–µ–Љ–љ–Њ–є —Б–Ї–ї–µ—А–Њ–і–µ—А–Љ–Є–µ–є. – –Т–Њ–њ—А. —А–µ–≤–Љ–∞—В. – 1982. – I. – –°. 33–38.
13. –Ъ–∞–ї–∞–Љ–Ї–∞—А—П–љ –Р.–Р., –Ф–Њ–ї–±–Є–љ –Р.–У., –§–µ–і–Њ—А–Њ–≤–∞ –Х.–У., –Ч–∞—А–µ—Ж–Ї–∞—П –Ѓ.–Ь. // –Р–љ—В–Є–≥–µ–љ—Л HLA —Г –±–Њ–ї—М–љ—Л—Е –Њ—З–∞–≥–Њ–≤–Њ–є —Б–Ї–ї–µ—А–Њ–і–µ—А–Љ–Є–µ–є – –∞—В—А–Њ—Д–Њ–і–µ—А–Љ–Є–µ–є –Я–∞–Ј–Є–љ–Є – –Я—М–µ—А–Є–љ–Є. – –Ь–∞—В–µ—А. –њ–ї–µ–љ—Г–Љ–∞ –Т—Б–µ—Б–Њ—О–Ј–љ. –і–µ—А–Љ–∞—В–Њ–≤–µ–љ–µ—А–Њ–ї–Њ–≥–Њ–≤. – –Ь. – 1977.
14. –°—Г—З–Ї–Њ–≤–∞ –Ґ.–Э. // –Э–∞—А—Г—И–µ–љ–Є–µ –Ґ-–Ї–ї–µ—В–Њ—З–љ–Њ–≥–Њ –Є–Љ–Љ—Г–љ–Є—В–µ—В–∞ —Г –±–Њ–ї—М–љ—Л—Е –Њ—З–∞–≥–Њ–≤–Њ–є —Б–Ї–ї–µ—А–Њ–і–µ—А–Љ–Є–µ–є // –Т–µ—Б—В–љ. –і–µ—А–Љ–∞—В–Њ–ї. – 1986. – II. – –°. 12–16.
15. –§–µ–і–Њ—А–Њ–≤–∞ –Х.–У. // –Ъ–Њ–ї–Є—З–µ—Б—В–≤–µ–љ–љ–∞—П –Њ—Ж–µ–љ–Ї–∞ –њ–Њ–њ—Г–ї—П—Ж–Є–є –Ґ-, –Т-, –љ—Г–ї–µ–≤—Л—Е –ї–Є–Љ—Д–Њ—Ж–Є—В–Њ–≤ —Г –±–Њ–ї—М–љ—Л—Е –Њ—З–∞–≥–Њ–≤–Њ–є —Б–Ї–ї–µ—А–Њ–і–µ—А–Љ–Є–µ–є // –Т–µ—Б—В–љ. –і–µ—А–Љ–∞—В–Њ–ї. – 1980. – 6. – –°. 17–19.
16. –С—Г—В–Њ–≤ –Ѓ.–°. // –Р–љ—В–Є–љ—Г–Ї–ї–µ–∞—А–љ—Л–µ –∞–љ—В–Є—В–µ–ї–∞ —Г –±–Њ–ї—М–љ—Л—Е —Б–Є—Б—В–µ–Љ–љ—Л–Љ–Є –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П–Љ–Є // –Т–µ—Б—В–љ. –і–µ—А–Љ–∞—В–Њ–ї. – 1980. – II. – 17–21.
17. –°—Г–≤–Њ—А–Њ–≤ –Р.–Я., –Ч–∞–≤—М—П–ї–Њ–≤ –Р.–Ш., –У—А–∞—И–Ї–Є–љ–∞ –Ш.–У. // –Ю–≥—А–∞–љ–Є—З–µ–љ–љ–∞—П —Б–Ї–ї–µ—А–Њ–і–µ—А–Љ–Є—П. – –Ь–µ—В–Њ–і–Є—З. —А–µ–Ї–Њ–Љ–µ–љ–і–∞—Ж., –°–∞—А–∞—В–Њ–≤. – 1990. – –°. 25.
18. Sonnichsen N. Vergleichende Unier suchuiigen zur pathogenese der Lupuserythematodes, der Scherodermic and der Dermatomyasitis – Dtsch Gesundheitswes 1983;39(14):526–30.
19. –У–∞–љ—З–µ–≤ –С. // –Ф–µ—А–Љ–∞—В–Њ-–≤–µ–љ–µ—А–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–∞—П —В–µ—А–Љ–Є–љ–Њ–ї–Њ–≥–Є—П. –°–Њ—Д–Є—П. – 1968.
20. Jablonska S. Classification of Scleroderma. Clinic in Dermatology 1994;12(2):225–8.
21. –£–≤–∞—А–Њ–≤–∞ –Э.–Э. // –Ъ–ї–Є–љ–Є—З–µ—Б–Ї–∞—П –Ї–∞—А—В–Є–љ–∞ –Є —В–µ—З–µ–љ–Є–µ —Б–Є—Б—В–µ–Љ–љ–Њ–є —Б–Ї–ї–µ—А–Њ–і–µ—А–Љ–Є–Є —Г –і–µ—В–µ–є. – –Р–≤—В–Њ—А–µ—Д. –і–Є—Б. –і–Њ–Ї—В. –Љ–µ–і. –љ–∞—Г–Ї. – –Ь. – 1989. – –°. 47.
22. –Т–ї–∞—Б–Њ–≤–∞ –Ґ.–Ь. // –Ю—Б–Њ–±–µ–љ–љ–Њ—Б—В–Є –Њ–≥—А–∞–љ–Є—З–µ–љ–љ–Њ–є —Б–Ї–ї–µ—А–Њ–і–µ—А–Љ–Є–Є —Г –і–µ—В–µ–є –Є –≤–Њ–Ј–Љ–Њ–ґ–љ–∞—П —Б–≤—П–Ј—М –µ–µ —Б —Б–Є—Б—В–µ–Љ–љ–Њ–є —Б–Ї–ї–µ—А–Њ–і–µ—А–Љ–Є–µ–є. – –Р–≤—В–Њ—А–µ—Д. –і–Є—Б. –Ї–∞–љ–і. –Љ–µ–і. –љ–∞—Г–Ї. – –Ь. – 1984. – –°. 26.
23. –Э–Є–Ї–Є—В–Є–љ–∞ –Ь.–Э. // –Ю–≥—А–∞–љ–Є—З–µ–љ–љ–∞—П —Б–Ї–ї–µ—А–Њ–і–µ—А–Љ–Є—П —Г –і–µ—В–µ–є. –Т–Њ–њ—А–Њ—Б—Л –Ї–ї–Є–љ–Є–Ї–Є, –њ–∞—В–Њ–≥–µ–љ–µ–Ј–∞ –Є –ї–µ—З–µ–љ–Є—П. – –Р–≤—В–Њ—А–µ—Д. –і–Є—Б. –і–Њ–Ї—В. –Љ–µ–і. –љ–∞—Г–Ї. – –Ь. – 1980. – –°. 37.












