Псориаз – мультифакторное заболевание с наследственной предрасположенностью, характеризующееся повышенной пролиферацией эпидермальных клеток, нарушением кератинизации и воспалительной реакци-ей в дерме, обусловленной активированными Т-лимфоцитами и синтезом провоспалительных цитокинов [3].
Бляшковидный псориаз – самая распространенная форма ювенильного псориаза, она встречается примерно у 75% детей и подростков с псориазом. Клинические проявления ювенильного псориаза могут отличаться от таковых у взрослых. У детей бляшки в основном располагаются на коже головы, заушной области, на локтях и коленях [13, 17, 27, 32]. Бляшки эритематозные с серебристыми чешуйками, тоньше, чем псориатические бляшки у взрослых. Линия волос и затылочная область – часто первое место поражения у детей [21, 26].
Хотя большинство случаев псориаза в детском возрасте считаются легкими, психосоциальные последствия данной патологии у детей и подростков могут быть глубокими. Поэтому для клиницистов очень важна оценка влияния псориаза на психологическое состояние детей и подростков. Даже легкие формы псориаза могут повлиять на детскую психосоциальную адаптацию и качество жизни [5, 12, 13, 26]. Бляшки на коже головы и возможная ассоциированная алопеция могут причинять дискомфорт в подростковом возрасте и оказать пагубное влияние на формирование личности в период полового созревания [26]. Эффективная терапия может помочь смягчить некоторые из этих эффектов. Основными целями лечения являются уменьшение клинических проявлений заболевания, снижение частоты реци-дивов, устранение отрицательных субъективных ощущений, улучшение качества жизни больного, снижение риска развития коморбидных заболеваний [3].
Терапия псориаза в подростковом возрасте имеет свои сложности. В настоящее время нет международных стандартизированных рекомендаций для лечения детского псориаза, доказательные данные, полученные в рандомизированных контролируемых исследованиях, также весьма ограниченны. Терапия основывается в первую очередь на опубликованных случаях лечения псориаза, рекомендациях для лечения у взрослых и опыте работы с этими препаратами при других заболеваниях у детей. Несмотря на различия между течением псориаза у взрослых и детей, используемое лечение не имеет существенных отличий. Большинство детей и подростков страдают псориазом легкой степени тяжести. Таким образом, у них используется местная терапия, которая рассматривается как терапия первой линии, так же как и у взрослых [8, 18, 26].
Топическая терапия может быть безопасной и эффективной в лечении ювенильного псориаза. К наиболее часто назначаемым препаратам относятся кортикостероиды, аналоги витамина D в сочетании или без кортикостероидов, лечебные шампуни, ингибиторы кальциневрина. Многие режимы включают комбинированную терапию. Выбор лекарственной формы и дозировки зависит от возраста, степени и тяжести заболевания, локализации псориаза, характера повреждения и предпочтений пациента. Имеющиеся в распоряжении формы выпуска включают в себя кремы, мази, пены, гели и лосьоны [8, 26].
Топические кортикостероиды
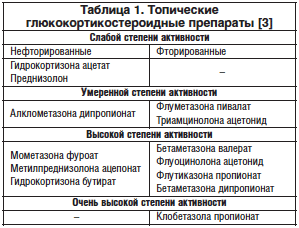
Топические кортикостероиды остаются препаратами первой линии для лечения псориаза среди подростков, так же как и среди всех других возрастных групп [18]. Эта группа препаратов применяется при любых формах псориаза в качестве монотерапии или в комбинации с другими наружными или системными средствами [3]. Доступен широкий выбор стероидов в зависимости от силы воздействия (табл. 1) и лекарственной формы. В зависимости от характера и локализации псориатических высыпаний топические глюкокортикостероидные препараты применяются в виде различных лекарственных форм – мазей, кремов или лосьонов [3, 8].
Эффективность топических глюкокортикостероидных средств имеет высокий уровень доказательности [3]. Нет исследований, непосредственно сравнивающих отдельные топические кортикостероиды, но систематические обзоры доказывают, что большинство препаратов приводят к значительному уменьшению симптомов псориаза. Эффективность этих препаратов при лечении псориаза основана на выраженном противовоспалительном и иммуномодулирующем действии, связанном с механизмом гормонорецепторного комплекса, который проникает в ядро клетки-мишени кожи и увеличивает экспрессию генов, кодирующих синтез пептидов, ингибирующих активность фосфолипазы. Этот механизм приводит к снижению образования медиаторов воспаления из фосфолипидов. В конечном итоге топические кортикостероиды уменьшают эритему, шелушение и зуд [2, 26]. Они являются относительно востребованными препаратами у пациентов, потому что они легко наносятся на кожу, не обладают сильным запахом, не окрашивают кожу и одежду, имеют быстрое начало действия [18].
Топические глюкокортикостероиды были одобрены для лечения кортикостероид-чувствительных дерматозов у детей и подростков, но их использование в этой возрастной группе имеет свои особенности. Дети имеют более высокую абсорбцию топических препаратов, обусловленную большей мощностью кожной пенетрации и большей площадью всасывания, чем у взрослых. Поэтому у детей могут чаще, чем у взрослых пациентов, встречаться местные и системные побочные эффекты, связанные с применением топических глюкокортикостероидов. Таким образом, применение данных препаратов у детей должно тщательно мониторироваться [26]. Для предупреждения системных побочных эффектов нужно придерживаться следующих правил использования данных препаратов:
1. Топические глюкокортикостероидные препараты рекомендуется назначать короткими интермиттирующими курсами, избегая длительного применения.
2. В детском возрасте лечение следует начинать с топических глюкокортикостероидов слабой или средней степени активности.
3. У детей первых лет жизни не рекомендуется применять топические глюкокортикостероиды на участках с тонкой кожей, таких как лицо, половые органы, сгибательные поверхности, а также назначать фторсодержащие препараты.
4. При наличии проявлений вторичной инфекции необходимо использовать топические комбинированные глюкокортикостероиды, содержащие антибактериальные и противогрибковые средства.
Обычно лечение топическими глюкокортикостероидными препаратами предполагает их ежедневные аппликации 1–2 р./сут в течение 3–4 нед. При уменьшении выраженности симптомов можно сократить кратность применения глюкокортикостероидов или назначить лечение другими средствами наружной терапии [3].
При лечении топическими кортикостероидами могут развиваться местные побочные эффекты, включающие в себя атрофию кожи, раздражение, плохое заживление ран, телеангиэктазии, угревую сыпь и тахифилаксию [18, 23]. Тахифилаксия определяется как потеря эффективности при длительном использовании топических стероидов, и, хотя она не была описана ни в одном исследовании (вероятно, из-за короткой продолжительности исследований), все же это должно быть принято во внимание при назначении данной группы препаратов. Кроме того, остается спорным, относится ли потеря эффективности со временем к тахифилаксии или это отражение ухудшения комплаентности, что, как правило, характеризует пациентов-подростков [18]. Атрофия кожи чаще развивается на коже лица, паховой области и складок. При длительном применении кортикостероидов, особенно с высокой активностью или при нанесении их на большую поверхность кожи, может наблюдаться системное действие препаратов, которое приводит к подавлению функции коры надпочечников. В связи с этим предпочтение следует отдавать препаратам с минимальной системной биодоступностью (например, мометазона фуроат обладает минимальной биодоступностью – из крема 0,4%, из мази – 0,7% нанесенной дозы). Частота развития побочных реакций зависит от локализации очагов поражения, активности кортикостероидов, лекарственной формы и длительности лечения [3].
Топические кортикостероиды, как правило, комбинируют с другими местными препаратами, такими как кератолитики (салициловая кислота), аналоги витамина D, как по отдельности, так и в фиксированных комбина-циях, или они могут назначаться в сочетании с системным лечением [18].
Топические аналоги витамина D
Топические аналоги витамина D – кальципотриен (синтетическая форма витамина D3, иногда называется кальципотриолом) и кальцитриол (1,25-дигидрокси-D3) обладают кератопластическим эффектом. Они стиму-лируют эпидермальную дифференциацию и подавляют пролиферацию кератиноцитов. Также обладают иммуномодулирующим эффектом, в частности уменьшая экспрессию ИЛ-2 и ИНФ-γ [2, 26].
Кальципотриен и кальцитриол используются как в виде монотерапии, так и в комбинации с фототерапией для лечения псориаза у пациентов с пораженной поверхностью от 5 до 20%. Эти препараты имеют более медленное начало действия, но более длинный период ремиссии, чем топические кортикостероиды. В отличие от топических стероидов возможно длительное применение данной группы препаратов. Возможно проведение повторных курсов лечения при последующих обострениях. Продолжительность лечения по интермиттирующей схеме не должна превышать 1 года [2, 3, 15, 22, 23].
После кортикостероидов кальципотриол – это самый часто назначаемый лекарственный препарат местного применения для лечения ювенильного псориаза. Согласно недавно проведенному в США исследованию, кальципотриол был вторым самым назначаемым лекарственным препаратом для лечения псориаза у детей на протяжении почти 30 лет (1979–2007). Кроме того, систематический обзор всех методов лечения псориаза у детей рекомендует кальципотриен и кальцитриол как эффективные и хорошо переносимые препараты (уровень доказательности А и В соответственно) [14, 18, 35]. Исследования показали в некоторых случаях даже значительное клиническое улучшение с незначительными побочными эффектами при лечении псориаза легкой или средней степени тяжести у детей и подростков кальципотриеном.
Кальципотриен был одобрен FDA для лечения псориаза у взрослых в 1993 г. [26]. Хотя нет официального одобрения для их использования при ювенильном псориазе, их эффективность документально и научно обоснована [18]. Местное раздражение кожи и зуд – наиболее распространенные побочные эффекты, и поэтому нужно избегать использования этих препаратов на участках с тонкой кожей, таких как лицо, кожные складки и половые органы [8, 30]. Также аналоги витамина D3 не следует наносить на непораженные участки кожи. При возникновении раздражения кожи целесообразно снизить кратность аппликаций или прервать терапию [3]. Серьезные нежелательные побочные эффекты, такие как гиперкальциемия и супрессия паратгормона, были зарегистрированы при использовании сверхтерапевтических доз и у пациентов с почечной недостаточностью [16, 23]. Системная абсорбция витамина D и повышение уровня кальция могут теоретически иметь место, но это маловероятно, если препараты используются должным образом [29]. Использование в дозе до 45 г/м2/нед. у педиатрических пациентов с псориазом, по мнению исследователей, не влияет на уровень кальция у детей от 3 до 14 лет [11, 25]. Аналоги витамина D не рекомендуется использовать у детей в возрасте до 2 лет [8].
Хотя аналоги витамина D могут использоваться в виде монотерапии, они часто назначаются в комбинации с топическими кортикостероидами, приводя к лекарственному синергизму и стероидсберегающему эффекту [8, 33, 34]. Для того чтобы избежать отдельного нанесения препаратов и для увеличения комплаентности пациента, был разработан комбинированный препарат, содержащий кальципотриол и бетаметазона пропионат [8]. Данная комбинация имеет различные лекарственные формы. Это мазьи гель для наружного применения, используемый для лечения как псориаза волосистой части головы, так и псориаза легкой и средней степени тяжести других частей тела. Комбинированные топические препараты обладают благоприятными клиническими характеристиками, обеспечивающими благоприятный профиль переносимости. Используемый в качестве основы мази 5% стеариловый эфир 15-полиоксипропилена обеспечивает оптимальную доставку активных компонентов в кожу. В этой основе хорошо растворяются как кальципотриол, так и бетаметазон. Она повышает проницаемость кожи для действующих веществ и гарантирует их высокую устойчивость [1, 26].
В 3-х исследованиях описываются эффективность и безопасность этого препарата у детей с псориазом [8, 20, 24]. В проспективном исследовании 73 детям (в возрасте от 3 до 18 лет) с простым псориазом проводилась терапия мазью кальципотриол/бетаметазона пропионат 1 р./сут 4 нед. и 4 дня в неделю после этого со средней продолжительностью лечения 35 нед. Наибольший эффект от использования мази кальципотриол/бетаметазона пропионат был достигнут в течение первых недель. Непрерывное лечение способствует стабилизации псориаза у этих детей. У 5 пациентов отмечались побочные эффекты, наиболее часто в виде появления стрий. Многоцентровое открытое исследование, проведенное М. Gooderham et al., показало хорошую переносимость и эффективность геля кальципотриол/бетаметазона пропионат при однократном нанесении в течение 8 нед. у подростков (в возрасте от 12 до 17 лет) с бляшковидным псориазом средней степени тяжести и тяжелым. Также было показано, что упрощение схемы лечения и улучшение способа доставки препарата могут увеличить приверженность пациентов к лечению и его эффективность у подростков.
А.М. Oostveen et al. продемонстрировали эффективность кальципотриена/бетаметазона пропионата геля у детей с псориазом кожи головы (пациенты в возрасте от 4 до 17 лет) в течение первых 12 нед. лечения (84 эпизода терапии) с сохранением этих эффектов в течение 48 нед. Стрии на коже (руки, туловище, ноги) были описаны у 3-х пациентов [8, 20, 24].
При проведении терапии аналогами витамина D3 нужно учитывать особенности их взаимодействия с другими препаратами. Одновременное наружное применение препаратов салициловой кислоты приводит к инак-тивации аналогов D3. Следует избегать сочетанного назначения других лекарственных средств, вызывающих раздражение кожи. При комбинированной системной терапии препаратами кальция, витамина D3, тиазидами возможно повышение уровня кальция в крови [3].
Ингибиторы кальциневрина
Данная группа препаратов ингибирует фермент кальциневрин, который, в свою очередь, блокирует производство и выпуск интерлейкина (IL)-2, цитокина, участвующего в патогенезе псориаза [10,18]. У взрослых доказана эффективность такролимуса (0,03% и 0,1%) и пимекролимуса (1%) при псориатических поражениях на лице, сгибательных поверхностях и половых органах с меньшим развитием атрофии кожи по сравнению с топическими кортикостероидами. Ингибиторы кальциневрина являются хорошей альтернативой топическим стероидам для лечения псориаза этой локализации из-за риска развития побочных эффектов при длительном использовании данной группы препаратов [8, 36]. Такролимус превосходит пимекролимус в уменьшении симптомов псориаза. Такролимус 0,03% и 0,1% (для детей 2–15 лет и старше 15 лет соответственно), а также пимекролимус 1% официально одобрены для прерывистого лечения атопического дерматита, но не для лечения псориаза у детей. В повседневной практике они часто используются для лечения псориаза на участках с высоким риском атрофии кожи, таких как лицо, половые органы и сгибательные поверхности [18]. Эффективность и безопасность такролимуса 0,1%, применяемого 2 р./сут у детей с псориазом, оценивалась в двух нерандомизированных клинических исследованиях. Все пациенты отмечали очищение кожи или значительное улучшение при использовании мази такролимуса в течение первых 30 дней лечения. Нежелательная побочная реакция в виде зуда была выявлена только у одного пациента [8, 9, 31]. В настоящее время нет достаточных доказательств для использования пимекролимуса у детей с псориазом, т. к. было описано всего 2 случая [14]. Хотя сообщения о зарегистрированных нежелательных побочных эффектах являются редкостью, эти препараты могут вызвать малигнизацию кожи и лимфому. В связи с этим необходимо избегать сопутствующей фототерапии и чрезмерного пребывания на солнце [8].
Таким образом, псориаз является хроническим дерматологическим заболеванием, которое может начаться в детстве или подростковом возрасте. Лечение псориаза не приводит к стойкому выздоровлению, и, следовательно, главная цель терапии – это установление контроля над заболеванием и достижение длительных периодов ремиссии. Местная терапия является основой лечения у подростков, так же как и у взрослых. Достижения в терапии улучшили прогноз для лечения ювенильного псориаза. Топические препараты аналогов витамина D и кортикостероиды являются первой линией лечения псориаза с учетом некоторых проблем безопасности.
Литература
1. Кочергин Н. Г., Смирнова Л. М. Последние тренды в лечении псориаза // Лечащий врач. 2011. № 5.
2. Олисова О.Ю., Теплюк Н.П., Пинегин В.Б. Современные методы лечения псориаза// РМЖ. 2015. № 9. С. 483–486.
3. Федеральные клинические рекомендации по ведению больных псо-риазом. Российское общество дерматовенерологов и косметологов. М., 2013.
4. Augustin M., Glaeske G., Radtke M.A. et al. Epidemiology and comorbidi-ty of psoriasis in children // Br. J. Dermatol. 2010. Vol.162. P. 633–636.
5. Beattie P.E., Lewis-Jones M.S. A comparative study of impairment of quality of life in children with skin disease and children with other chronic childhood diseases // Br. J. Dermatol. 2006. Vol. 155. P. 145–151.
6. Benoit S., Hamm H. Childhood psoriasis // Clin. Dermatol. 2007. Vol. 25. P. 555–562.
7. Bhutani T., Kamangar F., Cordoro K.M. Management of pediatric psoriasis // Pediatr. Ann. 2012. Vol. 41(1). P. e1–7.
8. Bronckers I.M., Paller A.S., van Geel M.J. et al. Psoriasis in Children and Adolescents: Diagnosis, Management and Comorbidities // Paediatr. Drugs. 2015. Jun 14. 9. Brune A., Miller D.W., Lin P. et al. Tacrolimus ointment is effective for psoria-sis on the face and intertriginous areas in pediatric patients // Pediatr. Derma-tol. 2007. Vol. 24(1). P. 76–80.
10. Cordoro K.M. Management of childhood psoriasis // Adv. Dermatol. 2008. Vol. 24. P.125–169.
11. Darley C.R., Cunliffe W.J., Green C.M. et al. Safety and efficacy of cal-cipotriol ointment (Dovonex) in treating children with psoriasis vulgaris // Br. J. Dermatol. 1996.Vol. 135(3). P. 390–393.
12. de Jager M.E., de Jong E.M., Evers A.W. et al. The burden of childhood psoriasis // Pediatr. Dermatol. 2011. Vol. 28. P. 736–737.
13. de Jager M.E., de Jong E.M., van de Kerkhof P.C. et al. Anintrapatient comparison of quality of life in psoriasis in childhood and adulthood // J. Eur. Acad. Dermatol. Venere-ol. 2011. Vol. 25. P. 828–831.
14. de Jager M.E., de Jong E.M., van de Kerkhof P.C., Seyger M.M. Efficacy and safety of treatments for childhood psoriasis: a systematic literature review // J. Am. Acad. Dermatol. 2010. Vol. 62. P. 1013–1030.
15. Del Rosso J.Q., Kim G.K. The rationale behind topical vitamin D analogs in the treat-ment of psoriasis: where does topical calcitrol fit in? // J. Clin. Aes-thetic. Derm. 2010. August. http://www.jcadonline.com/the-rationale-behind-topical-vitamin-d-analogs-in-the-treatment-of-psorias.... Accessed May 8, 2012.
16. Drugdex system. http://thomsonreuters.com/products_services/health care/healthcare_products/a-z/drugdex_system/. Accessed May 8, 2012
17. Fan X., Xiao F.L., Yang S. et al. Childhood psoriasis: a study of 277 pa-tients from China // J. Eur. Acad. Dermatol. Venereol: JEADV. 2007. Vol. 21(6). P. 762–765.
18. Fotiadou C., Lazaridou E., Ioannides D. Management of psoriasis in adolescence // Adolescent Health, Medicine and Therapeutics. 2014. Vol. 5. P. 25–34.
19. Fox F.E., Rumsey N., Morris M. «Ur skin is the thing that everyone sees and you cant change it!»: exploring the appearance-related concerns of young people with psoriasis // Dev. Neurorehabil. 2007. Vol. 10. P. 133–141.
20. Gooderham M., Debarre J.M., Keddy-Grant J. et al. Safety and efficacy of calcipotriol plus betamethasone dipropionate gel in the treatment of scalp pso-riasis in adolescents 12–17 years of age // Br. J. Dermatol. 2014. Vol. 171(6). P. 1470–1477.
21. Kumar B., Jain R., Sandhu K. et al. Epidemiology of childhood psoriasis: a study of 419 patients from northern India // Int. J. Dermatol. 2004. Vol. 43(9). P. 654–658.
22. Menter A., Korman N.J., Elmets C.A. et al. American Academy of Der-matology. Guidelines of care for the management of psoriasis and psoriatic ar-thritis. Section 3. Guidelines of care for the management and treatment of pso-riasis with topical therapies // J. Am. Acad. Dermatol. 2009. Vol. 60(4). P. 643–659.
23. Weigle N., McBane S. Psoriasis // Am. Fam. Physician. 2013. Vol. 87, № 9. P. 626–633.
24. Oostveen A.M., de Jong E.M., Donders A.R. et al. Treatment of paediat-ric scalp psoriasis with calcipotriene/betamethasone dipropionate scalp for-mulation:effectiveness, safety and influence on children’s quality of life in daily practice // J. Eur. Acad. Dermatol. Venereol: JEADV. 2015. Vol. 29(6). P. 1193–1197.
25. Oranje A.P., Marcoux D., Svensson A. et al. Topical calcipotriol in childhood psoriasis // J. Am. Acad. Dermatol. 1997. Vol. 36(2 Pt 1). P. 203–208.
26. Osier E., Gomez B., Eichenfield L.F. Adolescent Scalp Psoriasis: Update on Topical Combination Therapy // J. Clin. Aesthet. Dermatol. 2015. Vol. 8(7). P. 43–47. 27. Perman M.J., Lovell D.J., Denson L.A. et al. Five cases of anti-tumor necrosis factor alpha-induced psoriasis presenting with severe scalp involvement in chil-dren // Pediatr Dermatol. 2012. Vol. 29(4). P. 454–459.
28. Raychaudhuri S.P., Gross J. A comparative study of pediatric onset pso-riasis with adult onset psoriasis // Pediatr Dermatol. 2000. Vol. 17. P.174–178.
29. Silverberg N.B. Pediatric psoriasis: an update // Ther. Clin. Risk Manag. 2009. Vol.5. P. 849–856.
20. Stahle M., Atakan N., Boehncke W.H. et al. Juvenile psoriasis and its clinical management: a European expert group consensus // J. Ger. Soc. Dermatol. 2010. Vol. 8(10). P. 812–818. 31. Steele J.A., Choi C., Kwong P.C. Topical tacrolimus in the treatment of inverse psoriasis in children // J. Am. Acad. Dermatol. 2005. Vol. 53(4). P. 713–716.
32. Tollefson M.M., Crowson C.S., McEvoy M.T., Maradit K.H. Incidence of psoriasis in children: a population-based study // J. Am. Acad. Dermatol. 2010. Vol. 62. P. 979–987.
33. Tollefson M.M. Diagnosis and management of psoriasis in children // Pediatr. Clin. North Am. 2014. Vol. 61. P. 261–277.
34. van de Kerkhof P.C., Hoffmann V., Anstey A. et al. A new scalp formu-lation of calcipotriol plus betamethasone dipropionate compared with each of its active ingredients in the same vehicle for the treatment of scalp psoriasis: a randomized, double-blind, controlled trial // Br. J. Dermatol. 2009. Vol. 160(1). P. 170–176.
35. Vogel S.A., Yentzer B., Davis S.A. et al. Trends in pediatric psoriasis outpatient health care delivery in the United States // Arch. Dermatol. 2012. Vol. 148. P. 66–71.
36. Wang C., Lin A. Efficacy of topical calcineurin inhibitors in psoriasis // J. Cutan. Med. Surg. 2014. Vol. 18(1). P. 8–14.












