Одним из главных вопросов, обсуждаемых в литературе по поводу acne tarda, является возраст пациентки, с которого мы можем говорить о диагнозе поздних акне. Большинство отечественных и зарубежных специалистов сходятся во мнении, что это возраст 25 лет, в независимости от того, был ли это дебют заболевания или это постоянно рецидивирующие длительно существующие угревые высыпания, продолжающиеся с подросткового периода. У большинства женщин с acne tarda (около 80%, по разным данным) – это непрерывное (персистирующее) течение акне, начиная с пубертатного периода; реже встречаются акне позднего дебюта, возникающие после 25 лет и старше (20–40% случаев), и, наконец, наиболее редкая форма поздних акне – рецидивирующие акне или акне со «светлым промежутком», дебютирующие в подростковом возрасте, которые характеризуются длительным периодом ремиссии и вновь появляются в зрелом возрасте [1,7,8].
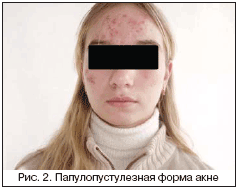
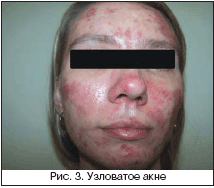
Среди клинических проявлений УБ у женщин наиболее распространена папулопустулезная форма – у 70–80% больных акне, комедональная форма и самое тяжелое проявление акне – конглобатные угри – встречаются у 15–20% больных. В отличие от подростковых угрей, характеризующихся, как правило, распространенностью патологического процесса, преобладанием среднетяжелых и тяжелых форм заболевания, при поздних акне у большинства больных диагностируется комедональная (рис. 1) и папулопустулезная форма заболевания (рис. 2). Процесс локализуется в основном в области лица, реже – в области верхней трети туловища, тяжелые узловато–кистозные акне (рис. 3) встречаются редко. Следует также отметить, что у больных с поздними формами акне помимо угревых высыпаний отмечаются признаки обезвоживания кожи вследствие предшествующего медикаментозного лечения, нерационального базисного ухода, а также фоновых возрастных изменений кожи. Было обнаружено, что у пациенток с поздними акне местное или системное применение антибиотиков, как правило, оказывается малоэффективным, по данным R. Rivera, A. Guerra, 82% женщин нечувствительны к антибиотикотерапии. Длительное торпидное течение и нерациональная терапия заболевания часто приводят к проявлениям постакне: рубцовым изменениям и поствоспалительной гиперпигментации [2,8–11].
Проведенные исследования показали, что развитие и течение дерматоза во многом зависит от семейной (генетической) предрасположенности, а также от типа, цвета кожи и национальных особенностей. Акне – это заболевания с высоким семейным накоплением (50%). Прослеживается общая закономерность: чем чаще встречается и тяжелее протекает акне у предшествующих родственников, тем более тяжелое и торпидное течение заболевания будет у потомства. Акне реже развивается и протекает в более легкой форме у японцев и китайцев, в то время как у кавказских народов отмечаются высокая частота встречаемости и более тяжелое течение дерматоза. По данным К.Н. Суворовой и соавт., различная экспрессивность и аллельные вариации генов, детерминирующих развитие сальных желез, их функциональная способность и активность ферментов могут играть большую роль в развитии акне и в значительной степени определяют тяжесть клинических проявлений. Имеются также сообщения о наличии ядерного R–фактора, определяющего генетическую предрасположенность. Этими фактами, вероятно, можно объяснить развитие у одних людей легких, а у других – тяжелых форм заболевания. В исследованиях Y. Pang, обследовавшего 238 пациентов с угревыми высыпаниями и 207 здоровых лиц, было обнаружено, что короткая длина повторения гена CAG и специфические галотипы андрогенного рецептора связаны с риском развития акне и, следовательно, могут рассматриваться как достоверный маркер предрасположенности к акне [11–14].
Известно, что кожа человека, и прежде всего ее придатки: волосяные фолликулы, сальные и потовые железы, – имеют стероидчувствительные рецепторы, которые воспринимают гормонрегулирующие влияния на развитие и секреторную активность этих структур. В период полового созревания эти взаимодействия впервые начинают себя активно проявлять. Основными кожными мишенями для половых стероидов являются эпидермис, волосяные фолликулы, сальные железы, меланоциты и фибробласты. Немецкий ученый С. Шмитц назвал кожу самой большой эндокринной железой в организме человека. Кожа принимает активное участие в метаболизме стероидных половых гормонов, в частности в экстрагландулярном образовании андрогенов из стероидов–предшественников, являясь одновременно основной тканью–мишенью для андрогенов. Кожа является периферическим звеном метаболизма мужских половых гормонов, их действие осуществляется через специфические андрогенные рецепторы (АР), которые обнаруживаются в различных андрогензависимых структурах кожи. Стимуляция АР повышает митотическую активность и дифференцировку клеток эпидермиса, увеличивает синтез межклеточных липидов, стимулирует рост волос и секрецию кожного сала [15,16].
По современным представлениям, в патогенезе акне ведущее значение отводится четырем факторам. Инициальным звеном является наследственно обусловленная гиперандрогения (ГА). ГА может проявляться в виде абсолютного увеличения количества андрогенов яичникового или надпочечникового происхождения в крови и при экскреции с мочой и подразделяется на надпочечниковую, овариальную и смешанную. Изменения в яичниках и надпочечниках могут быть как опухолевыми, так и функциональными (синдром поликистозных яичников, неклассическая форма врожденной дисфункции коры надпочечников). В ряде исследований была выявлена важная роль стероидных гормонов у женщин с поздними акне. Так, Н. Seirafi и соавт. отметили ключевую роль ДГЭА–С (андрогена надпочечникового происхождения) в патогенезе acne tarda у женщин старше 25 лет, в другом исследовании было выявлено большое значение 17–ОНП (гормона, вырабатывающегося как в яичниках, так и надпочечниках) в развитии торпидных акне у женщин [17–20].
При отсутствии повышения уровня основных андрогенов в плазме крови, а также при нормальной связывающей способности ПССГ (полового секс–связывающего глобулина, связанный с ним тестостерон наименее активен) предполагают рецепторную форму ГА, которая проявляется в виде повышенной чувствительности рецепторов к нормальному или сниженному количеству андрогенов. Основной причиной рецепторной (относительной) ГА является повышение активности фермента 5–α–редуктазы I, которая переводит тестостерон в более активный метаболит – дегидротестостерон (ДГТ), который и является непосредственным стимулятором пролиферации и созревания себоцитов [17,20].
Под действием гормонального фактора увеличивается объем кожного сала (продукция кожного сала при легкой степени акне увеличивается в 1,3 раза, при средней – в 1,7 раза, а при тяжелой – в 1,9 раза). В увеличенном объеме кожного сала снижается концентрация незаменимой a–линоленовой кислоты – основного регулятора дифференцировки кератиноцитов протока сально–волосяного фолликула (СВФ), и увеличивается экспрессия фермента трансглутаминазы. Это приводит к преобладанию процессов дискератоза и пролиферации над десквамацией эпителия СВФ, которые в конечном итоге вызывают фолликулярный гиперкератоз и закрытие протока СВФ, что клинически проявляется открытыми и закрытыми комедонами в зависимости от уровня закупорки СВФ [21,22].
Обтурация протока СВФ и богатое липидами кожное сало создают благоприятные условия для размножения факультативных анаэробов: Propionibacterium acnes и Propionibacterium granulosum, а также других представителей сапрофитной и условно–патогенной микрофлоры (Staphylococcus epidermidis, aureus, Pityrosporum ovale). Эти микроорганизмы продуцируют фермент липазу, который расщепляет диацил– и триацилгрицериды до глицерина и свободных жирных кислот. Данные вещества вместе с антигенами микроорганизмов привлекают из периферической крови нейтрофилы и фагоциты, продуцирующие ИЛ 1α, 1β и 8; ФНО–α. Эти провоспалительные цитокины активируют фермент циклооксигеназу, который способствует образованию из арахидоновой кислоты главного медиатора воспаления – ЛТВ4. Он в свою очередь стимулирует высвобождение гидролитических ферментов и монооксида азота из нейтрофилов, Т–лимфоцитов, моноцитов и эозинофилов, что приводит к разрушению стенки сальной железы с выходом ее содержимого в дерму и развитию воспалительной реакции в виде папулопустулезных и узловато–кистозных элементов [21,23].
Кроме того, P. acnes способны индуцировать экспрессию В–дефензинов – катионных пептидов иммунной системы, активных в отношении бактерий, грибков и многих вирусов. Помимо прямого противоинфекционного действия они выполняют множество других важных функций: действуют как медиаторы воспаления, влияют на хемотаксис, обладают иммуномодулирующей, цитотоксической активностью. В недавних исследованиях было выявлено, что P. acnes могут активировать систему инсулиноподобного фактора роста 1 и рецептора ИФР I типа (IGF 1/IGF–R1) в эпидермисе, действуя как инсулин, и способствуют пролиферации кератиноцитов. Стоит также отметить, что P. acnes имеет высокую провоспалительную активность, намного большую, чем у Staphylococcus aureus и Streptococcus [24,25].
Наиболее удобная и часто используемая классификация акне в дерматологической практике – это классификация, предложенная Американской академией дерматологии, согласно которой различают следующие степени тяжести акне.
1 степень – характеризуется наличием комедонов (закрытых и открытых) до 10 папул.
2 степень – комедоны, папулы, до 10 пустул.
3 степень – комедоны, папулопустулезная сыпь, до 3 узлов.
4 степень – выраженная воспалительная реакция в глубоких слоях дермы с формированием множественных болезненных узлов и кист.
Единственным недостатком этой классификации является отсутствие степеней тяжести в зависимости от распространенности процесса. Поэтому помимо классического деления с учетом степени тяжести акне целесообразно разделять пациентов на подгруппы в зависимости от локализации и распространенности процесса (А,В,С).
А – при локализации высыпаний в 1–ой анатомической области.
В – при локализации высыпаний в 2–х анатомических областях (например, лицо и спина).
С – при вовлечении в патологический процесс 3–х и более анатомических областей. Данная классификация наиболее полно отражает степень вовлеченности кожного покрова в патологический процесс.
Акне относится к особой группе кожных заболеваний – психосоматическим дерматозам, при которых велика роль психоэмоциональных нарушений, связанных с проблемой «дефекта внешности», что особенно выражено у женщин и девушек. Локализация дерматоза на открытых участках кожи приносит пациенткам глубокие психологические страдания, снижая самооценку, негативно влияя на качество жизни, социальный статус, профессиональную деятельность, личную жизнь. В структуре общей заболеваемости тревожно–депрессивными расстройствами больные акне, по некоторым данным, занимают второе место, опережая по этому показателю многие соматические и кожные заболевания, включая даже больных с онкологической патологией. Пациенты с акне демонстрируют более высокий уровень тревоги и депрессии по сравнению с другими дерматологическими больными. 30% подростков и 5% взрослых нуждаются в активной психолого–психиатрической помощи [10].
Британской ассоциацией дерматологов было установлено, что определенный вид дерматоза увеличивает риск суицидальных попыток. Элементы самоповреждающего поведения, в ряде случаев приведшего к завершенному суициду, чаще наблюдались при акне, псориазе, экземе и крапивнице. Пациенты с акне имеют высокий риск попыток самоубийства, а также могут нести угрозу для своих лечащих врачей [26,27].
По данным J.K. Tan и соавт., женский пол, зрелый возраст, длительность (более 5 лет) заболевания являются дополнительными факторами, оказывающими негативное влияние на качество жизни женщин, существенно снижая его. Пациентки с акне являются наиболее психологически уязвимыми, среди лиц с акне отмечается большое число (64%) неработающих женщин, с неустроенной личной жизнью. В другом исследовании также было показано, что у 40% пациентов кожное заболевание, сопровождающееся косметическим дефектом, приводит к снижению их социального статуса и негативным образом отражается на профессиональной деятельности [28,29].
Исследования, проведенные отечественными дерматологами, показали, что психоэмоциональные расстройства (ПЭР) различной степени выраженности наблюдаются у 41,3% больных с УБ и значительно чаще встречаются у женщин. В другом исследовании было выявлено, что депрессивная симптоматика, вызванная акне, чаще встречается и имеет более выраженный характер у женщин по сравнению с мужчинами [30,31].
Данные литературы, свидетельствующие о наличии взаимосвязи между стрессогенными факторами и возникновением акне, довольно противоречивы. Так, Goulden и соавт. выявили, что только 12% из 71% женщин, у которых стресс являлся причиной акне, называют его провоцирующим фактором заболевания. В то же время Poli, Dumont–Wallon и соавт. отметили, что стресс является одним из существенных факторов, провоцирующих возникновение угревых высыпаний у женщин, он выявлялся как триггерный фактор в 34–50% наблюдений. Связь между стрессом и обострением акне в настоящее время объясняется выработкой нейромедиаторов (субстанция Р), которая влияет на дифференцировку и деление себоцитов и стимулирует выработку кожного сала. Кожа людей со склонностью к акне характеризуется обилием нервных окончаний, увеличенным числом нервных волокон, способных секретировать субстанцию Р, а также большим числом тучных клеток [1,6,7,10].
Обострение акне чаще наблюдается зимой и весной. К ухудшению течения заболевания приводят постоянная механическая травматизация кожи (выдавливание угрей, частое мытье с мылом), негативное воздействие внешней среды (загрязнение кожи маслами, бензином, пылью производственного происхождения), прием ряда медикаментов (стероидные гормоны, галогенсодержащие препараты, противотуберкулезные средства, антидепрессанты, противоэпилептические средства), неадекватно подобранная линия косметических средств по уходу за кожей. Солнечное облучение у большинства пациентов оказывает благоприятное влияние на течение акне и способствует частичному разрешению угревых высыпаний, однако у 8–10% пациентов интенсивная инсоляция вызывает обострение заболевания [6,10,11].
В последнее время появились публикации о влиянии пищевых продуктов на появление угревых высыпаний. Такая гипотеза уже высказывалась около полувека назад, но потом была отвергнута. В настоящее время за рубежом проводятся исследования, посвященные пищевому рациону и его влиянию на течение акне. Было выявлено, что продукты со значительным содержанием сахара и других углеводов, увеличивая уровень гликемической нагрузки, влияют на концентрацию инсулина и IGF 1, которые в свою очередь повышают концентрацию основных андрогенов в плазме крови. Это приводит к гиперсекреции кожного сала и появлению акне. Следует также напомнить, что усиленный прием йод– или бромсодержащих продуктов питания, в том числе в больших количествах йодированной соли и морепродуктов, может привести к увеличению воспалительных высыпаний у больных с акне. С другой стороны, отмечено, что включение в пищевой рацион продуктов, содержащих антиоксиданты, омега–3 жирные кислоты, пищевые волокна, витамины А, Е, С, положительно влияет на течение акне, способствуя уменьшению количества высыпаний. A. Logan доказал, что рыбий жир, богатый омега–3 жирными кислотами, ингибирует лейкотриен В4 и способен уменьшить выраженность воспалительных явлений при акне [32–35].
В последних исследованиях была выявлена роль табака в развитии акне. Было отмечено, что курящие женщины имели более тяжелые формы акне по сравнению с некурящими. В двух исследованиях, проведенных в 2009 и 2010 г., было выявлено, что курение является главным фактором в развитии комедональных (невоспалительных) акне у женщин. По мнению авторов, это объясняется тем, что никотин увеличивает продукцию кожного сала и снижает концентрацию витамина Е в организме [9,36].
Диагностическая и терапевтическая модель ведения женщин с акне включает в себя прежде всего полное и всестороннее обследование пациенток с учетом не только дерматологического, но и прежде всего гормонально–эндокринного профиля женщины с обязательным привлечением гинеколога–эндокринолога. От результатов исследования во многом зависит тактика ведения пациентки. Но прежде всего необходимо тщательно собрать анамнез, обращая внимания на семейную отягощенность, опыт предшествующей терапии, наличие сопутствующей патологии, характер питания. При осмотре следует обратить внимание не только на характер высыпаний, но и отметить телосложение женщины, тип оволосения, степень развития вторичных половых признаков, оценить наличие избыточной массы тела. Необходимо выяснить особенности менструального цикла и его влияние на появление высыпаний, а также влияние беременностей и родов на течение дерматоза.
Пациенткам назначают гормональное исследование крови (5–7–й день менструального цикла) с определением концентрации яичниковых и надпочечниковых андрогенов, гормонов щитовидной железы и гипофиза; стероидный профиль мочи (2–я фаза менструального цикла), с помощью которого определяют суточную экскрецию андрогенов. Гормональные зонды целесообразно дополнить УЗИ органов малого таза (5–10–й день менструального цикла, оптимальнее всего – 5–7–й день), при необходимости – УЗИ надпочечников, КТ, МРТ/рентгенографией черепа, малой пробой с дексаметазоном и др.
Для исследования фонового состояния кожи у пациенток с акне, помимо клинической оценки степени тяжести заболевания, целесообразно использовать неинвазивные дерматологические методы исследования, которые помимо объективизации патологических процессов в коже также служат критерием эффективности и безопасности терапии при акне. Рекомендуется использовать следующие методы: себометрию, рН–метрию, корнеометрию (измерение уровня увлажненности кожи, особенно у пациенток с поздними угрями), а также исследование микрорельефа кожи методом оптического видеомониторинга.
Для определения влияния заболевания на качество жизни пациенток необходимо провести исследование дерматологического индекса качества жизни – ДИКЖ, русифицированного Н.Г. Кочергиным (2001 г.) варианта индекса Finlay, для оценки выраженности тревожно–депрессивной симптоматики – тестирование по госпитальной шкале тревоги и депрессии HADS, разработанной A.S. Zigmond и R.P. Snaith (1983 г.), и в случае необходимости подключить психолога или даже психиатра.
Лечебная тактика при акне у женщин зависит от стадии, распространенности заболевания, наличия или отсутствия патологических изменений в гормонально–эндокринном статусе женщины, а также от психоэмоционального состояния женщины. При выборе тактики лечения также необходимо учитывать возраст пациентки, сопутствующую патологию, возможность соблюдения режима лечения, предшествующую терапию. Современные подходы к терапии заболевания включают назначение различных системных и топических препаратов, влияющих на различные звенья патогенеза акне. Системная терапия назначается при 3–4–й степени акне, при упорном течении процесса при 2–й степени акне, а также при распространенных высыпаниях и отягощенности гормонально–эндокринного статуса при любой стадии акне (гормональная терапия).
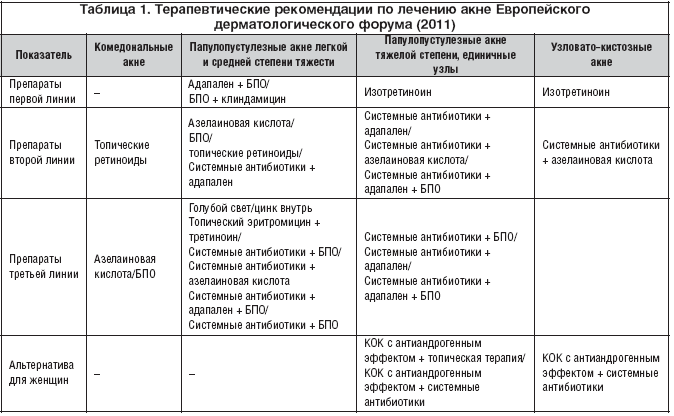
При 1–й степени акне проводится только местная терапия, причем препаратами первого выбора являются топические ретиноиды (адапален) (табл. 1), при 2–й степени к топической присоединяют системную терапию, как правило, это антибиотики. Возможны применение воздействия высокоинтенсивного голубого света на акне–элементы и прием препаратов цинка, однако уровень доказательности для данных видов терапии невысок. При назначении топических антибиотиков следует учитывать, что, по последним данным, клиндамицин является наиболее эффективным препаратом в отношении угревых высыпаний, с учетом последних данных о торпидности к системным и топическим антибиотикам у женщин с поздними угрями. Наибольший эффект достигается при сочетании адапалена и бензоилпероксида (ВПО), ВПО и клиндамицина, системных антибиотиков в сочетании с азелаиновой кислотой, адапаленом и ВПО.
При тяжелых формах акне у женщин показано назначение КОК с антиандрогенным эффектом в сочетании с топическими противоугревыми препаратами и, в тяжелых случаях, с системными антибиотиками. Для достижения выраженного терапевтического эффекта назначать КОК следует на длительный срок – от 6 мес. до 1 года. При противопоказаниях к назначению КОК применяются системные ретиноиды. Установлено, что степень выраженности положительных результатов терапии системными ретиноидами тяжелых форм акне является дозозависимой. Длительность приема препарата приводит к выраженному подавлению активности сальных желез, что гистологически подтверждается уменьшением их размеров. Для достижения наибольшей эффективности лечения, увеличения продолжительности ремиссий и снижения частоты рецидивов оптимально использование курсовой дозы – 120–150 мг/кг. Системные ретиноиды необходимо применять в течение 3–6 мес.
При противопоказаниях как к назначению КОК, так и системных ретиноидов наиболее показано применение системных антибиотиков в сочетании с препаратами азелаиновой кислоты (гель, крем) и другими топическими препаратами сроком не менее 1 мес.
При назначении препаратов у женщин следует учитывать их влияние на фертильность, возможность тератогенного действия, мутагенность, фетотоксичность, возможность сочетания с косметикой и духами, а также с косметологическими процедурами.
В качестве дополнительной терапии, так называемых средств ухода, необходимо использовать средства лечебной косметики, которые являются важным лечебным компонентом терапевтической программы ведения пациенток с акне. При выборе косметических средств необходимо учитывать тип кожи пациентки, данные аппаратных методик, позволяющих оценить степень выраженности жирности, увлажненности кожи и ее рН.
После удачного купирования воспалительных проявлений акне врачу часто приходится сталкиваться с трудностями в коррекции постакне. Наиболее частыми проявлениями постакне являются дисхромии и рубцы.
Для разрешения дисхромий успешно применяются: поверхностные пилинги с α–гидроксикислотами, срединные пилинги с ТСА. Хороший синергический эффект дает совместное использование азелаиновой кислоты вместе с пилингами, в качестве препилинговой подготовки и постпилингового ухода, особенно у пациентов со смуглой кожей в качестве профилактики гиперпигментации и обострений акне. Хороший эффект дают курс криомассажа (5–6 мин. 2–3 раза в нед. на курс 10–15 процедур), мезотерапия, курс лечебного массажа (15 процедур) в сочетании с электрофорезом с витамином С.
Для коррекции атрофических рубцов применяются химические пилинги, чаще срединные, микродермабразия, лазерная шлифовка, инъекции филлеров, криотерапия, мезотерапия, но наиболее эффективными являются комбинированные методы коррекции. Для лечения гипертрофических рубцов используют очаговое введение кортикостероидов, электрофорез с кортикостероидами, лидазой, коллагеназой, буки–терапию, фонофорез с контрактубексом, мадекассолом, криодеструкцию, мазевую терапию (медерма, куриозин, контратубекс), а также хирургическое иссечение рубцов при большой площади поражения.
Таким образом, тактика ведения женщин с акне требует междисциплинарного взгляда на проблему с учетом всех возможных факторов заболевания и привлечением ряда смежных специалистов. Терапия акне должна назначаться с учетом дерматологического, гормонально–эндокринного и психоэмоционального состояния женщины и воздействовать на основные патогенетические звенья заболевания. При назначении лечения необходимо также учитывать социальный, профессиональный статус женщины и возможность соблюдения курса лечения.

Литература
1. Dumont–Wallon G., Dreno B. Specificity of acne in women older than 25 years // Presse Med. 2008. Vol.37. P. 585–591.
2. Williams C., Layton A.M. Persistent acne in women: implications for the patient and for therapy // Am. J. Clin. Dermatol. 2006. Vol. 7. P. 281–290.
3. Del Rosso J.Q., Bikowski J., Baum E. Prevalence of truncal acne vulgaris: a population study based on private practice experience // J. Am. Acad. Dermatol. 2007. Vol. 56. AB3.
4. Эллинг. Д. Секреты дерматологии. – Спб, 1999. – С. 513.
5. Colleir Ch., Haper J., Cantell W. The prevalence of acne in adults 20 years and older // J. Am. Acad. Dermatol. 2008. Vol. 58. P.56.
6. Самцов. А.В. Акне и акнеформные дерматозы. – М., 2009.
7. Poli F., Dreno B., Verschoore M. An epidemiological study of acne in female adults: results of a survey conducted in France // J. Eur. Acad. Dermatol. Venereol. 2001. Vol. 15. P. 541–545.
8. Rivera R., Guerra A. Management of acne in women over 25 years of age // Actas Dermosifiliogr. 2009. Vol. 100. P. 33–37.
9. Preneau S., Dreno B. Female acne – a different subtype of teenager acne? // JEADV, 2011.
10. Майорова А.В, Шаповалов В.С, Ахтямов С.Н. угревая болезнь в практике врача дерматокосметолога. – М.: «Фирма Кавель», 2005.
11. Адаскевич В.Л Акне вульгарные и розовые. – НГМА, 2003.
12. Суворова К.Н, Котова Н.В. Тяжелые формы акне // Международный медицинский журнал. – 2000. – С.732–726.
13. Pang Y. et al. Combination of short CAG and GGN repeats in the androgen receptor gene is associated with acne rick in North East China, 2008.
14. Гусаков Н.И. Акне. – Акне, 2003. – С. 76.
15. Аравийская Е.Р. Современный взгляд на лечение акне: состояние проблемы и новые возможности //Леч. врач. – 2003. – № 4. – С. 4–6.
16. Масюкова С.А., Ахтямов С.Н. Акне: проблема и решение // Concilium medicum. – 2002. – Т. 4, № 5. – С. 217.
17. Доброхотова Ю.Э., Джобава Э.М., Рагимова З.Ю. и др. Синдром гиперандрогении в практике акушера–гинеколога, дерматолога, эндокринолога: руководство для врачей. – М. : ГЭОТАР–Медиа, 2009.
18. Seirafi H., Farnaghi F., Vasheghani–Farahani A. et al. Assessment of androgens in women with adult–onset acne // Int. J. Dermatol. 2007. Vol. 46. P.1188–1191.
19. Горячкина М.В. Роль гормонально–эндокринных факторов в патогенезе рефрактерных форм угревой болезни у женщин: автореферат дисс. к.м.н., 2009.
20. Vexiau P. et al. Acne in adult women: data from a national study on the relationship between type of acne and markers of clinical hyperandrogenism // Ann. Dermatol. Venerol. 2002. Vol. 129 (2). P. 174.
21. Монахов С.А., Иванов О.Л. Акне : методическое пособие для врачей. – М., 2010.
22. Webster G. F. Acne vulgaris // Br. J. Dermatol. 2002. Vol. 325. P. 475–479.
23. Jappe U., Igham E., Henwood J., Holland K.T. Propionibacterium acne and inflammation in acne: P acnes has T–cell mitogenic activity// Br. J Dermatol. 2002. Vol 146. P 202–209.
24. Isard O., Knol A.C., Aries M.F. et al. Proprionibacterium acnes activates the IGF–1 / IGF–1R system in the epidermis and induces keratinocytes proliferation // J. Invest. Dermatol. 2011. Vol. 131. P. 59–66.
25. Nagy I., Pivarcsi A., Koreck A. et al. Distinct strains of Propionibacterium acnes induce selective human beta–defensin–2 and interleukin–8 expression in human keratinocytes through toll–like receptors // J. Invest. Dermatol. 2005. Vol. 124. P. 931–938.
26. Cotterill J.A., Cunliffe W. Suicide in dermatological patients // British Association of dermatologists. 1997. Vol. 137. P. 246–250.
27. Вowe W. et al. Body dysmorphic disorder symptoms among patients with acne vulgaris // J. Am. Acad. Dermatol. 2007. Vol. 57. P.222–230.
28. Tan J.K. et al. Divergence of demographic factors associated with clinical severity compared with quality of life impact in acne // J. Cutan. Med. Surg. 2008. Vol. 12(5). P.235–242.
29. Bodermer W. Psychosodermatology // The Med. Journal. 2001. Vol. 6. P. 297–302.
30. Монахов С.А. Дифференцированная терапия акне с учетом тяжести кожного процесса и спектра психоэмоциональных расстройств: Автореф. дисс. к. м. н. – М., 2005.
31. Горячкина М.В. Роль психоэмоциональных факторов в развитии акне // Concilium Medicum. Дерматология. – 2008. – № 2.– С. 8–12.
32. Veith W.B., Silverberg N.B. The association of acne vulgaris with diet // Cutis. 2011 .Vol. 88(2). P.84–91.
33. Danby F.W. Nutrition and acne // Clin. Dermatol. 2010. Vol. 28(6). P. 598–604.
34. Melnik B.C., Schmitz G. Role of insulin, insulin–like growth factor–1, hyperglycaemic food and milk consumption in the pathogenesis of acne vulgaris // Exp. Dermatol. 2009. Vol.18(10). P. 833–841.
35. . Logan A. Omega–3 fatty acids and acne // Arch. Dermatol. 2003. Vol. 139. P.941.
36. Capitanio B., Sinagra J.L., Ottaviani M. et al. Acne and smoking // Dermatoendocrinol. 2009. Vol. 1. P.129–135.












