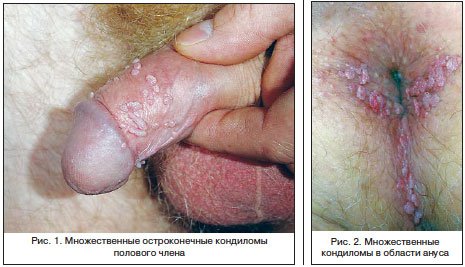
–°–µ–Ї—Б—Г–∞–ї—М–љ—Л–µ –Ї–Њ–љ—В–∞–Ї—В—Л – –Њ—Б–љ–Њ–≤–љ–Њ–є —Д–∞–Ї—В–Њ—А —А–Є—Б–Ї–∞ –Ј–∞—А–∞–ґ–µ–љ–Є—П –Т–Я–І. –Ш—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є–µ –њ—А–µ–Ј–µ—А–≤–∞—В–Є–≤–Њ–≤, —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ –Ј–∞—Й–Є—Й–∞—О—Й–µ–µ –Њ—В –і—А—Г–≥–Є—Е –Ш–Я–Я–Я, –љ–µ –Љ–Њ–ґ–µ—В –њ—А–µ–і—Г–њ—А–µ–і–Є—В—М –Њ—В –Є–љ—Д–Є—Ж–Є—А–Њ–≤–∞–љ–Є—П —Н—В–Є–Љ –≤–Є—А—Г—Б–Њ–Љ. –Ю–і–љ–∞–Ї–Њ –і–∞–љ–љ—Л–є –Љ–µ—В–Њ–і –Ј–∞—Й–Є—В—Л —П–≤–ї—П–µ—В—Б—П —Н—Д—Д–µ–Ї—В–Є–≤–љ—Л–Љ –±–∞—А—М–µ—А–Њ–Љ –і–ї—П –њ—А–Њ–љ–Є–Ї–љ–Њ–≤–µ–љ–Є—П –≤–Є—А—Г—Б–∞ –≤ —Н–њ–Є—В–µ–ї–Є–є —Б–ї–Є–Ј–Є—Б—В–Њ–є —И–µ–є–Ї–Є –Љ–∞—В–Ї–Є, –њ—А–µ–і–Њ—В–≤—А–∞—Й–∞—П —А–∞–Ј–≤–Є—В–Є–µ –∞–і–µ–љ–Њ–Ї–∞—А—Ж–Є–љ–Њ–Љ—Л. –Я–Њ—А–∞–ґ–µ–љ–Є–µ –Т–Я–І —Б–ї–Є–Ј–Є—Б—В—Л—Е –Є –Њ–Ї—А—Г–ґ–∞—О—Й–Є—Е –Є—Е –Ї–Њ–ґ–љ—Л—Е –њ–Њ–Ї—А–Њ–≤–Њ–≤ –њ—А–µ–≤–∞–ї–Є—А—Г–µ—В –≤ –≥—А—Г–њ–њ–µ –Љ–Њ–ї–Њ–і—Л—Е –ї–Є—Ж 15–25 –ї–µ—В, –≤–µ–і—Г—Й–Є—Е –∞–Ї—В–Є–≤–љ—Г—О –њ–Њ–ї–Њ–≤—Г—О –ґ–Є–Ј–љ—М —Б —А–∞–Ј–љ—Л–Љ–Є —Б–µ–Ї—Б—Г–∞–ї—М–љ—Л–Љ–Є –њ–∞—А—В–љ–µ—А–∞–Љ–Є. –Я–Њ—А–∞–ґ–µ–љ–Є—П –≤–Њ–Ј–љ–Є–Ї–∞—О—В, –Ї–∞–Ї –њ—А–∞–≤–Є–ї–Њ, –љ–∞ –Ї–Њ–ґ–µ –Є —Б–ї–Є–Ј–Є—Б—В—Л—Е –њ–Њ–ї–Њ–≤—Л—Е –Њ—А–≥–∞–љ–Њ–≤ –Є–ї–Є –≤ –∞–љ–∞–ї—М–љ–Њ–є –Њ–±–ї–∞—Б—В–Є –≤ –Љ–µ—Б—В–∞—Е —В—А–µ–љ–Є—П, —В—А–∞–≤–Љ–∞—В–Є–Ј–∞—Ж–Є–Є –Є –Љ–∞—Ж–µ—А–∞—Ж–Є–Є –Ї–Њ–ґ–Є (—А–Є—Б. 1, 2). –Т–∞–ґ–љ–Њ –њ–Њ–Љ–љ–Є—В—М, —З—В–Њ –Т–Я–І –Љ–Њ–ґ–µ—В –њ–µ—А–µ–і–∞–≤–∞—В—М—Б—П –љ–µ —В–Њ–ї—М–Ї–Њ –њ–Њ–ї–Њ–≤—Л–Љ, –љ–Њ –Є –≤–µ—А—В–Є–Ї–∞–ї—М–љ—Л–Љ –њ—Г—В–µ–Љ, –Є–љ—Д–Є—Ж–Є—А—Г—П —А–µ–±–µ–љ–Ї–∞ –≤–Њ –≤—А–µ–Љ—П —А–Њ–і–Њ–≤ –њ—А–Є –њ—А–Њ—Е–Њ–ґ–і–µ–љ–Є–Є –њ–Њ–ї–Њ–≤—Л—Е –њ—Г—В–µ–є, –Є —П–≤–Є—В—М—Б—П –њ—А–Є—З–Є–љ–Њ–є —А–∞–Ј–≤–Є—В–Є—П —А–µ—Ж–Є–і–Є–≤–Є—А—Г—О—Й–µ–≥–Њ —А–µ—Б–њ–Є—А–∞—В–Њ—А–љ–Њ–≥–Њ –њ–∞–њ–Є–ї–ї–Њ–Љ–∞—В–Њ–Ј–∞ [3].
–Т–Я–І –Њ—В–љ–Њ—Б–Є—В—Б—П –Ї –Љ–µ–ї–Ї–Є–Љ, –±–µ–Ј–Њ–±–Њ–ї–Њ—З–µ—З–љ—Л–Љ –≤–Є—А—Г—Б–∞–Љ, —Б–Њ–і–µ—А–ґ–∞—Й–Є–Љ –і–≤—Г—Е—Ж–µ–њ–Њ—З–µ—З–љ—Г—О –Ф–Э–Ъ, –Є–Љ–µ–µ—В –Є–Ї–Њ—Б–∞—Н–і—А–Є—З–µ—Б–Ї—Г—О —Д–Њ—А–Љ—Г –Є —А–∞–Ј–Љ–µ—А 45–55 –љ–Љ. –Ю–љ —П–≤–ї—П–µ—В—Б—П —Б—В—А–Њ–≥–Њ —Н–њ–Є—В–µ–ї–Є–Њ—В—А–Њ–њ–љ—Л–Љ, —В. –Ї. –њ–Њ—А–∞–ґ–∞–µ—В –±–∞–Ј–∞–ї—М–љ—Л–є —Б–ї–Њ–є —Н–њ–Є—В–µ–ї–Є—П –Ї–Њ–ґ–Є –Є —Б–ї–Є–Ј–Є—Б—В—Л—Е –Њ–±–Њ–ї–Њ—З–µ–Ї –≥–µ–љ–Є—В–∞–ї–Є–є –Є –і—А—Г–≥–Є—Е –Њ—А–≥–∞–љ–Њ–≤ (–≥–Њ—А—В–∞–љ—М, —А–Њ—В–Њ–≤–∞—П –њ–Њ–ї–Њ—Б—В—М, –≥–ї–∞–Ј–∞ –Є –і—А.), –Є –µ–≥–Њ –ґ–Є–Ј–љ–µ–љ–љ—Л–є —Ж–Є–Ї–ї —Б–≤—П–Ј–∞–љ —Б –і–Є—Д—Д–µ—А–µ–љ—Ж–Є–∞—Ж–Є–µ–є —Н–њ–Є—В–µ–ї–Є–∞–ї—М–љ—Л—Е –Ї–ї–µ—В–Њ–Ї. –†–µ–њ–ї–Є–Ї–∞—Ж–Є—П –Ф–Э–Ъ –Т–Я–І –њ—А–Њ–Є—Б—Е–Њ–і–Є—В —В–Њ–ї—М–Ї–Њ –≤ –Ї–ї–µ—В–Ї–∞—Е –±–∞–Ј–∞–ї—М–љ–Њ–≥–Њ —Б–ї–Њ—П, –∞ –≤ –Ї–ї–µ—В–Ї–∞—Е –і—А—Г–≥–Є—Е —Б–ї–Њ–µ–≤ —Н–њ–Є–і–µ—А–Љ–Є—Б–∞ –≤–Є—А—Г—Б–љ—Л–µ —З–∞—Б—В–Є—Ж—Л –ї–Є—И—М –њ–µ—А—Б–Є—Б—В–Є—А—Г—О—В. –Я—А–Є –Ј–∞—А–∞–ґ–µ–љ–Є–Є –Т–Я–І –≤ –Ї–ї–µ—В–Ї–∞—Е —Н–њ–Є–і–µ—А–Љ–Є—Б–∞ –љ–∞—А—Г—И–∞–µ—В—Б—П –љ–Њ—А–Љ–∞–ї—М–љ—Л–є –њ—А–Њ—Ж–µ—Б—Б –і–Є—Д—Д–µ—А–µ–љ—Ж–Є—А–Њ–≤–Ї–Є. –Я—А–Њ–Є—Б—Е–Њ–і–Є—В –Ї–ї–Њ–љ–∞–ї—М–љ–∞—П —Н–Ї—Б–њ–∞–љ—Б–Є—П –Є–љ—Д–Є—Ж–Є—А–Њ–≤–∞–љ–љ—Л—Е –Т–Я–І –Ї–ї–µ—В–Њ–Ї –±–∞–Ј–∞–ї—М–љ–Њ–≥–Њ —Б–ї–Њ—П —Б –Є—Е —В—А–∞–љ—Б—Д–Њ—А–Љ–∞—Ж–Є–µ–є –Є –≤–Њ–Ј–Љ–Њ–ґ–љ–Њ–є –њ–Њ—Б–ї–µ–і—Г—О—Й–µ–є –Љ–∞–ї–Є–≥–љ–Є–Ј–∞—Ж–Є–µ–є. –Ф–∞–љ–љ—Л–є –њ—А–Њ—Ж–µ—Б—Б –Ї–Њ–љ—В—А–Њ–ї–Є—А—Г–µ—В—Б—П –≥–µ–љ–∞–Љ–Є –Т–Я–І, –Ї–Њ–і–Є—А—Г—О—Й–Є–Љ–Є —А–∞–љ–љ–Є–µ –±–µ–ї–Ї–Є –Х6 –Є –Х7. –Я—А–Є —Н—В–Њ–Љ –њ—А–Њ–Є—Б—Е–Њ–і—П—В –Љ–Њ—А—Д–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є–µ –љ–∞—А—Г—И–µ–љ–Є—П –Є –і–µ—Д–Њ—А–Љ–∞—Ж–Є—П —Б–ї–Њ–µ–≤ —Н–њ–Є–і–µ—А–Љ–Є—Б–∞, –њ—А–Є–≤–Њ–і—П—Й–Є–µ –Ї —Г—В–Њ–ї—Й–µ–љ–Є—О –Ї–Њ–ґ–Є –Є —Б–ї–Є–Ј–Є—Б—В–Њ–є. –Т —Б—В–∞–і–Є–Є —А–∞–Ј–≤–Є—В–Њ–є –Є–љ—Д–µ–Ї—Ж–Є–Є –Ї–ї–µ—В–Ї–Є —И–Є–њ–Њ–≤–∞—В–Њ–≥–Њ —Б–ї–Њ—П –њ—А–Є –њ–µ—А–µ—Е–Њ–і–µ –≤ –Ј–µ—А–љ–Є—Б—В—Л–є –Њ–Ї–∞–Ј—Л–≤–∞—О—В—Б—П –љ–∞–Є–±–Њ–ї–µ–µ –∞–Ї—В–Є–≤–љ—Л–Љ–Є –≤ —Б–Є–љ—В–µ–Ј–µ –≤–Є—А—Г—Б–љ–Њ–є –Ф–Э–Ъ. –≠—В–∞ —Д–∞–Ј–∞ –ґ–Є–Ј–љ–µ–љ–љ–Њ–≥–Њ —Ж–Є–Ї–ї–∞ –Т–Я–І —Е–∞—А–∞–Ї—В–µ—А–Є–Ј—Г–µ—В –≤—В–Њ—А–Њ–є —Н—В–∞–њ —Н–Ї—Б–њ–∞–љ—Б–Є–Є –≤–Є—А—Г—Б–љ–Њ–є –Є–љ—Д–µ–Ї—Ж–Є–Є –≤–љ—Г—В—А–Є —Н–њ–Є–і–µ—А–Љ–Є—Б–∞. –≠–Ї—Б–њ—А–µ—Б—Б–Є—П –њ–Њ–Ј–і–љ–Є—Е –≥–µ–љ–Њ–≤ L1 –Є L2 –љ–∞—Б—В—Г–њ–∞–µ—В –љ–∞ –Ї–Њ–љ–µ—З–љ–Њ–є —Б—В–∞–і–Є–Є –і–Є—Д—Д–µ—А–µ–љ—Ж–Є—А–Њ–≤–Ї–Є –≤ —А–Њ–≥–Њ–≤–Њ–Љ —Б–ї–Њ–µ, –≥–і–µ –љ–∞–±–ї—О–і–∞–µ—В—Б—П –∞–Ї—В–Є–≤–љ–∞—П «—Б–±–Њ—А–Ї–∞» –Ј—А–µ–ї—Л—Е –≤–Є—А—Г—Б–љ—Л—Е —З–∞—Б—В–Є—Ж –Є –Є—Е –≤—Л–і–µ–ї–µ–љ–Є–µ –Є–Ј –Ї–ї–µ—В–Њ–Ї –љ–∞ –њ–Њ–≤–µ—А—Е–љ–Њ—Б—В–Є –Ї–Њ–ґ–Є. –£—З–∞—Б—В–Ї–Є –Ї–Њ–ґ–Є –Є —Б–ї–Є–Ј–Є—Б—В—Л—Е, –љ–∞ –њ–Њ–≤–µ—А—Е–љ–Њ—Б—В–Є –Ї–Њ—В–Њ—А—Л—Е –њ—А–Њ–Є—Б—Е–Њ–і–Є—В –∞–Ї—В–Є–≤–љ–Њ–µ –≤—Л–і–µ–ї–µ–љ–Є–µ –Є –њ–Њ—З–Ї–Њ–≤–∞–љ–Є–µ –≤–Є—А—Г—Б–∞, –њ—А–µ–і—Б—В–∞–≤–ї—П—О—В –љ–∞–Є–±–Њ–ї—М—И—Г—О –Њ–њ–∞—Б–љ–Њ—Б—В—М –і–ї—П –Ї–Њ–љ—В–∞–Ї—В–љ–Њ–≥–Њ –Ј–∞—А–∞–ґ–µ–љ–Є—П [4].
–Т –љ–∞—Б—В–Њ—П—Й–µ–µ –≤—А–µ–Љ—П –Є–і–µ–љ—В–Є—Д–Є—Ж–Є—А–Њ–≤–∞–љ–Њ –±–Њ–ї–µ–µ 200 —В–Є–њ–Њ–≤ –Т–Я–І, –Ї–Њ—В–Њ—А—Л–µ –њ—А–Є–≤–Њ–і—П—В –Ї —А–∞–Ј–ї–Є—З–љ—Л–Љ –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є–Љ –њ—А–Њ—П–≤–ї–µ–љ–Є—П–Љ –≤ –Ј–∞–≤–Є—Б–Є–Љ–Њ—Б—В–Є –Њ—В –ї–Њ–Ї–∞–ї–Є–Ј–∞—Ж–Є–Є –њ–Њ—А–∞–ґ–µ–љ–Є—П –Є –Є–Љ–Љ—Г–љ–љ–Њ–≥–Њ –Њ—В–≤–µ—В–∞ –њ–∞—Ж–Є–µ–љ—В–∞. –Ш–Љ–µ–љ–љ–Њ –Є–љ–і–Є–≤–Є–і—Г–∞–ї—М–љ—Л–Љ–Є –≤–∞—А–Є–∞—Ж–Є—П–Љ–Є –Ї–ї–µ—В–Њ—З–љ–Њ–≥–Њ –Є–Љ–Љ—Г–љ–Є—В–µ—В–∞ –Њ–±—К—П—Б–љ—П–µ—В—Б—П —А–∞–Ј–љ–Є—Ж–∞ –≤ —А–∞—Б–њ—А–Њ—Б—В—А–∞–љ–µ–љ–љ–Њ—Б—В–Є, —В—П–ґ–µ—Б—В–Є –Є –і–ї–Є—В–µ–ї—М–љ–Њ—Б—В–Є —Б—Г—Й–µ—Б—В–≤–Њ–≤–∞–љ–Є—П –њ—А–Њ—П–≤–ї–µ–љ–Є–є –Т–Я–І. –£ –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б —Б–Є–љ–і—А–Њ–Љ–Њ–Љ –њ—А–Є–Њ–±—А–µ—В–µ–љ–љ–Њ–≥–Њ –Є–Љ–Љ—Г–љ–Њ–і–µ—Д–Є—Ж–Є—В–∞ –Є –ї–Є–Љ—Д–Њ–Љ–∞–Љ–Є, –њ–Њ–ї—Г—З–∞—О—Й–Є—Е –Є–Љ–Љ—Г–љ–Њ—Б—Г–њ—А–µ—Б—Б–Є–≤–љ—Г—О —В–µ—А–∞–њ–Є—О, –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є–µ —Б–Є–Љ–њ—В–Њ–Љ—Л –Т–Я–І –њ–Њ—П–≤–ї—П—О—В—Б—П –≤ –±–Њ–ї—М—И–Њ–Љ –Њ–±—К–µ–Љ–µ –Є —Б—Г—Й–µ—Б—В–≤—Г—О—В –і–ї–Є—В–µ–ї—М–љ–Њ–µ –≤—А–µ–Љ—П.
–Т—Л–і–µ–ї—П—О—В –њ–∞–њ–Є–ї–ї–Њ–Љ–∞–≤–Є—А—Г—Б—Л –Ї–Њ–ґ–Є –Є —Б–ї–Є–Ј–Є—Б—В—Л—Е –Њ–±–Њ–ї–Њ—З–µ–Ї. –Э–∞–њ—А–Є–Љ–µ—А, –Ї –Ї–Њ–ґ–љ—Л–Љ —В–Є–њ–∞–Љ –Њ—В–љ–Њ—Б—П—В –Т–Я–І-1,-2,-3,-4; –Ї —Б–ї–Є–Ј–Є—Б—В–Њ-–Ї–Њ–ґ–љ—Л–Љ – –Т–Я–І-6,-11,-16,-18; –Ї —В–Є–њ–∞–Љ, –≤—Л–і–µ–ї—П–µ–Љ—Л–Љ –Є–Ј –Њ—З–∞–≥–Њ–≤ –≤–µ—А—Г—Ж–Є—Д–Њ—А–Љ–љ–Њ–є —Н–њ–Є–і–µ—А–Љ–Њ–і–Є—Б–њ–ї–∞–Ј–Є–Є, – –Т–Я–І-5–8. –С–Њ–ї—М—И–Є–љ—Б—В–≤–Њ –Ї–∞—А—Ж–Є–љ–Њ–Љ —И–µ–є–Ї–Є –Љ–∞—В–Ї–Є —Б–Њ–і–µ—А–ґ–∞—В –Т–Я–І-16,-18. –Ъ—А–Њ–Љ–µ —В–Њ–≥–Њ, –Т–Я–І –і–µ–ї—П—В –њ–Њ —Б—В–µ–њ–µ–љ–Є –Ї–∞–љ—Ж–µ—А–Њ–≥–µ–љ–љ–Њ–≥–Њ –њ–Њ—В–µ–љ—Ж–Є–∞–ї–∞: –љ–Є–Ј–Ї–Њ–є, —Б—А–µ–і–љ–µ–є –Є –≤—Л—Б–Њ–Ї–Њ–є —Б—В–µ–њ–µ–љ–Є —А–Є—Б–Ї–∞ (—В–∞–±–ї. 1).
–Ъ –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є–Љ –њ—А–Њ—П–≤–ї–µ–љ–Є—П–Љ –Т–Я–І –∞–љ–Њ–≥–µ–љ–Є—В–∞–ї—М–љ–Њ–є –Њ–±–ї–∞—Б—В–Є –Њ—В–љ–Њ—Б—П—В:
1. –Р–љ–Њ–≥–µ–љ–Є—В–∞–ї—М–љ—Л–µ –±–Њ—А–Њ–і–∞–≤–Ї–Є (–Њ—Б—В—А–Њ–Ї–Њ–љ–µ—З–љ—Л–µ –Ї–Њ–љ–і–Є–ї–Њ–Љ—Л).
2. –°–Є–Љ–њ—В–Њ–Љ–∞—В–Є—З–µ—Б–Ї–Є–µ –≤–љ—Г—В—А–Є—Н–њ–Є–і–µ—А–Љ–∞–ї—М–љ—Л–µ –љ–µ–Њ–њ–ї–∞–Ј–Є–Є –љ–∞ —А–∞–љ–љ–Є—Е —Б—В–∞–і–Є—П—Е –њ—А–Є –Њ—В—Б—Г—В—Б—В–≤–Є–Є –і–Є—Б–њ–ї–∞–Ј–Є–Є (–њ–ї–Њ—Б–Ї–Є–µ –Ї–Њ–љ–і–Є–ї–Њ–Љ—Л).
3. –°—Г–±–Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є–µ —Д–Њ—А–Љ—Л – –±–µ—Б—Б–Є–Љ–њ—В–Њ–Љ–љ—Л–µ –≤–љ—Г—В—А–Є—Н–њ–Є—В–µ–ї–Є–∞–ї—М–љ—Л–µ –љ–µ–Њ–њ–ї–∞–Ј–Є–Є –њ—А–Є –Њ—В—Б—Г—В—Б—В–≤–Є–Є –і–Є—Б–њ–ї–∞–Ј–Є–Є.
4. –Ы–∞—В–µ–љ—В–љ—Л–µ —Д–Њ—А–Љ—Л (–Њ—В—Б—Г—В—Б—В–≤–Є–µ –Љ–Њ—А—Д–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є—Е –Є –≥–Є—Б—В–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є—Е –Є–Ј–Љ–µ–љ–µ–љ–Є–є –њ—А–Є –Њ–±–љ–∞—А—Г–ґ–µ–љ–Є–Є –Ф–Э–Ъ –Т–Я–І).
–£ –±–Њ–ї—М—И–Є–љ—Б—В–≤–∞ –Є–љ—Д–Є—Ж–Є—А–Њ–≤–∞–љ–љ—Л—Е –Т–Я–І –љ–µ –≤–Њ–Ј–љ–Є–Ї–∞–µ—В –љ–Є–Ї–∞–Ї–Є—Е –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є—Е —Б–Є–Љ–њ—В–Њ–Љ–Њ–≤ –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П, —В. –Ї. —Б–Њ–±—Б—В–≤–µ–љ–љ–∞—П –Є–Љ–Љ—Г–љ–љ–∞—П —Б–Є—Б—В–µ–Љ–∞ —З–µ–ї–Њ–≤–µ–Ї–∞ —Н–ї–Є–Љ–Є–љ–Є—А—Г–µ—В –≤–Њ–Ј–±—Г–і–Є—В–µ–ї—П. –С—Л–ї–Њ –њ–Њ–Ї–∞–Ј–∞–љ–Њ, —З—В–Њ —В–Њ–ї—М–Ї–Њ —Г 24,8% –ґ–µ–љ—Й–Є–љ, –Є–љ—Д–Є—Ж–Є—А–Њ–≤–∞–љ–љ—Л—Е –Т–Я–І 6-–≥–Њ –Є–ї–Є 11-–≥–Њ —В–Є–њ–Њ–≤, —А–∞–Ј–≤–Є–≤–∞—О—В—Б—П –Њ—Б—В—А–Њ–Ї–Њ–љ–µ—З–љ—Л–µ –Ї–Њ–љ–і–Є–ї–Њ–Љ—Л. –Ґ–Њ—З–љ—Л–є –Љ–µ—Е–∞–љ–Є–Ј–Љ —Г–і–∞–ї–µ–љ–Є—П –≤–Є—А—Г—Б–∞ –Є–Ј –Њ—А–≥–∞–љ–Є–Ј–Љ–∞ –Є–Љ–Љ—Г–љ–љ–Њ–є —Б–Є—Б—В–µ–Љ–Њ–є –њ–Њ–Ї–∞ –љ–µ–Є–Ј–≤–µ—Б—В–µ–љ.
–Ъ –Ї–Њ—Д–∞–Ї—В–Њ—А–∞–Љ, –њ–Њ–≤—Л—И–∞—О—Й–Є–Љ —А–Є—Б–Ї —А–∞–Ј–≤–Є—В–Є—П –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є—Е –њ—А–Њ—П–≤–ї–µ–љ–Є–є –Є–љ—Д–µ–Ї—Ж–Є–Є –Т–Я–І, –Њ—В–љ–Њ—Б—П—В –Ј–ї–Њ—Г–њ–Њ—В—А–µ–±–ї–µ–љ–Є–µ –∞–ї–Ї–Њ–≥–Њ–ї–µ–Љ, –Ї—Г—А–µ–љ–Є–µ, –Є–Љ–Љ—Г–љ–Њ–і–µ—Д–Є—Ж–Є—В—Л, –Є–љ—Д–Є—Ж–Є—А–Њ–≤–∞–љ–Є–µ –≤–Є—А—Г—Б–Њ–Љ –њ—А–Њ—Б—В–Њ–≥–Њ –≥–µ—А–њ–µ—Б–∞ –Є –і—А—Г–≥–Є–Љ–Є –Ш–Я–Я–Я [5, 6].
–Э–∞–Є–±–Њ–ї–µ–µ —З–∞—Б—В—Л–Љ –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є–Љ –њ—А–Њ—П–≤–ї–µ–љ–Є–µ–Љ –Т–Я–І-–Є–љ—Д–µ–Ї—Ж–Є–Є –∞–љ–Њ–≥–µ–љ–Є—В–∞–ї—М–љ–Њ–є –Њ–±–ї–∞—Б—В–Є —П–≤–ї—П—О—В—Б—П –Њ—Б—В—А–Њ–Ї–Њ–љ–µ—З–љ—Л–µ –Ї–Њ–љ–і–Є–ї–Њ–Љ—Л, –≤–Њ–Ј–љ–Є–Ї–∞—О—Й–Є–µ –њ—А–Є –њ–Њ–њ–∞–і–∞–љ–Є–Є –љ–∞ –Ї–Њ–ґ—Г –Є —Б–ї–Є–Ј–Є—Б—В—Л–µ –Њ–±–Њ–ї–Њ—З–Ї–Є –Т–Я–І 6, 11, 16, 18, 42–44 –Є 54-–≥–Њ —В–Є–њ–Њ–≤. –Я–∞—В–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є–є –њ—А–Њ—Ж–µ—Б—Б —Г –Љ—Г–ґ—З–Є–љ –ї–Њ–Ї–∞–ї–Є–Ј—Г–µ—В—Б—П –љ–∞ –≤–љ—Г—В—А–µ–љ–љ–µ–Љ –Є –љ–∞—А—Г–ґ–љ—Л—Е –ї–Є—Б—В–Ї–∞—Е –Ї—А–∞–є–љ–µ–є –њ–ї–Њ—В–Є, –≥–Њ–ї–Њ–≤–Ї–µ –њ–Њ–ї–Њ–≤–Њ–≥–Њ —З–ї–µ–љ–∞, —Г –љ–∞—А—Г–ґ–љ–Њ–≥–Њ –Њ—В–≤–µ—А—Б—В–Є—П –Љ–Њ—З–µ–Є—Б–њ—Г—Б–Ї–∞—В–µ–ї—М–љ–Њ–≥–Њ –Ї–∞–љ–∞–ї–∞, –љ–∞ –Ї–Њ–ґ–µ –њ–∞—Е–Њ–≤—Л—Е —Б–Ї–ї–∞–і–Њ–Ї, –Љ–Њ—И–Њ–љ–Ї–Є, –њ–µ—А–Є–∞–љ–∞–ї—М–љ–Њ–є –Њ–±–ї–∞—Б—В–Є. –£ –ґ–µ–љ—Й–Є–љ –Ї–Њ–љ–і–Є–ї–Њ–Љ—Л —З–∞—Й–µ –њ–Њ—А–∞–ґ–∞—О—В –±–Њ–ї—М—И–Є–µ –Є –Љ–∞–ї—Л–µ –њ–Њ–ї–Њ–≤—Л–µ –≥—Г–±—Л, –Ї–ї–Є—В–Њ—А, –љ–∞—А—Г–ґ–љ–Њ–µ –Њ—В–≤–µ—А—Б—В–Є–µ –Љ–Њ—З–µ–Є—Б–њ—Г—Б–Ї–∞—В–µ–ї—М–љ–Њ–≥–Њ –Ї–∞–љ–∞–ї–∞, –Ї–Њ–ґ—Г –њ–∞—Е–Њ–≤—Л—Е —Б–Ї–ї–∞–і–Њ–Ї, –њ–µ—А–Є–∞–љ–∞–ї—М–љ—Г—О –Њ–±–ї–∞—Б—В—М. –°–љ–∞—З–∞–ї–∞ –њ–Њ—П–≤–ї—П—О—В—Б—П –µ–і–Є–љ–Є—З–љ—Л–µ —Г–Ј–µ–ї–Ї–Є –≤–µ–ї–Є—З–Є–љ–Њ–є —Б –±—Г–ї–∞–≤–Њ—З–љ—Г—О –≥–Њ–ї–Њ–≤–Ї—Г, —А–Њ–Ј–Њ–≤–Њ–≥–Њ –Є–ї–Є —Б–µ—А–Њ–≤–∞—В–Њ-–Ї—А–∞—Б–љ–Њ–≥–Њ —Ж–≤–µ—В–∞, —Б–Њ –≤—А–µ–Љ–µ–љ–µ–Љ –Є—Е —З–Є—Б–ї–Њ —Г–≤–µ–ї–Є—З–Є–≤–∞–µ—В—Б—П. –І–∞—Й–µ –≤—Л—Б—Л–њ–∞–љ–Є—П –њ—А–µ–і—Б—В–∞–≤–ї–µ–љ—Л —Б–≥—А—Г–њ–њ–Є—А–Њ–≤–∞–љ–љ—Л–Љ–Є –Њ—В 5 –і–Њ 15 —Г–Ј–µ–ї–Ї–Њ–≤—Л–Љ–Є –Њ–±—А–∞–Ј–Њ–≤–∞–љ–Є—П–Љ–Є, –Є–љ–Њ–≥–і–∞ —Б–ї–Є–≤–∞—О—Й–Є–Љ–Є—Б—П –≤ –±–ї—П—И–Ї–Є. –£–Ј–µ–ї–Ї–Є –Љ–Њ–≥—Г—В –Є–Љ–µ—В—М –≤—Л—В—П–љ—Г—В—Г—О —Д–Њ—А–Љ—Г –≤ –≤–Є–і–µ —Б–Њ—Б–Њ—З–Ї–Њ–≤, –Љ–Њ–≥—Г—В —Б–ї–Є–≤–∞—В—М—Б—П –Љ–µ–ґ–і—Г —Б–Њ–±–Њ–є, –Њ–±—А–∞–Ј—Г—П –Њ–њ—Г—Е–Њ–ї–µ–≤–Є–і–љ—Л–µ —А–∞–Ј—А–∞—Б—В–∞–љ–Є—П, –љ–∞–њ–Њ–Љ–Є–љ–∞—О—Й–Є–µ —Ж–≤–µ—В–љ—Г—О –Ї–∞–њ—Г—Б—В—Г, –њ–µ—В—Г—И–Є–љ—Л–є –≥—А–µ–±–µ–љ—М, –Љ–∞–ї–Є–љ—Г. –¶–≤–µ—В –Њ–±—А–∞–Ј–Њ–≤–∞–љ–Є–є –љ–∞ –±–Њ–ї–µ–µ –њ–Њ–Ј–і–љ–Є—Е —Б—В–∞–і–Є—П—Е –≤–∞—А—М–Є—А—Г–µ—В –Њ—В –±–µ–ї–Њ–≤–∞—В–Њ-—В–µ–ї–µ—Б–љ–Њ–≥–Њ –і–Њ —А–Њ–Ј–Њ–≤–∞—В–Њ-—Б–Є–љ—О—И–љ–Њ–≥–Њ, —А–µ–ґ–µ –Ї—А–∞—Б–љ–Њ–≤–∞—В–Њ- –Ї–Њ—А–Є—З–љ–µ–≤–Њ–≥–Њ. –Ъ–ї–Є–љ–Є—З–µ—Б–Ї–Є –≤—Л–і–µ–ї—П—О—В —З–µ—В—Л—А–µ —В–Є–њ–∞ –Њ—Б—В—А–Њ–Ї–Њ–љ–µ—З–љ—Л—Е –Ї–Њ–љ–і–Є–ї–Њ–Љ:
• –Ґ–Є–њ–Є—З–љ—Л–µ. –Ю–±—Л—З–љ–Њ –њ–Њ—А–∞–ґ–∞—О—В –≤–ї–∞–ґ–љ—Л–µ —Г—З–∞—Б—В–Ї–Є —Б–ї–Є–Ј–Є—Б—В—Л—Е –Є –Ї–Њ–ґ–Є, —В–∞–Ї–Є–µ –Ї–∞–Ї –њ—А–µ–і–і–≤–µ—А–Є–µ –≤–ї–∞–≥–∞–ї–Є—Й–∞, –Ј–∞–і–љ–Є–є –њ—А–Њ—Е–Њ–і, –≤–љ—Г—В—А–µ–љ–љ–Є–є –ї–Є—Б—В–Њ–Ї –Ї—А–∞–є–љ–µ–є –њ–ї–Њ—В–Є. –Т—Л—Б—Л–њ–∞–љ–Є—П –љ–µ—А–µ–і–Ї–Њ –љ–∞–њ–Њ–Љ–Є–љ–∞—О—В —Ж–≤–µ—В–љ—Г—О –Ї–∞–њ—Г—Б—В—Г.
• –У–Є–њ–µ—А–Ї–µ—А–∞—В–Њ—В–Є—З–µ—Б–Ї–Є–µ. –Я—А–Є —Н—В–Њ–Љ —В–Є–њ–µ –њ–Њ–≤–µ—А—Е–љ–Њ—Б—В—М –Ї–Њ–љ–і–Є–ї–Њ–Љ –њ–Њ–Ї—А—Л—В–∞ —А–Њ–≥–Њ–≤—Л–Љ–Є –љ–∞—Б–ї–Њ–µ–љ–Є—П–Љ–Є. –І–∞—Й–µ –≤—Б–µ–≥–Њ –Њ–љ–Є —А–∞—Б–њ–Њ–ї–∞–≥–∞—О—В—Б—П –љ–∞ —Г—З–∞—Б—В–Ї–∞—Е –Ї–Њ–ґ–Є —Б –Њ—А–Њ–≥–Њ–≤–µ–≤–∞—О—Й–Є–Љ —Н–њ–Є—В–µ–ї–Є–µ–Љ (–љ–∞—А—Г–ґ–љ—Л–є –ї–Є—Б—В–Њ–Ї –Ї—А–∞–є–љ–µ–є –њ–ї–Њ—В–Є, —В–µ–ї–Њ –њ–Њ–ї–Њ–≤–Њ–≥–Њ —З–ї–µ–љ–∞, –Љ–Њ—И–Њ–љ–Ї–∞, –±–Њ–ї—М—И–Є–µ –њ–Њ–ї–Њ–≤—Л–µ –≥—Г–±—Л).
• –Я–∞–њ—Г–ї–µ–Ј–љ—Л–µ. –Ш—Е –Њ—В–ї–Є—З–Є–µ –Њ—В –≥–Є–њ–µ—А–Ї–µ—А–∞—В–Њ—В–Є—З–µ—Б–Ї–Є—Е —Б–Њ—Б—В–Њ–Є—В –≤ —В–Њ–Љ, —З—В–Њ –Њ–љ–Є –ї–Є—И–µ–љ—Л —А–Њ–≥–Њ–≤—Л—Е –љ–∞—Б–ї–Њ–µ–љ–Є–є –Є –Є–Љ–µ—О—В –≥–ї–∞–і–Ї—Г—О –њ–Њ–≤–µ—А—Е–љ–Њ—Б—В—М.
• –Я–ї–Њ—Б–Ї–Є–µ. –Я—А–Њ—П–≤–ї—П—О—В—Б—П –≤ –≤–Є–і–µ –њ—П—В–µ–љ, –Ї–Њ—В–Њ—А—Л–µ –њ–Њ—З—В–Є –љ–µ –≤–Њ–Ј–≤—Л—И–∞—О—В—Б—П –љ–∞–і –њ–Њ–≤–µ—А—Е–љ–Њ—Б—В—М—О –Ї–Њ–ґ–Є. –Ш—Е —Б–ї–Њ–ґ–љ–Њ –Ј–∞–Љ–µ—В–Є—В—М –љ–µ–≤–Њ–Њ—А—Г–ґ–µ–љ–љ—Л–Љ –≥–ї–∞–Ј–Њ–Љ. –£ 25% –ґ–µ–љ—Й–Є–љ —Н—В–Њ—В —В–Є–њ –Ї–Њ–љ–і–Є–ї–Њ–Љ –ї–Њ–Ї–∞–ї–Є–Ј—Г–µ—В—Б—П –љ–∞ —И–µ–є–Ї–µ –Љ–∞—В–Ї–Є –Є –≤–Њ –≤–ї–∞–≥–∞–ї–Є—Й–µ. –Т –њ–Њ–і–∞–≤–ї—П—О—Й–µ–Љ –±–Њ–ї—М—И–Є–љ—Б—В–≤–µ —Б–ї—Г—З–∞–µ–≤ –Њ–љ–Є —П–≤–ї—П—О—В—Б—П –њ—А–Њ—П–≤–ї–µ–љ–Є–µ–Љ —Ж–µ—А–≤–Є–Ї–∞–ї—М–љ–Њ–є –Є–ї–Є –≤–∞–≥–Є–љ–∞–ї—М–љ–Њ–є –Є–љ—В—А–∞—Н–њ–Є—В–µ–ї–Є–∞–ї—М–љ–Њ–є –љ–µ–Њ–њ–ї–∞–Ј–Є–Є, –≤–њ–Њ—Б–ї–µ–і—Б—В–≤–Є–Є —В—А–∞–љ—Б—Д–Њ—А–Љ–Є—А—Г—О—Й–µ–є—Б—П –≤ —А–∞–Ї —И–µ–є–Ї–Є –Љ–∞—В–Ї–Є [7, 8].
–Ю—Б—В—А–Њ–Ї–Њ–љ–µ—З–љ—Л–µ –Ї–Њ–љ–і–Є–ї–Њ–Љ—Л –љ–µ–Њ–±—Е–Њ–і–Є–Љ–Њ –і–Є—Д—Д–µ—А–µ–љ—Ж–Є—А–Њ–≤–∞—В—М —Б –і—А—Г–≥–Є–Љ–Є –і–µ—А–Љ–∞—В–Њ–Ј–∞–Љ–Є, —З–∞—Б—В–Њ –≤—Б—В—А–µ—З–∞—О—Й–Є–Љ–Є—Б—П –≤ –∞–љ–Њ–≥–µ–љ–Є—В–∞–ї—М–љ–Њ–є –Њ–±–ї–∞—Б—В–Є (—В–∞–±–ї. 2).
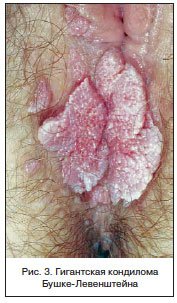
–£ –љ–µ–Ї–Њ—В–Њ—А—Л—Е –±–Њ–ї—М–љ—Л—Е —Б –≤—Л—А–∞–ґ–µ–љ–љ—Л–Љ–Є –љ–∞—А—Г—И–µ–љ–Є—П–Љ–Є –Ї–ї–µ—В–Њ—З–љ–Њ–≥–Њ –Є–Љ–Љ—Г–љ–Є—В–µ—В–∞ (–Т–Ш–І-–Є–љ—Д–µ–Ї—Ж–Є—П, –љ–∞ —Д–Њ–љ–µ –Є–Љ–Љ—Г–љ–Њ—Б—Г–њ—А–µ—Б—Б–Є–≤–љ–Њ–є —В–µ—А–∞–њ–Є–Є) –њ—А–Є –±–µ—А–µ–Љ–µ–љ–љ–Њ—Б—В–Є —А–∞–Ј–≤–Є–≤–∞—О—В—Б—П –і–Њ—Б—В–∞—В–Њ—З–љ–Њ –Ї—А—Г–њ–љ—Л–µ –≥–µ–љ–Є—В–∞–ї—М–љ—Л–µ –±–Њ—А–Њ–і–∞–≤–Ї–Є – –≥–Є–≥–∞–љ—В—Б–Ї–∞—П –Ї–Њ–љ–і–Є–ї–Њ–Љ–∞ –С—Г—И–Ї–µ-–Ы–µ–≤–µ–љ—И—В–µ–є–љ–∞ (—А–Є—Б. 3). –≠—В–∞ –њ—А–µ–і—А–∞–Ї–Њ–≤–∞—П –Є–љ–≤–∞–Ј–Є–≤–љ–∞—П –Є –і–µ—Б—В—А—Г–Ї—В–Є—А—Г—О—Й–∞—П –Њ–њ—Г—Е–Њ–ї—М –∞—Б—Б–Њ—Ж–Є–Є—А—Г–µ—В—Б—П —Б –Т–Я–І-6 –Є –Т–Я–І-11. –Т —А–µ–Ј—Г–ї—М—В–∞—В–µ –±—Л—Б—В—А–Њ–≥–Њ —А–Њ—Б—В–∞ –Є —Б–ї–Є—П–љ–Є—П –Њ—В–і–µ–ї—М–љ—Л—Е –Ї–Њ–љ–і–Є–ї–Њ–Љ –Њ–±—А–∞–Ј—Г–µ—В—Б—П –≥–Є–≥–∞–љ—В—Б–Ї–∞—П –Ї–Њ–љ–і–Є–ї–Њ–Љ–∞ –љ–∞ —И–Є—А–Њ–Ї–Њ–Љ –Њ—Б–љ–Њ–≤–∞–љ–Є–Є. –Э–∞ –µ–µ –њ–Њ–≤–µ—А—Е–љ–Њ—Б—В–Є —Д–Њ—А–Љ–Є—А—Г—О—В—Б—П –≤–µ–≥–µ—В–∞—Ж–Є–Є, –њ–Њ–Ї—А—Л—В—Л–µ —А–Њ–≥–Њ–≤—Л–Љ–Є —З–µ—И—Г–є–Ї–∞–Љ–Є, –≤–Њ—А—Б–Є–љ—З–∞—В–Њ–њ–Њ–і–Њ–±–љ—Л–µ –Њ–±—А–∞–Ј–Њ–≤–∞–љ–Є—П, —А–∞–Ј–і–µ–ї–µ–љ–љ—Л–µ –±–Њ—А–Њ–Ј–і–Ї–∞–Љ–Є, –≤ –Ї–Њ—В–Њ—А—Л—Е —Б–Ї–∞–њ–ї–Є–≤–∞–µ—В—Б—П —Н–Ї—Б—Б—Г–і–∞—В —Б –љ–µ–њ—А–Є—П—В–љ—Л–Љ –Ј–∞–њ–∞—Е–Њ–Љ. –Ґ–µ—З–µ–љ–Є–µ –љ–µ—Г–Ї–ї–Њ–љ–љ–Њ –њ—А–Њ–≥—А–µ—Б—Б–Є—А—Г—О—Й–µ–µ —Б –њ—А–Њ—А–∞—Б—В–∞–љ–Є–µ–Љ –≤ –њ–Њ–і–ї–µ–ґ–∞—Й–Є–µ —В–Ї–∞–љ–Є. –С–µ–Ј –ї–µ—З–µ–љ–Є—П –≥–Є–≥–∞–љ—В—Б–Ї–∞—П –Ї–Њ–љ–і–Є–ї–Њ–Љ–∞ —В—А–∞–љ—Б—Д–Њ—А–Љ–Є—А—Г–µ—В—Б—П –≤ –њ–ї–Њ—Б–Ї–Њ–Ї–ї–µ—В–Њ—З–љ—Л–є —А–∞–Ї –Ї–Њ–ґ–Є. –Т –Њ—В–ї–Є—З–Є–µ –Њ—В –Љ–љ–Њ–≥–Є—Е –і—А—Г–≥–Є—Е –Ш–Я–Я–Я –њ—А–Њ—П–≤–ї–µ–љ–Є—П –Т–Я–І –љ–µ —Б–≤—П–Ј–∞–љ—Л —Б –љ–µ–Љ–µ–і–ї–µ–љ–љ—Л–Љ —А–∞–Ј–≤–Є—В–Є–µ–Љ —В–∞–Ї–Є—Е —Б–Є–Љ–њ—В–Њ–Љ–Њ–≤, –Ї–∞–Ї –Ј—Г–і, –ґ–ґ–µ–љ–Є–µ, –њ–Њ—П–≤–ї–µ–љ–Є–µ –≤—Л–і–µ–ї–µ–љ–Є–є –Є–Ј –њ–Њ–ї–Њ–≤—Л—Е –Њ—А–≥–∞–љ–Њ–≤. –Ю—Б—В—А–Њ–Ї–Њ–љ–µ—З–љ—Л–µ –Ї–Њ–љ–і–Є–ї–Њ–Љ—Л –Њ–±—Л—З–љ–Њ –±–µ—Б—Б–Є–Љ–њ—В–Њ–Љ–љ—Л –Є —З–∞—Б—В–Њ —Б–ї—Г—З–∞–є–љ–Њ –≤—Л—П–≤–ї—П—О—В—Б—П —Б–∞–Љ–Є–Љ –±–Њ–ї—М–љ—Л–Љ –Є–ї–Є –≤—А–∞—З–Њ–Љ –њ—А–Є –Њ—Б–Љ–Њ—В—А–µ. –Ю–і–љ–∞–Ї–Њ –і–ї–Є—В–µ–ї—М–љ–Њ —Б—Г—Й–µ—Б—В–≤—Г—О—Й–Є–µ, –Ї—А—Г–њ–љ—Л–µ –Є–ї–Є —В—А–∞–≤–Љ–Є—А–Њ–≤–∞–љ–љ—Л–µ, –Є–Ј—К—П–Ј–≤–ї–µ–љ–љ—Л–µ –Є–ї–Є –њ–Њ–і–≤–µ—А–≥—И–Є–µ—Б—П –≤—В–Њ—А–Є—З–љ–Њ–Љ—Г –Є–љ—Д–Є—Ж–Є—А–Њ–≤–∞–љ–Є—О –±–Њ—А–Њ–і–∞–≤–Ї–Є —Б–Њ–њ—А–Њ–≤–Њ–ґ–і–∞—О—В—Б—П –Ј—Г–і–Њ–Љ, –±–Њ–ї—М—О, –љ–µ–њ—А–Є—П—В–љ—Л–Љ –Ј–∞–њ–∞—Е–Њ–Љ –Є –≥–љ–Њ–є–љ—Л–Љ –Њ—В–і–µ–ї—П–µ–Љ—Л–Љ [9].
–Т –љ–∞—Б—В–Њ—П—Й–µ–µ –≤—А–µ–Љ—П —Б—Г—Й–µ—Б—В–≤—Г–µ—В –Љ–љ–Њ–ґ–µ—Б—В–≤–Њ –Љ–µ—В–Њ–і–Њ–≤ –ї–µ—З–µ–љ–Є—П –≥–µ–љ–Є—В–∞–ї—М–љ—Л—Е –±–Њ—А–Њ–і–∞–≤–Њ–Ї. –Ю–і–љ–∞–Ї–Њ –њ–Њ—Б—В–Њ—П–љ–љ–Њ–≥–Њ –≤—Л—Б–Њ–Ї–Њ–≥–Њ —В–µ—А–∞–њ–µ–≤—В–Є—З–µ—Б–Ї–Њ–≥–Њ —Н—Д—Д–µ–Ї—В–∞ –љ–µ –≥–∞—А–∞–љ—В–Є—А—Г–µ—В –љ–Є –Њ–і–Є–љ –Є–Ј –љ–Є—Е, —В. –Ї. –љ–Є –Њ–і–Є–љ –љ–µ –Њ–±–µ—Б–њ–µ—З–Є–≤–∞–µ—В —Н—А–∞–і–Є–Ї–∞—Ж–Є–Є –Т–Я–І. –°—А–µ–і–љ—П—П —З–∞—Б—В–Њ—В–∞ —А–µ—Ж–Є–і–Є–≤–Є—А–Њ–≤–∞–љ–Є—П –і–Њ—Б—В–Є–≥–∞–µ—В 25–30% –≤ —В–µ—З–µ–љ–Є–µ 3-—Е –Љ–µ—Б. –њ–Њ—Б–ї–µ –ї–µ—З–µ–љ–Є—П. –Т—Л–±–Њ—А –Љ–µ—В–Њ–і–∞ –ї–µ—З–µ–љ–Є—П –Ј–∞–≤–Є—Б–Є—В –Њ—В –ї–Њ–Ї–∞–ї–Є–Ј–∞—Ж–Є–Є, —А–∞–Ј–Љ–µ—А–∞ –Є —В–Є–њ–∞ –Ї–Њ–љ–і–Є–ї–Њ–Љ, –∞ —В–∞–Ї–ґ–µ –Њ—В –≤–Њ–Ј—А–∞—Б—В–∞ –Є –Ї–Њ–Љ–њ–ї–∞–µ–љ—В–љ–Њ—Б—В–Є –њ–∞—Ж–Є–µ–љ—В–∞. –Я—А–Є –Њ—В—Б—Г—В—Б—В–≤–Є–Є —В–µ—А–∞–њ–Є–Є –≤–Њ–Ј–Љ–Њ–ґ–љ–Њ –њ–Њ—П–≤–ї–µ–љ–Є–µ –љ–Њ–≤—Л—Е –Њ—З–∞–≥–Њ–≤ –њ–Њ—А–∞–ґ–µ–љ–Є—П, —А–∞—Б–њ—А–Њ—Б—В—А–∞–љ–µ–љ–Є–µ –≤–Є—А—Г—Б–∞ –љ–∞ —А–∞–љ–µ–µ –љ–µ –њ–Њ—А–∞–ґ–µ–љ–љ—Л–µ —Г—З–∞—Б—В–Ї–Є –Ї–Њ–ґ–Є, –∞ —В–∞–Ї–ґ–µ –њ–µ—А–µ–і–∞—З–∞ –≤–Є—А—Г—Б–∞ –і—А—Г–≥–Є–Љ –ї—О–і—П–Љ. –°–ї–µ–і—Г–µ—В –≤ –Њ–±—П–Ј–∞—В–µ–ї—М–љ–Њ–Љ –њ–Њ—А—П–і–Ї–µ –Њ–±—Б–ї–µ–і–Њ–≤–∞—В—М —Б–µ–Ї—Б—Г–∞–ї—М–љ—Л—Е –њ–∞—А—В–љ–µ—А–Њ–≤ –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –∞–љ–Њ–≥–µ–љ–Є—В–∞–ї—М–љ—Л–Љ–Є –Ї–Њ–љ–і–Є–ї–Њ–Љ–∞–Љ–Є, –≤–Ї–ї—О—З–∞—П –Њ–±—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ —И–µ–є–Ї–Є –Љ–∞—В–Ї–Є –Є –≤–Ј—П—В–Є–µ –Љ–∞–Ј–Ї–∞ –њ–Њ –Я–∞–њ–∞–љ–Є–Ї–Њ–ї–∞—Г. –Э–µ–Њ–±—Е–Њ–і–Є–Љ–Њ —В–∞–Ї–ґ–µ –Њ–±—Б–ї–µ–і–Њ–≤–∞—В—М –љ–∞ –Т–Я–І –Љ—Г–ґ—З–Є–љ, —П–≤–ї—П—О—Й–Є—Е—Б—П –њ–Њ–ї–Њ–≤—Л–Љ–Є –њ–∞—А—В–љ–µ—А–∞–Љ–Є –ґ–µ–љ—Й–Є–љ —Б –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П–Љ–Є —И–µ–є–Ї–Є –Љ–∞—В–Ї–Є. –Ю–±–∞ –њ–Њ–ї–Њ–≤—Л—Е –њ–∞—А—В–љ–µ—А–∞ –і–Њ–ї–ґ–љ—Л –±—Л—В—М –њ—А–Њ–ї–µ—З–µ–љ—Л –Њ–і–љ–Њ–≤—А–µ–Љ–µ–љ–љ–Њ [10].
–Т –±–Њ–ї—М—И–Є–љ—Б—В–≤–µ —Б–ї—Г—З–∞–µ–≤ –њ—А–Є–Љ–µ–љ—П—О—В —В–Њ–њ–Є—З–µ—Б–Ї–Є–µ –њ—А–µ–њ–∞—А–∞—В—Л –Є —Д–Є–Ј–Є—З–µ—Б–Ї–Є–µ –Љ–µ—В–Њ–і—Л —В–µ—А–∞–њ–Є–Є, –љ–∞–њ—А–∞–≤–ї–µ–љ–љ—Л–µ –љ–∞ –і–µ—Б—В—А—Г–Ї—Ж–Є—О —Н–њ–Є–і–µ—А–Љ–∞–ї—М–љ—Л—Е —А–∞–Ј—А–∞—Б—В–∞–љ–Є–є –Є–ї–Є –Є–љ–і—Г–Ї—Ж–Є—О —Ж–Є—В–Њ—В–Њ–Ї—Б–Є—З–љ–Њ—Б—В–Є –њ—А–Њ—В–Є–≤ –Є–љ—Д–Є—Ж–Є—А–Њ–≤–∞–љ–љ—Л—Е –Ї–ї–µ—В–Њ–Ї. –Я—А–Є —А–∞—Б–њ—А–Њ—Б—В—А–∞–љ–µ–љ–љ—Л—Е –≤—Л—Б—Л–њ–∞–љ–Є—П—Е, –і–ї–Є—В–µ–ї—М–љ–Њ–Љ —А–µ—Ж–Є–і–Є–≤–Є—А—Г—О—Й–µ–Љ —В–µ—З–µ–љ–Є–Є –њ—А–Њ—Ж–µ—Б—Б–∞, –Њ—В—Б—Г—В—Б—В–≤–Є–Є —Н—Д—Д–µ–Ї—В–∞ –Њ—В –њ—А–Є–Љ–µ–љ—П–µ–Љ—Л—Е –ї–Њ–Ї–∞–ї—М–љ—Л—Е –Љ–µ—В–Њ–і–Њ–≤ —В–µ—А–∞–њ–Є–Є –њ—А–Є—Б–Њ–µ–і–Є–љ—П—О—В –Є–Љ–Љ—Г–љ–Њ–Љ–Њ–і—Г–ї—П—В–Њ—А—Л, —Б—В–Є–Љ—Г–ї–Є—А—Г—О—Й–Є–µ –Ї–ї–µ—В–Њ—З–љ—Л–є –Є–Љ–Љ—Г–љ–Є—В–µ—В –њ—А–Є –Т–Я–І (–Є–љ–Њ–Ј–Є–љ –њ—А–∞–љ–Њ–±–µ–Ї—Б, —Ж–Є–Љ–µ—В–Є–і–Є–љ, –Љ–µ–≥–ї—О–Љ–Є–љ–∞ –∞–Ї—А–Є–і–Њ–љ–∞—Ж–µ—В–∞—В, –Њ–Ї—Б–Њ–і–Є–≥–Є–і—А–Њ–∞–Ї—А–Є–і–Є–љ–Є–ї–∞—Ж–µ—В–∞—В –љ–∞—В—А–Є—П, —А–µ–Ї–Њ–Љ–±–Є–љ–∞–љ—В–љ—Л–є –Ш–§–Э-α). –Ф–ї—П –ї–µ—З–µ–љ–Є—П —А–µ—Д—А–∞–Ї—В–µ—А–љ—Л—Е –≥–µ–љ–Є—В–∞–ї—М–љ—Л—Е –±–Њ—А–Њ–і–∞–≤–Њ–Ї –Є—Б–њ–Њ–ї—М–Ј—Г—О—В —А–µ–Ї–Њ–Љ–±–Є–љ–∞–љ—В–љ—Л–µ –Є–љ—В–µ—А—Д–µ—А–Њ–љ—Л –≤ –≤–Є–і–µ –≤–љ—Г—В—А–Є–Њ—З–∞–≥–Њ–≤—Л—Е –Є–љ—К–µ–Ї—Ж–Є–є –Є–ї–Є –≤ —Д–Њ—А–Љ–µ —Б—Г–њ–њ–Њ–Ј–Є—В–Њ—А–Є–µ–≤: –≤–Є—Д–µ—А–Њ–љ, –≥–µ–љ—Д–µ—А–Њ–љ. –Ч–∞ —А—Г–±–µ–ґ–Њ–Љ –і–ї—П –ї–µ—З–µ–љ–Є—П —Г–њ–Њ—А–љ–Њ –њ—А–Њ—В–µ–Ї–∞—О—Й–Є—Е –Ї–Њ–љ–і–Є–ї–Њ–Љ –Є—Б–њ–Њ–ї—М–Ј—Г–µ—В—Б—П –Љ–Њ–і—Г–ї—П—В–Њ—А –Є–Љ–Љ—Г–љ–љ–Њ–≥–Њ –Њ—В–≤–µ—В–∞ —Б –Њ–≥—А–∞–љ–Є—З–µ–љ–љ—Л–Љ –њ—А–Є–Љ–µ–љ–µ–љ–Є–µ–Љ – 5% –Ї—А–µ–Љ –Є–Љ–Є—Е–Є–Љ–Њ–і. –Т —Б–≤—П–Ј–Є —Б –њ–ї–Њ—Е–Њ–є –њ–µ–љ–µ—В—А–∞—Ж–Є–µ–є –њ—А–µ–њ–∞—А–∞—В–∞ –≤ –Ї–Њ–ґ—Г —Б–љ–∞—З–∞–ї–∞ –њ—А–Њ–≤–Њ–і—П—В –ї–µ—З–µ–љ–Є–µ –ґ–Є–і–Ї–Є–Љ –∞–Ј–Њ—В–Њ–Љ, –Ј–∞—В–µ–Љ –љ–∞–љ–Њ—Б—П—В –њ—А–µ–њ–∞—А–∞—В 17% —Б–∞–ї–Є—Ж–Є–ї–Њ–≤–Њ–є –Ї–Є—Б–ї–Њ—В—Л –љ–∞ –љ–Њ—З—М, –∞ —Г—В—А–Њ–Љ –Є–Љ–Є—Е–Є–Љ–Њ–і –њ–Њ–і –Њ–Ї–Ї–ї—О–Ј–Є—О. –Ъ—Г—А—Б –ї–µ—З–µ–љ–Є—П – 6–9 –љ–µ–і., —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В—М –Љ–µ—В–Њ–і–∞ —Б–Њ—Б—В–∞–≤–ї—П–µ—В 50–100% [11, 12].
–Т –Ї–∞—З–µ—Б—В–≤–µ –њ–Њ—Б—В–Њ—П–љ–љ–Њ–≥–Њ –Њ–±—П–Ј–∞—В–µ–ї—М–љ–Њ–≥–Њ —В–µ—А–∞–њ–µ–≤—В–Є—З–µ—Б–Ї–Њ–≥–Њ –Ї–Њ–Љ–њ–Њ–љ–µ–љ—В–∞ –Є—Б–њ–Њ–ї—М–Ј—Г—О—В –Љ–µ—В–Њ–і—Л, –љ–∞–њ—А–∞–≤–ї–µ–љ–љ—Л–µ –љ–∞ –і–µ—Б—В—А—Г–Ї—Ж–Є—О –Њ–±—А–∞–Ј–Њ–≤–∞–љ–Є–є. –≠—В–Є –Љ–µ—В–Њ–і—Л –≤ –њ–µ—А–≤—Г—О –Њ—З–µ—А–µ–і—М –њ—А–Њ–≤–Њ–і—П—В—Б—П –±–Њ–ї—М–љ—Л–Љ —Б –±–Њ–ї—М—И–Є–Љ–Є –њ–Њ —А–∞–Ј–Љ–µ—А—Г –±–Њ—А–Њ–і–∞–≤–Ї–∞–Љ–Є, –≤—Л–Ј—Л–≤–∞—О—Й–Є–Љ–Є –і–Є—Б–Ї–Њ–Љ—Д–Њ—А—В, –±–Њ–ї–µ–Ј–љ–µ–љ–љ–Њ—Б—В—М –њ—А–Є —Е–Њ–і—М–±–µ –Є–ї–Є –Є–Ј-–Ј–∞ –Ї–Њ—Б–Љ–µ—В–Є—З–µ—Б–Ї–Є—Е –њ—А–Њ–±–ї–µ–Љ –≤–љ–µ—И–љ–µ–≥–Њ –≤–Є–і–∞. –Ь–µ—В–Њ–і—Л –Љ–Њ–ґ–љ–Њ —Г—Б–ї–Њ–≤–љ–Њ —А–∞–Ј–і–µ–ї–Є—В—М –љ–∞ –і–≤–µ –≥—А—Г–њ–њ—Л: —В–µ, –Ї–Њ—В–Њ—А—Л–µ –њ–∞—Ж–Є–µ–љ—В—Л –Љ–Њ–≥—Г—В –њ–Њ—Б–ї–µ –Ї–Њ–љ—Б—Г–ї—М—В–∞—Ж–Є–Є —Б –≤—А–∞—З–Њ–Љ –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞—В—М —Б–∞–Љ–Њ—Б—В–Њ—П—В–µ–ї—М–љ–Њ, –Є –Љ–µ—В–Њ–і—Л, –Њ—Б—Г—Й–µ—Б—В–≤–ї—П–µ–Љ—Л–µ –≤—А–∞—З–Њ–Љ. –Ъ –Њ–і–љ–Њ–Љ—Г –Є–Ј –љ–∞–Є–±–Њ–ї–µ–µ —З–∞—Б—В–Њ –њ—А–Є–Љ–µ–љ—П–µ–Љ—Л—Е –≤—А–∞—З–µ–±–љ—Л—Е –Љ–µ—В–Њ–і–Њ–≤ –Њ—В–љ–Њ—Б–Є—В—Б—П –Ї—А–Є–Њ–і–µ—Б—В—А—Г–Ї—Ж–Є—П (–љ–∞–љ–µ—Б–µ–љ–Є–µ –ґ–Є–і–Ї–Њ–≥–Њ –∞–Ј–Њ—В–∞ –љ–∞ –±–Њ—А–Њ–і–∞–≤–Ї—Г –≤ —В–µ—З–µ–љ–Є–µ 30–40 —Б). –Я—А–Њ—Ж–µ–і—Г—А—Г –њ–Њ–≤—В–Њ—А—П—О—В –љ–µ—Б–Ї–Њ–ї—М–Ї–Њ —А–∞–Ј —Б –Є–љ—В–µ—А–≤–∞–ї–Њ–Љ –≤ –љ–µ—Б–Ї–Њ–ї—М–Ї–Њ –љ–µ–і–µ–ї—М –і–Њ –њ–Њ–ї–љ–Њ–≥–Њ –≤—Л–Ј–і–Њ—А–Њ–≤–ї–µ–љ–Є—П. –Э–µ—А–µ–і–Ї–Њ –њ—А–Є–±–µ–≥–∞—О—В –Ї —Н–ї–µ–Ї—В—А–Њ–Ї–Њ–∞–≥—Г–ї—П—Ж–Є–Є, –Ї–Њ—В–Њ—А–∞—П –±–Њ–ї–µ–µ —Н—Д—Д–µ–Ї—В–Є–≤–љ–∞, –љ–Њ —В—А–µ–±—Г–µ—В –њ—А–µ–і–≤–∞—А–Є—В–µ–ї—М–љ–Њ–≥–Њ –Њ–±–µ–Ј–±–Њ–ї–Є–≤–∞–љ–Є—П, —В. –Ї. —Б–Њ–њ—А–Њ–≤–Њ–ґ–і–∞–µ—В—Б—П –≤—Л—А–∞–ґ–µ–љ–љ–Њ–є –±–Њ–ї–µ–Ј–љ–µ–љ–љ–Њ—Б—В—М—О –Є –Љ–Њ–ґ–µ—В –њ—А–Є–≤–Њ–і–Є—В—М –Ї —А—Г–±—Ж–µ–≤–∞–љ–Є—О. –Ы–∞–Ј–µ—А–љ–∞—П —В–µ—А–∞–њ–Є—П (–Є—Б–њ–Њ–ї—М–Ј—Г—О—В —Г–≥–ї–µ–Ї–Є—Б–ї—Л–є –ї–∞–Ј–µ—А) –њ—А–Є–Љ–µ–љ—П–µ—В—Б—П –њ—А–Є –љ–µ—Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В–Є –і—А—Г–≥–Є—Е –Љ–µ—В–Њ–і–Њ–≤. –°—Г—Й–µ—Б—В–≤–µ–љ–љ—Л–Љ–Є –љ–µ–і–Њ—Б—В–∞—В–Ї–∞–Љ–Є –њ–Њ—Б–ї–µ–і–љ–Є—Е –і–≤—Г—Е –Љ–µ—В–Њ–і–Њ–≤ —П–≤–ї—П—О—В—Б—П –і–Њ—А–Њ–≥–Њ–≤–Є–Ј–љ–∞, –±–Њ–ї–µ–Ј–љ–µ–љ–љ–Њ—Б—В—М –Є —А—Г–±—Ж–Њ–≤—Л–µ –Є–Ј–Љ–µ–љ–µ–љ–Є—П —В–Ї–∞–љ–µ–є. –Ф–ї—П –њ—А–Є–Љ–µ–љ–µ–љ–Є—П –Љ–µ—В–Њ–і–Њ–≤ —Д–Є–Ј–Є—З–µ—Б–Ї–Њ–є –і–µ—Б—В—А—Г–Ї—Ж–Є–Є –љ–µ–Њ–±—Е–Њ–і–Є–Љ—Л —Б–њ–µ—Ж–Є–∞–ї–Є–Ј–Є—А–Њ–≤–∞–љ–љ–Њ–µ –њ–Њ–Љ–µ—Й–µ–љ–Є–µ, –Њ–±—Г—З–µ–љ–љ—Л–є –Љ–µ–і–Є—Ж–Є–љ—Б–Ї–Є–є –њ–µ—А—Б–Њ–љ–∞–ї, –Є–Љ–µ—О—Й–Є–є —Б–µ—А—В–Є—Д–Є–Ї–∞—В –љ–∞ –і–∞–љ–љ—Л–є –≤–Є–і –і–µ—П—В–µ–ї—М–љ–Њ—Б—В–Є, —З—В–Њ —Б—Г—Й–µ—Б—В–≤–µ–љ–љ–Њ –Њ–≥—А–∞–љ–Є—З–Є–≤–∞–µ—В –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є–µ —Н—В–Є—Е –Љ–µ—В–Њ–і–Є–Ї –≤ —И–Є—А–Њ–Ї–Њ–є –њ—А–∞–Ї—В–Є–Ї–µ [13, 14].
–Т —Б–Њ–≤—А–µ–Љ–µ–љ–љ–Њ–є —В–µ—А–∞–њ–Є–Є –∞–љ–Њ–≥–µ–љ–Є—В–∞–ї—М–љ—Л—Е –±–Њ—А–Њ–і–∞–≤–Њ–Ї –љ–∞–Є–±–Њ–ї–µ–µ –∞–Ї—В–Є–≤–љ–Њ –Є—Б–њ–Њ–ї—М–Ј—Г—О—В—Б—П –Љ–µ—В–Њ–і—Л —Е–Є–Љ–Є—З–µ—Б–Ї–Њ–є –і–µ—Б—В—А—Г–Ї—Ж–Є–Є, –Ї–Њ—В–Њ—А—Л–µ –њ–∞—Ж–Є–µ–љ—В—Л –њ—А–Є–Љ–µ–љ—П—О—В —Б–∞–Љ–Њ—Б—В–Њ—П—В–µ–ї—М–љ–Њ –њ–Њ–і —А—Г–Ї–Њ–≤–Њ–і—Б—В–≤–Њ–Љ –≤—А–∞—З–∞, —В. –Ї. –Њ–љ–Є –±–µ–Ј–±–Њ–ї–µ–Ј–љ–µ–љ–љ—Л –Є –Љ–∞–ї–Њ–Ј–∞—В—А–∞—В–љ—Л. –Р–љ–∞–ї–Є–Ј –і–∞–љ–љ—Л—Е –ї–Є—В–µ—А–∞—В—Г—А—Л –њ–Њ–Ї–∞–Ј–∞–ї –њ—А–µ–Є–Љ—Г—Й–µ—Б—В–≤–Њ –њ–Њ–і–Њ—Д–Є–ї–ї–Њ—В–Њ–Ї—Б–Є–љ–∞ –Є –њ—А–µ–њ–∞—А–∞—В–Њ–≤ –љ–∞ –Њ—Б–љ–Њ–≤–µ –Ї—А–µ–њ–Ї–Є—Е –Ї–Є—Б–ї–Њ—В –њ–Њ –њ–Њ–Ї–∞–Ј–∞—В–µ–ї—О –Ј–∞—В—А–∞—В–љ–Њ—Б—В—М–—Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В—М. –Э–∞ —Н—В–Њ–Љ –Њ—Б–љ–Њ–≤–∞–љ–Є–Є –і–∞–љ–љ—Л–µ –њ—А–µ–њ–∞—А–∞—В—Л —А–µ–Ї–Њ–Љ–µ–љ–і—Г—О—В—Б—П –Ї–∞–Ї –њ—А–µ–њ–∞—А–∞—В—Л –њ–µ—А–≤–Њ–є –ї–Є–љ–Є–Є –і–ї—П –ї–µ—З–µ–љ–Є—П –Њ—Б—В—А–Њ–Ї–Њ–љ–µ—З–љ—Л—Е –Ї–Њ–љ–і–Є–ї–Њ–Љ. –Я—А–Є –Њ—Б—В—А–Њ–Ї–Њ–љ–µ—З–љ—Л—Е –Ї–Њ–љ–і–Є–ї–Њ–Љ–∞—Е —Б —Г—Б–њ–µ—Е–Њ–Љ –Є—Б–њ–Њ–ї—М–Ј—Г—О—В —Ж–Є—В–Њ—В–Њ–Ї—Б–Є—З–µ—Б–Ї–Є–µ –њ—А–µ–њ–∞—А–∞—В—Л: –њ–Њ–і–Њ—Д–Є–ї–ї–Є–љ, –њ–Њ–і–Њ—Д–Є–ї–ї–Њ—В–Њ–Ї—Б–Є–љ (–Њ—З–Є—Й–µ–љ–љ—Л–є –∞–Ї—В–Є–≤–љ—Л–є –Ї–Њ–Љ–њ–Њ–љ–µ–љ—В –њ–Њ–і–Њ—Д–Є–ї–ї–Є–љ–∞). –Я–Њ—Б–ї–µ–і–љ–Є–є –≤ –≤–Є–і–µ —А–∞—Б—В–≤–Њ—А–∞ –Є–ї–Є –≥–µ–ї—П –љ–∞–љ–Њ—Б—П—В 2 —А./—Б—Г—В —Б –Є–љ—В–µ—А–≤–∞–ї–Њ–Љ –≤ 12 —З –≤ —В–µ—З–µ–љ–Є–µ 3–—Е –і–љ–µ–є. –Ч–∞—В–µ–Љ –і–µ–ї–∞—О—В –њ–µ—А–µ—А—Л–≤ –љ–∞ 4–7 –і–љ–µ–є. –Я—А–Є –љ–µ–Њ–±—Е–Њ–і–Є–Љ–Њ—Б—В–Є —Ж–Є–Ї–ї –ї–µ—З–µ–љ–Є—П –њ–Њ–≤—В–Њ—А—П—О—В –і–Њ 4 —А–∞–Ј –і–Њ –њ–Њ–ї–љ–Њ–≥–Њ –Є—Б—З–µ–Ј–љ–Њ–≤–µ–љ–Є—П –Ї–Њ–љ–і–Є–ї–Њ–Љ.
–Я—А–µ–њ–∞—А–∞—В–∞–Љ–Є –≤—Л–±–Њ—А–∞, —Б–Њ–і–µ—А–ґ–∞—Й–Є–Љ–Є –≤ —Б–≤–Њ–µ–Љ —Б–Њ—Б—В–∞–≤–µ –Ї—А–µ–њ–Ї–Є–µ –Ї–Є—Б–ї–Њ—В—Л, —П–≤–ї—П—О—В—Б—П –і—Г–Њ—Д–Є–ї–Љ, –Ї–Њ–ї–ї–Њ–Љ–∞–Ї, —Б–Њ–ї–Ї–Њ–і–µ—А–Љ. –Ю–і–љ–Є–Љ –Є–Ј –љ–∞–Є–±–Њ–ї–µ–µ –≤–Њ—Б—В—А–µ–±–Њ–≤–∞–љ–љ—Л—Е –Є —Е–Њ—А–Њ—И–Њ –Ј–∞—А–µ–Ї–Њ–Љ–µ–љ–і–Њ–≤–∞–≤—И–Є—Е —Б–µ–±—П –≤ —В–µ—А–∞–њ–Є–Є –Њ—Б—В—А–Њ–Ї–Њ–љ–µ—З–љ—Л—Е –Ї–Њ–љ–і–Є–ї–Њ–Љ –±–µ–Ј—А–µ—Ж–µ–њ—В—Г—А–љ—Л—Е –Ї–µ—А–∞—В–Њ–ї–Є—В–Є—З–µ—Б–Ї–Є—Е –њ—А–µ–њ–∞—А–∞—В–Њ–≤, —Б–Њ–і–µ—А–ґ–∞—Й–Є—Е —Б–∞–ї–Є—Ж–Є–ї–Њ–≤—Г—О –Ї–Є—Б–ї–Њ—В—Г, —П–≤–ї—П–µ—В—Б—П –њ—А–µ–њ–∞—А–∞—В –Ї–Њ–ї–ї–Њ–Љ–∞–Ї –≤ –≤–Є–і–µ —А–∞—Б—В–≤–Њ—А–∞. –Ъ–Њ–ї–ї–Њ–Љ–∞–Ї – —Н—В–Њ –Љ–љ–Њ–≥–Њ–Ї–Њ–Љ–њ–Њ–љ–µ–љ—В–љ—Л–є –њ—А–µ–њ–∞—А–∞—В, –≤ —Б–Њ—Б—В–∞–≤ –Ї–Њ—В–Њ—А–Њ–≥–Њ, –њ–Њ–Љ–Є–Љ–Њ 2,0 –≥ —Б–∞–ї–Є—Ж–Є–ї–Њ–≤–Њ–є –Ї–Є—Б–ї–Њ—В—Л, –≤—Е–Њ–і—П—В 0,5 –≥ –Љ–Њ–ї–Њ—З–љ–Њ–є –Ї–Є—Б–ї–Њ—В—Л –Є 0,2 –≥ –њ–Њ–ї–Є–і–Њ–Ї–∞–љ–Њ–ї–∞, —П–≤–ї—П—О—Й–µ–≥–Њ—Б—П —Н–Љ—Г–ї—М–≥–∞—В–Њ—А–Њ–Љ. –Ъ—А–Њ–Љ–µ —В–Њ–≥–Њ, –≤ –µ–≥–Њ —Б–Њ—Б—В–∞–≤ –≤–Ї–ї—О—З–µ–љ—Л —Б–њ–µ—Ж–Є–∞–ї—М–љ—Л–µ –љ–∞–њ–Њ–ї–љ–Є—В–µ–ї–Є: –њ–ї–µ–љ–Ї–Њ–Њ–±—А–∞–Ј—Г—О—Й–µ–µ –≤–µ—Й–µ—Б—В–≤–Њ (—Н—В–Є–ї—Ж–µ–ї–ї—О–ї–Њ–Ј–∞ 5,5%), –њ–ї–∞—Б—В–Є—Д–Є–Ї–∞—В–Њ—А (–і–Є–±—Г—В–Є–ї—Д—В–∞–ї–∞—В 1%), —А–∞—Б—В–≤–Њ—А–Є—В–µ–ї–Є (–∞—Ж–µ—В–Њ–љ 6,65%). –°–∞–ї–Є—Ж–Є–ї–Њ–≤–∞—П –Ї–Є—Б–ї–Њ—В–∞ –Њ–Ї–∞–Ј—Л–≤–∞–µ—В –Ї–µ—А–∞—В–Њ–ї–Є—В–Є—З–µ—Б–Ї–Њ–µ –і–µ–є—Б—В–≤–Є–µ, –Њ–±–ї–∞–і–∞–µ—В —Б–ї–∞–±–Њ–є –њ—А–Њ—В–Є–≤–Њ–Љ–Є–Ї—А–Њ–±–љ–Њ–є –∞–Ї—В–Є–≤–љ–Њ—Б—В—М—О. –Ь–Њ–ї–Њ—З–љ–∞—П –Ї–Є—Б–ї–Њ—В–∞ —Б–њ–Њ—Б–Њ–±—Б—В–≤—Г–µ—В —Е–Є–Љ–Є—З–µ—Б–Ї–Њ–є –і–µ—Б—В—А—Г–Ї—Ж–Є–Є –Ї–Њ–љ–і–Є–ї–Њ–Љ, –њ–Њ–ї–Є–і–Њ–Ї–∞–љ–Њ–ї –≤—Л–Ј—Л–≤–∞–µ—В —Б–Ї–ї–µ—А–Њ–Ј–Є—А–Њ–≤–∞–љ–Є–µ –Є –Њ–±–ї–Є—В–µ—А–∞—Ж–Є—О –Љ–µ–ї–Ї–Є—Е –≤–µ–љ –Є –∞—А—В–µ—А–Є–є –≤ –Љ–µ—Б—В–µ –љ–∞–љ–µ—Б–µ–љ–Є—П. –Я—А–µ–њ–∞—А–∞—В –љ–∞–љ–Њ—Б—П—В —Б –њ–Њ–Љ–Њ—Й—М—О –∞–њ–њ–ї–Є–Ї–∞—В–Њ—А–∞ –љ–∞ –Ї–Њ–љ–і–Є–ї–Њ–Љ—Г 1–2 —А./—Б—Г—В. –Ф–ї–Є—В–µ–ї—М–љ–Њ—Б—В—М –ї–µ—З–µ–љ–Є—П —Г—Б—В–∞–љ–∞–≤–ї–Є–≤–∞–µ—В—Б—П –≤—А–∞—З–Њ–Љ –≤ –Ј–∞–≤–Є—Б–Є–Љ–Њ—Б—В–Є –Њ—В —А–∞–Ј–Љ–µ—А–∞, –Ї–Њ–ї–Є—З–µ—Б—В–≤–∞ –Њ–±—А–∞–Ј–Њ–≤–∞–љ–Є–є, –Њ—В–≤–µ—В–∞ –љ–∞ –њ—А–Њ–≤–Њ–і–Є–Љ—Г—О —В–µ—А–∞–њ–Є—О. –Ф–ї—П –≤–Ј—А–Њ—Б–ї—Л—Е –Љ–∞–Ї—Б–Є–Љ–∞–ї—М–љ–∞—П –і–Њ–Ј–∞ –Ї–Њ–ї–ї–Њ–Љ–∞–Ї–∞ —Б–Њ—Б—В–∞–≤–ї—П–µ—В 10 –Љ–ї/—Б—Г—В, —З—В–Њ —Б–Њ–Њ—В–≤–µ—В—Б—В–≤—Г–µ—В 2 –≥ —Б–∞–ї–Є—Ж–Є–ї–Њ–≤–Њ–є –Ї–Є—Б–ї–Њ—В—Л, –і–ї—П –і–µ—В–µ–є – 1 –Љ–ї, —З—В–Њ —Б–Њ–Њ—В–≤–µ—В—Б—В–≤—Г–µ—В 0,2 –≥ —Б–∞–ї–Є—Ж–Є–ї–Њ–≤–Њ–є –Ї–Є—Б–ї–Њ—В—Л. –Э–µ —А–µ–Ї–Њ–Љ–µ–љ–і—Г–µ—В—Б—П –і–Њ–њ—Г—Б–Ї–∞—В—М –њ—А–µ–≤—Л—И–µ–љ–Є—П —Н—В–Њ–є –і–Њ–Ј—Л –Є –Њ–±—А–∞–±–∞—В—Л–≤–∞—В—М –љ–µ—Б–Ї–Њ–ї—М–Ї–Њ —Г—З–∞—Б—В–Ї–Њ–≤ –Ї–Њ–ґ–Є –Њ–і–љ–Њ–≤—А–µ–Љ–µ–љ–љ–Њ. –Я—А–Є –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є–Є –њ—А–µ–њ–∞—А–∞—В–∞ –≤ –Љ–∞–Ї—Б–Є–Љ–∞–ї—М–љ–Њ–є —Б—Г—В–Њ—З–љ–Њ–є –і–Њ–Ј–µ —Г –≤–Ј—А–Њ—Б–ї—Л—Е –Є –і–µ—В–µ–є (—Б 2-–ї–µ—В–љ–µ–≥–Њ –≤–Њ–Ј—А–∞—Б—В–∞) –і–ї–Є—В–µ–ї—М–љ–Њ—Б—В—М –ї–µ—З–µ–љ–Є—П –љ–µ –і–Њ–ї–ґ–љ–∞ –њ—А–µ–≤—Л—И–∞—В—М 1 –љ–µ–і. –Т–Њ –≤—А–µ–Љ—П –±–µ—А–µ–Љ–µ–љ–љ–Њ—Б—В–Є –њ—А–Є–Љ–µ–љ–µ–љ–Є–µ –Ї–Њ–ї–ї–Њ–Љ–∞–Ї–∞ –і–Њ–њ—Г—Б—В–Є–Љ–Њ —В–Њ–ї—М–Ї–Њ –њ—А–Є –љ–∞–љ–µ—Б–µ–љ–Є–Є –µ–≥–Њ –љ–∞ –Њ–≥—А–∞–љ–Є—З–µ–љ–љ—Г—О –њ–Њ–≤–µ—А—Е–љ–Њ—Б—В—М – –љ–µ –±–Њ–ї–µ–µ 5 —Б–Љ [15–17].
–Т –њ–Њ—Б–ї–µ–і–љ–µ–µ –≤—А–µ–Љ—П –і–ї—П –њ—А–Њ—Д–Є–ї–∞–Ї—В–Є–Ї–Є –Ј–∞—А–∞–ґ–µ–љ–Є—П –Т–Я–І –≥–µ–љ–Є—В–∞–ї–Є–є —А–∞–Ј—А–∞–±–Њ—В–∞–љ—Л –≤–∞–Ї—Ж–Є–љ—Л, —Б–Њ–і–µ—А–ґ–∞—Й–Є–µ –≤–Є—А—Г—Б–Њ–њ–Њ–і–Њ–±–љ—Л–µ —З–∞—Б—В–Є—Ж—Л –Т–Я–І. –Т–∞–Ї—Ж–Є–љ–∞—Ж–Є—О —Б–ї–µ–і—Г–µ—В –њ—А–Њ–≤–Њ–і–Є—В—М –і–µ–≤–Њ—З–Ї–∞–Љ –Є –ґ–µ–љ—Й–Є–љ–∞–Љ –≤ –≤–Њ–Ј—А–∞—Б—В–µ –Њ—В 9 –і–Њ 26 –ї–µ—В. –†–µ–Ї–Њ–Љ–µ–љ–і—Г–µ—В—Б—П —З–µ—В—Л—А–µ—Е–≤–∞–ї–µ–љ—В–љ–∞—П –≤–∞–Ї—Ж–Є–љ–∞ (–У–∞—А–і–∞—Б–Є–ї) –і–ї—П —В–Є–њ–Њ–≤ 6, 11, 16, 18 –Є–ї–Є –±–Є–≤–∞–ї–µ–љ—В–љ–∞—П –≤–∞–Ї—Ж–Є–љ–∞ (–¶–µ—А–≤–∞—А–Є–Ї—Б) –і–ї—П —В–Є–њ–Њ–≤ 16 –Є 18. –Ш–Ј–≤–µ—Б—В–љ–Њ, —З—В–Њ –Њ–Ї–Њ–ї–Њ 90% —Б–ї—Г—З–∞–µ–≤ –≥–µ–љ–Є—В–∞–ї—М–љ—Л—Е –±–Њ—А–Њ–і–∞–≤–Њ–Ї –≤—Л–Ј—Л–≤–∞—О—В—Б—П –Т–Я–І-6 –Є –11, –∞ –Т–Я–І-16 –Є -18 —Б–ї—Г–ґ–∞—В –њ—А–Є—З–Є–љ–Њ–є —А–∞–Ј–≤–Є—В–Є—П –Њ–Ї–Њ–ї–Њ 70% —Б–ї—Г—З–∞–µ–≤ —А–∞–Ї–∞ —И–µ–є–Ї–Є –Љ–∞—В–Ї–Є. –Я—А–Њ–≤–µ–і–µ–љ–љ—Л–µ –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є–µ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П –њ–Њ–Ї–∞–Ј–∞–ї–Є, —З—В–Њ –≤–∞–Ї—Ж–Є–љ—Л —Н—Д—Д–µ–Ї—В–Є–≤–љ—Л –≤ 90% —Б–ї—Г—З–∞–µ–≤ –Ї–∞–Ї –Љ–Є–љ–Є–Љ—Г–Љ –≤ —В–µ—З–µ–љ–Є–µ 5 –ї–µ—В. –Э–µ—Б–Љ–Њ—В—А—П –љ–∞ –≤—Л—Б–Њ–Ї—Г—О –∞–Ї—В–Є–≤–љ–Њ—Б—В—М –≤ –њ–ї–∞–љ–µ –њ—А–Њ—Д–Є–ї–∞–Ї—В–Є–Ї–Є –Є–љ—Д–Є—Ж–Є—А–Њ–≤–∞–љ–Є—П –Т–Я–І, –≤–∞–Ї—Ж–Є–љ–∞ –љ–µ –Њ–±–ї–∞–і–∞–µ—В —В–µ—А–∞–њ–µ–≤—В–Є—З–µ—Б–Ї–Є–Љ —Н—Д—Д–µ–Ї—В–Њ–Љ –≤ —Б–ї—Г—З–∞–µ —Г–ґ–µ –Є–Љ–µ—О—Й–µ–є—Б—П –Є–љ—Д–µ–Ї—Ж–Є–Є. –Ю–і–љ–∞–Ї–Њ —Б–Њ–≤–µ—А—И–µ–љ–љ–Њ –Њ—З–µ–≤–Є–і–љ–Њ, —З—В–Њ —Б–≤–Њ–µ–≤—А–µ–Љ–µ–љ–љ–∞—П –≤–∞–Ї—Ж–Є–љ–∞—Ж–Є—П –±—Г–і–µ—В —Б–њ–Њ—Б–Њ–±—Б—В–≤–Њ–≤–∞—В—М —Б–љ–Є–ґ–µ–љ–Є—О –Ј–∞–±–Њ–ї–µ–≤–∞–µ–Љ–Њ—Б—В–Є –Ї–Њ–ґ–Є –Є —Б–ї–Є–Ј–Є—Б—В–Њ–є –∞–љ–Њ–≥–µ–љ–Є—В–∞–ї—М–љ–Њ–є –Њ–±–ї–∞—Б—В–Є, –Њ–±—Г—Б–ї–Њ–≤–ї–µ–љ–љ–Њ–є –Т–Я–І-–Є–љ—Д–µ–Ї—Ж–Є–µ–є, –Є —Г–Љ–µ–љ—М—И–µ–љ–Є—О –Ј–∞–±–Њ–ї–µ–≤–∞–µ–Љ–Њ—Б—В–Є —А–∞–Ї–Њ–Љ —И–µ–є–Ї–Є –Љ–∞—В–Ї–Є, –≤—Л–Ј–≤–∞–љ–љ—Л–Љ –Њ–љ–Ї–Њ–≥–µ–љ–љ—Л–Љ–Є —В–Є–њ–∞–Љ–Є –Т–Я–І [18].


–Ы–Є—В–µ—А–∞—В—Г—А–∞
1. –Ъ—Г–±–∞–љ–Њ–≤–∞ –Р.–Р., –Ъ—Г–±–∞–љ–Њ–≤ –Р.–Р., –Ь–µ–ї–µ—Е–Є–љ–∞ –Ы.–Х. –Є –і—А. –†–µ–Ј—Г–ї—М—В–∞—В—Л –і–µ—П—В–µ–ї—М–љ–Њ—Б—В–Є –Љ–µ–і–Є—Ж–Є–љ—Б–Ї–Є—Е –Њ—А–≥–∞–љ–Є–Ј–∞—Ж–Є–є –і–µ—А–Љ–∞—В–Њ–≤–µ–љ–µ—А–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Њ–≥–Њ –њ—А–Њ—Д–Є–ї—П –≤ –†–Њ—Б—Б–Є–є—Б–Ї–Њ–є –§–µ–і–µ—А–∞—Ж–Є–Є –Ј–∞ 2012 –≥–Њ–і // –Т–µ—Б—В–Є–Ї –і–µ—А–Љ. –Є –≤–µ–љ–µ—А. 2013. вДЦ 5. –°. 21–39.
2. –Я–Њ–і–Ј–Њ–ї–Ї–Њ–≤–∞ –Э.–Ь., –°–Њ–Ј–∞–µ–≤–∞ –Ы.–Ы., –Ю—Б–∞–і—З–µ–≤ –Т.–С. –Я–∞–њ–Є–ї–ї–Њ–Љ–∞–≤–Є—А—Г—Б–љ–∞—П –Є –≥–µ—А–њ–µ—В–Є—З–µ—Б–Ї–∞—П –Є–љ—Д–µ–Ї—Ж–Є–Є –∞ –∞–Ї—Г—И–µ—А—Б—В–≤–µ –Є –≥–Є–љ–µ–Ї–Њ–ї–Њ–≥–Є–Є. –£—З–µ–±–љ–Њ-–Љ–µ—В–Њ–і–Є—З–µ—Б–Ї–Њ–µ –њ–Њ—Б–Њ–±–Є–µ. –Ь., 2009. 46 —Б.
3. –Ь–Є—З–µ–љ–Ї–Њ –Р.–Т., –Ы—М–≤–Њ–≤ –Р.–Э.. –Р–љ–Њ–≥–µ–љ–Є—В–∞–ї—М–љ—Л–µ –Ї–Њ–љ–і–Є–ї–Њ–Љ—Л: —Б–Њ–≤—А–µ–Љ–µ–љ–љ—Л–µ –њ—А–µ–і—Б—В–∞–≤–ї–µ–љ–Є—П –Њ –њ–∞—В–Њ–≥–µ–љ–µ–Ј–µ –Є –њ–Њ–і—Е–Њ–і—Л –Ї —В–µ—А–∞–њ–Є–Є // Consilium Medicum (–њ—А–Є–ї/ –Ф–µ—А–Љ–∞—В–Њ–ї–Њ–≥–Є—П). 2010. вДЦ 2. –°. 37–42.
4. Doorbar J. The papillomaviruses life cycle // J.Clin. Virol. 2005. Vol. 32 (Suppl. 1). P. 57.
5. –Ь–Њ–ї–Њ—З–Ї–Њ–≤ –Ш.–Р., –Ъ–Є—Б–µ–ї–µ–≤ –Т.–Ш., –†—Г–і—Л—Е –Ш.–Т. –Є –і—А. –Я–∞–њ–Є–ї–ї–Њ–Љ–∞–≤–Є—А—Г—Б–љ–∞—П –Є–љ—Д–µ–Ї—Ж–Є—П – –Ї–ї–Є–љ–Є–Ї–∞, –і–Є–∞–≥–љ–Њ—Б—В–Є–Ї–∞, –ї–µ—З–µ–љ–Є–µ. –Я–Њ—Б–Њ–±–Є–µ –і–ї—П –≤—А–∞—З–µ–є. –Ь., 2005. 31—Б.
6. Goncalves M.A., Donadi E.A. Immune cellular response to HPV: current concepts // Braz. J. Infect. Dis. 2004. Vol. 8. P. 1–9.
7. –•—Н–±–Є—Д –Ґ.–Я. –Ъ–Њ–ґ–љ—Л–µ –±–Њ–ї–µ–Ј–љ–Є. –Ф–Є–∞–≥–љ–Њ—Б—В–Є–Ї–∞ –Є –ї–µ—З–µ–љ–Є–µ. –Я–µ—А. —Б –∞–љ–≥–ї.; 2-–µ –Є–Ј–і., 2006. –°. 194–120.
8. –•–∞–љ–і—Б—Д–Є–ї–і –•.–°. –Ч–∞–±–Њ–ї–µ–≤–∞–љ–Є—П, –њ–µ—А–µ–і–∞—О—Й–Є–µ—Б—П –њ–Њ–ї–Њ–≤—Л–Љ –њ—Г—В–µ–Љ. –Ь.: –С–Є–љ–Њ–Љ, 2004. –°. 126–142.
9. –Р–љ–і—А–Њ—Д–Є –≠.–Ф., –Ы–Њ–≤–Є –Ф.–Ы. –Ф–µ—А–Љ–∞—В–Њ–ї–Њ–≥–Є—П –§–Є—Ж–њ–∞—В—А–Є–Ї–∞ –≤ –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Њ–є –њ—А–∞–Ї—В–Є–Ї–µ. –Я–µ—А. —Б –∞–љ–≥–ї. 2013. –Ґ. вДЦ 3. –°. 2085–2096.
10. –Ш–≥–љ–∞—В—М–µ–≤ –Ф.–Т. –С–Њ—А—М–±–∞ —Б –≤–Є—А—Г—Б–Њ–Љ –њ–∞–њ–Є–ї–ї–Њ–Љ—Л —З–µ–ї–Њ–≤–µ–Ї–∞ // Consilium Medicum (–њ—А–Є–ї. –Ф–µ—А–Љ–∞—В–Њ–ї–Њ–≥–Є—П). 2009. вДЦ 3. –°. 29–34.
11. –Х–≤—А–Њ–њ–µ–є—Б–Ї–Њ–µ —А—Г–Ї–Њ–≤–Њ–і—Б—В–≤–Њ –њ–Њ –ї–µ—З–µ–љ–Є—О –і–µ—А–Љ–∞—В–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є—Е –±–Њ–ї–µ–Ј–љ–µ–є / –Я–Њ–і —А–µ–і. –Р.–Ф. –Ъ–∞—Ж–∞–Љ–±–∞—Б–∞, –Ґ.–Ь. –Ы–Њ—В—В–Є; –њ–µ—А. —Б –∞–љ–≥–ї.; 2-–µ –Є–Ј–і. 2009. –°. 84–88.
12. Poochareon V., Berman B., Villa A. Successful treatment of butcher's warts with imiquimod 5% cream // Clin. Exp. Dermatol. 2003. Vol. 28 (Suppl. 1). P. 42–44.
13. –†–∞–Ј–љ–∞—В–Њ–≤—Б–Ї–Є–є –Ъ.–Ш., –Ъ–Њ—В—А–µ—Е–Њ–≤–∞ –Ы.–Я. –°–Њ–≤—А–µ–Љ–µ–љ–љ—Л–µ –Љ–µ—В–Њ–і—Л –ї–µ—З–µ–љ–Є—П –Њ—Б—В—А–Њ–Ї–Њ–љ–µ—З–љ—Л—Е –Ї–Њ–љ–і–Є–ї–Њ–Љ // –Ы–µ—З–∞—Й–Є–є –≤—А–∞—З. 2007. вДЦ 9. C. 24–26.
14. Kimberlin D.W. Current status of antiviral therapy for juvelini-onset recurrent papillomatosis // Antiviral. Res. 2004. Vol. 63. P. 141–151.
15. Fox P.A., Tung M.Y. Human papillovirus: burden of illness and treatment cost considerations // Am. J. Clin. D–µrmatol .2005. Vol. 6(6). P. 365–381.
16. Rivera A.R., Tyring S.K. Therapy of cutaneous human papillomavirus infections // Dermatol. Ther. 2004. Vol. 17. P. 441–448.
17. Gibbs S., Harvey I., Sterling J.C. et al. Local treatments for cutaneous warts // Cochrane Database Syst. Rev. 2003. Vol. 3:CD001781.
18. Garland S.M., Hernandez-Avila M., Wheeler C.M. et al. Quadrivalent vaccine against human papillomavirus to prevent anogenital diseases // N. Engl. Med. 2007. Vol. 356 (19). P. 1928–1943.












