Diabetic retinopathy (DR) is a main cause of complete loss of sight and disability. The paper discusses the results of treatment of 49 patients with primary DR. An examination of 185 children suffering from type 1 diabetes mellitus identified a group of early abnormal changes in the fundus of the eye, which precede the development of DR.
Т.М. Миленькая – ведущий научный сотрудник инсититута диабета ЭНЦ РАМН, Л.Н. Щербачева – старший научный сотрудник ЭНЦ РАМН, В.С. Терентьев – научный сотрудник института диабета ЭНЦ РАМН
T.M. Mylenkaya, leading research worker, Institute of Diabetis, RERC RAMS, L.M. Scherbacheva, senior research worker, RERC RAMS, V.S. Terentiev, research worker, Institute of Diabetis, RERC RAMS
Одним из ранних сосудистых осложнений сахарного диабета (СД) является поражение органа зрения, чаще всего нарушения развиваются в сосудах и слоях сетчатки. Диабетическая ретинопатия (ДР) занимает одно из первых мест среди глазной патологии, приводящей к полной потере зрения и инвалидности. В основном страдают молодые больные инсулинзависимым СД.
Широкая распространенность СД (в развитых странах болеют до 4 – 5% населения) влечет за собой и рост числа больных ретинопатией [1 – 3]. Так, в США, где из 6 млн больных СД более 50 тыс. страдают слепотой, вызванной ДР, при этом число случаев потери зрения в результате осложнений ДР, имеет устойчивую тенденцию к росту [3, 4].
Несмотря на совершенствование методов контроля состояния больных СД, применение лазерной терапии и витреальной хирургии, потеря зрения в результате осложнений СД остается очень серьезной проблемой [5 – 10]. Это обусловлено, с одной стороны, тем, что на ранних стадиях ДР больные не предъявляют жалоб на снижение зрения, с другой – тем, что поражение сетчатки на ранних стадиях заболевания очень трудно выявить: для этого необходим тщательный квалифицированный офтальмологический контроль с применением современных методик [11 – 13].
Многими исследователями [4, 11, 14 – 16] подтверждено, что на развитие ДР оказывают существенное влияние такие факторы, как возраст больного, пол, возраст на момент выявления СД, длительность и тип диабета.
Выявлена устойчивая взаимосвязь между длительностью СД и развитием ДР. Ряд авторов [3, 13] обнаружили, что после 2 лет болезни ретинопатия выявляется у 2 – 7% больных с СД I типа. Среди пациентов, страдающих СД более 10 лет, поражение сетчатки выявляется у 50%, а свыше 15 лет – у 75 – 70%.
Больные с СД II типа нередко обращаются к офтальмологу с жалобами на снижение зрения, и только после диагностики ДР у этих больных выявляют СД.
Очень важной проблемой остаются выявление ранних изменений сетчатки и их корреляция на ранних стадиях. R. Klein и соавт. [13] изучали взаимосвязь между обнаруженными на глазном дне единичными микроаневризмами и развитием ДР за 10-летний период. У больных СД I типа в возрасте до 30 лет после 10-летнего наблюдения ДР развилась в 89% случаев, доля пролиферативной ДР составила 30%. Результаты этих исследований показали, что неблагоприятному течению ретинопатии в большей мере способствовал плохой метаболический контроль, а не старение организма больного и продолжительность СД [13, 17].
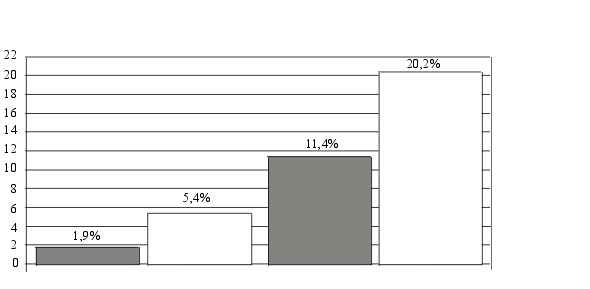
Рис. 1. Влияние возраста и длительности инсулинзависимого СД на развитие ДР у детей. По оси абсцисс – возраст больных; по оси ординат – частота выявления изменений на глазном дне (в %). Заштрихованные столбики – длительность СД до 5 лет, светлые – от 6 до 11 лет.
Однако многие авторы [9, 14, 16, 18, 19] высказывают мнение, что существуют и определенные механизмы, влияющие на развитие ДР. Таковыми являются, например, биохимические, гемодинамические и гормональные факторы, которые играют важную роль в развитии ретинопатии. Эти факторы не являются полностью независимыми друг от друга, до некоторой степени они взаимодействуют и вместе ответственны за хорошо известные нарушения васкулярной окклюзии, образование микроаневризм, геморрагий, твердых экссудативных очагов и в конечном итоге за формирование новообразованных сосудов.
Основными причинами развития ДР все же являются длительная гипергликемия и суточные резкие колебания уровня сахара в крови, вызванные плохим метаболическим контролем или даже его отсутствием в течение длительного периода [15, 16].
Биохимические отклонения при диабете приводят к ранним анатомическим и функциональным нарушениям в кровеносных сосудах глаз, в том числе утолщению базальной мембраны, уменьшению жизнеспособности клеток эндотелия, потере перицитов, развитию микроаневризм, ухудшению васкулярного состояния. Все это в конечном счете обусловливает плохую перфузию, гипоксию и нарушение проницаемости сосудистых стенок [4,16, 17].
Раннее выявление патологических изменений на глазном дне у детей с инсулинзависимым СД. В начальных стадиях ДР трудно выявить патологический процесс на глазном дне, он протекает без симптомов, пациенты не предъявляют жалоб и не обращаются к окулистам. Основную массу таких больных составляют молодые люди с длительностью диабета более 10 лет и дети.
В детском возрасте СД занимает ведущее место в структуре хронических заболеваний. До недавнего времени считалось, что микрососудистые осложнения у детей и подростков являются редкостью.
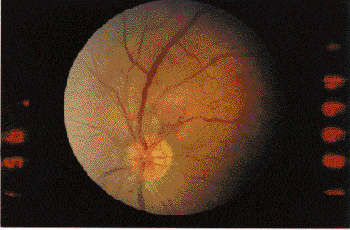
Рис. 2. Непролиферативная ДР. Парамакулярно твердые экссудативные очаги, микроаневризмы, парацентрально по ходу сосудов ретинальные кровоизлияния.
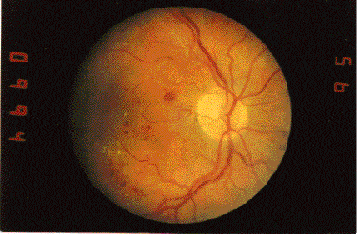
Рис. 3. Пролиферативная ДР. Парапапиллярно рост новообразованных сосудов в плоскости сетчатки.

Рис. 4. Пролиферативная ДР. Кровоизлияние в стекловидное тело, грубый витреоретинальный тяж с множеством новообразованных сосудов.
Известно, что одной из основных причин развития диабетических осложнений является гипергликемия, приводящая к патологическому усилению гликозилирования белков [11]. Наиболее хорошо изучен процесс гликозилирования гемоглобина (R. Giansanti, M. Boemi, 1994). Определение гликированного гемоглобина в процентах от общего содержания гемоглобина сегодня является наиболее объективным и современным методом оценки степени компенсации углеводного обмена у детей, больных СД.
Поскольку возможен регресс начальных проявлений диабетических осложнений при достижении компенсации углеводного обмена, их ранняя диагностика и мониторирование с контролем уровня гликированного гемоглобина, своевременная терапия являются средством профилактики развития диабетических осложнений.
С целью диагностики ДР в детском отделении ЭНЦ РАМН обследовано 185 детей из различных регионов России – 93 мальчика и 92 девочки в возрасте от 6 мес до 15 лет. Средний возраст детей составил 10,7 ± 2,5 года.
У наблюдаемых детей длительность СД составляла от нескольких месяцев до 13 лет. У большинства из них она не превышала 5 лет, только у 16 детей составляла более 10 лет.
Возраст, в котором был впервые выявлен СД, у большинства (45,9%) детей составил от 5 до 10 лет. В возрасте до 4 лет СД был выявлен выявлен у 67 (36,3%) детей, после 10 летнего возраста – у 33 (17,8%) обследованных.
В среднем возраст дебюта инсулинзависимого СД составил 6,9 года. У большинства детей СД не был компенсированным. Уровень гликированного гемоглобина (HbA1) колебался от 6,6 до 24%, составил в среднем – 13,2 ± 3,2%. Мы определяли уровень гликированного гемоглобина в группах детей с ретинальными изменениями и без таковых. У 86% детей с ДР уровень HbA1 был выше 11% и только у 14% – ниже 11%. У 72% детей без ретинальных изменений уровнь HbA1 был выше 11%, у 28% обследованных детей он был ниже 11%. Кроме офтальмоскопии всем детям проводилось исследование глазного дна с помощью сканирующей лазерной фундус-камеры (CSLO) фирмы “Zeiss” с последующей архивацией данных. Фиксировалось компьютерное изображение 4 – 5 участков глазного дна: область диска зрительного нерва, макулярная и парамакулярная области, 2 – 3 парацентральные зоны или локальные участки выраженных патологических изменений.
Фотографии глазного дна хранились у пациентов или в историях болезни, а их электронные копии – в базе данных компьютера.
Офтальмологические обследования позволили выделить группу из 14 (7,6%) больных от общего числа с выраженными микрососудистыми изменениями, значительным количеством микроаневризм и ретинальных геморрагий. Начальные изменения (единичные микроаневризмы, точечные ретинальные геморрагии) были обнаружены у 49 (26,5%) пациентов, причем в основном это были дети с длительностью СД менее 5 лет.
Результаты исследований взаимосвязи микрососудистых изменений на глазном дне с возрастом детей и длительностью СД были следующими: у (44,5%) детей старше 10 лет с длительностью СД 10 – 13 лет были обнаружены не только начальная, но и выраженная стадия непролиферативной ДР (в 7,6% случаев), а в 1,1% случаев была обнаружена пролиферативная ДР. Среди детей того же возраста (10 – 15 лет), но с длительностью СД до 5 лет начальные микрососудистые изменения были обнаружены только у 11,4%, а при длительности СД 5 – 10 лет – уже у 20,2% (рис. 1). Среди детей в возрасте до 10 лет при длительности СД до 5 лет начальные изменения на глазном дне были обнаружены только у 1,9%, а с длительностью СД до 10 лет – у 5,4%.
Мы наблюдали этих детей в течение 2 – 3 лет. Повторное обследование 157 (84,8%) детей было проведено через 6 – 12 мес. После обучения методам самоконтроля и оптимизации лечения у большинства из них метаболический контроль улучшился, было отмечено снижение уровня гликемии, средний уровень HbA1 составил 11,5 ± 2,9%. Результаты обследования показали, что процесс на глазном дне стабилизировался у 138 (87,9%) детей, у 7 (4,5%) детей отмечалось улучшение. У 12 (7,6%) детей процесс на глазном дне прогрессировал несмотря на улучшение уровня гликемии. На глазном дне у них появилось множество ретинальных геморрагий, микроаневризм, расширения капилляров, а также выраженная извитость мелких сосудов. Они пополнили группу больных с непролиферативной ДР, первоначально включавшую 14 детей с выраженными изменениями на глазном дне.
У 2 детей в возрасте 13 и 15 лет при длительности заболевания 12 лет через 3 мес от начальных патологических изменений произошел быстрый рост новообразованных сосудов в области диска зрительного нерва и других участках сетчатки, сопровождавшийся ретинальными и преретинальными кровоизлияниями.
Пациенты с неудовлетворительной компенсацией углеводного обмена, длительностью СД более 5 лет составляют группу риска развития ДР.
У 12 детей микрососудистые изменения на глазном дне прогрессировали на фоне высокого уровня HbA1 – в среднем 13,7% (рис. 2).
Этим больным (10 пациентам с непролиферативной ДР и двум с пролиферативной ДР) проведена лазерная аргоновая коагуляция сетчатки.
Показанием к проведению лазерной коагуляции у детей являются следующие изменения на глазном дне:
• множество ретинальных геморрагий в парацентральной области;
• множество микроаневризм в парамакулярной области;
• расширение капилляров, выраженная извитость мелких сосудов в парамакулярной области;
• сочетание вышеупомянутых факторов с гиперемией и нечеткостью границ диска зрительного нерва, расширением вен;
• наличие на глазном дне твердых экссудативных очагов или рост новообразованных сосудов.
В отдаленные сроки (от 12 до 24 мес после проведения лазерной коагуляции), у 6 (50%) детей наблюдали улучшение – рассасывание геморрагий и уменьшение микроаневризм, стойкая стабилизация процесса была отмечена у 4 детей, у 2 детей с непролиферативной и пролиферативной формами ДР наблюдали ухудшение. У одного ребенка с пролиферативной ДР наблюдали быстрое прогрессирование, рост неоваскуляризации и пролиферативной ткани в стекловидное тело, кровоизлияния в стекловидное тело. Было отмечено резкое снижение зрения (от 0,8 до 0,01). У второго ребенка 15 лет с длительностью СД 10,5 года ухудшения на глазном дне были незначительными, увеличилось количество твердых экссудативных очагов в парамакулярной области, при этом снижения зрения не отмечалось. После повторной лазерной коагуляции на глазном дне процесс был стабилизирован.
Своевременное выявление и лечение ДР позволяет снизить потерю зрения не только у детей, но в последующем и у взрослых, заболевших инсулинзависимым СД в детском возрасте.
Методы лечения ДР
Фотолазерная коагуляция сетчатки.
Криокоагуляция.
Витрэктомия.
Склеропластика.
Медикаментозная терапия.
Некоторые из этих методов лечения ДР мы рассмотрим подробно.
Эффективность применения аргоновой лазерной коагуляции у больных с инсулинзависимым СД
Лазерная коагуляция и в настоящее время является самым эффективным методом лечения в начальных стадиях ДР.
Мы провели анализ клинических данных 49 больных с начальной стадией ДР. Возраст больных составлял от 16 до 40 лет, в среднем – 21,3 ± 7,6 года), длительность СД – от 9 до 16 лет, в среднем – 12,5 ± 3,9 года. СД у этих больных был выявлен в возрасте от 2 до 22 лет (в среднем в 9,3 ± 5,3 года).
Уровень HbA1 был от 7,2 до 15,8% (в среднем 10,9 ± 1,8%). У больных с пролиферативной ДР также чаще отмечались суточные резкие колебания уровня гликемии – от 1,3 до 25 ммоль/л и выше.
Всем пациентам проводили фотографирование глазного дна с помощью сканирующей лазерной фундус-камеры (CSLO) фирмы “Zeiss” с последующей архивацией данных. Фиксировалось компьютерное изображение 4 – 5 участков глазного дна.
При повторных осмотрах (через 4 – 6 мес) фотографировали те же самые участки глазного дна и проводили сравнительную характеристику изменений в динамике.
Наблюдая в динамике больных, которым не проводилось предварительное лечение, путем сравнения фотографий глазного дна, мы обнаружили, что у 12 пациентов с непролиферативной ДР (рис. 2) и начальными изменениями на глазном дне (микроаневризмы, ретинальные геморрагии без твердых экссудативных очажков) через 4 – 6 мес появилась неоваскуляризация. Эти результаты убеждают нас в том, что упомянутые начальные изменения можно с большой вероятностью считать признаком возникновения и развития пролиферативной формы ДР.
У всех обследованных перед проведением лазерной коагуляции была диагностирована пролиферативная ДР (начальная стадия). Изменения на глазном дне были в большинстве случаев симметричными. Жалоб на снижение зрения больные не предъявляли. У наблюдаемых больных острота зрения составляла от 0,7 до 1,0. На глазном дне в макулярной, парамакулярной областях множество микроаневризм, расширение капилляров, извитость мелких сосудов, парапапиллярно или в области диска зрительного нерва рост новообразованных сосудов в небольшом количестве и в плоскости сетчатки (рис. 3, 4). Эти изменения на остроту зрения не влияли.
Всем наблюдаемым 49 больным проводили аргоновую лазерную коагуляцию сетчатки. Перед процедурой определяли уровень гликемии и артериального давления. У больных СД, которым проводилась лазерная коагуляция, артериальное давление было в пределах нормы, уровень гликированного гемоглобина не превышал 10%. В случаях выраженной декомпенсации СД, проведение лазерной коагуляции откладывали до улучшения показателей гликемии. Этим больным индивидуально подбирали инсулинотерапию, часть из них проходили обучение.
В ранние сроки (1 – 6 дней) после проведения лазерной коагуляции осложнений не наблюдалось. На глазном дне в первые 2 дня очаги лазерной коагуляции были светлыми с перифокальным отеком, после 3 дней отек в зоне очагов уменьшился, появились нежные отложения пигмента. Проведение лазерной коагуляции на остроту зрения не влияло.
Проведен анализ результатов лечения в отдаленные сроки (до 3 лет). Из 49 пациентов 20 постоянно контролировали уровень глюкозы в крови, артериального давления, каждые 3 – 6 мес консультировались у офтальмолога, 3 пациентам была проведена дополнительно лазерная коагуляция. На протяжении 3 лет у 19 (95%) пациентов этой группы процесс на глазном дне не прогрессировал. Уровень HbA1 составлял от 7,7 до 11,2%, в среднем 8,8%.
У остальных 29 больных метаболический контроль был плохим, уровень HbA1 составлял от 10,4 до 18% (в среднем – 13,6 ± 2,6%). К офтальмологу больные обращались 1 раз в год или даже 1 раз в 2 года, чаще с жалобами на снижение зрения. У 14 (48,3%) наблюдали стойкую стабилизацию процесса на глазном дне, а у остальных 15 (51,7%) пациентов этой группы процесс прогрессировал. Им дополнительно проводили лазерную коагуляцию, 4 больным – в сочетании с трансконъюнктивальной криокоагуляцией.
Анализ клинических данных показывает, что эффективность лазерной коагуляции намного выше у группе больных с лучшей компенсацией СД, постоянно наблюдающихся у эндокринологов и офтальмологов.
Криокоагуляция
Большинство больных инсулинзависимым СД обращаются к офтальмологам только тогда, когда отмечают резкое снижение зрения.
Нами проводилось лечение 72 больных с инсулинзависимым СД и грубыми пролиферативными изменениями на глазном дне, частичным гемофтальмом и тракционной отслойкой сетчатки. Средний возраст пациентов был 28,5 года, длительность СД – от 12 лет до 31 года. У всех пациентов СД был в основном декомпенсирован и отмечались резкие колебания уровня глюкозы в крови в течение суток. Уровень HbA1 у них составлял от 9,3 до 18,7% (в среднем – 10,9 ± 3,2%) и у большинства больных превышал 10,3%.
Из 72 пациентов 40 (52,6%) впервые обратились к окулисту за весь период течения СД только тогда, когда заметили резкое снижение зрения. При осмотре на глазном дне были выявлены грубые изменения: рост неоваскуляризации не только в плоскости сетчатки, но и в стекловидное тело, грубые пролиферативно-экссудативные изменения в центральной области с частичным гемофтальмом.
Оставшиеся 32 пациента были обследованы ранее офтальмологами, им проводились лазерная коагуляция сетчатки и медикаментозное лечение.
Из 72 наблюдаемых больных у 38 было двустороннее симметричное поражение глаз, а у 34 пациентов на одном глазу наблюдались начальные патологические изменения. Острота зрения у 72 больных (110 глаз) была от светоощущения до 0,1.
У больных с тяжелыми стадиями пролиферативной ДР мы применяли криокоагуляцию сетчатки.
Трансконъюнктивальная криокоагуляция проводилась на 64 глазах у 48 больных.
У 20 пациентов зрение улучшилось на следующий день после вмешательства. Объективно отмечались уменьшение помутнения в стекловидном теле и частичное рассасывание преретинальных кровоизлияний на глазном дне. У 26 больных после проведения криокоагуляции на следующий день изменения в стекловидном теле и на глазном дне не были обнаружены. На периферии сетчатки определялись нежные очаги криокоагуляции. Острота зрения оставалась прежней. У 2 больных после криокоагуляции несколько усилилось помутнение в стекловидном теле без (60,4%) больных через 1,5 – 2 мес наблюдали значительное рассасывание помутнений в стекловидном теле, у 21 (43,7%) пациента – обратное развитие пролиферативной ткани, запустевание новообразованных сосудов. Острота зрения повысилась от 0,01 – 0,05 до 0,1 – 0,3 и оставалась стабильной длительный период (от 2 до 24 мес).
У 13 (27,1%) больных после трансконъюнктивальной криокоагуляции на глазном дне процесс был стабилизирован. Несмотря на проведение криокоагуляции у 6 (12,5%) больных прогрессировал рост пролиферативной ткани и неоваскуляризации.
Повторная трансконъюнктивальная криокоагуляция проводилась через 2 – 4 мес у 27 больных с повторными кровоизлияниями, прогрессированием патологического процесса или при стабилизации процесса, но с обширной зоной поражения сетчатки.
У 16 больных после рассасывания кровоизлияний в стекловидном теле проводилась криокоагуляция в сочетании с лазерной коагуляцией сетчатки. С помощью трансконъюнктивальной криокоагуляции аппликации наносились в зоне экватора, а применение лазера давало возможность коагулировать парацентральные участки сетчатки, преретинальные кровоизлияния, расположенные вблизи диска зрительного нерва или по ходу темпоральных сосудов.
Транссклеральную криокоагуляцию и склеропластику заднего полюса глазного яблока проводили 24 пациентам с грубыми витреоретинальными изменениями (у 22 пациентов – на одном глазу, а у 2 – оперировали оба глаза).
В ранний послеоперационный период после транссклеральной криокоагуляции и склеропластики заднего полюса осложнений не наблюдалось. Через 3 мес после операции было отмечено улучшение зрения у 17 (70,8%) больных, у 4 (16,6%) больных патологический процесс не прогрессировал, у 3 (12,5%) больных наблюдали ухудшение, у 2 прогрессировала неоваскуляризация в заднем полюсе, у 1 больного развилась вторичная рубеозная глаукома.
12 больным вмешательство проводилось не только в нижней, но и (через 3 мес) в верхней половине глазного яблока. После второй операции улучшение зрения отмечалось у 8 больных.
У всех больных этой группы острота зрения повышалась лишь на несколько сотых долей единицы из-за грубых изменений сетчатки в центральной зоне. Несмотря на незначительные улучшения, после вмешательства больные получили возможность ориентироваться и обходиться без посторонней помощи.
Литература:
1. Балаболкин М.И. Сахарный диабет: возможно ли обуздать его распространение и частоту поздних сосудистых осложнений. // Тер. архив. – 1993. – (10). – С. 4–9.
2. Дедов И.И., Шестакова М.В., Мозвая М.Е. Генетические аспекты развития диабетической нефропатии // Тер. архив. – 1993. – № 10. – C. 9–13.
3. Kostraba JN, Klein R, Dorman JS, Becker DJ, Drash AL, Maser RE, Orchard TJ. The epidemiology of diabetes complications study. IV. Correlates of diabetic background and proliferative retinopathy. Am J Epidemiol 1991;15(4):381–91.
4. Frank RN. On the pathogenesis of diabetic retinopathy. A 1990 update. Ophthalmology 1991;98(5):586–93.
5. Беляева М.И. Профилактическая лазертерапия при ДР. // 5-й Всесоюз. съезд офтальмологов: Тезисы докл. – М., 1979. – Т.3. – С. 110–112.
6. Глинчук Я.И., Киселев А.В., Югай А.Г., Шамсиев А.С. Показания и методика проведения операции витрэктомии с одновременной эндолазерной коагуляцией сетчатки у больных с осложненными формами ДР. // Сб. науч. тр. Лазерные методы лечения заболеваний глаз. – М., 1990. – C. 69–74.
7. Нестеров А.П. Диабетические поражения органов зрения. // Проблемы эндокринологии. – 1997. – N3. – С. 16–19.
8. Blankenship GW. Fifteen-year argon laser and xenon photocoagulation results of Bascom Palmer. Ophthalmology 1991;98(2):125–8.
9. Kostraba JN, Klein R, Dorman JS, Becker DJ, Drash AL, Maser RE, Orchard TJ. The epidemiology of diabetes complications study. IV. Correlates of diabetic background and proliferative retinopathy. Am J Epidemiol 1991;15(4):381–91.
10. Meyer-Schwickerath G. Diabetic retinopathy treatment with argon coagulation and xenon coagulation. Ophthalmol Lit 1973;27(2):1078.
11. Bonney M, Hing SJ, Fung AT, Stephens MM, Fairchild JM, Donaghue KC, Howard NJ, Silink M. Development and progression of diabetic retinopathy: adolescents at risk. Diabet Med 1995;12(11):967–73.
12. Buckley S, Jenkins L, Benjamin L. Field loss after pain retinal photocoagulation with diode and argon lasers. Doc Ophthalmol 1992;82(4):317–22.
13. Klein R, Klein BE, Moss SE, Cruickshanks KJ. Ten-year incidence and progression of diabetic retinopathy. Arch Ophthalmol 1994;112(9):1217–28.
14. Forrester JV, Shafiee A, Schroder S, Knott R, Mcintosh L. The role of growth factors in proliferative diabetic retinopathy. Eye 1993;7(Pt2):276–87.
15. Klein B, Moss SE, Davis MD, Mets DL. The Wisconsin epidemiological study of diabetic retinopathy. Four-year incidence and progression of diabetic retinopathy when age at diagnosis is 30 years or more. Arch Ophthalmology 1989;107:244–9.
16. Rassam SM, Patel V, Kohner EM. The effect of experimental hypertension on retinal vascular autoregulation in humans: a mechanism for the progression of diabetic retinopathy. Exp Physiol 1995;80(1):53–68.
17. Kohner EM, Patel V, Rassam SM. Role of blood and impaired autoregulation in the pathogenesis of diabetic retinopathy. Diabetes 1995;44(6):603–7.
18. Falck A, Laatikainen L. Retinal vasodilation and hyperglycaemia in diabetic children and adolescents. Acta Ophthalmol.
19. Nagi DK, Mansfield MW, Sticland MH, Grand PJ. Angiotensin converting enzyme (ACE) insertion (ID) polymorphism, and diabetic retinopathy in subjects with IDDM and NIDDM. Diabet- Med 1995;12(11):997–1001.












