–†–Њ—Б—Б–Є–є—Б–Ї–∞—П –Љ–µ–і–Є—Ж–Є–љ—Б–Ї–∞—П –∞–Ї–∞–і–µ–Љ–Є—П –њ–Њ—Б–ї–µ–і–Є–њ–ї–Њ–Љ–љ–Њ–≥–Њ –Њ–±—А–∞–Ј–Њ–≤–∞–љ–Є—П
–Ф–Є–∞–±–µ—В–Є—З–µ—Б–Ї–∞—П —Б—В–Њ–њ–∞ –Њ—Б—В–∞–µ—В—Б—П –љ–∞–Є–±–Њ–ї–µ–µ —В—П–ґ–µ–ї—Л–Љ –њ–Њ–Ј–і–љ–Є–Љ –Њ—Б–ї–Њ–ґ–љ–µ–љ–Є–µ–Љ —Б–∞—Е–∞—А–љ–Њ–≥–Њ –і–Є–∞–±–µ—В–∞ (–°–Ф) –≤ —Б–≤—П–Ј–Є —Б –≤—Л—Б–Њ–Ї–Є–Љ –Љ–µ–і–Є—Ж–Є–љ—Б–Ї–Є–Љ, —Б–Њ—Ж–Є–∞–ї—М–љ—Л–Љ –Є —Н–Ї–Њ–љ–Њ–Љ–Є—З–µ—Б–Ї–Є–Љ —Г—Й–µ—А–±–Њ–Љ. –Э–µ—Б–Љ–Њ—В—А—П –љ–∞ –Њ—З–µ–≤–Є–і–љ—Л–µ —Г—Б–њ–µ—Е–Є –≤ –і–Њ—Б—В–Є–ґ–µ–љ–Є–Є —Ж–µ–ї–µ–є –°–µ–љ—В––Т–Є–љ—Б–µ–љ—В—Б–Ї–Њ–є –Ф–µ–Ї–ї–∞—А–∞—Ж–Є–Є, –≤ —В–Њ–Љ —З–Є—Б–ї–µ —Б–љ–Є–ґ–µ–љ–Є–Є –љ–∞ 50% –Ї–Њ–ї–Є—З–µ—Б—В–≤–∞ –∞–Љ–њ—Г—В–∞—Ж–Є–є, —З–Є—Б–ї–Њ –њ–Њ—Б–ї–µ–і–љ–Є—Е –Њ—Б—В–∞–µ—В—Б—П –≤—Л—Б–Њ–Ї–Є–Љ –Є –і–∞–ґ–µ –љ–∞–±–ї—О–і–∞–µ—В—Б—П –Є—Е —А–Њ—Б—В. –Т —В–Њ –≤—А–µ–Љ—П –Ї–∞–Ї –Њ—В—З–µ—В—Л –Ј–і—А–∞–≤–Њ–Њ—Е—А–∞–љ–µ–љ–Є—П –®–≤–µ—Ж–Є–Є –Є –У–Њ–ї–ї–∞–љ–і–Є–Є [1] —Г–Ї–∞–Ј—Л–≤–∞—О—В –љ–∞ —Б–љ–Є–ґ–µ–љ–Є–µ —З–Є—Б–ї–∞ –∞–Љ–њ—Г—В–∞—Ж–Є–є –љ–Є–ґ–љ–Є—Е –Ї–Њ–љ–µ—З–љ–Њ—Б—В–µ–є –≤—Б–ї–µ–і—Б—В–≤–Є–µ –і–Є–∞–±–µ—В–∞, –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П–Љ–Є, –њ—А–Њ–≤–µ–і–µ–љ–љ—Л–Љ–Є –≤ –У–µ—А–Љ–∞–љ–Є–Є [2], –љ–µ –Њ–±–љ–∞—А—Г–ґ–µ–љ–Њ –Є—Е —Г–Љ–µ–љ—М—И–µ–љ–Є—П. –°—В–∞—В–Є—Б—В–Є–Ї–∞ –љ–∞—Ж–Є–Њ–љ–∞–ї—М–љ—Л—Е —А–µ–≥–Є—Б—В—А–Њ–≤ –µ—Й–µ –Љ–µ–љ–µ–µ —Г—В–µ—И–Є—В–µ–ї—М–љ–∞ –Є —Б–≤–Є–і–µ—В–µ–ї—М—Б—В–≤—Г–µ—В –Њ 45% —Г–≤–µ–ї–Є—З–µ–љ–Є–Є –Њ–±—Й–µ–≥–Њ –Ї–Њ–ї–Є—З–µ—Б—В–≤–∞ –∞–Љ–њ—Г—В–∞—Ж–Є–є –≤ –Р–љ–≥–ї–Є–Є —Б 1990 –њ–Њ 1994 –≥–Њ–і—Л [3] –Є, –∞–љ–∞–ї–Њ–≥–Є—З–љ–Њ, –≤ –®–Њ—В–ї–∞–љ–і–Є–Є –≤ –њ–µ—А–Є–Њ–і –Љ–µ–ґ–і—Г 1993 –Є 1998 –≥–Њ–і–∞–Љ–Є. –°—В—А—Г–Ї—В—Г—А—Г –∞–Љ–њ—Г—В–∞—Ж–Є–є –њ—А–Є —Н—В–Њ–Љ —Б–Њ—Б—В–∞–≤–ї—П—О—В –∞–Љ–њ—Г—В–∞—Ж–Є–Є –њ–∞–ї—М—Ж–µ–≤ –≤ 25% —Б–ї—Г—З–∞–µ–≤, –∞–Љ–њ—Г—В–∞—Ж–Є–Є –љ–∞ —Г—А–Њ–≤–љ–µ –≥–Њ–ї–µ–љ–Є –Є —Б—В–Њ–њ—Л –≤ 50% —Б–ї—Г—З–∞–µ–≤, –±–µ–і—А–∞ —Г 25% –±–Њ–ї—М–љ—Л—Е [4].
–£–≤–µ–ї–Є—З–µ–љ–Є–µ –Њ–±—Й–µ–≥–Њ —З–Є—Б–ї–∞ –∞–Љ–њ—Г—В–∞—Ж–Є–є —З–∞—Б—В–Є—З–љ–Њ –Љ–Њ–ґ–µ—В –±—Л—В—М –Њ–±—К—П—Б–љ–µ–љ–Њ —Г–ї—Г—З—И–µ–љ–Є–µ–Љ —А–µ–≥–Є—Б—В—А–∞—Ж–Є–Є, –∞ —В–∞–Ї–ґ–µ —Н–њ–Є–і–µ–Љ–Є—З–µ—Б–Ї–Є–Љ —А–Њ—Б—В–Њ–Љ —А–∞—Б–њ—А–Њ—Б—В—А–∞–љ–µ–љ–љ–Њ—Б—В–Є —Б–∞–Љ–Њ–≥–Њ —Б–∞—Е–∞—А–љ–Њ–≥–Њ –і–Є–∞–±–µ—В–∞. –Х—Б–ї–Є —Н–Ї—Б—В—А–∞–њ–Њ–ї–Є—А–Њ–≤–∞—В—М –њ–Њ–ї—Г—З–µ–љ–љ—Л–µ –і–∞–љ–љ—Л–µ –љ–∞ –Љ–Є—А–Њ–≤–Њ–є —Г—А–Њ–≤–µ–љ—М, —В–Њ –Ї–Њ–ї–Є—З–µ—Б—В–≤–Њ –∞–Љ–њ—Г—В–∞—Ж–Є–є —Г –±–Њ–ї—М–љ—Л—Е —Б–∞—Е–∞—А–љ—Л–Љ –і–Є–∞–±–µ—В–Њ–Љ –≤ –≥–ї–Њ–±–∞–ї—М–љ–Њ–Љ –∞—Б–њ–µ–Ї—В–µ —Б–Њ—Б—В–∞–≤–Є—В 55 –∞–Љ–њ—Г—В–∞—Ж–Є–є –≤ —З–∞—Б [5].
–Ъ–∞–Ї –љ–∞–Є–±–Њ–ї–µ–µ —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ –њ—А–µ–і–Њ—В–≤—А–∞—В–Є—В—М —Г–≥—А–Њ–ґ–∞—О—Й–Є–є –Њ–±—Й–µ—Б—В–≤—Г —А–Њ—Б—В –∞–Љ–њ—Г—В–∞—Ж–Є–є –≤—Б–ї–µ–і—Б—В–≤–Є–µ –і–Є–∞–±–µ—В–Є—З–µ—Б–Ї–Њ–є —Б—В–Њ–њ—Л? –Ю–њ—Л—В –Љ–љ–Њ–≥–Є—Е —Б—В—А–∞–љ —Г–±–µ–ґ–і–∞–µ—В, —З—В–Њ –і–ї—П –і–Њ—Б—В–Є–ґ–µ–љ–Є—П –і–∞–љ–љ–Њ–є —Ж–µ–ї–Є –љ–µ–Њ–±—Е–Њ–і–Є–Љ–∞ —Б–Є—Б—В–µ–Љ–∞ –Љ–µ—А –≥–Њ—Б—Г–і–∞—А—Б—В–≤–µ–љ–љ–Њ–≥–Њ –Љ–∞—Б—И—В–∞–±–∞. –Ю–љ–∞ –≤–Ї–ї—О—З–∞–µ—В –≤ —Б–µ–±—П: —Б–≤–Њ–µ–≤—А–µ–Љ–µ–љ–љ—Г—О –і–Є–∞–≥–љ–Њ—Б—В–Є–Ї—Г —Д–∞–Ї—В–Њ—А–Њ–≤ —А–Є—Б–Ї–∞ –і–Є–∞–±–µ—В–Є—З–µ—Б–Ї–Њ–є —Б—В–Њ–њ—Л; –Њ–Ї–∞–Ј–∞–љ–Є–µ –Ї–≤–∞–ї–Є—Д–Є—Ж–Є—А–Њ–≤–∞–љ–љ–Њ–є –Љ—Г–ї—М—В–Є–і–Є—Б—Ж–Є–њ–ї–Є–љ–∞—А–љ–Њ–є –њ–Њ–Љ–Њ—Й–Є, –Њ—Б–љ–Њ–≤–∞–љ–љ–Њ–є –љ–∞ –њ—А–Є–љ—Ж–Є–њ–∞—Е –њ—А–µ–µ–Љ—Б—В–≤–µ–љ–љ–Њ—Б—В–Є, –і–Њ–ї–≥–Њ—Б—А–Њ—З–љ–Њ—Б—В–Є –Є –Љ–љ–Њ–≥–Њ—Г—А–Њ–≤–љ–µ–≤–Њ–є –Њ—А–≥–∞–љ–Є–Ј–∞—Ж–Є–Є; –Њ–±–µ—Б–њ–µ—З–µ–љ–Є–µ –Њ—А—В–Њ–њ–µ–і–Є—З–µ—Б–Ї–Њ–є –Њ–±—Г–≤—М—О –±–Њ–ї—М–љ—Л—Е –≥—А—Г–њ–њ—Л –≤—Л—Б–Њ–Ї–Њ–≥–Њ —А–Є—Б–Ї–∞ —Б –Њ—Ж–µ–љ–Ї–Њ–є –µ–µ –њ—А–Њ—В–Є–≤–Њ—А–µ—Ж–Є–і–Є–≤–љ–Њ–є —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В–Є; —Г—З–µ—В–µ –∞–Љ–њ—Г—В–∞—Ж–Є–є –Є —П–Ј–≤–µ–љ–љ—Л—Е –і–µ—Д–µ–Ї—В–Њ–≤ —Б—В–Њ–њ –Є —Б–Њ–Ј–і–∞–љ–Є–µ —А–µ–≥–Є—Б—В—А–∞ –і–∞–љ–љ—Л—Е.
–§–∞–Ї—В–Њ—А—Л —А–Є—Б–Ї–∞ —А–∞–Ј–≤–Є—В–Є—П –і–Є–∞–±–µ—В–Є—З–µ—Б–Ї–Њ–є —П–Ј–≤—Л —Б—В–Њ–њ—Л
–Ъ–Њ–Љ–±–Є–љ–∞—Ж–Є—П —А–∞–Ј–ї–Є—З–љ—Л—Е —Д–∞–Ї—В–Њ—А–Њ–≤, –њ—А–µ–ґ–і–µ –≤—Б–µ–≥–Њ –њ–µ—А–Є—Д–µ—А–Є—З–µ—Б–Ї–Њ–є –љ–µ–є—А–Њ–њ–∞—В–Є–Є, –Љ–∞–Ї—А–Њ–∞–љ–≥–Є–Њ–њ–∞—В–Є–Є –Є –і–µ—Д–Њ—А–Љ–∞—Ж–Є–є –њ—А–Є–≤–Њ–і–Є—В –Ї –њ–Њ–≤—Л—И–µ–љ–Є—О —А–Є—Б–Ї–∞ –Њ–±—А–∞–Ј–Њ–≤–∞–љ–Є—П —П–Ј–≤, –Ї–Њ—В–Њ—А—Л–µ –њ–Њ –і–∞–љ–љ—Л–Љ —А–∞–Ј–ї–Є—З–љ—Л—Е —Н–њ–Є–і–µ–Љ–Є–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є—Е –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–є —Е–∞—А–∞–Ї—В–µ—А–Є–Ј—Г—О—В—Б—П —З–∞—Б—В–Њ—В–Њ–є 4–10% –Є –µ–ґ–µ–≥–Њ–і–љ–Њ–є –Ј–∞–±–Њ–ї–µ–≤–∞–µ–Љ–Њ—Б—В—М—О 2–3% —Б—А–µ–і–Є –њ–Њ–њ—Г–ї—П—Ж–Є–Є –±–Њ–ї—М–љ—Л—Е –і–Є–∞–±–µ—В–Њ–Љ [6].
–Ю–і–љ–∞–Ї–Њ —З–Є—Б–ї–Њ –±–Њ–ї—М–љ—Л—Е, —Б–Њ—Б—В–∞–≤–ї—П—О—Й–Є—Е –≥—А—Г–њ–њ—Г —А–Є—Б–Ї–∞ —А–∞–Ј–≤–Є—В–Є—П —П–Ј–≤ –Є –∞–Љ–њ—Г—В–∞—Ж–Є–є, –Ј–љ–∞—З–Є—В–µ–ї—М–љ–Њ –њ—А–µ–≤—Л—И–∞–µ—В –Ї–Њ–ї–Є—З–µ—Б—В–≤–Њ –љ–µ–њ–Њ—Б—А–µ–і—Б—В–≤–µ–љ–љ–Њ —Б–∞–Љ–Є—Е –Њ—Б–ї–Њ–ґ–љ–µ–љ–Є–є. –Ъ—А—Г–њ–љ–Њ–µ —Н–њ–Є–і–µ–Љ–Є–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Њ–µ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ, –њ—А–Њ–≤–µ–і–µ–љ–љ–Њ–µ –≤ –°–µ–≤–µ—А–Њ––Ч–∞–њ–∞–і–љ–Њ–є –Р–љ–≥–ї–Є–Є, –≤—Л—П–≤–Є–ї–Њ —Г 55% –≤–Ј—А–Њ—Б–ї–Њ–є –њ–Њ–њ—Г–ї—П—Ж–Є–Є –±–Њ–ї—М–љ—Л—Е –і–Є–∞–±–µ—В–Њ–Љ –њ—А–Є—Б—Г—В—Б—В–≤–Є–µ –і–≤—Г—Е –Є –±–Њ–ї–µ–µ —Д–∞–Ї—В–Њ—А–Њ–≤, –њ–Њ–Ј–≤–Њ–ї–Є–≤—И–Є—Е –Њ—В–љ–µ—Б—В–Є –±–Њ–ї—М–љ—Л—Е –Ї –≥—А—Г–њ–њ–µ –≤—Л—Б–Њ–Ї–Њ–≥–Њ —А–Є—Б–Ї–∞ [7].
–°—В—А–∞—В–µ–≥–Є—З–µ—Б–Ї–Є –≤–∞–ґ–љ—Л–Љ —Б —В–Њ—З–Ї–Є –Ј—А–µ–љ–Є—П –њ—А–µ–і–Њ—В–≤—А–∞—Й–µ–љ–Є—П –∞–Љ–њ—Г—В–∞—Ж–Є–є –Є —Н–Ї–Њ–љ–Њ–Љ–Є—З–µ—Б–Ї–Є –Њ–њ—А–∞–≤–і–∞–љ–љ—Л–Љ —П–≤–ї—П–µ—В—Б—П –Њ—Б—Г—Й–µ—Б—В–≤–ї–µ–љ–Є–µ —Б–Ї—А–Є–љ–Є–љ–≥–∞ –≥—А—Г–њ–њ—Л —А–Є—Б–Ї–∞ –і–Є–∞–±–µ—В–Є—З–µ—Б–Ї–Њ–є —Б—В–Њ–њ—Л –љ–∞ —Г—А–Њ–≤–љ–µ –њ–µ—А–≤–Є—З–љ–Њ–≥–Њ –Љ–µ–і–Є—Ж–Є–љ—Б–Ї–Њ–≥–Њ –Ј–≤–µ–љ–∞, –њ—А–Њ–≤–µ–і–µ–љ–Є–µ –Њ–±—Г—З–µ–љ–Є—П –Є –љ–∞–њ—А–∞–≤–ї–µ–љ–Є—П –≤ —Б–њ–µ—Ж–Є–∞–ї–Є–Ј–Є—А–Њ–≤–∞–љ–љ—Л–µ —Ж–µ–љ—В—А—Л, –≥–і–µ –Њ–Ї–∞–Ј—Л–≤–∞–µ—В—Б—П –Љ—Г–ї—М—В–Є–і–Є—Б—Ж–Є–њ–ї–Є–љ–∞—А–љ–∞—П –њ–Њ–Љ–Њ—Й—М. –Я—А–Њ–≤–µ–і–µ–љ–љ—Л–µ –љ–∞–Љ–Є –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П –њ–Њ–Ї–∞–Ј–∞–ї–Є, —З—В–Њ –≤ –≥—А—Г–њ–њ—Г —А–Є—Б–Ї–∞ —Б–ї–µ–і—Г–µ—В –≤–Ї–ї—О—З–∞—В—М –±–Њ–ї—М–љ—Л—Е —Б–∞—Е–∞—А–љ—Л–Љ –і–Є–∞–±–µ—В–Њ–Љ 2 —В–Є–њ–∞, 1 —В–Є–њ–∞ —Б –і–ї–Є—В–µ–ї—М–љ–Њ—Б—В—М—О –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П –±–Њ–ї–µ–µ 8 –ї–µ—В, —Б –љ–µ—Г–і–Њ–≤–ї–µ—В–≤–Њ—А–Є—В–µ–ї—М–љ—Л–Љ –≥–ї–Є–Ї–µ–Љ–Є—З–µ—Б–Ї–Є–Љ –Ї–Њ–љ—В—А–Њ–ї–µ–Љ, –њ—А–Є–Ј–љ–∞–Ї–∞–Љ–Є –њ–µ—А–Є—Д–µ—А–Є—З–µ—Б–Ї–Њ–є –љ–µ–≤—А–Њ–њ–∞—В–Є–Є –Є –Љ–∞–Ї—А–Њ–∞–љ–≥–Є–Њ–њ–∞—В–Є–Є–Є, —Б –≤–Є–і–Є–Љ—Л–Љ–Є –і–µ—Д–Њ—А–Љ–∞—Ж–Є—П–Љ–Є —Б—В–Њ–њ, —П–Ј–≤–∞–Љ–Є –Є –∞–Љ–њ—Г—В–∞—Ж–Є—П–Љ–Є –≤ –∞–љ–∞–Љ–љ–µ–Ј–µ, –њ—А–Њ–ї–Є—Д–µ—А–∞—В–Є–≤–љ–Њ–є —Б—В–∞–і–Є—П–Љ–Є —А–µ—В–Є–љ–Њ–њ–∞—В–Є–Є, –Љ–Є–Ї—А–Њ–∞–ї—М–±—Г–Љ–Є–љ—Г—А–Є—З–µ—Б–Ї–Њ–є –Є –њ—А–Њ—В–µ–Є–љ—Г—А–Є—З–µ—Б–Ї–Њ–є —Б—В–∞–і–Є—П–Љ–Є –љ–µ—Д—А–Њ–њ–∞—В–Є–Є, –≤ –≤–Њ–Ј—А–∞—Б—В–µ —Б—В–∞—А—И–µ 60 –ї–µ—В [7].
–Т–∞–ґ–љ–µ–є—И–Є–Љ —Д–∞–Ї—В–Њ—А–Њ–Љ —А–Є—Б–Ї–∞ —Б–Є–љ–і—А–Њ–Љ–∞ –і–Є–∞–±–µ—В–Є—З–µ—Б–Ї–Њ–є —Б—В–Њ–њ—Л –њ—А–Є–Ј–љ–∞–љ–∞ –њ–µ—А–Є—Д–µ—А–Є—З–µ—Б–Ї–∞—П —Б–µ–љ—Б–Њ–Љ–Њ—В–Њ—А–љ–∞—П –љ–µ–≤—А–Њ–њ–∞—В–Є—П (–Я–Э). –Ш–Ј—Г—З–∞—О—В—Б—П —А–∞–Ј–ї–Є—З–љ—Л–µ —Д–∞–Ї—В–Њ—А—Л, –Ї–Њ—В–Њ—А—Л–µ –Љ–Њ–≥—Г—В «–њ—А–µ–і—Б–Ї–∞–Ј—Л–≤–∞—В—М» –µ–µ –љ–∞–ї–Є—З–Є–µ –њ—А–Є –њ–Њ–њ—Г–ї—П—Ж–Є–Њ–љ–љ–Њ–Љ —Б–Ї—А–Є–љ–Є–љ–≥–µ. –Я–Э –љ–µ –Љ–Њ–ґ–µ—В –±—Л—В—М —Г—Б—В–∞–љ–Њ–≤–ї–µ–љ–∞ —В–Њ–ї—М–Ї–Њ –љ–∞ –Њ—Б–љ–Њ–≤–∞–љ–Є–Є –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є—Е —Б–Є–Љ–њ—В–Њ–Љ–Њ–≤. –Ю—Ж–µ–љ–Ї–∞ –њ–Њ—А–Њ–≥–∞ –≤–Є–±—А–∞—Ж–Є–Њ–љ–љ–Њ–≥–Њ —З—Г–≤—Б—В–≤–∞ (–Я–Т–І) –Ј–∞—В—А—Г–і–љ–µ–љ–∞ –≤—Б–ї–µ–і—Б—В–≤–Є–µ –≤–ї–Є—П–љ–Є—П –≤–Њ–Ј—А–∞—Б—В–љ–Њ–≥–Њ —Д–∞–Ї—В–Њ—А–∞, –њ—А–Њ–≤–Њ–і—П—В—Б—П –њ–Њ–њ—Л—В–Ї–Є –µ–≥–Њ –љ–Є–≤–µ–ї–Є—А–Њ–≤–∞–љ–Є—П –њ—Г—В–µ–Љ –Љ–Њ–і–Є—Д–Є–Ї–∞—Ж–Є–є –Љ–µ—В–Њ–і–∞ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П –Я–Т–І. –Ы—Г—З—И–Є–Љ–Є –њ—А–µ–і–Є–Ї—В–Њ—А–∞–Љ–Є –љ–µ–≤—А–Њ–њ–∞—В–Є–Є, –і–Њ—Б—В–Є–≥—И–µ–є –њ–Њ—А–Њ–≥–∞ «–љ–∞—А—Г—И–µ–љ–Є—П –њ—А–Њ—В–µ–Ї—В–Є–≤–љ–Њ–є —З—Г–≤—Б—В–≤–Є—В–µ–ї—М–љ–Њ—Б—В–Є» –њ—А–Є–Ј–љ–∞–љ—Л –Љ–Њ–љ–Њ—Д–Є–ї–∞–Љ–µ–љ—В Semmes Weinstein 5,07 (10 –≥—А–∞–Љ–Љ) —Б –Њ—Ж–µ–љ–Ї–Њ–є —З—Г–≤—Б—В–≤–Є—В–µ–ї—М–љ–Њ—Б—В–Є –Ї –і–∞–≤–ї–µ–љ–Є—О –Љ–Њ–љ–Њ—Д–Є–ї–∞–Љ–µ–љ—В–∞ –≤ –љ–µ—Б–Ї–Њ–ї—М–Ї–Є—Е —В–Њ—З–Ї–∞—Е —Б—В–Њ–њ—Л –Є —И–Ї–∞–ї–∞ –љ–µ–є—А–Њ–њ–∞—В–Є—З–µ—Б–Ї–Њ–≥–Њ –і–Є—Б—Д—Г–љ–Ї—Ж–Є–Њ–љ–∞–ї—М–љ–Њ–≥–Њ —Б—З–µ—В–∞ (–Э–Ф–°) [9]. –£–і–Њ–≤–ї–µ—В–≤–Њ—А–Є—В–µ–ї—М–љ—Л–µ —А–µ–Ј—Г–ї—М—В–∞—В—Л –њ–Њ–ї—Г—З–µ–љ—Л –њ—А–Є –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є–Є —Г–Ї–Њ–ї–∞ —В—Г–њ–Њ–є –Є–≥–ї–Њ–є, –Њ–і–љ–∞–Ї–Њ –і–Є–∞–≥–љ–Њ—Б—В–Є—З–µ—Б–Ї–∞—П —Ж–µ–љ–љ–Њ—Б—В—М –њ—А–Є —Б–Ї—А–Є–љ–Є–љ–≥–µ –љ–µ –њ—А–µ–≤—Л—И–∞–µ—В 60–80%. –°–Њ—З–µ—В–∞–љ–љ–Њ–µ –њ—А–Є–Љ–µ–љ–µ–љ–Є–µ –љ–µ—Б–Ї–Њ–ї—М–Ї–Є—Е –Љ–µ—В–Њ–і–Њ–≤ –Є, —Б–Њ–Њ—В–≤–µ—В—Б—В–≤–µ–љ–љ–Њ, —И–Ї–∞–ї—Л –Э–Ф–°, –Ј–љ–∞—З–Є—В–µ–ї—М–љ–Њ –њ–Њ–≤—Л—И–∞–µ—В –љ–∞–і–µ–ґ–љ–Њ—Б—В—М —А–µ–Ј—Г–ї—М—В–∞—В–∞ –Є –њ–Њ–Ј–≤–Њ–ї—П–µ—В –і–Є–∞–≥–љ–Њ—Б—В–Є—А–Њ–≤–∞—В—М –љ–µ–≤—А–Њ–њ–∞—В–Є—О —Б —З—Г–≤—Б—В–≤–Є—В–µ–ї—М–љ–Њ—Б—В—М—О –Є —Б–њ–µ—Ж–Є—Д–Є—З–љ–Њ—Б—В—М—О –±–Њ–ї–µ–µ 90%.
–°–Њ—З–µ—В–∞–љ–Є–µ —Д–∞–Ї—В–Њ—А–Њ–≤ —А–Є—Б–Ї–∞ –і–Є–∞–±–µ—В–Є—З–µ—Б–Ї–Њ–є —Б—В–Њ–њ—Л —Г—Б–Є–ї–Є–≤–∞–µ—В –Ї–Њ–љ–µ—З–љ—Л–є –Њ—В–љ–Њ—Б–Є—В–µ–ї—М–љ—Л–є —А–Є—Б–Ї (–Ю–†) —А–∞–Ј–≤–Є—В–Є—П —П–Ј–≤—Л —Б—В–Њ–њ—Л –Є –њ–Њ–Ј–≤–Њ–ї—П–µ—В –Њ—В–љ–Њ—Б–Є—В—М –±–Њ–ї—М–љ—Л—Е –Ї –Ї–∞—В–µ–≥–Њ—А–Є–Є —А–Є—Б–Ї–∞ – –љ–Є–Ј–Ї–Њ–≥–Њ, –≤—Л—Б–Њ–Ї–Њ–≥–Њ –Є–ї–Є –Њ—З–µ–љ—М –≤—Л—Б–Њ–Ї–Њ–≥–Њ, –Њ–њ—А–µ–і–µ–ї—П—В—М —З–∞—Б—В–Њ—В—Г –Є —Е–∞—А–∞–Ї—В–µ—А –њ—А–Њ—Д–Є–ї–∞–Ї—В–Є—З–µ—Б–Ї–Є—Е –Љ–µ—А–Њ–њ—А–Є—П—В–Є–є. –Э–∞–Є–±–Њ–ї—М—И–Є–є —А–Є—Б–Ї (–Ю–†=45) –Є–Љ–µ—О—В –±–Њ–ї—М–љ—Л–µ —Б –љ–∞–ї–Є—З–Є–µ–Љ —П–Ј–≤ –Є –∞–Љ–њ—Г—В–∞—Ж–Є–є, –Њ—Б–Њ–±–µ–љ–љ–Њ –Љ–∞–ї—Л—Е –∞–Љ–њ—Г—В–∞—Ж–Є–є, –≤ –∞–љ–∞–Љ–љ–µ–Ј–µ. –Ш–Љ –љ–µ–Њ–±—Е–Њ–і–Є–Љ—Л –њ—А–Њ—Д–Є–ї–∞–Ї—В–Є—З–µ—Б–Ї–Є–µ –Њ—Б–Љ–Њ—В—А—Л –≤ –Ї–∞–±–Є–љ–µ—В–∞—Е –і–Є–∞–±–µ—В–Є—З–µ—Б–Ї–Њ–є —Б—В–Њ–њ—Л –љ–µ —А–µ–ґ–µ 1 —А–∞–Ј–∞ –≤ 3 –Љ–µ—Б—П—Ж–∞. –Ю–±—П–Ј–∞—В–µ–ї—М–љ–Њ –Њ–±–µ—Б–њ–µ—З–µ–љ–Є–µ –Њ—А—В–Њ–њ–µ–і–Є—З–µ—Б–Ї–Њ–є –Њ–±—Г–≤—М—О.
–†–Њ–ї—М –љ–µ–≤—А–Њ–њ–∞—В–Є–Є –≤ —А–∞–Ј–≤–Є—В–Є–Є –і–Є–∞–±–µ—В–Є—З–µ—Б–Ї–Њ–є —Б—В–Њ–њ—Л
–Т—Л—Б–Њ–Ї–∞—П —З–∞—Б—В–Њ—В–∞ –љ–µ—В—А–∞–≤–Љ–∞—В–Є—З–µ—Б–Ї–Є—Е –∞–Љ–њ—Г—В–∞—Ж–Є–є —Г –±–Њ–ї—М–љ—Л—Е —Б–∞—Е–∞—А–љ—Л–Љ –і–Є–∞–±–µ—В–Њ–Љ –Њ–±—К—П—Б–љ—П–µ—В—Б—П –Ї–Њ–Љ–њ–ї–µ–Ї—Б–Њ–Љ —Д–∞–Ї—В–Њ—А–Њ–≤, –љ–Њ –њ—А–µ–ґ–і–µ –≤—Б–µ–≥–Њ —Б–≤—П–Ј–∞–љ–∞ —Б –њ—А–Є—Б—Г—В—Б—В–≤–Є–µ–Љ –њ–µ—А–Є—Д–µ—А–Є—З–µ—Б–Ї–Њ–є –љ–µ–≤—А–Њ–њ–∞—В–Є–Є. –Т —В–µ—З–µ–љ–Є–µ –њ–Њ—Б–ї–µ–і–љ–Є—Е –і–µ—Б—П—В–Є–ї–µ—В–Є–є –≤–Ј–≥–ї—П–і—Л –љ–∞ –њ–∞—В–Њ–≥–µ–љ–µ–Ј –Ф–° –њ—А–µ—В–µ—А–њ–µ–ї–Є –Ј–љ–∞—З–Є—В–µ–ї—М–љ—Л–µ –Є–Ј–Љ–µ–љ–µ–љ–Є—П. –Я–µ—А–Є—Д–µ—А–Є—З–µ—Б–Ї–Њ–є –љ–µ–≤—А–Њ–њ–∞—В–Є–µ–є –Є —Б–≤—П–Ј–∞–љ–љ–Њ–є —Б –љ–µ–є –Љ–Є–Ї—А–Њ—Ж–Є—А–Ї—Г–ї—П—В–Њ—А–љ–Њ–є –і–Є—Б—Д—Г–љ–Ї—Ж–Є–µ–є –Њ–±—К—П—Б–љ—П–µ—В—Б—П –љ–∞—А—Г—И–µ–љ–Є–µ –≤–Њ—Б–њ–∞–ї–Є—В–µ–ї—М–љ–Њ–≥–Њ –Њ—В–≤–µ—В–∞ –љ–∞ —В—А–∞–≤–Љ—Г –Є —А–∞–Ј–≤–Є—В–Є–µ –љ–µ–є—А–Њ–њ–∞—В–Є—З–µ—Б–Ї–Њ–≥–Њ –Њ—В–µ–Ї–∞, —З—В–Њ –≤—Л–Ј—Л–≤–∞–µ—В –±—Л—Б—В—А–Њ–µ –њ—А–Њ–≥—А–µ—Б—Б–Є—А–Њ–≤–∞–љ–Є–µ –Є–љ—Д–µ–Ї—Ж–Є–Є –≤ —В–Ї–∞–љ–Є —Б—В–Њ–њ—Л –Є –њ—А–µ–њ—П—В—Б—В–≤—Г–µ—В –Ј–∞–ґ–Є–≤–ї–µ–љ–Є—О —А–∞–љ—Л.
–І–∞—Б—В–Њ—В–∞ –Я–Э —П–≤–љ–Њ –њ—А–µ–≤–∞–ї–Є—А—Г–µ—В –љ–∞–і –њ–∞—В–Њ–ї–Њ–≥–Є–µ–є –Љ–∞–≥–Є—Б—В—А–∞–ї—М–љ—Л—Е —Б–Њ—Б—Г–і–Њ–≤, –Ї–∞–Ї –Њ—Б–љ–Њ–≤–љ–Њ–є —Д–∞–Ї—В–Њ—А —А–∞–Ј–≤–Є—В–Є—П –Ф–°: 92% –њ—А–Њ—В–Є–≤ 27%, –њ–Њ —А–µ–Ј—Г–ї—М—В–∞—В–∞–Љ –Њ—В—З–µ—В–∞ DFSG (Diabetic Foot Study Group, 2000). –Я—А–Є —Н—В–Њ–Љ —Г–і–µ–ї—П–µ—В—Б—П –≤–љ–Є–Љ–∞–љ–Є–µ –љ–µ —В–Њ–ї—М–Ї–Њ —Б–µ–љ—Б–Њ—А–љ—Л–Љ –љ–∞—А—Г—И–µ–љ–Є—П–Љ, –Ї–Њ—В–Њ—А—Л–µ, –њ—А–Њ–≥—А–µ—Б—Б–Є—А—Г—П, –њ–µ—А–µ—Е–Њ–і—П—В –њ–Њ—А–Њ–≥ «–љ–∞—А—Г—И–µ–љ–Є—П –њ—А–Њ—В–µ–Ї—В–Є–≤–љ–Њ–є —З—Г–≤—Б—В–≤–Є—В–µ–ї—М–љ–Њ—Б—В–Є», –Њ—Б—В–∞–≤–ї—П—П —Б—В–Њ–њ—Г –±–µ–Ј —Б–Є–≥–љ–∞–ї–Њ–≤ –Ј–∞—Й–Є—В—Л –Њ—В –Њ–ґ–Њ–≥–∞ –Є–ї–Є –Љ–µ—Е–∞–љ–Є—З–µ—Б–Ї–Њ–є —В—А–∞–≤–Љ—Л. –Ю—Б—В–∞—О—В—Б—П –љ–µ–Ј–∞–Љ–µ—З–µ–љ–љ—Л–Љ–Є —А–∞–Ј–≤–Є–≤–∞—О—Й–Є–µ—Б—П –Љ–Њ—В–Њ—А–љ—Л–µ –љ–µ–≤—А–Њ–њ–∞—В–Є—З–µ—Б–Ї–Є–µ —А–∞—Б—Б—В—А–Њ–є—Б—В–≤–∞, –Ї–Њ—В–Њ—А—Л–µ –њ—А–Њ—П–≤–ї—П—О—В—Б—П –њ—А–µ–ґ–і–µ –≤—Б–µ–≥–Њ —Б–љ–Є–ґ–µ–љ–Є–µ–Љ —В–Њ–љ—Г—Б–∞ –Є —Б–ї–∞–±–Њ—Б—В—М—О –Љ—Л—И—Ж —Б—В–Њ–њ—Л. –Т–Њ–Ј–љ–Є–Ї–∞—О—В –Є–Ј–Љ–µ–љ–µ–љ–Є—П –±–Є–Њ–Љ–µ—Е–∞–љ–Є—З–µ—Б–Ї–Є—Е —Б–≤–Њ–є—Б—В–≤ —Б—В–Њ–њ—Л, –і–Є—Б—Д—Г–љ–Ї—Ж–Є—П –Є –Њ–≥—А–∞–љ–Є—З–µ–љ–Є—П –њ–Њ–і–≤–Є–ґ–љ–Њ—Б—В–Є –Љ–µ–ї–Ї–Є—Е –Є –Ї—А—Г–њ–љ—Л—Е —Б—Г—Б—В–∞–≤–Њ–≤. –Ю–±—А–∞–Ј—Г—О—В—Б—П –Ј–Њ–љ—Л –њ–Њ–≤—Л—И–µ–љ–љ—Л—Е –њ–ї–∞–љ—В–∞—А–љ—Л—Е –і–∞–≤–ї–µ–љ–Є–є, –≥–і–µ —Д–Њ—А–Љ–Є—А—Г—О—Й–Є–µ—Б—П –≤–њ–Њ—Б–ї–µ–і—Б—В–≤–Є–Є –≥–Є–њ–µ—А–Ї–µ—А–∞—В–Њ–Ј—Л —Б–њ–Њ—Б–Њ–±—Б—В–≤—Г—О—В —А–∞–Ј–≤–Є—В–Є—О –њ–ї–∞–љ—В–∞—А–љ—Л—Е —П–Ј–≤ –≤ —В–Є–њ–Є—З–љ—Л—Е –Љ–µ—Б—В–∞—Е –±–Є–Њ–Љ–µ—Е–∞–љ–Є—З–µ—Б–Ї–Њ–≥–Њ –љ–∞–≥—А—Г–ґ–µ–љ–Є—П. –†–∞–љ–љ–Є–µ –љ–∞—А—Г—И–µ–љ–Є—П –њ–Њ—Е–Њ–і–Ї–Є –Њ—Б—В–∞—О—В—Б—П –љ–µ–Ј–∞–Љ–µ—З–µ–љ–љ—Л–Љ–Є, –Ї–∞–Ї –Є –њ–Њ–Ј–і–љ–Є–µ –∞–љ–Њ–Љ–∞–ї–Є–Є, –љ–∞–њ—А–Є–Љ–µ—А, —З–∞—Б—В—Л–µ –њ–∞–і–µ–љ–Є—П –±–Њ–ї—М–љ—Л—Е –≤—Б–ї–µ–і—Б—В–≤–Є–µ –љ–∞—А—Г—И–µ–љ–Є—П –Ї–Њ–Љ–њ–µ–љ—Б–∞—В–Њ—А–љ–Њ–≥–Њ –Њ—В—Б—В–∞–≤–ї–µ–љ–Є—П –љ–Њ–≥–Є –≤ —Б—В–Њ—А–Њ–љ—Г –њ—А–Є –љ–µ—Г—Б—В–Њ–є—З–Є–≤–Њ—Б—В–Є [10].
–Я–µ—А–Є—Д–µ—А–Є—З–µ—Б–Ї–∞—П —Б–µ–љ—Б–Њ–Љ–Њ—В–Њ—А–љ–∞—П –љ–µ–є—А–Њ–њ–∞—В–Є—П —И–Є—А–Њ–Ї–Њ —А–∞—Б–њ—А–Њ—Б—В—А–∞–љ–µ–љ–∞ –Ї–∞–Ї –≤–Њ –≤–Ј—А–Њ—Б–ї–Њ–є –њ–Њ–њ—Г–ї—П—Ж–Є–Є –±–Њ–ї—М–љ—Л—Е —Б–∞—Е–∞—А–љ—Л–Љ –і–Є–∞–±–µ—В–Њ–Љ 1 –Є 2 —В–Є–њ–∞ (–і–Њ 50%), —В–∞–Ї –Є —Б—А–µ–і–Є –і–µ—В–µ–є –Є –њ–Њ–і—А–Њ—Б—В–Ї–Њ–≤.
–Ю—Б–љ–Њ–≤–љ—Л–Љ–Є —Д–∞–Ї—В–Њ—А–∞–Љ–Є –њ–∞—В–Њ–≥–µ–љ–µ–Ј–∞ –Я–Э —П–≤–ї—П—О—В—Б—П –Є–Ј–Љ–µ–љ–µ–љ–Є—П, –Ї–Њ—В–Њ—А—Л–µ, –њ–Њ —Б—Г—В–Є, –Є–љ–і—Г—Ж–Є—А—Г—О—В –Љ–µ—В–∞–±–Њ–ї–Є—З–µ—Б–Ї–Є–µ –Є —Б–Њ—Б—Г–і–Є—Б—В—Л–µ —А–∞—Б—Б—В—А–Њ–є—Б—В–≤–∞ –≤ –љ–µ—А–≤–љ–Њ–Љ –≤–Њ–ї–Њ–Ї–љ–µ, —Е–∞—А–∞–Ї—В–µ—А–Є–Ј—Г—О—Й–Є–µ—Б—П –Ї–∞–Ї –і–µ–Љ–Є–µ–ї–Є–љ–Є–Ј–Є—А—Г—О—Й–∞—П –љ–µ–≤—А–Њ–њ–∞—В–Є—П.
–Я–∞—В–Њ–≥–µ–љ–µ–Ј –љ–µ–≤—А–Њ–њ–∞—В–Є–Є –Љ—Г–ї—М—В–Є—Д–∞–Ї—В–Њ—А–Є–∞–ї–µ–љ. –Я–Њ—Б—В–Њ—П–љ–љ–∞—П –≥–Є–њ–µ—А–≥–ї–Є–Ї–µ–Љ–Є—П —Г–≤–µ–ї–Є—З–Є–≤–∞–µ—В –∞–Ї—В–Є–≤–љ–Њ—Б—В—М –њ–Њ–ї–Є–Њ–ї–Њ–≤–Њ–≥–Њ –њ—Г—В–Є –Њ–±–Љ–µ–љ–∞ —Б –љ–∞–Ї–Њ–њ–ї–µ–љ–Є–µ–Љ —Б–Њ—А–±–Є—В–Њ–ї–∞ –Є —Д—А—Г–Ї—В–Њ–Ј—Л –≤ –љ–µ—А–≤–µ, —Б–Њ–њ—Г—В—Б—В–≤—Г—О—Й–µ–µ —Б–љ–Є–ґ–µ–љ–Є–µ —Б–Њ–і–µ—А–ґ–∞–љ–Є—П –Љ–Є–Њ–Є–љ–Њ–Ј–Є—В–Њ–ї–∞ —Б–њ–Њ—Б–Њ–±—Б—В–≤—Г–µ—В –Ј–∞–і–µ—А–ґ–Ї–µ –љ–∞—В—А–Є—П, –Њ—В–µ–Ї—Г, —Г—В–Њ–ї—Й–µ–љ–Є—О –Љ–Є–µ–ї–Є–љ–∞, –∞–Ї—Б–Њ–љ–∞–ї—М–љ–Њ–є –і–Є—Б—Д—Г–љ–Ї—Ж–Є–Є –Є –і–µ–≥–µ–љ–µ—А–∞—Ж–Є–Є –љ–µ—А–≤–∞.
–У–Є–њ–µ—А–≥–ї–Є–Ї–µ–Љ–Є—П –Ј–∞–њ—Г—Б–Ї–∞–µ—В –Ї–∞—Б–Ї–∞–і —А–µ–∞–Ї—Ж–Є–є —Б –Њ–±—А–∞–Ј–Њ–≤–∞–љ–Є–µ–Љ –Ї–Њ–љ–µ—З–љ—Л—Е –њ—А–Њ–і—Г–Ї—В–Њ–≤ –≥–ї–Є–Ї–Є—А–Њ–≤–∞–љ–Є—П (AGEs), –њ–Њ–≤—А–µ–ґ–і–∞—О—Й–Є—Е —Н–љ–і–Њ—В–µ–ї–Є–є, —Б–њ–Њ—Б–Њ–±—Б—В–≤—Г—О—Й–Є—Е —А–∞–Ј–≤–Є—В–Є—О –Њ–Ї—Б–Є–і–∞—В–Є–≤–љ–Њ–≥–Њ —Б—В—А–µ—Б—Б–∞, –Є–Ј–±—Л—В–Њ—З–љ–Њ–Љ—Г —Б–Є–љ—В–µ–Ј—Г —Б–≤–Њ–±–Њ–і–љ—Л—Е —А–∞–і–Є–Ї–∞–ї–Њ–≤, —Б–љ–Є–ґ–µ–љ–Є—О –Њ–Ї–Є—Б–ї–µ–љ–Є—П –ї–Є–њ–Њ–њ—А–Њ—В–µ–Є–і–Њ–≤ –љ–Є–Ј–Ї–Њ–є –њ–ї–Њ—В–љ–Њ—Б—В–Є, –∞–Ї—В–Є–≤–∞—Ж–Є–Є –њ—А–Є—Б—В–µ–љ–Њ—З–љ–Њ–≥–Њ —В—А–Њ–Љ–±–Њ–Њ–±—А–∞–Ј–Њ–≤–∞–љ–Є—П –Є —Б–љ–Є–ґ–µ–љ–Є—О –∞–Ї—В–Є–≤–љ–Њ—Б—В–Є –∞–љ—В–Є–Њ–Ї—Б–Є–і–∞–љ—В–љ–Њ–є –Ј–∞—Й–Є—В—Л. –Э–∞—А—Г—И–µ–љ–Є–µ —Б–Є–љ—В–µ–Ј–∞ —Н–љ–і–Њ—В–µ–ї–Є–µ–Љ –≤–∞–Ј–Њ–∞–Ї—В–Є–≤–љ—Л—Е —Д–∞–Ї—В–Њ—А–Њ–≤, –≤ —В–Њ–Љ —З–Є—Б–ї–µ NO (–Њ–Ї—Б–Є–і–∞ –∞–Ј–Њ—В–∞) –≤—Л–Ј—Л–≤–∞–µ—В —Г–≤–µ–ї–Є—З–µ–љ–Є–µ –≤–љ—Г—В—А–Є–Ї–∞–њ–Є–ї–ї—П—А–љ–Њ–≥–Њ –і–∞–≤–ї–µ–љ–Є—П, —А–∞–Ј–≤–Є—В–Є–µ —Н–љ–і–Њ–љ–µ–≤—А–∞–ї—М–љ–Њ–≥–Њ –Њ—В–µ–Ї–∞ –Є –≥–Є–њ–Њ–Ї—Б–Є–Є.
–Ъ–ї–∞—Б—Б–Є—Д–Є–Ї–∞—Ж–Є—П. –Ъ–ї–Є–љ–Є—З–µ—Б–Ї–Є–µ —Д–Њ—А–Љ—Л
–Я–∞—А–∞–ї–ї–µ–ї—М–љ–Њ –і–ї–Є—В–µ–ї—М–љ–Њ—Б—В–Є –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П, –њ–Њ –љ–∞—А–∞—Б—В–∞—О—Й–µ–є –њ—А–Њ–Є—Б—Е–Њ–і–Є—В –њ–Њ—Б—В–µ–њ–µ–љ–љ–∞—П –≥–Є–±–µ–ї—М –љ–µ—А–≤–љ–Њ–≥–Њ –≤–Њ–ї–Њ–Ї–љ–∞, –≤ –њ—А–Њ—Ж–µ—Б—Б–µ –Ї–Њ—В–Њ—А–Њ–є –Љ–Њ–ґ–љ–Њ –≤—Л–і–µ–ї–Є—В—М —А—П–і –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є—Е —Б—В–∞–і–Є–є: —Б—Г–±–Ї–ї–Є–љ–Є—З–µ—Б–Ї—Г—О, –Ї–ї–Є–љ–Є—З–µ—Б–Ї—Г—О –Є —Б—В–∞–і–Є—О –њ–Њ–Ј–і–љ–Є—Е –Њ—Б–ї–Њ–ґ–љ–µ–љ–Є–є [11].
–°—Г–±–Ї–ї–Є–љ–Є—З–µ—Б–Ї–∞—П —Б—В–∞–і–Є—П —Е–∞—А–∞–Ї—В–µ—А–Є–Ј—Г–µ—В—Б—П –Њ—В—Б—Г—В—Б—В–≤–Є–µ–Љ —Б–Є–Љ–њ—В–Њ–Љ–Њ–≤ –Є –њ—А–Є–Ј–љ–∞–Ї–Њ–≤ –љ–µ–є—А–Њ–њ–∞—В–Є–Є, –і–Є–∞–≥–љ–Њ–Ј —Г—Б—В–∞–љ–∞–≤–ї–Є–≤–∞–µ—В—Б—П –њ—А–Є —Б–њ–µ—Ж–Є–∞–ї–Є–Ј–Є—А–Њ–≤–∞–љ–љ–Њ–Љ —Н–ї–µ–Ї—В—А–Њ—Д–Є–Ј–Є–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Њ–Љ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є. –Я–Њ –Љ–µ—А–µ –њ—А–Њ–≥—А–µ—Б—Б–Є—А–Њ–≤–∞–љ–Є—П –њ–Њ—А–∞–ґ–µ–љ–Є—П –љ–µ—А–≤–∞ –њ–Њ—П–≤–ї—П–µ—В—Б—П —Б–Є–Љ–њ—В–Њ–Љ–∞—В–Є–Ї–∞ –Є –Њ–±–љ–∞—А—Г–ґ–Є–≤–∞—О—В—Б—П –њ—А–Є–Ј–љ–∞–Ї–Є –њ–Њ—А–∞–ґ–µ–љ–Є—П –љ–µ—А–≤–∞ –њ—А–Є –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Њ–Љ –Њ–±—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є.
–Ъ–ї–Є–љ–Є—З–µ—Б–Ї–∞—П –љ–µ–≤—А–Њ–њ–∞—В–Є—П –Љ–Њ–ґ–µ—В –њ—А–Њ—В–µ–Ї–∞—В—М –≤ —Д–Њ—А–Љ–µ –Њ—Б—В—А–Њ–є –±–Њ–ї–µ–≤–Њ–є –љ–µ–≤—А–Њ–њ–∞—В–Є–Є, –ї–Њ–Ї–∞–ї–Є–Ј—Г—О—Й–µ–є—Б—П —З–∞—Б—В–Њ –≤ –Њ–±–ї–∞—Б—В–Є —В—Г–ї–Њ–≤–Є—Й–∞ –Є –љ–µ —Б–Њ–њ—А–Њ–≤–Њ–ґ–і–∞—О—Й–µ–є—Б—П –Ј–љ–∞—З–Є—В–µ–ї—М–љ—Л–Љ–Є –Њ–±—К–µ–Ї—В–Є–≤–љ—Л–Љ–Є –њ—А–Є–Ј–љ–∞–Ї–∞–Љ–Є –њ–Њ—А–∞–ґ–µ–љ–Є—П. –Ґ–Є–њ–Є—З–љ—Л–Љ –≤–∞—А–Є–∞–љ—В–Њ–Љ —П–≤–ї—П–µ—В—Б—П —Е—А–Њ–љ–Є—З–µ—Б–Ї–∞—П –±–Њ–ї–µ–≤–∞—П –љ–µ–є—А–Њ–њ–∞—В–Є—П, —Е–∞—А–∞–Ї—В–µ—А–Є–Ј—Г—О—Й–∞—П—Б—П –ґ–ґ–µ–љ–Є–µ–Љ, –±–Њ–ї—М—О –Є–ї–Є –Њ–љ–µ–Љ–µ–љ–Є–µ–Љ –њ–Њ —В–Є–њ—Г «–љ–Њ—Б–Ї–Є––њ–µ—А—З–∞—В–Ї–Є», —Г—Б–Є–ї–µ–љ–Є–µ–Љ —Б–Є–Љ–њ—В–Њ–Љ–Њ–≤ –љ–Њ—З—М—О. –Э–∞–ї–Є—З–Є–µ –±–Њ–ї–Є –Љ–Њ–ґ–µ—В –Њ—В—А–∞–ґ–∞—В—М –њ—А–Њ—Ж–µ—Б—Б –і–µ–≥–µ–љ–µ—А–∞—Ж–Є–Є–—А–µ–≥–µ–љ–µ—А–∞—Ж–Є–Є –љ–µ—А–≤–љ—Л—Е –≤–Њ–ї–Њ–Ї–Њ–љ —Б —Д–Њ—А–Љ–Є—А–Њ–≤–∞–љ–Є–µ–Љ –≤–Њ–Ј–±—Г–ґ–і–µ–љ–Є—П –љ–Њ—Ж–Є—Ж–µ–њ—В–Є–≤–љ—Л—Е –Њ–±—А–∞–Ј–Њ–≤–∞–љ–Є–є, –њ–∞—В–Њ–ї–Њ–≥–Є—З–µ—Б–Ї—Г—О –∞–Ї—В–Є–≤–љ–Њ—Б—В—М —Б–Є–љ–∞–њ—Б–Њ–≤ —Б–њ–Є–љ–љ–Њ–≥–Њ –Љ–Њ–Ј–≥–∞, –њ–µ—А–Є—Д–µ—А–Є—З–µ—Б–Ї–Є—Е —Б–Є–Љ–њ–∞—В–Є—З–µ—Б–Ї–Є—Е –љ–µ–є—А–Њ–љ–Њ–≤ –Є–ї–Є –≤–Њ–Ј–љ–Є–Ї–љ–Њ–≤–µ–љ–Є—П –љ–∞—А—Г—И–µ–љ–Є–є –≤ –Њ–±–ї–∞—Б—В—П—Е –Љ–Њ–Ј–≥–∞, –Њ—В–≤–µ—В—Б—В–≤–µ–љ–љ—Л—Е –Ј–∞ –≤–Њ—Б–њ—А–Є—П—В–Є–µ –±–Њ–ї–Є [10]. –Ф–Є–∞–±–µ—В–Є—З–µ—Б–Ї–∞—П –∞–Љ–Є–Њ—В—А–Њ—Д–Є—П –њ—А–Њ—П–≤–ї—П–µ—В—Б—П –±–Њ–ї—М—О, —В—П–ґ–µ–ї–Њ–є –∞—Б—Б–Є–Љ–µ—В—А–Є—З–љ–Њ–є –∞—В—А–Њ—Д–Є–µ–є –њ—А–Њ–Ї—Б–Є–Љ–∞–ї—М–љ—Л—Е –Љ—Л—И—Ж –љ–Є–ґ–љ–Є—Е –Ї–Њ–љ–µ—З–љ–Њ—Б—В–µ–є (iliopsoas, quadrice—Аs) –Є —Б–≤—П–Ј–∞–љ–∞ —Б –Њ—Б—В—А–Њ–є –Є—И–µ–Љ–Є–µ–є –Є –Љ–љ–Њ–ґ–µ—Б—В–≤–µ–љ–љ—Л–Љ–Є –Є–љ—Д–∞—А–Ї—В–∞–Љ–Є –њ—А–Њ–Ї—Б–Є–Љ–∞–ї—М–љ—Л—Е –љ–µ—А–≤–љ—Л—Е —Б—В–≤–Њ–ї–Њ–≤ –Є –њ–Њ—П—Б–љ–Є—З–љ–Њ––Ї—А–µ—Б—В—Ж–Њ–≤–Њ–≥–Њ –љ–µ—А–≤–љ–Њ–≥–Њ —Б–њ–ї–µ—В–µ–љ–Є—П. –Ф–Є–∞–±–µ—В–Є—З–µ—Б–Ї–∞—П –∞–Љ–Є–Њ—В—А–Њ—Д–Є—П —А–∞–Ј—А–µ—И–∞–µ—В—Б—П —Б–∞–Љ–Њ—Б—В–Њ—П—В–µ–ї—М–љ–Њ –≤ —В–µ—З–µ–љ–Є–µ 1–3 –ї–µ—В. –С–µ–Ј–±–Њ–ї–µ–≤–∞—П –љ–µ–є—А–Њ–њ–∞—В–Є—П —Б —З–∞—Б—В–Є—З–љ–Њ–є –Є–ї–Є –њ–Њ–ї–љ–Њ–є –њ–Њ—В–µ—А–µ–є —З—Г–≤—Б—В–≤–Є—В–µ–ї—М–љ–Њ—Б—В–Є —П–≤–ї—П–µ—В—Б—П –њ—А–Њ–≥—А–µ–і–Є–µ–љ—В–љ–Њ–є —Б—В–∞–і–Є–µ–є –Я–Э, –њ—А–µ–і—Б—В–∞–≤–ї—П—О—Й–µ–є —П–≤–љ—Г—О —Г–≥—А–Њ–Ј—Г –≤–Њ–Ј–љ–Є–Ї–љ–Њ–≤–µ–љ–Є—П –њ–Њ—А–∞–ґ–µ–љ–Є–є —Б—В–Њ–њ—Л.
–°—В–∞–і–Є—П –њ–Њ–Ј–і–љ–Є—Е –Њ—Б–ї–Њ–ґ–љ–µ–љ–Є–є –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Њ–є –љ–µ–є—А–Њ–њ–∞—В–Є–Є –≤–Ї–ї—О—З–∞–µ—В –≤—Б–µ –≤–∞—А–Є–∞–љ—В—Л –љ–µ–є—А–Њ–њ–∞—В–Є—З–µ—Б–Ї–Є—Е —Д–Њ—А–Љ —Б–Є–љ–і—А–Њ–Љ–∞ –і–Є–∞–±–µ—В–Є—З–µ—Б–Ї–Њ–є —Б—В–Њ–њ—Л: –љ–µ–є—А–Њ–њ–∞—В–Є—З–µ—Б–Ї–Є–µ —П–Ј–≤—Л, –љ–µ–є—А–Њ–Њ—Б—В–µ–Њ–∞—А—В—А–Њ–њ–∞—В–Є—О –Є –љ–µ—В—А–∞–≤–Љ–∞—В–Є—З–µ—Б–Ї–Є–µ –∞–Љ–њ—Г—В–∞—Ж–Є–Є, —З–∞—Й–µ –љ–∞ —Г—А–Њ–≤–љ–µ –њ–∞–ї—М—Ж–µ–≤ –Є–ї–Є —Б—В–Њ–њ—Л –≤ —Б–≤—П–Ј–Є —Б –≤—Л—Б–Њ–Ї–Є–Љ–Є –≤–Њ–Ј–Љ–Њ–ґ–љ–Њ—Б—В—П–Љ–Є –Ј–∞–ґ–Є–≤–ї–µ–љ–Є—П —А–∞–љ—Л –њ—А–Є —Е–Њ—А–Њ—И–µ–Љ –Љ–∞–≥–Є—Б—В—А–∞–ї—М–љ–Њ–Љ –Ї—А–Њ–≤–Њ—В–Њ–Ї–µ. –Ґ–∞–Ї–Є–Љ –Њ–±—А–∞–Ј–Њ–Љ, –љ–µ–є—А–Њ–њ–∞—В–Є—З–µ—Б–Ї–∞—П –і–Є–∞–±–µ—В–Є—З–µ—Б–Ї–∞—П —Б—В–Њ–њ–∞ –≤ –њ–Њ–ї–љ–Њ–є –Љ–µ—А–µ —П–≤–ї—П–µ—В—Б—П –њ–Њ–Ј–і–љ–Є–Љ –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є–Љ –Њ—Б–ї–Њ–ґ–љ–µ–љ–Є–µ–Љ –і–Є–∞–±–µ—В–Є—З–µ—Б–Ї–Њ–є –њ–µ—А–Є—Д–µ—А–Є—З–µ—Б–Ї–Њ–є –љ–µ–≤—А–Њ–њ–∞—В–Є–Є.
–° —В–Њ—З–Ї–Є –Ј—А–µ–љ–Є—П –Њ—Б–Њ–±–µ–љ–љ–Њ—Б—В–µ–є –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Њ–є –Ї–∞—А—В–Є–љ—Л –Є —Д–Њ—А–Љ–Є—А–Њ–≤–∞–љ–Є—П –і–Є—Д—Д–µ—А–µ–љ—Ж–Є—А–Њ–≤–∞–љ–љ–Њ–≥–Њ –ї–µ—З–µ–љ–Є—П –Є —А–µ–∞–±–Є–ї–Є—В–∞—Ж–Є–Є —Ж–µ–ї–µ—Б–Њ–Њ–±—А–∞–Ј–љ–Њ –≤—Л–і–µ–ї—П—В—М –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є–µ —Д–Њ—А–Љ—Л —Б–Є–љ–і—А–Њ–Љ–∞ –і–Є–∞–±–µ—В–Є—З–µ—Б–Ї–Њ–є —Б—В–Њ–њ—Л: –љ–µ–є—А–Њ–њ–∞—В–Є—З–µ—Б–Ї–Є–µ —П–Ј–≤—Л —Б—В–Њ–њ—Л, –љ–µ–є—А–Њ–Њ—Б—В–µ–Њ–∞—А—В—А–Њ–њ–∞—В–Є—О (—Б—В–Њ–њ—Г –®–∞—А–Ї–Њ) –Є –љ–µ–є—А–Њ–Є—И–µ–Љ–Є—З–µ—Б–Ї–Є–µ —П–Ј–≤—Л —Б—В–Њ–њ—Л (—А–Є—Б. 1).
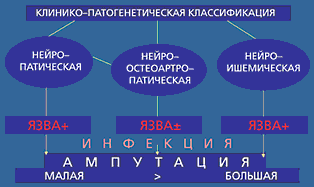
–†–Є—Б. 1. –Ъ–ї–Є–љ–Є—З–µ—Б–Ї–Є–µ —Д–Њ—А–Љ—Л —Б–Є–љ–і—А–Њ–Љ–∞ –і–Є–∞–±–µ—В–Є—З–µ—Б–Ї–Њ–є —Б—В–Њ–њ—Л
–Э–µ–є—А–Њ–њ–∞—В–Є—З–µ—Б–Ї–Є–µ –Є –љ–µ–є—А–Њ–Є—И–µ–Љ–Є—З–µ—Б–Ї–Є–µ —П–Ј–≤—Л —А–∞–Ј–ї–Є—З–∞—О—В—Б—П –њ—А–µ–ґ–і–µ –≤—Б–µ–≥–Њ —Д–∞–Ї—В–Њ–Љ –Њ—В—Б—Г—В—Б—В–≤–Є—П —Б–µ—А—М–µ–Ј–љ–Њ–≥–Њ –њ–Њ—А–∞–ґ–µ–љ–Є—П –Љ–∞–≥–Є—Б—В—А–∞–ї—М–љ—Л—Е –∞—А—В–µ—А–Є–є —Г –њ–µ—А–≤—Л—Е –Є –µ–≥–Њ –љ–∞–ї–Є—З–Є–µ–Љ —Г –≤—В–Њ—А—Л—Е (—Б–ї–µ–і–Њ–≤–∞—В–µ–ї—М–љ–Њ, —В—П–ґ–µ—Б—В—М –Є—И–µ–Љ–Є–Є –Њ–њ—А–µ–і–µ–ї—П–µ—В —Е–∞—А–∞–Ї—В–µ—А –Є —А–µ–Ј—Г–ї—М—В–∞—В –ї–µ—З–µ–љ–Є—П –љ–µ–є—А–Њ–Є—И–µ–Љ–Є—З–µ—Б–Ї–Є—Е —П–Ј–≤). –Я—А–Њ–≥—А–µ—Б—Б–Є–≤–љ–Њ–µ —Б–љ–Є–ґ–µ–љ–Є–µ –Ї–Њ–ґ–љ–Њ–є –Њ–Ї—Б–Є–≥–µ–љ–∞—Ж–Є–Є (–Ґ—Б—А–Ю2) –≤ –Њ–±–ї–∞—Б—В–Є –љ–µ–є—А–Њ–Є—И–µ–Љ–Є—З–µ—Б–Ї–Њ–є —П–Ј–≤—Л —П–≤–ї—П–µ—В—Б—П –Ї—А–Є—В–Є—З–µ—Б–Ї–Њ–є —Д–Є–Ј–Є–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Њ–є –і–µ—В–µ—А–Љ–Є–љ–∞–љ—В–Њ–є, –Њ–њ—А–µ–і–µ–ї—П—О—Й–µ–є –≤–Њ–Ј–Љ–Њ–ґ–љ–Њ—Б—В—М –µ–µ –Ј–∞–ґ–Є–≤–ї–µ–љ–Є—П, –Є –њ—А–Є —Г—А–Њ–≤–љ–µ –Ґ—Б—А–Ю2 –љ–Є–ґ–µ 20 –Љ–Љ —А—В.—Б—В. —Б–Њ–Њ—В–≤–µ—В—Б—В–≤—Г–µ—В –Ї—А–Є—В–Є—З–µ—Б–Ї–Њ–Љ—Г —Б–љ–Є–ґ–µ–љ–Є—О –ї–Њ–Ї–∞–ї—М–љ–Њ–є –Љ–Є–Ї—А–Њ—Ж–Є—А–Ї—Г–ї—П—Ж–Є–Є –Є –≤—Л—Б–Њ–Ї–Њ–є –≤–µ—А–Њ—П—В–љ–Њ—Б—В–Є –∞–Љ–њ—Г—В–∞—Ж–Є–Є –≤—Л—И–µ –ї–Њ–і—Л–ґ–Ї–Є [12]. –†–µ–Ј—Г–ї—М—В–∞—В –ї–µ—З–µ–љ–Є—П –љ–µ–є—А–Њ–њ–∞—В–Є—З–µ—Б–Ї–Є—Е —П–Ј–≤ —Д–∞–Ї—В–Є—З–µ—Б–Ї–Є –Њ–њ—А–µ–і–µ–ї—П–µ—В—Б—П —В–Њ–ї—М–Ї–Њ —В—П–ґ–µ—Б—В—М—О –Є–љ—Д–µ–Ї—Ж–Є–Є (–Ю–†>40), –њ–Њ–Ї–∞–Ј–∞—В–µ–ї—М —В—А–∞–љ—Б–Ї—Г—В–∞–љ–љ–Њ–є –Њ–Ї—Б–Є–Љ–µ—В—А–Є–Є –њ—А–Є —Н—В–Њ–Љ –љ–µ —Б–љ–Є–ґ–∞–µ—В—Б—П —Б—В–Њ–ї—М –Ј–љ–∞—З–Є—В–µ–ї—М–љ–Њ, —З—В–Њ –Њ–±–µ—Б–њ–µ—З–Є–≤–∞–µ—В –њ–Њ—В–µ–љ—Ж–Є–∞–ї—М–љ—Г—О —Б–њ–Њ—Б–Њ–±–љ–Њ—Б—В—М —П–Ј–≤—Л –Ї –Ј–∞–ґ–Є–≤–ї–µ–љ–Є—О –њ–Њ—Б–ї–µ –ї–Є–Ї–≤–Є–і–∞—Ж–Є–Є –Є–љ—Д–µ–Ї—Ж–Є–Є.–°—В–∞–љ–і–∞—А—В–љ–Њ–µ –Љ—Г–ї—М—В–Є–і–Є—Б—Ж–Є–њ–ї–Є–љ–∞—А–љ–Њ–µ –ї–µ—З–µ–љ–Є–µ —П–Ј–≤–µ–љ–љ—Л—Е –і–µ—Д–µ–Ї—В–Њ–≤ —Б—В–Њ–њ –њ—А–Є —Б–∞—Е–∞—А–љ–Њ–Љ –і–Є–∞–±–µ—В–µ –њ–Њ–Ј–≤–Њ–ї—П–µ—В –і–Њ—Б—В–Є—З—М –≤—Л—Б–Њ–Ї–Є—Е –њ–Њ–Ї–∞–Ј–∞—В–µ–ї–µ–є –Ј–∞–ґ–Є–≤–ї–µ–љ–Є—П –Є —Б–Њ—Е—А–∞–љ–Є—В—М –Њ–њ–Њ—А–Њ—Б–њ–Њ—Б–Њ–±–љ–Њ—Б—В—М –Ї–Њ–љ–µ—З–љ–Њ—Б—В–Є –≤ 90% —Б–ї—Г—З–∞–µ–≤, –і–∞–ґ–µ –≤ —Б–ї—Г—З–∞—П—Е —А–∞–Ј–≤–Є–≤—И–µ–≥–Њ—Б—П —Б–µ–њ—Б–Є—Б–∞ [13]. –Я–Њ –і–∞–љ–љ—Л–Љ –¶–µ–љ—В—А–∞ «–Ф–Є–∞–±–µ—В–Є—З–µ—Б–Ї–∞—П c—В–Њ–њ–∞» –Љ–µ–ґ–і—Г–љ–∞—А–Њ–і–љ–Њ–є –њ—А–Њ–≥—А–∞–Љ–Љ—Л –њ–Њ –і–Є–∞–±–µ—В—Г –љ–∞ –±–∞–Ј–µ –§–µ–і–µ—А–∞–ї—М–љ–Њ–≥–Њ –¶–µ–љ—В—А–∞ —Н–Ї—Б–њ–µ—А—В–Є–Ј—Л –Є —А–µ–∞–±–Є–ї–Є—В–∞—Ж–Є–Є –Є–Є–љ–≤–∞–ї–Є–і–Њ–≤ —А–µ–Ј—Г–ї—М—В–∞—В–Њ–Љ –ї–µ—З–µ–љ–Є—П —П–Ј–≤ —Б—В–Њ–њ —П–≤–Є–ї–Њ—Б—М –њ–µ—А–≤–Є—З–љ–Њ–µ –Ј–∞–ґ–Є–≤–ї–µ–љ–Є–µ —Г 74,7% –±–Њ–ї—М–љ—Л—Е, –њ–Њ—Б–ї–µ —Е–Є—А—Г—А–≥–Є–Є —Б—В–Њ–њ—Л –Є –Љ–∞–ї—Л—Е –∞–Љ–њ—Г—В–∞—Ж–Є–є – —Г 15,5% —З–µ–ї–Њ–≤–µ–Ї, –∞–Љ–њ—Г—В–∞—Ж–Є—П –≤—Л—И–µ –ї–Њ–і—Л–ґ–Ї–Є –њ—А–Њ–≤–µ–і–µ–љ–∞ —Г 9,8% –±–Њ–ї—М–љ—Л—Е [12].
–Ю—Б–Њ–±—Г—О —Д–Њ—А–Љ—Г –љ–µ–Є–љ—Д–µ–Ї—Ж–Є–Њ–љ–љ–Њ–≥–Њ –і–µ—Б—В—А—Г–Ї—В–Є–≤–љ–Њ–≥–Њ –њ–Њ—А–∞–ґ–µ–љ–Є—П –Ї–Њ—Б—В–µ–є –Є —Б—Г—Б—В–∞–≤–Њ–≤ —Б—В–Њ–њ—Л, —Б–≤—П–Ј–∞–љ–љ—Г—О —Б –љ–µ–є—А–Њ–њ–∞—В–Є–µ–є, –њ—А–µ–і—Б—В–∞–≤–ї—П–µ—В —Б—В–Њ–њ–∞ –®–∞—А–Ї–Њ (–°–®) –Є–ї–Є –љ–µ–є—А–Њ–Њ—Б—В–µ–Њ–∞—А—В—А–Њ–њ–∞—В–Є—П. –°—В–Њ–њ–∞ –®–∞—А–Ї–Њ —А–∞–Ј–≤–Є–≤–∞–µ—В—Б—П –≤—Б–ї–µ–і—Б—В–≤–Є–µ –≤–Њ–Ј–і–µ–є—Б—В–≤–Є—П –Љ–µ—Е–∞–љ–Є—З–µ—Б–Ї–Њ–є —В—А–∞–≤–Љ—Л (–њ–Њ–≤—В–Њ—А—П—О—Й–µ–є—Б—П –Є–ї–Є –Љ–∞–ї–Њ–є) –≤ –Ј–Њ–љ–∞—Е —В–Є–њ–Є—З–љ–Њ–≥–Њ –ї–Є–±–Њ –∞—В–Є–њ–Є—З–љ–Њ–≥–Њ –±–Є–Њ–Љ–µ—Е–∞–љ–Є—З–µ—Б–Ї–Њ–≥–Њ –љ–∞–≥—А—Г–ґ–µ–љ–Є—П –Ї–Њ—Б—В–љ—Л—Е —Б—В—А—Г–Ї—В—Г—А —Б—В–Њ–њ—Л, –Є–Ј–Љ–µ–љ–µ–љ–љ—Л—Е –≤—Б–ї–µ–і—Б—В–≤–Є–µ –і–Є–∞–±–µ—В–Є—З–µ—Б–Ї–Њ–є –љ–µ–є—А–Њ–њ–∞—В–Є–Є. –Я–Њ –і–∞–љ–љ—Л–Љ –¶–µ–љ—В—А–∞ «–Ф–Є–∞–±–µ—В–Є—З–µ—Б–Ї–∞—П —Б—В–Њ–њ–∞», —Г 103 –Њ–±—Б–ї–µ–і–Њ–≤–∞–љ–љ—Л—Е –±–Њ–ї—М–љ—Л—Е —Б–Њ —Б—В–Њ–њ–Њ–є –®–∞—А–Ї–Њ –љ–∞–±–ї—О–і–∞–ї–Є—Б—М —П–Ј–≤—Л –≤ –∞–љ–∞–Љ–љ–µ–Ј–µ –≤ 59% —Б–ї—Г—З–∞–µ–≤, –Љ–∞–ї—Л–µ –∞–Љ–њ—Г—В–∞—Ж–Є–Є –њ–Њ—А–∞–ґ–µ–љ–љ–Њ–є —Б—В–Њ–њ—Л –≤ –∞–љ–∞–Љ–љ–µ–Ј–µ – –≤ 19,4% —Б–ї—Г—З–∞–µ–≤, –і–Є–∞–±–µ—В–Є—З–µ—Б–Ї–∞—П –Њ—Б—В–µ–Њ–∞—А—В—А–Њ–њ–∞—В–Є—П —Е–∞—А–∞–Ї—В–µ—А–Є–Ј–Њ–≤–∞–ї–∞—Б—М –і–≤—Г—Б—В–Њ—А–Њ–љ–љ–Є–Љ –њ–Њ—А–∞–ґ–µ–љ–Є–µ–Љ —Г 24% –±–Њ–ї—М–љ—Л—Е –Є –њ—А–Є–≤–µ–ї–∞ –Ї —А–∞–Ј–≤–Є—В–Є—О —П–Ј–≤–µ–љ–љ—Л—Е –і–µ—Д–µ–Ї—В–Њ–≤ —Г 30% –±–Њ–ї—М–љ—Л—Е –Є –њ—А–Њ–≤–µ–і–µ–љ–Є—О –±–Њ–ї—М—И–Є—Е –∞–Љ–њ—Г—В–∞—Ж–Є–є – —Г 3,8% –±–Њ–ї—М–љ—Л—Е. –Т—Б–µ –Њ–±—Б–ї–µ–і–Њ–≤–∞–љ–љ—Л–µ –±–Њ–ї—М–љ—Л–µ –Є–Љ–µ–ї–Є —Б–Њ—Е—А–∞–љ–љ—Л–є –Љ–∞–≥–Є—Б—В—А–∞–ї—М–љ—Л–є –Ї—А–Њ–≤–Њ—В–Њ–Ї –Є –Ј–љ–∞—З–Є—В–µ–ї—М–љ–Њ –≤—Л—А–∞–ґ–µ–љ–љ—Л–µ –њ—А–Є–Ј–љ–∞–Ї–Є —Б–µ–љ—Б–Њ–Љ–Њ—В–Њ—А–љ–Њ–є –Є –∞–≤—В–Њ–љ–Њ–Љ–љ–Њ–є –љ–µ–є—А–Њ–њ–∞—В–Є–Є. –£ 80% –±–Њ–ї—М–љ—Л—Е –Њ–±–љ–∞—А—Г–ґ–µ–љ–∞ –њ—А–Њ–ї–Є—Д–µ—А–∞—В–Є–≤–љ–∞—П —А–µ—В–Є–љ–Њ–њ–∞—В–Є—П, –Ї–Њ—В–Њ—А–∞—П —В–∞–Ї–ґ–µ –Є–Љ–µ–ї–∞ –Ј–љ–∞—З–Є—В–µ–ї—М–љ—Г—О —Б–≤—П–Ј—М —Б –∞–≤—В–Њ–љ–Њ–Љ–љ–Њ–є –љ–µ–є—А–Њ–њ–∞—В–Є–µ–є (–Ї–Њ—Н—Д—Д–Є—Ж–Є–µ–љ—В –Ї–Њ—А—А–µ–ї—П—Ж–Є–Є +0,85). –Я–∞—В–Њ–≥–µ–љ–µ–Ј —Б—В–Њ–њ—Л –®–∞—А–Ї–Њ –Њ—Б—В–∞–µ—В—Б—П –љ–µ–і–Њ—Б—В–∞—В–Њ—З–љ–Њ —П—Б–љ—Л–Љ, –њ–Њ—Б–Ї–Њ–ї—М–Ї—Г –і–∞–ї–µ–Ї–Њ –љ–µ —Г –≤—Б–µ—Е –±–Њ–ї—М–љ—Л—Е —Б –≤—Л—А–∞–ґ–µ–љ–љ—Л–Љ–Є –њ—А–Є–Ј–љ–∞–Ї–∞–Љ–Є –љ–µ–є—А–Њ–њ–∞—В–Є–Є –Є —П–Ј–≤–∞–Љ–Є —Б—В–Њ–њ—Л —А–∞–Ј–≤–Є–≤–∞–µ—В—Б—П –°–®. –Я–Њ––≤–Є–і–Є–Љ–Њ–Љ—Г, –≤–ї–Є—П–љ–Є–µ –Њ–Ї–∞–Ј—Л–≤–∞–µ—В –Ї–Њ–Љ–њ–ї–µ–Ї—Б —Д–∞–Ї—В–Њ—А–Њ–≤, –≤–µ–і—Г—Й–Є–Љ –Є–Ј –Ї–Њ—В–Њ—А—Л—Е –Њ–Ї–∞–Ј—Л–≤–∞–µ—В—Б—П –љ–µ–є—А–Њ–њ–∞—В–Є—П. –Т—Л—Б–Ї–∞–Ј—Л–≤–∞–µ—В—Б—П –Љ–љ–µ–љ–Є–µ –Њ –≤–Њ–Ј–Љ–Њ–ґ–љ–Њ—Б—В–Є –Њ—Б–Њ–±–Њ–≥–Њ —В–Є–њ–∞ –њ–Њ—А–∞–ґ–µ–љ–Є—П –њ–µ—А–Є—Д–µ—А–Є—З–µ—Б–Ї–Є—Е –љ–µ—А–≤–Њ–≤ –њ—А–Є –°–®, –≤–µ–ї–Є–Ї–∞ —А–Њ–ї—М –Њ—А—В–Њ–њ–µ–і–Є—З–µ—Б–Ї–Є—Е –њ—А–µ–і—А–∞—Б–њ–Њ–ї–∞–≥–∞—О—Й–Є—Е —Д–∞–Ї—В–Њ—А–Њ–≤, —А–∞—Б–Ї—А—Л—В–Є—О —А–Њ–ї–Є –Ї–Њ—В–Њ—А—Л—Е —Г–і–µ–ї—П–µ—В—Б—П –љ–µ–і–Њ—Б—В–∞—В–Њ—З–љ–Њ –≤–љ–Є–Љ–∞–љ–Є—П. –Ш—И–µ–Љ–Є—П, –≤–Њ–Ј–Љ–Њ–ґ–љ–Њ, –Є–≥—А–∞–µ—В —А–Њ–ї—М —Б–≤–Њ–µ–±—А–∞–Ј–љ–Њ–≥–Њ —Д–∞–Ї—В–Њ—А–∞ «–Ј–∞—Й–Є—В—Л» –Њ—В —Г—Б–Ї–Њ—А–µ–љ–Є—П –Ї—А–Њ–≤–Њ—В–Њ–Ї–∞ –Є –≤–љ—Г—В—А–Є–Ї–∞–њ–Є–ї–ї—П—А–љ–Њ–є –≥–Є–њ–µ—А—В–µ–љ–Ј–Є–Є, –Ї–Њ—В–Њ—В–Њ—А–∞—П –Љ–Њ–ґ–µ—В –Ј–∞–њ—Г—Б–Ї–∞—В—М –њ—А–Њ—Ж–µ—Б—Б —А–µ–Ј–Њ—А–±—Ж–Є–Є –Ї–Њ—Б—В–Є –Є –≤–Њ–Ј–љ–Є–Ї–љ–Њ–≤–µ–љ–Є—П –Љ–Є–Ї—А–Њ—В—А–∞–±–µ–Ї—Г–ї—П—А–љ—Л—Е –њ–µ—А–µ–ї–Њ–Љ–Њ–≤.
–Т–∞–ґ–љ–µ–є—И–Є–Љ –і–Њ–Ї–∞–Ј–∞—В–µ–ї—М—Б—В–≤–Њ–Љ –љ–∞–ї–Є—З–Є—П –°–® —П–≤–ї—П–µ—В—Б—П —В–Є–њ–Є—З–љ–∞—П –Ї–ї–Є–љ–Є–Ї–Њ–—А–µ–љ—В–≥–µ–љ–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–∞—П —Е–∞—А–∞–Ї—В–µ—А–Є—Б—В–Є–Ї–∞ (–Њ—Б—В–µ–Њ–ї–Є–Ј–Є—Б, —Д—А–∞–≥–Љ–µ–љ—В–∞—Ж–Є—П, –і–Є—Б–ї–Њ–Ї–∞—Ж–Є—П –Ї–Њ—Б—В–µ–є) –њ—А–Є –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Њ–Љ —Б–Є–Љ–њ—В–Њ–Љ–Њ–Ї–Њ–Љ–њ–ї–µ–Ї—Б–µ –≤–Њ—Б–њ–∞–ї–Є—В–µ–ї—М–љ—Л—Е —А–µ–∞–Ї—В–Є–≤–љ—Л—Е –Є–Ј–Љ–µ–љ–µ–љ–Є–є –Њ–Ї—А—Г–ґ–∞—О—Й–Є—Е –Љ—П–≥–Ї–Є—Е —В–Ї–∞–љ–µ–є —Б—В–Њ–њ—Л. –¶–µ–ї–µ—Б–Њ–Њ–±—А–∞–Ј–љ–Њ –≤—Л–і–µ–ї—П—В—М –Ї–ї–Є–љ–Є–Ї–Њ–—А–µ–љ—В–≥–µ–љ–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є–µ —Б—В–∞–і–Є–Є: –Њ—Б—В—А—Г—О, –њ–Њ–і–Њ—Б—В—А—Г—О –Є —Е—А–Њ–љ–Є—З–µ—Б–Ї—Г—О. –Ъ–Њ–ґ–љ–∞—П —В–µ—А–Љ–Њ–Љ–µ—В—А–Є—П –Љ–Њ–ґ–µ—В —Б–ї—Г–ґ–Є—В—М –Љ–µ—В–Њ–і–Њ–Љ –і–Є–∞–≥–љ–Њ—Б—В–Є–Ї–Є –Є –Љ–Њ–љ–Є—В–Њ—А–Є—А–Њ–≤–∞–љ–Є—П –Њ—Б—В—А–Њ—В—Л –њ—А–Њ—Ж–µ—Б—Б–∞. –†–∞–Ј–љ–Є—Ж–∞ –Ї–Њ–ґ–љ–Њ–є —В–µ–Љ–њ–µ—А–∞—В—Г—А—Л –Љ–µ–ґ–і—Г –Ј–і–Њ—А–Њ–≤–Њ–є –Є –њ–Њ—А–∞–ґ–µ–љ–љ–Њ–є –Ї–Њ–љ–µ—З–љ–Њ—Б—В—М—О –±–Њ–ї–µ–µ 2,5°–° —Г–Ї–∞–Ј—Л–≤–∞–µ—В –љ–∞ –Њ—Б—В—А—Г—О —Б—В–∞–і–Є—О, –Љ–µ–љ–µ–µ 1,5°–° – –љ–∞ –њ–µ—А–µ—Е–Њ–і –≤ —Е—А–Њ–љ–Є—З–µ—Б–Ї—Г—О —Б—В–∞–і–Є—О. –Ю—Б–љ–Њ–≤–љ—Л–Љ–Є –Љ–µ—В–Њ–і–∞–Љ–Є –ї–µ—З–µ–љ–Є—П –°–® —П–≤–ї—П—О—В—Б—П —А–∞–љ–љ—П—П –і–Є–∞–≥–љ–Њ—Б—В–Є–Ї–∞, –Є–Љ–Љ–Њ–±–Є–ї–Є–Ј–∞—Ж–Є—П –њ—А–Є –њ–Њ–Љ–Њ—Й–Є –≥–Є–њ—Б–∞ –Є–ї–Є –Њ—А—В–Њ–њ–µ–і–Є—З–µ—Б–Ї–Є—Е –∞–њ–њ–∞—А–∞—В–Њ–≤, –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є–µ –Њ—А—В–Њ–њ–µ–і–Є—З–µ—Б–Ї–Њ–є –Њ–±—Г–≤–Є. –•–Є—А—Г—А–≥–Є—З–µ—Б–Ї–Є–µ —Б–њ–Њ—Б–Њ–±—Л –ї–µ—З–µ–љ–Є—П –Ј–∞–Ї–ї—О—З–∞—О—В—Б—П –≤ —Б—В–∞–±–Є–ї–Є–Ј–∞—Ж–Є–Є —Б—Г—Б—В–∞–≤–Њ–≤ –њ—А–Є –њ–Њ–Љ–Њ—Й–Є –∞—А—В—А–Њ–і–µ–Ј–Њ–≤, –Ї–Њ—В–Њ—А—Л–µ –Њ—Б–ї–Њ–ґ–љ—П—О—В—Б—П –Є–љ—Д–µ–Ї—Ж–Є–µ–є (30% —Б–ї—Г—З–∞–µ–≤) –Є–ї–Є –∞–Љ–њ—Г—В–∞—Ж–Є–µ–є –≤—Л—И–µ –ї–Њ–і—Л–ґ–Ї–Є.
–Ы–µ—З–µ–љ–Є–µ –љ–µ–є—А–Њ–њ–∞—В–Є–Є
–Я–µ—А–≤–Є—З–љ–∞—П –њ—А–Њ—Д–Є–ї–∞–Ї—В–Є–Ї–∞ —А–∞–Ј–≤–Є—В–Є—П –і–Є–∞–±–µ—В–Є—З–µ—Б–Ї–Њ–є —Б—В–Њ–њ—Л –Љ–Њ–ґ–µ—В –±—Л—В—М —А–∞—Б—Б–Љ–Њ—В—А–µ–љ–∞ –њ–Њ–і —Г–≥–ї–Њ–Љ –њ—А–µ–і–Њ—В–≤—А–∞—Й–µ–љ–Є—П –Њ—Б–љ–Њ–≤–љ—Л—Е —Д–∞–Ї—В–Њ—А–Њ–≤ —А–Є—Б–Ї–∞, –њ—А–µ–ґ–і–µ –≤—Б–µ–≥–Њ, –њ–µ—А–Є—Д–µ—А–Є—З–µ—Б–Ї–Њ–є –љ–µ–є—А–Њ–њ–∞—В–Є–Є. –°–Њ–≤—А–µ–Љ–µ–љ–љ—Л–µ –њ–Њ–і—Е–Њ–і—Л –Ї –њ—А–Њ—Д–Є–ї–∞–Ї—В–Є–Ї–µ –Я–Э –≤–Ї–ї—О—З–∞—О—В –і–Њ—Б—В–Є–ґ–µ–љ–Є–µ —Е–Њ—А–Њ—И–µ–≥–Њ –≥–ї–Є–Ї–µ–Љ–Є—З–µ—Б–Ї–Њ–≥–Њ –Ї–Њ–љ—В—А–Њ–ї—П —Б–Њ–≥–ї–∞—Б–љ–Њ —А–µ–Ј—Г–ї—М—В–∞—В–∞–Љ DCCT (Diabetes Control and Complication Trial), –∞ —В–∞–Ї–ґ–µ –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є–µ —А–∞–Ј–ї–Є—З–љ—Л—Е –Љ–µ–і–Є–Ї–∞–Љ–µ–љ—В–Њ–Ј–љ—Л—Е —Б—А–µ–і—Б—В–≤ –њ–∞—В–Њ–≥–µ–љ–µ—В–Є—З–µ—Б–Ї–Њ–≥–Њ –Є —Б–Є–Љ–њ—В–Њ–Љ–∞—В–Є—З–µ—Б–Ї–Њ–≥–Њ –ї–µ—З–µ–љ–Є—П. –†–∞—Б—Б–Љ–∞—В—А–Є–≤–∞—О—В—Б—П —А–∞–Ј–ї–Є—З–љ—Л–µ —В–µ—А–∞–њ–µ–≤—В–Є—З–µ—Б–Ї–Є–µ —Б—В—А–∞—В–µ–≥–Є–Є, –љ–Њ –љ–∞–Є–±–Њ–ї–µ–µ –њ–µ—А—Б–њ–µ–Ї—В–Є–≤–љ—Л–Љ–Є –≥—А—Г–њ–њ–∞–Љ–Є –њ—А–µ–њ–∞—А–∞—В–Њ–≤ —П–≤–ї—П—О—В—Б—П –∞–љ—В–Є–Њ–Ї—Б–Є–і–∞–љ—В—Л, –Є–љ–≥–Є–±–Є—В–Њ—А—Л –∞–ї—М–і–Њ–Ј–Њ—А–µ–і—Г–Ї—В–∞–Ј—Л –Є –≤–∞–Ј–Њ–і–Є–ї–∞—В–∞—В–Њ—А—Л (–Њ—В—З–µ—В –Э–µ–≤—А–Њ–і–Є–∞–±, 2000).
–Ш–љ–≥–Є–±–Є—В–Њ—А—Л –∞–ї—М–і–Њ–Ј–Њ—А–µ–і—Г–Ї—В–∞–Ј—Л –њ—А–µ–і–Њ—В–≤—А–∞—Й–∞—О—В –љ–∞–Ї–Њ–њ–ї–µ–љ–Є–µ —Б–Њ—А–±–Є—В–Њ–ї–∞ –Є —Д—А—Г–Ї—В–Њ–Ј—Л –≤ —В–Ї–∞–љ—П—Е –Є —Б–Њ–Њ—В–≤–µ—В—Б—В–≤–µ–љ–љ–Њ –Љ–µ—В–∞–±–Њ–ї–Є—З–µ—Б–Ї–Є–µ –і–µ–≥–µ–љ–µ—А–∞—В–Є–≤–љ—Л–µ –Є–Ј–Љ–µ–љ–µ–љ–Є—П –љ–µ—А–≤–∞. –†–µ–Ј—Г–ї—М—В–∞—В—Л –і–Њ—Б—В–∞—В–Њ—З–љ–Њ –њ—А–Њ—В–Є–≤–Њ—А–µ—З–Є–≤—Л. –°–µ–є—З–∞—Б –≤ –°–®–Р –Є –Ъ–∞–љ–∞–і–µ –њ—А–Њ–≤–Њ–і–Є—В—Б—П –Љ—Г–ї—М—В–Є—Ж–µ–љ—В—А–Њ–≤–Њ–µ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ —Б –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є–µ–Љ —В—Й–∞—В–µ–ї—М–љ–Њ —Б—В–∞–љ–і–∞—А—В–Є–Ј–Є—А–Њ–≤–∞–љ–љ—Л—Е –Ї—А–Є—В–µ—А–Є–µ–≤ –≤–Ї–ї—О—З–µ–љ–Є—П –Є –Њ—Ж–µ–љ–Ї–Є —А–µ–Ј—Г–ї—М—В–∞—В–Њ–≤. –°—А–µ–і–Є –∞–љ—В–Є–Њ–Ї—Б–Є–і–∞–љ—В–Њ–≤ –њ—А–Є–Њ—А–Є—В–µ—В –Њ—В–і–∞–µ—В—Б—П a-–ї–Є–њ–Њ–µ–≤–Њ–є (—В–Є–Њ–Ї—В–Њ–≤–Њ–є) –Ї–Є—Б–ї–Њ—В–µ. –®–Є—А–Њ–Ї–Њ–µ –њ—А–Є–Љ–µ–љ–µ–љ–Є–µ –Њ–±–Њ—Б–љ–Њ–≤–∞–љ–Њ –±–Њ–ї—М—И–Є–Љ –Ї–Њ–ї–Є—З–µ—Б—В–≤–Њ–Љ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–є, –њ–Њ–і—В–≤–µ—А–ґ–і–∞—О—Й–Є—Е –µ–µ —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В—М –Ї–∞–Ї –њ—А–µ–њ–∞—А–∞—В–∞ —Б –њ–∞—В–Њ–≥–µ–љ–µ—В–Є—З–µ—Б–Ї–Њ–є –љ–∞–њ—А–∞–≤–ї–µ–љ–љ–Њ—Б—В—М—О (—Г–Љ–µ–љ—М—И–µ–љ–Є–µ —Б–µ–љ—Б–Њ–Љ–Њ—В–Њ—А–љ–Њ–≥–Њ –і–µ—Д–Є—Ж–Є—В–∞, —Г–ї—Г—З—И–µ–љ–Є–µ —Н–ї–µ–Ї—В—А–Њ—Д–Є–Ј–Є–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є—Е –њ–Њ–Ї–∞–Ј–∞—В–µ–ї–µ–є –њ—А–Є –њ—А–Є–µ–Љ–µ –≤ –і–Њ–Ј–µ –Њ—В 600 –і–Њ 1800 –Љ–≥ –≤ —Б—Г—В–Ї–Є), —В–∞–Ї –Є —Б–Є–Љ–њ—В–Њ–Љ–∞—В–Є—З–µ—Б–Ї–Њ–≥–Њ –і–µ–є—Б—В–≤–Є—П (–±—Л—Б—В—А—Л–є –Њ–±–µ–Ј–±–Њ–ї–Є–≤–∞—О—Й–Є–є —Н—Д—Д–µ–Ї—В –њ—А–Є –≤–љ—Г—В—А–Є–≤–µ–љ–љ–Њ–Љ –≤–≤–µ–і–µ–љ–Є–Є –≤ –і–Њ–Ј–µ 600 –Љ–≥) –њ—А–Є –≤—Л—Б–Њ–Ї–Њ–є –±–µ–Ј–Њ–њ–∞—Б–љ–Њ—Б—В–Є –њ—А–µ–њ–∞—А–∞—В–∞. –°–µ–є—З–∞—Б –≤ –°–®–Р –Є –†–Њ—Б—Б–Є–Є –≤—Л–њ–Њ–ї–љ—П—О—В—Б—П –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П NATAN –Є Sydney, –Ї–Њ—В–Њ—А—Л–µ –њ–Њ–Ј–≤–Њ–ї—П—В –і–∞—В—М –Њ–Ї–Њ–љ—З–∞—В–µ–ї—М–љ—Г—О –Њ—Ж–µ–љ–Ї—Г —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В–Є a-–ї–Є–њ–Њ–µ–≤–Њ–є –Ї–Є—Б–ї–Њ—В—Л, –≤ —В–Њ–Љ —З–Є—Б–ї–µ –њ—А–Є –і–ї–Є—В–µ–ї—М–љ–Њ–Љ –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є–Є.
–≠—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В—М –њ—А–Є–Љ–µ–љ–µ–љ–Є—П –њ—А–µ–њ–∞—А–∞—В–Њ–≤ —Б–Њ—Б—Г–і–Њ—А–∞—Б—И–Є—А—П—О—Й–µ–≥–Њ –і–µ–є—Б—В–≤–Є—П (–Є–љ–≥–Є–±–Є—В–Њ—А—Л –∞–љ–≥–Є–Њ—В–µ–љ–Ј–Є–љ–њ—А–µ–≤—А–∞—Й–∞—О—Й–µ–≥–Њ —Д–µ—А–Љ–µ–љ—В–∞, –њ—А–Њ—Б—В–∞–≥–ї–∞–љ–і–Є–љ I2) —Б–≤—П–Ј–∞–љ–∞ —Б —Г–ї—Г—З—И–µ–љ–Є–µ–Љ –Љ–Є–Ї—А–Њ—Ж–Є—А–Ї—Г–ї—П—Ж–Є–Є –≤ –љ–µ—А–≤–љ—Л—Е –≤–Њ–ї–Њ–Ї–љ–∞—Е. –Т –ї–Є—В–µ—А–∞—В—Г—А–µ –Є–Љ–µ—О—В—Б—П —А–µ–Ј—Г–ї—М—В–∞—В—Л –Љ–љ–Њ–≥–Њ—З–Є—Б–ї–µ–љ–љ—Л—Е –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є—Е –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–є –њ–Њ –њ—А–Є–Љ–µ–љ–µ–љ–Є—О –њ—А–µ–њ–∞—А–∞—В–Њ–≤ —А–∞–Ј–ї–Є—З–љ—Л—Е –≥—А—Г–њ–њ: –Љ–Є–Њ–Є–љ–Њ–Ј–Є—В–Њ–ї–∞ (–≤ —Б—Г—В–Њ—З–љ–Њ–Љ –Ї–Њ–ї–Є—З–µ—Б—В–≤–µ 1600–3200 –Љ–≥, –≤ –≤–Є–і–µ –њ–Є–≤–љ—Л—Е –і—А–Њ–ґ–ґ–µ–є), g-–ї–Є–љ–Њ–ї–µ–љ–Њ–≤–Њ–є –Ї–Є—Б–ї–Њ—В—Л, —Г–≤–µ–ї–Є—З–Є–≤–∞—О—Й–µ–є —Б–Є–љ—В–µ–Ј –Љ–µ–Љ–±—А–∞–љ–љ—Л—Е —Д–Њ—Б—Д–Њ–ї–Є–њ–Є–і–Њ–≤, –∞–Љ–Є–љ–Њ–≥—Г–∞–љ–Є–і–Є–љ–∞, –Є–љ–≥–Є–±–Є—А—Г—О—Й–µ–≥–Њ –і–µ–є—Б—В–≤–Є–µ AGEs –љ–∞ –≥–ї–Є–Ї–Є—А–Њ–≤–∞–љ–Є–µ –њ—А–Њ—В–µ–Є–љ–Њ–≤. –Т –Ї–∞—З–µ—Б—В–≤–µ —Б–Є–Љ–њ—В–Њ–Љ–∞—В–Є—З–µ—Б–Ї–Є—Е —Б—А–µ–і—Б—В–≤ –ї–µ—З–µ–љ–Є—П –±–Њ–ї–Є –њ–Њ––њ—А–µ–ґ–љ–µ–Љ—Г –њ—А–Є–Љ–µ–љ—П—О—В—Б—П —В—А–Є—Ж–Є–Ї–ї–Є—З–µ—Б–Ї–Є–µ –∞–љ—В–Є–і–µ–њ—А–µ—Б—Б–∞–љ—В—Л (–∞–Љ–Є—В—А–Є–њ—В–Є–ї–Є–љ, –Є–Љ–Є–њ—А–∞–Љ–Є–љ), –∞–љ—В–Є–Ї–Њ–љ–≤—Г–ї—М—Б–∞–љ—В—Л (–Ї–∞—А–±–∞–Љ–∞–Ј–µ–њ–Є–љ, –≥–∞–±–∞–њ–µ–љ—В–Є–љ), –∞–љ—В–Є–∞—А–Є—В–Љ–Є–Ї–Є (–ї–Є–і–Њ–Ї–∞–Є–љ, –Љ–µ–Ї—Б–Є–ї–µ—В–Є–љ), –Ї–∞–њ—Б–∞–Є—Ж–Є–љ (–њ—А–Њ–Є–Ј–≤–Њ–і—П—Й–Є–є—Б—П –Є–Ј –Ї—А–∞—Б–љ–Њ–≥–Њ –њ–µ—А—Ж–∞) –њ—А–Є 4––Ї—А–∞—В–љ–Њ–Љ –љ–∞–љ–µ—Б–µ–љ–Є–Є –љ–∞ –Ї–Њ–ґ—Г –≤ —Б—Г—В–Ї–Є. –°–ї–µ–і—Г–µ—В –Њ—В–Љ–µ—В–Є—В—М, —З—В–Њ –і–Њ –љ–∞—Б—В–Њ—П—Й–µ–≥–Њ –≤—А–µ–Љ–µ–љ–Є –љ–µ –љ–∞–є–і–µ–љ–Њ —Г–љ–Є—Д–Є—Ж–Є—А–Њ–≤–∞–љ–љ–Њ–≥–Њ —Б—А–µ–і—Б—В–≤–∞ –ї–µ—З–µ–љ–Є—П –њ–µ—А–Є—Д–µ—А–Є—З–µ—Б–Ї–Њ–є –љ–µ–є—А–Њ–њ–∞—В–Є–Є, –Є —Б–∞–Љ—Л–Љ –≤–∞–ґ–љ—Л–Љ –Њ—Б—В–∞–µ—В—Б—П –і–Њ—Б—В–Є–ґ–µ–љ–Є–µ —Б—В–Њ–є–Ї–Њ–є –љ–Њ—А–Љ–∞–ї–Є–Ј–∞—Ж–Є–Є –≥–ї–Є–Ї–µ–Љ–Є–Є, –њ—А–µ–і—Г–њ—А–µ–ґ–і–∞—О—Й–µ–є –њ–µ—А–≤–Є—З–љ—Г—О –њ—А–Є—З–Є–љ—Г –њ–Њ—А–∞–ґ–µ–љ–Є—П –љ–µ—А–≤–Њ–≤.
–Я—А–Њ—Д–Є–ї–∞–Ї—В–Є—З–µ—Б–Ї–Є–є —Г—Е–Њ–і –Ј–∞ —Б—В–Њ–њ–Њ–є
–С–Њ–ї—М—И–Њ–µ –Ї–Њ–ї–Є—З–µ—Б—В–≤–Њ –њ–Њ—А–∞–ґ–µ–љ–Є–є —Б—В–Њ–њ —Г –±–Њ–ї—М–љ—Л—Е –і–Є–∞–±–µ—В–Њ–Љ –Љ–Њ–ґ–љ–Њ –њ—А–µ–і–Њ—В–≤—А–∞—В–Є—В—М –њ—Г—В–µ–Љ —А–µ–≥—Г–ї—П—А–љ–Њ–≥–Њ –Њ—Б–Љ–Њ—В—А–∞ –Є —Г—Е–Њ–і–∞ –Ј–∞ —Б—В–Њ–њ–Њ–є. –Ф–ї—П –і–Њ—Б—В–Є–ґ–µ–љ–Є—П —Н—В–Њ–є —Ж–µ–ї–Є –љ–µ–Њ–±—Е–Њ–і–Є–Љ–Њ —Б–ї–µ–і–Њ–≤–∞—В—М —А—П–і—Г —Б—В—А–∞—В–µ–≥–Є–є: –Є–і–µ–љ—В–Є—Д–Є—Ж–Є—А–Њ–≤–∞—В—М –±–Њ–ї—М–љ—Л—Е –≥—А—Г–њ–њ—Л –≤—Л—Б–Њ–Ї–Њ–≥–Њ —А–Є—Б–Ї–∞, –Њ–±—Г—З–∞—В—М –±–Њ–ї—М–љ—Л—Е –Њ—Б–Љ–Њ—В—А—Г —Б—В–Њ–њ—Л –Є –Њ–±—Г–≤–Є, –Њ–±—Г—З–∞—В—М –≤—А–∞—З–µ–є –Є —А–Њ–і—Б—В–≤–µ–љ–љ–Є–Ї–Њ–≤ –±–Њ–ї—М–љ—Л—Е, –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞—В—М —Б–Њ–Њ—В–≤–µ—В—Б—В–≤—Г—О—Й—Г—О –Њ–±—Г–≤—М, –ї–µ—З–Є—В—М –њ–∞—В–Њ–ї–Њ–≥–Є—О —Б—В–Њ–њ—Л, –њ—А–µ–і—И–µ—Б—В–≤—Г—О—Й—Г—О —А–∞–Ј–≤–Є—В–Є—О —П–Ј–≤—Л. –†–µ–≥—Г–ї—П—А–љ–Њ–µ –њ–Њ—Б–µ—Й–µ–љ–Є–µ –±–Њ–ї—М–љ—Л–Љ–Є –њ–Њ–і–Є–∞—В—А–Є—З–µ—Б–Ї–Є—Е –Ї–∞–±–Є–љ–µ—В–Њ–≤, –∞ —В–∞–Ї–ґ–µ –њ–Њ–і–Є–∞—В—А–Є—З–µ—Б–Ї–Є–є —Г—Е–Њ–і –љ–∞ –і–Њ–Љ—Г —И–Є—А–Њ–Ї–Њ —А–∞–Ј–≤–Є—В –≤ —Б—В—А–∞–љ–∞—Е –Х–≤—А–Њ–њ—Л –Є –°–®–Р. –Т –†–Њ—Б—Б–Є–Є —Б–њ–µ—Ж–Є–∞–ї—М–љ–Њ—Б—В—М –њ–Њ–і–Є–∞—В—А–∞ —В–Њ–ї—М–Ї–Њ –Ј–∞—А–Њ–ґ–і–∞–µ—В—Б—П –љ–∞ –Њ—Б–љ–Њ–≤–µ –і–Є–∞–±–µ—В–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Њ–є —Б–ї—Г–ґ–±—Л. –С–Њ–ї—М–љ—Л–Љ —В—А–µ–±—Г–µ—В—Б—П —Б–Њ–Њ—В–≤–µ—В—Б—В–≤—Г—О—Й–µ–µ –ї–µ—З–µ–љ–Є–µ –Љ–Њ–Ј–Њ–ї–µ–є, –Ї–Њ–ґ–љ—Л—Е —В—А–µ—Й–Є–љ, —Б—Г—Е–Њ–є –Ї–Њ–ґ–Є, –њ–∞—В–Њ–ї–Њ–≥–Є–Є –љ–Њ–≥—В–µ–є, –Ї–Њ—В–Њ—А–Њ–µ –і–Њ–ї–ґ–µ–љ –Њ—Б—Г—Й–µ—Б—В–≤–ї—П—В—М —Б–њ–µ—Ж–Є–∞–ї–Є—Б—В –њ–Њ —Г—Е–Њ–і—Г –Ј–∞ —Б—В–Њ–њ–Њ–є, –Є–Љ–µ—О—Й–Є–є –Њ–њ—А–µ–і–µ–ї–µ–љ–љ—Л–µ –љ–∞–≤—Л–Ї–Є —А–∞–±–Њ—В—Л.
–Ь—Г–ї—М—В–Є–і–Є—Б—Ж–Є–њ–ї–Є–љ–∞—А–љ–Њ–µ –≤–µ–і–µ–љ–Є–µ –і–Є–∞–±–µ—В–Є—З–µ—Б–Ї–Є—Е –њ–Њ—А–∞–ґ–µ–љ–Є–є —Б—В–Њ–њ
–Ф–Є–∞–±–µ—В–Є—З–µ—Б–Ї–Є–µ —П–Ј–≤—Л —Б—В–Њ–њ —П–≤–ї—П—О—В—Б—П —А–µ–Ј—Г–ї—М—В–∞—В–Њ–Љ –≤–Њ–Ј–і–µ–є—Б—В–≤–Є—П –Ї–Њ–Љ–њ–ї–µ–Ї—Б–∞ —Д–∞–Ї—В–Њ—А–Њ–≤, –њ–Њ—Н—В–Њ–Љ—Г –Є—Е –ї–µ—З–µ–љ–Є–µ –і–Њ–ї–ґ–љ–Њ –±—Л—В—М –Љ–љ–Њ–≥–Њ—Д–∞–Ї—В–Њ—А–љ—Л–Љ –і–ї—П –і–Њ—Б—В–Є–ґ–µ–љ–Є—П –Њ–њ—В–Є–Љ–∞–ї—М–љ–Њ–≥–Њ —А–µ–Ј—Г–ї—М—В–∞—В–∞. –Ь—Г–ї—М—В–Є–і–Є—Б—Ж–Є–њ–ї–Є–љ–∞—А–љ—Л–є (–Ь–Ф) –Ї–Њ–Љ–∞–љ–і–љ—Л–є –њ—А–Є–љ—Ж–Є–њ –Њ—А–≥–∞–љ–Є–Ј–∞—Ж–Є–Є –њ–Њ–Љ–Њ—Й–Є –±–Њ–ї—М–љ—Л–Љ —Б –і–Є–∞–±–µ—В–Є—З–µ—Б–Ї–Є–Љ–Є —П–Ј–≤–∞–Љ–Є —Б—В–Њ–њ —Г–ґ–µ —Б—В–∞–ї —Б—В–∞–љ–і–∞—А—В–љ—Л–Љ –≤ –њ—А–∞–Ї—В–Є–Ї–µ –Љ–љ–Њ–≥–Є—Е —А–∞–Ј–≤–Є—В—Л—Е –Є —А–∞–Ј–≤–Є–≤–∞—О—Й–Є—Е—Б—П —Б—В—А–∞–љ –≤ —В–µ—З–µ–љ–Є–µ –њ–Њ—Б–ї–µ–і–љ–µ–≥–Њ –і–µ—Б—П—В–Є–ї–µ—В–Є—П. –Э–µ–Њ–±—Е–Њ–і–Є–Љ–Њ—Б—В—М –Є —Г—Б–њ–µ—И–љ–Њ—Б—В—М —В–∞–Ї–Њ–≥–Њ –њ–Њ–і—Е–Њ–і–∞ –Њ–±–Њ—Б–љ–Њ–≤–∞–љ–∞ –≤ –Љ–љ–Њ–≥–Њ—З–Є—Б–ї–µ–љ–љ—Л—Е –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П—Е [14,15].
–Ь–µ–ґ–і–Є—Б—Ж–Є–њ–ї–Є–љ–∞—А–љ–∞—П –њ–Њ–Љ–Њ—Й—М –Ј–∞–Ї–ї—О—З–∞–µ—В—Б—П —Д–∞–Ї—В–Є—З–µ—Б–Ї–Є –≤ –Ї–Њ–Њ—А–і–Є–љ–Є—А–Њ–≤–∞–љ–љ–Њ–є —А–∞–±–Њ—В–µ –і–Є–∞–±–µ—В–Њ–ї–Њ–≥–∞ –Є —Е–Є—А—Г—А–≥–∞––Њ—А—В–Њ–њ–µ–і–∞, –і–Є–∞–±–µ—В–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Њ–є —Б–µ—Б—В—А—Л, –њ–Њ–і–Є–∞—В—А–∞ –Є –Њ—А—В–µ–Ј–Є—Б—В–∞ –≤ —В–µ—Б–љ–Њ–є –Ї–Њ–Њ–њ–µ—А–∞—Ж–Є–Є —Б —Б–Њ—Б—Г–і–Є—Б—В—Л–Љ —Е–Є—А—Г—А–≥–Њ–Љ. –°–њ–µ—Ж–Є–∞–ї–Є—Б—В–Њ–Љ, –Ј–∞–љ–Є–Љ–∞—О—Й–Є–Љ—Б—П –Њ–±—Г—З–µ–љ–Є–µ–Љ –±–Њ–ї—М–љ—Л—Е, –Љ–Њ–ґ–µ—В –±—Л—В—М –і–Є–∞–±–µ—В–Њ–ї–Њ–≥, –њ–Њ–і–Є–∞—В—А –Є–ї–Є –Љ–µ–і–Є—Ж–Є–љ—Б–Ї–∞—П —Б–µ—Б—В—А–∞ (Concensus). –Э–µ–Њ–±—Е–Њ–і–Є–Љ—Л–Љ –Љ–Њ–Љ–µ–љ—В–Њ–Љ –њ—А–Є —Н—В–Њ–Љ —П–≤–ї—П–µ—В—Б—П –њ–Њ—Б—В–Њ—П–љ–љ–Њ–µ –Њ–±–µ—Б–њ–µ—З–µ–љ–Є–µ –±–Њ–ї—М–љ—Л—Е –Њ—А—В–Њ–њ–µ–і–Є—З–µ—Б–Ї–Њ–є –Ј–∞—Й–Є—В–љ–Њ–є –Є –ї–µ—З–µ–±–љ–Њ–є –Њ–±—Г–≤—М—О, –∞ —В–∞–Ї–ґ–µ –љ–∞–±–ї—О–і–µ–љ–Є–µ –Ј–∞ –≥—А—Г–њ–њ–Њ–є –±–Њ–ї—М–љ—Л—Е –њ–Њ—Б–ї–µ –Ј–∞–ґ–Є–≤–ї–µ–љ–Є—П –Є–ї–Є –∞–Љ–њ—Г—В–∞—Ж–Є–Є —Б —З–∞—Б—В–Њ—В–Њ–є –љ–µ —А–µ–ґ–µ 2 —А–∞–Ј –≤ –≥–Њ–і. –Т–∞–ґ–љ–Њ—Б—В—М –і–ї–Є—В–µ–ї—М–љ–Њ–≥–Њ –љ–∞–±–ї—О–і–µ–љ–Є—П –Њ–±–Њ—Б–љ–Њ–≤–∞–љ–∞ —Д–∞–Ї—В–Њ–Љ —А–∞–Ј–≤–Є—В–Є—П —А–µ—Ж–Є–і–Є–≤–Њ–≤ —П–Ј–≤ —Г 50% –±–Њ–ї—М–љ—Л—Е –≤ —В–µ—З–µ–љ–Є–µ 2 –ї–µ—В [16].
–Ф–ї—П –≤–љ–µ–і—А–µ–љ–Є—П —В–∞–Ї–Њ–є –Љ–µ–ґ–і–Є—Б—Ж–Є–њ–ї–Є–љ–∞—А–љ–Њ–є –њ—А–Њ–≥—А–∞–Љ–Љ—Л –љ–µ–Њ–±—Е–Њ–і–Є–Љ–Њ 3 —Г—А–Њ–≤–љ—П: –њ–µ—А–≤–Є—З–љ—Л–є – –≤—А–∞—З–Є –Њ–±—Й–µ–є –њ—А–∞–Ї—В–Є–Ї–Є, –Љ–µ–і–Є—Ж–Є–љ—Б–Ї–Є–µ —Б–µ—Б—В—А—Л, –њ–Њ–і–Є–∞—В—А—Л; –≤—В–Њ—А–Є—З–љ—Л–є – –і–Є–∞–±–µ—В–Њ–ї–Њ–≥–Є, —Е–Є—А—Г—А–≥–Є; —В—А–µ—В–Є—З–љ—Л–є – —Б–њ–µ—Ж–Є–∞–ї–Є–Ј–Є—А–Њ–≤–∞–љ–љ—Л–є —Ж–µ–љ—В—А –њ–Њ —Г—Е–Њ–і—Г –Ј–∞ —Б—В–Њ–њ–Њ–є.
–°—Г—Й–µ—Б—В–≤—Г–µ—В —З–µ—В–Ї–∞—П –≤–Ј–∞–Є–Љ–Њ—Б–≤—П–Ј—М –Љ–µ–ґ–і—Г –≤–љ–µ–і—А–µ–љ–Є–µ–Љ –Љ—Г–ї—М—В–Є–і–Є—Б—Ж–Є–њ–ї–Є–љ–∞—А–љ–Њ–є –Ї–Њ–Љ–∞–љ–і—Л –њ–Њ —Г—Е–Њ–і—Г –Ј–∞ —Б—В–Њ–њ–Њ–є –Є —Б–љ–Є–ґ–µ–љ–Є–µ–Љ —З–Є—Б–ї–∞ –∞–Љ–њ—Г—В–∞—Ж–Є–є. –Я—А–Є —Н—В–Њ–Љ –≤ –Њ–±—П–Ј–∞–љ–љ–Њ—Б—В—М —Б–њ–µ—Ж–Є–∞–ї–Є—Б—В–Њ–≤ –Є–Ј –Ї–Њ–Љ–∞–љ–і—Л –њ–Њ —Г—Е–Њ–і—Г –Ј–∞ —Б—В–Њ–њ–Њ–є –≤—Е–Њ–і–Є—В –Њ–Ї–∞–Ј–∞–љ–Є–µ –њ–µ—А–≤–Є—З–љ–Њ–є –њ–Њ–Љ–Њ—Й–Є –Є –Њ–±–µ—Б–њ–µ—З–µ–љ–Є–µ –њ–Њ–≤—Л—И–µ–љ–Є—П –Ј–љ–∞–љ–Є–є –≤—А–∞—З–µ–є –Њ–±—Й–µ–≥–Њ –њ—А–Њ—Д–Є–ї—П (Concensus).
–Э–µ–Њ–±—Е–Њ–і–Є–Љ–Њ—Б—В—М –Є–љ—В–µ–≥—А–∞—Ж–Є–Є —Б–њ–µ—Ж–Є–∞–ї–Є–Ј–Є—А–Њ–≤–∞–љ–љ–Њ–є –і–Є–∞–±–µ—В–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Њ–є –Ї–Њ–Љ–∞–љ–і—Л (–≤–Ї–ї—О—З–∞—О—Й–µ–є, –Ї–∞–Ї –Љ–Є–љ–Є–Љ—Г–Љ, –і–Є–∞–±–µ—В–Њ–ї–Њ–≥–∞, –Љ–µ–і—Б–µ—Б—В—А—Г, –і–Є–µ—В–Њ–ї–Њ–≥–∞ –Є —Е–Є—А–Њ–њ–Њ–і–Є—Б—В–∞) –Є –њ–µ—А–≤–Є—З–љ–Њ–≥–Њ –Ј–≤–µ–љ–∞ –Љ–µ–і–Є—Ж–Є–љ—Б–Ї–Њ–є –њ–Њ–Љ–Њ—Й–Є –Њ–±–Њ—Б–љ–Њ–≤–∞–љ–∞ –≤ —А–∞–±–Њ—В–µ –і–∞—В—Б–Ї–Є—Е —Б–њ–µ—Ж–Є–∞–ї–Є—Б—В–Њ–≤ [17]. –° —Н—В–Њ–є —Ж–µ–ї—М—О —А–µ–Ї–Њ–Љ–µ–љ–і—Г–µ—В—Б—П –Њ—А–≥–∞–љ–Є–Ј–∞—Ж–Є—П –Ї–Њ–Њ—А–і–Є–љ–∞—Ж–Є–Њ–љ–љ—Л—Е –Ї–Њ–Љ–Є—В–µ—В–Њ–≤ –њ–Њ –Ї–Њ–Њ–њ–µ—А–∞—Ж–Є–Є, –≤—Л–і–µ–ї–µ–љ–Є–µ –Њ—В–≤–µ—В—Б—В–≤–µ–љ–љ—Л—Е –і–Њ–ї–ґ–љ–Њ—Б—В–µ–є —Б—А–µ–і–Є —Б–њ–µ—Ж–Є–∞–ї–Є—Б—В–Њ–≤ –њ–µ—А–≤–Є—З–љ–Њ–≥–Њ –Ј–≤–µ–љ–∞, –њ—А–Њ–≤–µ–і–µ–љ–Є–µ —А–∞–±–Њ—З–Є—Е —Б–µ–Љ–Є–љ–∞—А–Њ–≤, –≤—Л–њ—Г—Б–Ї –Љ–µ—В–Њ–і–Є—З–µ—Б–Ї–Њ–є –ї–Є—В–µ—А–∞—В—Г—А—Л –Є –і—А—Г–≥–Є–µ —Д–Њ—А–Љ—Л, —Б–њ–Њ—Б–Њ–±—Б—В–≤—Г—О—Й–Є–µ –ї—Г—З—И–µ–Љ—Г –і–Њ—Б—В–Є–ґ–µ–љ–Є—О —А–µ–Ј—Г–ї—М—В–∞—В–∞.
1. Larson J, Apelqvist J, Agardh C–D, Strenstrom A. Decreasing incidence of major amputation in diabetic patients: a consequence of a multi–disciplinary foot care approach? // Diab Med –1995.–v.12.– p.770–776
2. Stiegler H.,Standl E., Frank S., Mendler G. Falure of reducing lower extremity amputations in diabetic patients: results of two subsequent population based surveys 1990 and 1995 in Germany // VASA .–1998.– v.27.–p.10–14.
3. Anonimous. An audit of amputations in rural health district. // Pract Diabet Int.– 1997– v.14.–p.175–178.
4. Hewitt D. Data currently avaliable to the department of Health on diabetes.In: Dawson A., Ferrero M. (eds), Chronic Disease Management Registers. London: HMSO.– 1996.– p.34–38
5. The Foot in Diabetes, 3d Ed. A.J.M.Boulton, H.Connor, P.Cavanagh (eds).J.Wiley& Sons.Inc.– 2000.–p.364.
6. Reiber G.E. The epidemiology of the diabetic foot problems // Diabetic Medicine. – 1996. – v. 13, suppl 1, – s. 6–11.
7. Carrington A.L., Mawdsley S.K., Morley M., Kincey J., Boulton A.J. Psychological status of diabetic people with or without lower limb disability // Diabet Res Clin Pract. – 1996. – v. 32. – p. 19–25.
8. –Ъ–Њ–Љ–µ–ї—П–≥–Є–љ–∞ –Х.–Ѓ. –Р–ї–≥–Њ—А–Є—В–Љ –≤—Л—П–≤–ї–µ–љ–Є—П –њ–∞—Ж–Є–µ–љ—В–Њ–≤ –Є–Ј –≥—А—Г–њ–њ—Л —А–Є—Б–Ї–∞ —А–∞–Ј–≤–Є—В–Є—П —Б–Є–љ–і—А–Њ–Љ–∞ –і–Є–∞–±–µ—В–Є—З–µ—Б–Ї–Њ–є —Б—В–Њ–њ—Л: –Р–≤—В–Њ—А–µ—Д. –і–Є—Б—Б. –Ї–∞–љ–і. –Љ–µ–і. –љ–∞—Г–Ї. – –Ь., 1998. – 22—Б.
9. –Ф–Є–∞–±–µ—В–Є—З–µ—Б–Ї–∞—П –њ–µ—А–Є—Д–µ—А–Є—З–µ—Б–Ї–∞—П —Б–µ–љ—Б–Њ–Љ–Њ—В–Њ—А–љ–∞—П –љ–µ–є—А–Њ–њ–∞—В–Є—П. –Я–∞—В–Њ–≥–µ–љ–µ–Ј, –Ї–ї–Є–љ–Є–Ї–∞ –Є –і–Є–∞–≥–љ–Њ—Б—В–Є–Ї–∞ / –Ь–µ—В–Њ–і–Є—З–µ—Б–Ї–Є–µ —А–µ–Ї–Њ–Љ–µ–љ–і–∞—Ж–Є–Є. –°–Њ—Б—В–∞–≤–Є—В–µ–ї–Є: –Ш.–Т. –У—Г—А—М–µ–≤–∞, –Х.–Ѓ. –Ъ–Њ–Љ–µ–ї—П–≥–Є–љ–∞, –Ш.–Т. –Ъ—Г–Ј–Є–љ–∞. – –Ь., 2000. – 23 —Б.
10. Vinic A.I., Holland M.T., Beau J.M. et al. Diabetic neuropathies // Diabetes Care. – 1992. – v. 15, вДЦ 12. – p. 1926–1975.
11. International Guidelines on the Outpatient Management of Diabetic peripheral neuropathy. The Medicine Group (Education), UK. – 1996 – 16 p.
12. –У—Г—А—М–µ–≤–∞ –Ш.–Т., –Ъ—Г–Ј–Є–љ–∞ –Ш.–Т., –Т–Њ—А–Њ–љ–Є–љ –Р.–Т., –Ь–∞–Љ–Њ–љ—В–Њ–≤–∞ –Х.–Ѓ. –Є –і—А. –Ю—Б–Њ–±–µ–љ–љ–Њ—Б—В–Є –і–Є–∞–≥–љ–Њ—Б—В–Є–Ї–Є –Є –ї–µ—З–µ–љ–Є—П –і–Є–∞–±–µ—В–Є—З–µ—Б–Ї–Є—Е –њ–Њ—А–∞–ґ–µ–љ–Є–є —Б—В–Њ–њ. // –•–Є—А—Г—А–≥–Є—П.– 1999.–вДЦ10.–—Б.39–43.
13. –Ь–µ–ґ–і—Г–љ–∞—А–Њ–і–љ–Њ–µ —Б–Њ–≥–ї–∞—И–µ–љ–Є–µ –њ–Њ –і–Є–∞–±–µ—В–Є—З–µ—Б–Ї–Њ–є —Б—В–Њ–њ–µ. –°–Њ—Б—В–∞–≤–ї–µ–љ –Ь–µ–ґ–і—Г–љ–∞—А–Њ–і–љ–Њ–є —А–∞–±–Њ—З–µ–є –≥—А—Г–њ–њ–Њ–є –њ–Њ –і–Є–∞–±–µ—В–Є—З–µ—Б–Ї–Њ–є —Б—В–Њ–њ–µ. – –Ь.: «–Ш–Ј–і–∞—В–µ–ї—М—Б—В–≤–Њ –С–µ—А–µ–≥«. – 2000. – 96 —Б.
14. Armstrong D.G., Harkless L.B. Outcomes of preventative care in a diabetic foot specialty clinic // J Foot Ankle Surg. – 1998. – v. 37, вДЦ 6. – p. 460–466.
15. Larsson J., Apelqvist J., Agardh C.D., Stenstrom A. Decreasing incidence of major amputation in diabetic patients: a conseguence of multidisciplinary foot care team approach? // Diabetic Medicine. – 1995. – v. 12, вДЦ 9. – p. 770–76.
16. De Heus–van Putten M.A., Schaper N.C., Bakker K. The clinical examination of the diabetic foot in daily practise // Diabetic Medicine. – 1996. – v. 13, suppl 1. – s. 55–57.
17. Deckert T., Feldt–Rasmussen B., Borch–Johnsen K., Jensen T. and Kofoed Evevoldsen A. Albuminuria reflects widespread vascular damage: The Steno Hypothesis // Diabetologia. – 1989. – v. 32. – p. 219–26.












