Тиреотоксикоз – клинический синдром, обусловленный стойким избытком тиреоидных гормонов в организме. Выделяют три патогенетических варианта этого синдрома:
1. Гиперпродукция тиреоидных гормонов (гипертиреоз) – щитовидная железа в избытке продуцирует тиреоидные гормоны. Это наиболее частый и имеющий наибольшее клиническое значение вариант тиреотоксикоза; он развивается при болезни Грейвса (диффузном токсическом зобе), многоузловом токсическом зобе и ряде других заболеваний.
2. Деструктивный (тиреолитический) тиреотоксикоз развивается в результате разрушения фолликулов щитовидной железы и попадания в кровяное русло избытка тиреоидных гормонов, содержащихся в коллоиде и тироцитах. Такой патогенетический вариант тиреотоксикоза развивается при подостром (тиреоидит ДеКервена), послеродовом, безболевом («молчащем») и цитокининдуцированном тиреоидитах.
3. Медикаментозный тиреотоксикоз развивается при передозировке препаратами тиреоидных гормонов.
В этой статье хотелось бы подробнее остановиться на вопросах диагностики и лечения двух заболеваний, протекающих с синдромом стойкого тиреотоксикоза и доминирующих в его этиологической структуре: на болезни Грейвса (диффузном токсическом зобе) и многоузловом токсическом зобе.
Болезнь Грейвса представляет собой органоспецифическое аутоиммунное заболевание, характеризующееся стойким патологическим повышением продукции тиреоидных гормонов, как правило, диффузно увеличенной щитовидной железой, которое в 50–75% случаев сочетается с эндокринной офтальмопатией. В основе патогенеза болезни Грейвса лежит выработка стимулирующих антител к рецептору тиреотропного гормона (ТТГ), которые обусловливают стойкую гиперстимуляцию тиреоцитов. Болезнь Грейвса является одним из наиболее часто встречающихся аутоиммунных заболеваний – распространенность достигает 0,1% населения. Болеют им преимущественно женщины молодого возраста, пик заболеваемости приходится на возраст между 25 и 40 годами. В регионах с адекватным йодным обеспечением (например, в США, Великобритании, Канаде, странах Скандинавии) болезнь Грейвса является наиболее частой причиной тиреотоксикоза (заболеваемость многоузловым токсическим зобом здесь сравнительно низка).
Многоузловой и узловой токсический зоб в большинстве случаев является йододефицитным заболеванием, при котором стойкая патологическая гиперпродукция тиреоидных гормонов обусловлена формированием в щитовидной железе автономно функционирующих тироцитов. Если при нормальном йодном обеспечении это заболевание встречается достаточно редко, то в йододефицитных регионах, к которым относится вся территория Российской Федерации, а также большая часть континентальной Европы, многоузловой токсический зоб конкурирует с болезнью Грейвса за первое место в этиологической структуре синдрома тиреотоксикоза. Интересно заметить, что если руководства по эндокринологии, выпущенные в США и Великобритании, начинают обсуждение проблемы тиреотоксикоза с болезни Грейвса и лишь в конце этого раздела кратко упоминают о многоузловом токсическом зобе, то руководства, выпущенные, например, в Германии начинают главу по тиреотоксикозу исключительно с обсуждения функциональной автономии щитовидной железы, самым частым клиническим вариантом которой является многоузловой токсический зоб.
Остановимся несколько подробнее на патогенезе функциональной автономии щитовидной железы. Как уже указывалось, это йододефицитное заболевание и по сути – исход длительного, продолжающегося многие десятилетия, морфогенеза йододефицитного зоба (рис. 1). В условиях йодного дефицита щитовидная железа подвержена воздействию комплекса стимулирующих факторов, которые обеспечивают продукцию адекватного количества тиреоидных гормонов в условиях дефицита основного субстрата для их синтеза. В результате у наиболее предрасположенных лиц происходит увеличение щитовидной железы – формируется диффузный эутиреоидный зоб (этап I). В зависимости от выраженности йодного дефицита, он может формироваться у 10–80% всего населения. Отдельные клетки щитовидной железы оказываются более чувствительными к указанным стимулирующим влияниям, благодаря чему получают преимущественный рост. Так формируется узловой и многоузловой эутиреоидный зоб (этап II). На очередном, III этапе описанные компенсаторные процессы начинают приобретать патологическое значение. В отдельных активно делящихся тироцитах начинают запаздывать репаративные процессы, в связи с чем накапливаются мутации, среди которых наибольшее значение приобретают так называемые активирующие, в результате чего дочерние клетки приобретают способность автономно, то есть вне регулирующих эффектов тиреотропного гормона (ТТГ), продуцировать тиреоидные гормоны. Конечным этапом естественного морфогенеза йододефицитного зоба является узловой и многоузловой токсический зоб (этап IV). Этот процесс занимает многие десятилетия, и как следствие – узловой и многоузловой токсический зоб наиболее часто встречается у лиц пожилого возраста. По мнению большинства экспертов, одной из наиболее серьезных проблем легкого и умеренного йодного дефицита является высокая заболеваемость многоузловым и узловым токсическим зобом в старшей возрастной группе. По данным ряда популяционных исследований, заболеваемость тиреотоксикозом в популяции, проживающей в условиях йодного дефицита, в целом больше, и это связано именно с высокой заболеваемостью многоузловым токсическим зобом. Кроме того, как это следует из таблицы 1, на фоне внедрения массовой йодной профилактики заболеваемость тиреотоксикозом в популяции постепенно снижается.

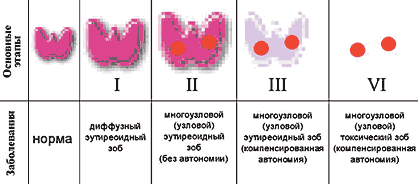
Рис. 1. Этапы естественного течения йододефицитного зоба
Переходя к обсуждению клинической диагностики токсического зоба, заметим, что очень часто причиной неудачного лечения токсического зоба являются как раз ошибки в дифференциальной диагностике болезни Грейвса и многоузлового токсического зоба.Клиническая картина токсического зоба в первую очередь определяется синдромом тиреотоксикоза, который подробно описывается в большинстве руководств и учебников, что избавляет нас от необходимости останавливаться на этом вопросе. Заметим лишь, что клиническая картина тиреотоксикоза имеет закономерную возрастную особенность: у молодых людей, у которых, как правило, речь идет о болезни Грейвса, в большинстве случаев имеет место развернутая классическая клиническая картина тиреотоксикоза, тогда как у пожилых пациентов, у которых в нашем регионе чаще встречается многоузловой токсический зоб, нередко имеет место олиго– и даже моносимптомное течение тиреотоксикоза. Например, единственным его проявлением могут быть суправентрикулярные аритмии, которые долго связываются с ИБС, или необъяснимый субфебрилитет.
На следующем этапе диагностического поиска у пациентов с соответствующими клиническими симптомами тиреотоксикоз должен быть подтвержден или отвергнут при гормональном исследовании. Подчеркнем, что по современным представлениям правильная интерпретация данных гормонального исследования, оценивающего функцию щитовидной железы, без определения уровня ТТГ невозможна. Современные лабораторные методы, в частности, методы 3–го поколения определения уровня ТТГ, позволяют диагностировать два варианта тиреотоксикоза, которые очень часто являются стадиями одного процесса:
1. Субклинический тиреотоксикоз характеризуется снижением уровня ТТГ в сочетании с нормальными уровнями свободного тироксина (fT4) и трийодтиронина (fT3).
2. Манифестный (явный) тиреотоксикоз характеризуется снижением уровня ТТГ и повышением уровня fT4 и/или fT3.
В том случае, если наличие у пациента тиреотоксикоза было подтверждено при гормональном исследовании, на очередном этапе диагностического поиска (этап этиологической диагностики) в большинстве случаев приходится дифференцировать болезнь Грейвса и функциональную автономию щитовидной железы (узловой и многоузловой токсический зоб), отчего принципиальным образом будет зависеть тактика лечения (табл. 2).

Ценным исследованием, которое позволяет дифференцировать болезнь Грейвса и функциональную автономию, является определение уровня антител к щитовидной железе. Высокие титры антител к тиреоидной пероксидазе (ТПО) и тиреоглобулину (ТГ) встречаются примерно в 75% случаев болезни Грейвса, но не являются специфичными для этого заболевания, поскольку могут определяться при любых других аутоиммунных заболеваниях щитовидной железы, а также у здоровых лиц. При функциональной автономии щитовидной железы они в большинстве случаев отсутствуют. Значительно большей специфичностью обладает определение антител к рецептору ТТГ, особенно, если речь идет о втором поколении методов исследования стимулирующих антител.
Лечение токсического зоба является весьма трудоемкой и кропотливой задачей для врача. Как уже указывалось, методы лечения болезни Грейвса и различных клинических вариантов функциональной автономии щитовидной железы отличаются. Главное отличие заключается в том, что в случае функциональной автономии щитовидной железы на фоне тиреостатической терапии невозможно достижение стойкой ремиссии тиреотоксикоза; после отмены тиреостатиков он закономерно развивается вновь. Таким образом, лечение функциональной автономии (многоузловой и узловой токсический зоб, а также диссеминированная форма) подразумевает хирургическое удаление щитовидной железы или ее деструкцию при помощи радиоактивного йода–131. В случае болезни Грейвса у отдельных групп пациентов возможно проведение длительной консервативной терапии, которая при правильном отборе больных в 30–40% случаев приведет к стойкой ремиссии заболевания (табл. 3).

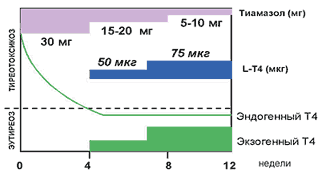
Рис. 2. Лечение болезни Грейвса по схеме "блокируй и замещай"
Как это следует из схемы, представленной на рисунке 2, при тиреотоксикозе средней тяжести сначала обычно назначается около 30 мг тиамазола. На этом фоне (примерно через 4 недели) в большинстве случаев удается достигнуть эутиреоз, о чем будет свидетельствовать нормализация уровня fT4 крови (уровень ТТГ еще долго будет оставаться низким). Начиная с этого момента, доза тиамазола постепенно снижается до поддерживающей (10–15 мг) и к лечению добавляется левотироксин (L–T4) в дозе 50–75 мкг в сутки. Указанную терапию под периодическим контролем уровня ТТГ и fТ4 пациент получает 18–24 месяца, после чего она отменяется. В случае развития рецидива после курса тиреостатической терапии, а также если исходно не удовлетворяются критерии, перечисленные в таблице 3, пациенту показано радикальное лечение: оперативное вмешательство или терапия радиоактивным йодом. В настоящее время все больше специалистов во всем мире склоняются к тому, что целью радикального лечения болезни Грейвса является стойкий гипотиреоз, который достигается почти полным оперативным удалением щитовидной железы (предельно субтотальная резекция) или введением достаточных для этого доз I131, после чего пациенту назначается заместительная терапия левотироксином. Крайне нежелательным следствием более экономных резекций щитовидной железы являются многочисленные случаи послеоперационных рецидивов тиреотоксикоза. В связи с этим важно понимать, что патогенез тиреотоксикоза при болезни Грейвса преимущественно связан не с большим объемом гиперфункционирующей ткани щитовидной железы (она может быть вообще не увеличена), а с циркуляцией стимулирующих щитовидную железу антител, которые продуцируются лимфоцитами. Таким образом, при удалении во время операции по поводу болезни Грейвса не всей щитовидной железы в организме оставляется «мишень» для антител к рецептору ТТГ, которые даже после полного удаления щитовидной железы могут продолжать циркулировать у пациента на протяжении всей жизни. То же самое относится и к лечению болезни Грейвса радиоактивным I131. Наряду с этим современные препараты левотироксина позволяют поддерживать у пациентов с гипотиреозом качество жизни, которое мало отличается от такового у здоровых людей. Это подтверждает не только клиническая практика, но и данные многих исследований, прицельно изучавших этот вопрос. При условии ежедневного приема заместительной дозы левотироксина для пациента практически отсутствуют какие–либо ограничения; что принципиально, женщины могут планировать беременность и рожать, не опасаясь развития рецидива тиреотоксикоза во время беременности или (достаточно часто) после родов. Очевидно, что в прошлом, когда, собственно, и сложились подходы к лечению болезни Грейвса, подразумевающие более экономные резекции щитовидной железы, гипотиреоз закономерно рассматривался, как неблагоприятный исход операции, поскольку терапия экстрактами щитовидной железы животных (тиреоидин) не могла обеспечить должную компенсацию гипотиреоза. Алгоритм лечения болезни Грейвса приведен на рисунке 3. Оперативное лечение и терапия радиоактивным йодом являются конкурирующими методами лечения токсического зоба; у каждого из них есть плюсы и минусы, которые кратко суммированы в таблице 4.
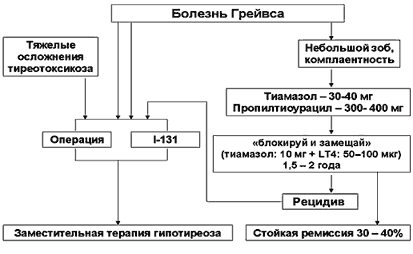
Рис. 3. Алгоритм лечения болезни Грейвса

- Безопасность
- Единственные противопоказания: беременность и грудное вскармливание
- Стоимость – дешевле, чем при хирургическом лечении
- Не требует подготовки тиреостатиками
- Госпитализация всего на несколько дней (в США лечение проводится амбулаторно)
- При необходимости можно повторить
- Нет ограничений для пациентов преклонного возраста и в отношении наличия любой сопутствующей патологии.
В заключение хотелось бы заметить, что активное развитие клинической тиреоидологии, которая за последнее десятилетие обогатилась большим числом исследований, выполненных на методологической базе доказательной медицины, позволило на сегодняшний день сформулировать клинические рекомендации для практических врачей по большинству аспектов проблемы диагностики и лечения токсического зоба. Многие из них остались за рамками нашего обсуждения (тиреотоксикоз у беременных, субклинический тиреотоксикоз, эндокринная офтальмопатия и др.). Это не означает, что все проблемы решены – число публикаций увеличивается с каждым днем.
1. Дедов И.И., Мельниченко Г.А., Фадеев В.В. Эндокринология (учебник для студентов медицинских вузов). – М. Медицина, 2000.
2. Laurberg P., Nohr S.B., Pedersen K.M., et al. Thyroid disorders in mild iodine deficiency. // Thyroid – 2000 – Vol. 10. P. 951 – 963.
3. Leech N.J., Dayan C.M. Controversies in the management of Graves’ disease. // Clin Endocrinol – 1998 – Vol. 49. – P. 273 – 280.
4. Weetman A.P. Graves’ disease. // N Engl J Med – 2000 – Vol. 343. – P. 1236 – 1248.












