В конце 2011 г. был принят «Консенсус совета экспертов Российской ассоциации эндокринологов (РАЭ) по инициации и интенсификации сахароснижающей терапии СД 2–го типа», четко определяющий место ПСМ в терапии СД 2–го типа. Монотерапия ПСМ (за исключением глибенкламида) может быть альтернативой метформину, если уровень HbA1c находится в диапазоне 6,5–7,5%. Комбинированная терапия ПСМ и метформином рекомендована при установлении диагноза СД 2–го типа, если уровень HbA1c находится в диапазоне 7,6–9,0%, а также в случае неэффективности в течение 6 мес. после установления диагноза любой монотерапии, что определяется как снижение уровня HbA1c менее чем на 0,5% или недостижение индивидуальной цели лечения [5].
Сахароснижающее действие ПСМ основано на стимуляции секреции инсулина b–клетками поджелудочной железы за счет взаимодействия с регуляторными субъединицами КАТФ–каналов [6]. Принципиальным отличием ПСМ 3–го поколения глимепирида, вошедшего в клиническую практику в 1995 г., является взаимодействие с низкомолекулярной субъединицей SURx, в то время как ПСМ 2–го поколения взаимодействуют с высокомолекулярной субъединицей SUR1. Более быстрая ассоциация и диссоциация глимепирида с SURx, чем ассоциация и диссоциация ПСМ 2–го поколения с SUR1, приводит к развитию сахароснижающего эффекта при меньшем уровне инсулинемии [7], а это, в свою очередь, снижает вероятность развития как легких, так и тяжелых гипогликемических состояний при длительном лечении [8], а также замедляет истощение запасов инсулина в b–клетках и развитие вторичной резистентности [9,10].
Более высокая эффективность комбинирования метформина с глимепиридом по сравнению с монотерапией метформином или глимепиридом была изучена в исследовании G. Charpentier и соавт. [9]. Анализ Флорентийского регистра продемонстрировал большую выживаемость пациентов с СД 2–го типа, принимавших метформин в комбинации с глимепиридом, чем пациентов, принимавших метформин с другими секретагогами инсулина: глибенкламидом, гликлазидом, репаглинидом [10].
Эффективность и хорошая переносимость комбинированной терапии глимепиридом и метформином (медиана суточной дозы 2 и 1000 мг соответственно) у пациентов с СД 2–го типа была подтверждена в исследовании реальной практики (2010–2011 гг.) в 25 городах Российской Федерации [11]. 279 пациентам с СД 2–го типа, у которых не был достигнут установленный в качестве критерия эффективности целевой уровень HbA1c<7% при монотерапии метформином, по решению лечащих врачей был добавлен глимепирид. Через 6 мес. применения метформина и глимепирида было отмечено статистически значимое снижение среднего уровня HbA1c на 1,1% (p<0,001), более половины пациентов достигли целевого уровня НbА1c<7% (рис. 1).
При этом уровень зарегистрированных гипогликемических состояний между 3 и 6–м мес. наблюдения после прекращения титрации глимепирида был минимальным – ночные гипогликемии были зарегистрированы у 0,4%, симптоматические – у 6,1% больных. Ни одного случая тяжелой гипогликемии, потребовавшей вмешательства медперсонала или третьих лиц, в течение 6 мес. зарегистрировано не было. Имеются данные, что частота гипогликемий при комбинации глимепирида с метформином достоверно ниже, чем глибенкламида с метформином [12].
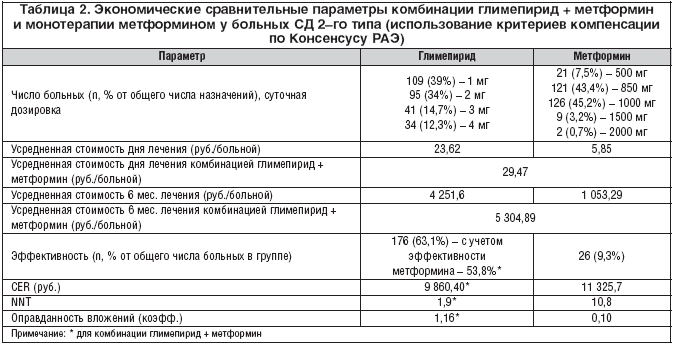
Поскольку критерии для включения в анализ были разработаны до вступления в силу Консенсуса РАЭ, установившего индивидуальные целевые уровни компенсации СД 2–го типа в зависимости от возраста, наличия тяжелых осложнений заболевания, риска гипогликемий, то дополнительный анализ с учетом критерия «пожилой возраст» (лица старше 60 лет) показал, что у 26 (9,3%) человек до добавления глимепирида к терапии был достигнут индивидуальный целевой уровень HbA1c от 7,0 до 7,5%. Через 6 мес. наблюдательной программы в результате комбинированной терапии «глимепирид + метформин» целевой уровень HbA1c был достигнут у 176 (63,1%) человек, таким образом, эффективность комбинации составила 53,8%, что статистически значимо выше, чем при монотерапии метформином (OШ 15,94; 8,65–29,4; p<0,001). Следует отметить, что из числа всех больных, достигших целевого гликемического контроля, 53 (30,1%) человека получали глимепирид в дозе 1 мг/сут., а 89 (49,7%) человек – 2 мг/сут. Таким образом, большинство пациентов получили глимепирид в минимально рекомендуемых терапевтических дозах, которые эффективно контролировали уровень гликемии, что существенно снижает риск гипогликемии.
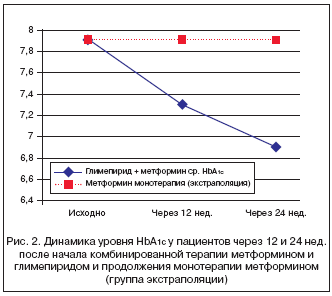
Метаанализ, проведенный Klarenbach и соавт. [20], показал, что с фармакоэкономической точки зрения интенсификация сахароснижающей терапии путем добавления ПСМ к метформину превосходит интенсификацию при помощи любого другого класса ПССП, в т.ч. тиазолидиндионов и ингибиторов ДПП–4. Фармакоэкономическая эффективность добавления ПСМ к терапии метформином была показана относительно продолжения монотерапии метформином [20]. Поскольку исходно наша наблюдательная программа не ставила целью сравнение фармакоэкономической эффективности добавления глимепирида к метформину с какой–либо другой интенсификацией сахароснижающей терапии, то для проведения этой оценки в условиях реальной клинической практики мы применили математическую модель United Kingdom Prospective Diabetes Study Outcomes Model [21]. Мы создали эквивалентную по числу участников и клиническим характеристикам группу пациентов и на основе вышеуказанной модели предположили, что группа продолжит принимать метформин как минимум без дальнейшего ухудшения гликемического контроля, несмотря на хорошо известное прогрессирующее течение СД 2–го типа (рис. 2).
С этой целью был проанализирован фармакоэкономический показатель «стоимость/эффект» в группе, принимавшей комбинацию глимепирида и метформина, в сравнении с группой экстраполяции с применением расчетов по формуле [13]:
CER = прямые затраты/эффект,
где CER – показатель «стоимость/эффект»;
прямые затраты – стоимость применения ПССП за 6 мес.;
эффект – число больных (в % из группы), достигших целей лечения СД 2–го типа по критериям РАЭ.
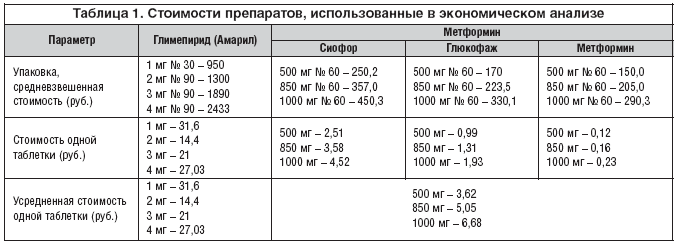
За основу стоимости препаратов взяты средневзвешенные цены по предложению в аптеках г. Москвы на глимепирид в упаковках по 1 мг, 2 мг, 3 мг, 4 мг (Амарил, «Санофи Авентис» Дойчланд ГмбХ, Германия) и метформин в упаковках 500 мг, 850 мг, 1000 мг («Сиофор» Берлин–Хеми / Менарини Фарма ГмбХ, Германия), которые получали 168 (60,2%) пациентов, Глюкофаж («Мерк Сантэ» с.а.с., Франция) – 98 (35,1%) пациентов и метформин отечественных производителей – 13 (4,7%) пациентов соответственно [14] (табл. 1). Усредненная стоимость каждого препарата в этом наблюдении определялась по формуле:
УС = ДС1 х ЧН1 + ДС2 х ЧН2 + … + ДСi х ЧНi,
где УС – усредненная стоимость суточной дозы глимепирида или метформина (руб.);
ДС1,2,i – дневная стоимость глимепирида или метформина в соответствующей дозе (руб.);
ЧН1,2,i – частота назначения глимепирида или метформина в соответствующей дозе среди всех назначений этих препаратов.
Предварительно была высчитана УС 1 таблетки для 500, 850 и 1000 мг метформина, поскольку стоимость упаковок препарата различных производителей была разной. Подсчет для каждой дозировки таблетки производился по формуле:
УСм = СТ1 х ЧН1 + СТ2 х ЧН2 + СТ3 х ЧН3,
где УСм – усредненная стоимость таблетки метформина в соответствующей дозировке;
СТ1 – стоимость таблетки метформина в соответствующей дозировке соответствующего производителя;
ЧН1 – частота применения метформина соответствующего производителя в группе больных.
Данные по использованной в расчетах утилитарной стоимости препаратов приведены в таблице 1.
Поскольку дозы метформина после добавления глимепирида не изменялись, прямые затраты на комбинацию складывались из усредненной стоимости лечения компонентами. Усредненная дневная стоимость умножалась на 180 дней лечения, что соответствовало сроку применения метформина в экстраполяторной группе и сроку наблюдения после назначения комбинации.
Также определялся показатель NNT (Number Needed to Treat) [15] – число больных, которых нужно пролечить в течение 180 дней для достижения 1 компенсации СД 2–го типа по формуле:
NNT = 1/Δ абсолютного риска недостижения компенсации СД 2–го типа.
Параметр эффективности вложений определялся как отношение стоимости лечения у тех, кто достиг компенсации, к таковой у тех, кто компенсации не достиг (на 100 больных).
Были получены следующие результаты, представленные в таблице 2. Усредненная стоимость дня лечения при использовании метформина была в 4 раза ниже, чем стоимость его комбинации с глимепиридом. Вместе с тем, параметр «стоимость/эффект» для монотерапии метформином был на 14,9% выше, чем для комбинации, а параметр NNT – в 5,8 раза. Также существенным образом отличался коэффициент эффективности вложений – в 10 раз. Эти данные подтверждают, что утилитарная стоимость (стоимость упаковки) не может служить основанием для вывода об экономической эффективности препарата. Экономическая целесообразность подключения глимепирида к метформину в данном исследовании выше, чем продолжение монотерапии метформином. Фактически показано, что на каждый вложенный в комбинацию рубль в течение 6 мес. получается экономическая выгода в 16%, в то время как терапия только метформином не дает такого результата.
Эти данные согласуются с опубликованными результатами других исследований, где показана не только клиническая эффективность комбинирования глимепирида и метформина, но и более выраженный сахароснижающий эффект и лучшая переносимость этой комбинации в сравнении, например, с комбинацией «глибенкламид + метформин» [12,16], равно как и подтверждаются результаты фармакоэкономической эффективности данной комбинации, показанные в исследовании Scott Klarenbach в 2011 г. [20].
В настоящее время наряду с оценкой эффективности, безопасности и переносимости большое внимание уделяется качеству жизни больных при осуществлении любого фармакотерапевтического вмешательства. Отечественные данные, полученные еще в начале века, показали статистически значимое повышение качества жизни при применении глимепирида в сочетании с метформином у больных, мотивированных принимать адекватные решения на основе самоконтроля [19]. С учетом клинико–фармакологического профиля глимепирида и основываясь на этих результатах, можно считать, что его длительный прием в целевой группе не вызывает толерантности, феномена «ускользания» результата.
В качестве терапии первой линии при уровне HbA1c 6,5–7,5% рекомендованы метформин/ингибиторы ДПП–4/агонисты ГПП–1, а монотерапия ПСМ, и в частности глимепиридом, рассматривается как альтернативный вариант. Вместе с тем, в настоящее время монотерапию ПСМ получают около 20% пациентов в Российской Федерации, что может быть обусловлено как непереносимостью или наличием противопоказаний к назначению вышеназванных препаратов, так и пока еще высокой стоимостью агонистов ГПП–1 и ингибиторов ДПП–4. Эффективность монотерапии ПСМ, и в частности глимепиридом, была показана во многих рандомизированных клинических исследованиях. Вместе с тем, эти результаты не могут быть в полной мере экстраполированы на рутинную клиническую практику. Это послужило предпосылкой для проведения наблюдательной программы по изучению применения монотерапии глимепиридом (Амарил, «Санофи Авентис» Дойчланд ГмбХ, Германия) у пациентов с СД 2–го типа с противопоказаниями к назначению метформина.
В эту программу длительностью 24 нед., проводившуюся в 49 городах Российской Федерации в 2010–2011 гг., были включены 240 пациентов с СД 2–го типа (148 женщин и 92 мужчины), соответствовавших следующим критериям:
• пациенты с СД 2–го типа в возрасте 18–75 лет, не достигшие удовлетворительного гликемического контроля в результате изменения образа жизни в течение как минимум 12 нед. после установления диагноза СД 2–го типа;
• 7%< HbA1c<8,5% в течение максимум 2 нед. до включения в программу;
• мнение лечащего врача о целесообразности назначения в качестве сахароснижающей терапии глимепирида (противопоказания к назначению метформина);
• желание и возможность исследования уровня HbA1c через 3 и 6 мес.после начала терапии глимепиридом (Амарил);
• подписанное информированное согласие.
Оценка эффективности проводилась по динамике уровня HbA1c через 6 мес. после начала терапии глимепиридом (Амарил) по сравнению с его исходным уровнем. Безопасность лечения оценивалась по количеству документально подтвержденных гипогликемий (бессимптомных, симптоматических, ночных и тяжелых).
При включении в наблюдательную программу средний возраст пациентов составил 57,3±8,6 лет, средняя длительность СД – 1,4±2,4 года. Основными причинами, по которым больным не назначался метформин, были диспепсия при его первичном приеме (59,9%), противопоказания согласно инструкции по применению (31,2%), другие причины (8,9%).
Через 12 нед. после начала терапии глимепиридом отмечено снижение уровня HbA1c с 7,9±0,5% до 7,2±0,6%, а через 24 нед. – до 6,6±0,7% (p<0,001 для обоих значений относительно исходного уровня). Таким образом, в течение первых 3–х мес. терапии среднее снижение HbA1c составило 0,7±0,5% (р<0,01) до 7,2±0,6%, а через 24 нед. – уже 6,6±0,7% (изменение от исходного уровня –1,3±0,7%, p<0,001).
Доля пациентов, достигших целевого уровня HbA1c<7% на фоне монотерапии глимепиридом, через 24 нед. составила 34,2%, а через 24 нед. – 62,9% (OШ по отношению к эффективности через 12 нед. – 4,76; ДИ 2,87–7,91, p<0,001).
Динамика суточных доз глимепирида представлена на рисунке 3. Через 12 нед. наблюдения большая часть больных получала препарат в дозах 1 и 2 мг/сут., а через 24 нед. – 2 и 3 мг/сут. Таким образом, остается возможность для дальнейшей титрации дозы глимепирида и достижения целевого уровня HbA1c у пациентов, не достигших этого значения в течение 24 нед. терапии.
Усредненная доза препарата была подсчитана по формуле:
УД = СД1 х ЧН1 + СД2 х ЧН2 + … + СДi х ЧНi,
где УД – усредненная суточная доза (мг);
СД1,2,i – соответствующая суточная доза (мг);
ЧН1,2,i – частота назначения препарата в соответствующей суточной дозе среди всех назначений этого препарата.
УД для 12 нед. лечения составила 1,97 мг, а к концу периода наблюдения (к 24–й нед.) она возросла на 29,4% и составила 2,55 мг/сут.
Усредненные прямые расходы на препарат подсчитаны по формуле:
УС = ДС1 х ЧН1 + ДС2 х ЧН2 + … + ДСi х ЧНi,
где УС – усредненная стоимость суточной дозы (руб.);
ДС1,2,i – дневная стоимость препарата в соответствующей дозе (руб.);
ЧН1,2,i – частота назначения препарата в соответствующей дозе среди всех назначений этого препарата.
Стоимости упаковок глимепирида (Амарил), так же как и в наблюдательной программе по комбинированному применению, взяты исходя из средневзвешенных цен в аптеках г. Москва (табл. 1). Основываясь на данных различной стоимости препарата в разных упаковках и исходя из процентного соотношения суточных дозировок, был произведен подсчет УС. За 12–недельный срок наблюдения стоимость глимепирида составила 23,75 руб./сут., а через 24 нед. – 28,28 руб./сут. Стоимость 12 нед. лечения глимепиридом составила 23,75 руб. х 84 дня = 1995 руб., стоимость вторых 12 нед. лечения – 28,28 руб. х 84 дня = 2 375,52 руб. Общая усредненная стоимость применения глимепирида – 4 370,52 руб. за 24 нед. Параметр «стоимость/эффект» составил 4 370,52 руб. : 62,9% = 6 948,4 руб.
За весь период наблюдения была зарегистрирована лишь 1 бессимптомная гипогликемия. Симптоматические гипогликемии за первые 12 нед. были зарегистрированы 39 раз у 11 больных, за следующие 12 нед. – 62 раза у 25 больных (р>0,05). Ночные симптоматические гипогликемии за первые 12 нед. были зарегистрированы у 2 больных (по 1 эпизоду), а за вторые 12 нед. – у 4 больных (6 эпизодов). Тяжелых гипогликемий, потребовавших медицинской помощи или вмешательства третьих лиц, за всю наблюдательную программу зарегистрировано не было. Таким образом, эти результаты подтверждают удовлетворительный профиль безопасности глимепирида.
За 24 нед. ни одному больному не потребовалась госпитализация, количество амбулаторных посещений соответствовало плановому графику, экстренная медицинская помощь не оказывалась, в связи с чем стоимость этих мероприятий в прямых затратах не учитывалась. В течение 24 нед. сопутствующая терапия не менялась. Наиболее часто применялись ингибиторы АПФ и блокаторы рецепторов к ангиотензину II (30,8% всех назначений), гиполипидемические средства и диуретики (по 8,0%), а также β–адреноблокаторы (6,8%).
Заключение
• Инициация монотерапии глимепиридом у пациентов с СД 2–го типа при невозможности применения метформина (противопоказания/непереносимость), так же как и добавление глимепирида к монотерапии метформином при неэффективности последнего, в течение 6 мес. лечения привели к улучшению гликемического контроля у пациентов с СД 2–го типа.
• Как монотерапия глимепиридом, так и комбинированная терапия метформином и глимепиридом в условиях рутинной клинической практики продемонстрировали удовлетворительный профиль безопасности и хорошую переносимость.
• Комбинация глимепирида и метформина экономически приемлема и является оправданной для системы государственного (страхового) возмещения.
Ограничения исследования: Фармакоэкономический анализ выполнен на основании применения математической модели United Kingdom Prospective
Diabetes Study Outcomes Model
Данный материал опубликован
при финансовой поддержке компании Санофи.
![Рис. 1. Доля пациентов с уровнем HbA1c<7% через 3 и 6 мес. после начала комбинированной терапии метформином и глимепиридом [11]](/data/articles/Image/t20/n32/1573-1.gif)

Литература
1. Шестакова М.В. Реальная клиническая практика лечения сахарного диабета 2 типа в Российской Федерации по данным открытой проспективной наблюдательной программы «ДИА–КОНТРОЛЬ» // Сахарный диабет. – 2011. – № 4. – С. 75–80.
2. www.idf.org (обращение 11 октября 2012 г.)
3. Management of Hyperglycemia in Type 2 Diabetes: A Patient–Centered Approach Position Statement of the American Diabetes Association (ADA) and the European Association for the Study of Diabetes (EASD) // Diabetes Care. 2012. Vol. 35. P. 1–16.
4. www.aace.com (обращение 11 октября 2012 г.)
5. Дедов И.И., Шестакова М.В., Аметов А.С. и др. Консенсус совета экспертов Российской Ассоциации эндокринологов (РАЭ) по инициации и интенсификации сахароснижающей терапии СД 2 типа // Сахарный диабет. – 2011. – № 4. – С. 6–17.
6. Ashcroft F.M., Gribble, F.M.. ATP–sensitive K+ channels and insulin secretion: their role in health and disease // Diabetol. 1999. Vol.42. P. 903– 919.
7. Muller G. The molecular mechanism of the insulin–mimetic/sensitizing activity of the antidiabetic sulfonylurea drug Amaryl // Mol. Med. 2000. Vol. 6(11). P. 907–933.
8. Holstein A., Plaschke A., Egberts E–H. Lower incidence of severe hypoglycaemia in patients with type 2 diabetes treated with glimepiride versus glibenclamide // Diabet. Metabol. Res. Rew. 2001. Vol. 17. P. 467–473.
9. Charpentier G., Fleury F., Kabir М. et al. Improved glycaemic control by addition of glimepiride tо metformin monotherapy in type 2 diabetic patients // Diabet Med. 2001. Vol.18. P. 828–834.
10. Monami M. et al. Three–year mortality in diabetic patients treated with different combinations of insulin secretagogues and metformin // Diabet. Metab. Res. Rev. 2006. Vol. 22. P. 477–482.
11. Глинкина И.В., Королева А.В., Зилов А.В. Эффективность и безопасность свободной комбинации глимепирида и метформина у пациентов сахарным диабетом 2 типа в условиях реальной клинической практики: наблюдательная программа // Эффективная фармакотерапия. Эндокринология. – 2012. – № 2. – С. 12–16.
12. Gonza’lez–Ortiz M., Guerrero–Romero J.F., Violante–Ortiz R. et al. Efficacy of glimepiride/metformin combination versus glibenclamide/metformin in patients with uncontrolled type 2 diabetes mellitus // J. Diabet. Complications. 2009. Vol. 23(6). P. 376–379.
13. Фармакоэкономика и фармакоэпидемиология – практика приемлемых решений / Под ред. В.Б. Герасимова, А.Л. Хохлова, О.И. Карпова. – М.: Медицина, 2005. – 352 с.
14. http://www.piluli.ru/ по состоянию на 21октября 2012 г.
15. Флетчер Р., Флетчер С., Вагнер Э. Клиническая эпидемиология. Основы доказательной медицины. – М.: Медицина, 1998. – 352с.
16. Колбин А.С. Клинико–экономическая экспертиза фиксированной комбинации глимепирид/метформин // Клин. фармакология и терапия. – 2011. – Т. 20 (4). – С. 93–96.
17. Olsson J., Lindberg G., Gottsater M. et al. Increased mortality in Type II diabetic patients using sulphonylurea and metformin in combination: a population–based observational study // Diabetol. 2000. Vol. 43. P. 558–560.
18. Pantalone K.M., Kattan M.W., Yu C. et al. The risk of overall mortality in patients with Type 2 diabetes receiving different combinations of sulfonylureas and metformin: a retrospective analysis // Diabet. Med. 2012. Vol. 29(8). P. 1029–1035.
19. Демидова И.Ю., Рагозин А.К., Игнатова Н.Г. Качество жизни пациентов с сахарным диабетом типа 2 на фоне комплексной сахароснижающей терапии с использованием глимепирида (Амарила) // Качеств. клин. практика. – 2002. – № 3. – С. 36–42.
20. Klarenbach at al. Cost–effectiveness of second–line antihyperglycemic therapy in patients with type 2 diabetes mellitus inadequately controlled on metformin // CMAJ. 2011. Vol. 183(16). P. e1213–e1220.
21. Clarke P.M. at al. A model to estimate the lifetime health outcomes of patients with type 2 diabetes: the United Kingdom Prospective Diabetes Study (UKPDS) Outcomes Model (UKPDS no. 68) // Diabetol. 2004. Vol. 47(10). P. 1747–59. Epub 2004 Oct 27.












