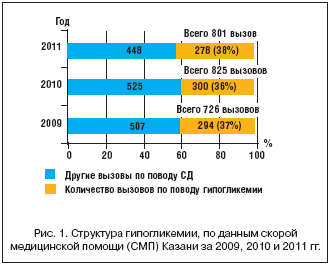
–Т –љ–∞—Б—В–Њ—П—Й–µ–µ –≤—А–µ–Љ—П –≤ –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Њ–є –њ—А–∞–Ї—В–Є–Ї–µ –њ—А–Є –≤–µ–і–µ–љ–Є–Є –±–Њ–ї—М–љ—Л—Е –°–Ф 2 —В–Є–њ–∞ –∞–Ї—В—Г–∞–ї—М–љ—Л–Љ–Є —П–≤–ї—П—О—В—Б—П –і–≤–µ –≥–ї–∞–≤–љ—Л–µ –њ—А–Њ–±–ї–µ–Љ—Л: –њ—А–Є –Њ–≥—А–Њ–Љ–љ–Њ–Љ –≤—Л–±–Њ—А–µ —Б–∞—Е–∞—А–Њ—Б–љ–Є–ґ–∞—О—Й–Є—Е –њ—А–µ–њ–∞—А–∞—В–Њ–≤ –±–Њ–ї—М—И–∞—П —З–∞—Б—В—М –њ–∞—Ж–Є–µ–љ—В–Њ–≤, –Њ—Б–Њ–±–µ–љ–љ–Њ —Б—В–∞—А—И–µ–є –≤–Њ–Ј—А–∞—Б—В–љ–Њ–є –≥—А—Г–њ–њ—Л, –њ—А–Њ–і–Њ–ї–ґ–∞—О—В –ї–µ—З–µ–љ–Є–µ —В—А–∞–і–Є—Ж–Є–Њ–љ–љ—Л–Љ–Є –њ—А–µ–њ–∞—А–∞—В–∞–Љ–Є —Б—Г–ї—М—Д–Њ–љ–Є–ї–Љ–Њ—З–µ–≤–Є–љ—Л (–Я–°–Ь), –≤—В–Њ—А–∞—П –њ—А–Њ–±–ї–µ–Љ–∞ – –љ–µ–∞–і–µ–Ї–≤–∞—В–љ—Л–є –Ї–Њ–љ—В—А–Њ–ї—М –≥–ї–Є–Ї–µ–Љ–Є–Є. –Ґ–∞–Ї, –њ—А–Є –∞–љ–∞–ї–Є–Ј–µ –Ј–∞ 2009–2011 –≥–≥. –≤—Б–µ—Е —Б–ї—Г—З–∞–µ–≤ «—Б–Ї–Њ—А–Њ–њ–Њ–Љ–Њ—Й–љ–Њ–є» –≥–Њ—Б–њ–Є—В–∞–ї–Є–Ј–∞—Ж–Є–Є –≤ –Ъ–∞–Ј–∞–љ–Є –њ–Њ –њ–Њ–≤–Њ–і—Г –і–µ–Ї–Њ–Љ–њ–µ–љ—Б–∞—Ж–Є–Є –°–Ф 2 —В–Є–њ–∞ —З–∞—Б—В–Њ—В–∞ –≥–Є–њ–Њ–≥–ї–Є–Ї–µ–Љ–Є–Є —Б–Њ—Б—В–∞–≤–Є–ї–∞ —Б–Њ–Њ—В–≤–µ—В—Б—В–≤–µ–љ–љ–Њ –њ–Њ –≥–Њ–і–∞–Љ 37, 36 –Є 38% (—А–Є—Б. 1).
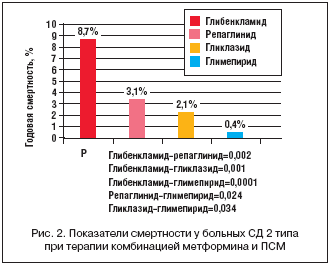
–Ъ–∞–Ї –Є–Ј–≤–µ—Б—В–љ–Њ, –Ї–Њ–Љ–±–Є–љ–∞—Ж–Є—П –Љ–µ—В—Д–Њ—А–Љ–Є–љ–∞ —Б –Я–°–Ь —П–≤–ї—П–µ—В—Б—П —Б–≤–Њ–µ–≥–Њ —А–Њ–і–∞ «–Ј–Њ–ї–Њ—В—Л–Љ —Б—В–∞–љ–і–∞—А—В–Њ–Љ» –њ–µ—А–Њ—А–∞–ї—М–љ–Њ–є —Б–∞—Е–∞—А–Њ—Б–љ–Є–ґ–∞—О—Й–µ–є —В–µ—А–∞–њ–Є–Є, –њ–Њ–Ј–≤–Њ–ї—П—О—Й–µ–є –љ–∞ –Њ–њ—А–µ–і–µ–ї–µ–љ–љ–Њ–є —Б—В–∞–і–Є–Є –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П –і–Њ—Б—В–Є–≥–љ—Г—В—М —Ж–µ–ї–µ–≤—Л—Е –њ–Њ–Ї–∞–Ј–∞—В–µ–ї–µ–є –Ї–Њ–Љ–њ–µ–љ—Б–∞—Ж–Є–Є —Г–≥–ї–µ–≤–Њ–і–љ–Њ–≥–Њ –Њ–±–Љ–µ–љ–∞ —Г –±–Њ–ї—М—И–Є–љ—Б—В–≤–∞ –±–Њ–ї—М–љ—Л—Е –°–Ф 2 —В–Є–њ–∞. –Т–Љ–µ—Б—В–µ —Б —В–µ–Љ, –Ї–∞–Ї —Б–≤–Є–і–µ—В–µ–ї—М—Б—В–≤—Г–µ—В –§–ї–Њ—А–µ–љ—В–Є–є—Б–Ї–Њ–µ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ (Florense Registry, 2006) [6], –≥–Њ–і–Њ–≤–∞—П —Б–Љ–µ—А—В–љ–Њ—Б—В—М —Н—В–Є—Е –±–Њ–ї—М–љ—Л—Е –Ј–љ–∞—З–Є—В–µ–ї—М–љ–Њ –Є –і–Њ—Б—В–Њ–≤–µ—А–љ–Њ —А–∞–Ј–ї–Є—З–∞–µ—В—Б—П –≤ –Ј–∞–≤–Є—Б–Є–Љ–Њ—Б—В–Є –Њ—В —В–Њ–≥–Њ –Є–ї–Є –Є–љ–Њ–≥–Њ –њ—А–µ–њ–∞—А–∞—В–∞ – –њ—А–Њ–Є–Ј–≤–Њ–і–љ–Њ–≥–Њ —Б—Г–ї—М—Д–Њ–љ–Є–ї–Љ–Њ—З–µ–≤–Є–љ—Л. –Ґ–∞–Ї, —Б–∞–Љ–∞—П –≤—Л—Б–Њ–Ї–∞—П —Б–Љ–µ—А—В–љ–Њ—Б—В—М –±—Л–ї–∞ –Њ—В–Љ–µ—З–µ–љ–∞ —Г –±–Њ–ї—М–љ—Л—Е, –њ–Њ–ї—Г—З–∞–≤—И–Є—Е –Љ–µ—В—Д–Њ—А–Љ–Є–љ –Є –≥–ї–Є–±–µ–љ–Ї–ї–∞–Љ–Є–і, –≤ 4 —А–∞–Ј–∞ –Љ–µ–љ—М—И–∞—П – –њ—А–Є –Ї–Њ–Љ–±–Є–љ–∞—Ж–Є–Є –Љ–µ—В—Д–Њ—А–Љ–Є–љ–∞ –Є –≥–ї–Є–Ї–ї–∞–Ј–Є–і–∞ –Є –≤ 20 —А–∞–Ј – –њ—А–Є –Ї–Њ–Љ–±–Є–љ–∞—Ж–Є–Є –Љ–µ—В—Д–Њ—А–Љ–Є–љ–∞ —Б –≥–ї–Є–Љ–µ–њ–Є—А–Є–і–Њ–Љ (—А–Є—Б. 2).
–Ю—Б–Њ–±–µ–љ–љ–Њ—Б—В—М—О –≥–Є–њ–Њ–≥–ї–Є–Ї–µ–Љ–Є–є, —Б–≤—П–Ј–∞–љ–љ—Л—Е —Б —Б—Г–ї—М—Д–Њ–љ–Є–ї–Љ–Њ—З–µ–≤–Є–љ–Њ–є (–≤ –Њ—В–ї–Є—З–Є–µ –Њ—В –±–Њ–ї—М—И–Є–љ—Б—В–≤–∞ –≥–Є–њ–Њ–≥–ї–Є–Ї–µ–Љ–Є–є –љ–∞ —Д–Њ–љ–µ –Є–љ—Б—Г–ї–Є–љ–∞), —П–≤–ї—П–µ—В—Б—П –Є—Е –±–Њ–ї—М—И–∞—П –њ—А–Њ–і–Њ–ї–ґ–Є—В–µ–ї—М–љ–Њ—Б—В—М –Є —Б–Ї–ї–Њ–љ–љ–Њ—Б—В—М –Ї —А–µ—Ж–Є–і–Є–≤–∞–Љ –≤ —В–µ—З–µ–љ–Є–µ 3 —Б—Г—В. –њ–Њ—Б–ї–µ —Г—Б–њ–µ—И–љ–Њ–є –Ї–Њ—А—А–µ–Ї—Ж–Є–Є —Г—А–Њ–≤–љ—П –≥–ї—О–Ї–Њ–Ј—Л. –Ю–±—К—П—Б–љ–µ–љ–Є–µ–Љ —В–Њ–Љ—Г —П–≤–ї—П–µ—В—Б—П –і–ї–Є—В–µ–ї—М–љ—Л–є –њ–µ—А–Є–Њ–і –њ–Њ–ї—Г–≤—Л–≤–µ–і–µ–љ–Є—П –Я–°–Ь (–Њ—Б–Њ–±–µ–љ–љ–Њ –≥–ї–Є–±–µ–љ–Ї–ї–∞–Љ–Є–і–∞), –≤ –±–Њ–ї—М—И–µ–є —Б—В–µ–њ–µ–љ–Є —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ –њ–Њ–ґ–Є–ї–Њ–≥–Њ –≤–Њ–Ј—А–∞—Б—В–∞. –Э–µ–Њ–±—Е–Њ–і–Є–Љ–Њ –Ј–∞–Љ–µ—В–Є—В—М, —З—В–Њ –њ–Њ–і–Њ–±–љ–∞—П –≥–Є–њ–Њ–≥–ї–Є–Ї–µ–Љ–Є—П —Г –ї–Є—Ж –њ–Њ–ґ–Є–ї–Њ–≥–Њ –≤–Њ–Ј—А–∞—Б—В–∞, –Њ—Б–Њ–±–µ–љ–љ–Њ –њ—А–Є —Б—В–µ–љ–Њ–Ј–Є—А—Г—О—Й–µ–Љ –∞—В–µ—А–Њ—Б–Ї–ї–µ—А–Њ–Ј–µ —Б–Њ—Б—Г–і–Њ–≤ —Б–µ—А–і—Ж–∞ –Є –≥–Њ–ї–Њ–≤–љ–Њ–≥–Њ –Љ–Њ–Ј–≥–∞, –љ–∞—З–Є–љ–∞–µ—В—Б—П –њ–Њ—Б—В–µ–њ–µ–љ–љ–Њ, –±–µ–Ј —П—А–Ї–Њ–є –≤–µ–≥–µ—В–∞—В–Є–≤–љ–Њ–є —Б–Є–Љ–њ—В–Њ–Љ–∞—В–Є–Ї–Є –Є –Љ–Њ–ґ–µ—В —Б–Њ–њ—А–Њ–≤–Њ–ґ–і–∞—В—М—Б—П –Њ—З–∞–≥–Њ–≤—Л–Љ–Є –љ–µ–≤—А–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є–Љ–Є –Ј–љ–∞–Ї–∞–Љ–Є, –Є–Љ–Є—В–Є—А—Г—П –љ–∞—А—Г—И–µ–љ–Є–µ –Љ–Њ–Ј–≥–Њ–≤–Њ–≥–Њ –Ї—А–Њ–≤–Њ–Њ–±—А–∞—Й–µ–љ–Є—П [7,8].
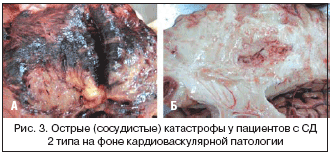
–Т—Б–µ –Я–°–Ь –Њ–±–ї–∞–і–∞—О—В —Б–њ–Њ—Б–Њ–±–љ–Њ—Б—В—М—О –Ј–∞–Ї—А—Л–≤–∞—В—М –Ъ–Р–Ґ–§––Ј–∞–≤–Є—Б–Є–Љ—Л–µ –Ї–∞–љ–∞–ї—Л β––Ї–ї–µ—В–Њ–Ї, –≤—Л–Ј—Л–≤–∞—П —Г–≤–µ–ї–Є—З–µ–љ–Є–µ —Б–µ–Ї—А–µ—Ж–Є–Є –Є–љ—Б—Г–ї–Є–љ–∞ –Є–Ј –њ–Њ–і–ґ–µ–ї—Г–і–Њ—З–љ–Њ–є –ґ–µ–ї–µ–Ј—Л. –Я—А–Є –љ–∞–ї–Є—З–Є–Є –≤ —Б–≤–Њ–µ–Љ —Б—В—А–Њ–µ–љ–Є–Є –Њ–њ—А–µ–і–µ–ї–µ–љ–љ—Л—Е —Е–Є–Љ–Є—З–µ—Б–Ї–Є—Е –≥—А—Г–њ–њ –њ–Њ–і–Њ–±–љ—Л–µ –њ—А–µ–њ–∞—А–∞—В—Л –Љ–Њ–≥—Г—В —Б–≤—П–Ј—Л–≤–∞—В—М—Б—П —В–∞–Ї–ґ–µ –Є —Б –Ъ–Р–Ґ–§––Ј–∞–≤–Є—Б–Є–Љ—Л–Љ–Є –Ї–∞–љ–∞–ї–∞–Љ–Є –Ї–ї–µ—В–Њ–Ї —Б–µ—А–і–µ—З–љ–Њ–—Б–Њ—Б—Г–і–Є—Б—В–Њ–є —Б–Є—Б—В–µ–Љ—Л, –њ—А–Є–≤–Њ–і—П –Ї –Є—Е –Ј–∞–Ї—А—Л—В–Є—О –Є –њ–Њ—Б–ї–µ–і—Г—О—Й–µ–є –Є—И–µ–Љ–Є–Є —В–Ї–∞–љ–µ–є. –≠—В–Њ –Њ–±—К—П—Б–љ—П–µ—В –њ—А–Є—З–Є–љ—Г —Г—Е—Г–і—И–µ–љ–Є—П –Ї–Њ—А–Њ–љ–∞—А–љ–Њ–≥–Њ –њ—А–Њ–≥–љ–Њ–Ј–∞ –њ—А–Є –њ—А–Є–µ–Љ–µ —Б—Г–ї—М—Д–∞–љ–Є–ї–∞–Љ–Є–і–Њ–≤ —Г –±–Њ–ї—М–љ—Л—Е –°–Ф 2 —В–Є–њ–∞ —Б —В—П–ґ–µ–ї—Л–Љ —В–µ—З–µ–љ–Є–µ–Љ –Ї–∞—А–і–Є–Њ–≤–∞—Б–Ї—Г–ї—П—А–љ–Њ–є –њ–∞—В–Њ–ї–Њ–≥–Є–Є. –Э–∞ —А–Є—Б—Г–љ–Ї–µ 3 –њ—А–µ–і—Б—В–∞–≤–ї–µ–љ—Л –Љ–∞–Ї—А–Њ—Б–Њ—Б—Г–і–Є—Б—В—Л–µ –Њ—Б–ї–Њ–ґ–љ–µ–љ–Є—П –Ї–∞–Ї –Є—Б—Е–Њ–і –і–µ–Ї–Њ–Љ–њ–µ–љ—Б–∞—Ж–Є–Є –°–Ф: –Њ—Б—В—А—Л–є –Є–љ—Д–∞—А–Ї—В –Љ–Є–Њ–Ї–∞—А–і–∞ (–Р) –Є –Њ—Б—В—А–Њ–µ –љ–∞—А—Г—И–µ–љ–Є–µ –Љ–Њ–Ј–≥–Њ–≤–Њ–≥–Њ –Ї—А–Њ–≤–Њ–Њ–±—А–∞—Й–µ–љ–Є—П (–С).
–Э–µ–Њ–±—Е–Њ–і–Є–Љ–Њ —Г—З–Є—В—Л–≤–∞—В—М —В–∞–Ї–ґ–µ, —З—В–Њ –љ–µ–Ї–Њ—В–Њ—А—Л–µ –ї–µ–Ї–∞—А—Б—В–≤–∞, –≤ —В–Њ–Љ —З–Є—Б–ї–µ β––∞–і—А–µ–љ–Њ–±–ї–Њ–Ї–∞—В–Њ—А—Л, –Є–љ–≥–Є–±–Є—В–Њ—А—Л –Р–Я–§, —В–µ—В—А–∞—Ж–Є–Ї–ї–Є–љ—Л –Є –і—А., —Г—Б–Є–ї–Є–≤–∞—О—В –≥–ї—О–Ї–Њ–Ј–Њ—Б–љ–Є–ґ–∞—О—Й–µ–µ –і–µ–є—Б—В–≤–Є–µ –њ—А–µ–њ–∞—А–∞—В–Њ–≤ —Б—Г–ї—М—Д–Њ–љ–Є–ї–Љ–Њ—З–µ–≤–Є–љ—Л.
–Я–Њ–і –љ–∞—И–Є–Љ –љ–∞–±–ї—О–і–µ–љ–Є–µ–Љ –±—Л–ї–Њ 1106 –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –°–Ф 2 —В–Є–њ–∞, –њ–Њ–ї—Г—З–∞—О—Й–Є—Е –њ–µ—А–Њ—А–∞–ї—М–љ—Л–µ —Б–∞—Е–∞—А–Њ—Б–љ–Є–ґ–∞—О—Й–Є–µ –њ—А–µ–њ–∞—А–∞—В—Л. –°—А–µ–і–Є –љ–Є—Е —А–µ–≥—Г–ї—П—А–љ–Њ –љ–∞–±–ї—О–і–∞—О—В—Б—П —Г —Н–љ–і–Њ–Ї—А–Є–љ–Њ–ї–Њ–≥–∞ –њ–Њ –Љ–µ—Б—В—Г –ґ–Є—В–µ–ї—М—Б—В–≤–∞ —З—Г—В—М –±–Њ–ї—М—И–µ —В—А–µ—В–Є (413 –њ–∞—Ж–Є–µ–љ—В–Њ–≤, 37,3%). –Т–Њ –≤—А–µ–Љ—П –≤–Є–Ј–Є—В–∞ –≤—Б–µ–Љ –њ–∞—Ж–Є–µ–љ—В–∞–Љ —А–∞–Ј–і–∞–≤–∞–ї–Є –Њ–њ—А–Њ—Б–љ–Є–Ї, –≥–і–µ –љ—Г–ґ–љ–Њ –±—Л–ї–Њ —Г–Ї–∞–Ј–∞—В—М –њ–∞—Б–њ–Њ—А—В–љ—Г—О —З–∞—Б—В—М, —Б—В–∞–ґ –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П, –љ–∞—З–∞–ї–Њ —Б–∞—Е–∞—А–Њ—Б–љ–Є–ґ–∞—О—Й–µ–є —В–µ—А–∞–њ–Є–Є —Б —Г–Ї–∞–Ј–∞–љ–Є–µ–Љ –і–Њ–Ј—Л –Є –Ї—А–∞—В–љ–Њ—Б—В–Є –њ—А–Є–µ–Љ–∞, —З–∞—Б—В–Њ—В—Г –Ї–Њ–љ—В—А–Њ–ї—П –≥–ї–Є–Ї–µ–Љ–Є–Є, —Б–Њ–њ—Г—В—Б—В–≤—Г—О—Й–Є–µ —Е—А–Њ–љ–Є—З–µ—Б–Ї–Є–µ –±–Њ–ї–µ–Ј–љ–Є –Є —Б—Г–±—К–µ–Ї—В–Є–≤–љ—Л–µ –њ—А–Њ—П–≤–ї–µ–љ–Є—П –≥–Є–њ–Њ–≥–ї–Є–Ї–µ–Љ–Є–Є (—А–µ–Ј–Ї–∞—П —Б–ї–∞–±–Њ—Б—В—М, —В—А–µ–Љ–Њ—А —А—Г–Ї, —З—Г–≤—Б—В–≤–Њ –≥–Њ–ї–Њ–і–∞, —Б–µ—А–і—Ж–µ–±–Є–µ–љ–Є–µ, –њ–Њ—В–µ—А—П —Б–Њ–Ј–љ–∞–љ–Є—П).
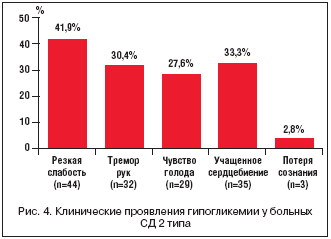
–Ф–ї–Є—В–µ–ї—М–љ–Њ—Б—В—М –°–Ф 2 —В–Є–њ–∞ –≤ —Б—А–µ–і–љ–µ–Љ —Б–Њ—Б—В–∞–≤–Є–ї–∞ 6,0±4,1 –≥–Њ–і–∞. –Я–Њ –і–∞–љ–љ—Л–Љ –∞–љ–Ї–µ—В–Є—А–Њ–≤–∞–љ–Є—П –Є —А–µ–Ј—Г–ї—М—В–∞—В–Њ–≤ –ї–∞–±–Њ—А–∞—В–Њ—А–љ—Л—Е –і–∞–љ–љ—Л—Е, –≥–Є–њ–Њ–≥–ї–Є–Ї–µ–Љ–Є—О –Њ—В–Љ–µ—В–Є–ї–Є —Г 105 –њ–∞—Ж–Є–µ–љ—В–Њ–≤ (25,4%), –≤ —В–Њ–Љ —З–Є—Б–ї–µ —Г 87 (83%) –ґ–µ–љ—Й–Є–љ –Є 18 (17%) –Љ—Г–ґ—З–Є–љ –≤ –≤–Њ–Ј—А–∞—Б—В–µ 61,2±11,3 –≥–Њ–і–∞. –Ъ–∞–Ї –≤–Є–і–љ–Њ –Є–Ј —А–Є—Б—Г–љ–Ї–∞ 4, –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є–Љ–Є —Н–Ї–≤–Є–≤–∞–ї–µ–љ—В–∞–Љ–Є –≥–Є–њ–Њ–≥–ї–Є–Ї–µ–Љ–Є–Є –±—Л–ї–Є —А–µ–Ј–Ї–∞—П —Б–ї–∞–±–Њ—Б—В—М (41,9%), —В—А–µ–Љ–Њ—А —А—Г–Ї (30,4%), —З—Г–≤—Б—В–≤–Њ –≥–Њ–ї–Њ–і–∞ (27,6%), —Г—З–∞—Й–µ–љ–љ–Њ–µ —Б–µ—А–і—Ж–µ–±–Є–µ–љ–Є–µ (33,3%), –њ–Њ—В–µ—А—П —Б–Њ–Ј–љ–∞–љ–Є—П (2,8%).
–Я—А–Є —Н—В–Њ–Љ —Б—А–µ–і–љ–Є–µ –њ–Њ–Ї–∞–Ј–∞—В–µ–ї–Є –≥–Є–њ–Њ–≥–ї–Є–Ї–µ–Љ–Є–Є —Г –±–Њ–ї—М—И–Є–љ—Б—В–≤–∞ –љ–∞–±–ї—О–і–∞–µ–Љ—Л—Е –≤ —Б—А–µ–і–љ–µ–Љ —Б–Њ—Б—В–∞–≤–Є–ї–Є 3,5±0,6 –Љ–Љ–Њ–ї—М/–ї, –∞ —Г 7 –њ–∞—Ж–Є–µ–љ—В–Њ–≤ – –њ—А–Є —Г—А–Њ–≤–љ–µ —Б–∞—Е–∞—А–∞ –њ–Њ –і–Њ–Љ–∞—И–љ–µ–Љ—Г –≥–ї—О–Ї–Њ–Љ–µ—В—А—Г – –Њ—В 4,3 –і–Њ 5,2 –Љ–Љ–Њ–ї—М/–ї.
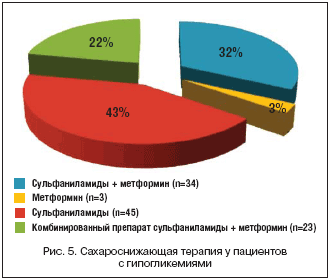
–Я—А–Є –∞–љ–∞–ї–Є–Ј–µ —Б–∞—Е–∞—А–Њ—Б–љ–Є–ґ–∞—О—Й–µ–є —В–µ—А–∞–њ–Є–Є –≤—Л—П–≤–ї–µ–љ–Њ, —З—В–Њ 45 (42,8%) –њ–∞—Ж–Є–µ–љ—В–Њ–≤ –њ–Њ–ї—Г—З–∞—О—В –Я–°–Ь (–≥–ї–Є–±–µ–љ–Ї–ї–∞–Љ–Є–і, –≥–ї–Є–Ї–ї–∞–Ј–Є–і, –≥–ї–Є–Љ–µ–њ–Є—А–Є–і) –≤ —А–∞–Ј–ї–Є—З–љ—Л—Е –і–Њ–Ј–∞—Е –Є –Ї—А–∞—В–љ–Њ—Б—В–Є –њ—А–Є–µ–Љ–∞, 34 (32,4%) – –≤ –Ї–Њ–Љ–±–Є–љ–∞—Ж–Є–Є —Б –њ—А–µ–њ–∞—А–∞—В–∞–Љ–Є –Љ–µ—В—Д–Њ—А–Љ–Є–љ–∞, 23 (21,9%) – –Ї–Њ–Љ–±–Є–љ–Є—А–Њ–≤–∞–љ–љ—Л–є –њ—А–µ–њ–∞—А–∞—В —Б—Г–ї—М—Д–Њ–љ–Є–ї–Љ–Њ—З–µ–≤–Є–љ—Л + –Љ–µ—В—Д–Њ—А–Љ–Є–љ –≤ —А–∞–Ј–ї–Є—З–љ—Л—Е –і–Њ–Ј–∞—Е –Є 3 (2,8%) – –Љ–µ—В—Д–Њ—А–Љ–Є–љ –≤ –і–Њ–Ј–µ 2,5 –≥/—Б—Г—В. (—А–Є—Б. 5).
–Э–µ–Њ–±—Е–Њ–і–Є–Љ–Њ –њ–Њ–і—З–µ—А–Ї–љ—Г—В—М, —З—В–Њ –Њ–і–Є–љ –њ–∞—Ж–Є–µ–љ—В –љ–∞ —Д–Њ–љ–µ —В–µ—А–∞–њ–Є–Є –Ї–Њ–Љ–±–Є–љ–Є—А–Њ–≤–∞–љ–љ—Л–Љ —Б–∞—Е–∞—А–Њ—Б–љ–Є–ґ–∞—О—Й–Є–Љ –њ—А–µ–њ–∞—А–∞—В–Њ–Љ –Є –і–≤–Њ–µ – –Я–°–Ь —Б –Љ–µ—В—Д–Њ—А–Љ–Є–љ–Њ–Љ, –≤—Л–Ј—Л–≤–∞–ї–Є –°–Ь–Я –≤ —Б–≤—П–Ј–Є —Б –≥–Є–њ–Њ–≥–ї–Є–Ї–µ–Љ–Є–µ–є. –¶–Є—Д—А—Л –≥–ї–Є–Ї–µ–Љ–Є–Є –њ–Њ –≥–ї—О–Ї–Њ–Љ–µ—В—А—Г —Б–Њ—Б—В–∞–≤–Є–ї–Є 2,2, 1,8 –Є 2,1 —Б–Њ–Њ—В–≤–µ—В—Б—В–≤–µ–љ–љ–Њ.
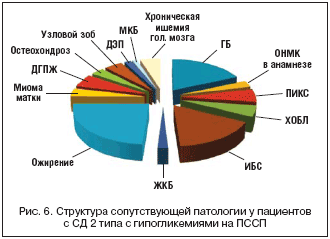
–£ –±–Њ–ї—М—И–µ–є —З–∞—Б—В–Є –њ–∞—Ж–Є–µ–љ—В–Њ–≤ (78,3%), –њ–Њ –і–∞–љ–љ—Л–Љ –∞–Љ–±—Г–ї–∞—В–Њ—А–љ–Њ–є –Ї–∞—А—В—Л, –Є–Љ–µ–ї–Є—Б—М —В–µ –Є–ї–Є –Є–љ—Л–µ –њ–Њ–Ј–і–љ–Є–µ –Њ—Б–ї–Њ–ґ–љ–µ–љ–Є—П –°–Ф 2 —В–Є–њ–∞. –°—А–µ–і–Є –љ–Є—Е – –љ–µ–є—А–Њ–њ–∞—В–Є—П —Г 69 (83,1%) —З–µ–ї–Њ–≤–µ–Ї, —А–µ—В–Є–љ–Њ–њ–∞—В–Є—П – —Г 16(19,2%) –њ–∞—Ж–Є–µ–љ—В–Њ–≤ –Є –љ–µ—Д—А–Њ–њ–∞—В–Є—П – —Г 23 (27,7%) –љ–∞–±–ї—О–і–∞–≤—И–Є—Е—Б—П. –Я—А–Є —Н—В–Њ–Љ —Г –≤—Б–µ—Е –њ–∞—Ж–Є–µ–љ—В–Њ–≤ –≤—Л—П–≤–ї–µ–љ–Њ –Њ—В –і–≤—Г—Е –Є –±–Њ–ї–µ–µ —Б–Њ–њ—Г—В—Б—В–≤—Г—О—Й–Є—Е –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є–є (—А–Є—Б. 6).
–Я–Њ–Ї–∞–Ј–∞—В–µ–ї–Є –∞—А—В–µ—А–Є–∞–ї—М–љ–Њ–≥–Њ –і–∞–≤–ї–µ–љ–Є—П —Г –њ—А–Њ–∞–љ–∞–ї–Є–Ј–Є—А–Њ–≤–∞–љ–љ—Л—Е –њ–∞—Ж–Є–µ–љ—В–Њ–≤ –≤ —Б—А–µ–і–љ–µ–Љ —Б–Њ—Б—В–∞–≤–Є–ї–Є 143±11,2 /87±5,3 –Љ–Љ. —А—В.—Б—В. –Т—Б–µ –њ–Њ–ї—Г—З–∞–ї–Є –≥–Є–њ–Њ—В–µ–љ–Ј–Є–≤–љ—Г—О —В–µ—А–∞–њ–Є—О: β––±–ї–Њ–Ї–∞—В–Њ—А—Л – 64,2% –њ–∞—Ж–Є–µ–љ—В–Њ–≤, –Є–љ–≥–Є–±–Є—В–Њ—А—Л –Р–Я–§ – 57,8%, –∞ —В–∞–Ї–ґ–µ –∞–љ—В–Є–∞–≥—А–µ–≥–∞–љ—В—Л – 77,3%, –љ–Є—В—А–∞—В—Л – 41,1% –љ–∞–±–ї—О–і–∞–≤—И–Є—Е—Б—П.
–Ґ–∞–Ї–Є–Љ –Њ–±—А–∞–Ј–Њ–Љ, –і–ї—П –і–Њ—Б—В–Є–ґ–µ–љ–Є—П —Б—В–∞–±–Є–ї—М–љ–Њ–є –Є –і–ї–Є—В–µ–ї—М–љ–Њ–є –Ї–Њ–Љ–њ–µ–љ—Б–∞—Ж–Є–Є —Г–≥–ї–µ–≤–Њ–і–љ–Њ–≥–Њ –Њ–±–Љ–µ–љ–∞, –∞ —В–∞–Ї–ґ–µ —Г–ї—Г—З—И–µ–љ–Є—П –≥–ї–Є–Ї–µ–Љ–Є—З–µ—Б–Ї–Њ–≥–Њ –Ї–Њ–љ—В—А–Њ–ї—П —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б—В–∞—А—И–µ–є –≤–Њ–Ј—А–∞—Б—В–љ–Њ–є –≥—А—Г–њ–њ—Л –љ–µ–Њ–±—Е–Њ–і–Є–Љ–Њ –Њ–њ—А–µ–і–µ–ї–µ–љ–Є–µ –Є–љ–і–Є–≤–Є–і—Г–∞–ї—М–љ—Л—Е —Ж–µ–ї–µ–є –ї–µ—З–µ–љ–Є—П —Б —Г—З–µ—В–Њ–Љ –≤–Њ–Ј—А–∞—Б—В–∞, –љ–∞–ї–Є—З–Є—П –Њ—Б–ї–Њ–ґ–љ–µ–љ–Є–є, —А–Є—Б–Ї–∞ –≥–Є–њ–Њ–≥–ї–Є–Ї–µ–Љ–Є–є. –°—В—А–∞—В–Є—Д–Є–Ї–∞—Ж–Є—П —В–µ—А–∞–њ–µ–≤—В–Є—З–µ—Б–Ї–Њ–є —В–∞–Ї—В–Є–Ї–Є –Њ–њ—А–µ–і–µ–ї—П–µ—В—Б—П –Є—Б—Е–Њ–і–љ—Л–Љ —Г—А–Њ–≤–љ–µ–Љ –Љ–µ—В–∞–±–Њ–ї–Є—З–µ—Б–Ї–Њ–≥–Њ –Ї–Њ–љ—В—А–Њ–ї—П.
–У–Є–њ–Њ–≥–ї–Є–Ї–µ–Љ–Є–Є, –Њ—Б–Њ–±–µ–љ–љ–Њ —В—П–ґ–µ–ї—Л–µ —Н–њ–Є–Ј–Њ–і—Л, –Ј–љ–∞—З–Є—В–µ–ї—М–љ–Њ –њ–Њ–≤—Л—И–∞—О—В –њ—А—П–Љ—Л–µ –Є –љ–µ–њ—А—П–Љ—Л–µ —А–∞—Б—Е–Њ–і—Л –љ–∞ —В–µ—А–∞–њ–Є—О –Є —Б–љ–Є–ґ–∞—О—В –њ—А–Њ–Є–Ј–≤–Њ–і–Є—В–µ–ї—М–љ–Њ—Б—В—М —В—А—Г–і–∞. –Э–∞–њ—А–Є–Љ–µ—А, –≤ –Т–µ–ї–Є–Ї–Њ–±—А–Є—В–∞–љ–Є–Є –±—Л–ї–Њ –њ–Њ–і—Б—З–Є—В–∞–љ–Њ, —З—В–Њ —Б—В–Њ–Є–Љ–Њ—Б—В—М —В—П–ґ–µ–ї–Њ–є –≥–Є–њ–Њ–≥–ї–Є–Ї–µ–Љ–Є–Є –њ—А–Є –°–Ф 2 —В–Є–њ–∞ (–љ–µ –≤–Ї–ї—О—З–∞—П —Б–≤—П–Ј–∞–љ–љ—Л–µ —Б –љ–µ–є —А–∞—Б—Е–Њ–і—Л –љ–∞ –љ–µ—В—А—Г–і–Њ—Б–њ–Њ—Б–Њ–±–љ–Њ—Б—В—М, –Є–љ–≤–∞–ї–Є–і–љ–Њ—Б—В—М –Є–ї–Є –њ–Њ—В–µ—А—О —А–∞–±–Њ—В—Л) —Б–Њ—Б—В–∞–≤–ї—П–µ—В –Њ–Ї–Њ–ї–Њ 7,4 –Љ–ї–љ —Д—Г–љ—В–Њ–≤ —Б—В–µ—А–ї–Є–љ–≥–Њ–≤.
–°–Њ–≤—А–µ–Љ–µ–љ–љ–∞—П —Б—В—А–∞—В–µ–≥–Є—П –≤ —В–µ—А–∞–њ–Є–Є –°–Ф 2 —В–Є–њ–∞ –њ—А–µ–і–њ–Њ–ї–∞–≥–∞–µ—В –Ї–Њ—А—А–µ–Ї—Ж–Є—О —Е—А–Њ–љ–Є—З–µ—Б–Ї–Њ–є –≥–ї–Є–Ї–µ–Љ–Є–Є –Ј–∞ —Б—З–µ—В –њ—А–µ–Њ–і–Њ–ї–µ–љ–Є—П –Є–љ—Б—Г–ї–Є–љ–Њ—А–µ–Ј–Є—Б—В–µ–љ—В–љ–Њ—Б—В–Є –Є —Г–ї—Г—З—И–µ–љ–Є—П β––Ї–ї–µ—В–Њ—З–љ–Њ–є —Д—Г–љ–Ї—Ж–Є–Є –њ–Њ–і–ґ–µ–ї—Г–і–Њ—З–љ–Њ–є –ґ–µ–ї–µ–Ј—Л, –∞ —В–∞–Ї–ґ–µ –≤—Л—Б–Њ–Ї—Г—О –±–µ–Ј–Њ–њ–∞—Б–љ–Њ—Б—В—М. –Ъ–Њ–Љ–±–Є–љ–∞—Ж–Є—П —Б–µ–љ—Б–Є—В–∞–є–Ј–µ—А–Њ–≤ –Є–љ—Б—Г–ї–Є–љ–∞ –Є —Б–µ–Ї—А–µ—В–Њ–≥–µ–љ–Њ–≤ –њ—А–Є –ї–µ—З–µ–љ–Є–Є –°–Ф 2 —В–Є–њ–∞ –≤—Б–µ —З–∞—Й–µ –≤—Б—В—А–µ—З–∞–µ—В—Б—П –≤ —Б–Њ–≤—А–µ–Љ–µ–љ–љ–Њ–є –њ—А–∞–Ї—В–Є–Ї–µ —Н–љ–і–Њ–Ї—А–Є–љ–Њ–ї–Њ–≥–Њ–≤. –Я—А–Є—З–µ–Љ, –≤ –њ–Њ—Б–ї–µ–і–љ–µ–µ –≤—А–µ–Љ—П –≤ –Ї–∞—З–µ—Б—В–≤–µ —Б–µ–Ї—А–µ—В–Њ–≥–µ–љ–Њ–≤ –Є–љ—Б—Г–ї–Є–љ–∞ –њ—А–Є –Ї–Њ–Љ–±–Є–љ–Є—А–Њ–≤–∞–љ–љ–Њ–є —В–µ—А–∞–њ–Є–Є –°–Ф —З–∞—Б—В–Њ –Є—Б–њ–Њ–ї—М–Ј—Г—О—В –Є–љ–Ї—А–µ—В–Є–љ–Њ–Љ–Є–Љ–µ—В–Є–Ї–Є. –Ъ –њ—А–µ–і—Б—В–∞–≤–Є—В–µ–ї—П–Љ –Њ–і–љ–Њ–≥–Њ –Є–Ј –Ї–ї–∞—Б—Б–Њ–≤ –Є–љ–Ї—А–µ—В–Є–љ–Њ–Љ–Є–Љ–µ—В–Є–Ї–Њ–≤ –Њ—В–љ–Њ—Б—П—В—Б—П –Є–љ–≥–Є–±–Є—В–Њ—А—Л –і–Є–њ–µ–њ—В–Є–і–Є–ї–њ–µ–њ—В–Є–і–∞–Ј—Л–4 (–Ф–Я–Я–4). –Ф–Я–Я–4 –Є–љ–≥–Є–±–Є—А—Г—О—В —Д–µ—А–Љ–µ–љ—В –Ф–Я–Я–4, —З–µ–Љ –≤—Л–Ј—Л–≤–∞—О—В –њ–Њ–≤—Л—И–µ–љ–Є–µ –∞–Ї—В–Є–≤–љ–Њ—Б—В–Є –Њ—Б–љ–Њ–≤–љ—Л—Е –Є–љ–Ї—А–µ—В–Є–љ–Њ–≤ –Њ—А–≥–∞–љ–Є–Ј–Љ–∞: –≥–ї—О–Ї–∞–≥–Њ–љ–Њ–њ–Њ–і–Њ–±–љ–Њ–≥–Њ –њ–µ–њ—В–Є–і–∞–1 (–У–Я–Я–1) –Є –≥–ї—О–Ї–Њ–Ј–Њ–Ј–∞–≤–Є—Б–Є–Љ–Њ–≥–Њ –Є–љ—Б—Г–ї–Є–љ–Њ—В—А–Њ–њ–љ–Њ–≥–Њ –њ–Њ–ї–Є–њ–µ–њ—В–Є–і–∞ (–У–Ш–Я). –Ш–љ–Ї—А–µ—В–Є–љ—Л – —Н—В–Њ –≥–Њ—А–Љ–Њ–љ—Л —Б –Њ—З–µ–љ—М –Ї–Њ—А–Њ—В–Ї–Є–Љ –њ–µ—А–Є–Њ–і–Њ–Љ –∞–Ї—В–Є–≤–љ–Њ—Б—В–Є, –≤—Л—А–∞–±–∞—В—Л–≤–∞–µ–Љ—Л–µ –≤ –Ї–Є—И–µ—З–љ–Є–Ї–µ, –Є—Е –і–µ–є—Б—В–≤–Є–µ –ї–µ–ґ–Є—В –≤ –Њ—Б–љ–Њ–≤–µ —Б–µ–Ї—А–µ—Ж–Є–Є –Є–љ—Б—Г–ї–Є–љ–∞ –њ–Њ—Б–ї–µ –љ–∞–≥—А—Г–Ј–Ї–Є –≥–ї—О–Ї–Њ–Ј–Њ–є. –≠—В–Њ—В –Њ—В–≤–µ—В –њ—А–Њ–Є—Б—Е–Њ–і–Є—В –≤ –≥–ї—О–Ї–Њ–Ј–Њ–Ј–∞–≤–Є—Б–Є–Љ–Њ–є –Љ–∞–љ–µ—А–µ, –≤ –Њ—В–ї–Є—З–Є–µ –Њ—В –Є–љ—Б—Г–ї–Є–љ–Њ–≤—Л—Е —Б–µ–Ї—А–µ—В–Њ–≥–µ–љ–Њ–≤, –≤ —З–∞—Б—В–љ–Њ—Б—В–Є –Я–°–Ь.
–Ґ–∞–Ї–Њ–є «–≥–ї—О–Ї–Њ–Ј–Њ–Ј–∞–≤–Є—Б–Є–Љ—Л–є» –Љ–µ—Е–∞–љ–Є–Ј–Љ –њ—А–µ–і–Њ—В–≤—А–∞—Й–∞–µ—В —А–Є—Б–Ї –≥–Є–њ–Њ–≥–ї–Є–Ї–µ–Љ–Є–є. –Ш–љ–≥–Є–±–Є—В–Њ—А –Ф–Я–Я–4 –≤–Є–ї–і–∞–≥–ї–Є–њ—В–Є–љ —П–≤–ї—П–µ—В—Б—П –љ–∞–Є–±–Њ–ї–µ–µ —Е–Њ—А–Њ—И–Њ –Є–Ј—Г—З–µ–љ–љ—Л–Љ –њ—А–µ–њ–∞—А–∞—В–Њ–Љ –і–∞–љ–љ–Њ–є –≥—А—Г–њ–њ—Л, —И–Є—А–Њ–Ї–Њ–Љ–∞—Б—И—В–∞–±–љ–∞—П –њ—А–Њ–≥—А–∞–Љ–Љ–∞ –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Њ–≥–Њ –Є–Ј—Г—З–µ–љ–Є—П —Н—В–Њ–≥–Њ –њ—А–µ–њ–∞—А–∞—В–∞ –і–Њ–Ї–∞–Ј–∞–ї–∞ –µ–≥–Њ –≤—Л—Б–Њ–Ї—Г—О —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В—М, –і–Њ—Б—В–Њ–≤–µ—А–љ—Г—О –±–µ–Ј–Њ–њ–∞—Б–љ–Њ—Б—В—М –Є —Е–Њ—А–Њ—И—Г—О –њ–µ—А–µ–љ–Њ—Б–Є–Љ–Њ—Б—В—М. –Я—А–µ–њ–∞—А–∞—В –Њ–±–µ—Б–њ–µ—З–Є–≤–∞–µ—В —Г–ї—Г—З—И–µ–љ–Є–µ –≥–ї–Є–Ї–µ–Љ–Є—З–µ—Б–Ї–Њ–≥–Њ –Ї–Њ–љ—В—А–Њ–ї—П –њ—А–Є –љ–∞–Ј–љ–∞—З–µ–љ–Є–Є –µ–≥–Њ –Ї–∞–Ї –≤ –Љ–Њ–љ–Њ—В–µ—А–∞–њ–Є–Є, —В–∞–Ї –Є –≤ –Ї–Њ–Љ–±–Є–љ–∞—Ж–Є–Є —Б –Њ—З–µ–љ—М –љ–Є–Ј–Ї–Є–Љ —А–Є—Б–Ї–Њ–Љ –≥–Є–њ–Њ–≥–ї–Є–Ї–µ–Љ–Є–є –Є –љ–µ–є—В—А–∞–ї—М–љ—Л–Љ –≤–ї–Є—П–љ–Є–µ–Љ –љ–∞ –Љ–∞—Б—Б—Г —В–µ–ї–∞.
–Ы–Є—В–µ—А–∞—В—Г—А–∞
1. Ohkubo Y., Kishikawa H., Araki E. et al. Intensive insulintherapy prevents the progression of diabetic microvascular complications in Japanese patients with NIDDM: a randomized prospective 6–year study // Diabetes Res. Clin. Pract. – 1995. – Vol. 28. – P.103–117.
2. UK Prospective Diabetes Study (UKPDS). Group Intensive blood–glucose control with sulfonilureas or insulin compared with conventional treatment and risk of complications in patients with type 2 diabetes. (UKPDS 33) // Lan—Бet. – 1998. – Vol. 352 (9131). – P. 837–853.
3. Turner R. C. et al. The UK Prospective Diabetes Study Group: glycemic control with diet, sulfonylurea, metformin or insulin in patients with type 2 diabetes mellitus: progressive requirement for multiple therapies (UKPDS 49) // JAMA. – 1999. – Vol. 281. – P. 2005–2012.
4. –®–µ—Б—В–∞–Ї–Њ–≤–∞ –Ь.–Т., –Ч–Є–ї–Њ–≤ –Р.–Т. –Т—Л–±–Њ—А –Њ–њ—В–Є–Љ–∞–ї—М–љ–Њ–є —Б–∞—Е–∞—А–Њ—Б–љ–Є–ґ–∞—О—Й–µ–є —В–µ—А–∞–њ–Є–Є —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б —Б–∞—Е–∞—А–љ—Л–Љ –і–Є–∞–±–µ—В–Њ–Љ –≤ –і–µ–±—О—В–µ –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П // Consilium medicum. – 2010. – –Ґ. 12. вДЦ 12. – C. 5–10.
5. –Ч–Є–ї–Њ–≤ –Р.–Т., –Я–∞–≤–ї–Њ–≤–∞ –Ь.–У. –Ш–љ–≥–Є–±–Є—В–Њ—А—Л –і–Є–њ–µ–њ—В–Є–і–Є–ї–њ–µ–њ—В–Є–і–∞–Ј—Л–4 –≤ —А—Г—В–Є–љ–љ–Њ–є –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Њ–є –њ—А–∞–Ї—В–Є–Ї–µ – –Њ—Ж–µ–љ–Ї–∞ —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В–Є –Є –±–µ–Ј–Њ–њ–∞—Б–љ–Њ—Б—В–Є —А–∞–Ј–љ—Л—Е —А–µ–ґ–Є–Љ–Њ–≤ —В–µ—А–∞–њ–Є–Є // –Ы–µ—З–∞—Й–Є–є –≤—А–∞—З. – 2012.– вДЦ 3.– –°.87–90.
6. Monami M., Luzzi C., Chiasserini V. et al. Three–year mortality in diabetic patients treated with different combinations of insulin secretagogues and metformin // Diabet. Metab. Res. Rev. – 2006. – Vol. 22. – P. 477.
7. Garber A.J., Donovan D.S. Jr, Bruce S., Park J.S. Efficacy of glyburide/metformin tablets compared with initial monotherapy in type 2 diabetes // J. Clin. Endocrinol. Metab. – 2003. – Vol. 88. – P. 3598–3604.
8. –Ь–Ї—А—В—Г–Љ—П–љ –Р.–Ь., –С–Є—А—О–Ї–Њ–≤–∞ –Х.–Т. –°–∞—Е–∞—А–љ—Л–є –і–Є–∞–±–µ—В 2 —В–Є–њ–∞: –ї–µ—З–µ–љ–Є–µ –≤ –њ–Њ–ґ–Є–ї–Њ–Љ –≤–Њ–Ј—А–∞—Б—В–µ // –†–Ь–Ц. – 2005. – вДЦ 27. – –°.– 1838–1842.












