–°–Њ–≥–ї–∞—Б–љ–Њ –Ї—А–Є—В–µ—А–Є—П–Љ, –Ї–Њ—В–Њ—А—Л–µ –±—Л–ї–Є —А–∞–Ј—А–∞–±–Њ—В–∞–љ—Л –Ї–Њ–Љ–Є—В–µ—В–Њ–Љ —Н–Ї—Б–њ–µ—А—В–Њ–≤ –Э–∞—Ж–Є–Њ–љ–∞–ї—М–љ–Њ–є –Њ–±—А–∞–Ј–Њ–≤–∞—В–µ–ї—М–љ–Њ–є –њ—А–Њ–≥—А–∞–Љ–Љ—Л –њ–Њ —Е–Њ–ї–µ—Б—В–µ—А–Є–љ—Г (ATPIII, 2001 –≥.), –і–Є–∞–≥–љ–Њ–Ј –Ь–° —Г—Б—В–∞–љ–∞–≤–ї–Є–≤–∞–µ—В—Б—П, –µ—Б–ї–Є —Г –њ–∞—Ж–Є–µ–љ—В–∞ –Њ–±–љ–∞—А—Г–ґ–Є–≤–∞–µ—В—Б—П —В—А–Є –Є –±–Њ–ї–µ–µ –Є–Ј —Б–ї–µ–і—Г—О—Й–Є—Е –њ—А–Є–Ј–љ–∞–Ї–Њ–≤ [30]:
• –∞–±–і–Њ–Љ–Є–љ–∞–ї—М–љ–Њ–µ –Њ–ґ–Є—А–µ–љ–Є–µ (–Ю–Ґ>102 —Б–Љ —Г –Љ—Г–ґ—З–Є–љ, –Ю–Ґ>88 —Г –ґ–µ–љ—Й–Є–љ);
• —Г—А–Њ–≤–µ–љ—М —В—А–Є–≥–ї–Є—Ж–µ—А–Є–і–Њ–≤ >1,7 –Љ–Љ–Њ–ї—М/–ї (>150 –Љ–≥/–і–ї);
• –•–° –Ы–Я–Т–Я <1 –Љ–Љ–Њ–ї—М/–ї (<40 –Љ–≥/–і–ї) —Г –Љ—Г–ґ—З–Є–љ, <1,3 –Љ–Љ–Њ–ї—М/–ї (< 50 –Љ–≥/–і–ї) —Г –ґ–µ–љ—Й–Є–љ;
• –Р—А—В–µ—А–Є–∞–ї—М–љ–∞—П –≥–Є–њ–µ—А—В–µ–љ–Ј–Є—П (–Р–Ф>130/85 –Љ–Љ —А—В.—Б—В.);
• –њ–Њ–Ї–∞–Ј–∞—В–µ–ї–Є –≥–ї—О–Ї–Њ–Ј—Л –љ–∞—В–Њ—Й–∞–Ї >6,1 –Љ–Љ–Њ–ї—М/–ї (>110 –Љ–≥/–і–ї).
–Э–Њ–≤–∞—П —А–µ–і–∞–Ї—Ж–Є—П –Њ–њ—А–µ–і–µ–ї–µ–љ–Є—П –Ь–° —Г –ї–Є—Ж –±–µ–ї–Њ–є —А–∞—Б—Л –±—Л–ї–∞ –њ—А–µ–і—Б—В–∞–≤–ї–µ–љ–∞ –Ь–µ–ґ–і—Г–љ–∞—А–Њ–і–љ–Њ–є –§–µ–і–µ—А–∞—Ж–Є–µ–є –і–Є–∞–±–µ—В–∞ –≤ 2005 –≥–Њ–і—Г [31] (—В–∞–±–ї. 1).
–Ю–і–љ–∞–Ї–Њ —Б–ї–µ–і—Г–µ—В –Њ–±—А–∞—В–Є—В—М –≤–љ–Є–Љ–∞–љ–Є–µ, —З—В–Њ —З–µ–ї–Њ–≤–µ–Ї –Љ–Њ–ґ–µ—В –Є–Љ–µ—В—М –Ь–° –Є –њ—А–Є –љ–µ–Ј–љ–∞—З–Є—В–µ–ї—М–љ–Њ–Љ –Є–Ј–±—Л—В–Ї–µ –Љ–∞—Б—Б—Л —В–µ–ї–∞ (–Є–ї–Є –њ—А–Є –µ–≥–Њ –Њ—В—Б—Г—В—Б—В–≤–Є–Є) –≤ —Б–ї—Г—З–∞–µ –Њ–±–љ–∞—А—Г–ґ–µ–љ–Є—П 3 –і—А—Г–≥–Є—Е –Ї–Њ–Љ–њ–Њ–љ–µ–љ—В–Њ–≤ —Б–Є–љ–і—А–Њ–Љ–∞. –Я—А–∞–Ї—В–Є—З–µ—Б–Ї–Є –≤—Б–µ –Ї–Њ–Љ–њ–Њ–љ–µ–љ—В—Л, —Б–Њ—Б—В–∞–≤–ї—П—О—Й–Є–µ –Ь–°, —П–≤–ї—П—О—В—Б—П –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є –Ј–љ–∞—З–Є–Љ—Л–Љ–Є —Д–∞–Ї—В–Њ—А–∞–Љ–Є —А–Є—Б–Ї–∞ —А–∞–Ј–≤–Є—В–Є—П —Б–µ—А–і–µ—З–љ–Њ–—Б–Њ—Б—Г–і–Є—Б—В—Л—Е –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є–є, –∞ —Б–Њ—З–µ—В–∞–љ–Є–µ –љ–µ—Б–Ї–Њ–ї—М–Ї–Є—Е –Ї–Њ–Љ–њ–Њ–љ–µ–љ—В–Њ–≤ —Б—Г—Й–µ—Б—В–≤–µ–љ–љ–Њ —Г–≤–µ–ї–Є—З–Є–≤–∞–µ—В –Њ–њ–∞—Б–љ–Њ—Б—В—М –Є—Е —А–∞–Ј–≤–Є—В–Є—П [1,17]. –Ґ–∞–Ї, —А–µ–Ј—Г–ї—М—В–∞—В—Л –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П BOTNIA, –≤–Ї–ї—О—З–Є–≤—И–µ–≥–Њ 4483 –њ–∞—Ж–Є–µ–љ—В–∞, –њ–Њ–Ї–∞–Ј–∞–ї–Є, —З—В–Њ, –≤–µ—А–Њ—П—В–љ–Њ—Б—В—М —А–∞–Ј–≤–Є—В–Є—П –Ш–С–° –Є –Є–љ—Б—Г–ї—М—В–∞ —Г –ї–Є—Ж —Б –Ь–° –≤ 3–3,5 —А–∞–Ј–∞ –≤—Л—И–µ. –Ъ—А–Њ–Љ–µ —В–Њ–≥–Њ, –њ–∞—Ж–Є–µ–љ—В—Л —Б –Ь–° —Г–Љ–Є—А–∞—О—В –≤ —З–µ—В—Л—А–µ —А–∞–Ј–∞ —З–∞—Й–µ, –∞ –њ—А–Є –љ–∞–ї–Є—З–Є–Є —Б–µ—А–і–µ—З–љ–Њ–—Б–Њ—Б—Г–і–Є—Б—В—Л—Е –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є–є – –≤ 5,5 —А–∞–Ј —З–∞—Й–µ –њ–Њ —Б—А–∞–≤–љ–µ–љ–Є—О —Б –њ–∞—Ж–Є–µ–љ—В–∞–Љ–Є, –љ–µ –Є–Љ–µ—О—Й–Є–Љ–Є –і–∞–љ–љ–Њ–≥–Њ —Б–Є–љ–і—А–Њ–Љ–∞ [9].
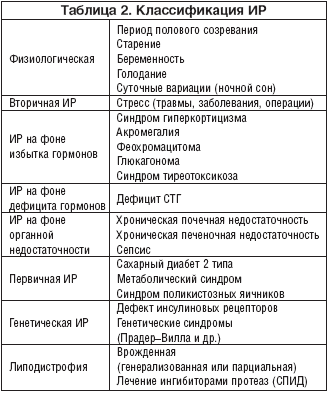
–Я–∞—В–Њ—Д–Є–Ј–Є–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є–Љ –Ј–≤–µ–љ–Њ–Љ, –Њ–±—К–µ–і–Є–љ—П—О—Й–Є–Љ –Ї–Њ–Љ–њ–ї–µ–Ї—Б —А–∞–Ј–ї–Є—З–љ—Л—Е –љ–∞—А—Г—И–µ–љ–Є–є, —А–∞–Ј–≤–Є–≤–∞—О—Й–Є—Е—Б—П –љ–∞ —Д–Њ–љ–µ –Ь–°, —П–≤–ї—П–µ—В—Б—П —А–µ–Ј–Є—Б—В–µ–љ—В–љ–Њ—Б—В—М –Ї –Є–љ—Б—Г–ї–Є–љ—Г. –°—В–µ–њ–µ–љ—М –Ш–† –Ј–∞–≤–Є—Б–Є—В –Њ—В —А—П–і–∞ —Д–∞–Ї—В–Њ—А–Њ–≤, –≤–Ї–ї—О—З–∞—П –≥–µ–љ–µ—В–Є—З–µ—Б–Ї–Є–µ –Њ—Б–Њ–±–µ–љ–љ–Њ—Б—В–Є –Њ—А–≥–∞–љ–Є–Ј–Љ–∞, —Г—Б–ї–Њ–≤–Є—П –≤–љ—Г—В—А–Є—Г—В—А–Њ–±–љ–Њ–≥–Њ —А–∞–Ј–≤–Є—В–Є—П –Є —Б—А–µ–і–Њ–≤—Л–µ –≤–Њ–Ј–і–µ–є—Б—В–≤–Є—П [8,23]. –Ъ —Д–∞–Ї—В–Њ—А–∞–Љ –≤–љ–µ—И–љ–µ–є —Б—А–µ–і—Л, —Б–њ–Њ—Б–Њ–±—Б—В–≤—Г—О—Й–Є–Љ –≤–Њ–Ј–љ–Є–Ї–љ–Њ–≤–µ–љ–Є—О –Ь–°, –Њ—В–љ–Њ—Б—П—В –≤—Л—Б–Њ–Ї–Њ–Ї–∞–ї–Њ—А–Є–є–љ–Њ–µ –њ–Є—В–∞–љ–Є–µ –∞—В–µ—А–Њ–≥–µ–љ–љ–Њ–≥–Њ —Е–∞—А–∞–Ї—В–µ—А–∞, –Є–Ј–±—Л—В–Њ—З–љ—Г—О –Љ–∞—Б—Б—Г —В–µ–ї–∞, —Б—В—А–µ—Б—Б—Л, –≤—А–µ–і–љ—Л–µ –њ—А–Є–≤—Л—З–Ї–Є. –Э–µ–і–Њ—Б—В–∞—В–Њ—З–љ–∞—П —Д–Є–Ј–Є—З–µ—Б–Ї–∞—П –∞–Ї—В–Є–≤–љ–Њ—Б—В—М —Б–њ–Њ—Б–Њ–±—Б—В–≤—Г–µ—В —А–∞–Ј–≤–Є—В–Є—О –Њ–ґ–Є—А–µ–љ–Є—П –Є —Б–љ–Є–ґ–∞–µ—В —З—Г–≤—Б—В–≤–Є—В–µ–ї—М–љ–Њ—Б—В—М —Б–Ї–µ–ї–µ—В–љ—Л—Е –Љ—Л—И—Ж –Ї –Є–љ—Б—Г–ї–Є–љ—Г. –Т –њ–Њ—Б–ї–µ–і–љ–Є–µ –≥–Њ–і—Л –њ–Њ–ї—Г—З–µ–љ—Л –љ–Њ–≤—Л–µ –і–∞–љ–љ—Л–µ –Њ –Љ–µ—Е–∞–љ–Є–Ј–Љ–∞—Е –Ш–† –Є –µ–µ —А–Њ–ї–Є –≤ —А–∞–Ј–≤–Є—В–Є–Є –Љ–љ–Њ–≥–Њ—З–Є—Б–ї–µ–љ–љ—Л—Е –≥–Њ—А–Љ–Њ–љ–∞–ї—М–љ–Њ––Љ–µ—В–∞–±–Њ–ї–Є—З–µ—Б–Ї–Є—Е –љ–∞—А—Г—И–µ–љ–Є–є, —Е–∞—А–∞–Ї—В–µ—А–љ—Л—Е –і–ї—П –і–∞–љ–љ–Њ–≥–Њ —Б–Є–љ–і—А–Њ–Љ–∞. –Ш–† –Љ–Њ–ґ–µ—В –±—Л—В—М –Ї–∞–Ї –≥–µ–љ–µ—В–Є—З–µ—Б–Ї–Є –і–µ—В–µ—А–Љ–Є–љ–Є—А–Њ–≤–∞–љ–љ–Њ–є, —В–∞–Ї –Є –њ—А–Є–Њ–±—А–µ—В–µ–љ–љ–Њ–є. –Т –љ–∞—Б—В–Њ—П—Й–µ–µ –≤—А–µ–Љ—П –Є–Ј–≤–µ—Б—В–љ–Њ –±–Њ–ї–µ–µ 40 —А–∞–Ј–ї–Є—З–љ—Л—Е —Б–Њ—Б—В–Њ—П–љ–Є–є –Є –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є–є, –њ—А–Є –Ї–Њ—В–Њ—А—Л—Е —А–∞–Ј–≤–Є–≤–∞–µ—В—Б—П –Ш–† (—В–∞–±–ї. 2). –Э–∞—А—П–і—Г —Б —Н—В–Є–Љ —Д–Є–Ј–Є–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–∞—П –Ш–† —Е–∞—А–∞–Ї—В–µ—А–љ–∞ –і–ї—П –њ—Г–±–µ—А—В–∞—В–љ–Њ–≥–Њ –њ–µ—А–Є–Њ–і–∞, –±–µ—А–µ–Љ–µ–љ–љ–Њ—Б—В–Є –Є –њ–Њ–ґ–Є–ї–Њ–≥–Њ –≤–Њ–Ј—А–∞—Б—В–∞.
–Ш–Ј—Г—З–µ–љ–Є–µ –≥–µ–љ–µ—В–Є—З–µ—Б–Ї–Є—Е —Д–∞–Ї—В–Њ—А–Њ–≤ –њ–Њ–Ї–∞–Ј–∞–ї–Њ, —З—В–Њ –Ш–† – —Н—В–Њ –њ–Њ–ї–Є–≥–µ–љ–љ–∞—П –њ–∞—В–Њ–ї–Њ–≥–Є—П, –і–ї—П —А–∞–Ј–≤–Є—В–Є—П –Ї–Њ—В–Њ—А–Њ–є –Љ–Њ–≥—Г—В –Є–Љ–µ—В—М –Ј–љ–∞—З–µ–љ–Є–µ –Љ—Г—В–∞—Ж–Є–Є –≥–µ–љ–Њ–≤ —Б—Г–±—Б—В—А–∞—В–∞ –Є–љ—Б—Г–ї–Є–љ–Њ–≤–Њ–≥–Њ —А–µ—Ж–µ–њ—В–Њ—А–∞ (IRS–1 –Є IRS–2), –≥–ї–Є–Ї–Њ–≥–µ–љ—Б–Є–љ—В–µ—В–∞–Ј—Л, –≥–µ–Ї—Б–Њ–Ї–Є–љ–∞–Ј—Л II, b3––∞–і—А–µ–љ–Њ—А–µ—Ж–µ–њ—В–Њ—А–Њ–≤, —А–∞–Ј–Њ–±—Й–∞—О—Й–µ–≥–Њ –њ—А–Њ—В–µ–Є–љ–∞ (UCP–1), –∞ —В–∞–Ї–ґ–µ –Љ–Њ–ї–µ–Ї—Г–ї—П—А–љ—Л–µ –і–µ—Д–µ–Ї—В—Л –±–µ–ї–Ї–Њ–≤ —Б–Є–≥–љ–∞–ї—М–љ–Њ–≥–Њ –њ—Г—В–Є –Є–љ—Б—Г–ї–Є–љ–∞ (–≤–љ—Г—В—А–Є–Ї–ї–µ—В–Њ—З–љ—Л–µ —В—А–∞–љ—Б–њ–Њ—А—В–µ—А—Л –≥–ї—О–Ї–Њ–Ј—Л), –±–µ–ї–Ї–Њ–≤, —Б–≤—П–Ј—Л–≤–∞—О—Й–Є—Е –ґ–Є—А–љ—Л–µ –Ї–Є—Б–ї–Њ—В—Л (FABP–II) [18].
–Ш–Ј–≤–µ—Б—В–љ–Њ, —З—В–Њ —З—Г–≤—Б—В–≤–Є—В–µ–ї—М–љ–Њ—Б—В—М —В–Ї–∞–љ–µ–є –Ї –Є–љ—Б—Г–ї–Є–љ—Г —Б–љ–Є–ґ–∞–µ—В—Б—П –±–Њ–ї–µ–µ —З–µ–Љ –љ–∞ 40% –њ—А–Є –њ—А–µ–≤—Л—И–µ–љ–Є–Є –Є–і–µ–∞–ї—М–љ–Њ–≥–Њ –≤–µ—Б–∞ –љ–∞ 35–40%. –Т–Љ–µ—Б—В–µ —Б —В–µ–Љ –Ш–† –Њ–њ—А–µ–і–µ–ї—П–µ—В—Б—П —Е–∞—А–∞–Ї—В–µ—А–Њ–Љ —А–∞—Б–њ—А–µ–і–µ–ї–µ–љ–Є—П –ґ–Є—А–Њ–≤–Њ–є —В–Ї–∞–љ–Є –≤ –Њ—А–≥–∞–љ–Є–Ј–Љ–µ. –Т–∞–ґ–љ—Г—О —А–Њ–ї—М –≤ —А–∞–Ј–≤–Є—В–Є–Є –Є –њ—А–Њ–≥—А–µ—Б—Б–Є—А–Њ–≤–∞–љ–Є–Є –Ш–† –Є–≥—А–∞–µ—В –Є–Љ–µ–љ–љ–Њ –≤–Є—Б—Ж–µ—А–∞–ї—М–љ–∞—П –ґ–Є—А–Њ–≤–∞—П —В–Ї–∞–љ—М, —Б–Њ—Б—В–∞–≤–ї—П—О—Й–∞—П –Њ–Ї–Њ–ї–Њ 6–20% –Њ–±—Й–µ–є –Љ–∞—Б—Б—Л —В–µ–ї–∞. –Р–і–Є–њ–Њ—Ж–Є—В—Л –≤–Є—Б—Ж–µ—А–∞–ї—М–љ–Њ–≥–Њ, –≤ –Њ—В–ї–Є—З–Є–µ –Њ—В –њ–Њ–і–Ї–Њ–ґ–љ–Њ–≥–Њ –ґ–Є—А–∞, –Є–Љ–µ—О—В –≤—Л—Б–Њ–Ї—Г—О –њ–ї–Њ—В–љ–Њ—Б—В—М –Є —З—Г–≤—Б—В–≤–Є—В–µ–ї—М–љ–Њ—Б—В—М b––∞–і—А–µ–љ–Њ—А–µ—Ж–µ–њ—В–Њ—А–Њ–≤, –Ї–Њ—А—В–Є–Ј–Њ–ї–∞, –∞ —В–∞–Ї–ґ–µ –љ–Є–Ј–Ї—Г—О –њ–ї–Њ—В–љ–Њ—Б—В—М –Є —З—Г–≤—Б—В–≤–Є—В–µ–ї—М–љ–Њ—Б—В—М –Є–љ—Б—Г–ї–Є–љ–Њ–≤—Л—Е —А–µ—Ж–µ–њ—В–Њ—А–Њ–≤ [1,13]. –Ю–њ–Є—Б–∞–љ–љ—Л–µ –Љ–µ—В–∞–±–Њ–ї–Є—З–µ—Б–Ї–Є–µ –њ—А–Є–Ј–љ–∞–Ї–Є –Њ–њ—А–µ–і–µ–ї—П—О—В –њ–Њ–≤—Л—И–µ–љ–љ—Г—О —З—Г–≤—Б—В–≤–Є—В–µ–ї—М–љ–Њ—Б—В—М –≤–Є—Б—Ж–µ—А–∞–ї—М–љ—Л—Е –∞–і–Є–њ–Њ—Ж–Є—В–Њ–≤ –Ї –ї–Є–њ–Њ–ї–Є—В–Є—З–µ—Б–Ї–Є–Љ –≤–Њ–Ј–і–µ–є—Б—В–≤–Є—П–Љ, –Є –љ–∞–Њ–±–Њ—А–Њ—В, –љ–Є–Ј–Ї—Г—О – –Ї –∞–љ—В–Є–ї–Є–њ–Њ–ї–Є—В–Є—З–µ—Б–Ї–Њ–Љ—Г —Н—Д—Д–µ–Ї—В—Г –Є–љ—Б—Г–ї–Є–љ–∞. –Ъ—А–Њ–Љ–µ —В–Њ–≥–Њ, —Ж–Є—В–Њ–Ї–Є–љ—Л, —Б–µ–Ї—А–µ—В–Є—А—Г–µ–Љ—Л–µ –≤–Є—Б—Ж–µ—А–∞–ї—М–љ—Л–Љ–Є –∞–і–Є–њ–Њ—Ж–Є—В–∞–Љ–Є, –≤—Б–ї–µ–і—Б—В–≤–Є–µ –∞–љ–∞—В–Њ–Љ–Њ–—В–Њ–њ–Њ–≥—А–∞—Д–Є—З–µ—Б–Ї–Є—Е –Њ—Б–Њ–±–µ–љ–љ–Њ—Б—В–µ–є –њ–Њ—Б—В—Г–њ–∞—О—В –њ—А–µ–Є–Љ—Г—Й–µ—Б—В–≤–µ–љ–љ–Њ –≤ –њ–Њ—А—В–∞–ї—М–љ—Г—О —Б–Є—Б—В–µ–Љ—Г. –Т –Њ—В–ї–Є—З–Є–µ –Њ—В —Н—В–Њ–≥–Њ, –∞–і–Є–њ–Њ—Ж–Є—В–Њ–Ї–Є–љ—Л –Є–Ј –њ–Њ–і–Ї–Њ–ґ–љ—Л—Е –ґ–Є—А–Њ–≤—Л—Е –і–µ–њ–Њ –њ–Њ—Б—В—Г–њ–∞—О—В —Б—А–∞–Ј—Г –≤ —Б–Є—Б—В–µ–Љ–љ—Л–є –Ї—А–Њ–≤–Њ—В–Њ–Ї. –°–ї–µ–і–Њ–≤–∞—В–µ–ї—М–љ–Њ, –≤–Є—Б—Ж–µ—А–∞–ї—М–љ–∞—П –ґ–Є—А–Њ–≤–∞—П —В–Ї–∞–љ—М –Њ–Ї–∞–Ј—Л–≤–∞–µ—В –Ј–љ–∞—З–Є—В–µ–ї—М–љ–Њ–µ –≤–ї–Є—П–љ–Є–µ –љ–∞ –Љ–µ—В–∞–±–Њ–ї–Є—З–µ—Б–Ї–Є–µ –њ—А–Њ—Ж–µ—Б—Б—Л, –њ—А–Њ–Є—Б—Е–Њ–і—П—Й–Є–µ –≤ –њ–µ—З–µ–љ–Є. –Ю–і–љ–∞–Ї–Њ —В–Њ—З–љ—Л–µ –Љ–µ—Е–∞–љ–Є–Ј–Љ—Л, –ї–µ–ґ–∞—Й–Є–µ –≤ –Њ—Б–љ–Њ–≤–µ –≤–Ј–∞–Є–Љ–Њ—Б–≤—П–Ј–Є –Љ–µ–ґ–і—Г –≤–Є—Б—Ж–µ—А–Њ––∞–±–і–Њ–Љ–Є–љ–∞–ї—М–љ—Л–Љ –Њ–ґ–Є—А–µ–љ–Є–µ–Љ –Є –Ь–°, –Њ–Ї–Њ–љ—З–∞—В–µ–ї—М–љ–Њ –љ–µ —П—Б–љ—Л, –Є, –≤–µ—А–Њ—П—В–љ–Њ, —Б–ї–Њ–ґ–љ—Л.
–Ш–љ—В–µ–љ—Б–Є–≤–љ—Л–є –ї–Є–њ–Њ–ї–Є–Ј –≤ —Г—Б–ї–Њ–≤–Є—П—Е –Є–Ј–±—Л—В–Њ—З–љ–Њ–≥–Њ –Њ—В–ї–Њ–ґ–µ–љ–Є—П –≤–Є—Б—Ж–µ—А–∞–ї—М–љ–Њ–≥–Њ, –Є–љ—В—А–∞–∞–±–і–Њ–Љ–Є–љ–∞–ї—М–љ–Њ–≥–Њ –ґ–Є—А–∞ –њ—А–Є–≤–Њ–і–Є—В –Ї –њ–Њ–≤—Л—И–µ–љ–љ–Њ–є –Љ–Њ–±–Є–ї–Є–Ј–∞—Ж–Є–Є —Б–≤–Њ–±–Њ–і–љ—Л—Е –ґ–Є—А–љ—Л—Е –Ї–Є—Б–ї–Њ—В (–°–Ц–Ъ) –Є–Ј –ґ–Є—А–Њ–≤–Њ–є —В–Ї–∞–љ–Є, –Ї–Њ–љ—Ж–µ–љ—В—А–∞—Ж–Є—П –Ї–Њ—В–Њ—А—Л—Е –Љ–Њ–ґ–µ—В –≤ 20–30 —А–∞–Ј –њ—А–µ–≤—Л—И–∞—В—М –Є—Е –Ї–Њ–љ—Ж–µ–љ—В—А–∞—Ж–Є—О, –љ–∞–±–ї—О–і–∞–µ–Љ—Г—О –њ—А–Є –Њ—В—Б—Г—В—Б—В–≤–Є–Є –≤–Є—Б—Ж–µ—А–∞–ї—М–љ–Њ–≥–Њ –Њ–ґ–Є—А–µ–љ–Є—П [7,13]. –°–Ц–Ъ —П–≤–ї—П—О—В—Б—П –≤–∞–ґ–љ–Њ–є –і–µ—В–µ—А–Љ–Є–љ–∞–љ—В–Њ–є —А–∞–Ј–≤–Є—В–Є—П –Љ–љ–Њ–≥–Њ—З–Є—Б–ї–µ–љ–љ—Л—Е –Љ–µ—В–∞–±–Њ–ї–Є—З–µ—Б–Ї–Є—Е –љ–∞—А—Г—И–µ–љ–Є–є. –Я–Њ—Б—В—Г–њ–∞—П —З–µ—А–µ–Ј —Б–Є—Б—В–µ–Љ—Г –≤–Њ—А–Њ—В–љ–Њ–є –≤–µ–љ—Л –≤ –њ–µ—З–µ–љ—М, –°–Ц–Ъ –Є—Б–њ–Њ–ї—М–Ј—Г—О—В—Б—П –њ–µ—З–µ–љ—М—О –Ї–∞–Ї —Б—Г–±—Б—В—А–∞—В—Л –і–ї—П –Њ–±—А–∞–Ј–Њ–≤–∞–љ–Є—П –Ґ–У, —З—В–Њ –Њ–±—К—П—Б–љ—П–µ—В –≥–Є–њ–µ—А—В—А–Є–≥–ї–Є—Ж–µ—А–Є–і–µ–Љ–Є—О – —Е–∞—А–∞–Ї—В–µ—А–љ—Л–є –њ—А–Є–Ј–љ–∞–Ї –Ь–°. –Ъ—А–Њ–Љ–µ —В–Њ–≥–Њ, –њ–Њ–≤—Л—И–µ–љ–љ—Л–µ –Ї–Њ–љ—Ж–µ–љ—В—А–∞—Ж–Є–Є –°–Ц–Ъ —Г—Б—Г–≥—Г–±–ї—П—О—В –њ–µ—А–Є—Д–µ—А–Є—З–µ—Б–Ї—Г—О –Ш–†, –∞ –Ї–Њ–Љ–њ–µ–љ—Б–∞—В–Њ—А–љ–∞—П –≥–Є–њ–µ—А–Є–љ—Б—Г–ї–Є–љ–µ–Љ–Є—П (–У–Ш) —Б–њ–Њ—Б–Њ–±—Б—В–≤—Г–µ—В –µ—Й–µ –±–Њ–ї—М—И–µ–Љ—Г —Г–≤–µ–ї–Є—З–µ–љ–Є—О –Љ–∞—Б—Б—Л —В–µ–ї–∞ –±–Њ–ї—М–љ—Л—Е –Ь–°. –Ш–Ј–≤–µ—Б—В–љ–Њ, —З—В–Њ –њ–Њ–≤—Л—И–µ–љ–Є–µ —Г—А–Њ–≤–љ—П –°–Ц–Ъ –≤–µ–і–µ—В –Ї –њ–Њ–і–∞–≤–ї–µ–љ–Є—О –њ—А–Њ—Ж–µ—Б—Б–Њ–≤ —В—А–∞–љ—Б–њ–Њ—А—В–∞ –Є —Д–Њ—Б—Д–Њ—А–Є–ї–Є—А–Њ–≤–∞–љ–Є—П –≥–ї—О–Ї–Њ–Ј—Л –Є, –Ї–∞–Ї —Б–ї–µ–і—Б—В–≤–Є–µ, –Ї —Б–љ–Є–ґ–µ–љ–Є—О –Њ–Ї–Є—Б–ї–µ–љ–Є—П –≥–ї—О–Ї–Њ–Ј—Л –Є —Б–Є–љ—В–µ–Ј–∞ –≥–ї–Є–Ї–Њ–≥–µ–љ–∞ –≤ –Љ—Л—И—Ж–∞—Е. –£–Љ–µ–љ—М—И–µ–љ–Є–µ —З—Г–≤—Б—В–≤–Є—В–µ–ї—М–љ–Њ—Б—В–Є –њ–µ—З–µ–љ–Є –Ї –і–µ–є—Б—В–≤–Є—О –Є–љ—Б—Г–ї–Є–љ–∞ —В–∞–Ї–ґ–µ –≤–µ–і–µ—В –Ї —Б–љ–Є–ґ–µ–љ–Є—О —Б–Є–љ—В–µ–Ј–∞ –≥–ї–Є–Ї–Њ–≥–µ–љ–∞, —Г—Б–Є–ї–µ–љ–Є—О –≥–ї–Є–Ї–Њ–≥–µ–љ–Њ–ї–Є–Ј–∞ –Є –≥–ї—О–Ї–Њ–љ–µ–Њ–≥–µ–љ–µ–Ј–∞.
–Т —Г—Б–ї–Њ–≤–Є—П—Е –Ш–† –Є –У–Ш —Д–Њ—А–Љ–Є—А—Г–µ—В—Б—П –∞—В–µ—А–Њ–≥–µ–љ–љ–∞—П –і–Є—Б–ї–Є–њ–Є–і–µ–Љ–Є—П, —Е–∞—А–∞–Ї—В–µ—А–Є–Ј—Г—О—Й–∞—П—Б—П –≥–Є–њ–µ—А—В—А–Є–≥–ї–Є—Ж–µ—А–Є–і–µ–Љ–Є–µ–є, –њ–Њ–≤—Л—И–µ–љ–Є–µ–Љ —Б–Њ–і–µ—А–ґ–∞–љ–Є—П –•–° –Ы–Я–Э–Я, —Б–љ–Є–ґ–µ–љ–Є–µ–Љ –Ї–Њ–љ—Ж–µ–љ—В—А–∞—Ж–Є–Є –•–° –Ы–Я–Т–Я [19]. –Ш–Ј–≤–µ—Б—В–љ–Њ, —З—В–Њ –≥–Є–њ–µ—А—В—А–Є–≥–ї–Є—Ж–µ—А–Є–і–µ–Љ–Є—П –≤ —Б–Њ—З–µ—В–∞–љ–Є–Є —Б –љ–Є–Ј–Ї–Є–Љ —Г—А–Њ–≤–љ–µ–Љ –•–° –Ы–Я–Т–Я —П–≤–ї—П–µ—В—Б—П –љ–µ–Ј–∞–≤–Є—Б–Є–Љ—Л–Љ –Є —Б—Г—Й–µ—Б—В–≤–µ–љ–љ—Л–Љ —Д–∞–Ї—В–Њ—А–Њ–Љ —А–Є—Б–Ї–∞ –Є–љ—Д–∞—А–Ї—В–∞ –Љ–Є–Њ–Ї–∞—А–і–∞/–Є–љ—Б—Г–ї—М—В–∞ —Г –±–Њ–ї—М–љ—Л—Е –Ь–°. –Ш–Ј–Љ–µ–љ–µ–љ–Є—П –ї–Є–њ–Є–і–љ—Л—Е –њ–∞—А–∞–Љ–µ—В—А–Њ–≤ –Є–Љ–µ—О—В –љ–µ —В–Њ–ї—М–Ї–Њ –Ї–Њ–ї–Є—З–µ—Б—В–≤–µ–љ–љ—Л–є, –љ–Њ –Є –Ї–∞—З–µ—Б—В–≤–µ–љ–љ—Л–є —Е–∞—А–∞–Ї—В–µ—А. –Ґ–∞–Ї, –љ–µ—А–µ–і–Ї–Њ –њ—А–Є –љ–Њ—А–Љ–∞–ї—М–љ–Њ–є –Ї–Њ–љ—Ж–µ–љ—В—А–∞—Ж–Є–Є –•–° –Ы–Я–Э–Я —Г –±–Њ–ї—М–љ—Л—Е —Б –Ь–° —Н—В–Є –ї–Є–њ–Њ–њ—А–Њ—В–µ–Є–і—Л –Є–Љ–µ—О—В –Љ–µ–љ—М—И–Є–є —А–∞–Ј–Љ–µ—А, –±–Њ–ї—М—И—Г—О –њ–ї–Њ—В–љ–Њ—Б—В—М, –ї–µ–≥—З–µ –њ–Њ–і–≤–µ—А–≥–∞—О—В—Б—П –њ–µ—А–µ–Ї–Є—Б–љ–Њ–Љ—Г –Њ–Ї–Є—Б–ї–µ–љ–Є—О –Є –Љ–Є–≥—А–Є—А—Г—О—В –≤ —Б—Г–±—Н–љ–і–Њ—В–µ–ї–Є–∞–ї—М–љ–Њ–µ –њ—А–Њ—Б—В—А–∞–љ—Б—В–≤–Њ, –Є–љ–Є—Ж–Є–Є—А—Г—П –±—Л—Б—В—А–Њ–µ –Њ–±—А–∞–Ј–Њ–≤–∞–љ–Є–µ –∞—В–µ—А–Њ—Б–Ї–ї–µ—А–Њ—В–Є—З–µ—Б–Ї–Њ–є –±–ї—П—И–Ї–Є.
–Я—А–Њ–±–ї–µ–Љ–∞ –ї–µ—З–µ–љ–Є—П –Ь–° –њ–Њ––њ—А–µ–ґ–љ–µ–Љ—Г –Њ—Б—В–∞–µ—В—Б—П –≤ —Ж–µ–љ—В—А–µ –≤–љ–Є–Љ–∞–љ–Є—П –њ—А–∞–Ї—В–Є—З–µ—Б–Ї–Є—Е –≤—А–∞—З–µ–є. –Ю—Б–љ–Њ–≤–љ–∞—П —Ж–µ–ї—М —В–µ—А–∞–њ–Є–Є –±–Њ–ї—М–љ—Л—Е —Б –Ь–° – –Љ–∞–Ї—Б–Є–Љ–∞–ї—М–љ–Њ–µ —Б–љ–Є–ґ–µ–љ–Є–µ —А–Є—Б–Ї–∞ —А–∞–Ј–≤–Є—В–Є—П —Б–µ—А–і–µ—З–љ–Њ–—Б–Њ—Б—Г–і–Є—Б—В—Л—Е –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є–є –Є –Є—Е –Њ—Б–ї–Њ–ґ–љ–µ–љ–Є–є. –Ы–µ—З–µ–љ–Є–µ –Ь–° –≤–Ї–ї—О—З–∞–µ—В –Є–Ј–Љ–µ–љ–µ–љ–Є–µ –Њ–±—А–∞–Ј–∞ –ґ–Є–Ј–љ–Є –Є –і–Є–µ—В–Є—З–µ—Б–Ї–Є–µ —А–µ–Ї–Њ–Љ–µ–љ–і–∞—Ж–Є–Є: —Б–љ–Є–ґ–µ–љ–Є–µ –Ї–∞–ї–Њ—А–Є–є–љ–Њ—Б—В–Є —А–∞—Ж–Є–Њ–љ–∞, –њ–Њ–ї–љ–Њ–µ –Є—Б–Ї–ї—О—З–µ–љ–Є–µ –∞–ї–Ї–Њ–≥–Њ–ї—П, –Њ–≥—А–∞–љ–Є—З–µ–љ–Є–µ –ґ–Є—А–Њ–≤ –ґ–Є–≤–Њ—В–љ–Њ–≥–Њ –њ—А–Њ–Є—Б—Е–Њ–ґ–і–µ–љ–Є—П –Є —Е–Њ–ї–µ—Б—В–µ—А–Є–љ–∞ (–Љ–µ–љ–µ–µ 300 –Љ–≥/—Б—Г—В.), —Г–њ–Њ—В—А–µ–±–ї–µ–љ–Є–µ –њ–Њ–ї–Є–љ–µ–љ–∞—Б—Л—Й–µ–љ–љ—Л—Е –ґ–Є—А–љ—Л—Е –Ї–Є—Б–ї–Њ—В (–≤ —З–∞—Б—В–љ–Њ—Б—В–Є, –Љ–Њ—А—Б–Ї–Њ–є —А—Л–±—Л), –∞–Ї—В–Є–≤–љ—Г—О —Д–Є–Ј–Є—З–µ—Б–Ї—Г—О –љ–∞–≥—А—Г–Ј–Ї—Г (4–5 –Ј–∞–љ—П—В–Є–є –≤ –љ–µ–і–µ–ї—О –њ–Њ 30 –Љ–Є–љ—Г—В –≤ –і–µ–љ—М –њ—А–Є –Њ—В—Б—Г—В—Б—В–≤–Є–Є –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є—Е –њ—А–Є–Ј–љ–∞–Ї–Њ–≤ –Ш–С–°).
–°–Њ–≥–ї–∞—Б–љ–Њ —Б–Њ–≤—А–µ–Љ–µ–љ–љ—Л–Љ —А–µ–Ї–Њ–Љ–µ–љ–і–∞—Ж–Є—П–Љ, –љ–∞—З–∞–ї—М–љ–Њ–µ —Б–љ–Є–ґ–µ–љ–Є–µ –Љ–∞—Б—Б—Л —В–µ–ї–∞ —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –Ь–° –і–Њ–ї–ґ–љ–Њ —Б–Њ—Б—В–∞–≤–ї—П—В—М –љ–µ –Љ–µ–љ–µ–µ 10% –Њ—В –Є—Б—Е–Њ–і–љ–Њ–є –Љ–∞—Б—Б—Л [1]. –°–љ–Є–ґ–µ–љ–Є–µ –Љ–∞—Б—Б—Л —В–µ–ї–∞ –њ–Њ–Ј–≤–Њ–ї—П–µ—В —Г–Љ–µ–љ—М—И–Є—В—М –Ш–†, –∞ —В–∞–Ї–ґ–µ –њ–Њ–ї—Г—З–Є—В—М –њ–Њ–ї–Њ–ґ–Є—В–µ–ї—М–љ—Л–є —Н—Д—Д–µ–Ї—В –≤ –Њ—В–љ–Њ—И–µ–љ–Є–Є –∞—А—В–µ—А–Є–∞–ї—М–љ–Њ–є –≥–Є–њ–µ—А—В–µ–љ–Ј–Є–Є –Є –њ–Њ–Ї–∞–Ј–∞—В–µ–ї–µ–є –ї–Є–њ–Є–і–љ–Њ–≥–Њ —Б–њ–µ–Ї—В—А–∞ –Ї—А–Њ–≤–Є.
–Т–∞–ґ–љ—Л–Љ –љ–∞–њ—А–∞–≤–ї–µ–љ–Є–µ–Љ —Д–∞—А–Љ–∞–Ї–Њ—В–µ—А–∞–њ–Є–Є —П–≤–ї—П–µ—В—Б—П –Ї–Њ—А—А–µ–Ї—Ж–Є—П –Ш–† – –Ї–ї—О—З–µ–≤–Њ–≥–Њ –Ј–≤–µ–љ–∞ –Ь–°. –Т –љ–∞—Б—В–Њ—П—Й–µ–µ –≤—А–µ–Љ—П –Њ–і–љ–Є–Љ –Є–Ј –њ—А–µ–њ–∞—А–∞—В–Њ–≤ –њ–µ—А–≤–Њ–≥–Њ –≤—Л–±–Њ—А–∞ —Д–∞—А–Љ–∞–Ї–Њ—В–µ—А–∞–њ–Є–Є –Ь–° —П–≤–ї—П–µ—В—Б—П –Љ–µ—В—Д–Њ—А–Љ–Є–љ. –°–Њ–≥–ї–∞—Б–љ–Њ —А–µ–Ї–Њ–Љ–µ–љ–і–∞—Ж–Є—П–Љ –Ь–µ–ґ–і—Г–љ–∞—А–Њ–і–љ–Њ–є –§–µ–і–µ—А–∞—Ж–Є–Є –і–Є–∞–±–µ—В–∞ (2005), –Љ–µ—В—Д–Њ—А–Љ–Є–љ —А–µ–Ї–Њ–Љ–µ–љ–і—Г–µ—В—Б—П –≤ –Ї–∞—З–µ—Б—В–≤–µ –њ—А–µ–њ–∞—А–∞—В–∞ –њ–µ—А–≤–Њ–≥–Њ —А—П–і–∞ –і–ї—П –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –°–Ф 2 [31]. –Ь–µ—В—Д–Њ—А–Љ–Є–љ – –њ—А–µ–њ–∞—А–∞—В, –Њ—В–љ–Њ—Б—П—Й–Є–є—Б—П –Ї –≥—А—Г–њ–њ–µ –±–Є–≥—Г–∞–љ–Є–і–Њ–≤, –њ–Њ–≤—Л—И–∞–µ—В –њ–µ—З–µ–љ–Њ—З–љ—Г—О –Є –њ–µ—А–Є—Д–µ—А–Є—З–µ—Б–Ї—Г—О —З—Г–≤—Б—В–≤–Є—В–µ–ї—М–љ–Њ—Б—В—М –Ї —Н–љ–і–Њ–≥–µ–љ–љ–Њ–Љ—Г –Є–љ—Б—Г–ї–Є–љ—Г, –љ–µ –≤–ї–Є—П—П –љ–∞ –µ–≥–Њ —Б–µ–Ї—А–µ—Ж–Є—О [13,17]. –§–∞—А–Љ–∞–Ї–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є–µ —Н—Д—Д–µ–Ї—В—Л –Љ–µ—В—Д–Њ—А–Љ–Є–љ–∞ – —Н—В–Њ —А–µ–Ј—Г–ї—М—В–∞—В –≤–Њ–Ј–і–µ–є—Б—В–≤–Є—П –њ—А–µ–њ–∞—А–∞—В–∞ –љ–∞ —З—Г–≤—Б—В–≤–Є—В–µ–ї—М–љ–Њ—Б—В—М –Ї –Є–љ—Б—Г–ї–Є–љ—Г –љ–∞ —Г—А–Њ–≤–љ–µ –њ–µ—З–µ–љ–Є, –Љ—Л—И–µ—З–љ–Њ–є –Є –ґ–Є—А–Њ–≤–Њ–є —В–Ї–∞–љ–µ–є. –•–Њ—В—П –њ—А–µ–Њ–±–ї–∞–і–∞—О—Й–Є–Љ —П–≤–ї—П–µ—В—Б—П –≤–ї–Є—П–љ–Є–µ –Љ–µ—В—Д–Њ—А–Љ–Є–љ–∞ –љ–∞ –њ—А–Њ–і—Г–Ї—Ж–Є—О –≥–ї—О–Ї–Њ–Ј—Л –њ–µ—З–µ–љ—М—О, –Є–Љ–µ–љ–љ–Њ –Ї–Њ–Љ–±–Є–љ–∞—Ж–Є—П –µ–≥–Њ —Н—Д—Д–µ–Ї—В–Њ–≤ –љ–∞ —Г—А–Њ–≤–љ–µ –≤—Б–µ—Е —В—А–µ—Е —В–Ї–∞–љ–µ–є, –њ–Њ––≤–Є–і–Є–Љ–Њ–Љ—Г, –Њ–±—Г—Б–ї–Њ–≤–ї–Є–≤–∞–µ—В –±–ї–∞–≥–Њ–њ—А–Є—П—В–љ—Л–є —Д–∞—А–Љ–∞–Ї–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є–є –њ—А–Њ—Д–Є–ї—М –њ—А–µ–њ–∞—А–∞—В–∞.
–Ю—Б–љ–Њ–≤–љ—Л–Љ –Љ–µ—Е–∞–љ–Є–Ј–Љ–Њ–Љ –і–µ–є—Б—В–≤–Є—П –Љ–µ—В—Д–Њ—А–Љ–Є–љ–∞ —П–≤–ї—П–µ—В—Б—П —Б–љ–Є–ґ–µ–љ–Є–µ –њ—А–Њ–і—Г–Ї—Ж–Є–Є –≥–ї—О–Ї–Њ–Ј—Л –њ–µ—З–µ–љ—М—О [14]. –Ґ–∞–Ї–Њ–є –Љ–µ—Е–∞–љ–Є–Ј–Љ –і–µ–є—Б—В–≤–Є—П –њ—А–µ–њ–∞—А–∞—В–∞ –≤ –Њ—Б–љ–Њ–≤–љ–Њ–Љ —Б–≤—П–Ј–∞–љ —Б –њ–Њ–і–∞–≤–ї–µ–љ–Є–µ–Љ –њ—А–Њ—Ж–µ—Б—Б–Њ–≤ –≥–ї—О–Ї–Њ–љ–µ–Њ–≥–µ–љ–µ–Ј–∞ –Є –≤ –Љ–µ–љ—М—И–µ–є —Б—В–µ–њ–µ–љ–Є –≥–ї–Є–Ї–Њ–≥–µ–љ–Њ–ї–Є–Ј–∞.
–Э–∞—А—П–і—Г —Б —Н—В–Є–Љ, –њ–Њ–і –≤–ї–Є—П–љ–Є–µ–Љ –Љ–µ—В—Д–Њ—А–Љ–Є–љ–∞ —Г–ї—Г—З—И–∞–µ—В—Б—П —З—Г–≤—Б—В–≤–Є—В–µ–ї—М–љ–Њ—Б—В—М –Ї –Є–љ—Б—Г–ї–Є–љ—Г —Б–Ї–µ–ї–µ—В–љ—Л—Е –Љ—Л—И—Ж –Є –ґ–Є—А–Њ–≤–Њ–є —В–Ї–∞–љ–Є, —З—В–Њ —А–µ–∞–ї–Є–Ј—Г–µ—В—Б—П –њ–Њ—Б—А–µ–і—Б—В–≤–Њ–Љ —А—П–і–∞ –Ї–ї–µ—В–Њ—З–љ—Л—Е –Љ–µ—Е–∞–љ–Є–Ј–Љ–Њ–≤ [15,21]. –£—Б–Є–ї–Є–≤–∞—П –Ї—А–Њ–≤–Њ–Њ–±—А–∞—Й–µ–љ–Є–µ –≤ –њ–µ—З–µ–љ–Є –Є —Г—Б–Ї–Њ—А—П—П –њ—А–Њ—Ж–µ—Б—Б –њ—А–µ–≤—А–∞—Й–µ–љ–Є—П –≥–ї—О–Ї–Њ–Ј—Л –≤ –≥–ї–Є–Ї–Њ–≥–µ–љ, –Љ–µ—В—Д–Њ—А–Љ–Є–љ —Г–≤–µ–ї–Є—З–Є–≤–∞–µ—В —Б–Є–љ—В–µ–Ј –≥–ї–Є–Ї–Њ–≥–µ–љ–∞ –≤ –њ–µ—З–µ–љ–Є [14].
–Я—А–µ–њ–∞—А–∞—В –Ј–∞–Љ–µ–і–ї—П–µ—В –њ—А–Њ—Ж–µ—Б—Б—Л –≤—Б–∞—Б—Л–≤–∞–љ–Є—П —Г–≥–ї–µ–≤–Њ–і–Њ–≤ –≤ –ґ–µ–ї—Г–і–Њ—З–љ–Њ––Ї–Є—И–µ—З–љ–Њ–Љ —В—А–∞–Ї—В–µ, –∞ —В–∞–Ї–ґ–µ –Њ–±–ї–∞–і–∞–µ—В –∞–љ–Њ—А–µ–Ї—Б–Є–≥–µ–љ–љ—Л–Љ–Є —Б–≤–Њ–є—Б—В–≤–∞–Љ–Є [14,22]. –Я–Њ–ї–∞–≥–∞—О—В, —З—В–Њ –Њ–і–Є–љ –Є–Ј –Љ–µ—Е–∞–љ–Є–Ј–Љ–Њ–≤ –∞–љ–Њ—А–µ–Ї—Б–Є–≥–µ–љ–љ–Њ–≥–Њ –і–µ–є—Б—В–≤–Є—П –Љ–µ—В—Д–Њ—А–Љ–Є–љ–∞ —Б–≤—П–Ј–∞–љ —Б –µ–≥–Њ –≤–ї–Є—П–љ–Є–µ–Љ –љ–∞ –Љ–µ—В–∞–±–Њ–ї–Є–Ј–Љ –≥–ї—О–Ї–Њ–≥–Њ–љ–Њ–њ–Њ–і–Њ–±–љ–Њ–≥–Њ –њ–µ–њ—В–Є–і–∞–1 (–У–Я–Я–1). –Ґ–∞–Ї, –≤ —А–∞–±–Њ—В–µ Mannucci E. –Є —Б–Њ–∞–≤—В. –Њ–њ—А–µ–і–µ–ї—П–ї–Є —Г—А–Њ–≤–љ–Є –У–Я–Я–1 (7–36)–∞–Љ–Є–і–∞/(7–37) –Є—Б—Е–Њ–і–љ–Њ –Є —З–µ—А–µ–Ј 15 –і–љ–µ–є —В–µ—А–∞–њ–Є–Є –Љ–µ—В—Д–Њ—А–Љ–Є–љ–Њ–Љ (2550 –Љ–≥/—Б—Г—В.) —Г –±–Њ–ї—М–љ—Л—Е —Б –Њ–ґ–Є—А–µ–љ–Є–µ–Љ –і–Њ –Є –њ–Њ—Б–ї–µ –љ–∞–≥—А—Г–Ј–Ї–Є –У–Ґ–Ґ [20]. –° —Ж–µ–ї—М—О —Г—Б—В—А–∞–љ–µ–љ–Є—П –≤–ї–Є—П–љ–Є—П –Є–љ—Б—Г–ї–Є–љ–µ–Љ–Є–Є –Є –≥–ї–Є–Ї–µ–Љ–Є–Є –љ–∞ —Б–µ–Ї—А–µ—Ж–Є—О –У–Я–Я–1 –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ –њ—А–Њ–≤–Њ–і–Є–ї–Њ—Б—М –≤ —Г—Б–ї–Њ–≤–Є—П—Е —Н—Г–≥–ї–Є–Ї–µ–Љ–Є—З–µ—Б–Ї–Њ–≥–Њ –≥–Є–њ–µ—А–Є–љ—Б—Г–ї–Є–љ–µ–Љ–Є—З–µ—Б–Ї–Њ–≥–Њ –Ї–ї—Н–Љ–њ–∞. –Р–≤—В–Њ—А—Л –љ–µ –Њ–±–љ–∞—А—Г–ґ–Є–ї–Є –Є–Ј–Љ–µ–љ–µ–љ–Є–є –Ї–Њ–љ—Ж–µ–љ—В—А–∞—Ж–Є–є –У–Я–Я–1 —Г –ї–Є—Ж –Ї–Њ–љ—В—А–Њ–ї—М–љ–Њ–є –≥—А—Г–њ–њ—Л. –Т–Љ–µ—Б—В–µ —Б —В–µ–Љ —Г –±–Њ–ї—М–љ—Л—Е —Б –Њ–ґ–Є—А–µ–љ–Є–µ–Љ –Љ–µ—В—Д–Њ—А–Љ–Є–љ –≤—Л–Ј—Л–≤–∞–ї —Б—Г—Й–µ—Б—В–≤–µ–љ–љ–Њ–µ —Г–≤–µ–ї–Є—З–µ–љ–Є–µ –Ї–Њ–љ—Ж–µ–љ—В—А–∞—Ж–Є–Є –У–Я–Я–1 (7–36)–∞–Љ–Є–і–∞/(7–37) –љ–∞ 30 –Є 60 –Љ–Є–љ—Г—В–∞—Е —В–µ—Б—В–∞ –њ—А–Є –љ–µ–Є–Ј–Љ–µ–љ–µ–љ–љ–Њ–Љ –±–∞–Ј–∞–ї—М–љ–Њ–Љ —Г—А–Њ–≤–љ–µ –њ–µ–њ—В–Є–і–∞. –Т —Б–Љ–µ—И–∞–љ–љ–Њ–є –њ–ї–∞–Ј–Љ–µ (–њ–Њ—Б–ї–µ 30 –Љ–Є–љ. –Є–љ–Ї—Г–±–∞—Ж–Є–Є –њ—А–Є 37°–°), –∞ —В–∞–Ї–ґ–µ –≤ —А–∞—Б—В–≤–Њ—А–µ –±—Г—Д–µ—А–∞, —Б–Њ–і–µ—А–ґ–∞—Й–µ–Љ –і–Є–њ–µ–њ—В–Є–і–Є–ї––њ–µ–њ—В–Є–і–∞–Ј—Г–4, –Љ–µ—В—Д–Њ—А–Љ–Є–љ –Є–љ–≥–Є–±–Є—А–Њ–≤–∞–ї –і–µ–≥—А–∞–і–∞—Ж–Є—О –У–Я–Я–1.
–Т–∞–ґ–љ—Л–Љ —Н—Д—Д–µ–Ї—В–Њ–Љ –Љ–µ—В—Д–Њ—А–Љ–Є–љ–∞ —П–≤–ї—П–µ—В—Б—П —Г–Љ–µ–љ—М—И–µ–љ–Є–µ –Є–ї–Є —Б—В–∞–±–Є–ї–Є–Ј–∞—Ж–Є—П –Љ–∞—Б—Б—Л —В–µ–ї–∞, –∞ —В–∞–Ї–ґ–µ —Б–љ–Є–ґ–µ–љ–Є–µ –Њ—В–ї–Њ–ґ–µ–љ–Є—П –≤–Є—Б—Ж–µ—А–∞–ї—М–љ–Њ–≥–Њ –ґ–Є—А–∞. –°–Њ–≥–ї–∞—Б–љ–Њ —А–µ–Ј—Г–ї—М—В–∞—В–∞–Љ —Н–Ї—Б–њ–µ—А–Є–Љ–µ–љ—В–∞–ї—М–љ—Л—Е –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–є –љ–∞ –ґ–Є–≤–Њ—В–љ—Л—Е –Љ–Њ–і–µ–ї—П—Е, –∞–љ–Њ—А–µ–Ї—Б–Є–≥–µ–љ–љ—Л–є —Н—Д—Д–µ–Ї—В –Љ–µ—В—Д–Њ—А–Љ–Є–љ–∞, –њ–Њ––≤–Є–і–Є–Љ–Њ–Љ—Г, —Б–≤—П–Ј–∞–љ —Б —Ж–µ–љ—В—А–∞–ї—М–љ—Л–Љ –і–µ–є—Б—В–≤–Є–µ–Љ –њ—А–µ–њ–∞—А–∞—В–∞ –љ–∞ —Г—А–Њ–≤–љ–µ –≥–Є–њ–Њ—В–∞–ї–∞–Љ–Є—З–µ—Б–Ї–Є—Е –љ–µ–є—А–Њ–љ–Њ–≤ [4]. –Ь–Њ–і—Г–ї–Є—А—Г—П —Н–Ї—Б–њ—А–µ—Б—Б–Є—О –Њ—А–µ–Ї—Б–Є–≥–µ–љ–љ–Њ–≥–Њ –љ–µ–є—А–Њ–њ–µ–њ—В–Є–і–∞ Y, –Љ–µ—В—Д–Њ—А–Љ–Є–љ —Б–њ–Њ—Б–Њ–±—Б—В–≤—Г–µ—В —Б–љ–Є–ґ–µ–љ–Є—О –Љ–∞—Б—Б—Л —В–µ–ї–∞. –Т —А–∞–Ј–ї–Є—З–љ—Л—Е –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П—Е —Г—Б—В–∞–љ–Њ–≤–ї–µ–љ–Њ, —З—В–Њ –≤ –Ј–∞–≤–Є—Б–Є–Љ–Њ—Б—В–Є –Њ—В –і–ї–Є—В–µ–ї—М–љ–Њ—Б—В–Є –њ—А–Є–µ–Љ–∞ –Љ–µ—В—Д–Њ—А–Љ–Є–љ–∞ —Б–љ–Є–ґ–µ–љ–Є–µ –Љ–∞—Б—Б—Л —В–µ–ї–∞ —Г –±–Њ–ї—М–љ—Л—Е —Б –Ь–° —Б–Њ—Б—В–∞–≤–Є–ї–Њ –Њ—В 0,5 –і–Њ 4,5 –Ї–≥ [4,5,22]. –Т —А–∞–±–Њ—В–µ Kurukulasusuriya R. –Є —Б–Њ–∞–≤—В. –њ–Њ–Ї–∞–Ј–∞–љ–Њ, —З—В–Њ –Ї–Њ–ї–Є—З–µ—Б—В–≤–Њ –≤–Є—Б—Ж–µ—А–∞–ї—М–љ–Њ–≥–Њ –ґ–Є—А–∞ –љ–∞ —Д–Њ–љ–µ —В–µ—А–∞–њ–Є–Є –Љ–µ—В—Д–Њ—А–Љ–Є–љ–Њ–Љ —Б–љ–Є–Ј–Є–ї–Њ—Б—М –љ–∞ 15,5%, –≤ —В–Њ –≤—А–µ–Љ—П –Ї–∞–Ї –Є–Ј–Љ–µ–љ–µ–љ–Є–µ –Њ–±—Й–µ–є –Љ–∞—Б—Б—Л –њ–Њ–і–Ї–Њ–ґ–љ–Њ–≥–Њ –ґ–Є—А–∞ –≤ –Ї–Њ–љ—Ж–µ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П –±—Л–ї–Њ –љ–µ–і–Њ—Б—В–Њ–≤–µ—А–љ–Њ [16]. –Ю–њ—Г–±–ї–Є–Ї–Њ–≤–∞–љ–љ—Л–µ –і–∞–љ–љ—Л–µ –њ–Њ –њ—А–Є–Љ–µ–љ–µ–љ–Є—О –Љ–µ—В—Д–Њ—А–Љ–Є–љ–∞ —Г –њ–Њ–і—А–Њ—Б—В–Ї–Њ–≤ —Б –Ь–° –≤ —В–µ—З–µ–љ–Є–µ 6 –Љ–µ—Б—П—Ж–µ–≤ –њ–Њ–Ї–∞–Ј–∞–ї–Є, —З—В–Њ –њ—А–Є–Љ–µ–љ–µ–љ–Є–µ –Љ–µ—В—Д–Њ—А–Љ–Є–љ–∞ —Б–Њ–њ—А–Њ–≤–Њ–ґ–і–∞–ї–Њ—Б—М —Б–љ–Є–ґ–µ–љ–Є–µ–Љ –Є–љ–і–µ–Ї—Б–∞ –Љ–∞—Б—Б—Л —В–µ–ї–∞ (–Ш–Ь–Ґ), –Њ–±—К–µ–Љ–∞ —В–∞–ї–Є–Є, –Ї–Њ–ї–Є—З–µ—Б—В–≤–∞ –≤–Є—Б—Ж–µ—А–∞–ї—М–љ–Њ–є –ґ–Є—А–Њ–≤–Њ–є —В–Ї–∞–љ–Є (—Б–Љ2), –Ї–Њ–љ—Ж–µ–љ—В—А–∞—Ж–Є–Є –Є–љ—Б—Г–ї–Є–љ–∞ –љ–∞—В–Њ—Й–∞–Ї [28].
–Э–∞—А—П–і—Г —Б —Н—В–Є–Љ, –Љ–µ—В—Д–Њ—А–Љ–Є–љ –Њ–±–ї–∞–і–∞–µ—В –Є —А—П–і–Њ–Љ –і—А—Г–≥–Є—Е –Љ–µ—В–∞–±–Њ–ї–Є—З–µ—Б–Ї–Є—Е –Є –≥–µ–Љ–Њ–і–Є–љ–∞–Љ–Є—З–µ—Б–Ї–Є—Е —Н—Д—Д–µ–Ї—В–Њ–≤, –њ–Њ–Ј–≤–Њ–ї—П—О—Й–Є—Е –њ–Њ–Ј–Є—В–Є–≤–љ–Њ –≤–Њ–Ј–і–µ–є—Б—В–≤–Њ–≤–∞—В—М –љ–∞ —А–∞–Ј–ї–Є—З–љ—Л–µ –Ї–Њ–Љ–њ–Њ–љ–µ–љ—В—Л –Ь–°. –Ы–µ—З–µ–љ–Є–µ –Љ–µ—В—Д–Њ—А–Љ–Є–љ–Њ–Љ —Б–Њ–њ—А–Њ–≤–Њ–ґ–і–∞–µ—В—Б—П —Б–љ–Є–ґ–µ–љ–Є–µ–Љ –Ї–Њ–љ—Ж–µ–љ—В—А–∞—Ж–Є–Є —В—А–Є–≥–ї–Є—Ж–µ—А–Є–і–Њ–≤ –љ–∞ 10–20%, –•–° –Ы–Я–Э–Я – –љ–∞ 10% –Є, –Ї–∞–Ї —Б–ї–µ–і—Б—В–≤–Є–µ, —Б–љ–Є–ґ–µ–љ–Є–µ–Љ –њ–µ—З–µ–љ–Њ—З–љ–Њ–≥–Њ —Б–Є–љ—В–µ–Ј–∞ –Є –њ–Њ–≤—Л—И–µ–љ–Є–µ–Љ –Ї–ї–Є—А–µ–љ—Б–∞ –Ы–Я–Ю–Э–Я, –њ–Њ–≤—Л—И–µ–љ–Є–µ–Љ –Ї–Њ–љ—Ж–µ–љ—В—А–∞—Ж–Є–Є –•–° –Ы–Я–Т–Я –љ–∞ 10–20% [5,6,22]. –Ь–љ–Њ–≥–Є–µ –Є–Ј —Н—В–Є—Е —Н—Д—Д–µ–Ї—В–Њ–≤ –Љ–µ—В—Д–Њ—А–Љ–Є–љ–∞ –Њ–±—Г—Б–ї–Њ–≤–ї–µ–љ—Л —Г–Љ–µ–љ—М—И–µ–љ–Є–µ–Љ –Ш–†. –°–љ–Є–ґ–µ–љ–Є–µ –њ–Њ—Б—В—Г–њ–ї–µ–љ–Є—П –°–Ц–Ъ –≤ –њ–µ—З–µ–љ—М –Є –Ї–Њ–љ—Ж–µ–љ—В—А–∞—Ж–Є–Є –Ґ–У –њ–Њ–і –≤–ї–Є—П–љ–Є–µ–Љ –Љ–µ—В—Д–Њ—А–Љ–Є–љ–∞ –≤ —Г—Б–ї–Њ–≤–Є—П—Е —Г–ї—Г—З—И–µ–љ–Є—П —З—Г–≤—Б—В–≤–Є—В–µ–ї—М–љ–Њ—Б—В–Є –Ї –Є–љ—Б—Г–ї–Є–љ—Г –њ—А–Є–≤–Њ–і—П—В –Ї —Г–Љ–µ–љ—М—И–µ–љ–Є—О —П–≤–ї–µ–љ–Є–є –≥–µ–њ–∞—В–Њ—Б—В–µ–∞—В–Њ–Ј–∞ – –Є–Ј–≤–µ—Б—В–љ–Њ–≥–Њ –Ї–Њ–Љ–њ–Њ–љ–µ–љ—В–∞ –Ь–° [13,15].
–Я–Њ–≤—Л—И–∞—П –њ–µ—З–µ–љ–Њ—З–љ—Г—О –Є –њ–µ—А–Є—Д–µ—А–Є—З–µ—Б–Ї—Г—О —З—Г–≤—Б—В–≤–Є—В–µ–ї—М–љ–Њ—Б—В—М –Ї —Н–љ–і–Њ–≥–µ–љ–љ–Њ–Љ—Г –Є–љ—Б—Г–ї–Є–љ—Г, –Љ–µ—В—Д–Њ—А–Љ–Є–љ –љ–∞–њ—А—П–Љ—Г—О –љ–µ –≤–ї–Є—П–µ—В –љ–∞ —Б–µ–Ї—А–µ—Ж–Є—О –Є–љ—Б—Г–ї–Є–љ–∞. –Э–µ –Њ–Ї–∞–Ј—Л–≤–∞—П –њ—А—П–Љ—Л—Е —Н—Д—Д–µ–Ї—В–Њ–≤ –љ–∞ b––Ї–ї–µ—В–Ї–Є, –Љ–µ—В—Д–Њ—А–Љ–Є–љ –Њ–њ–Њ—Б—А–µ–і–Њ–≤–∞–љ–љ–Њ —Г–ї—Г—З—И–∞–µ—В —Б–µ–Ї—А–µ—Ж–Є—О –Є–љ—Б—Г–ї–Є–љ–∞, —Б–њ–Њ—Б–Њ–±—Б—В–≤—Г–µ—В —Б–Њ—Е—А–∞–љ–µ–љ–Є—О —Д—Г–љ–Ї—Ж–Є–Њ–љ–∞–ї—М–љ–Њ–є –∞–Ї—В–Є–≤–љ–Њ—Б—В–Є b––Ї–ї–µ—В–Њ–Ї, —Б–љ–Є–ґ–∞—П –≥–ї—О–Ї–Њ–Ј–Њ—В–Њ–Ї—Б–Є—З–љ–Њ—Б—В—М –Є –ї–Є–њ–Њ—В–Њ–Ї—Б–Є—З–љ–Њ—Б—В—М [22,26,34]. –Я—А–Є —Н—В–Њ–Љ –љ–∞ —Д–Њ–љ–µ —Г–Љ–µ–љ—М—И–µ–љ–Є—П –Ш–† —Б–љ–Є–ґ–∞–µ—В—Б—П –±–∞–Ј–∞–ї—М–љ—Л–є —Г—А–Њ–≤–µ–љ—М –Є–љ—Б—Г–ї–Є–љ–∞ –≤ —Б—Л–≤–Њ—А–Њ—В–Ї–µ –Ї—А–Њ–≤–Є [28].
–Ъ—А–Њ–Љ–µ —В–Њ–≥–Њ, —Г –±–Њ–ї—М–љ—Л—Е –Ь–° –Љ–µ—В—Д–Њ—А–Љ–Є–љ –Њ–Ї–∞–Ј—Л–≤–∞–µ—В –Ї–∞—А–і–Є–Њ–≤–∞—Б–Ї—Г–ї—П—А–љ—Л–µ –њ—А–Њ—В–µ–Ї—В–Є–≤–љ—Л–µ —Н—Д—Д–µ–Ї—В—Л [32]. –Ґ–∞–Ї, –Љ–µ—В—Д–Њ—А–Љ–Є–љ –њ–Њ–ї–Њ–ґ–Є—В–µ–ї—М–љ–Њ –≤–ї–Є—П–µ—В –љ–∞ —Б–Є—Б—В–µ–Љ—Г –≥–µ–Љ–Њ—Б—В–∞–Ј–∞ –Є —А–µ–Њ–ї–Њ–≥–Є—О –Ї—А–Њ–≤–Є, –Њ–±–ї–∞–і–∞–µ—В —Б–њ–Њ—Б–Њ–±–љ–Њ—Б—В—М—О –љ–µ —В–Њ–ї—М–Ї–Њ —В–Њ—А–Љ–Њ–Ј–Є—В—М –∞–≥—А–µ–≥–∞—Ж–Є—О —В—А–Њ–Љ–±–Њ—Ж–Є—В–Њ–≤, –љ–Њ –Є —Б–љ–Є–ґ–∞—В—М —А–Є—Б–Ї –Њ–±—А–∞–Ј–Њ–≤–∞–љ–Є—П —В—А–Њ–Љ–±–Њ–≤ [15]. –Ъ—А–Њ–Љ–µ —В–Њ–≥–Њ, –Љ–µ—В—Д–Њ—А–Љ–Є–љ –Њ–Ї–∞–Ј—Л–≤–∞–µ—В –∞–љ—В–Є–Њ–Ї—Б–Є–і–∞–љ—В–љ–Њ–µ –≤–ї–Є—П–љ–Є–µ –љ–∞ —В—А–Њ–Љ–±–Њ—Ж–Є—В—Л, —Б–љ–Є–ґ–∞–µ—В —Г—А–Њ–≤–µ–љ—М —В—А–Њ–Љ–±–Њ—Ж–Є—В–∞—А–љ–Њ–≥–Њ —Д–∞–Ї—В–Њ—А–∞ 4 –Є b–—В—А–Њ–Љ–±–Њ–≥–ї–Њ–±—Г–ї–Є–љ–∞, —П–≤–ї—П—О—Й–Є—Е—Б—П –Љ–∞—А–Ї–µ—А–∞–Љ–Є –∞–Ї—В–Є–≤–∞—Ж–Є–Є —В—А–Њ–Љ–±–Њ—Ж–Є—В–Њ–≤ [11]. –Э–µ–і–∞–≤–љ–Є–µ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П –њ–Њ–Ї–∞–Ј–∞–ї–Є —Г–ї—Г—З—И–µ–љ–Є–µ –њ—А–Њ—Ж–µ—Б—Б–Њ–≤ —Д–Є–±—А–Є–љ–Њ–ї–Є–Ј–∞ –њ–Њ–і –≤–ї–Є—П–љ–Є–µ–Љ —В–µ—А–∞–њ–Є–Є –Љ–µ—В—Д–Њ—А–Љ–Є–љ–Њ–Љ, —З—В–Њ –Њ–±—Г—Б–ї–Њ–≤–ї–µ–љ–Њ —Б–љ–Є–ґ–µ–љ–Є–µ–Љ —Г—А–Њ–≤–љ—П –Ш–Р–Я–1, –Є–љ–∞–Ї—В–Є–≤–Є—А—Г—О—Й–µ–≥–Њ —В–Ї–∞–љ–µ–≤–Њ–є –∞–Ї—В–Є–≤–∞—В–Њ—А –њ–ї–∞–Ј–Љ–Є–љ–Њ–≥–µ–љ–∞ [5,26]. –Т–∞–ґ–љ–Њ –Њ—В–Љ–µ—В–Є—В—М, —З—В–Њ in vitro –Љ–µ—В—Д–Њ—А–Љ–Є–љ —В–Њ—А–Љ–Њ–Ј–Є—В –≤–Ї–ї—О—З–µ–љ–Є–µ –ї–Є–њ–Є–і–Њ–≤ –≤ —Б–Њ—Б—Г–і–Є—Б—В—Г—О —Б—В–µ–љ–Ї—Г, –њ—А–Њ–ї–Є—Д–µ—А–∞—Ж–Є—О –≥–ї–∞–і–Ї–Њ–Љ—Л—И–µ—З–љ—Л—Е –Ї–ї–µ—В–Њ–Ї —Б–Њ—Б—Г–і–Њ–≤ [3,12,19]. –Т–ї–Є—П—П –љ–∞ –њ—А–Њ—Ж–µ—Б—Б—Л –њ–Њ–ї–Є–Љ–µ—А–Є–Ј–∞—Ж–Є–Є –Є –∞–≥—А–µ–≥–∞—Ж–Є–Є —Д–Є–±—А–Є–љ–∞, –Љ–µ—В—Д–Њ—А–Љ–Є–љ –≤—Л–Ј—Л–≤–∞–µ—В –љ–∞—А—Г—И–µ–љ–Є–µ —Б—В—А—Г–Ї—В—Г—А—Л –Є —Д—Г–љ–Ї—Ж–Є–Є —Д–Є–±—А–Є–љ–∞.
–Т–∞–Ј–Њ–њ—А–Њ—В–µ–Ї—В–Є–≤–љ—Л–µ —Н—Д—Д–µ–Ї—В—Л –Љ–µ—В—Д–Њ—А–Љ–Є–љ–∞ –Ј–∞–Ї–ї—О—З–∞—О—В—Б—П –≤ –љ–Њ—А–Љ–∞–ї–Є–Ј–∞—Ж–Є–Є —Ж–Є–Ї–ї–∞ —Б–Њ–Ї—А–∞—Й–µ–љ–Є—П/—А–∞—Б—Б–ї–∞–±–ї–µ–љ–Є—П –∞—А—В–µ—А–Є–Њ–ї, —Г–Љ–µ–љ—М—И–µ–љ–Є–Є –њ—А–Њ–љ–Є—Ж–∞–µ–Љ–Њ—Б—В–Є —Б–Њ—Б—Г–і–Є—Б—В–Њ–є —Б—В–µ–љ–Ї–Є –Є —В–Њ—А–Љ–Њ–ґ–µ–љ–Є–Є –њ—А–Њ—Ж–µ—Б—Б–Њ–≤ –љ–µ–Њ–∞–љ–≥–Є–Њ–≥–µ–љ–µ–Ј–∞, –≤–Њ—Б—Б—В–∞–љ–Њ–≤–ї–µ–љ–Є–Є —Д—Г–љ–Ї—Ж–Є–Є –њ–µ–є—Б–Љ–µ–Ї–µ—А–љ—Л—Е –Ї–ї–µ—В–Њ–Ї, —А–µ–≥—Г–ї–Є—А—Г—О—Й–Є—Е —Ж–Є–Ї–ї–Є—З–µ—Б–Ї—Г—О –≤–∞–Ј–Њ–і–≤–Є–≥–∞—В–µ–ї—М–љ—Г—О –∞–Ї—В–Є–≤–љ–Њ—Б—В—М [12,15]. –Э–∞ —Д–Њ–љ–µ —В–µ—А–∞–њ–Є–Є –Љ–µ—В—Д–Њ—А–Љ–Є–љ–Њ–Љ –њ–Њ–≤—Л—И–∞–µ—В—Б—П —В—А–∞–љ—Б–њ–Њ—А—В –≥–ї—О–Ї–Њ–Ј—Л –≤ —Н–љ–і–Њ—В–µ–ї–Є–Є –Є –≥–ї–∞–і–Ї–Є—Е –Љ—Л—И—Ж–∞—Е —Б–Њ—Б—Г–і–Њ–≤, –∞ —В–∞–Ї–ґ–µ –≤ –Љ—Л—И—Ж–µ —Б–µ—А–і—Ж–∞, —Г–ї—Г—З—И–∞–µ—В—Б—П —Н–љ–і–Њ—В–µ–ї–Є–є – –Ј–∞–≤–Є—Б–Є–Љ–∞—П –≤–∞–Ј–Њ–і–Є–ї–∞—В–∞—Ж–Є—П [21,32].
–Т –љ–∞—И–Є –і–љ–Є –±–Њ–ї—М—И–Њ–µ –≤–љ–Є–Љ–∞–љ–Є–µ —Г–і–µ–ї—П–µ—В—Б—П –∞–Ї—В–Є–≤–љ–Њ–є –њ—А–Њ—Д–Є–ї–∞–Ї—В–Є–Ї–µ –°–Ф 2 [1,22,34]. –°–Њ–≥–ї–∞—Б–љ–Њ –Љ–љ–µ–љ–Є—О Laaksonen D.F. –Є —Б–Њ–∞–≤—В., —А–Є—Б–Ї —А–∞–Ј–≤–Є—В–Є—П –°–Ф 2 —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –Ь–° –њ–Њ–≤—Л—И–∞–µ—В—Б—П –≤ 7–9 —А–∞–Ј, –њ–Њ —Б—А–∞–≤–љ–µ–љ–Є—О —Б –Є–љ–і–Є–≤–Є–і–∞–Љ–Є, –љ–µ –Є–Љ–µ—О—Й–Є–Љ–Є –Ь–° [17]. –Т –љ–∞—Б—В–Њ—П—Й–µ–µ –≤—А–µ–Љ—П –≤ –Љ–Є—А–µ –љ–∞—Б—З–Є—В—Л–≤–∞–µ—В—Б—П —Б–≤—Л—И–µ 300 –Љ–Є–ї–ї–Є–Њ–љ–Њ–≤ –ї—О–і–µ–є —Б –Э–Ґ–У [33]. –°–Њ–≥–ї–∞—Б–љ–Њ —Н–њ–Є–і–µ–Љ–Є–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є–Љ –њ—А–Њ–≥–љ–Њ–Ј–∞–Љ, –Ї 2025 –≥. —З–Є—Б–ї–Њ –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –Э–Ґ–У –њ–Њ–≤—Л—Б–Є—В—Б—П –і–Њ 500 –Љ–Є–ї–ї–Є–Њ–љ–Њ–≤. –Х–ґ–µ–≥–Њ–і–љ–Њ –њ—А–Є–Љ–µ—А–љ–Њ —Г 1,5–7,3% –ї–Є—Ж —Б –Э–Ґ–У —А–∞–Ј–≤–Є–≤–∞–µ—В—Б—П –°–Ф 2. –Т –Ї—А—Г–њ–љ–µ–є—И–µ–Љ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є DPP (Diabetes Prevention Program, 2002) –±—Л–ї–Њ –њ–Њ–Ї–∞–Ј–∞–љ–Њ, —З—В–Њ —В–µ—А–∞–њ–Є—П –Љ–µ—В—Д–Њ—А–Љ–Є–љ–Њ–Љ –Љ–Њ–ґ–µ—В —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ –Є –±–µ–Ј–Њ–њ–∞—Б–љ–Њ –њ—А–µ–і–Њ—В–≤—А–∞—Й–∞—В—М —А–∞–Ј–≤–Є—В–Є–µ –°–Ф 2 —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –Э–Ґ–У, –Њ—Б–Њ–±–µ–љ–љ–Њ —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –Ш–Ь–Ґ –±–Њ–ї–µ–µ 25 –Ї–≥/–Љ2 –Є –Є–Љ–µ—О—Й–Є—Е –≤—Л—Б–Њ–Ї–Є–є —А–Є—Б–Ї —А–∞–Ј–≤–Є—В–Є—П –°–Ф 2 [8].
–Ч–∞ –і–Њ–ї–≥–Є–µ –≥–Њ–і—Л –њ—А–Є–Љ–µ–љ–µ–љ–Є—П –≤ –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Њ–є –њ—А–∞–Ї—В–Є–Ї–µ –Љ–µ—В—Д–Њ—А–Љ–Є–љ, —П–≤–ї—П—О—Й–Є–є—Б—П –і–Є–Љ–µ—В–Є–ї–±–Є–≥—Г–∞–љ–Є–і–Њ–Љ –Є –∞–±—Б–Њ—А–±–Є—А—Г—О—Й–Є–є—Б—П –≤ –Њ—Б–љ–Њ–≤–љ–Њ–Љ –≤ —В–Њ–љ–Ї–Њ–Љ –Ї–Є—И–µ—З–љ–Є–Ї–µ, –њ—А–Њ–і–µ–Љ–Њ–љ—Б—В—А–Є—А–Њ–≤–∞–ї –≤—Л—Б–Њ–Ї—Г—О –±–µ–Ј–Њ–њ–∞—Б–љ–Њ—Б—В—М. –Ь–µ—В—Д–Њ—А–Љ–Є–љ –њ—А–∞–Ї—В–Є—З–µ—Б–Ї–Є –љ–µ –Љ–µ—В–∞–±–Њ–ї–Є–Ј–Є—А—Г–µ—В—Б—П –≤ –Њ—А–≥–∞–љ–Є–Ј–Љ–µ –Є –њ–Њ–ї–љ–Њ—Б—В—М—О –≤—Л–≤–Њ–і–Є—В—Б—П –њ–Њ—З–Ї–∞–Љ–Є –≤ –љ–µ–Є–Ј–Љ–µ–љ–µ–љ–љ–Њ–Љ –≤–Є–і–µ (–њ–µ—А–Є–Њ–і –њ–Њ–ї—Г–≤—Л–≤–µ–і–µ–љ–Є—П – 1,5–4,9 —З–∞—Б.).
–Т –њ–Њ—Б–ї–µ–і–љ–µ–µ –≤—А–µ–Љ—П –њ–Њ—П–≤–Є–ї—Б—П –њ—А–µ–њ–∞—А–∞—В –Љ–µ—В—Д–Њ—А–Љ–Є–љ–∞ –С–∞–≥–Њ–Љ–µ—В 850 –≤ –≤–Є–і–µ —В–∞–±–ї–µ—В–Ї–Є –љ–∞ –Њ—Б–љ–Њ–≤–µ «–≥–Є–і—А–Њ—Д–Є–ї—М–љ–Њ–є –Љ–∞—В—А–Є—Ж—Л». –Ґ–∞–±–ї–µ—В–Ї–∞ –Њ—В—Д–Њ—А–Љ–Њ–≤–∞–љ–∞ –љ–∞ –Њ—Б–љ–Њ–≤–µ –≥–Є–њ—А–Њ–Љ–µ–ї–ї–Њ–Ј—Л («–Є—Б–Ї—Г—Б—Б—В–≤–µ–љ–љ–∞—П —Б–ї–µ–Ј–∞»), –Љ–µ–ґ–і—Г –љ–Є—В—П–Љ–Є –Ї–Њ—В–Њ—А–Њ–є –і–Є—Д—Д—Г–Ј–љ–Њ —А–∞—Б–њ–Њ–ї–Њ–ґ–µ–љ—Л –≥—А–∞–љ—Г–ї—Л –Љ–µ—В—Д–Њ—А–Љ–Є–љ–∞. –І–µ—А–µ–Ј –љ–µ—Б–Ї–Њ–ї—М–Ї–Њ —З–∞—Б–Њ–≤ –њ–Њ—Б–ї–µ –њ–Њ–њ–∞–і–∞–љ–Є—П –≤ –ґ–Є–і–Ї—Г—О —Б—А–µ–і—Г –≤–µ—А—Е–љ–Є–є –≥–Є–і—А–Њ—Д–Є–ї—М–љ—Л–є —Б–ї–Њ–є –њ—А–Є–Њ–±—А–µ—В–∞–µ—В –≥–µ–ї–µ–Њ–±—А–∞–Ј–љ—Л–є –≤–Є–і, –≤–Њ–ї–Њ–Ї–љ–∞ –≥–Є–њ—А–Њ–Љ–µ–ї–ї–Њ–Ј—Л –њ–Њ—Б—В–µ–њ–µ–љ–љ–Њ «—А–∞—Б–њ–ї–µ—В–∞—О—В—Б—П», –Њ—Б–≤–Њ–±–Њ–ґ–і–∞—П –≥—А–∞–љ—Г–ї—Л –Љ–µ—В—Д–Њ—А–Љ–Є–љ–∞, –Ї–Њ—В–Њ—А—Л–є –њ–Њ—Б—В–µ–њ–µ–љ–љ–Њ, —Б–ї–Њ–є –Ј–∞ —Б–ї–Њ–µ–Љ, —А–∞—Б—В–≤–Њ—А—П–µ—В—Б—П –≤ –Ї–Є—И–µ—З–љ–Њ–Љ —Б–Њ–і–µ—А–ґ–Є–Љ–Њ–Љ. –Я–Њ–і–Њ–±–љ–∞—П —А–∞–Ј—А–∞–±–Њ—В–Ї–∞ –њ–Њ–Ј–≤–Њ–ї—П–µ—В –њ–Њ–ї—Г—З–Є—В—М –і–ї–Є—В–µ–ї—М–љ–Њ–µ, —Б—В–∞–±–Є–ї—М–љ–Њ–µ, –Њ—В–ї–Є—З–∞—О—Й–µ–µ—Б—П –Њ—В—Б—Г—В—Б—В–≤–Є–µ–Љ «–њ–Є–Ї–Њ–≤» –і–µ–є—Б—В–≤–Є–µ –Љ–µ—В—Д–Њ—А–Љ–Є–љ–∞. –Я—А–µ–њ–∞—А–∞—В –Є–Љ–µ–µ—В –њ—А–Њ–і–Њ–ї–ґ–Є—В–µ–ї—М–љ–Њ–µ – 12–—З–∞—Б–Њ–≤–Њ–µ –і–µ–є—Б—В–≤–Є–µ –Є –њ–Њ–ї–љ–Њ—Б—В—М—О –њ–µ—А–µ–Ї—А—Л–≤–∞–µ—В –љ–Њ—З–љ–Њ–є –њ–Є–Ї –≥–µ–њ–∞—В–Є—З–µ—Б–Ї–Њ–є –њ—А–Њ–і—Г–Ї—Ж–Є–Є –≥–ї—О–Ї–Њ–Ј—Л. –£–і–Њ–±—Б—В–≤–Њ –њ—А–Є–Љ–µ–љ–µ–љ–Є—П –њ—А–µ–њ–∞—А–∞—В–∞ –њ–Њ–≤—Л—И–∞–µ—В –њ—А–Є–≤–µ—А–ґ–µ–љ–љ–Њ—Б—В—М –њ–∞—Ж–Є–µ–љ—В–Њ–≤ –ї–µ—З–µ–љ–Є—О.
–Я—А–Њ—В–Є–≤–Њ–њ–Њ–Ї–∞–Ј–∞–љ–Є—П–Љ–Є –Ї –љ–∞–Ј–љ–∞—З–µ–љ–Є—О –Љ–µ—В—Д–Њ—А–Љ–Є–љ–∞ —П–≤–ї—П—О—В—Б—П –љ–∞—А—Г—И–µ–љ–Є—П —Д—Г–љ–Ї—Ж–Є–є –њ–Њ—З–µ–Ї (—Б–љ–Є–ґ–µ–љ–Є–µ –Ї–ї–Є—А–µ–љ—Б–∞ –Ї—А–µ–∞—В–Є–љ–Є–љ–∞ –љ–Є–ґ–µ 50 –Љ–ї/–Љ–Є–љ. –Є–ї–Є –Ї–Њ–љ—Ж–µ–љ—В—А–∞—Ж–Є—П –Ї—А–µ–∞—В–Є–љ–Є–љ–∞ –Ї—А–Њ–≤–Є –±–Њ–ї–µ–µ 132 –Љ–Љ–Њ–ї—М/–ї —Г –Љ—Г–ґ—З–Є–љ –Є –±–Њ–ї–µ–µ 123 –Љ–Љ–Њ–ї—М/–ї —Г –ґ–µ–љ—Й–Є–љ), –≥–Є–њ–Њ–Ї—Б–Є—З–µ—Б–Ї–Є–µ —Б–Њ—Б—В–Њ—П–љ–Є—П –ї—О–±–Њ–є –њ—А–Є—А–Њ–і—Л, –∞ —В–∞–Ї–ґ–µ –Ј–ї–Њ—Г–њ–Њ—В—А–µ–±–ї–µ–љ–Є–µ –∞–ї–Ї–Њ–≥–Њ–ї–µ–Љ. –°–ї–µ–і—Г–µ—В –≤–Њ–Ј–і–µ—А–ґ–∞—В—М—Б—П –Њ—В –љ–∞–Ј–љ–∞—З–µ–љ–Є—П –њ—А–µ–њ–∞—А–∞—В–∞ –≤ –њ–µ—А–Є–Њ–і –±–µ—А–µ–Љ–µ–љ–љ–Њ—Б—В–Є –Є –ї–∞–Ї—В–∞—Ж–Є–Є [14].
–Ы–µ—З–µ–љ–Є–µ –њ—А–µ–њ–∞—А–∞—В–Њ–Љ –Є–љ–Є—Ж–Є–Є—А—Г—О—В —Б 500–850 –Љ–≥, –њ—А–Є–љ–Є–Љ–∞–µ–Љ—Л—Е –≤–Њ –≤—А–µ–Љ—П —Г–ґ–Є–љ–∞ –Є–ї–Є –љ–∞ –љ–Њ—З—М. –Т –і–∞–ї—М–љ–µ–є—И–µ–Љ –і–Њ–Ј–∞ –њ—А–µ–њ–∞—А–∞—В–∞ —Г–≤–µ–ї–Є—З–Є–≤–∞–µ—В—Б—П –љ–∞ 500–850 –Љ–≥ –Ї–∞–ґ–і—Л–µ 1–2 –љ–µ–і–µ–ї–Є. –Ь–∞–Ї—Б–Є–Љ–∞–ї—М–љ–∞—П —А–µ–Ї–Њ–Љ–µ–љ–і–Њ–≤–∞–љ–љ–∞—П –і–Њ–Ј–∞ —Г –±–Њ–ї—М–љ—Л—Е —Б –Ь–° —Б–Њ—Б—В–∞–≤–ї—П–µ—В 1500–1700 –Љ–≥ –≤ —Б—Г—В–Ї–Є –≤ —А–µ–ґ–Є–Љ–µ 2–3 –њ—А–Є–µ–Љ–Њ–≤. –Т–Њ –Є–Ј–±–µ–ґ–∞–љ–Є–µ –њ–Њ–±–Њ—З–љ—Л—Е —П–≤–ї–µ–љ–Є–є –Љ–µ—В—Д–Њ—А–Љ–Є–љ–∞ (–і–Є–∞—А–µ—П, –Љ–µ—В–µ–Њ—А–Є–Ј–Љ, –∞–±–і–Њ–Љ–Є–љ–∞–ї—М–љ—Л–є –і–Є—Б–Ї–Њ–Љ—Д–Њ—А—В, –Љ–µ—В–∞–ї–ї–Є—З–µ—Б–Ї–Є–є –≤–Ї—Г—Б –≤–Њ —А—В—Г) –љ–µ–Њ–±—Е–Њ–і–Є–Љ–∞ –њ–Њ—Б—В–µ–њ–µ–љ–љ–∞—П —В–Є—В—А–∞—Ж–Є—П –і–Њ–Ј—Л –њ—А–µ–њ–∞—А–∞—В–∞.
–Т –Ј–∞–Ї–ї—О—З–µ–љ–Є–µ —Б–ї–µ–і—Г–µ—В –Њ—В–Љ–µ—В–Є—В—М, —З—В–Њ –≤ –љ–∞—Б—В–Њ—П—Й–µ–µ –≤—А–µ–Љ—П —А–∞—Ж–Є–Њ–љ–∞–ї—М–љ–∞—П —В–µ—А–∞–њ–Є—П –Ь–° –Љ–µ—В—Д–Њ—А–Љ–Є–љ–Њ–Љ, –Њ–±–ї–∞–і–∞—О—Й–Є–Љ –±–ї–∞–≥–Њ–њ—А–Є—П—В–љ—Л–Љ —Б–њ–µ–Ї—В—А–Њ–Љ —Д–∞—А–Љ–∞–Ї–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є—Е —Н—Д—Д–µ–Ї—В–Њ–≤, –≤ —Б–Њ—З–µ—В–∞–љ–Є–Є —Б –љ–µ—Д–∞—А–Љ–∞–Ї–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є–Љ–Є –Љ–µ—В–Њ–і–∞–Љ–Є —П–≤–ї—П–µ—В—Б—П —Н—Д—Д–µ–Ї—В–Є–≤–љ—Л–Љ —Б–њ–Њ—Б–Њ–±–Њ–Љ –Ї–Њ—А—А–µ–Ї—Ж–Є–Є –Ш–† –Є –њ–Њ–Ј–≤–Њ–ї—П–µ—В —Б—Г—Й–µ—Б—В–≤–µ–љ–љ–Њ –њ–Њ–≤–ї–Є—П—В—М –љ–∞ –Ї–∞—З–µ—Б—В–≤–Њ –ґ–Є–Ј–љ–Є –њ–∞—Ж–Є–µ–љ—В–Њ–≤ –Є –њ—А–µ–і–Њ—В–≤—А–∞—В–Є—В—М –≤–Њ–Ј–љ–Є–Ї–љ–Њ–≤–µ–љ–Є–µ –Њ–њ–∞—Б–љ—Л—Е –і–ї—П –ґ–Є–Ј–љ–Є —Б–µ—А–і–µ—З–љ–Њ–—Б–Њ—Б—Г–і–Є—Б—В—Л—Е –Њ—Б–ї–Њ–ґ–љ–µ–љ–Є–є.

–Ы–Є—В–µ—А–∞—В—Г—А–∞
1. Aronne L.J., Segal R.K. Adiposity and fat distribution outcome measures:assessment and clinical implications // Obes Res–2002; 10(1): 14S–21S.
2. Bosello O., Zamboni M. Visceral obesity and metabolic syndrome// Obes. Rev.–2000, 1, 47–56
3. Bradley J. D., Zhonglin X., Benoit V., and Ming–Hui Z. Activation of the AMP–Activated Kinase by Antidiabetes Drug Metformin Stimulates Nitric Oxide Synthesis In Vivo by Promoting the Association of Heat Shock Protein 90 and Endothelial Nitric Oxide Synthase.// Diabetes.–2005 55: 496–505
4. Chau–Van C., Gamba M., Salvi R. et al. Metformin Inhibits Adenosine 5’–Monophosphate–Activated Kinase Activation and Prevents Increases in Neuropeptide Y Expression in Cultured Hypothalamic Neurons. // Endocrinology.– 2007; 148(2): 507 – 511.
5. Charles M.A., Morange P., Eschwege E. et al. Effects of weight change and metformin on fibrolysis and the von Willebrand factor in obese nondiabetic subjects. The BIGPRO1 Study.// Diabetes Care–1998; 21:1967–75
6. Charles M.A., Eschwege E., Grandmottet and al. Treatment with metformin of non–diabetic men with hypertension. Hypertriglyceridemia and central fat distribution: the BIGPRO 1.2 trial. // Diabetes Metab Res Rev.– 2000; 16: 2–7
7. Dagher Z., Ruderman N., Tornheim K., Ido Y.: Acute regulation of fatty acid oxidation and AMP–activated protein kinase in human umbilical vein endotehlial cells.// Circ Res.–2001; 88 :1276 –1282
8. Diabetes Prevention Program Research Group/ Reduction in the incidence of type 2 diabetes with lifesyill intervention or metformin. // N Engl J Med.–2002; 346, 393–403
9. Isomaa, B., Lahti, K., Almengren P. et al. Cardiovascular morbidity and mortality associated with the metabolic syndrome.// Diabetes Care 24 (2001), 683–689.
10. Ford E.S., Giles W.H., Dietz W.H. Prevalence of the metabolic syndrome among U.S. adults: findings from the third National Health and Nutrition Examination Survey.// JAMA.– 2002;287:356–359
11. Grand P.J. Beneficial effects of metformin on hemostasis and vascular function in man.. // Diabetes Meteb.–2003, 29/6S45–52
12. Jadhav S., Ferrell W., Greer I. A. et al. Effects of Metformin on Microvascular Function and Exercise Tolerance in Women With Angina and Normal Coronary Arteries: Randomized, Double–Blind, Placebo– Controlled Study// J. Am. Coll. Cardiol.– 2006; 48(5): 956 – 963.
13. Kahn BB, Flier JS: Obesity and insulin resistance.// J Clin Invest –2000;106:473–81
14. Kirpichnikov D., McFarlane S.I., Sowers J.R, Metformin:An Update //Ann Intern Med.– 2002; 137: 25 –33
15. Klip A., Leiter L.A Cellular mechanism of action of metformin // Diabetes Care.– 1990; 13 (6): 696–704
16. Kurukulasusuriya R., Banerij M.A., Chaiken R., Lebovitz H. Selective decrease in visceral fat is associated with weight loss during metformin treatment in African Americans with type 2 diabetes (abstract)/ //Diabetes.–1999, 48, A315.
17. Laaksonen D.F., Laaka H.M., Niskanen L.K. et al Metabolic syndrome and development of diabetes mellitus: application and validation of recently suggested definition of the metabolic syndrome in a prospective cohort stady. // Am J Epidemiol. –2002; 156, 1070–7.
18. McFarlane S.I., Banerij M., Sowers J.R. Insulin resistance and cardiovascular disease. //J Clin Endocrinol Metab. – 2001; 86: 713–8
19. Mamputu J.C., Wiernsperger N.F., Renier G. A. Antiatherogenic properties of metformin: the experimental evidence. // Diabetes Meteb.–2003, 29/6S71–6
20. Mannucci E., Ognibene A.,, Cremasco F. et al Effect of Metformin on Glucagon–Like Peptide 1 (GLP–1) and Leptin Levels in Obese Nondiabetic Subjects. // Diabetes Care– 2001; 24 (3): 489–494
21. Matthaei S., Hamann A., Klein H.H., Benecke H. et al. Association of Metformin’s effect to increase insulin–stimulated glucose transport with potentiation of insulin–induced translocation of glucose transporters from intracellular pool to plasma membrane in rat adipocytes // Diabetes. –1999; 40(7): 850–857
22. Matthaei S., Stumvoll M., Kellerer M., H?ring H.–U. Pathophysiology and pharmacological treatment of insulin resistance// Endocr. Rev.– 2000; 21(6): 585 – 618
23. Miller J, Rosenbloom A, Silverstein J: Childhood obesity.// J Clin Endocrinol Metabol –2004;89–9:4211–18
24. Ming–Hui Z., Kirkpatrick S.S., Davis B.J.et al. Activation of the AMP–activated protein kinase by the anti–diabetic drug metformin in vivo: role of mitochondrial reactive nitrogen species. //J Biol Chem.–2004279 :43940 –51
25. Nagi D.K., Yudkin J.S. Effects of metformin on insulin resistance, risk factors for cardiovascular disease, and plasminogen activator inhibitor in NIDDM subjects. A study of two ethnic groups // Diabetes Care. – 1993; 16 (4): 621–629.
26. Patane G., Piro S., Rabuazzo A.M., Anello M. et al. Metformin restores insulin secretion altered by chronic exposure to free fatty acids or high glucose: a direct metformin effect on pancreatic beta–cells // Diabetes. –2001; 49(5): 735–740
27. Piatti P.M., Monti L.D., Galli l. Et al. Relationship betweem endotelin–1 concentration and metabolic alteration typical of the insulin resistance syndrom. // Metabolism.–2000, 49,748–52.
28. Srinivasan S., Ambler G. R., Baur L. A. Randomized, Controlled Trial of Metformin for Obesity and Insulin Resistance in Children and Adolescents: Improvement in Body Composition and Fasting Insulin.// J. Clin. Endocrinol. Metab.–2006; 91(6): 2074 – 2080.
29. Steinberg HO, Baron AD: Vascular function, insulin resistance and fatty acids.// Diabetologia–2002; 45:623–4
30. Third report of the National Cholesterol Education Program (NCEP) expert panel on detection, evaluation, and treatment of high blood cholesterol in adults (Adult Treatment Panel III). NIH Publication 2001; 5. N 01–3670.
31. The IDF concensus worldwide definition of the metabolic syndrome. Availeble from: http://www.idf.org
32. Vitale C., Mercuro G., Cornoldi A. et al. Metformin improves endothelial function in patients with metabolic syndrome.// J Intern Med.–2005; 258 :250 –6
33. Zimmet P. The burden of type 2 diabetes: are we doing enough? // Diabetes Metabolism.– 2003; 29: 6S9–6S18.
34. Zimmet P., Shaw J., Alberti G. Preventing type 2 diabetes and the dysmetabolic syndrome in the real world: a realistic view. Diabetic medicine // 2003.– 20(9): 693–702.












