Число людей, страдающих СД, неуклонно возрастает. По данным Diabetes Atlas 2000, в 2000 году в мире был зарегистрирован 151 млн. больных СД 2 типа. По данным 2006 года – 246 млн. человек, из них 50% – наиболее активного трудоспособного возраста (40–59 лет). По прогнозам Всемирной Организации Здравоохранения, к 2025 году ожидается увеличение числа больных СД в 2–3 раза по сравнению с сегодняшним и может достигнуть цифры более 380 млн.(!) человек (в 2000 году этот прогноз составлял 300 млн.).
В России на начало 2000 года 8 млн. человек страдали СД, т.е. около 5,5% населения России (по статистике – всего 2 млн., на 01.01.08 официально зарегистрировано 2,83 млн.) к 2025 г., по прогнозам ВОЗ, это число увеличится до 13,2 млн. человек. Одна из причин такого расхождения статистических и реальных данных заключается в том, что нередко СД 2 типа диагностируется спустя некоторое время (иногда спустя более чем 5 лет) после истинной манифестации этого заболевания, что связано с особенностями его клинического течения.
Сердечно–сосудистые осложнения являются основной причиной инвалидизации и смертности у больных СД 2 типа. Относительный риск смерти у лиц с нарушенной толерантностью к глюкозе повышен на 30%, у лиц с недиагностированным СД – на 80% и у людей, у которых диагноз СД стоит, относительный риск смерти увеличен в 2,8 раза по сравнению с лицами, не имеющими СД.
Следует обратить внимание на то, что 75% пациентов, страдающих СД 2 типа, имеют повышенные цифры артериального давления (АД), а при сочетании СД 2 типа и артериальной гипертензии (АГ) риск инфаркта миокарда возрастает в 5 раз. При этом смертность после перенесенного инфаркта миокарда при том же сочетании увеличивается в 6 раз. Риск развития ОНМК возрастает в 8 раз при сочетании СД 2 типа и АГ.
Факторы риска развития ИБС и атеросклероза:
Наиболее часто изучаемые факторы условно можно разделить на следующие группы:
– некорригируемые:
• возраст;
• пол – до наступления менопаузы женщины
значительно реже страдают ИБС (их защищает
эстрадиол). Однако после того, как происходит
угасание функции яичников, частота встречае-
мости ИБС у мужчин и женщин выравнивает-
ся. При наличии СД, независимо от сохранно-
сти функции яичников, ИБС и атеросклероз
встречаются с одинаковой частотой у мужчин
и женщин;
• наследственность.
– корригируемые (повышенные цифры АД, курение, несбалансированное питание, ожирение и гиподинамия);
– частично корригируемые (дислипидемия: снижение количества ЛПВП и повышение ЛПНП; СД (гиперинсулинемия и инсулинорезистентность, психоэмоциональное напряжение).
Все эти факторы риска развития неоднократно изучались в многочисленных исследованиях. Хотелось бы более подробно остановиться на некоторых из них.
Дислипидемия. Хотя уровень ЛПНП обычно нормальный, скорость синтеза и удаления ЛПНП увеличены. Размер плотности частиц ЛПНП у людей, страдающих СД 2 типа, в значительной степени зависит от уровня триглицеридов. При гипертриглицеридемии повышается содержание мелких, более плотных фракций ЛПНП. Осахаренные (гликозилированные) ЛПНП более склонны к окислительной модификации.
При эпидемиологических исследованиях людей, страдающих СД 2 типа, часто обнаруживают гиперхолестеринемию, связанную с повышением ЛПНП. По данным ряда исследований, повышение холестерина плазмы выявляется у 54–77% пациентов. Однако частота гиперхолестеринемии при СД 2 типа у людей, не имеющих данной патологии, примерно одинакова. Большинство исследователей считают, что повышение ЛПНП у больных СД 2 типа обусловлено в основном генетическими причинами.
Уменьшение уровня триглицеридов отмечается при терапии инсулином или препаратами метформина, а также при снижении веса у больных СД 2 типа с ожирением. Однако часто уровень триглицеридов остается повышенным у такой категории пациентов, несмотря на нормализацию уровня гликемии. При этом чем выше уровень общего холестерина у больных СД 2 типа, тем выше риск сердечно–сосудистной смертности у данного пациента. В то же время выявлено, что при одном и том же уровне холестерина смертность больных в связи с наличием ИБС выше в 3–4 раза при сопутствующем СД 2 типа в сравнении с ситуацией, когда СД 2 типа отсутствует.
Среди причин формирования атеросклероза у пациентов СД 2 типа выделяют количественные и качественные изменения липопротеинов крови. Из количественных изменений наиболее характерны гипертриглицеридемия и уменьшение холестерина ЛПВП, которые встречаются приблизительно у 20% больных. Уменьшение холестерина ЛПВП выявляется как при впервые выявленном СД 2 типа, так и у больных с ранее диагностированным СД 2 типа и находящихся на комплексной терапии, включающей в себя как диету, так и пероральные сахароснижающие препараты и/или инсулин. Из качественных изменений – образование маленьких плотных частиц ЛПНП. Гиперхолистеринемию, обусловленную повышением ХС ЛПНП, при СД 2 типа находят с такой же частотой, как и у лиц без СД.
Выявлена связь между уровнем триглицеридов и риском возникновения ИБС и атеросклероза у больных СД 2 типа. По данным 11–летнего исследования (Paris Prospective Study), уровень триглицеридов связан с риском смерти от ИБС и ее осложнений при сочетании с СД 2 типа. Уровень триглицеридов может иметь наибольшую прогностическую ценность в отношении развития коронарного атеросклероза, чем другие факторы риска.
По мнению M. Laakso и соавт., важное прогностическое значение в отношении заболеваемости и смертности от ИБС и ее осложнений у пациентов с СД 2 типа имеет снижение ЛПВП, уменьшение которых < 0,9 ммоль/л сопровождается четырехкратным увеличением риска смерти от сердечной патологии. В Финляндии было проведено проспективное исследование с участием 1059 человек, страдающих СД 2 типа, среднего возраста, где было показано, что повышение триглицеридов >2,3 моль/л и снижение ЛПВП <1,0 ммольл сопровождается двукратным увеличением риска развития осложнений и смертности в связи с ИБС независимо от других факторов риска.
Гиперинсулинемия и инсулинорезистентность вне зависимости от нарушений липидного обмена являются независимыми факторами риска развития ИБС. Выявлена связь между инсулинорезистентностью и низким уровнем ЛПВП. Количество ЛПВП увеличивается при терапии СД 2 типа инсулином и снижением веса пациентов. Гиперинсулинемия является независимым предиктором риска развития инфаркта миокарда и смерти от осложнений ИБС вне зависимости от возраста, индекса массы тела (ИМТ), артериального давления и уровня холестерина, курения и физической активности. Проспективные эпидемиологические исследования показали, что гиперинсулинемия увеличивает риск развития ангиографически подтвержденного коронарного атеросклероза и коррелирует с повышенной смертностью от него. Одномоментное исследование (Atherosklerosis Risk in Communities Study) подтвердило взаимосвязь между уровнем инсулина натощак и степенью атеросклеротического поражения стенок артерий.
Имеющиеся данные свидетельствуют о том, что инсулинорезистентность в значительно большей степени, чем гиперинсулинемия, ассоциируются с атеросклерозом, тромбогенезом, гипертонией, ожирением и сахарным диабетом. При ожирении базальная и суточная секреции инсулина в 3–4 раза выше, чем у лиц с нормальной массой тела.
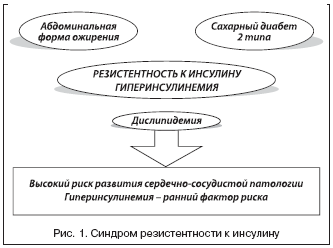
Исследование японских ученых с участием больных с ангиографически подтвержденным коронарным атеросклерозом выявили существование тесной взаимосвязи между степенью резистентности к инсулину и выраженностью коронарного атеросклероза (рис. 1).
Здесь также играет роль и наследственность, как по развитию СД, так и по развитию ИБС и атеросклероза. Не стоит упускать из вида и наличие в семьях нарушений липидного обмена, свертываемости крови, АД, реактивности со стороны нервной системы и, разумеется, СД. Роль наследственного фактора определяется наличием генов, мутации которых могут вызвать гиперхолестеринемию и ранний атеросклероз.
Как правило, гиперинсулинемией, с последующим возможным развитием инсулинорезистентности, страдают люди с избыточной массой тела и ожирением. Причем наиболее неблагоприятной является категория лиц именно с избыточной массой тела, т.е. ИМТ от 25 до 29 кг/м2. По данным Фрамингемского исследования, смертность мужчин с массой тела, превышающей идеальную на 10–20%, в 2 раза выше по сравнению с лицами с нормальной массой тела (ИМТ от 18 до 25 кг/м2). В последнее время четко доказана неблагоприятность в плане прогноза ожирения по так называемому центральному типу, т.е со скоплением жировых отложений на передней брюшной стенке и что самое неприятное – вокруг внутренних органов. Этот тип ожирения оказывает влияние на атеросклеротическое поражение сосудов. При этом следует помнить, что 80% пациентов со 2 типом СД страдают ожирением в той или иной степени его выраженности.
Отдельно следует остановиться еще на одном факторе развития ИБС и атеросклероза, а именно на дисфункции эпителия и курении. Основное воздействие курения на патогенез атеросклероза связывают с его системным воздействием на сердечно–сосудистые показатели: увеличение ударного объема, учащение ЧСС, повышение минутного объема, воздействие на липидный и углеводный обмен, обмен катехоламинов, свертываемость крови. Существует четкая зависимость степени стенозирования сосудов атеросклеротическими бляшками и количеством потребляемого никотина. Доказана реакция сердечно–сосудистой системы в виде возможного спазма коронарных артерий и метаболических изменений под влиянием никотина (необходимо отметить тот факт, что «легкие» сигареты влияют на сосудистую стенку не меньше, чем обычные сигареты).
Причина таких изменений лежит в дисфункции эндотелия, возникающего под воздействием никотина. Дисфункции эпителия в настоящее время уделяется очень большое и пристальное внимание. Эндотелий – монослой клеток вытянутой формы, гетерогенных по размеру, тесно связанных между собой. Эндотелий секретирует мощные вазоактивные вещества: вазодилататоры (оксид азота NO, эндотелиальный гиперполяризующий фактор, простациклин) и вазоконстрикторы (ангиотензин II, эндотелин, свободные радикалы недоокисленных жирных кислот, простагландин F2a, тромбоксан А2). Наиболее важным и значимым вазодилататором считается оксид азота NO. Он вызывает расслабление гладкомышечных клеток сосудов, предупреждает структурные изменения эндотелия, ингибируя рост и миграцию глакомышечных клеток. NO присутствует во всех эндотелиальных клетках, независимо от размера и функции сосудов. В покое эндотелий постоянно секретирует NO, поддерживая нормальный тонус артерий. Дисфункция эндотелия протекает с высвобождением вазоконстрикторных субстанций, свободных радикалов, факторов, угнетающих эндотелиальный фибринолиз и усиливающих агрегацию тромбоцитов, пролиферативную и миграционную активность лейкоцитов (макрофагов) и гладкомышечных клеток сосудов, что способствует тромбозу и формированию атеросклеротической бляшки. Здесь необходимо отметить тот факт, что при СД гипергликемия сама по себе является мощным фактором, инициирующим образование свободных радикалов различными путями (аутоокисление глюкозы, полиоловый шунт и другие). Помимо этого, стойкая гипергликемия снижает активность факторов антиоксидантной защиты – супероксиддисмутазы, витамина С (аскорбиновой кислоты) и Е (a–токоферола) и прочих. Высокая активность окислительных реакций при СД напрямую коррелирует с выраженностью сосудистых осложнений.
На фоне формирования в последние годы такого разветвления науки, как элементология (содержание микроэлементов в организме и их роль в жизнедеятельности), небезынтересен факт влияния некоторых микроэлементов на состояние сердечно–сосудистой системы, в частности, при СД. Так, например, магний, являясь универсальным регулятором обменных процессов в организме, участвует в энергетическом (комплексирование с АТФ и активация АТФ–аз, окислительное фосфорилирование, гликолиз), пластическом (синтез белка, липидов, нуклеиновых кислот), электролитном обменах. Выполняя роль естественного антагониста кальция, магний принимает участие в расслаблении мышечных волокон, снижая агрегационную способность тромбоцитов, поддерживает нормальный трансмембральный потенциал в электровозбудимых тканях.
Магний влияет на эндотелий, который играет ключевую роль в сосудистом гомеостазе, в частности, за счет продукции оксида азота и участия в управлении агрегацией тромбоцитов. Доказано, что дефицит ионов магния увеличивает активность тромбоксана А2, что сопровождается повреждением сосудистой стенки.
Представляет интерес вопрос об антиатерогенной активности магния. Длительный дефицит магния – одно из необходимых условий для манифестации и развертывания генетически детерминированной программы атеросклероза. В условиях атерогенной диеты недостаток в пище магния способствует прогрессированию склеротического поражения сосудов и, наоборот, назначение магния приводит к регрессу гиперхолестеринемии. При дефиците магния в крови повышено содержание триглицеридов, липопротеидов низкой плотности и очень низкой плотности и, напротив, снижен уровень липопротеидов высокой плотности. Согласно результатам исследования The Atherosclerosis Risk in Communities (ARIC) гипомагниемия сопровождает развитие ишемической болезни сердца (ИБС). Подобный вывод был сделан на основании наблюдения 13922 пациентов на протяжении 4–7 лет с учетом социо–демографических характеристик, вредных привычек, уровней холестерина, фибриногена и других факторов. Более того, известно, что наиболее выраженный дефицит магния имеется у лиц с повышенным содержанием атерогенных липидов.
Исследования показали, что длительно существующий дефицит магния, особенно на фоне эссенциальной гипертонии, является достоверным фактором риска возникновения острых нарушений мозгового кровообращения. Кровеносные сосуды, снабжающие ткань мозга, чрезвычайно чувствительны к магниевому балансу.
Гипомагниемия усиливается при СД 2 типа, который стал частым спутником больных старших возрастов с кардиоваскулярной патологией. Недостаток магния сопряжен с нарушенной толерантностью к глюкозе, а препараты магния способны улучшать инсулинозависимую утилизацию, снижая тем самым инсулинорезистентность и сердечно–сосудистый риск.
Учитывая, к каким серьезным последствиям приводит гиперинсулинемия и инсулинорезистентность, лечение СД 2 типа при наличии этих двух компонентов следует направлять не только на нормализацию уровня гликемии, но и на устранение гиперинсулинемии и инсулинорезистентности.
Препаратами выбора в данном случае являются бигуаниды [2,4,5,9]. В настоящее время единственным препаратом этой группы, разрешенным к применению, является метформин.
Помимо стандартной комбинированной терапии пероральными сахароснижающими препаратами, в комплекс лечения целесообразно включать препараты магния, в частности, оротат магния (Магнерот®). Оротовая кислота, входящая в состав препарата, поддерживает холестерин в коллоидном состоянии, что, возможно, препятствует его отложению на стенках сосудов. Этот эффект крайне важен в свете того, что нарушение углеводного обмена сопровождается, как правило, и дислипидемией. Оротовая кислота улучшает также усваиваемость магния из пищевых продуктов, богатых магнием – злаковые культуры, бобовые, шоколад, зелень, орехи. Ограничение многих из этих продуктов при СД и формирование самостоятельного сердечно–сосудистого риска на фоне инсулинорезистентности и гиперинсулинемии, также подчеркивает необходимость добавления магния к комплексной терапии СД 2 типа.
Магнерот® хорошо переносится, процент побочных эффектов весьма невелик (чуть более одного процента) и выражается в нарушениях со стороны пищеварительной системы (диарея, запоры), что, как правило, возникает при приеме препарата в высоких дозах и обычно проходит при снижении дозы. Единственным противопоказанием для назначения данного препарата является наличие почечной патологии – мочекаменная болезнь и нарушения почечной функции. Магнерот®, назначаемый в дозе по 2 таблетки 3 раза в сутки в течение 7 дней, с переходом на 1 таблетку 2–3 раза в сутки ежедневно можно применять длительное время.
Таким образом, коррекция нарушений при СД сводится не только к контролю за гликемией, но и нормализации всех остальных процессов и минимизации сердечно–сосудистого риска, который является неоспоримым при наличии СД. С этой целью в комплексное лечение необходимо включать не только стандартные схемы терапии СД, но и микроэлементы.
Литература
1. Балаболкин М.И. Эндокринология, М, «Универсум Паблишинг», 1998, с. 367–470.
2. Балаболкин М.И., Клебанова Е.М., Креминская В.М. Возможности лечения сахарного диабета 2 типа на современном этапе.// Русский медицинский журнал. – Т.10. – №11. – 2002. – С.496–502.
3. Бутрова С.А. Эффективность Глюкофажа в профилактике сахарного диабета 2 типа.// Русский медицинский журнал. – Т.11. – №27. – 2003. – С.1494–1498.
4. Дедов И.И., Шестакова М.В. Сахарный диабет. Руководство для врачей. – М. – 2003. – С.151–175, 282–292.
5. Дедов И.И., Шестакова М.В., Максимова М.А. «Федеральная целевая программа сахарный диабет», М 2002
6. Метелица В.И. Справочник по клинической фармакологии сердечнососудистых лекарственных средств. 2е изд., перераб. и доп. М.: Издательство Бином – Спб.: Невский Диалект, 2002; 926.
7. Метаболизм магния и терапевтическое значение его препаратов. М.: ИД Медпрактика – М. 2002; 28.
8. Применение магния и оротовой кислоты в кардиологии. М.: ИД Медпрактика – М. 2002; 20.
9. Смирнова О.М. Впервые выявленный сахарный диабет 2 типа. Диагностика, тактика лечении. Методическое пособие.
10. Стуров Н.В. Кафедра общей и клинической фармакологии РУДН, Москва. Препараты магния – обоснование применения в кардиологической практике. Medi. Ru «Подробности о лекарствах». Woerwad Pharma.
11. Ожирение. Метаболический синдром. Сахарный диабет 2 типа. Под редакцией акад. РАМН. И.И.Дедова. М. – 2000. – С.111.
12. Терапия магнезиуморотатом. Таблетки Магнерот. Научный обзор. Медпрактика. 2001; 31.
13. Чугунова Л.А., Шамхалова М.Ш., Шестакова М.В. Лечебная тактика при сахарном диабете 2 типа с дислипидемией (по результатам крупных международных исследований), инф. сист.
14. Физиология человека. Под редакцией Агаджаняна Н.А., Циркина В.И. Спб.: Сотис 1998; 528.
15. Diabetes Prevention Program Research Group. N EnglJ Med 2002; 346: 393–403.
16. Head K.A. Peripheral neuropathy: pathogenic mechanisms and alternative therapies // Altern Med Rev. 2006 Dec; 11: 4: 294–9.
17. Howard B.V. Pathogenesis of diabetic dyslipidaemia. Diabetes Rev 1995; 3: 423–432 .
18. Laakso M. Epidemiology of Diabetic Dyslipidemia. Diabetes Rev 1995; 3: 408–422.
19. Koyama K., Chen G., Lee Y., Unger R.H. Tissue triglycerides, insulin resistance, and insulin production: implications for hyperinsulinemia of obesity // Am. J. Physiol. – 1997. – Vol. 273. – P. 708–713.
20. Ma B., Lawson A.B., Liese A.D. et al. Dairy, magnesium, and calcium intake in relation to insulin sensitivity: approaches to modeling a dosedependent association // Am J Epidemiol. 2006; Sep 1; 164: 5: 449–58.
21. Manzato E., Zambon A., Lapolla A. et al. Lipoprotein Abnormalities in well–treated type II diabetic patients. Diabetes Care 1993; 16: 469–475.
22. Sueta C.A., Clarke S.W., Dunlap S.H. Effect of acute magnesium administration on the frequency of ventricular arrhythmia in patients with heart failure // Circulation. Feb 1994; 89: 660–666.
23. Stamler J., Vaccaro O., Neaton J.D. et al. for the Multiple Risk Factor Intervention Trial Research Group: Diabetes, other risk factors, and 12–yr cardiovascular mortality for men screened in the Multiple Risk Factor Intervention Trial. Diabetes Care 1993; 16: 434–444.
24. Sacks F.M., Pfeffer M.A., Moye L.A. et al. for the Cholesterol and Recurrent Events Trial Investigators. The effect of pravastatin on coronary events after myocardial infarction in patients with average cholesterol levels. N Engl J Med 1996; 335: 1001–1009.
25. United Kingdom Prospective Diabetes Study Group: Tight blood pressure control and risk of macrovascular and microvascular complications in type 2 diabetes: UKPDS 38. BMJ 317:703–713, 1998.












