К сожалению, исследования последних лет убедительно демонстрируют увеличение распространенности МС среди подростков и лиц молодого возраста. Проспективный анализ по распространенности МС также не утешителен – к 2025 году прирост пациентов составит примерно 50%.
Особый интерес и внимание к МС ассоциируется с высокой степенью риска развития и прогрессирования сердечно–сосудистых заболеваний, сопряженных с атеросклерозом и сахарным диабетом 2 типа (СД–2), а также с высокой смертностью от этих заболеваний. Примерно у 70–80% пациентов с СД–2 развивается ишемическая болезнь сердца (ИБС). Атеросклеротические поражения коронарных, цереброваскулярных и периферических сосудов в 80% случаев служат главной причиной летальных исходов у пациентов СД–2. Основные компоненты МС в настоящее время представлены абдоминально–висцеральным ожирением, инсулинорезистентностью и гиперинсулинемией, нарушением толерантности к глюкозе (НТГ) или СД–2, артериальной гипертензией (АГ), дислипидемией, микроальбуминурией, гиперрурикемией, нарушением гемостаза. Кроме этого, МС нередко сопутствуют такие заболевания, как синдром поликистозных яичников, синдром ночного апное, эректильная дисфункция и др.
Центральную позицию в патогенезе МС занимает инсулинорезистентность, частота и степень выраженности которой возрастает по мере увеличения жировой массы тела и характера перераспределения жира с формированием абдоминального типа ожирения. Ожирение, как известно, увеличивает вероятность развития компонентов МС, в частности, АГ, СД–2, дислипидемии. И, наоборот, снижение массы тела значительно улучшает толерантность к глюкозе, снижает уровень АД и триглицеридов.
Инсулинорезистентность является результатом разнообразных взаимоотношений генетических факторов (нарушение рецепторных и пострецепторных механизмов передачи сигнала инсулина) и факторов внешней среды. Среди внешних факторов важнейшее значение имеют нарастающая с каждым годом гиподинамия населения, высококалорийное питание, излишнее употребление алкоголя и др. Следует заметить, что генетическая предрасположенность к инсулинорезистентности может никогда не реализоваться и не проявить себя клинически (МС и/или СД–2) при отсутствии неблагоприятного воздействия внешних факторов. Итак, в результате снижения чувствительности периферических тканей к действию инсулина нарушается поступление глюкозы в инсулинозависимые ткани (мышцы, печень, жировая ткань), повышается продукция глюкозы печенью, иными словами, создаются предпосылки к развитию гипергликемии. Однако благодаря компенсаторному повышению секреции инсулина b–клетками поджелудочной железы состояние нормогликемии может оставаться в течение продолжительного периода времени. С одной стороны, гиперинсулинемия является компенсаторной, т.е. необходимой для преодоления инсулинорезистентности и поддержания нормального транспорта глюкозы в клетки. В то же время гиперинсулинемию можно рассматривать как патологический процесс, способствующий развитию метаболических, гемодинамических, органных нарушений, приводящих в конечном итоге к манифестации СД–2, ИБС и проявлений атеросклероза.
Инсулинорезистентность прежде всего начинает проявлять себя в мышечной ткани, печени, а в последующем, по мере накопления жировой массы, метаболические нарушения происходят в адипоцитах. Скелетные мышцы являются периферической тканевой мишенью, захватывающей 80–90% глюкозы. Поэтому инсулинорезистентность скелетных мышц играет одну из ключевых ролей в патогенезе метаболического синдрома. Молекулярные механизмы инсулинорезистентности включают нарушение передачи гормонального сигнала, активности ферментов и переносчиков, доступности субстратов и модуляции кровотока. У пациентов с СД–2 и ожирением в мышцах нижних конечностей обнаружено снижение кровотока в состоянии покоя, а также неспособность инсулина повышать капиллярный кровоток. Очевидно, что уменьшение доступности циркулирующих в крови глюкозы и инсулина способствуют, таким образом, снижению общего захвата глюкозы скелетными мышцами. Полагают, что в развитие метаболических нарушений вовлечены морфологические изменения скелетных мышц. Установлено, что у больных СД–2 мышцы содержат преимущественно волокна II типа, обладающие более низкой чувствительностью к инсулину по сравнению с волокнами I типа. Мышечные волокна пациентов с СД–2 и/или выраженным ожирением содержат также меньшее число рецепторов к инсулину, в них снижено содержание и степень фосфорилирования ИРС–1 и фосфатидилинозитол–3–киназы. Важным проявлением инсулинорезистнентности у пациентов с СД–2 и ожирением в скелетных мышцах служит нарушение транспорта глюкозы, которое обеспечивается транспортером глюкозы ГЛЮТ–4, что приводит к уменьшению зависимого от инсулина захвата глюкозы. Инсулинорезистентность вызывает не только нарушение захвата глюкозы, но и ее утилизации скелетными мышцами. При СД–2 обнаружено снижение процесса фосфорилирования глюкозы, стимулируемое инсулином при активном участии фермента гексокиназы. Поскольку структура этого фермента, как было показано, не изменена, то полагают, что дефект кроется либо в снижении экспрессии мРНК гексокиназы, либо в снижении активности самого фермента за счет нарушения связывания ее с митохондриями или же уменьшения доступа АТФ. В условиях инсулинорезистентности нарушается окислительный путь метаболизма глюкозы с возрастанием в цитоплазме активности ферментов креатинкиназы и фосфофруктокиназы с последующим усилением анаэробного ресинтеза АТФ. В процессе нарушения инсулинзависимой утилизации глюкозы принимают также участие избыточно образующиеся свободные жирные кислоты (СЖК), способствуя усилению периферической инсулинорезистентности.
Гиперинсулинемия ассоциируется с увеличением массы тела, тем самым в еще большей степени усугубляя степень выраженности ожирения. Как известно, инсулин является своеобразным «сберегателем жира» – его способность стимулировать окисление углеводов и подавлять окисление жирных кислот была продемонстрирована в исследованиях с использованием эугликемического инсулинового клэмпа (введение инсулина вызывало увеличение дыхательного коэффициента). Два своих основных эффекта по накоплению жира инсулин оказывает, воздействуя на ферменты липопротеинлипазу (ЛПЛ) и гормон–чувствительную липазу (табл. 1). Инсулин стимулирует активность ЛПЛ и ингибирует гормон–чувствительную липазу, ускоряя тем самым липогенез и тормозя липолиз. При ожирении из–за большого количества жировой ткани для подавления липолиза требуется и повышенное количество инсулина. В то же самое время чувствительность инсулина к ЛПЛ сохраняется. В результате происходит увеличение массы жира, усиливается процесс липолиза и развивается инсулинорезистентность к инсулину углеводного обмена.
Существенный вклад в прогрессирование инсулинорезистентности и метаболических нарушений вносят сопутствующие нейрогормональные нарушения и повышенная активность симпатической нервной системы. Особая роль в развитии метаболических нарушений отводится абдоминальному типу ожирения. Суть заключается в том, что адипоциты висцерального жира имеют очень высокую плотность и чувствительность b–адренорецепторов (особенно b3–типа), в то же время содержание инсулиновых рецепторов и a–адренорецепторов значительно снижено. Эти особенности и определяют повышенную чувствительность адипоцитов висцерального жира к липолитическому воздействию и низкую чувствительность к антилиполитическому действию инсулина. В результате высокой липолитической активности выделяется огромное количество СЖК, устремляющихся преимущественно через портальную систему в печень. Согласно научным исследованиям избыточная концентрация СЖК в печени препятствует связыванию инсулина гепатоцитами, уменьшает метаболический клиренс инсулина, обусловливая тем самым развитие инсулинорезистентности на уровне печени и системную гиперинсулинемию. СЖК активизируют процессы глюконеогенеза, гликогенолиза, способствуя увеличению продукции глюкозы печенью и развитию гипергликемии натощак. Кроме того, избыточное поступление СЖК в печень становится субстратом для образования атерогенных липопротеидов (ЛПОНП, богатые триглицеридами). В условиях инсулинорезистентности, помимо количественных изменений, в составе липопротеидов низкой плотности (ЛПНП) наблюдаются качественные изменения. Это связывают с повышенным окислительным стрессом, который активируется особенно у пациентов СД–2 в условиях хронической постпрандиальной гипергликемии. При этом ЛПНП, легко окисляясь, усиленно поглощаются макрофагами, которые превращаются в пенистые клетки и инфильтрируют стенки сосудов. Периваскулярное отложение жира также способствует развитию эндотелиальной дисфункции, нарушающей реактивность и сосудистый тонус. Наряду с этим хроническое повышение СЖК, поступающих в системный кровоток, оказывает прямое повреждающее воздействие (липотоксический эффект) на функцию b–клеток поджелудочной железы. В конечном итоге инсулина, вырабатываемого b–клетками, может оказаться недостаточно для преодоления инсулинорезистентности, что неминуемо повлечет за собой развитие относительного дефицита инсулина, со всеми вытекающими из этого последствиями – умеренная гипергликемия вплоть до полной манифестации СД–2. Итак, характерными признаками дислипидемии при МС являются: гипертриглицеридемия, повышение ЛПОНП и ЛПНП, изменение структуры ЛПНП, снижение ЛПВП. Следует обратить особое внимание и помнить о том, что МС у пациентов ассоциируется с постпрандиальной гиперлипидемией. В условиях инсулинорезистентности гиперинсулинемия принимает активное участие в механизмах, участвующих в регуляции артериального давления (АД). Механизмы повышения АД реализуются посредством стимуляции центров симпатической нервной системы, повышения чувствительности сосудов к прессорным агентам (ангиотензин II, катехоламины), увеличения реабсорбции натрия и воды проксимальными канальцами почек, изменения электролитного состава клеток гладкой мускулатуры сосудов. Вместе с этим гиперинсулинемия способствует пролиферации сосудистых гладкомышечных клеток, фибробластов, избыточному синтезу коллагена, повышению сосудистого сопротивления.
Инсулинорезистентность, гиперинсулинемия и дислипидемия также способствуют развитию нарушений в свертывающей системе крови. Характерными признаками прокоагулянтного состояния являются повышенный уровень фибриногена и протромбогенного фактора XIII свертывания крови, а также снижение активности фибринолиза вследствие накопления ингибитора фибринолиза фактора VII и ингибитора активатора плазминогена – 1 (ИАП–1).
Таким образом, инсулинорезистентность и сопутствующая ей гиперинсулинемия вместе с сопряженными с ними метаболическими нарушениями вносят большую лепту в развитие и прогрессирование СД–2, АГ, атеросклероза.
В апреле 2005 г. на I Международном конгрессе по предиабету и МС в Берлине были выдвинуты единые, ставшие более жесткими, критерии МС. В отличие от ранее существующих критериев МС, принципиально новой позицией является утверждение абдоминального ожирения основным диагностическим критерием с изменением параметров окружности талии для мужчин > 94 см, для женщин >80 см у европеоидной расы при сочетании, как минимум, с двумя из следующих факторов:
• уровень триглицеридов (ТГ) > 1,7 ммоль/л или специфическое лечение дислипидемии;
• снижение ЛПВП <1,03 ммоль/л у мужчин и <1,29 ммоль/л у женщин или специфическое лечение;
• повышение систолического АД > 130 и диастолического АД >85 мм рт.ст.;
• повышение глюкозы венозной плазмы натощак > 5,6 ммоль/л или ранее установленный СД–2.
Помимо основных диагностических критериев, IDF рекомендует также изучение ряда дополнительных факторов, сопряженных с МС. В частности, рекомендуется определять характер распределения жира и биомаркеры жировой ткани (лептин и адипонектин), содержание жира в печени, показатели инсулинорезистентности (уровень инсулина/проинсулина натощак, индекс HOMA, СЖК), показатели дислипидемии, сосудистые нарушения (эндотелиальная дисфункция) микроальбуминурия и т.д. Безусловно, изучение дополнительных факторов, ассоциированных с МС, послужит ценным научным вкладом для понимания их роли в развитии сердечно–сосудистых заболеваний и СД–2.
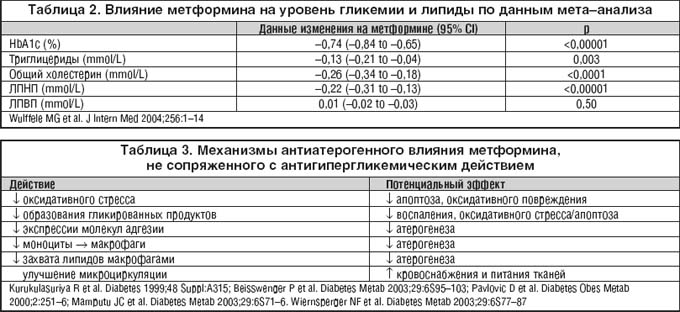
Сегодня уже ни у кого не вызывает сомнения – залогом успешного лечения МС служит прежде всего модификация образа жизни, что нашло свое научное подтверждение в исследованиях Diabetes Prevention Study, проведенное в Финляндии, и Diabetes Prevention Program, выполненное в США. Пожалуй, это самое сложное как для наших пациентов в плане приверженности выполнения врачебных рекомендаций, так и для самого врача. Ведь от врача требуются не только профессиональные знания, но и огромное терпение, большие затраты собственной энергии для формирования устойчивой мотивации, на выполнение пациентом в течение длительного периода времени рекомендаций по режиму питания, физической активности, искоренению вредных привычек, приему лекарственных препаратов. Многим пациентам, как подсказывает и собственный опыт, не под силу справиться с задачей по изменению образа жизни. Мы все прекрасно понимаем, что в подобных случаях не представляется возможным обойтись без подключения медикаментозной терапии. На современном этапе также не возникает сомнений и в том, что одним из наиболее эффективных и доступных для пациентов лекарственных препаратов в борьбе с инсулинерезистентностью является метформин (Глюкофаж). Согласно рекомендациям IDF (Internation Diabetes Federation, 2005 г.) метформин рекомендуется в качестве первого препарата для пациентов с СД–2. Основное действие метформина направлено на устранение инсулинорезистентности печени и периферических тканей. В печени метформин ингибирует процессы глюконеогенеза (из лактата) и гликогенолиза, а также подавляет окисление СЖК и липидов. Стимуляция тирозинкиназной активности инсулинового рецептора и активация транспортера глюкозы ГЛЮТ–4 под влиянием метформина способствует повышению поглощения глюкозы и увеличению чувствительности к инсулину жировой и мышечной тканей. Помимо антигипергликемического действия, метформин оказывает антиатерогенный эффект. Лечение метформином пациентов с СД–2, ожирением улучшает показатели липидного профиля, способствуя снижению триглицеридов в среднем на 10–20%, холестерина ЛПНП – на 10%, СЖК – на 10–30%, повышению ЛПВП в среднем на 10–20% (табл. 2).
Оптимальными значениями липидов у пациентов с повышенным риском развития сердечно–сосудистых заболеваний, включая и СД–2, в соответствии с Европейскими и Российскими рекомендациями по профилактике атеросклероза являются следующие показатели: общий холестерин – <4,5 ммоль/л; ХС ЛНП – <2,5 ммоль/л; ТГ – <1,7 ммоль/л; ХС ЛПВП – >1,03 ммоль/л (для мужчин), >1,2 ммоль/л (для женщин).
Очень важной особенностью в действии метформина является замедление всасывания углеводов из кишечника, обеспечивающего уменьшение постпрандиальной гликемии. Метформин обладает анорексигенным эффектом. Снижение потребления пищи активно сказывается на снижении массы тела пациентов, а значит, на степени ожирения. В разных исследованиях показано, что метформин оказывает благоприятное воздействие на систему гемостаза и реологические свойства крови (уменьшает активность прокоагулянтных факторов, активирует фибринолиз, угнетает активность ИАП–1), улучшает эндотелий–зависимую вазодилатацию (табл. 3). Кардиопротективное действие метформина впервые было изучено в исследовании UKPDS (UK Prospective Diabetes Study, 1998 г.), в котором использовался оригинальный метформин – Глюкофаж, а в последующем подтверждено результатами исследования PRESTO (Prevention of REStenosis with Tranilast and its Outcomes). В рамках последнего исследования показано, что применение метформина снижает относительный риск развития любого сердечно–сосудистого осложнения более чем на 20%, смертельных исходов на 60%, инфаркта миокарда примерно на 70%, операции реваскуляризации сосудов на 20%.
Все положительные стороны действия метформина позволили применять его в качестве препарата для первичной профилактики СД–2 (Diabetes Prevention Program, 2002 г.).
В начале статьи мы говорили о том, что первой ступенькой в лечении пациентов с МС и/или СД–2 является модификация образа жизни. В случае неудачи пациенту рекомендован метформин. В настоящее время активно обсуждаются вопросы об одномоментном с изменением стиля жизни подключении метформина, а также о возможном расширении показаний для его применения.
В заключение можно еще раз по достоинству оценить препарат метформин (Глюкофаж), особенно в связи с установленным в последние годы его кардиопротективным эффектом, и рекомендовать в качестве препарата первого выбора пациентам с метаболическим синдромом.