Коррекция ИР, ключевого звена СД 2 типа – одно из важных направлений фармакотерапии, и в настоящее время к числу препаратов первого выбора относится метформин [9,10,15]. Основные фармакологические эффекты метформина являются результатом воздействия на чувствительность к инсулину на уровне печени, мышечной и жировой тканей. Хотя преобладающим является его влияние на продукцию глюкозы печенью, именно комбинация его эффектов на указанных уровнях, по–видимому, обусловливает благоприятный фармакологический профиль препарата. При этом, повышая чувствительность печени и периферических тканей к инсулину, метформин не влияет на секрецию гормона [10,15].
Основным механизмом действия метформина является снижение гепатической продукции глюкозы, что связано с подавлением процессов глюконеогенеза и в меньшей степени гликогенолиза. Препарат способствует инсулин–индуцированному подавлению глюконеогенеза из таких предшественников глюкозы, как лактат, пируват, глицерол и некоторые аминокислоты, а также противодействует глюконеогенетическому действию глюкагона. В первую очередь это происходит вследствие торможения поступления перечисленных субстратов и ингибирования ключевых ферментов глюконеогенеза в гепатоцитах – пируваткарбоксилазы, фруктозо–1,6–бифосфатазы и глюкозо–6–фосфатазы [10]. Общепризнано, что последствия повышенной гепатической продукции глюкозы в ночное время крайне неблагоприятны ввиду стимуляции процессов атерогенеза. Под влиянием метформина со стороны рецепторов инсулина наблюдается повышение их числа и аффинности. Кроме того, происходит стимуляция тирозинкиназной активности инсулинового рецептора, а также экспрессии и активности транспортеров глюкозы, их транслокация из внутриклеточного пула на клеточную мембрану [10,14,15]. Вышеперечисленные процессы приводят к увеличению поглощения глюкозы органами–мишенями инсулина – печенью, мышечной и жировой тканями. Усиливая кровообращение в печени и ускоряя процесс превращения глюкозы в гликоген, метформин увеличивает синтез печеночного гликогена.
Следует отметить, что метформин оказывает влияние на всасывание углеводов в желудочно–кишечном тракте, замедляя его скорость, а также снижает аппетит [10,13]. Интестинальные эффекты метформина вносят существенный вклад в предотвращение постпрандиальных гипергликемических пиков, ассоциированных с риском преждевременной смертности от ССЗ [12,16,20]. Полагают, что один их механизмов анорексигенного действия метформина связан с влиянием препарата на метаболизм глюкогоноподобного пептида–1 (ГПП–1), регулирующего пищевое поведение. Так, в работе Mannucci E. с соавт. (2001) определяли уровни ГПП–1 (7–36) амида/(7–37) исходно и через 15 дней терапии метформином (25–50 мг/сут.) у больных с ожирением до и после нагрузки глюкозой [13]. С целью устранения влияния инсулинемии и гликемии на секрецию ГПП–1 исследование проводилось в условиях эугликемического гиперинсулинемического клэмпа. Авторы не обнаружили изменений концентраций ГПП–1 у лиц контрольной группы. В то же время у больных с ожирением метформин вызывал существенное увеличение концентрации ГПП–1 (7–36)амида/(7–37) на 30 и 60–й минутах теста при неизмененном базальном уровне пептида. В смешанной плазме (после 30 мин. инкубации при 37оС), а также в растворе буфера, содержащем дипептидил–пептидазу–4, метформин ингибировал деградацию ГПП–1. Согласно результатам экспериментальных исследований на животных моделях анорексигенный эффект метформина, по–видимому, также связан с центральным действием препарата на уровне гипоталамических нейронов [5]. Модулируя экспрессию орексигенного нейропептида Y, метформин способствует снижению массы тела. Другим важным эффектом метформина является уменьшение или стабилизация массы тела, а также снижение отложения висцерального жира [4,11,17].
Вот уже полвека, как метформин с быстрым высвобождением используется в клинической практике. Практически все последние рекомендации для лечения сахарного диабета 2 типа (ADA/EASD, NICE – National Institute for Health and Clinical Excellence, Великобритания, а также отечественный Проект), в качестве первого сахароснижающего препарата рекомендуют использовать метформин. Эта рекомендация основана преимущественно на данных Проспективного британского исследования сахарного диабета 2 типа (UKPDS – UK Prospective Diabetes Study), показавшего снижение частоты микро– и макрососудистых осложнений на фоне приема метформина. К сожалению, применение метформина ограничено из–за желудочно–кишечных побочных эффектов, развивающихся у значительной части пациентов (до 25%) [8]. По различным данным, 5–10% пациентов прекращает прием препарата в связи с негативными явлениями со стороны желудочно–кишечного тракта [8], механизм развития которых пока не установлен. Фармакокинетика метформина с быстрым высвобождением и его прием не менее двух раз в сутки снижают приверженность пациентов к терапии [6]. Низкая комплайентность больных к терапии при хронических заболеваниях является глобальной проблемой. Исправить сложившуюся ситуацию можно, если в арсенале врачей все чаще будут появляться эффективные и безопасные лекарства, позволяющие минимизировать кратность их приема.
Абсолютная биодоступность метформина, введенного per os, cоставляет 50–60%. Почти весь метформин, попадающий в кровоток, всасывается на ограниченном участке верхних отделов желудочно–кишечного тракта (рис. 1), и лишь незначительная часть метформина всасывается в более дистальных отделах пищеварительного тракта.
Кроме того, всасывание метформина в тонком кишечнике является «насыщающимся». Это означает, что при увеличении концентрации метформина в просвете кишечника выше определенного порогового уровня происходит «насыщение всасывания», тем самым значительная часть препарата проходит мимо «окна абсорбции» и не всасывается вовсе. Таким образом, уровень всасывания метформина из ЖКТ зависит от скорости эвакуации метформина из желудка.
Эти особенности определяют сложность разработки таблеток метформина с замедленным высвобождением, пригодных для приема один раз в сутки.
Традиционно используемые для этого лекарственные формы основываются на простом замедлении высвобождения активного вещества из таблетки, а его всасывание происходит на всем протяжении кишечника. Но даже в этом случае нередко имеется период относительно быстрого поступления препарата в кровоток вскоре после приема таблетки.
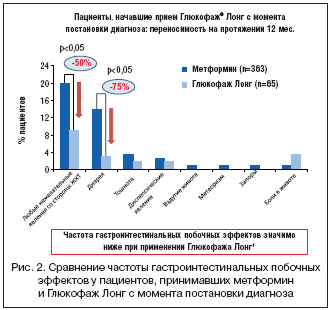
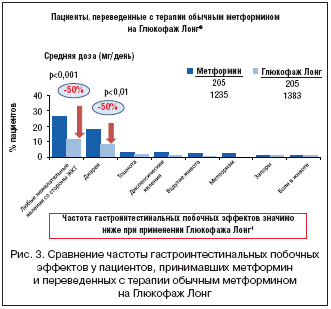
Такое традиционное строение таблетки нельзя применить для препарата Глюкофаж® Лонг ввиду того, что метформин не будет всасываться после прохождения таблеткой абсорбционного окна. Кроме того, начальный период быстрого высвобождения вещества из таблетки может «насытить» абсорбционное окно и привести к потере активного ингредиента. После приема метформина с быстрым высвобождением пиковая концентрация препарата в крови наступает в течение 3 часов. Разработанная новая форма метформина XR (Глюкофаж Лонг) имеет целью устранить проблемы, связанные с желудочно–кишечной непереносимостью, с одной стороны, и многократным приемом препарата, с другой стороны. Замедленное высвобождение препарата увеличивает время достижения пиковой концентрации до 7 часов при снижении ее максимального уровня [19]. Таким образом, лекарственная форма Глюкофаж Лонг имеет сниженную пиковую концентрацию, но аналогичную с метформином быстрого высвобождения биодоступность. В рандомизированном двойном слепом исследовании в параллельных группах Глюкофаж Лонг показал такую же эффективность в снижении уровня гликированного гемоглобина, как и метформин быстрого высвобождения [7]. С целью сравнения гастроинтестинальной переносимости метформина с пролонгированным и быстрым высвобождением был проведен ретроспективный анализ медицинских карт пациентов с сахарным диабетом 2 типа в четырех центрах США, где было выявлено существенное снижение частоты желудочно–кишечных нежелательных явлений у пациентов, переведенных с терапии метформином быстрого высвобождения на Глюкофаж Лонг [2] (рис. 2 и 3).
Пролонгированный эффект Глюкофажа Лонг обеспечивается оригинальной структурой таблетки (рис. 4), в которой создана система диффузии через гелевый барьер (рис. 5). Метформин содержится внутри двухслойного гидрофильного полимерного матрикса, что обеспечивает высвобождение препарата путем диффузии. Наружный, закрытый полимерный матрикс (без метформина) окружает внутренний полимер, содержащий суммарно 500 мг метформина в таблетке. При проглатывании, таблетка впитывает влагу и набухает, образуя слой геля на внешней стороне таблетки, что обеспечивает дозированное высвобождение метформина в кишечнике. Важно отметить, что скорость растворения метформина не зависит от перистальтики, уровня pH, что помогает свести к минимуму вариабельность поступления метформина в ЖКТ как у одного пациента, так и в группах пациентов.
Всасывание метформина из таблетки с пролонгированным высвобождением медленное и более длительное по сравнению с обычной формой. В исследовании по фармакокинетике изучались метформин с пролонгированным высвобождением (2000 мг один раз в сутки) и обычный метформин (1000 мг два раза в сутки) после достижения равновесной концентрации. Время достижения максимальной концентрации в плазме (Tmax) после приема метформина с пролонгированным высвобождением было больше, чем после обычного метформина (7 часов по сравнению с 3–4 часами). Кроме того, максимальная концентрация препарата в плазме (Cmax) на фоне приема пролонгированной формы была на 25% меньше. Суммарное воздействие метформина на пациента было сходным. В действительности, анализ площади под кривой зависимости концентрация–время свидетельствует о биоэквивалентности данных препаратов.
Таким образом, фармакокинетический профиль метформина с пролонгированным высвобождением позволяет избежать быстрого подъема концентрации метформина в плазме, характерного для обычного метформина. Более плавное поступление метформина позволяет избежать появления нежелательных явлений со стороны ЖКТ, и может улучшать переносимость препарата.
Повышение приверженности пациентов к лечению, а также снижение нежелательных явлений со стороны желудочно–кишечного тракта являются важными достоинствами препарата, однако первостепенное значение имеет влияние на показатели гликемии у больных сахарным диабетом 2 типа. Полученные результаты подтверждают имеющиеся данные, что сахароснижающий эффект метформина с пролонгированным высвобождением при приеме 1 раз в сутки сравним с эффектом обычного метформина, назначаемого в несколько приемов в течение дня.
В исследовании по определению дозы Глюкофажа Лонг была показана его дозозависимая эффективность при приеме 1 раз в сутки. Максимальное действие этой формы препарата было достигнуто на дозе 1500–2000 мг/сут. В проведенном исследовании также изучалась эффективность Глюкофажа Лонг 1000 мг, назначаемым 2 раза в сутки по сравнению с однократным приемом той же формы, но в дозе 2000 мг 1 раз в сутки. Динамика уровня HbA1c (снижение в среднем на 1,2% при режиме 1000 мг 2 раза в сутки) была сходной с таковой для группы пациентов, получавших препарат 2000 мг 1 раз в сутки (снижение в среднем на 1%).



Литература
1. Бутрова С.А. Метаболический синдром: патогенез, клиника, диагностика, подходы к лечению. // РМЖ 2001; 2 (9): 56–60
2. Blonde L, Dailey GE, Jabbour SA, Reasner CA, Mills DJ. Gastrointestinal tolerability of extended–release metformin tablets compared to immediate–release metformin tablets: results of a retrospective cohort study. Curr Med Res Opin 2004; 20: 565–572.
3. Bosello O., Zamboni M. Visceral obesity and metabolic syndrome// Obes. Rev.–2000, 1, 47–56
4. Charles M.A., Eschwege E., Grandmottet T. et al. Treatment with metformin of non–diabetic men with hypertension. Hypertriglyceridemia and central fat distribution: the BIGPRO 1.2 trial. // Diabetes Metab Res Rev.– 2000; 16: 2–7
5. Chau–Van C., Gamba M., Salvi R. et al. Metformin Inhibits Adenosine 5’–Monophosphate–Activated Kinase Activation and Prevents Increases in Neuropeptide Y Expression in Cultured Hypothalamic Neurons. // Endocrinology.– 2007; 148(2): 507 – 511.
6. Donnan PT, MacDonald TM, Morris AD. Adherence to prescribed oral hypoglycaemic medication in a population of patients with Type 2 diabetes: a retrospective cohort study. Diabet Med 2002; 19: 279–284.
7. Fujioka K, Pans M, Joyal S. Glycemic control in patients with type 2 diabetes mellitus switched from twice–daily immediate–release metformin to a once–daily extendedrelease formulation. Clin Ther 2003; 25: 515–529.
8. Garber AJ, Duncan TG, Goodman AM, Mills DJ, Rohlf JL. Efficacy of metformin in type II diabetes: results of a double–blind, placebo–controlled, dose–response trial. Am J Med 1997; 103: 491–497.
9. Kahn BB, Flier JS: Obesity and insulin resistance.// J Clin Invest 2000;106:473–81
10. Kirpichnikov D., McFarlane S.I., Sowers J.R, Metformin:An Update //Ann Intern Med. 2002; 137: 25 –33
11. Kurukulasusuriya R., Banerij M.A., Chaiken R., Lebovitz H. Selective decrease in visceral fat is associated with weight loss during metformin treatment in African Americans with type 2 diabetes (abstract)/ //Diabetes.1999; 48: A315.
12. Laaksonen D.F., Laaka H.M., Niskanen L.K. et al Metabolic syndrome and development of diabetes mellitus: application and validation of recently suggested definition of the metabolic syndrome in a prospective cohort stady. // Am J Epidemiol. 2002; 156, 1070–7.
13. Mannucci E., Ognibene A.,, Cremasco F. et al Effect of Metformin on Glucagon–Like Peptide 1 (GLP–1) and Leptin Levels in Obese Nondiabetic Subjects . // Diabetes Care 2001; 24 (3): 489–494
14. Matthaei S., Hamann A., Klein H.H., Benecke H. et al. Association of Metformin’s effect to increase insulin–stimulated glucose transport with potentiation of insulin–induced translocation of glucose transporters from intracellular pool to plasma membrane in rat adipocytes // Diabetes 1999; 40(7): 850–857
15. Matthaei S., Stumvoll M., Kellerer M., Haring H.–U. Pathophysiology and pharmacological treatment of insulin resistance// Endocr. Rev. 2000; 21(6): 585 – 618
16. McFarlane S.I., Banerij M., Sowers J.R. Insulin resistance and cardiovascular disease. //J Clin Endocrinol Metab. 2001; 86: 713–8
17. Srinivasan S., Ambler G. R., Baur L.A. Randomized, Controlled Trial of Metformin for Obesity and Insulin Resistance in Children and Adolescents: Improvement in Body Composition and Fasting Insulin.// J. Clin. Endocrinol. Metab. 2006; 91(6): 2074 – 2080.
18. The IDF concensus worldwide definition of the metabolic syndrome. Availeble from: http://www.idf.org
19. Timmins P, Donahue S, Meeker J, Marathe P. Steadystate pharmacokinetics of a novel extended–release metformin formulation. Clin Pharmacokinet 2005; 44: 721–729.
20. Visseren F.L.J. Vascular consequences of metabolic syndrome in early life. // EHJ 2008 29: 693–694.












