Клинические проявления гиперкальциемии наблюдаются лишь при повышении уровня общего кальция до 12–14 мг/дл.
Алиментарный фактор в формировании патологической гиперкальциемии в настоящее время не актуален. Это обусловлено диетологическими пристрастиями и особенностями.
Суточное потребление кальция можно рассчитать при помощи формулы:
суточная потребность в кальции = кальций молочных продуктов (мг) + 350 мг.
При анкетировании пациентов, больных ОП, было выявлено:
• 45% принимали, по их мнению, достаточное количество кальция с продуктами питания. Однако при анализе пищевых дневников было отмечено, что всего 11% получают дневную норму кальция, 3% получают незначительное избыточное количество, а 86% не получают достаточного количества;
• 38% отметили, что «не доедают» продукты, богатые кальцием;
• 27% респондентов затруднились ответить.
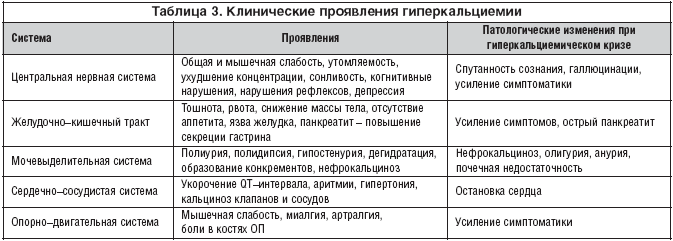
Причины гиперкальцемии представлены в таблице 2. Клинические проявления гиперкальциемии отличаются многообразием (табл. 3).
Наиболее частой причиной гиперкальциемии является преобладание резорбции костной ткани над ее образованием, что приводит к развитию вторичного ОП. Таким образом, неоспорима взаимосвязь между ОП и гиперкальциемией.
Лечение гиперкальциемии, также как и ОП, носит патогенетический характер, так, параллельно с симптоматической терапией проводится комплекс диагностических мероприятий, направленных на верификацию причины.
Первичный гиперпаратиреоз является наиболее частой причиной гиперкальциемии. Его частота возрастает через 30 и более лет после радиационного облучения шеи. Она также выше у женщин и в пожилом возрасте. Первичный гиперпаратиреоз существует в несемейной и семейной формах.
Гистологические исследования обнаруживают аденому паращитовидной железы почти у 90% больных, хотя при легкой гиперкальциемии (уровень кальция ниже 12 мг) иногда трудно отличить аденому от нормальной ткани железы. Остальные 10% случаев – это гиперплазия двух или более паращитовидных желез (7%) и рак паращитовидной железы (3%). Таким образом, у данной категории пациентов необходимо проводить хирургическое лечение – экстирпацию паращитовидной железы.
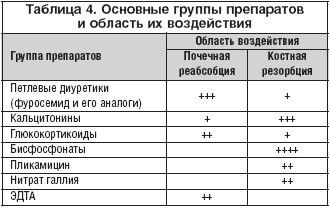
Основными патогенетическими направлениями в коррекции гиперкальциемии (табл. 4), что объединяется с ведением больных ОП, являются препараты:
• влияющие на костную резорбцию;
• подавляющие почечную реабсорбцию кальция;
• комплексного воздействия.
В ряде случаев для терапии гиперкальциемии используется гемодиализ.
В настоящее время бисфосфонаты являются «золотым стандартом», а также наиболее перспективными препаратами не только для лечения, но и для профилактики ОП. В России зарегистрированы препараты следующих групп бисфосфонатов: алендронат, ибандронат, золендроновая кислота, ризиндронат, азотсодержащие препараты [1]. К последней группе относится монокалиевая соль дигидрат 1–гидроксиэтилидендифосфорной кислоты. Ксидифон является синтетическим аналогом неорганического пирофосфата, способным взаимодействовать с кальцием на уровне клетки. Он восстанавливает нормальный минеральный обмен, предотвращает избыточное выведение кальция из костей и отложение его в виде малорастворимых солей в мягких тканях и суставах. Также снижается количество и активность остеокластов. Важным влиянием препарата является возможность поддержания кальция в растворенном состоянии: это уменьшает возможность образования нерастворимых соединений кальция с оксалатами, мукополисахаридами и фосфатами, что способствует предупреждению рецидивов камнеобразования. Помимо этого, Ксидифон оказывает тормозящее действие на выделение медиаторов воспаления и аллергии – лейкопротеинов и фактора активации тромбоцитов, – снижает степень дегрануляции базофилов (является показателем уровня сенсибилизации), увеличивает содержание Т–супрессоров, снижает уровень иммуно-глобулина Е в плазме и трансмембранное перемещение ионов кальция в стимулированных лейкоцитах, что крайне важно при присоединении инфекции и склонности к камнеобразованию.
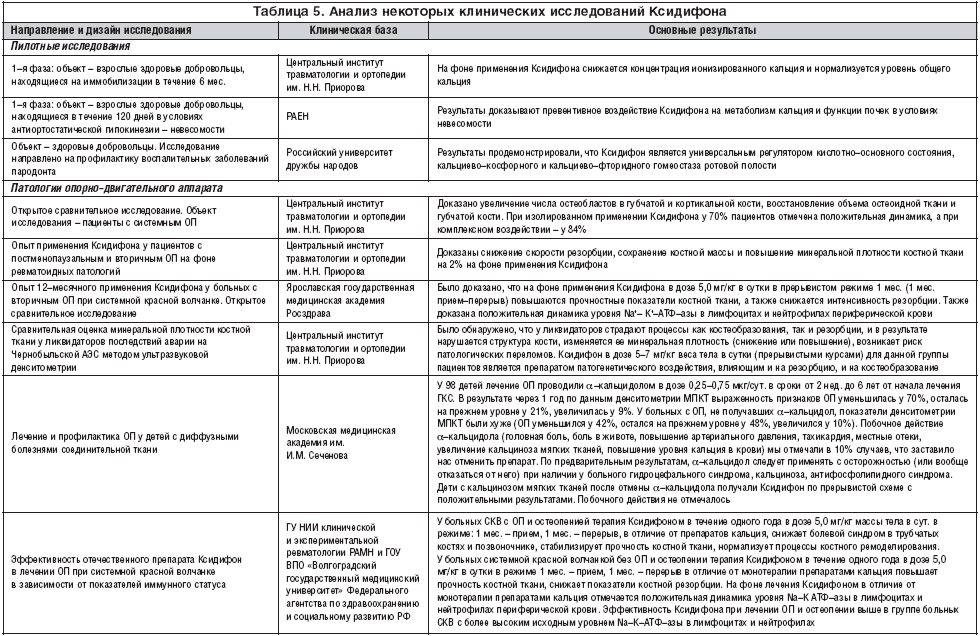
С середины 80–х годов ХХ в. проводились клинико–экспериментальные исследования [1,3–6,11–13] эффективности, безопасности и областей применения Ксидифона (табл. 5).
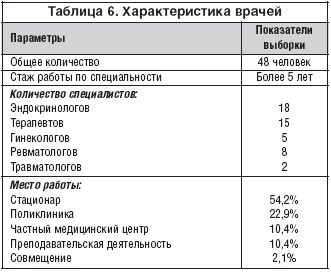
Ряд работ [7–10] продемонстрировали профилактическое воздействие Ксидифона на рецидивы мочекаменной болезни, отмечено местное анальгезирующее действие у больных с дисметаболическй нефропатией, остеохондрозом, прогрессирующим оссифицирующим миозите и невралгии, выведение ряда тяжелых металлов (хрома, висмута, кремния, свинца, бора и др.), уменьшение кристалурии, снижение липидурии и т.д. Таким образом, учитывая широкие терапевтические возможности бисфосфоната – Ксидифона, проведено анкетирование врачей следующих специальностей – эндокринологов, терапевтов, гинекологов, ревматологов и травматологов. Характеристика интервьюируемых представлена в таблице 6.
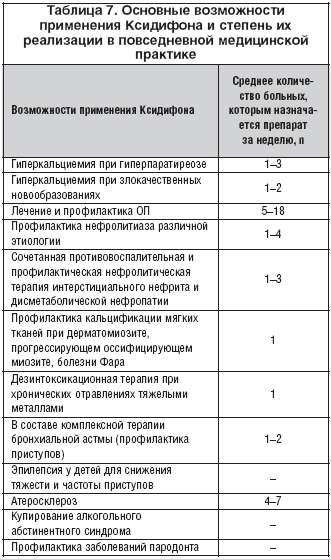
Всем врачам были заданы вопросы о применении Ксидифона в своей практике, основные результаты анкетирования представлены в таблице 7.
В ряде случаев низкая частота применения бисфосфонатов, по всей видимости, обусловлена особенностями выборки анкетируемого контингента. Однако в ряде случаев, например при лечении атеросклероза, причина кроется в недостаточной информированности врачей. Таким образом, целесообразно более активное использование всех современных препаратов, учитывая их фармакологические возможности.


Литература
1. Остеопороз. Диагностика, профилактика и лечение. Клинические рекомендации / Под. ред. О.М. Лесняк, Л.И. Беневоленской. М.: «ГЭОТАР–Медиа», 2010.
2. NIH Consensus Development Conference on Osteoporosis: Prevention, Diagnosis and Therapy. JAMA, 2000 № 287 р. 785–795
3. Вельтищев Ю.Е. Ксидифон – новое средство регуляции кальция в организме при патологии // Деп ВНИИМИ № 72–13–85. 1985. С. 180.
4. Вельтищев Ю.Е., Юрьева Э.А., Архипова О.Г., Алексеева Н.В. Способ диагностики гиперпаратиреоза у больных остеопороом и мочекаменной болезнью: Авт. свид. № 1347017.
5. Беляева Е.А. Остеопроз в клинической практике: от современного диагноза к рациональной терапии // Consilium Medicum. Т. 11. 2009. № 2. С. 13–16.
6. Ершова А.К. О применении препарата Ксидифон при нарушениях кальциевого обмена // РМЖ. 2010. №14 (378). С. 884–886.
7. Чалов М.Б., Архипова О.Г., Криницкая Л.В. и др. Антиканцерогенная активность Ксидифона у экспериментальных животных // Новый хелатирующий агент– Ксидифон. М., 1990. С. 70–74.
8. Козлов С.А., Карлов В.А., Селезнев В.И. и др. Применение Ксидифона в комплексной терапии эпилептических припадков // Новый хелатирующий агент – Ксидифон. М., 1990. С. 30–32
9. Дорофеева М.Ю., Юрьева Э.А., Темин П.А. Изучение эффективности ксидифона в лечении резистентных форм эпилепсии // Материалы VIII съезда педиатров России. М., 1998. С. 290–291.
10. Карлов В.А. Терапия нервных болезней. М., 1990.
11. Родионова С.С., Соловов В.Д., Дорохов В.В., Банаков В.В. Сравнительная оценка минеральной плотности костной ткани у ликвидаторов последствий аварии на ЧАЭС методом ультразвуковой денситометрии // Настоящее и будущее костной патологии. М., 1997. С. 116–118.
12. Голованова Н.Ю., Лыскина Г.А., Шарова А.А., Им В.Л. Лечение и профилактика остеопороза у детей с диффузными болезнями соединительной ткани // http://www.mediasphera.aha.ru /mjmp/2000/11/r11–00–20.htm
13. Коренская Е.Г. Эффективность отечественного препарата Ксидифон в лечении остеопороза при системной красной волчанке в зависимости от показателей иммунного статуса: Автореферат диссертации на соискание ученой степени кандидата медицинских наук. Волгоград, 2007.












