–С–Є–Њ–Љ–µ—Е–∞–љ–Є–Ї–∞ –њ–∞–і–µ–љ–Є—П
–Я–∞–і–µ–љ–Є–µ, –Ї–∞–Ї –њ—А–∞–≤–Є–ї–Њ, –Њ–±—Г—Б–ї–Њ–≤–ї–µ–љ–Њ –Љ–љ–Њ–ґ–µ—Б—В–≤–Њ–Љ –њ—А–Є—З–Є–љ, –Є –≤—Б–µ –ґ–µ –Ї–ї—О—З–µ–≤–Њ–є —Д–∞–Ї—В–Њ—А – —Н—В–Њ –љ–µ—Б–њ–Њ—Б–Њ–±–љ–Њ—Б—В—М –Њ—В–і–µ–ї—М–љ–Њ–≥–Њ —З–µ–ї–Њ–≤–µ–Ї–∞ –∞–і–µ–Ї–≤–∞—В–љ–Њ «–Њ—В–≤–µ—В–Є—В—М» –љ–∞ –њ–Њ—В–µ—А—О —А–∞–≤–љ–Њ–≤–µ—Б–Є—П, —Б–Љ–µ—Й–µ–љ–Є–µ —Ж–µ–љ—В—А–∞ —В—П–ґ–µ—Б—В–Є. –Я–Њ—З—В–Є –ї—О–±–Њ–µ –і–≤–Є–ґ–µ–љ–Є–µ –≤ —В–µ—З–µ–љ–Є–µ –і–љ—П —Б–≤—П–Ј–∞–љ–Њ —Б –њ–µ—А–µ–Љ–µ—Й–µ–љ–Є–µ–Љ —Ж–µ–љ—В—А–∞ —В—П–ґ–µ—Б—В–Є, –∞ —Г–і–µ—А–ґ–∞–љ–Є–µ —А–∞–≤–љ–Њ–≤–µ—Б–Є—П –Њ–Ј–љ–∞—З–∞–µ—В —Г–і–µ—А–ґ–∞–љ–Є–µ —Ж–µ–љ—В—А–∞ —В—П–ґ–µ—Б—В–Є –љ–∞–і –Њ–њ–Њ—А–Њ–є [10]. –†–µ–∞–Ї—Ж–Є—П —Г–і–µ—А–ґ–∞–љ–Є—П –±–∞–ї–∞–љ—Б–∞ –Љ–Њ–ґ–µ—В –Њ—Б—Г—Й–µ—Б—В–≤–ї—П—В—М—Б—П –њ—Г—В–µ–Љ –љ–∞–њ—А—П–ґ–µ–љ–Є—П –Љ—Л—И—Ж –≥–Њ–ї–µ–љ–Є, –±–µ–і—А–∞, —Б–≤—П–Ј–Њ—З–љ–Њ–≥–Њ –∞–њ–њ–∞—А–∞—В–∞ —Б—Г—Б—В–∞–≤–∞, –∞ —З–∞—Й–µ –ї—О–і–Є —Г–≤–µ–ї–Є—З–Є–≤–∞—О—В –њ–ї–Њ—Й–∞–і—М –Њ–њ–Њ—А—Л, —Б–Њ–≤–µ—А—И–∞—П —И–∞–≥ –Є–ї–Є —Г–і–µ—А–ґ–Є–≤–∞—П—Б—М –Ј–∞ –њ–Њ—Б—В–Њ—А–Њ–љ–љ–Є–є –њ—А–µ–і–Љ–µ—В [11,12]. –†–µ–∞–Ї—Ж–Є—П «–Є–Ј–Љ–µ–љ–µ–љ–Є–µ –њ–ї–Њ—Й–∞–і–Є –Њ–њ–Њ—А—Л» –Є–Љ–µ–µ—В –±–µ—Б—Б–њ–Њ—А–љ–Њ–µ –њ—А–µ–Є–Љ—Г—Й–µ—Б—В–≤–Њ, —Б–Њ–≤–µ—А—И–∞–µ—В—Б—П –Њ—З–µ–љ—М –±—Л—Б—В—А–Њ, —А–µ—Д–ї–µ–Ї—В–Њ—А–љ–Њ, –Є –њ—А–µ–≤–Њ—Б—Е–Њ–і–Є—В –њ–Њ —Б–Ї–Њ—А–Њ—Б—В–Є –Є —В–Њ—З–љ–Њ—Б—В–Є –ї—О–±–Њ–µ –Ј–∞—А–∞–љ–µ–µ —Б–њ–ї–∞–љ–Є—А–Њ–≤–∞–љ–љ–Њ–µ –Њ—Б–Њ–Ј–љ–∞–љ–љ–Њ–µ –і–≤–Є–ґ–µ–љ–Є–µ [13]. –£—Б–њ–µ—Е –Є–ї–Є –љ–µ—Г—Б–њ–µ—Е —Г–і–µ—А–ґ–∞–љ–Є—П –±–∞–ї–∞–љ—Б–∞ –Ј–∞–≤–Є—Б–Є—В –Њ—В —Б–њ–Њ—Б–Њ–±–љ–Њ—Б—В–Є –Њ—А–≥–∞–љ–Є–Ј–Љ–∞ –≤ –Ї—А–∞—В—З–∞–є—И–Є–µ —Б—А–Њ–Ї–Є –Њ—Ж–µ–љ–Є—В—М –≤–Њ–Ј–Љ–Њ–ґ–љ—Л–µ –њ—А–µ–њ—П—В—Б—В–≤–Є—П, –љ–∞–њ—А–∞–≤–ї–µ–љ–Є–µ –і–≤–Є–ґ–µ–љ–Є—П, —Г—З–∞—Б—В–Њ–Ї –Њ–њ–Њ—А—Л –Є, –≥–ї–∞–≤–љ–Њ–µ, –Њ–±–µ—Б–њ–µ—З–Є—В—М –∞–і–µ–Ї–≤–∞—В–љ—Г—О —Б–Ї–Њ—А–Њ—Б—В—М –Є —Б–Є–ї—Г —Б–Њ–Ї—А–∞—Й–µ–љ–Є—П —Б–Ї–µ–ї–µ—В–љ–Њ–є –Љ—Л—И—Ж—Л [10].
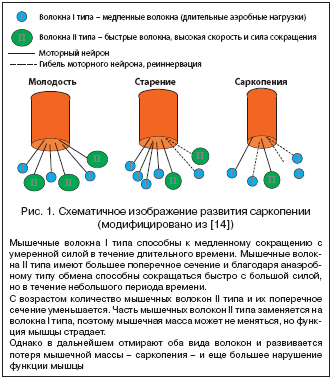
–Т–Њ–Ј—А–∞—Б—В–љ—Л–µ –Є–Ј–Љ–µ–љ–µ–љ–Є—П –љ–µ—А–≤–љ–Њ–є —Б–Є—Б—В–µ–Љ—Л, –љ–µ—А–≤–љ–Њ––Љ—Л—И–µ—З–љ–Њ–є –њ–µ—А–µ–і–∞—З–Є, —З—Г–≤—Б—В–≤–Є—В–µ–ї—М–љ–Њ—Б—В–Є –Є —Б–љ–Є–ґ–µ–љ–Є–µ –Љ—Л—И–µ—З–љ–Њ–є —Б–Є–ї—Л, –≤–њ–Њ–ї–љ–µ –≤–µ—А–Њ—П—В–љ–Њ, —Б—В–∞–љ–Њ–≤—П—В—Б—П –њ—А–Є—З–Є–љ–Њ–є –љ–µ–∞–і–µ–Ї–≤–∞—В–љ–Њ–є —А–µ–∞–Ї—Ж–Є–Є —Г–і–µ—А–ґ–∞–љ–Є—П —А–∞–≤–љ–Њ–≤–µ—Б–Є—П –Є –њ–∞–і–µ–љ–Є—П. –Т–Њ–Ј—А–∞—Б—В–љ—Л–µ –Є–Ј–Љ–µ–љ–µ–љ–Є—П —Д—Г–љ–Ї—Ж–Є–Є –Љ—Л—И—Ж –Њ–±—Г—Б–ї–Њ–≤–ї–µ–љ—Л –њ–Њ—В–µ—А–µ–є –Љ—Л—И–µ—З–љ–Њ–є –Љ–∞—Б—Б—Л – —Б–∞—А–Ї–Њ–њ–µ–љ–Є–µ–є (–≥—А–µ—З–µ—Б–Ї–Є–є sarx – –њ–ї–Њ—В—М, penia – –њ–Њ—В–µ—А—П). –Т –љ–Њ—А–Љ–µ –Љ—Л—И—Ж–∞ —Б–Њ—Б—В–Њ–Є—В –Є–Ј –Љ–љ–Њ–ґ–µ—Б—В–≤–∞ –Љ–Њ—В–Њ—А–љ—Л—Е –µ–і–Є–љ–Є—Ж (–Љ–Њ—В–Њ–љ–µ–є—А–Њ–љ –Є –Љ—Л—И—Ж–∞), –Ї–Њ—В–Њ—А—Л–µ –≤ –Ј–∞–≤–Є—Б–Є–Љ–Њ—Б—В–Є –Њ—В –Ї–Њ–ї–Є—З–µ—Б—В–≤–∞ —Д–Є–±—А–Є–ї–ї –Є —В–Є–њ–∞ –Љ–Є–Њ–Ј–Є–љ–∞ –і–µ–ї—П—В—Б—П –љ–∞: 1) –Љ–µ–і–ї–µ–љ–љ—Л–µ –Љ–Њ—В–Њ—А–љ—Л–µ –µ–і–Є–љ–Є—Ж—Л (–Љ–∞–ї–Њ —Д–Є–±—А–Є–ї–ї, –Љ–Є–Њ–Ј–Є–љ I —В–Є–њ–∞, –∞—Н—А–Њ–±–љ—Л–є —В–Є–њ –Њ–±–Љ–µ–љ–∞, –Њ–њ—В–Є–Љ–∞–ї—М–љ—Л –і–ї—П –і–ї–Є—В–µ–ї—М–љ—Л—Е —А–µ–≥—Г–ї—П—А–љ—Л—Е –љ–∞–≥—А—Г–Ј–Њ–Ї); 2) –±—Л—Б—В—А—Л–µ –Љ–Њ—В–Њ—А–љ—Л–µ –µ–і–Є–љ–Є—Ж—Л (—Б–њ–Њ—Б–Њ–±–љ—Л —А–∞–Ј–≤–Є—В—М –±–Њ–ї—М—И—Г—О —Б–Є–ї—Г –Є —Б–Ї–Њ—А–Њ—Б—В—М —Б–Њ–Ї—А–∞—Й–µ–љ–Є—П –Ј–∞ –Ї–Њ—А–Њ—В–Ї–Є–є –њ–µ—А–Є–Њ–і –≤—А–µ–Љ–µ–љ–Є, —В.–Ї. —Б–Њ–і–µ—А–ґ–∞—В –±–Њ–ї—М—И–µ –Љ–Є–Њ—Д–Є–±—А–Є–ї–ї –Є –Љ–Є–Њ–Ј–Є–љ —В–Є–њ–∞ IIx); 3) –±—Л—Б—В—А—Л–µ —А–µ–Ј–Є—Б—В–µ–љ—В–љ—Л–µ –Ї —Г—В–Њ–Љ–ї–µ–љ–Є—О –Љ–Њ—В–Њ—А–љ—Л–µ –µ–і–Є–љ–Є—Ж—Л (—Б—А–µ–і–љ–µ–µ –Љ–µ–ґ–і—Г –≤–Њ–ї–Њ–Ї–љ–∞–Љ–Є I –Є II) [14]. –° –≤–Њ–Ј—А–∞—Б—В–Њ–Љ –њ—А–Њ–Є—Б—Е–Њ–і–Є—В –њ–Њ—В–µ—А—П –±—Л—Б—В—А—Л—Е –Љ–Њ—В–Њ—А–љ—Л—Е –µ–і–Є–љ–Є—Ж –Є —Г–Љ–µ–љ—М—И–µ–љ–Є–µ –Є—Е –њ–Њ–њ–µ—А–µ—З–љ–Њ–≥–Њ —Б–µ—З–µ–љ–Є—П, –≤ –Љ–µ–љ—М—И–µ–є —Б—В–µ–њ–µ–љ–Є –≤—Л—А–∞–ґ–µ–љ–∞ –њ–Њ—В–µ—А—П –Љ–µ–і–ї–µ–љ–љ—Л—Е –Љ–Њ—В–Њ—А–љ—Л—Е –µ–і–Є–љ–Є—Ж –Є–ї–Є –Ј–∞–Љ–µ–љ–∞ –±—Л—Б—В—А—Л—Е –Љ–Њ—В–Њ—А–љ—Л—Е –µ–і–Є–љ–Є—Ж –љ–∞ –Љ–µ–і–ї–µ–љ–љ—Л–µ, –∞ —В–∞–Ї–ґ–µ –≥–Є–±–µ–ї—М –Љ–Њ—В–Њ–љ–µ–є—А–Њ–љ–Њ–≤ –Є —А–µ–Є–љ–љ–µ—А–≤–∞—Ж–Є—П (—А–Є—Б. 1) [14]. –Т—Б–ї–µ–і—Б—В–≤–Є–µ —Н—В–Њ–≥–Њ —Б—В—А–∞–і–∞–µ—В –≤–Њ–Ј–Љ–Њ–ґ–љ–Њ—Б—В—М –±—Л—Б—В—А–Њ–≥–Њ —Б–Є–ї—М–љ–Њ–≥–Њ —Б–Њ–Ї—А–∞—Й–µ–љ–Є—П –њ—А–Є —Г–≥—А–Њ–Ј–µ –њ–∞–і–µ–љ–Є—П, –Є–Ј–Љ–µ–љ—П—О—В—Б—П —И–∞–≥–Њ–≤—Л–µ —А–µ–∞–Ї—Ж–Є–Є, –љ–µ–Њ–±—Е–Њ–і–Є–Љ—Л–µ –і–ї—П —Г–і–µ—А–ґ–∞–љ–Є—П —А–∞–≤–љ–Њ–≤–µ—Б–Є—П. –Ґ–∞–Ї, –і–ї—П –Є–Ј–±–µ–ґ–∞–љ–Є—П –њ–∞–і–µ–љ–Є—П –≤–њ–µ—А–µ–і —И–∞–≥ –≤–њ–µ—А–µ–і —Б—В–∞–љ–Њ–≤–Є—В—Б—П –Љ–µ–і–ї–µ–љ–љ–µ–µ –Є —Б–Њ–њ—А–Њ–≤–Њ–ґ–і–∞–µ—В—Б—П –і–Њ–њ–Њ–ї–љ–Є—В–µ–ї—М–љ—Л–Љ–Є –Ї–Њ–Љ–њ–µ–љ—Б–∞—В–Њ—А–љ—Л–Љ–Є —И–∞–ґ–Ї–∞–Љ–Є –≤–±–Њ–Ї, —З—В–Њ —Б –≤—Л—Б–Њ–Ї–Њ–є –≤–µ—А–Њ—П—В–љ–Њ—Б—В—М—О –њ—А–Є–≤–Њ–і–Є—В –Ї –њ–∞–і–µ–љ–Є—О –≤–±–Њ–Ї. –Я–Њ–њ—Л—В–Ї–∞ –љ–µ —Г–њ–∞—Б—В—М –≤–±–Њ–Ї —Б–Њ–њ—А–Њ–≤–Њ–ґ–і–∞–µ—В—Б—П –љ–µ—Б–Ї–Њ–ї—М–Ї–Є–Љ–Є —И–∞–ґ–Ї–∞–Љ–Є –≤–±–Њ–Ї –≤–Љ–µ—Б—В–Њ –Њ–і–љ–Њ–≥–Њ –њ–µ—А–µ–Ї—А–µ—Б—В–љ–Њ–≥–Њ —И–∞–≥–∞, –±–Њ–ї–µ–µ —В–Њ–≥–Њ, –љ–µ–±–Њ–ї—М—И–Є–µ —И–∞–ґ–Ї–Є –≤–±–Њ–Ї –љ–µ—А–µ–і–Ї–Њ –Ј–∞–Ї–∞–љ—З–Є–≤–∞—О—В—Б—П –љ–∞–ї–Њ–ґ–µ–љ–Є–µ–Љ –Њ–і–љ–Њ–є —Б—В—Г–њ–љ–Є –љ–∞ –і—А—Г–≥—Г—О –Є –љ–µ–Љ–Є–љ—Г–µ–Љ—Л–Љ –њ–∞–і–µ–љ–Є–µ–Љ –≤–±–Њ–Ї [15–17]. –Т–Љ–µ—Б—В–µ —Б —В–µ–Љ, –Є–Љ–µ–љ–љ–Њ –њ–∞–і–µ–љ–Є–µ –≤–±–Њ–Ї, –Ї—А–∞–є–љ–µ —А–µ–і–Ї–Њ–µ –≤ –Љ–Њ–ї–Њ–і–Њ–Љ –≤–Њ–Ј—А–∞—Б—В–µ –Є —З–∞—Б—В–Њ–µ —Г –ї—О–і–µ–є —Б—В–∞—А—И–µ 65, – –≤–∞–ґ–љ–µ–є—И–Є–є —Д–∞–Ї—В–Њ—А —А–Є—Б–Ї–∞ –њ–µ—А–µ–ї–Њ–Љ–∞ –±–µ–і—А–∞. –Т –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є –њ–Њ –љ–Є–Ј–Ї–Њ—В—А–∞–≤–Љ–∞—В–Є—З–љ—Л–Љ –њ–µ—А–µ–ї–Њ–Љ–∞–Љ —Е–∞—А–∞–Ї—В–µ—А –њ–∞–і–µ–љ–Є—П –±—Л–ї –њ—А–Њ–∞–љ–∞–ї–Є–Ј–Є—А–Њ–≤–∞–љ —Г 130 –ґ–µ–љ—Й–Є–љ, –њ–µ—А–µ–љ–µ—Б—И–Є—Е –њ–µ—А–µ–ї–Њ–Љ –±–µ–і—А–∞, 294 –њ–∞—Ж–Є–µ–љ—В–Њ–Ї —Б –њ–µ—А–µ–ї–Њ–Љ–Њ–Љ –ї—Г—З–µ–≤–Њ–є –Ї–Њ—Б—В–Є –Є 467 –ґ–µ–љ—Й–Є–љ, —Г–њ–∞–≤—И–Є—Е –±–µ–Ј –њ–Њ—Б–ї–µ–і—Б—В–≤–Є–є. –Я–∞–і–µ–љ–Є–µ –≤–±–Њ–Ї —Б—В–∞—В–Є—Б—В–Є—З–µ—Б–Ї–Є –Ј–љ–∞—З–Є–Љ–Њ –±–Њ–ї–µ–µ —З–µ–Љ –≤ 4 —А–∞–Ј–∞ —Г–≤–µ–ї–Є—З–Є–≤–∞–ї–Њ —А–Є—Б–Ї –њ–µ—А–µ–ї–Њ–Љ–∞ –±–µ–і—А–∞ (–Њ—В–љ–Њ—И–µ–љ–Є–µ –љ–µ—А–∞–≤–µ–љ—Б—В–≤–∞ – 4,3), –њ–∞–і–µ–љ–Є–µ –≤–њ–µ—А–µ–і –Њ–Ї–∞–Ј–∞–ї–Њ—Б—М –≤—Л—Б–Њ–Ї–Є–Љ —Д–∞–Ї—В–Њ—А–Њ–Љ —А–Є—Б–Ї–∞ –њ–µ—А–µ–ї–Њ–Љ–∞ –ї—Г—З–µ–≤–Њ–є –Ї–Њ—Б—В–Є, –≤ —В–Њ –≤—А–µ–Љ—П –Ї–∞–Ї –њ–∞–і–µ–љ–Є–µ –љ–∞–Ј–∞–і —А–µ–ґ–µ —Б–Њ–њ—А–Њ–≤–Њ–ґ–і–∞–ї–Њ—Б—М –њ–µ—А–µ–ї–Њ–Љ–∞–Љ–Є [18]. –Т –і—А—Г–≥–Њ–Љ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є —Б—А–∞–≤–љ–Є–≤–∞–ї–Є—Б—М –њ–Њ–ґ–Є–ї—Л–µ –ї—О–і–Є, –Ї–Њ—В–Њ—А—Л–µ —Г–њ–∞–ї–Є –Є —Б–ї–Њ–Љ–∞–ї–Є –±–µ–і—А–µ–љ–љ—Г—О –Ї–Њ—Б—В—М (n=72), –Є —В–µ, –Ї–Њ–Љ—Г —Г–і–∞–ї–Њ—Б—М —Г–њ–∞—Б—В—М –±–µ–Ј –њ–µ—А–µ–ї–Њ–Љ–Њ–≤ (n=77) [19]. –Э–∞ –Њ—Б–љ–Њ–≤–∞–љ–Є–Є –Љ–љ–Њ–ґ–µ—Б—В–≤–µ–љ–љ–Њ–≥–Њ –ї–Њ–≥–Є—Б—В–Є—З–µ—Б–Ї–Њ–≥–Њ —А–µ–≥—А–µ—Б—Б–Є–Њ–љ–љ–Њ–≥–Њ –∞–љ–∞–ї–Є–Ј–∞ –±—Л–ї–Є –≤—Л–і–µ–ї–µ–љ—Л –љ–µ–Ј–∞–≤–Є—Б–Є–Љ—Л–µ —Д–∞–Ї—В–Њ—А—Л —А–Є—Б–Ї–∞ –њ–µ—А–µ–ї–Њ–Љ–Њ–≤: –њ–∞–і–µ–љ–Є–µ –≤–±–Њ–Ї, –Ь–Я–Ъ–Ґ —И–µ–є–Ї–Є –±–µ–і—А–∞, —Н–љ–µ—А–≥–Є—П –њ–∞–і–µ–љ–Є—П, —Б–љ–Є–ґ–µ–љ–Є–µ –Є–љ–і–µ–Ї—Б–∞ –Љ–∞—Б—Б—Л —В–µ–ї–∞ (–Ш–Ь–Ґ). –Э–∞–Є–±–Њ–ї–µ–µ —Б—Г—Й–µ—Б—В–≤–µ–љ–љ—Л–Љ —Д–∞–Ї—В–Њ—А–Њ–Љ —А–Є—Б–Ї–∞ –њ–µ—А–µ–ї–Њ–Љ–Њ–≤ —И–µ–є–Ї–Є –±–µ–і—А–∞ —Б—В–∞–ї–Њ –њ–∞–і–µ–љ–Є–µ –≤–±–Њ–Ї, –Њ–љ–Њ —Г–≤–µ–ї–Є—З–Є–≤–∞–ї–Њ —А–Є—Б–Ї –њ–µ—А–µ–ї–Њ–Љ–∞ –≤ 5,7 —А–∞–Ј–∞ (95% –Ф–Ш [2,3–14] p<0,001), –≤ —В–Њ –≤—А–µ–Љ—П –Ї–∞–Ї —Б–љ–Є–ґ–µ–љ–Є–µ –Ь–Я–Ъ–Ґ —И–µ–є–Ї–Є –±–µ–і—А–∞ –љ–∞ 1 —Б—В–∞–љ–і–∞—А—В–љ–Њ–µ –Њ—В–Ї–ї–Њ–љ–µ–љ–Є–µ (SD) —Г–≤–µ–ї–Є—З–Є–≤–∞–ї–Њ —А–Є—Б–Ї –њ–µ—А–µ–ї–Њ–Љ–∞ –ї–Є—И—М –≤ 2,7 —А–∞–Ј–∞ (95% –Ф–Ш [1,6–4,6] p<0,001) [19]. –°—Е–Њ–і–љ—Л–µ —А–µ–Ј—Г–ї—М—В–∞—В—Л –±—Л–ї–Є –Њ–±–љ–∞—А—Г–ґ–µ–љ—Л –њ—А–Є –∞–љ–∞–ї–Є–Ј–µ —Д–∞–Ї—В–Њ—А–Њ–≤ —А–Є—Б–Ї–∞ –њ–µ—А–µ–ї–Њ–Љ–Њ–≤ —Г 797 –њ–∞—Ж–Є–µ–љ—В–Њ–≤. –Ц–µ–љ—Й–Є–љ—Л, –њ–µ—А–µ–љ–µ—Б—И–Є–µ –њ–µ—А–µ–ї–Њ–Љ—Л, –≤ 2,9 —А–∞–Ј–∞ (95% –Ф–Ш 2,0–4,1) —З–∞—Й–µ –Є–Љ–µ–ї–Є –і–Є–∞–≥–љ–Њ–Ј –Њ—Б—В–µ–Њ–њ–Њ—А–Њ–Ј–∞ –Є –≤ 4 —А–∞–Ј–∞ (95% –Ф–Ш 2,7–5,9) —З–∞—Й–µ –њ–∞–і–∞–ї–Є –њ–Њ —Б—А–∞–≤–љ–µ–љ–Є—О —Б –ґ–µ–љ—Й–Є–љ–∞–Љ–Є –±–µ–Ј –њ–µ—А–µ–ї–Њ–Љ–Њ–≤ –≤ –∞–љ–∞–Љ–љ–µ–Ј–µ [20].
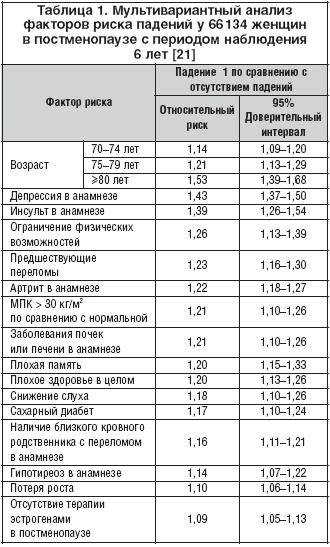
–§–∞–Ї—В–Њ—А—Л —А–Є—Б–Ї–∞ –њ–∞–і–µ–љ–Є–є
–Я—А–Њ–≤–µ–і–µ–љ–Њ –Љ–љ–Њ–ґ–µ—Б—В–≤–Њ –љ–∞—Г—З–љ—Л—Е —А–∞–±–Њ—В —Б —Ж–µ–ї—М—О –≤—Л—П–≤–Є—В—М —Д–∞–Ї—В–Њ—А—Л —А–Є—Б–Ї–∞ –њ–∞–і–µ–љ–Є–є. –Ю–і–љ–Њ –Є–Ј –њ–Њ—Б–ї–µ–і–љ–Є—Е –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–є, –≤–Ї–ї—О—З–Є–≤—И–µ–µ 66134 –ґ–µ–љ—Й–Є–љ—Л –≤ –њ–Њ—Б—В–Љ–µ–љ–Њ–њ–∞—Г–Ј–µ –≤ –≤–Њ–Ј—А–∞—Б—В–µ –і–Њ 65 –ї–µ—В (–±–Њ–ї—М—И–∞—П –њ–Њ–ї–Њ–≤–Є–љ–∞) –Є —Б—В–∞—А—И–µ 65, –њ–Њ–Ї–∞–Ј–∞–ї–Њ –≤—Л—Б–Њ–Ї—Г—О —З–∞—Б—В–Њ—В—Г –њ–∞–і–µ–љ–Є–є – 38,2% –ґ–µ–љ—Й–Є–љ –њ–∞–і–∞–ї–Є —Е–Њ—В—П –±—Л 1 —А–∞–Ј –≤ –≥–Њ–і [21]. –°–∞–Љ—Л–Љ —Б—Г—Й–µ—Б—В–≤–µ–љ–љ—Л–Љ —Д–∞–Ї—В–Њ—А–Њ–Љ —А–Є—Б–Ї–∞ –њ–∞–і–µ–љ–Є–є —Б—В–∞–ї–Њ –њ–∞–і–µ–љ–Є–µ –≤ –∞–љ–∞–Љ–љ–µ–Ј–µ (–Ю–® 2,7). –Ъ—А–Њ–Љ–µ —В–Њ–≥–Њ, –±—Л–ї–Њ –≤—Л—П–≤–ї–µ–љ–Њ 17 –і—А—Г–≥–Є—Е –љ–µ–Ј–∞–≤–Є—Б–Є–Љ—Л—Е —Д–∞–Ї—В–Њ—А–Њ–≤ —А–Є—Б–Ї–∞ –њ–∞–і–µ–љ–Є–є. –Ф–∞–љ–љ—Л–µ —Н—В–Њ–≥–Њ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П –њ—А–µ–і—Б—В–∞–≤–ї–µ–љ—Л –≤ —В–∞–±–ї–Є—Ж–µ 1.
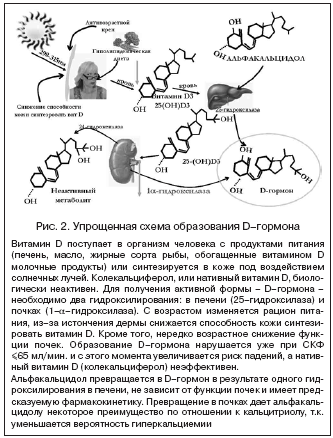
–°–Њ—З–µ—В–∞–љ–Є–µ –љ–µ—Б–Ї–Њ–ї—М–Ї–Є—Е —Д–∞–Ї—В–Њ—А–Њ–≤ —А–Є—Б–Ї–∞, –њ–Њ–ї—Г—З–µ–љ–љ—Л—Е –≤ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є, –µ—Й–µ –±–Њ–ї—М—И–µ —Г–≤–µ–ї–Є—З–Є–≤–∞–ї–Њ —А–Є—Б–Ї –њ–∞–і–µ–љ–Є–є. –Ъ—А–Њ–Љ–µ —В–Њ–≥–Њ, –≤ –і—А—Г–≥–Є—Е –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П—Е –±—Л–ї–Њ –≤—Л—П–≤–ї–µ–љ–Њ, —З—В–Њ —Б–љ–Є–ґ–µ–љ–Є–µ —Б–Њ–і–µ—А–ґ–∞–љ–Є—П —Г—А–Њ–≤–љ—П –≤–Є—В–∞–Љ–Є–љ–∞ D –≤ —Б—Л–≤–Њ—А–Њ—В–Ї–µ –Ї—А–Њ–≤–Є (25(–Ю–Э)D<40 –љ–≥/–Љ–ї, –њ–Њ –љ–µ–Ї–Њ—В–Њ—А—Л–Љ –і–∞–љ–љ—Л–Љ <20 –љ–≥/–Љ–ї) –њ–Њ–≤—Л—И–∞–µ—В —А–Є—Б–Ї –њ–∞–і–µ–љ–Є—П [22,23]. –Т —Н—В–Њ–є —Б–≤—П–Ј–Є –Є–љ—В–µ—А–µ—Б–љ—Л–Љ –Ї–∞–ґ–µ—В—Б—П —Г–≤–µ–ї–Є—З–µ–љ–Є–µ –≤ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є NORA [21] —А–Є—Б–Ї–∞ –њ–∞–і–µ–љ–Є–є —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П–Љ–Є –њ–Њ—З–µ–Ї –Є –њ–µ—З–µ–љ–Є, –∞ —В–∞–Ї–ґ–µ —Б –Њ–ґ–Є—А–µ–љ–Є–µ–Љ. –Ф–µ–є—Б—В–≤–Є—В–µ–ї—М–љ–Њ, –Њ—Б–љ–Њ–≤–љ–∞—П —З–∞—Б—В—М –љ–∞—В–Є–≤–љ–Њ–≥–Њ –≤–Є—В–∞–Љ–Є–љ–∞ D –љ–∞—Е–Њ–і–Є—В—Б—П –≤ –ґ–Є—А–Њ–≤–Њ–Љ –і–µ–њ–Њ. –£ –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –Њ–ґ–Є—А–µ–љ–Є–µ–Љ –і–µ—Д–Є—Ж–Є—В –≤–Є—В–∞–Љ–Є–љ–∞ D –Љ–Њ–ґ–µ—В —А–∞–Ј–≤–Є–≤–∞—В—М—Б—П –і–∞–ґ–µ –њ—А–Є –µ–≥–Њ –љ–Њ—А–Љ–∞–ї—М–љ–Њ–Љ –њ–Њ—Б—В—Г–њ–ї–µ–љ–Є–Є –≤ –Њ—А–≥–∞–љ–Є–Ј–Љ –Є–Ј––Ј–∞ —З—А–µ–Ј–Љ–µ—А–љ–Њ–≥–Њ –њ–Њ–≥–ї–Њ—Й–µ–љ–Є—П –ґ–Є—А–Њ–≤–Њ–є —В–Ї–∞–љ—М—О. –Ю–і–љ–∞–Ї–Њ –±–Є–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є–µ —Н—Д—Д–µ–Ї—В—Л –љ–∞ –Ї–Њ—Б—В–љ—Г—О —В–Ї–∞–љ—М –Є –Љ—Л—И—Ж—Л –Њ–Ї–∞–Ј—Л–≤–∞–µ—В –љ–µ –љ–∞—В–Є–≤–љ—Л–є –≤–Є—В–∞–Љ–Є–љ D, –∞ –µ–≥–Њ –∞–Ї—В–Є–≤–љ–∞—П —Д–Њ—А–Љ–∞, D––≥–Њ—А–Љ–Њ–љ. –Я—А–µ–≤—А–∞—Й–µ–љ–Є–µ –Ї–Њ–ї–µ–Ї–∞–ї—М—Ж–Є—Д–µ—А–Њ–ї–∞ –≤ D––≥–Њ—А–Љ–Њ–љ –њ—А–µ–і—Б—В–∞–≤–ї–µ–љ–Њ –љ–∞ —А–Є—Б—Г–љ–Ї–µ 2. –Э–∞—А—Г—И–µ–љ–Є–µ —Д—Г–љ–Ї—Ж–Є–Є –њ–µ—З–µ–љ–Є –Є/–Є–ї–Є –њ–Њ—З–µ–Ї –њ—А–Є–≤–Њ–і–Є—В –Ї –љ–∞—А—Г—И–µ–љ–Є—О –Њ–±—А–∞–Ј–Њ–≤–∞–љ–Є—П D––≥–Њ—А–Љ–Њ–љ–∞ –Є, –Ї–∞–Ї —Б–ї–µ–і—Б—В–≤–Є–µ, —Б–љ–Є–ґ–µ–љ–Є—О –µ–≥–Њ –±–Є–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Њ–≥–Њ –≤–Њ–Ј–і–µ–є—Б—В–≤–Є—П –љ–∞ –Ї–Њ—Б—В–Є –Є –Љ—Л—И—Ж—Л. –Ъ–∞–Ї –њ—А–∞–≤–Є–ї–Њ, —Д—Г–љ–Ї—Ж–Є—П 25––≥–Є–і—А–Њ–Ї—Б–Є–ї–∞–Ј—Л —Б—В—А–∞–і–∞–µ—В –ї–Є—И—М –њ—А–Є —В—П–ґ–µ–ї–Њ–Љ –њ–Њ—А–∞–ґ–µ–љ–Є–Є –њ–µ—З–µ–љ–Є – —Ж–Є—А—А–Њ–Ј–µ, –≤ —В–Њ –≤—А–µ–Љ—П –Ї–∞–Ї —Б–љ–Є–ґ–µ–љ–Є–µ —Б–Ї–Њ—А–Њ—Б—В–Є –Ї–ї—Г–±–Њ—З–Ї–Њ–≤–Њ–є —Д–Є–ї—М—В—А–∞—Ж–Є–Є (–°–Ъ–§) –Љ–µ–љ–µ–µ 65 –Љ–ї/–Љ–Є–љ. –і–Њ—Б—В–∞—В–Њ—З–љ–Њ –і–ї—П –Ј–љ–∞—З–Є—В–µ–ї—М–љ–Њ–≥–Њ —Г—Е—Г–і—И–µ–љ–Є—П —Д—Г–љ–Ї—Ж–Є–Є 1–a––≥–Є–і—А–Њ–Ї—Б–Є–ї–∞–Ј—Л –Є —Б–љ–Є–ґ–µ–љ–Є—П —Б–Є–љ—В–µ–Ј–∞ D––≥–Њ—А–Љ–Њ–љ–∞. –Т –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є —Б —Г—З–∞—Б—В–Є–µ–Љ 1781 –Љ—Г–ґ—З–Є–љ—Л –Є –ґ–µ–љ—Й–Є–љ—Л —Б –Њ—Б—В–µ–Њ–њ–Њ—А–Њ–Ј–Њ–Љ —В–∞–Ї–Њ–µ –≤–Њ–Ј—А–∞—Б—В–љ–Њ–µ —Б–љ–Є–ґ–µ–љ–Є–µ —Д—Г–љ–Ї—Ж–Є–Є –њ–Њ—З–µ–Ї –±—Л–ї–Њ –њ—А–Є–Ј–љ–∞–љ–Њ –љ–µ–Ј–∞–≤–Є—Б–Є–Љ—Л–Љ —Д–∞–Ї—В–Њ—А–Њ–Љ —А–Є—Б–Ї–∞ –њ–∞–і–µ–љ–Є–є –Є —Б–љ–Є–ґ–µ–љ–Є—П —Д—Г–љ–Ї—Ж–Є–Њ–љ–∞–ї—М–љ—Л—Е –≤–Њ–Ј–Љ–Њ–ґ–љ–Њ—Б—В–µ–є –њ–∞—Ж–Є–µ–љ—В–Њ–≤ (—Е—Г–і—И–µ–µ –≤—Л–њ–Њ–ї–љ–µ–љ–Є–µ —Д—Г–љ–Ї—Ж–Є–Њ–љ–∞–ї—М–љ—Л—Е —В–µ—Б—В–Њ–≤) [24]. –Ґ–∞–Ї–Є–Љ –Њ–±—А–∞–Ј–Њ–Љ, —Г–ґ–µ –љ–∞ –њ—А–Є–µ–Љ–µ –≤—А–∞—З–∞ –ї–µ–≥–Ї–Њ –≤—Л–і–µ–ї–Є—В—М –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –≤—Л—Б–Њ–Ї–Є–Љ —А–Є—Б–Ї–Њ–Љ –њ–∞–і–µ–љ–Є–є –Є–Ј––Ј–∞ —Б–љ–Є–ґ–µ–љ–Є—П –°–Ъ–§, –њ—А–Є–Љ–µ–љ–Є–≤ —Д–Њ—А–Љ—Г–ї—Г Cockcroft–Gault.
–Ф–ї—П –Љ—Г–ґ—З–Є–љ:
(–Ъ–ї–Ъ—А=((140––≤–Њ–Ј—А–∞—Б—В)*–≤–µ—Б)/(72*–Ї—А–µ–∞—В–Є–љ–Є–љ (–Љ–≥/–і–ї)), –Є–ї–Є
–Ъ–ї–Ъ—А=(140––≤–Њ–Ј—А–∞—Б—В)*–≤–µ—Б)*1,23/–Ї—А–µ–∞—В–Є–љ–Є–љ (–Љ–Ї–Љ–Њ–ї—М/–ї))
–Ф–ї—П –ґ–µ–љ—Й–Є–љ:
(–Ъ–ї–Ъ—А=((140––≤–Њ–Ј—А–∞—Б—В)*–≤–µ—Б)/(72*–Ї—А–µ–∞—В–Є–љ–Є–љ (–Љ–≥/–і–ї))*0,85, –Ъ–ї–Ъ—А=(140––≤–Њ–Ј—А–∞—Б—В)*–≤–µ—Б)*1,04/–Ї—А–µ–∞—В–Є–љ–Є–љ (–Љ–Ї–Љ–Њ–ї—М/–ї))
(–Ъ–ї–Ъ—А – –Њ—Ж–µ–љ–Ї–∞ –Ї–ї–Є—А–µ–љ—Б–∞ –Ї—А–µ–∞—В–Є–љ–Є–љ–∞, –Љ–ї/–Љ–Є–љ., –≤–µ—Б – –Љ–∞—Б—Б–∞ —В–µ–ї–∞, –Ї–≥)
–Ґ–∞–Ї–ґ–µ –Љ–Њ–ґ–љ–Њ –≤–Њ—Б–њ–Њ–ї—М–Ј–Њ–≤–∞—В—М—Б—П –Ї–∞–ї—М–Ї—Г–ї—П—В–Њ—А–Њ–Љ MDRD (www.mdrd.com), –њ—А–µ–і—Б—В–∞–≤–ї–µ–љ–љ—Л–Љ –≤ –Ш–љ—В–µ—А–љ–µ—В–µ.
–Т–∞–ґ–љ–Њ—Б—В—М D––≥–Њ—А–Љ–Њ–љ–∞ –і–ї—П —А–∞–Ј–≤–Є—В–Є—П –Љ—Л—И—Ж –Є –Є—Е —Д—Г–љ–Ї—Ж–Є–Њ–љ–∞–ї—М–љ—Л—Е –≤–Њ–Ј–Љ–Њ–ґ–љ–Њ—Б—В–µ–є –±—Л–ї–∞ –њ—А–Њ–і–µ–Љ–Њ–љ—Б—В—А–Є—А–Њ–≤–∞–љ–∞ –≤–Њ –Љ–љ–Њ–ґ–µ—Б—В–≤–µ —А–∞–±–Њ—В. Birge –Є Haddad –µ—Й–µ –≤ —Б–µ—А–µ–і–Є–љ–µ 1970–—Е –≥–≥. –њ–Њ–Ї–∞–Ј–∞–ї–Є, —З—В–Њ 25(–Ю–Э)D3 –Њ–Ї–∞–Ј—Л–≤–∞–µ—В –≤–ї–Є—П–љ–Є–µ –љ–∞ —Д–Њ—Б—Д–∞—В–љ—Л–є –Љ–µ—В–∞–±–Њ–ї–Є–Ј–Љ –≤ –Љ—Л—И—Ж–∞—Е –і–Є–∞—Д—А–∞–≥–Љ—Л –Ї—А—Л—Б —Б –і–µ—Д–Є—Ж–Є—В–Њ–Љ –≤–Є—В–∞–Љ–Є–љ–∞ D [25]. –Т —А–µ–Ј—Г–ї—М—В–∞—В–µ –і–∞–ї—М–љ–µ–є—И–Є—Е –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–є —А–µ—Ж–µ–њ—В–Њ—А –Ї –∞–Ї—В–Є–≤–љ–Њ–є —Д–Њ—А–Љ–µ –≤–Є—В–∞–Љ–Є–љ–∞ D (1,25––і–Є–≥–Є–і—А–Њ—Е–Њ–ї–µ–Ї–∞–ї—М—Ж–Є—Д–µ—А–Њ–ї), –Є–ї–Є D––≥–Њ—А–Љ–Њ–љ—Г, –±—Л–ї –Њ–±–љ–∞—А—Г–ґ–µ–љ –љ–∞ –Ї–ї–µ—В–Ї–∞—Е —Б–Ї–µ–ї–µ—В–љ–Њ–є –Љ—Г—Б–Ї—Г–ї–∞—В—Г—А—Л [26]. –Э–∞ —Б–µ–≥–Њ–і–љ—П—И–љ–Є–є –і–µ–љ—М –њ–Њ–Ї–∞–Ј–∞–љ–Њ, —З—В–Њ D––≥–Њ—А–Љ–Њ–љ –≤–ї–Є—П–µ—В –љ–∞ —Б–Ї–µ–ї–µ—В–љ—Г—О –Љ—Г—Б–Ї—Г–ї–∞—В—Г—А—Г –љ–∞ –≥–µ–љ–µ—В–Є—З–µ—Б–Ї–Њ–Љ —Г—А–Њ–≤–љ–µ (–Є–Ј–Љ–µ–љ–µ–љ–Є–µ —В—А–∞–љ—Б–Ї—А–Є–њ—Ж–Є–Є –≥–µ–љ–Њ–≤) –Є –љ–∞ —В–Ї–∞–љ–µ–≤–Њ–Љ —Г—А–Њ–≤–љ–µ —З–µ—А–µ–Ј —А–µ–≥—Г–ї—П—Ж–Є—О –Љ–µ—В–∞–±–Њ–ї–Є–Ј–Љ–∞ –Ї–∞–ї—М—Ж–Є—П –Є –Ї–Њ–љ—В—А–Њ–ї—М –Љ—Л—И–µ—З–љ—Л—Е —Б–Њ–Ї—А–∞—Й–µ–љ–Є–є –Є —А–∞—Б—Б–ї–∞–±–ї–µ–љ–Є–є [27–30]. –Ч–љ–∞—З–µ–љ–Є–µ —Н—Д—Д–µ–Ї—В–Њ–≤ D––≥–Њ—А–Љ–Њ–љ–∞ –і–ї—П —А–µ–∞–Ї—Ж–Є–Є —Г–і–µ—А–ґ–∞–љ–Є—П —А–∞–≤–љ–Њ–≤–µ—Б–Є—П –±—Л–ї–Њ –і–Њ–њ–Њ–ї–љ–Є—В–µ–ї—М–љ–Њ –њ–Њ–і—В–≤–µ—А–ґ–і–µ–љ–Њ –љ–µ–і–∞–≤–љ–Њ –≤ —А–µ–Ј—Г–ї—М—В–∞—В–µ –і–≤—Г—Е –њ—А–Њ—Б–њ–µ–Ї—В–Є–≤–љ—Л—Е –≥–µ–љ–µ—В–Є—З–µ—Б–Ї–Є—Е –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–є. –С—Л–ї–Њ –Њ–±–љ–∞—А—Г–ґ–µ–љ–Њ, —З—В–Њ –њ–Њ–ї–Є–Љ–Њ—А—Д–Є–Ј–Љ —А–µ—Ж–µ–њ—В–Њ—А–∞ –Ї –≤–Є—В–∞–Љ–Є–љ—Г D –њ—А–Є–≤–Њ–і–Є—В –Ї —Г–≤–µ–ї–Є—З–µ–љ–Є—О —З–∞—Б—В–Њ—В—Л –њ–∞–і–µ–љ–Є–є –Є —Б–љ–Є–ґ–µ–љ–Є—О –Љ—Л—И–µ—З–љ–Њ–є —Б–Є–ї—Л [31].
–° –≤–Њ–Ј—А–∞—Б—В–Њ–Љ, –Њ—Б–Њ–±–µ–љ–љ–Њ —Г –њ–Њ–ґ–Є–ї—Л—Е –ї—О–і–µ–є, –љ–∞–±–ї—О–і–∞–µ—В—Б—П —Б–љ–Є–ґ–µ–љ–Є–µ —Н–Ї—Б–њ—А–µ—Б—Б–Є–Є —А–µ—Ж–µ–њ—В–Њ—А–∞ –Ї D––≥–Њ—А–Љ–Њ–љ—Г [32]. –Ю—Ж–µ–љ–Є—В—М –µ–µ —Б—В–µ–њ–µ–љ—М –≤ —А–µ–∞–ї—М–љ–Њ–є –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Њ–є –њ—А–∞–Ї—В–Є–Ї–µ –љ–µ –њ—А–µ–і—Б—В–∞–≤–ї—П–µ—В—Б—П –≤–Њ–Ј–Љ–Њ–ґ–љ—Л–Љ. –Ю–і–љ–∞–Ї–Њ –≤ —А—П–і–µ —А—Г–Ї–Њ–≤–Њ–і—Б—В–≤, –≤ —З–∞—Б—В–љ–Њ—Б—В–Є –≤ –љ–µ–Љ–µ—Ж–Ї–Є—Е –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є—Е —А–µ–Ї–Њ–Љ–µ–љ–і–∞—Ж–Є—П—Е, –њ—А–µ–і–ї–Њ–ґ–µ–љ—Л —Д—Г–љ–Ї—Ж–Є–Њ–љ–∞–ї—М–љ—Л–µ —В–µ—Б—В—Л, –њ–Њ–Ј–≤–Њ–ї—П—О—Й–Є–µ –Њ—Ж–µ–љ–Є—В—М —А–Є—Б–Ї –њ–∞–і–µ–љ–Є—П —Г –∞–Љ–±—Г–ї–∞—В–Њ—А–љ—Л—Е –њ–∞—Ж–Є–µ–љ—В–Њ–≤: —В–µ—Б—В «–≤—Б—В–∞—В—М –Є –Є–і—В–Є –љ–∞ –≤—А–µ–Љ—П», —В–µ—Б—В «–њ–Њ–і—К–µ–Љ —Б–Њ —Б—В—Г–ї–∞» [33].
–Ф–ї—П –њ—А–Њ–≤–µ–і–µ–љ–Є—П —В–µ—Б—В–∞ «–≤—Б—В–∞—В—М –Є –Є–і—В–Є –љ–∞ –≤—А–µ–Љ—П» –љ–µ–Њ–±—Е–Њ–і–Є–Љ —Б—В—Г–ї —Б –њ–Њ–і–ї–Њ–Ї–Њ—В–љ–Є–Ї–∞–Љ–Є (—Б–Є–і–µ–љ—М–µ –≤—Л—Б–Њ—В–Њ–є 48 —Б–Љ, –≤—Л—Б–Њ—В–∞ –њ–Њ–і–ї–Њ–Ї–Њ—В–љ–Є–Ї–Њ–≤ 68 —Б–Љ), —Б–µ–Ї—Г–љ–і–Њ–Љ–µ—А –Є –њ—А–Њ—Б—В—А–∞–љ—Б—В–≤–Њ –і–ї–Є–љ–Њ–є 3 –Љ. –Я–∞—Ж–Є–µ–љ—В–∞ –њ—А–Њ—Б—П—В –≤—Б—В–∞—В—М —Б–Њ —Б—В—Г–ї–∞, –њ—А–Њ–є—В–Є 3 –Љ, –Њ–±–Њ–є—В–Є –њ—А–µ–і–Љ–µ—В –љ–∞ –њ–Њ–ї—Г, –≤–µ—А–љ—Г—В—М—Б—П –Є —Б–µ—Б—В—М —Б–љ–Њ–≤–∞ –љ–∞ —Б—В—Г–ї. –С–Њ–ї—М–љ–Њ–≥–Њ –њ—А–µ–і—Г–њ—А–µ–ґ–і–∞—О—В, —З—В–Њ –≤—А–µ–Љ—П, –Ј–∞ –Ї–Њ—В–Њ—А–Њ–µ –Њ–љ(–∞) –≤—Л–њ–Њ–ї–љ–Є—В —Н—В–Њ –і–µ–є—Б—В–≤–Є–µ, –±—Г–і–µ—В –Є–Ј–Љ–µ—А–µ–љ–Њ, –њ–∞—Ж–Є–µ–љ—В –Љ–Њ–ґ–µ—В –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞—В—М –ї—О–±—Л–µ –њ—А–Є–≤—Л—З–љ—Л–µ –њ—А–Є—Б–њ–Њ—Б–Њ–±–ї–µ–љ–Є—П –і–ї—П —Е–Њ–і—М–±—Л (–љ–∞–њ—А–Є–Љ–µ—А, —В—А–Њ—Б—В—М) [34,35]. –Х—Б–ї–Є –≤—А–µ–Љ—П, –Ј–∞ –Ї–Њ—В–Њ—А–Њ–µ –±–Њ–ї—М–љ–Њ–є –≤—Л–њ–Њ–ї–љ–Є–ї —В–µ—Б—В, 10 —Б –Є–ї–Є –Љ–µ–љ—М—И–µ, —Н—В–Њ –љ–Њ—А–Љ–∞, 11–29 —Б – —Б–Њ–Љ–љ–Є—В–µ–ї—М–љ—Л–є —А–µ–Ј—Г–ї—М—В–∞—В, —А–µ—И–µ–љ–Є–µ –Ї–Њ–Љ–ї–µ–Ї—Б–љ–Њ–µ, –љ–∞ –Њ—Б–љ–Њ–≤–∞–љ–Є–Є –і—А—Г–≥–Є—Е –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є—Е –і–∞–љ–љ—Л—Е, 30 —Б –Є –±–Њ–ї–µ–µ —Б–≤–Є–і–µ—В–µ–ї—М—Б—В–≤—Г–µ—В –Њ–± —Г—Е—Г–і—И–µ–љ–Є–Є —Д—Г–љ–Ї—Ж–Є–Њ–љ–∞–ї—М–љ—Л—Е –≤–Њ–Ј–Љ–Њ–ґ–љ–Њ—Б—В–µ–є –Є —Г–≤–µ–ї–Є—З–µ–љ–Є–Є —А–Є—Б–Ї–∞ –њ–∞–і–µ–љ–Є–є. –С—Л–ї–Њ –њ–Њ–Ї–∞–Ј–∞–љ–Њ, —З—В–Њ —Г–≤–µ–ї–Є—З–µ–љ–Є–µ –≤—А–µ–Љ–µ–љ–Є –њ—А–Њ–≤–µ–і–µ–љ–Є—П —В–µ—Б—В–∞ –љ–∞ 2,6 —Б —Б–Њ—З–µ—В–∞–µ—В—Б—П —Б —Г–≤–µ–ї–Є—З–µ–љ–Є–µ–Љ —А–Є—Б–Ї–∞ –≤–љ–µ–њ–Њ–Ј–≤–Њ–љ–Њ—З–љ—Л—Е –њ–µ—А–µ–ї–Њ–Љ–Њ–≤ –љ–∞ 24% [36].
–Ф–ї—П –њ—А–Њ–≤–µ–і–µ–љ–Є—П —В–µ—Б—В–∞ «–њ–Њ–і—К–µ–Љ —Б–Њ —Б—В—Г–ї–∞» –љ–µ–Њ–±—Е–Њ–і–Є–Љ —Б—В—Г–ї –±–µ–Ј –њ–Њ–і–ї–Њ–Ї–Њ—В–љ–Є–Ї–Њ–≤, —Б–µ–Ї—Г–љ–і–Њ–Љ–µ—А. –Я–∞—Ж–Є–µ–љ—В–∞ –њ—А–Њ—Б—П—В –≤—Б—В–∞–љ—М —Б–Њ —Б—В—Г–ї–∞ 5 —А–∞–Ј –њ–Њ–і—А—П–і —Б —А—Г–Ї–∞–Љ–Є, —Б–ї–Њ–ґ–µ–љ–љ—Л–Љ–Є –љ–∞ –≥—А—Г–і–Є, –Ї–Њ–ї–µ–љ–Є –і–Њ–ї–ґ–љ—Л –±—Л—В—М –њ–Њ–ї–љ–Њ—Б—В—М—О —А–∞–Ј–Њ–≥–љ—Г—В—Л –њ—А–Є –Ї–∞–ґ–і–Њ–Љ –њ–Њ–і—К–µ–Љ–µ. –С–Њ–ї—М–љ–Њ–Љ—Г —Б–Њ–Њ–±—Й–∞—О—В, —З—В–Њ –Ј–∞—В—А–∞—З–µ–љ–љ–Њ–µ –≤—А–µ–Љ—П –±—Г–і–µ—В –Є–Ј–Љ–µ—А—П—В—М—Б—П. –Ґ–µ—Б—В –≥–ї–∞–≤–љ—Л–Љ –Њ–±—А–∞–Ј–Њ–Љ –і–∞–µ—В –Є–љ—Д–Њ—А–Љ–∞—Ж–Є—О –Њ —Б–Є–ї–µ –Є —Б–Ї–Њ—А–Њ—Б—В–Є —А–∞–±–Њ—В—Л –Љ—Л—И—Ж –љ–Є–ґ–љ–Є—Е –Ї–Њ–љ–µ—З–љ–Њ—Б—В–µ–є. –Т—А–µ–Љ—П, –Ј–∞—В—А–∞—З–µ–љ–љ–Њ–µ –љ–∞ –њ–Њ–і—К–µ–Љ, —А–∞–≤–љ–Њ–µ 10 —Б –Є –Љ–µ–љ–µ–µ, —Б–≤–Є–і–µ—В–µ–ї—М—Б—В–≤—Г–µ—В –Њ —Е–Њ—А–Њ—И–Є—Е —Д—Г–љ–Ї—Ж–Є–Њ–љ–∞–ї—М–љ—Л—Е –≤–Њ–Ј–Љ–Њ–ґ–љ–Њ—Б—В—П—Е, 11 —Б –Є –±–Њ–ї–µ–µ – –Њ—В—А–∞–ґ–∞–µ—В –љ–µ—Г—Б—В–Њ–є—З–Є–≤–Њ—Б—В—М –њ–Њ—Е–Њ–і–Ї–Є [37,38].
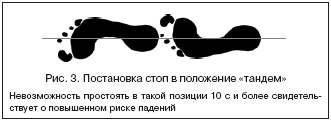
–Ф–Њ—Б—В–∞—В–Њ—З–љ–Њ —З–∞—Б—В–Њ –Є—Б–њ–Њ–ї—М–Ј—Г–µ—В—Б—П —В–µ—Б—В –љ–∞ —А–∞–≤–љ–Њ–≤–µ—Б–Є–µ. –Я–∞—Ж–Є–µ–љ—В—Г –њ—А–µ–і–ї–∞–≥–∞–µ—В—Б—П 10 —Б –њ—А–Њ—Б—В–Њ—П—В—М –≤ –њ–Њ–ї–Њ–ґ–µ–љ–Є–Є «—Б—В—Г–њ–љ–Є —Б–ґ–∞—В—Л –≤–Љ–µ—Б—В–µ», –Ј–∞—В–µ–Љ 10 —Б –≤ –њ–Њ–ї–Њ–ґ–µ–љ–Є–Є «–Њ–і–љ–∞ —Б—В—Г–њ–љ—П –њ–µ—А–µ–і –і—А—Г–≥–Њ–є» –Є, –љ–∞–Ї–Њ–љ–µ—Ж, –≤ –њ–Њ–ї–Њ–ґ–µ–љ–Є–Є «—В–∞–љ–і–µ–Љ» (—А–Є—Б. 3). –Э–µ–≤–Њ–Ј–Љ–Њ–ґ–љ–Њ—Б—В—М —Б—В–Њ—П—В—М –≤ –њ–Њ–ї–Њ–ґ–µ–љ–Є–Є «—В–∞–љ–і–µ–Љ» 10 —Б –њ—А–µ–і—Б–Ї–∞–Ј—Л–≤–∞–µ—В –≤—Л—Б–Њ–Ї–Є–є —А–Є—Б–Ї –њ–∞–і–µ–љ–Є—П [38,39].
–Ъ—А–Њ–Љ–µ —В–Њ–≥–Њ, –≤–Њ—Б—М–Љ–Є–ї–µ—В–љ–µ–µ –њ—А–Њ—Б–њ–µ–Ї—В–Є–≤–љ–Њ–µ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ —Б —Г—З–∞—Б—В–Є–µ–Љ 2928 –ґ–µ–љ—Й–Є–љ –≤ –њ–Њ—Б—В–Љ–µ–љ–Њ–њ–∞—Г–Ј–µ –њ–Њ–Ј–≤–Њ–ї–Є–ї–Њ –≤—Л—П–≤–Є—В—М –љ–∞–Є–±–Њ–ї–µ–µ –Ј–љ–∞—З–Є–Љ—Л–µ —В–µ—Б—В—Л –і–ї—П –Њ—Ж–µ–љ–Ї–Є —А–Є—Б–Ї–∞ —А–∞–Ј–≤–Є—В–Є—П –њ–µ—А–µ–ї–Њ–Љ–Њ–≤, —Б–≤—П–Ј–∞–љ–љ—Л—Е —Б —Г–≤–µ–ї–Є—З–µ–љ–Є–µ–Љ —А–Є—Б–Ї–∞ –њ–∞–і–µ–љ–Є–є –Є –љ–µ–Љ–Њ—Й–љ–Њ—Б—В–Є –њ–Њ–ґ–Є–ї—Л—Е –њ–∞—Ж–Є–µ–љ—В–Њ–≤. –Ґ–∞–Ї, –љ–µ—Б–њ–Њ—Б–Њ–±–љ–Њ—Б—В—М —Б—В–Њ—П—В—М –љ–∞ –Њ–і–љ–Њ–є –љ–Њ–≥–µ –≤ —В–µ—З–µ–љ–Є–µ 10 —Б —Г–≤–µ–ї–Є—З–Є–≤–∞–µ—В —А–Є—Б–Ї –њ–µ—А–µ–ї–Њ–Љ–Њ–≤ –≤ 9,11 —А–∞–Ј–∞ (95% –Ф–Ш 1,98–42,0), –∞ –љ–µ—Б–њ–Њ—Б–Њ–±–љ–Њ—Б—В—М –њ—А–Њ–є—В–Є –±–Њ–ї–µ–µ 100 –Љ, –Њ–њ—А–µ–і–µ–ї—П–µ–Љ–∞—П —Б–∞–Љ–Є–Љ –њ–∞—Ж–Є–µ–љ—В–Њ–Љ, —Г–≤–µ–ї–Є—З–Є–≤–∞–µ—В —А–Є—Б–Ї –њ–µ—А–µ–ї–Њ–Љ–∞ –ї–Њ–і—Л–ґ–Ї–Є –≤ 2,36 —А–∞–Ј–∞ (1,10–5,08), –±–µ–і—А–∞ – –≤ 11,57 —А–∞–Ј–∞ (2,73–49,15) –Є –њ–µ—А–µ–ї–Њ–Љ–Њ–≤ –њ–Њ–Ј–≤–Њ–љ–Ї–Њ–≤ – –≤ 3,85 —А–∞–Ј–∞ (1,45–10,22) [40].
–Я—А–Њ—Д–Є–ї–∞–Ї—В–Є–Ї–∞ –њ–∞–і–µ–љ–Є–є
–£—Б–ї–Њ–≤–љ–Њ –Љ–Њ–ґ–љ–Њ –≤—Л–і–µ–ї–Є—В—М –љ–µ—Б–Ї–Њ–ї—М–Ї–Њ –љ–∞–њ—А–∞–≤–ї–µ–љ–Є–є –њ—А–µ–і—Г–њ—А–µ–ґ–і–µ–љ–Є—П –њ–∞–і–µ–љ–Є–є. –Т —А—П–і–µ —Б–ї—Г—З–∞–µ–≤ —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ –ї–µ—З–µ–љ–Є–µ –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є–є (–∞—А–Є—В–Љ–Є–є, —Н–њ–Є–ї–µ–њ—Б–Є–Є, –Ї–∞—В–∞—А–∞–Ї—В—Л –Є —В.–і.), –Ї–Њ—В–Њ—А—Л–µ —Б–∞–Љ–Њ—Б—В–Њ—П—В–µ–ї—М–љ–Њ —Г–≤–µ–ї–Є—З–Є–≤–∞—О—В —А–Є—Б–Ї –њ–∞–і–µ–љ–Є–є. –Ф–Њ—Б—В–Њ–≤–µ—А–љ–Њ–µ —Б–љ–Є–ґ–µ–љ–Є–µ —З–∞—Б—В–Њ—В—Л –њ–∞–і–µ–љ–Є–є –±—Л–ї–Њ –њ—А–Њ–і–µ–Љ–Њ–љ—Б—В—А–Є—А–Њ–≤–∞–љ–Њ –њ—А–Є –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є–Є –≤–Њ–і–Є—В–µ–ї–µ–є —А–Є—В–Љ–∞ —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б —Б–Є–љ–Ї–Њ–њ–∞–ї—М–љ—Л–Љ–Є —Б–Њ—Б—В–Њ—П–љ–Є—П–Љ–Є [41]. –Т –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є PROFET [42], –њ–Њ—Б–≤—П—Й–µ–љ–љ–Њ–Љ –њ—А–µ–і–Њ—В–≤—А–∞—Й–µ–љ–Є—О –њ–µ—А–µ–ї–Њ–Љ–Њ–≤ —Г –њ–Њ–ґ–Є–ї—Л—Е, –≤ –Ї–Њ—В–Њ—А–Њ–Љ –∞–љ–∞–ї–Є–Ј–Є—А–Њ–≤–∞–ї–Є—Б—М –њ—А–Є—З–Є–љ—Л –њ–∞–і–µ–љ–Є–є –Є–љ–і–Є–≤–Є–і—Г–∞–ї—М–љ–Њ –Є –љ–∞–Ј–љ–∞—З–∞–ї–Њ—Б—М —Б–њ–µ—Ж–Є—Д–Є—З–µ—Б–Ї–Њ–µ –ї–µ—З–µ–љ–Є–µ, –≤ —В–µ—Е —Б–ї—Г—З–∞—П—Е, –Ї–Њ–≥–і–∞ –њ—А–Є—З–Є–љ—Г –њ–∞–і–µ–љ–Є–є —Г–і–∞–≤–∞–ї–Њ—Б—М —Г—Б—В–∞–љ–Њ–≤–Є—В—М, –∞ —В–∞–Ї–ґ–µ –≤ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П—Е, –≤ –Ї–Њ—В–Њ—А—Л—Е –њ–∞—Ж–Є–µ–љ—В–∞–Љ –±—Л–ї–Є —Г–Љ–µ–љ—М—И–µ–љ—Л –і–Њ–Ј—Л –њ—Б–Є—Е–Њ—В—А–Њ–њ–љ—Л—Е –њ—А–µ–њ–∞—А–∞—В–Њ–≤ [43], –њ–Њ–ї—Г—З–µ–љ–Њ —Б—В–∞—В–Є—Б—В–Є—З–µ—Б–Ї–Є –Ј–љ–∞—З–Є–Љ–Њ–µ —Б–љ–Є–ґ–µ–љ–Є–µ —А–Є—Б–Ї–∞ –њ–∞–і–µ–љ–Є–є.
–Ю—З–µ–љ—М –њ–Њ–њ—Г–ї—П—А–љ—Л —А–µ–Ї–Њ–Љ–µ–љ–і–∞—Ж–Є–Є –њ–Њ –Є–Ј–Љ–µ–љ–µ–љ–Є—О –њ–Њ–≤–µ–і–µ–љ–Є—П –Є –і–Њ–Љ–∞—И–љ–µ–є –Њ–±—Б—В–∞–љ–Њ–≤–Ї–Є —Г –њ–Њ–ґ–Є–ї—Л—Е –ї—О–і–µ–є —Б —Ж–µ–ї—М—О –Љ–Є–љ–Є–Љ–Є–Ј–Є—А–Њ–≤–∞—В—М —А–Є—Б–Ї–Є –њ–∞–і–µ–љ–Є–є (—В–∞–±–ї. 2).
–Ш, –љ–∞–Ї–Њ–љ–µ—Ж, –≤–µ–і—Г—В—Б—П —А–∞–±–Њ—В—Л –њ–Њ –Љ–µ–і–Є–Ї–∞–Љ–µ–љ—В–Њ–Ј–љ–Њ–Љ—Г –њ—А–µ–і—Г–њ—А–µ–ґ–і–µ–љ–Є—О –њ–∞–і–µ–љ–Є–є. –Я–∞–і–µ–љ–Є–µ –Є —Г—Е—Г–і—И–µ–љ–Є–µ —Д—Г–љ–Ї—Ж–Є–Њ–љ–∞–ї—М–љ—Л—Е –≤–Њ–Ј–Љ–Њ–ґ–љ–Њ—Б—В–µ–є –Њ—А–≥–∞–љ–Є–Ј–Љ–∞ –≤ –і–∞–љ–љ–Њ–є —Б–Є—В—Г–∞—Ж–Є–Є —А–∞—Б—Б–Љ–∞—В—А–Є–≤–∞–µ—В—Б—П –Ї–∞–Ї –њ—А–Њ—П–≤–ї–µ–љ–Є–µ —Б—В–∞—А–µ–љ–Є—П –Њ—А–≥–∞–љ–Є–Ј–Љ–∞, –Є–Ј–Љ–µ–љ–µ–љ–Є–µ –Ї–∞—З–µ—Б—В–≤–∞ –Є –Ї–Њ–ї–Є—З–µ—Б—В–≤–∞ –Љ—Л—И–µ—З–љ—Л—Е –≤–Њ–ї–Њ–Ї–Њ–љ, —Г—Е—Г–і—И–µ–љ–Є–µ –љ–µ—А–≤–љ–Њ––Љ—Л—И–µ—З–љ–Њ–є –њ–µ—А–µ–і–∞—З–Є, —З—Г–≤—Б—В–≤–Є—В–µ–ї—М–љ–Њ—Б—В–Є –Є –Ї–Њ–≥–љ–Є—В–Є–≤–љ—Л—Е —Д—Г–љ–Ї—Ж–Є–є. –°—А–µ–і–Є –њ—А–Є—З–Є–љ —Г—Е—Г–і—И–µ–љ–Є—П –Љ—Л—И–µ—З–љ—Л—Е —Д—Г–љ–Ї—Ж–Є–є —А–∞—Б—Б–Љ–∞—В—А–Є–≤–∞–µ—В—Б—П —Б–Њ–Љ–∞—В–Њ–њ–∞—Г–Ј–∞ (—Б–љ–Є–ґ–µ–љ–Є–µ —Б–µ–Ї—А–µ—Ж–Є–Є —Б–Њ–Љ–∞—В–Њ—В—А–Њ–њ–љ–Њ–≥–Њ –≥–Њ—А–Љ–Њ–љ–∞ – –°–Ґ–У – –≥–Є–њ–Њ—Д–Є–Ј–Њ–Љ –Є —Г–Љ–µ–љ—М—И–µ–љ–Є–µ –∞–љ–∞–±–Њ–ї–Є—З–µ—Б–Ї–Њ–≥–Њ –≤–ї–Є—П–љ–Є—П –Є–љ—Б—Г–ї–Є–љ–Њ–њ–Њ–і–Њ–±–љ–Њ–≥–Њ —Д–∞–Ї—В–Њ—А–∞ —А–Њ—Б—В–∞ –Ш–†–§–1), –Љ–µ–љ–Њ–њ–∞—Г–Ј–∞ –Є –∞–љ–і—А–Њ–њ–∞—Г–Ј–∞, –і–µ—Д–Є—Ж–Є—В D––≥–Њ—А–Љ–Њ–љ–∞ [14]. –Я—А–Є–Љ–µ–љ–µ–љ–Є–µ –≥–Њ—А–Љ–Њ–љ–∞ —А–Њ—Б—В–∞ —Г –њ–Њ–ґ–Є–ї—Л—Е –њ–∞—Ж–Є–µ–љ—В–Њ–≤ –Њ–Ї–∞–Ј–∞–ї–Њ—Б—М –љ–µ—Н—Д—Д–µ–Ї—В–Є–≤–љ—Л–Љ –і–ї—П —Г–≤–µ–ї–Є—З–µ–љ–Є—П –Љ—Л—И–µ—З–љ–Њ–є –Љ–∞—Б—Б—Л [44], —З—Г—В—М –ї—Г—З—И–Є–є —Н—Д—Д–µ–Ї—В –љ–∞–±–ї—О–і–∞–ї—Б—П –њ—А–Є —Н–љ–і–Њ–≥–µ–љ–љ–Њ–є —Б—В–Є–Љ—Г–ї—П—Ж–Є–Є –°–Ґ–У —Б–Њ–Љ–∞—В–Њ–ї–Є–±–µ—А–Є–љ–Њ–Љ [45] –Є–ї–Є –љ–∞–Ј–љ–∞—З–µ–љ–Є–Є –Ш–†–§–1 [46]. –° –і—А—Г–≥–Њ–є —Б—В–Њ—А–Њ–љ—Л, —Д–Є–Ј–Є—З–µ—Б–Ї–Є–µ —Г–њ—А–∞–ґ–љ–µ–љ–Є—П (–њ—А–Њ–≥—А–∞–Љ–Љ—Л —Б–Є–ї–Њ–≤—Л—Е —Г–њ—А–∞–ґ–љ–µ–љ–Є–є –Є —Г–њ—А–∞–ґ–љ–µ–љ–Є—П –љ–∞ –±–∞–ї–∞–љ—Б) –і–Њ–Ї–∞–Ј–∞–ї–Є —Б–≤–Њ—О —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В—М –і–ї—П —Г–ї—Г—З—И–µ–љ–Є—П —Д—Г–љ–Ї—Ж–Є–Њ–љ–∞–ї—М–љ—Л—Е –≤–Њ–Ј–Љ–Њ–ґ–љ–Њ—Б—В–µ–є –Є –њ—А–µ–і—Г–њ—А–µ–ґ–і–µ–љ–Є—П –њ–∞–і–µ–љ–Є–є, –≤ —В–Њ–Љ —З–Є—Б–ї–µ, –≤–Њ–Ј–Љ–Њ–ґ–љ–Њ, –±–ї–∞–≥–Њ–і–∞—А—П —Н–љ–і–Њ–≥–µ–љ–љ–Њ–є —Б—В–Є–Љ—Г–ї—П—Ж–Є–Є –°–Ґ–У, –Ш–†–§–1 –Є —В–µ—Б—В–Њ—Б—В–µ—А–Њ–љ–∞ [47–51]. –Я—А–Є–Љ–µ–љ–µ–љ–Є–µ —В–µ—Б—В–Њ—Б—В–µ—А–Њ–љ–∞ —Г –Љ—Г–ґ—З–Є–љ —Б –≥–Є–њ–Њ–≥–Њ–љ–∞–і–Є–Ј–Љ–Њ–Љ –Њ–Ї–∞–Ј—Л–≤–∞–ї–Њ –њ–Њ–ї–Њ–ґ–Є—В–µ–ї—М–љ—Л–є —Н—Д—Д–µ–Ї—В –љ–∞ –Љ—Л—И–µ—З–љ—Г—О —Б–Є–ї—Г [52,53]. –Ш—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ —Б —Г—З–∞—Б—В–Є–µ–Љ 199 –Љ—Г–ґ—З–Є–љ –Є 246 –ґ–µ–љ—Й–Є–љ —Б—В–∞—А—И–µ 65 –ї–µ—В –њ–Њ–Ї–∞–Ј–∞–ї–Њ, —З—В–Њ –Ї–∞–Ї –Љ—Г–ґ—З–Є–љ—Л, —В–∞–Ї –Є –ґ–µ–љ—Й–Є–љ—Л —Б –±–Њ–ї–µ–µ –≤—Л—Б–Њ–Ї–Є–Љ —Г—А–Њ–≤–љ–µ–Љ —В–µ—Б—В–Њ—Б—В–µ—А–Њ–љ–∞ –Є –і–µ–≥–Є–і—А–Њ—Н–њ–Є–∞–љ–і—А–Њ—Б—В–µ—А–Њ–љ–∞ —Б—Г–ї—М—Д–∞—В–∞ (–≤–µ—А—Е–љ—П—П —З–µ—В–≤–µ—А—В—М –љ–Њ—А–Љ–∞–ї—М–љ—Л—Е –Ј–љ–∞—З–µ–љ–Є–є) –Є–Љ–µ–ї–Є –љ–∞ 60% –±–Њ–ї–µ–µ –љ–Є–Ј–Ї–Є–є —А–Є—Б–Ї –њ–∞–і–µ–љ–Є–є. –Ф–Њ–±–∞–≤–Ї–∞ –љ–∞—В–Є–≤–љ–Њ–≥–Њ –≤–Є—В–∞–Љ–Є–љ–∞ D –Є –Ї–∞–ї—М—Ж–Є—П –њ–Њ–Ј–≤–Њ–ї–Є–ї–∞ –і–Њ–њ–Њ–ї–љ–Є—В–µ–ї—М–љ–Њ —Б–љ–Є–Ј–Є—В—М —А–Є—Б–Ї –њ–∞–і–µ–љ–Є–є —Б—А–µ–і–Є –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –≤—Л—Б–Њ–Ї–Є–Љ —Г—А–Њ–≤–љ–µ–Љ —В–µ—Б—В–Њ—Б—В–µ—А–Њ–љ–∞ –і–Њ 78–84% —Б—А–µ–і–Є –Љ—Г–ґ—З–Є–љ –Є 66–85% —Б—А–µ–і–Є –ґ–µ–љ—Й–Є–љ [54]. –Ю—З–µ–≤–Є–і–љ–Њ, —З—В–Њ –њ–∞—Ж–Є–µ–љ—В—Л —Б –≤—Л—Б–Њ–Ї–Є–Љ —Г—А–Њ–≤–љ–µ–Љ –≥–Њ—А–Љ–Њ–љ–Њ–≤, —Б–Ї–Њ—А–µ–µ –≤—Б–µ–≥–Њ, –≤ —Ж–µ–ї–Њ–Љ –±—Л–ї–Є –±–Њ–ї–µ–µ –Ј–і–Њ—А–Њ–≤—Л, –Є –µ—Б–ї–Є –љ–∞–±–ї—О–і–∞–ї—Б—П –і–µ—Д–Є—Ж–Є—В –≤–Є—В–∞–Љ–Є–љ–∞ D, –µ–≥–Њ –Ї–Њ–Љ–њ–µ–љ—Б–∞—Ж–Є—П –Є–Љ–µ–ї–∞ —Е–Њ—А–Њ—И–Є–є —А–µ–Ј—Г–ї—М—В–∞—В. –Ф–µ–є—Б—В–≤–Є—В–µ–ї—М–љ–Њ, –љ–∞–Ј–љ–∞—З–µ–љ–Є–µ –і–Њ–±–∞–≤–Њ–Ї –Ї–Њ–ї–µ–Ї–∞–ї—М—Ж–Є—Д–µ—А–Њ–ї–∞, –њ–Њ –і–∞–љ–љ—Л–Љ —Б–Њ–≤—А–µ–Љ–µ–љ–љ–Њ–≥–Њ –Љ–µ—В–∞––∞–љ–∞–ї–Є–Ј–∞, –Є–Љ–µ–µ—В –љ–µ–Ї–Њ—В–Њ—А—Л–є –њ–Њ–ї–Њ–ґ–Є—В–µ–ї—М–љ—Л–є —Н—Д—Д–µ–Ї—В –і–ї—П —Б–љ–Є–ґ–µ–љ–Є—П —А–Є—Б–Ї–∞ –њ–∞–і–µ–љ–Є–є [55]. –Т—Б–µ–≥–Њ –±—Л–ї–Њ –≤–Ї–ї—О—З–µ–љ–Њ 9 —А–∞–љ–і–Њ–Љ–Є–Ј–Є—А–Њ–≤–∞–љ–љ—Л—Е –Ї–Њ–љ—В—А–Њ–ї–Є—А—Г–µ–Љ—Л—Е –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–є: –Њ—В–љ–Њ—Б–Є—В–µ–ї—М–љ—Л–є —А–Є—Б–Ї –њ–∞–і–µ–љ–Є–є —Г –ґ–µ–љ—Й–Є–љ –≤ –њ–Њ—Б—В–Љ–µ–љ–Њ–њ–∞—Г–Ј–µ —Б—А–µ–і–Є –њ–Њ–ї—Г—З–∞–≤—И–Є—Е –≤–Є—В–∞–Љ–Є–љ D —Б–Њ—Б—В–∞–≤–Є–ї 0,92 (95% –Ф–Ш 0,75–1,12), –Њ–і–љ–∞–Ї–Њ —А–∞–Ј–ї–Є—З–Є—П (c2–—В–µ—Б—В) –њ–Њ —Б—А–∞–≤–љ–µ–љ–Є—О —Б —В–µ–Љ–Є –њ–∞—Ж–Є–µ–љ—В–∞–Љ–Є, –Ї–Њ—В–Њ—А—Л–µ –љ–µ –њ–Њ–ї—Г—З–∞–ї–Є –і–Њ–±–∞–≤–Ї—Г –≤–Є—В–∞–Љ–Є–љ–∞ D, –±—Л–ї–Є –љ–µ–і–Њ—Б—В–Њ–≤–µ—А–љ—Л–Љ–Є [55]. –Э–∞–Є–±–Њ–ї–µ–µ –≤–µ—А–Њ—П—В–љ–Њ, —Н—В–Њ —Б–≤—П–Ј–∞–љ–Њ —Б —В–µ–Љ, —З—В–Њ –Ї–Њ–ї–µ–Ї–∞–ї—М—Ж–Є—Д–µ—А–Њ–ї —Б–∞–Љ –њ–Њ —Б–µ–±–µ –љ–µ –Њ–±–ї–∞–і–∞–µ—В –±–Є–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Њ–є –∞–Ї—В–Є–≤–љ–Њ—Б—В—М—О –Є –љ—Г–ґ–і–∞–µ—В—Б—П –≤ —Ж–µ–ї–Њ–Љ —А—П–і–µ –њ—А–µ–≤—А–∞—Й–µ–љ–Є–є –і–ї—П –Њ–±—А–∞–Ј–Њ–≤–∞–љ–Є—П D––≥–Њ—А–Љ–Њ–љ–∞, —В.–µ. –љ–∞—В–Є–≤–љ—Л–є –≤–Є—В–∞–Љ–Є–љ – —Н—В–Њ –њ–Є—Й–µ–≤–∞—П –і–Њ–±–∞–≤–Ї–∞ (–љ–µ–≤–Њ–Ј–Љ–Њ–ґ–љ–Њ –њ—А–µ–і—Б–Ї–∞–Ј–∞—В—М —Д–∞—А–Љ–∞–Ї–Њ–Ї–Є–љ–µ—В–Є–Ї—Г), —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є–µ –Ї–Њ–ї–µ–Ї–∞–ї—М—Ж–Є—Д–µ—А–Њ–ї–∞ —В–Њ–ї—М–Ї–Њ —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –і–µ—Д–Є—Ж–Є—В–Њ–Љ –≤–Є—В–∞–Љ–Є–љ–∞ D (25(OH)D <30 –љ–Љ–Њ–ї—М/–ї, –Є–ї–Є <12 –љ–≥/–Љ–ї). –Я–Њ—Н—В–Њ–Љ—Г –≤–∞–ґ–љ–Њ –њ–Њ–љ–Є–Љ–∞—В—М —А–∞–Ј–љ–Є—Ж—Г –≤ –њ—А–Њ—Д–Є–ї–∞–Ї—В–Є—З–µ—Б–Ї–Њ–Љ –љ–∞–Ј–љ–∞—З–µ–љ–Є–Є –і–Њ–±–∞–≤–Ї–Є –≤–Є—В–∞–Љ–Є–љ–∞ D –њ–Њ–ґ–Є–ї—Л–Љ –њ–∞—Ж–Є–µ–љ—В–∞–Љ —Б –і–µ—Д–Є—Ж–Є—В–Њ–Љ –≤–Є—В–∞–Љ–Є–љ–∞ D –Є —Д–∞—А–Љ–∞–Ї–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Њ–є —В–µ—А–∞–њ–Є–µ–є, –љ–µ–Ј–∞–≤–Є—Б–Є–Љ–Њ –Њ—В —Г—А–Њ–≤–љ—П 25(OH)D –≤ —Б—Л–≤–Њ—А–Њ—В–Ї–µ –Ї—А–Њ–≤–Є [57]. –Я–Њ–ґ–Є–ї—Л–µ –њ–∞—Ж–Є–µ–љ—В—Л, –њ–∞—Ж–Є–µ–љ—В—Л, –њ–Њ–ї—Г—З–∞—О—Й–Є–µ —В–µ—А–∞–њ–Є—О –≥–ї—О–Ї–Њ–Ї–Њ—А—В–Є–Ї–Њ–Є–і–∞–Љ–Є, –±–Њ–ї—М–љ—Л–µ —Б–Њ —Б–љ–Є–ґ–µ–љ–љ–Њ–є —Д—Г–љ–Ї—Ж–Є–µ–є –њ–Њ—З–µ–Ї, –љ–µ—Д—А–Њ–њ–∞—В–Є–µ–є, –≥–Є–њ–µ—А—В–µ–љ–Ј–Є–µ–є, —Е—А–Њ–љ–Є—З–µ—Б–Ї–Є–Љ–Є –≤–Њ—Б–њ–∞–ї–Є—В–µ–ї—М–љ—Л–Љ–Є –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П–Љ–Є –Є —Б–∞—Е–∞—А–љ—Л–Љ –і–Є–∞–±–µ—В–Њ–Љ 1––≥–Њ —В–Є–њ–∞ —Б –≤—Л—Б–Њ–Ї–Њ–є –≤–µ—А–Њ—П—В–љ–Њ—Б—В—М—О –Љ–Њ–≥—Г—В –±—Л—В—М —А–µ–Ј–Є—Б—В–µ–љ—В–љ—Л–Љ–Є –Ї —В–µ—А–∞–њ–Є–Є –і–Њ–±–∞–≤–Ї–∞–Љ–Є –≤–Є—В–∞–Љ–Є–љ–∞ D [56,58]. –Р–Ї—В–Є–≤–љ–∞—П —Д–Њ—А–Љ–∞ –≤–Є—В–∞–Љ–Є–љ–∞ D (–∞–ї—М—Д–∞–Ї–∞–ї—М—Ж–Є–і–Њ–ї) –љ—Г–ґ–і–∞–µ—В—Б—П –≤ –Њ–і–љ–Њ–Љ –≥–Є–і—А–Њ–Ї—Б–Є–ї–Є—А–Њ–≤–∞–љ–Є–Є –≤ –њ–µ—З–µ–љ–Є (25––≥–Є–і—А–Њ–Ї—Б–Є–ї–∞–Ј–∞) –і–ї—П –њ—А–µ–≤—А–∞—Й–µ–љ–Є—П –≤ D––≥–Њ—А–Љ–Њ–љ (—А–Є—Б. 2). –Ф–∞–љ–љ–∞—П —А–µ–∞–Ї—Ж–Є—П –Њ–±–µ—Б–њ–µ—З–Є–≤–∞–µ—В –∞–ї—М—Д–∞–Ї–∞–ї—М—Ж–Є–і–Њ–ї—Г –њ—А–µ–Є–Љ—Г—Й–µ—Б—В–≤–Њ –њ–Њ —Б—А–∞–≤–љ–µ–љ–Є—О —Б –Ї–∞–ї—М—Ж–Є—В—А–Є–Њ–ї–Њ–Љ –≤ –Њ—В–љ–Њ—И–µ–љ–Є–Є –њ—А–Њ–і–Њ–ї–ґ–Є—В–µ–ї—М–љ–Њ—Б—В–Є –і–µ–є—Б—В–≤–Є—П –Є —З–∞—Б—В–Њ—В—Л –≥–Є–њ–µ—А–Ї–∞–ї—М—Ж–Є–µ–Љ–Є–Є. –Ґ–∞–Ї–Є–Љ –Њ–±—А–∞–Ј–Њ–Љ, –∞–ї—М—Д–∞–Ї–∞–ї—М—Ж–Є–і–Њ–ї –Њ—Б—В–∞–µ—В—Б—П —Н—Д—Д–µ–Ї—В–Є–≤–љ—Л–Љ –њ—А–Є —Б–љ–Є–ґ–µ–љ–Є–Є –°–Ъ–§; —В–∞–Ї–ґ–µ –Њ–њ–Є—Б–∞–љ–∞ –µ–≥–Њ —Б–њ–Њ—Б–Њ–±–љ–Њ—Б—В—М –њ—А–µ–Њ–і–Њ–ї–µ–≤–∞—В—М —А–µ–Ј–Є—Б—В–µ–љ—В–љ–Њ—Б—В—М —А–µ—Ж–µ–њ—В–Њ—А–Њ–≤ –Ї D––≥–Њ—А–Љ–Њ–љ—Г –Є —Г–≤–µ–ї–Є—З–Є–≤–∞—В—М –Є—Е —Н–Ї—Б–њ—А–µ—Б—Б–Є—О [32]. –Я—А–Є —Б—А–∞–≤–љ–Є—В–µ–ї—М–љ–Њ–Љ –Љ–µ—В–∞––∞–љ–∞–ї–Є–Ј–µ (–≤—Б–µ–≥–Њ –≤–Ї–ї—О—З–µ–љ–Њ 14 –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–є —Б –Њ–±—Й–Є–Љ –Ї–Њ–ї–Є—З–µ—Б—В–≤–Њ–Љ –њ–∞—Ж–Є–µ–љ—В–Њ–≤ 21268) –±—Л–ї–Њ –њ–Њ–Ї–∞–Ј–∞–љ–Њ, —З—В–Њ –∞–Ї—В–Є–≤–љ—Л–µ –Љ–µ—В–∞–±–Њ–ї–Є—В—Л –≤–Є—В–∞–Љ–Є–љ–∞ D (–∞–ї—М—Д–∞–Ї–∞–ї—М—Ж–Є–і–Њ–ї –Є –Ї–∞–ї—М—Ж–Є—В—А–Є–Њ–ї) —Б—В–∞—В–Є—Б—В–Є—З–µ—Б–Ї–Є –Ј–љ–∞—З–Є–Љ–Њ (—А=0,049) –±–Њ–ї—М—И–µ —Г–Љ–µ–љ—М—И–∞—О—В —А–Є—Б–Ї –њ–∞–і–µ–љ–Є–є 0,79 (95% –Ф–Ш 0,64–0,96) –њ–Њ —Б—А–∞–≤–љ–µ–љ–Є—О —Б –і–Њ–±–∞–≤–Ї–Њ–є –≤–Є—В–∞–Љ–Є–љ–∞ D 0,94 (95% –Ф–Ш 0,87–1,01) [56].
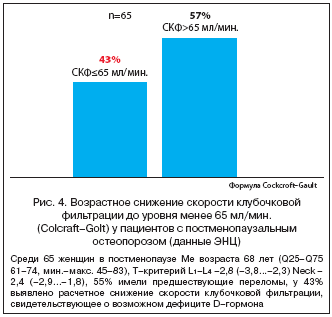
–Ы–µ—З–µ–љ–Є–µ –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –Њ—Б—В–µ–Њ–њ–Њ—А–Њ–Ј–Њ–Љ –∞–ї—М—Д–∞–Ї–∞–ї—М—Ж–Є–і–Њ–ї–Њ–Љ –≤ –і–Њ–Ј–µ 1 –Љ–Ї–≥ –≤ —В–µ—З–µ–љ–Є–µ 3–6 –Љ–µ—Б. –њ—А–Є–≤–Њ–і–Є–ї–Њ –Ї –Њ—В–љ–Њ—Б–Є—В–µ–ї—М–љ–Њ–Љ—Г —Г–≤–µ–ї–Є—З–µ–љ–Є—О –Љ—Л—И–µ—З–љ—Л—Е –≤–Њ–ї–Њ–Ї–Њ–љ —В–Є–њ–∞ –Р –Є –љ–µ–Ї–Њ—В–Њ—А–Њ–Љ—Г —Г–Љ–µ–љ—М—И–µ–љ–Є—О –≤–Њ–ї–Њ–Ї–Њ–љ —В–Є–њ–∞ B, —З—В–Њ —Б–Њ—З–µ—В–∞–ї–Њ—Б—М —Б —Г–≤–µ–ї–Є—З–µ–љ–Є–µ–Љ –њ–Њ–њ–µ—А–µ—З–љ–Њ–≥–Њ —Б–µ—З–µ–љ–Є—П –≤–Њ–ї–Њ–Ї–Њ–љ —В–Є–њ–∞ –Р [59]. –Ъ–ї–Є–љ–Є—З–µ—Б–Ї–Є –≤—А–µ–Љ—П, –Ї–Њ—В–Њ—А–Њ–µ —В—А–µ–±–Њ–≤–∞–ї–Њ—Б—М –њ–∞—Ж–Є–µ–љ—В–∞–Љ, —З—В–Њ–±—Л –Њ–і–µ—В—М—Б—П, —Б—В–∞—В–Є—Б—В–Є—З–µ—Б–Ї–Є –Ј–љ–∞—З–Є–Љ–Њ —Г–Љ–µ–љ—М—И–∞–ї–Њ—Б—М [59]. –Ъ—А–Њ–Љ–µ —В–Њ–≥–Њ, —В–µ—А–∞–њ–Є—П –∞–ї—М—Д–∞–Ї–∞–ї—М—Ж–Є–і–Њ–ї–Њ–Љ –≤ —В–µ—З–µ–љ–Є–µ 6 –Љ–µ—Б. —Г –њ–Њ–ґ–Є–ї—Л—Е –ґ–µ–љ—Й–Є–љ —Б –і–µ—Д–Є—Ж–Є—В–Њ–Љ –≤–Є—В–∞–Љ–Є–љ–∞ D –њ—А–Є–≤–Њ–і–Є–ї–∞ –Ї —Б—В–∞—В–Є—Б—В–Є—З–µ—Б–Ї–Є –Ј–љ–∞—З–Є–Љ–Њ–Љ—Г —Г–ї—Г—З—И–µ–љ–Є—О –Љ—Л—И–µ—З–љ–Њ–є —Б–Є–ї—Л (–Є–Ј–Њ–Љ–µ—В—А–Є—З–µ—Б–Ї–Њ–є —Б–Є–ї—Л —А–∞–Ј–≥–Є–±–∞–љ–Є—П –Ї–Њ–ї–µ–љ–∞) –Є —Д—Г–љ–Ї—Ж–Є–Њ–љ–∞–ї—М–љ—Л—Е –≤–Њ–Ј–Љ–Њ–ґ–љ–Њ—Б—В–µ–є –њ–∞—Ж–Є–µ–љ—В–Њ–≤ (—А–∞—Б—Б—В–Њ—П–љ–Є–µ, –Ї–Њ—В–Њ—А–Њ–µ –ґ–µ–љ—Й–Є–љ—Л –Љ–Њ–≥–ї–Є –њ—А–Њ–є—В–Є –Ј–∞ 2 –Љ–Є–љ.) [60]. –Я–∞—Ж–Є–µ–љ—В—Л —Б –Њ—Б—В–µ–Њ–њ–µ–љ–Є–µ–є –љ–∞ —Д–Њ–љ–µ —А–µ–≤–Љ–∞—В–Њ–Є–і–љ–Њ–≥–Њ –∞—А—В—А–Є—В–∞ –Є –љ–Њ—А–Љ–∞–ї—М–љ—Л–Љ —Г—А–Њ–≤–љ–µ–Љ –≤–Є—В–∞–Љ–Є–љ–∞ D (49–59 –љ–Љ–Њ–ї—М/–ї), –Ї–Њ—В–Њ—А—Л–µ –њ–Њ–ї—Г—З–∞–ї–Є 1 –Љ–Ї–≥ –∞–ї—М—Д–∞–Ї–∞–ї—М—Ж–Є–і–Њ–ї–∞ –µ–ґ–µ–і–љ–µ–≤–љ–Њ, –њ–Њ–Ї–∞–Ј–∞–ї–Є —Б—В–∞—В–Є—Б—В–Є—З–µ—Б–Ї–Є –Ј–љ–∞—З–Є–Љ–Њ–µ —Г–ї—Г—З—И–µ–љ–Є–µ –Љ—Л—И–µ—З–љ–Њ–є —Б–Є–ї—Л (–љ–∞ 60%) –њ–Њ —Б—А–∞–≤–љ–µ–љ–Є—О —Б —Г–ї—Г—З—И–µ–љ–Є–µ–Љ –Љ—Л—И–µ—З–љ–Њ–є —Б–Є–ї—Л –ї–Є—И—М –љ–∞ 18% —Г —В–∞–Ї–Є—Е –ґ–µ –±–Њ–ї—М–љ—Л—Е, –њ–Њ–ї—Г—З–∞–≤—И–Є—Е –і–Њ–±–∞–≤–Ї—Г –≤–Є—В–∞–Љ–Є–љ–∞ D –≤ –і–Њ–Ј–µ 1000 –Ь–Х –µ–ґ–µ–і–љ–µ–≤–љ–Њ [61]. –Э–∞ –Њ—Б–љ–Њ–≤–∞–љ–Є–Є –≤–њ–Њ–ї–љ–µ —Г—Б–њ–µ—И–љ—Л—Е –њ–Є–ї–Њ—В–љ—Л—Е –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–є –±—Л–ї–Є –њ—А–Њ–≤–µ–і–µ–љ—Л —А–∞–љ–і–Њ–Љ–Є–Ј–Є—А–Њ–≤–∞–љ–љ—Л–µ –њ–ї–∞—Ж–µ–±–Њ––Ї–Њ–љ—В—А–Њ–ї–Є—А—Г–µ–Љ—Л–µ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П, –і–Њ–Ї–∞–Ј–∞–≤—И–Є–µ –≤–Њ–Ј–Љ–Њ–ґ–љ–Њ—Б—В–Є –∞–ї—М—Д–∞–Ї–∞–ї—М—Ж–Є–і–Њ–ї–∞ –њ—А–µ–і–Њ—В–≤—А–∞—Й–∞—В—М –њ–∞–і–µ–љ–Є—П –Є –њ–µ—А–µ–ї–Њ–Љ—Л —Г –ґ–µ–љ—Й–Є–љ —Б –Њ—Б—В–µ–Њ–њ–µ–љ–Є–µ–є –≤ –≤–Њ–Ј—А–∞—Б—В–µ 65–77 –ї–µ—В –љ–∞ —Д–Њ–љ–µ –Ч–У–Ґ –њ–Њ —Б—А–∞–≤–љ–µ–љ–Є—О —Б —В–µ–Љ–Є, –Ї—В–Њ –њ–Њ–ї—Г—З–∞–ї —В–Њ–ї—М–Ї–Њ –Ч–У–Ґ [62,63], –∞ —В–∞–Ї–ґ–µ —Г –Љ—Г–ґ—З–Є–љ –Є –ґ–µ–љ—Й–Є–љ (—Б—А–µ–і–љ–Є–є –≤–Њ–Ј—А–∞—Б—В 75 –ї–µ—В) –∞–ї—М—Д–∞–Ї–∞–ї—М—Ж–Є–і–Њ–ї 1 –Љ–Ї–≥ –њ–Њ–Ј–≤–Њ–ї–Є–ї —Б–љ–Є–Ј–Є—В—М —А–Є—Б–Ї –њ–∞–і–µ–љ–Є–є –Ј–∞ 9 –Љ–µ—Б. –љ–∞–±–ї—О–і–µ–љ–Є—П [64]. –Ю–і–љ–∞–Ї–Њ –Њ—Б–Њ–±–µ–љ–љ–Њ —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ –љ–∞–Ј–љ–∞—З–µ–љ–Є–µ –Р–ї—М—Д–∞––Ф3––Ґ–µ–≤–∞ –≤ –і–Њ–Ј–µ 1 –Љ–Ї–≥ –±—Л–ї–Њ —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –≤–Њ–Ј—А–∞—Б—В–љ—Л–Љ —Б–љ–Є–ґ–µ–љ–Є–µ–Љ —Б–Ї–Њ—А–Њ—Б—В–Є –Ї–ї—Г–±–Њ—З–Ї–Њ–≤–Њ–є —Д–Є–ї—М—В—А–∞—Ж–Є–Є (<65 –Љ–ї/–Љ–Є–љ.). –£ —Н—В–Є—Е –±–Њ–ї—М–љ—Л—Е —Б—В–∞—В–Є—Б—В–Є—З–µ—Б–Ї–Є –Ј–љ–∞—З–Є–Љ–Њ –Є –±–µ–Ј–Њ–њ–∞—Б–љ–Њ —Г–Љ–µ–љ—М—И–∞–µ—В—Б—П –≤—Л—Б–Њ–Ї–Є–є —А–Є—Б–Ї –њ–∞–і–µ–љ–Є–є (–71%) [65]. –°—А–µ–і–Є –њ–Њ–ґ–Є–ї—Л—Е –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –Њ—Б—В–µ–Њ–њ–Њ—А–Њ–Ј–Њ–Љ –њ–Њ–і–Њ–±–љ–Њ–µ —Б–љ–Є–ґ–µ–љ–Є–µ —Б–Ї–Њ—А–Њ—Б—В–Є –Ї–ї—Г–±–Њ—З–Ї–Њ–≤–Њ–є —Д–Є–ї—М—В—А–∞—Ж–Є–Є –≤—Б—В—А–µ—З–∞–µ—В—Б—П –і–Њ—Б—В–∞—В–Њ—З–љ–Њ —З–∞—Б—В–Њ. –Т –§–У–£ –≠–Э–¶ –њ—А–Є –∞–љ–∞–ї–Є–Ј–µ –і–∞–љ–љ—Л—Е 65 –ґ–µ–љ—Й–Є–љ —Б –њ–Њ—Б—В–Љ–µ–љ–Њ–њ–∞—Г–Ј–∞–ї—М–љ—Л–Љ –Њ—Б—В–µ–Њ–њ–Њ—А–Њ–Ј–Њ–Љ –Љ–µ–і–Є–∞–љ–∞ –≤–Њ–Ј—А–∞—Б—В–∞ 68 –ї–µ—В (–Љ–Є–љ–Є–Љ—Г–Љ 45, –Љ–∞–Ї—Б–Є–Љ—Г–Љ 83 –≥–Њ–і–∞). –°–љ–Є–ґ–µ–љ–Є–µ –°–Ъ–§ –і–Њ —Г—А–Њ–≤–љ—П –Љ–µ–љ–µ–µ 65 –Љ–ї/–Љ–Є–љ. –±—Л–ї–Њ –Њ–±–љ–∞—А—Г–ґ–µ–љ–Њ —Г 43% –њ–∞—Ж–Є–µ–љ—В–Њ–≤ (—А–Є—Б. 4), —В.–µ. —Н—В–Є –ґ–µ–љ—Й–Є–љ—Л —Б –≤—Л—Б–Њ–Ї–Њ–є –≤–µ—А–Њ—П—В–љ–Њ—Б—В—М—О –і–∞–ґ–µ –њ—А–Є –љ–Њ—А–Љ–∞–ї—М–љ–Њ–Љ —Б–Њ–і–µ—А–ґ–∞–љ–Є–Є –≤–Є—В–∞–Љ–Є–љ–∞ D —Б—В—А–∞–і–∞—О—В –Њ—В –і–µ—Д–Є—Ж–Є—В–∞ –±–Є–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є –∞–Ї—В–Є–≤–љ–Њ–є —Д–Њ—А–Љ—Л – D––≥–Њ—А–Љ–Њ–љ–∞.
–Х—Б—В–µ—Б—В–≤–µ–љ–љ–Њ, —Б–љ–Є–ґ–µ–љ–Є–µ —А–Є—Б–Ї–∞ –њ–∞–і–µ–љ–Є–є –і–Њ–ї–ґ–љ–Њ –њ—А–Є–≤–Њ–і–Є—В—М –Ї —Б–љ–Є–ґ–µ–љ–Є—О —А–Є—Б–Ї–∞ –њ–µ—А–µ–ї–Њ–Љ–Њ–≤ –і–∞–ґ–µ –љ–µ–Ј–∞–≤–Є—Б–Є–Љ–Њ –Њ—В –њ—А–Є–±–∞–≤–Ї–Є –Ь–Я–Ъ–Ґ. –Т–Љ–µ—Б—В–µ —Б —В–µ–Љ, –ї–µ—З–µ–љ–Є–µ –∞–ї—М—Д–∞–Ї–∞–ї—М—Ж–Є–і–Њ–ї–Њ–Љ –≤ –і–Њ–Ј–µ 1 –Љ–Ї–≥ —Б–њ–Њ—Б–Њ–±—Б—В–≤—Г–µ—В –љ–µ–±–Њ–ї—М—И–Њ–є –њ—А–Є–±–∞–≤–Ї–µ –Ь–Я–Ъ–Ґ –Є —Г–ї—Г—З—И–µ–љ–Є—О –Ї–∞—З–µ—Б—В–≤–∞ –Ї–Њ—Б—В–Є, —З—В–Њ —Б–Њ–њ—А–Њ–≤–Њ–ґ–і–∞–µ—В—Б—П –і–Њ–Ї–∞–Ј–∞–љ–љ—Л–Љ —Б–љ–Є–ґ–µ–љ–Є–µ–Љ —А–Є—Б–Ї–∞ –њ–µ—А–µ–ї–Њ–Љ–Њ–≤ –њ–Њ–Ј–≤–Њ–љ–Ї–Њ–≤ –Є –≤–љ–µ–њ–Њ–Ј–≤–Њ–љ–Њ—З–љ—Л—Е –њ–µ—А–µ–ї–Њ–Љ–Њ–≤ –Ї–∞–Ї —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –њ–Њ—Б—В–Љ–µ–љ–Њ–њ–∞—Г–Ј–∞–ї—М–љ—Л–Љ –Є —Б–µ–љ–Є–ї—М–љ—Л–Љ –Њ—Б—В–µ–Њ–њ–Њ—А–Њ–Ј–Њ–Љ (–Њ—В–љ–Њ—Б–Є—В–µ–ї—М–љ—Л–є —А–Є—Б–Ї (–Ю–†) –њ–µ—А–µ–ї–Њ–Љ–Њ–≤ –њ–Њ–Ј–≤–Њ–љ–Ї–Њ–≤ 0,53 (95% –Ф–Ш 0,47–0,60) –Є –Ю–† –≤–љ–µ–њ–Њ–Ј–≤–Њ–љ–Њ—З–љ—Л—Е –њ–µ—А–µ–ї–Њ–Љ–Њ–≤ 0,34 (95% –Ф–Ш 0,16–0,71)) [66,67], —В–∞–Ї –Є –њ—А–Є –≥–ї—О–Ї–Њ–Ї–Њ—А—В–Є–Ї–Њ–Є–і–Є–љ–і—Г—Ж–Є—А–Њ–≤–∞–љ–љ–Њ–Љ –Њ—Б—В–µ–Њ–њ–Њ—А–Њ–Ј–µ [67]. –І–∞—Б—В–Њ—В–∞ –њ–µ—А–µ–ї–Њ–Љ–Њ–≤ –±–µ–і—А–∞ –Ј–љ–∞—З–Є–Љ–Њ —Б–љ–Є–Ј–Є–ї–∞—Б—М —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤, –њ–µ—А–µ–љ–µ—Б—И–Є—Е –Є–љ—Б—Г–ї—М—В, —Г–ґ–µ —З–µ—А–µ–Ј 6 –Љ–µ—Б. –ї–µ—З–µ–љ–Є—П –∞–ї—М—Д–∞–Ї–∞–ї—М—Ж–Є–і–Њ–ї–Њ–Љ –≤ –і–Њ–Ј–µ 1 –Љ–Ї–≥ [69] –Є —З–µ—А–µ–Ј 18 –Љ–µ—Б. –ї–µ—З–µ–љ–Є—П –њ–Њ–ґ–Є–ї—Л—Е –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –±–Њ–ї–µ–Ј–љ—М—О –Я–∞—А–Ї–Є–љ—Б–Њ–љ–∞ [69].
–Э–∞—А—П–і—Г —Б —Е–Њ—А–Њ—И–µ–є —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В—М—О –∞–ї—М—Д–∞–Ї–∞–ї—М—Ж–Є–і–Њ–ї–∞ (–Р–ї—М—Д–∞ –Ф3––Ґ–µ–≤–∞) –і–ї—П –њ—А–µ–і–Њ—В–≤—А–∞—Й–µ–љ–Є—П –њ–∞–і–µ–љ–Є–є –Є –њ–µ—А–µ–ї–Њ–Љ–Њ–≤ —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –њ–Њ—Б—В–Љ–µ–љ–Њ–њ–∞—Г–Ј–∞–ї—М–љ—Л–Љ –Є —Б–µ–љ–Є–ї—М–љ—Л–Љ –Њ—Б—В–µ–Њ–њ–Њ—А–Њ–Ј–Њ–Љ –њ—А–µ–њ–∞—А–∞—В —Е–Њ—А–Њ—И–Њ –њ–µ—А–µ–љ–Њ—Б–Є—В—Б—П. –Т –њ–Њ—Б—В–Љ–∞—А–Ї–µ—В–Є–љ–≥–Њ–≤–Њ–Љ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є —Б—А–µ–і–Є 13550 –њ–∞—Ж–Є–µ–љ—В–Њ–≤ –Љ–Є–љ–Є–Љ–∞–ї—М–љ—Л–µ –њ–Њ–±–Њ—З–љ—Л–µ —Н—Д—Д–µ–Ї—В—Л –≤—Б—В—А–µ—З–∞–ї–Є—Б—М –ї–Є—И—М –≤ 1,1% —Б–ї—Г—З–∞–µ–≤, –≤–Ї–ї—О—З–∞—П 0,22% –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –≥–Є–њ–µ—А–Ї–∞–ї—М—Ж–Є–µ–Љ–Є–µ–є –±–µ–Ј –Ї–∞–Љ–љ–µ–Њ–±—А–∞–Ј–Њ–≤–∞–љ–Є—П –≤ –њ–Њ—З–Ї–∞—Е [70]. –Ф–ї—П –Є—Б–Ї–ї—О—З–µ–љ–Є—П –≥–Є–њ–µ—А–Ї–∞–ї—М—Ж–Є–µ–Љ–Є–Є –љ–µ–Њ–±—Е–Њ–і–Є–Љ–Њ –њ—А–Њ–≤–µ—А—П—В—М —Г—А–Њ–≤–µ–љ—М –Ї–∞–ї—М—Ж–Є—П –≤ —Б—Л–≤–Њ—А–Њ—В–Ї–µ –Ї—А–Њ–≤–Є –Є –Љ–Њ—З–µ –њ–µ—А–µ–і –љ–∞–Ј–љ–∞—З–µ–љ–Є–µ–Љ –њ—А–µ–њ–∞—А–∞—В–∞ –Є —З–µ—А–µ–Ј 1–3–6 –Љ–µ—Б. –њ–Њ—Б–ї–µ –љ–∞—З–∞–ї–∞ —В–µ—А–∞–њ–Є–Є. –Я—А–Є –њ–Њ–≤—Л—И–µ–љ–Є–Є —Г—А–Њ–≤–љ—П –Ї–∞–ї—М—Ж–Є—П –≤ –Ї—А–Њ–≤–Є –≤—Л—И–µ –љ–Њ—А–Љ–∞–ї—М–љ—Л—Е –Ј–љ–∞—З–µ–љ–Є–є —В–µ—А–∞–њ–µ–≤—В–Є—З–µ—Б–Ї—Г—О –і–Њ–Ј—Г –њ—А–µ–њ–∞—А–∞—В–∞ 1 –Љ–Ї–≥ –Љ–Њ–ґ–љ–Њ —Г–Љ–µ–љ—М—И–Є—В—М –і–Њ 0,5 –Љ–Ї–≥.
–Ь–љ–Њ–≥–Њ–Њ–±–µ—Й–∞—О—Й–Є–Љ–Є –Ї–∞–ґ—Г—В—Б—П –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П –њ–Њ —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В–Є –Ї–Њ–Љ–±–Є–љ–Є—А–Њ–≤–∞–љ–љ–Њ–є —В–µ—А–∞–њ–Є–Є –±–Є—Б—Д–Њ—Б—Д–Њ–љ–∞—В–∞–Љ–Є –Є –∞–ї—М—Д–∞–Ї–∞–ї—М—Ж–Є–і–Њ–ї–Њ–Љ, –њ–Њ–Ї–∞–Ј–∞–≤—И–Є–µ –ї—Г—З—И—Г—О –њ—А–Є–±–∞–≤–Ї—Г –Ь–Я–Ъ –њ–Њ —Б—А–∞–≤–љ–µ–љ–Є—О —Б –њ—А–Є–µ–Љ–Њ–Љ –∞–ї–µ–љ–і—А–Њ–љ–∞—В–∞ –≤ —Б–Њ—З–µ—В–∞–љ–Є–Є —Б –љ–∞—В–Є–≤–љ—Л–Љ –≤–Є—В–∞–Љ–Є–љ–Њ–Љ D [71]. –Ю—Б–Њ–±–µ–љ–љ–Њ –Є–љ—В–µ—А–µ—Б–љ—Л –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П –љ–∞ –ґ–Є–≤–Њ—В–љ—Л—Е, –њ—А–Њ–і–µ–Љ–Њ–љ—Б—В—А–Є—А–Њ–≤–∞–≤—И–Є–µ, —З—В–Њ –њ—А–Є –Ї–Њ–Љ–±–Є–љ–Є—А–Њ–≤–∞–љ–љ–Њ–Љ –ї–µ—З–µ–љ–Є–Є –љ–µ —В–Њ–ї—М–Ї–Њ —Б–Ї–ї–∞–і—Л–≤–∞—О—В—Б—П –њ–Њ–Ј–Є—В–Є–≤–љ—Л–µ —Н—Д—Д–µ–Ї—В—Л –±–Є—Б—Д–Њ—Б—Д–Њ–љ–∞—В–Њ–≤ –Є –∞–ї—М—Д–∞–Ї–∞–ї—М—Ж–Є–і–Њ–ї–∞ –љ–∞ –Ь–Я–Ъ, –љ–Њ –Є —Г–ї—Г—З—И–∞–µ—В—Б—П –Ї–∞—З–µ—Б—В–≤–Њ –Ї–Њ—Б—В–љ–Њ–є —В–Ї–∞–љ–Є, –Њ—Ж–µ–љ–µ–љ–љ–Њ–µ –њ—А–Є –≥–Є—Б—В–Њ–Љ–Њ—А—Д–Њ–Љ–µ—В—А–Є–Є, –∞ —В–∞–Ї–ґ–µ —Г–≤–µ–ї–Є—З–Є–≤–∞–µ—В—Б—П —Б–Є–ї–∞, –Ї–Њ—В–Њ—А—Г—О –љ—Г–ґ–љ–Њ –њ—А–Є–ї–Њ–ґ–Є—В—М, —З—В–Њ–±—Л —Б–ї–Њ–Љ–∞—В—М –Ї–Њ—Б—В—М [72].
–Ч–∞–Ї–ї—О—З–µ–љ–Є–µ
–Я–∞–і–µ–љ–Є—П – —Б–µ—А—М–µ–Ј–љ–∞—П –њ—А–Њ–±–ї–µ–Љ–∞ —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ –њ–Њ–ґ–Є–ї–Њ–≥–Њ –≤–Њ–Ј—А–∞—Б—В–∞, –Њ–і–Є–љ –Є–Ј –љ–∞–Є–±–Њ–ї–µ–µ —Б—Г—Й–µ—Б—В–≤–µ–љ–љ—Л—Е —Д–∞–Ї—В–Њ—А–Њ–≤ —А–Є—Б–Ї–∞ –≤–љ–µ–њ–Њ–Ј–≤–Њ–љ–Њ—З–љ—Л—Е –њ–µ—А–µ–ї–Њ–Љ–Њ–≤, –∞ —В–∞–Ї–ґ–µ —В—А–∞–≤–Љ –Љ—П–≥–Ї–Є—Е —В–Ї–∞–љ–µ–є. –Ю—Ж–µ–љ–Ї–∞ —Б–Ї–Њ—А–Њ—Б—В–Є –Ї–ї—Г–±–Њ—З–Ї–Њ–≤–Њ–є —Д–Є–ї—М—В—А–∞—Ж–Є–Є, —Д–∞–Ї—В–Њ—А–Њ–≤ —А–Є—Б–Ї–∞ –њ–∞–і–µ–љ–Є—П –Є –њ—А–Њ–≤–µ–і–µ–љ–Є–µ —Д—Г–љ–Ї—Ж–Є–Њ–љ–∞–ї—М–љ—Л—Е —В–µ—Б—В–Њ–≤ –њ–Њ–Љ–Њ–≥—Г—В –≤—Л–і–µ–ї–Є—В—М –њ–∞—Ж–Є–µ–љ—В–Њ–≤, –Ї–Њ—В–Њ—А—Л–µ –Њ—Б–Њ–±–µ–љ–љ–Њ –љ—Г–ґ–і–∞—О—В—Б—П –≤ –њ—А–Њ—Д–Є–ї–∞–Ї—В–Є–Ї–µ –њ–∞–і–µ–љ–Є–є. –Я—А–Є–Љ–µ–љ–µ–љ–Є–µ –∞–ї—М—Д–∞–Ї–∞–ї—М—Ж–Є–і–Њ–ї–∞ (–Р–ї—М—Д–∞––Ф3––Ґ–µ–≤–∞) –Є–Љ–µ–µ—В –њ–∞—В–Њ–≥–µ–љ–µ—В–Є—З–µ—Б–Ї–Њ–µ –Њ–±–Њ—Б–љ–Њ–≤–∞–љ–Є–µ –Є –і–Њ–Ї–∞–Ј–∞—В–µ–ї—М–љ—Г—О –±–∞–Ј—Г —Г—А–Њ–≤–љ—П –Р (–Љ–µ—В–∞––∞–љ–∞–ї–Є–Ј—Л) –≤ –Њ—В–љ–Њ—И–µ–љ–Є–Є –њ—А–µ–і—Г–њ—А–µ–ґ–і–µ–љ–Є—П –њ–∞–і–µ–љ–Є–є –Є –њ–µ—А–µ–ї–Њ–Љ–Њ–≤ —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ –њ–Њ–ґ–Є–ї–Њ–≥–Њ –≤–Њ–Ј—А–∞—Б—В–∞ —Б –њ–µ—А–≤–Є—З–љ—Л–Љ –Њ—Б—В–µ–Њ–њ–Њ—А–Њ–Ј–Њ–Љ, –∞ —В–∞–Ї–ґ–µ –≥–ї—О–Ї–Њ–Ї–Њ—А—В–Є–Ї–Њ–Є–і–љ—Л–Љ –Њ—Б—В–µ–Њ–њ–Њ—А–Њ–Ј–Њ–Љ –Є –Њ—Б—В–µ–Њ–њ–Њ—А–Њ–Ј–Њ–Љ –љ–∞ —Д–Њ–љ–µ –Є–Љ–Љ–Њ–±–Є–ї–Є–Ј–∞—Ж–Є–Є (–Є–љ—Б—Г–ї—М—В, –њ–∞—А–Ї–Є–љ—Б–Њ–љ–Є–Ј–Љ). –Р–Ї—В–Є–≤–љ—Л–µ –Љ–µ—В–∞–±–Њ–ї–Є—В—Л –≤–Є—В–∞–Љ–Є–љ–∞ D (–Р–ї—М—Д–∞––Ф3––Ґ–µ–≤–∞) –Њ—Б–Њ–±–µ–љ–љ–Њ —Н—Д—Д–µ–Ї—В–Є–≤–љ—Л –і–ї—П –њ—А–µ–і—Г–њ—А–µ–ґ–і–µ–љ–Є—П –њ–∞–і–µ–љ–Є–є —Г –±–Њ–ї—М–љ—Л—Е —Б–Њ —Б–љ–Є–ґ–µ–љ–љ–Њ–є —Б–Ї–Њ—А–Њ—Б—В—М—О –Ї–ї—Г–±–Њ—З–Ї–Њ–≤–Њ–є —Д–Є–ї—М—В—А–∞—Ж–Є–Є, –љ–Њ —В–∞–Ї–ґ–µ —Б–љ–Є–ґ–∞—О—В —А–Є—Б–Ї –њ–∞–і–µ–љ–Є–є –≤ –Њ–±—Й–µ–є –њ–Њ–њ—Г–ї—П—Ж–Є–Є —Б—В–∞—В–Є—Б—В–Є—З–µ—Б–Ї–Є –Ј–љ–∞—З–Є–Љ–Њ –ї—Г—З—И–µ, —З–µ–Љ –Ї–Њ–ї–µ–Ї–∞–ї—М—Ж–Є—Д–Є—А–Њ–ї.

–Ы–Є—В–µ—А–∞—В—Г—А–∞
1. Tinetti ME, Williams CS.: The effect of falls and fall injuries on functioning in community–dwelling older persons.// J. Gerontol A Biol Sci Med Sci, 1998, Vol. 53 M112–119.
2. Tinetti ME, Williams CS.: Falls, injuries due to falls, and the risk of admission to a nursing home.// New England J. Medicine, 1997, Vol. 337, pp. 1279–1284.
3. Tinetti ME, Speechley M, Ginter SF.: Risk factors for falls among elderly persons living in the community.// New England J. Medicine, 1988, Vol. 319, pp. 1701–1707.
4. Sattin RW, Lambert HAD, DeVitro CA, et.al.: The incidence of fall injury events among the elderly in a defined population.// Am. J. Epidemol., 1990, Vol. 131, pp. 1028–1037.
5. Rekeneire N, Visser M, Peila R, et.al.: Is a fall just a fall: correlates of falling in healthy older persons. The Health, aging and body composition study. J. Am Geriatr Soc, 2003, Vol. 51, pp. 841–846.
6. Nevitt MC, Cummings SR, Kidd S, et.al.: Risk factors for recurrent nonsyncopal falls. A prospective study. JAMA, 1989, Vol. 261, pp. 2663–2668.
7. Jarvinen TLN, Sievanen H, Khan KM, Heinonen A, Kannus P.: Shifting the focus in fracture prevention from osteoporosis to falls.// British Medical J., 2008, Vol.336, pp. 124–126.
8. Kannus P, Niemi S, Parkkari J, Palvanen M, Heinonen A, Sievanen H, et al. Why is the age–standardized incidence of low–trauma fractures rising in many elderly populations? J Bone Miner Res 2002, Vol. 17, pp.1363–1367.
9. Kannus P, Sievanen H, Palvanen M, Jarvinen T, Parkkari J. Prevention of falls and consequent injuries in elderly people. Lancet 2005, Vol. 366 pp.1885–1893.
10. Maki BE, Mcllroy WE.: Control of rapid limb movements for balance recovery: age–related changes and implications for fall prevention// Age and Ageing, 2006, Vol. 35–S2, ii.12–18.
11. Maki BE, Mcllroy WE.: The role of limb movements in maintaining uptight stance: the “change–in–support strategy.// Phys Ther, 1997, Vol. 77, pp. 488–507.
12. Maki BE, Mcllroy WE.: Control of compensatory stepping reactions: age–related impairment and the potential for remedial intervention.// Phusiotherapy Theory Pract, 1999, Vol. 15, pp. 69–90.
13. Burleigh AL, Horak FB, Malouin F.: Modification of postural responses and step initiation: evidence for goal–directed postural interactions.// J. Neurophysiology, 1994, Vol. 72, pp. 2892–290.
14. Lang T, Streeper T, Cawthon P, Baldwin K, Taaffe DR, Harris TB.: Sarcopenia: etiology, clinical consequences, intervention, and assessment.// J. Osteoporosis International, 2009, epub ahead of printing.
15. Mcllroy WE, Maki BE.: Age–related changes in compensatory stepping in response to unpredictable perturbations.// J. Gerontol, 1996, Vol.51A: M289–296.
16. Maki BE, Edmondstone MA, Perry SD, Heung E, Quant S, Mcllroy WE.: Control of rapid limb movements for balance recovery: do age–related changes predict falling risk? In: Duysens J, Smits–Engelsman BCM, Kingma H, eds. Control of Posture and Gait. Maastricht, Netherlands: International Society for Postural and Gait Research, 2001, pp. 126–129.
17. Maki BE, Edmondstone MA, Mcllroy WE.: Age–related differences in laterally directed compensatory stepping behavior.// Gerontology, 2000, Vol. 55A, M270–277
18. Nevitt MC, Cummings SR.: Type of fall and risk of hip and wrist fractures: the study of osteoporotic fractures.// J. Am Geriatr Soc, 1993, Vol.41, pp.1226–1234.
19. Greenspan SL, Myers ER, Maitland LA, Resnick NM, Hayes WC.: Fall severity and bone mineral density as risk factors for hip fracture in ambulatory elderly.// JAMA, 1994, Vol. 271, pp. 123–128.
20. Helden S, Geel AC, Geusens PP, Kessels A, Nieuwenhuijzen Kruseman AC, Brink PR.: Bone and fall–related fracture risks in women and men with a recent clinical fracture.// J. Bone Joint Surg Am., 2008, Vol.90, pp.241–248.
21, Barret–Connor E, Weiss TW, McHorney CA, Miller PD, Siris ES.: Predictors of falls among postmenopausal women: results from the National Osteoporosis Risk Assessment (NORA).// J. Osteoporosis International, 2009, Vol. 20, pp. 715–722.
22. Gerdhem P, Ringsberg KAM, Obrant KJ, Akesson K.: Association between 25–hydroxy vitamin D levels, physical activity, muscle strength and fractures in the prospective population–based OPRA study of elderly women.//J. Osteoporosis International, 2005, Vol.16, pp.1425–1431.
23. Nakamura K, Oshiki R, Hatakeyama K, Nishiwaki T, Ueno K, Nashimoto M, Saito T, Tsuchiya Y, Okuda Y, Yamamoto M.: Vitamin D status, postural sway, and the incidence of falls in elderly community–dwelling Japanese women.// Arch Osteoporosis, 2006, Vol.1, pp. 21–27.
24. Dukas L, Schacht E, Runge M.: Independent from muscle power and balance performance, a creatinine clearance below 65 ml/min is a significant and independent risk factor for falls and fall–related fractures in elderly men and women diagnosed with osteoporosis.// Osteoporosis International, 2009, published online 22 September.
25. Birge SJ, Haddad JG.: 25–Hydroxycholecalciferol stimulation of muscle metabolism.// J. Clin Invest, 1975, Vol. 56, pp. 1100–1107.
26. Bischoff HA, Borchers M, Gudat F, Duermueller U, Theiler R, Stahelin HB, Dick W.: Un situ detection of 1,25 dihydroxyvitamin D receptor in human skeletal muscle tissue.// Histochem, 2001, Vol.33, pp. 19–24.
27. Boland R.: Role of vitamin D in skeletal muscle function.// Endocr Rev, 1986, Vol.7, pp. 434–448.
28. Costa EM, Blau HM, Feldman D.: 1,25–Dihydroxyvitamin D3 receptors and hormonal responses in cloned human skeletal muscle cells.// Endocrinology, 1986, Vol. 119, pp. 2214–2220.
29. Janssen HCJP, Samson MM, Verhaar HHJ.: Vitamin D deficiency, muscle function, and falls in elderly people// Am J Clin Nutr, 2002, Vol. 75, pp. 611–615.
30. Boland R, de Boland AR, Marinissen MJ, Santillan G, Vazquez G, Zannello S.: Avian muscle cells as targets for the secosteroid hormone 1,25 dihydroxyvitamin D3.// J Mol Cell Endocrinol, 1995, Vol. 114, pp.1–8.
31. Barr R, Macdonald H, Stewart A, McGuigan F, Rogers A, Eastell R, Felsenberg D, Gluer G, Roux C, Reid M.: Association between vitamin D receptor gene polymorphisms, falls, balance and muscle power: results from two independent studies (APOSS and OPUS)// J. Osteoporosis International, published online 24 July, 2009.
32. Schacht E, Richy F, Reginster J–Y.: The therapeutic effects of alfacalcidol on bone strength, muscle metabolism and prevention of falls and fractures.// J. Musculoskelet Neuronal Interact, 2005, Vol. 5, pp. 273–284.
33. Baum E, Peters KM: The diagnosis and treatment of primary osteoporosis according to current guidelines.// Dtsch Arztebl Int, 2008, Vol. 105, pp. 573–582.
34. Podsialdo D, Richardson S.: The timed “Up and go”: a test of basic functional mobility for frail elderly persons” J. Am. Geriatr Soc, 1991, Vol. 39 (2), pp. 142–148.
35. Mathias S, Nayak US, Isaacs B.: Balance in elderly patients: the “get–up and go” test.// Arch Phys Med Rehabil, 1986, Vol. 67, pp. 387–389.
36. Zhu K, Devine A, Prince RL: Timed Up and Go test and BMD as predictors of fractures: a 10–year longitudinal study.// J. Bone Mineral Research, 2008, Vol. 23, s119.
37. Runge M, Rehfeld G, Resnicek E.: Balance training and exercise in geriatric patients.// J. Musculoskel Neuronal Interact, 2000, Vol. 1, pp. 54–58.
38. Gill TM, Williams CS, Tinetti ME.: Assessing risk for the onset of functional dependence among older adults: the role of physical performance.// J. American Geriatr Soc, 1995, Vol. 43, pp. 603–609.
39. Guralnik JM, Ferrucci L, Simonsick EM, Salive ME, Wallace RB.: Lower–extremity function in persons over the age of 70 years as a predictor of subsequent disability.// New England J. Medicine, 1995, Vol. 332, pp. 556–561.
40. Karkkainen M, Rikkonen T, Kroger H, Sirola J, Tuppurainen M, Salovaara K, Arokoski J, Jurvelin J, Honkanen R, Alhava E.: Association between functional capacity tests and fractures: an eight–year prospective population–based cohort study.// Osteoporosis International, 2008, published ached of printing.
41. Kenny RA, Richardson DA, Steen N, Bexton RS, Shaw FE, Bond J.: Carotid sinus syndrome: a modifiable risk factor for nonaccidental falls in older adults (SAFE PACE).// J. Am Coll Cardiol, 2001, Vol. 38, pp. 1491–1496.
42. Close J, Ellis M, Hooper R, Glucksman E, Jackson S, Swift C.: Prevention of falls in the elderly trial (PROFET): a randomized controlled trial.// Lancet, 1999, Vol. 353, pp. 93–97.
43. Swift CC.: The role of medical assessment and intervention in the prevention of falls.// J. Age and Ageing, 2006, Vol.35–S2, ii65–ii68.
44. Borst SE.: Interventions for sarcopenia and muscle weakness in older people.// Age Ageing, 2004, Vol. 33, pp. 548–555.
45. Fuh VL, Bach MA.: Growth hormone secretagogues: mechanism of action and use in ageing.// Growth Horm IGF Res, 1998, Vol. 8, pp. 13–20.
46. Boonen S, Rosen C, Bouillon R, Sommer A, McKay M, Rosen D, Adams S, Broos P, Lenaerts J, Raus J, Vanderschueren D, Geusens P.: Musculoskeletal effects of the recombinant human IGF–1/IGF binding protein–3 complex in osteoporotic patients with proximal femoral fracture: a double–blind, placebo–controlled pilot study.// J. Clinical Endocrinology and Metabolism, 2002, Vol. 87, pp. 1593–1599.
47. Campbell AJ, Robertson MC, Gardner MM, Norton RN, Tilyard MW, Buchner DM.: Randomized controlled trial of a general practice programme of home based exercise to prevent falls in elderly women.// British Medical J, 1997, Vol.315, pp. 1065–1069.
48. Province MA, Hadley EC, Hornbrook MC, et.al.: The effects of exercise on falls in elderly patients. A preplanned meta–analysis of the FISCIT trials. JAMA, 1995, Vol.273, pp.1341–1347.
49. Robertson MC, Delvin N, Gardner MM, Campbell AJ.: Effectiveness and economic evaluation of a nurse delivered home exercise programme to prevent falls. 1: Randomised controlled trial.// British Medical J, 2001, Vol.322, pp. 697–701
50. Robertson MC, Gardner MM, Delvin N, McGee R, Campbell AJ.: Effectiveness and economic evaluation of a nurse delivered home exercise programme to prevent falls. 2: Controlled trial in multiple centres.// British Medical J., 2001, Vol. 322, pp. 701–704.
51. Tinetti ME, Baker DI, McAvay G, et al.: A multifactorial intervention to reduce the risk of falling among elderly people living in the community.// New England J Medicine, 1994, Vol. 331, pp.821–827.
52. Wang C, Swerdloff RS, Iranmanesh A, Dobs A, Snyder PJ, Cunningham G, Matsumoto AM, Weber T, Berman N.: Transdermal testosterone gel improves sexual function, mood, muscle strength, and body composition parameters in hypogonadal man.// J. Clin. Endocrinology and Metabolism, 2000, Vol. 85, pp. 2839–2853
53. Brodsky IG, Balagopal P, Nair KS.: Effects of testosterone replacement on muscle mass and muscle protein synthesis in hypogonadal men – a clinical research center study.// J. Clinical Endocrinology Metabolism, 1996, Vol. 81, pp. 3469–3475.
54. Bischoff–Ferrari HA, Orav EJ, Dawson–Hughes B.: Additive benefit of higher testosterone levels and vitamin D plus calcium supplementation in regard to fall risk reduction among older men and women.// Osteoporosis International, 2008, Vol. 19, pp. 1307–1314.
55. Jackson C, Gaugris S, Sen SS, Hosking D.: The effect of cholecalciferol (vitamin D3) on the risk of fall and fracture: a meta–analysis// Q J Med, 2007, Vol.100, pp. 185–192.
56. Richy F, Dukas L, Schacht E.: Differential effects of D–Hormone analogs and native vitamin D on the risk of falls: a comparative meta–analysis.// Calcific Tissue International, 2008, epub ahead of print.
57. Ringe JD, Schacht E.: Prevention and therapy of osteoporosis: the respective roles of plain vitamin D and alfacalcidol.// Rheumatol Int, 2004, Vol. 24, pp. 189–197.
58. Lau KHW, Baylink DJ.: Vitamin D therapy of osteoporosis: plain vitamin D therapy vs active vitamin D analog (D–hormone) therapy // Calcific Tissue International, 1999, Vol. 65, pp. 307–310.
59. Sorensen OH, Lund BI, Saltin B, Lund BJ, Andersen RB, Hjorth L, Melson F, Mosekilde F.: Myopathy in bone loss of ageing: improvement by treatment with 1–alphahydroxycholecalciferol and calcium.// J. Clinical Science, 1979, Vol. 56, pp. 157–161.
60. Verhaar HJJ, Samson MM, Jansen PAF, de Vreede PL, Manten JW, Duursma SA.: Muscle strength, functional mobility and vitamin D in older women.// Aging Clin Exp Res, 2000, Vol. 12, pp. 268–274
61. Sharla SH, Schacht E, Bawey S, Kamilli I, Holle D, Lempert UG.: Pleiotropic effects of alfacalcidol in elderly patients with rheumatoid arthritis.// Arthritis + Rheuma, 2003, Vol. 23, pp. 268–274.
62. Gallagher JC, Fowler SE, Detter JR, Sherman SS.: Combination treatment with estrogen and calcitriol in the prevention of age–related bone loss.// J. Clin Endocrinol Metab, 2001, Vol. 86, pp. 3618–3628.
63. Gallagher JC.: The effects of calcitriol on falls and fractures and physical performance tests.// J. Steroid Biochem Mol Biol, 2004, Vol. 89–90, pp. 497–501.
64. Dukas L, Bischoff HA, Lindpaintner LS, Schacht E, Birkner–Binder D, Damm TN, Thalmann B, Stahelin HB.: Alfacalcidol reduces the number of fallers in a community–dwelling elderly population with a minimum calcium intake of more than 500 mg daily.// J Am Geriatr Soc, 2004, Vol. 52, pp. 230–236.
65. Dukas L, Schacht E, Mazor Z, Stahelin HB.: treatment with alfacalcidol in elderly people significantly decreases the high risk of falls associated with a low creatinine clearance of < 5ml/min.// Osteoporosis International, 2005, Vol. 16, pp. 198–203.
66. Papadimitropoulos E, Wells G, Shea B, Gillepsie W, Weaver B, Zytaruk N, Cranney A, Adachi J, Tugwell P, Josse R, Greenwood C, Guyatt G.: The osteoporosis methodology group, and the osteoporosis research advisory gropup. Meta–analysis of the efficacy of vitamin D treatment in preventing osteoporosis in postmenopausal women.// J. Endocrin Review, 2002, Vol. 23, pp. 560–569.
67. Richy F, Ethgen O, Bruyere O, Reginster J–Y.: Efficacy of alfacalcidol and calcitriol in primary and corticosteroid–induced osteoporosis: a meta–analysis of their effects on bone mineral density and fracture rate.// Osteoporosis International, 2004, Vol.15, pp.301–310.
68. Sato Y, Maruoka H, Oizumi K.: Amelioration of hemiplegia–associated osteopenia more than 4 years after stroke by 1a–hydroxyvitamin D3 and calcium supplementation.// J. Stroke, 1997, Vol. 28, pp. 736–739.
69. Sato Y, Manabe S, Kuno H, Oizumi K.: Amelioration of osteopenia and hypovitaminosis D by 1a–hydroxyvitamin D3 in elderly patients with Parkinson’s disease.// J. Neurol Neurosurg Psychiatry, 1999, Vol.66, pp.64–68.
70. Orimo H.: Clinical application of 1a(OH)D3 in Japan.// Aktuel Rheumatol, 1994, Vol. 19 (suppl), pp. 27.
71. Ones K, Schacht E, Dukas L, Caglar N.: Effects of combined treatment with alendronate and alfacalcidol on bone mineral density and bone turnover in postmenopausal osteoporosis: a two–years randomized multiarm controlled trial.// The Internet J endocrinology, 2007, Vol.4, published online.
72. Ito M, Azuma Y, Takagli H, Komoriya K, Ohta T, Kawaguchi H.: Curative effects of combined treatment with alendronate and 1a–Hydroxyvitamin D3 on bone loss by ovariectomy in aged rats.// Jpn J. Pharmacol, 2002, Vol. 89, pp. 255–266.












