В патогенезе развития и прогрессирования сосудистых осложнений СД 2 типа ключевая роль принадлежит хронической гипергликемии, что было подтверждено исследованием DCCT [1]. Результаты этого исследования свидетельствуют, что даже пограничное повышение глюкозы крови вызывало достоверное повышение распространенности сердечно–сосудистой патологии. Основой управления сахарным диабетом является достижение хорошей компенсации углеводного и липидного обмена, а также снижение уровня АД до целевых значений [2,3]. Все направления одинаково важны, однако достижение нормогликемии считается первоочередной задачей лечения СД 2 типа. Крупнейшее исследование UKPDS (United Kingdom Prospective Diabetes Study) показало, что при уменьшении уровня HbA1c на 1% общая летальность при СД 2 типа снижается на 21%, риск развития микрососудистых осложнений – на 37%, а инфаркта миокарда – на 14% [4]. Результаты этого исследования подчеркивают необходимость строгой компенсации углеводного обмена.
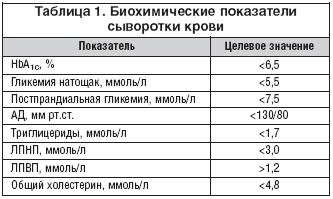
В настоящее время, согласно рекомендациям International Diabetes Federation, целью лечения больных СД 2 типа является снижение гликозилированного гемоглобина (HbA1c) до уровня 6,5% (табл. 1). В консенсусе, принятом в 2006 г. Американской диабетологической ассоциацией и Европейской ассоциацией по изучению сахарного диабета, указано, что показатель HbA1c>7,0% следует рассматривать как недостаточную компенсацию углеводного обмена, и рекомендована дальнейшая коррекция сахароснижающей терапии до достижения цели лечения [5]. По данным NHNES, только 50% пациентов с СД 2 типа достигают цели лечения HbA1c?7,0%, 20% больных поддерживают уровень HbA1c между 7 и 8%, остальные 30% больных СД 2 типа имеют HbA1c>8% [6]. Прогрессирующее течение СД 2 типа, ухудшение функции ?–клеток и увеличение инсулинорезистентности обусловливают постепенное ухудшение гликемического контроля и требуют расширения терапии для достижения долгосрочных целей лечения. В исследовании UKRDS показано, что монотерапия метформином или препаратами сульфонилмочевины позволяет контролировать параметры углеводного обмена в течение непродолжительного времени: через 3 года лечения 50% больных нуждаются в комбинированном лечении, а через 9 лет только 25% больных способны достичь цели на монотерапии [7]. Первая задача комбинированной терапии – получить аддитивный или синергичный эффект с целью улучшения гликемического контроля, а также нейтрализовать возможные побочные эффекты применяемых препаратов [8]. Кроме того, согласно современным принципам ведения пациентов с СД 2 типа, терапия должна быть патогенетически обоснованной и учитывать гетерогенность метаболических нарушений.
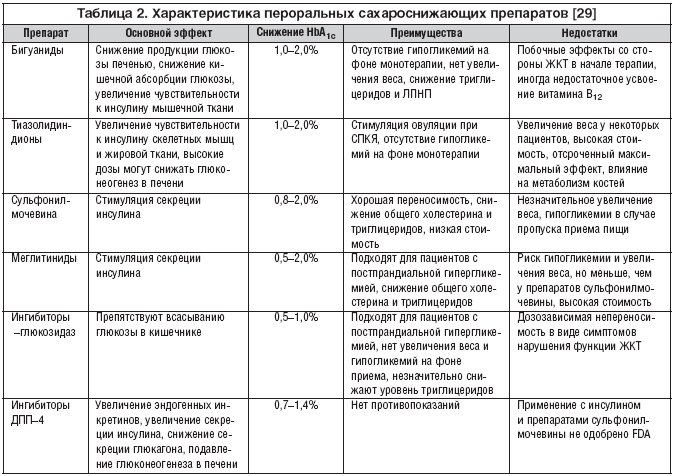
Как известно, в развитии СД 2 типа принимают участие два основных патофизиологических дефекта: инсулинорезистентность (ИР) и дисфункция ?–клеток поджелудочной железы [9]. Вследствие нарушения чувствительности к инсулину развивается хроническая гипергликемия и компенсаторная гиперинсулинемия, что приводит со временем к декомпенсации функции ?–клеток. Таким образом, ИР рассматривается в настоящее время как основополагающее патофизиологическое нарушение в развитии СД 2 типа, и, соответственно, коррекция ИР приобретает ведущую роль в терапии СД 2 типа. В настоящее время существует 6 классов пероральных сахароснижающих препаратов (табл. 2). Из всех перечисленных препаратов только тиазолидиндионы и метформин воздействуют на инсулинорезистентность и эти препараты оказывают мощный эффект в плане снижения уровня гликозилированного гемоглобина.
В Консенсусе по управлению СД 2 типа метформин рекомендован как препарат первого выбора, который назначается сразу после постановки диагноза сахарного диабета. Сахароснижающее, а точнее антигипергликемическое действие метформина обусловлено несколькими механизмами. В первую очередь это уменьшение скорости образования глюкозы печенью за счет подавления глюконеогенеза и гликогенолиза, а также улучшение утилизации глюкозы периферическими тканями. Последний механизм реализуется путем повышения активности глюкозных транспортеров GLUT–1, GLUT–3 и GLUT–4, что способствует улучшению транспорта глюкозы в клетки. Метформин уменьшает продукцию глюкозы печенью в среднем на 30%, что приводит к снижению уровня глюкозы крови натощак. Доказано, что при уменьшении продукции глюкозы печенью на 17,6% гликемия натощак снижается примерно на 40% [10]. Помимо указанных эффектов, метформин задерживает интестинальную абсорбцию глюкозы, в результате чего снижаются пики постпрандиальной гликемии. Благодаря этому эффекту применение метформина, по данным UKPDS, снижает риск развития инфаркта миокарда и инсульта на 39 и 41% соответственно. Кроме того, назначение метформина ассоциируется со снижением избыточной массы тела, улучшением липидного профиля и фибринолитической активности крови.
При неудовлетворительном гликемическом контроле рекомендована комбинированная терапия с добавлением препаратов сульфонилмочевины, тиазолидиндионов или базального инсулина. Наиболее предпочтительной с точки зрения особенностей патогенеза и течения СД 2 типа представляется комбинация метформина с тиазолидиндионами. Следует отметить, что в принятом Консенсусе впервые рекомендуется более широкое использование тиазолидиндионов. Росиглитазона малеат (Авандия) – современный, эффективный препарат из группы тиазолидиндионов, имеющий богатый опыт клинического применения. Авандия относится к агонистам ядерных ?–рецепторов, активируемых пролифератором пероксисом (PPAR–?), которые контролируют экспрессию генов, регулирующих углеводный и липидный обмен в мышцах и жировой ткани. Основной терапевтический эффект Авандии заключается в увеличении чувствительности периферических тканей к инсулину и, как следствие, улучшении утилизации глюкозы. Действие препарата связано с его влиянием на экспрессию генов в адипоцитах и активизацию дифференцировки преадипоцитов в адипоциты, что приводит к образованию популяции более чувствительных к инсулину жировых клеток [11]. Под влиянием Авандии в жировой ткани, наряду с ускорением дифференцировки адипоцитов, на их мембранах происходит увеличение количества рецепторов к инсулину и повышение экспрессии генов–транспортеров глюкозы GLUT–1 и GLUT–4. Кроме того, назначение Авандии приводит к снижению уровня свободных жирных кислот и уменьшению экспрессии в жировой ткани фактора некроза опухоли–? (ФНО–?), которые способствуют развитию инсулинорезистентности и ингибируют секрецию инсулина ?–клетками поджелудочной железы [12].
Результаты исследований демонстрируют, что применение Авандии сопровождается улучшением традиционных факторов риска сердечно–сосудистых заболеваний [13,14]. Авандия способствует повышению уровня холестерина липопротеидов высокой плотности (ЛПВП), снижению концентрации триглицеридов и липопротеидов очень низкой плотности (ЛПОНП) и увеличению содержания более крупных частиц липопротеидов низкой плотности (ЛПНП), обладающих менее выраженным атерогенным эффектом.
Известно, что у большинства больных СД 2 типа при длительном течении заболевания развивается вторичная резистентность к препаратам, обладающим секретогенным действием, что приводит к декомпенсации углеводного обмена, несмотря на повышение суточной дозы применяемых препаратов. Авандия оказывает положительное влияние на функциональное состояние ?–клеток поджелудочной железы, что подтверждается снижением отношения проинсулин/инсулин в сыворотке крови на фоне лечения [15]. Улучшение функции ?–клеток происходит вследствие торможения процессов апоптоза, а также уменьшения глюкозо– и липотоксичности [16]. Нужно отметить, что препараты сульфонилмочевины таким эффектом не обладают [17].
Комбинированная терапия росиглитазоном и метформином имеет ряд дополнительных преимуществ. В комбинации метформина и росиглитазона малеата два препарата, воздействуя разными способами на инсулинорезистентность, позволяют добиться хорошего гликемического контроля, снизить частоту возникновения побочных эффектов и улучшить комплаентность пациентов. В настоящее время существует комбинированный препарат росиглитазона и метформина – Авандамет (GlaxoSmithKline, Великобритания).
Эффективность росиглитазона малеата в комбинации с метформином неоднократно доказана, однако клиническая эффективность, продемонстрированная в ходе исследований, не всегда соотносится с реальной клинической практикой. В обсервационном исследовании, проведенном Rosak et al., изучалась эффективность терапии росиглитазоном малеатом в добавление к метформину в реальной клинической практике [18]. В исследовании принимали участие 11 тыс. пациентов с СД 2 типа с избыточной массой тела (ИМТ в среднем 29,3) и уровнем гликозилированного гемоглобина более 7%, получавшие лечение метформином в суточной дозе от 500 до 2550 мг. Всем больным был назначен росиглитазон малеат в начальной суточной дозе 4 мг с последующим увеличением дозы по мере необходимости. По окончании 6 мес. наблюдения 71% больных не потребовалось увеличение дозы росиглитазона, 87% пациентов продолжали принимать ту же дозу метформина, что и в начале периода наблюдения. Уровень HbA1c снизился на 1,3% (с 8,1 до 6,8%, р<0,0001), концентрация глюкозы крови натощак уменьшилась на 47 мг/дл (с 171 до 124 мг/дл, р<0,0001). Также произошло увеличение числа больных, достигших цели лечения HbA1c?6,5% с 5,3 до 38,8%. При этом у 63,7% пациентов с изначально плохим гликемическим контролем уровень HbA1c снизился до 7%. Уровень артериального давления снизился на 7/3 мм рт.ст., причем процентное соотношение больных, получающих гипотензивную терапию, было равным в начале и по окончании периода наблюдения. Кроме того, на фоне комбинированной терапии росиглитазоном малеатом и метформином наблюдалось снижение веса на 1,7 кг (с 87,4 кг до 85,7 кг, р<0,0001). Снижение веса коррелировало с уровнем гликозилированного гемоглобина: уменьшение HbA1c на 1% сопровождалось снижением массы тела на 0,62 кг (р<0,001). Таким образом, результаты приведенного исследования показывают, что добавление росиглитазона малеата к терапии метформином способствует улучшению гликемического контроля и ведет к увеличению числа пациентов, достигших цели лечения. Кроме того, продемонстрировано, что результаты контролируемых исследований могут быть перенесены в реальную клиническую практику.
В ретроспективном исследовании 9533 больных СД 2 типа, получающих монотерапию пероральными сахароснижающими препаратами (ПССП), продемонстрировано, что с момента достижения HbA1c уровня 10% до изменения фармакотерапии проходит около 9 мес. [19]. Ранняя комбинированная терапия ПССП с дополняющим друг друга действием может улучшить течение СД 2 типа и позволит добиться долгосрочного гликемического контроля [20]. В исследовании Rosenstock et al. оценивалась эффективность и безопасность Авандамета у больных СД 2 типа с неудовлетворительным гликемическим контролем в сравнении с монотерапией метформином или росиглитазоном [22]. В исследование включались пациенты с СД 2 типа, не получающие сахароснижающую терапию, с уровнем HbA1с 7,5–11% и гликемии натощак до 15 ммоль/л. 468 больных были рандомизированы в 3 группы приема препаратов Авандамет, Авандия (росиглитазон малеат) и метформин. Начальная доза Авандамета составила 2 мг/500 мг, Авандии – 4 мг, метформина – 500 мг, с постепенной титрацией дозы до уровня средней суточной гликемии 6,1 ммоль/л. Окончательные средние дозы для каждой группы лечения были следующими: Авандамет 7,2 мг/1799 мг, Авандия – 7,7 мг, метформин – 1847 мг. Пациенты, которым не удалось добиться снижения уровня гликемии натощак менее 13,3 ммоль/л, выбыли из исследования. Исследование завершили 88% пациентов из группы приема Авандамета, 86%, получавших лечение Авандией, и 80% – метформином.
В результате 32 недель терапии наблюдалось снижение уровня гликозилированного гемоглобина во всех группах. Снижение HbA1с на фоне приема Авандамета составило 2,3% (с 8,9 до 6,6%), что было значительно больше, чем в группе приема Авандии (1,8%, р<0,0001) и метформина (1,6%, р=0,0008). Цели лечения HbA1с?7,0% достигли 77% больных, получавших Авандамет, в сравнении с 58,1% на фоне терапии Авандией (р<0,0001) и 57,3% на фоне приема метформина (р<0,001). Снижение гликозилированного гемоглобина наблюдалось через 24 нед. лечения и оставалось стабильным на протяжении всего периода наблюдения. Подобные результаты были получены при оценке гликемии натощак. Среднее снижение гликемии натощак в группе приема Авандамета составило 4,1 vs. 2,6 в группе Авандии (р<0,0001) и 2,8 в группе метформина (р<0,0001). Уровня гликемии натощак 6,1 ммоль/л достигли 38,8% пациентов, принимающих Авандамет, 20% – Авандию (р<0,0001) и 15,3% больных, получавших метформин (р<0,0001). Увеличение чувствительности к инсулину, определяемое с помощью индекса НОМА, также было более выражено в группе приема Авандамета (61,7% vs. 36,1% на фоне лечения Авандией (р=0,010) и 35,9% на фоне приема метформина (р=0,02).
Количество эпизодов гиполикемии было схожим в трех группах: 12% пациентов отмечали гипогликемии на фоне приема Авандамета, 8% – на фоне лечения Авандией и 9% больных, принимавших метформин. Не отмечалось статистически значимых отличий в изменении веса на фоне лечения между тремя группами.
Назначение более мощных сахароснижающих препаратов в начале лечения дает быстрое достижение целевых значений показателей углеводного обмена и обеспечивает стабильный гликемический контроль [21]. Инициация терапии СД 2 типа препаратом Авандамет позволяет большему числу больных достичь целевых уровней гликозилированного гемоглобина и гликемии натощак, чем монотерапия росиглитазоном малеатом или метформином [22].
Те же авторы изучали эффективность фиксированной комбинации росиглитазона и метформина (Авандамет) у пациентов с СД 2 типа с очень плохим гликемическим контролем [23]. Такие больные, как правило, переводятся на терапию инсулином либо получают препараты сульфонилмочевины в максимальных дозах. В исследовании принимали участие 190 пациентов с впервые выявленным СД 2 типа либо с установленным диагнозом СД 2 типа, не применяющие сахароснижающую терапию, с уровнем гликозилированного гемоглобина больше 11% и гликемии натощак больше 15 ммоль/л. Средняя длительность СД 2 типа включенных в исследование пациентов соответствовала 4,1 г, индекс массы тела – 32,5. Начальная доза Авандамета составляла 4 мг/1000 мг (росиглитазон/метформин) с последующей титрацией с шагом 2 мг/500 мг с интервалом 4 недели до суточной дозы 8 мг/2000 мг или максимально переносимой дозы. Пациенты, не достигшие снижения уровня гликемии натощак менее 13,3 ммоль/л через 4 нед. терапии выбыли из исследования (процентное соотношение таких больных составило 8,4%, 1,6% из них не достигли достаточного терапевтического эффекта вследствие низкой комплаентности). Исследование завершили 78% больных.
Через 24 нед. лечения наблюдалось снижение уровня HbA1c на 4% (с 11,8 до 7,8%, р<0,0001), гликемии натощак на 7,7 ммоль/л (с 16,9 до 9,8 ммоль/л, р<0,0001) на фоне приема Авандамета в средней суточной дозе 7,6 мг/1910 мг. Отмечался быстрый терапевтический эффект: уже через 4 нед. лечения Авандаметом в дозе 4 мг/1000 мг произошло снижение гликемии натощак на 5,2 ммоль/л. Несмотря на изначально высокий уровень гликозилированного гемоглобина, 44% больных достигли цели лечения HbA1c?7,0% и 33% – HbA1c?6,5%. Кроме того, через 24 нед. терапии Авандаметом отмечено увеличение индекса чувствительности к инсулину НОМА на 68% (р<0,0001). Также наблюдалось статистически значимое улучшение показателей липидного спектра: увеличение ЛПВП на 4,4% и снижение ЛПНП на 0,7%, триглицеридов на 13,4% и общего холестерина на 3,7%.
Лечение хорошо переносилось, большинство нежелательных явлений были легкой и умеренной степени тяжести и, по мнению исследователей, не были связаны с применяемым препаратом. Наиболее часто отмечались следующие нежелательные явления: диарея (12%), инфекции верхних дыхательных путей (7%) и тошнота (5%). Отеки отмечались у 3% больных. Гипогликемии зафиксированы у 2% пациентов в процессе титрации дозы Авандамета, все случаи были нетяжелыми. Только 3% пациентов выбыли из исследования по причине нежелательных явлений. Увеличение веса составило в среднем 2,6 кг, что значительно меньше, чем на монотерапии тиазолидиндионами [24].
Таким образом, на фоне приема Авандамета около половины пациентов достигли цели лечения HbA1c?7,0% в течение непродолжительного времени (4 нед.) с минимальным числом гипогликемий (2% пациентов). Согласно рекомендациям АДА, инсулинотерапия показана больным СД 2 типа с уровнем HbA1c более 10% [25]. Однако, несмотря на преимущества инсулинотерапии, гипогликемия считается существенным ограничением. Кроме того, 27% пациентов отказываются от инсулинотерапии по субъективным причинам [26]. Назначение Авандамета пациентам с СД 2 типа с очень плохим гликемическим контролем может стать хорошей альтернативой инсулинотерапии (если нет других показаний к инсулинотерапии).
Учитывая особенности течения СД 2 типа и прогрессирующий характер дисфункции ?–клеток, неизбежно наступает момент, когда пациенты нуждаются в заместительной терапии инсулином. Часто вследствие имеющейся инсулинорезистентности приходится использовать большие дозы инсулина, что увеличивает риск гипогликемий [27]. Доказано, что комбинированное лечение инсулином и ПССП позволяет снизить дозу инсулина и достичь цели лечения. Большое число пациентов получают терапию росиглитазоном и метформином. Целью исследования Home et al. было сравнение эффективности комбинированной терапии росиглитазона малеатом, метформином и инсулином или исулином у больных СД 2 типа, получавших лечение росиглитазоном и метформином и имеющих на фоне этого лечения неудовлетворительный гликемический контроль [28]. В исследование включались пациенты с HbA1c 7,1–10%, ИМТ более 25, принимающие метформин в суточной дозе более 1500 мг в виде монотерапии или в сочетании с другим сахароснижающим препаратом. Пациенты были рандомизированы в две группы: росиглитазона малеат + метформин в суточной дозе 8 мг + 2000 мг и инсулин или плацебо и инсулин. Начальная доза инсулина составила 24 Ед (12 Ед перед завтраком и 12 Ед перед ужином), доза корректировалась каждые 3–5 дней до достижения целевого уровня гликемии перед завтраком и перед ужином 6,5 ммоль/л. Доза инсулина в обеих группах была окончательно подобрана к 4–й неделе наблюдения.
Через 24 недели наблюдения доза инсулина в группе комбинированной терапии росиглитазона малеат + метформин + инсулин составила 33,5 Ед, в группе, получавшей инсулин и плацебо – 59 Ед, разница составила 26,6 Ед (р<0,001). 70% больных достигли цели лечения HbA1c?7,0% (средний уровень HbA1c 6,8%) на фоне комбинированной терапии в сравнении в 34% (средний уровень HbA1c 7,5%) на фоне монотерапии инсулином (р<0,001). Процентное соотношение пациентов, имеющих минимум один эпизод гипогликемии на протяжении последних 12 недель наблюдения, было практически одинаковым в обеих группах (25% и 27% в группе комбинированной терапии с ПССП и группе монотерапии инсулином соответственно). Оба терапевтических режима хорошо переносились, в группе комбинированной терапии отмечено несколько большее увеличение веса (3,7 кг vs. 2,6 кг, р<0,02). Пациенты, получавшие росиглитазона малеат + метформин и инсулин, отмечают большее удовлетворение лечением, чем больные, получавшие инсулин и плацебо. Таким образом, добавление инсулина к терапии комбинацией препаратов росиглитазона малеата и метформина позволяет добиться хорошего гликемического контроля большему числу больных с меньшей дозой инсулина, чем монотерапия инсулином.
Приведенные исследования доказывают высокую эффективность препарата Авандамет. Комбинация росиглитазона и метформина в составе таблетки Авандамета позволяет значительно улучшить гликемический контроль, снизить частоту возникновения побочных эффектов препаратов и увеличить комплаентность пациентов. Авандамет может быть рекомендован для широкого клинического применения в лечении пациентов с СД 2 типа.
Литература
1. Cleary P, Orhard T, Zinman B et al. Coronary calcification in the diabetes Control and Complication trial (DCCT/EDIC) cohort for the DCCT/EDIC study group program and abstract of the ADA 63rd Annual Scientific sessions; June 13–17 2003; New Orlean, Louisiana.
2. UK Prospective Diabetes Study (UKPDS) Group. Intensive blood glucose control with sulphonylureas or insulin compared with conventional treatment of risk of complications in patients with type 2 diabetes (UKPDS 33) // Lancet. – 1998. – Vol. 352. – P. 837–853.
3. UK Prospective Diabetes Study (UKPDS) Group. Effects of intensive blood glucose control with metformin on complications in overweight patients with type 2 diabetes (UKPDS 34) // Lancet. – 1998. – Vol. 352. – P. 854–865.
4. Stratton I. M., Adler A. L., Neil H. A. et al., Association of glycaemia with macrovascular and microvascular complications of type 2 diabetes (UKPDS 35): prospective observational study// B M J. – 2000. – Vol. 321. – 405–412.
5. Nathan D.M., Buse J.B., Davidson M.B. et al., Management of hyperglycemia in type 2 diabetes: a consensus algorithm for the initiation and adjustment of therapy // Diabetologia – 2006 – Vol. 49 – P. 1711–1721.
6. Resnik NE, Foster GL, Bardsley G, Ratner E, Achievement of American Diabetes Association clinical practice recommendations among U.S. adults with diabetes, 1999–2002: the National Health and Nutrition Examination Survey// Diabetes care – 2006 – 29(3) – p. 531–537.
7. Turner RC, Cull CA, Frighi V et al. Glycemic control with diet, sulfonylurea, metformin, or insulin in patients with type 2 diabetes mellitus: progressive requirement for multiple therapies (UKPDS 49). UK Prospective Diabetes Study (UKPDS) Group. JAMA 1999; 281: 2005–12.
8. American Diabetes Association: standarts of medical care in diabetes 2007// Diabetes care – 2007 – 30(1) – p. 4–41.
9. Аметов А.С. Инсулиносекреция и инсулинорезистентность: две стороны одной медали// Проблемы эндокринологии – 2002 – т. 48, №3 – стр.31–36.
10. Дедов И.И., Демидова И.Ю., Основные принципы терапии сахарного диабета 2 типа// Сахарный диабет – 1999 – 1(2).
11. Arner P., Free fatty acids–do they play a central role in type 2 diabetes? // Diabetes Obes Metab. – 2001. – Vol. 3. – P. 11–19.
12. Балаболкин М.И., Клебанова Е.М. Значение и место Авандии в комплексной терапии больных сахарным диабетом 2 типа// РМЖ – 2007 – стр.1107–1112.
13. Leonard T. B., Bakst A., Warsi G. et al., Rosiglitazone may reduce insulin resistance related cardiovascular disease risk in patients with type 2 diabetes // Diabetes. – 2001. – Vol. 50. – Suppl. 2. – P. 441.
14. Parulkar A.A., Pendergrass M.L., Granda–Ayala R. et al., Nonhypoglycemic effects of thiazolidinediones // Ann Intern Med – 2001 – Vol. 134 – P. 61–71.
15. Porter L. E., Freed M. I., Jones N. P. et al., Rosiglitazone improves ?–cell function as measured by proinsulin/insulin ratio in patients with type 2 diabetes // Diabetes. – 2000. – Vol. 49. – Suppl. 1. – P. 122.
16. Ovalle F., Bell D. S. H., Lipoprotein effects of different thiazolidinedione in clinical practice. // Endocr Pract. – 2002. – Vol. 8. – P. 406–410.
17. Kubo K., Effect of pioglitazone on blood proinsulin levels in patients with type 2 diabetes mellitus // Endocr J. – 2002. – 49(3): 323–8.
18. Rosak C., Petzoldt R. Wolf R., et al, Rosiglitazone plus metformin is effective and well tolerated in clinical practice: results from large observational studies in people with type 2 diabetes// Int J Clin Pract – 2005 – V.59, №10 – p.1131–1136.
19. Yood MU, Lafata JE, Koro C, Wells KE, Pladevall M. Time to pharmacotherapy change in response to elevated HbA1c test results. Curr Med Res Opin 2006; 22: 1567–1574.
20. Leichter SB, Thomas S. Combination medications in diabetes care: an opportunity that merits more attention. Clin Diabetes 2003; 21: 175–178.
21. Charpentier G. Oral combination therapy for type 2 diabetes. Diabetes Metab Res Rev 2002; 18(Suppl. 3): S70–S76.
22. Rosenstock J.et al. Treatment with fixed–dose combination therapy compared with monotherapy// Diabetes Obesity and Metabolism – 2006 – V.8 – p. 650–660.
23. Rosenstock J., Rood J., Cobitz A, Huang C. and Garber A. Improvement in glycaemic control with rosiglitazone/metformin fixed–dose combination therapy in patients with type 2 diabetes with very poor glycaemic control// Obesity and Metabolism – 2006 – V.8 – p.643–649.
24. Yki–Ja rvinen H. Thiazolidinediones. N Engl J Med 2004; 351: 1106–1118.
25. American Diabetes Association. Standards of medical care in diabetes – 2006. Diabetes Care 2006; 29(Suppl.1): S4–S42.
26. United Kingdom Prospective Diabetes Study Group. United Kingdom prospective diabetes study (UKPDS) 13: relative efficacy of randomly allocated diet, sulphonylurea, insulin, or metformin in patients with newly diagnosed non–insulin dependent diabetes followed for three years. BMJ 1995; 310: 83–88.
27. Klein R, Klein BE, Moss SE, Cruickshanks KJ. The medical management of hyperglycemia over a 10–year period in people with diabetes. Diabetes Care 1996; 19: 744–750.
28. Home P. D., Bailey C. J., Donaldson J., Chen H. and. Stewart M. W. A double–blind randomized study comparing the effects of continuing or not continuing rosiglitazone+metformin therapy when starting insulin therapy in people with Type 2 diabetes// Diabetic Medicine – 2007 – V.24 – p.618–625.
29. Smiley D., Umpierres G., Metformin/rosiglitazone combination pill (Avandamet) for the treatment of patients with type 2 diabetes// Expert Opin. Pharmacother. – 2007 – V.8(9) – p.1353–1364.
Статья опубликована при финансовой поддержке
компании ГлаксоСмитКляйн. Мнение автора может
не совпадать с позицией компании.












